液体张力计算
液体张力计算

液体张力计算
液体的张力可以用以下公式计算:
T = γL
其中T为液体表面张力,γ为液体的表面张力系数,L为液体表面上的长度。
液体表面的长度L可以通过实验测定,而表面张力系数γ则因液体种类而异,同种液体在不同温度下表面张力系数也会有所不同。
一般地,表面张力系数可以通过静力学、动力学等方法来测定。
在工程实际中,由于液体的表面张力非常小,因此经常采用附加了一些表面活性剂或表面吸附剂的液体来替代真实液体进行实验和计算。
液体表面张力系数的测定实验报告

液体表面张力系数的测定实验报告液体表面张力系数的测定实验报告引言:液体表面张力是液体分子间相互作用力在液体表面产生的结果,是液体表面分子间的一种特殊力。
液体表面张力的大小对于液体的性质和应用有着重要的影响,因此准确测定液体表面张力系数具有重要的科学意义和实际应用价值。
实验目的:本实验旨在通过测定液体表面张力系数,了解液体的性质和分子间相互作用力,掌握测定液体表面张力的方法和技巧。
实验原理:液体表面张力系数的测定常用的方法有测量液体表面降低高度法和测量液滴形状法。
本实验采用测量液滴形状法。
实验仪器和药品:1. 精密天平2. 滴定管3. 滴定管架4. 滴定瓶5. 蒸馏水6. 乙醇溶液实验步骤:1. 将实验室温度调至恒定,避免温度对实验结果的影响。
2. 用精密天平称取一定质量的滴定瓶。
3. 在滴定管架上放置一只干净的滴定管。
4. 将滴定瓶倒置并将液体滴入滴定管中,直到滴定管口外溢。
5. 记录液滴的质量和滴定管口外溢的时间。
6. 重复以上步骤3-5,每次使用不同的液体进行实验。
实验数据处理:根据实验数据,可以计算液体表面张力系数。
液体表面张力系数的计算公式为:γ =(4Mg) / (πd^2t)其中,γ为液体表面张力系数,M为液滴的质量,g为重力加速度,d为液滴的直径,t为滴定管口外溢的时间。
实验结果与分析:通过实验测量和计算,得到了不同液体的表面张力系数。
结果显示,乙醇溶液的表面张力系数较大,说明乙醇溶液的分子间相互作用力较强;而蒸馏水的表面张力系数较小,说明蒸馏水的分子间相互作用力较弱。
结论:通过本实验的测定,我们成功地测量了不同液体的表面张力系数,并得出了相应的结论。
液体表面张力系数的测定对于了解液体的性质和分子间相互作用力具有重要意义,对于液体的应用和研究也具有实际价值。
实验中可能存在的误差:1. 实验过程中,滴定管口外溢的时间可能受到人为操作的影响,导致实验结果的误差。
2. 液滴的直径的测量可能存在一定的误差,影响了液体表面张力系数的计算结果。
液体张力简单计算(医)

液体张力简单计算液体疗法的目的是纠正水、电解质和酸碱平衡紊乱,以恢复机体的正常生理功能。
补液方案应根据病史、临床表现及必要的实验室检查结果,综合分析水和电解质紊乱的程度、性质而定.首先确定补液的总量、组成、步骤和速度。
补液总量包括补充累积损失量、继续损失量及供给生理需要量三个方面。
1.补充累积损失量指补充发病后至补液时所损失的水和电解质量。
(1)补液量:根据脱水严重程度而定。
原则上轻度脱水补50ml/kg,中度脱水补50~100ml/kg,重度脱水补100~120ml/kg。
实际应用时一般先按上述量的2/3量给予。
(2)补液成分:根据脱水性质而定.一般而论,低渗性脱水补充高渗溶液,等渗性脱水补充等张溶液,高渗性脱水补充低渗溶液。
若临床判断脱水性质有困难,可先按等渗性脱水处理。
有条件者最好测血钠含量,以确定脱水性质。
(3)补液速度:累积损失量应在开始输液的8~12小时内补足,重度脱水或有循环衰竭者,应首先静脉推注或快速静脉滴入以扩充血容量,改善血液循环及肾功能,一般用2:1等张含钠液(2份生理盐水加1份1。
4%碳酸氢钠)20ml/kg,总量不超过300ml,于30~60分钟内静脉推注或快速滴入。
2.补充继续损失量指补液开始后,因呕吐腹泻等继续损失的液体量。
应按实际损失量补充,但腹泻患儿的大便量较难准确计算,一般根据次数和量的多少大致估计,适当增减。
补充继续损失量的液体种类,一般用l/3张~1/2张含钠液,于24小时内静脉缓慢滴入.3.供给生理需要量小儿每日生理需水量约为60~80ml/kg,钠、钾、氯各需1~2mmol/kg。
这部分液体应尽量口服补充,口服有困难者,给予生理维持液(1/5张含钠液十0.15%氯化钾),于24小时内均匀滴入.在实际补液中,要对上述三方面需要综合分析,混合使用。
对腹泻等丢失液体引起脱水的补液量:一般轻度脱水约90-120ml/kg;中度脱水约120~150ml/kg;重度脱水约150-180ml/kg。
液体张力怎么计算

液体张力怎么计算计算液体表面张力公式:S=ds/de。
凡作用于液体表面,使液体表面积缩小的力,称为液体表面张力。
液体张力怎么计算液体表面张力公式为:S=ds/de,de为悬滴的最大直径,ds为离顶点距离为de处悬滴截面的直径。
式中b为液滴顶点O处的曲率半径,此式最早是由Andreas,Hauser和Tucker 提出,若相对应与悬滴的S值得到的1/H为已知,即可求出表(界)面张力。
应用Bashforth-Adams法,即可算出作为S的函数的1/H值。
因为可采用定期摄影或测量ds/de数值随时间的变化,悬滴法可方便地用于测定表(界)面张力。
凡作用于液体表面,使液体表面积缩小的力,称为液体表面张力。
它产生的原因是液体跟气体接触的表面存在一个薄层,叫做表面层,表面层里的分子比液体内部稀疏,分子间的距离比液体内部大一些,分子间的相互作用表现为引力。
液体张力的定义液体张力,膜两侧容积发生了变化,压力也发生了变化,这种通过渗透维持的溶液的平衡压力就是渗透压,指液体压力。
渗透压是溶液的特性,是受半透膜的性质来决定的。
比如细胞膜作为半透膜,仅允许水分子自由通过,通过的量由细胞膜两侧溶质的浓度来控制。
水分子通过细胞膜向溶质高的一侧转移,逐渐达到膜两侧溶质浓度相近,这一现象就叫渗透。
由此,膜两侧容积发生了变化,压力也发生了变化,这种通过渗透维持的溶液的平衡压力就是渗透压。
摩尔浓度通常被用作渗透压的单位。
液体张力的应用一、生活中的应用1、吹出超级肥皂泡我们用普通方法配制的肥皂液,很难吹出大肥皂泡。
罗用小刀把香皂切成小薄片,放入杯子里,加热水搅拌溶化,再加入少许砂糖并放入一包茶,盖上盖子放一夜。
明天,就可以用这种皂液吹出超级肥皂泡。
含有糖和茶液的肥皂膜,表面物质的连接力大大增强了,所以不易破裂。
2、牙膏清洁口腔液体与气体接触的表面层,由于表面张力会出现表面收缩的趋势;液体与固体接触的附着层会出现浸润与不浸润现象;由于表面层和附着层的影响,在毛细管内又会出现毛细观象。
表面张力公式

表面张力公式
表面张力公式是一种描述表面张力的物理模型,它可以用来计算液体表面的张力。
它是由德国物理学家威尔弗雷德·谢尔登于1908年提出的,也称为谢尔登-普利兹曼公式。
表面张力公式用于描述液体表面的张力,它被用来计算液体的表面的张力,尤其是对于非常细小的液体分子而言。
它的公式是:γ = γ0 + γs,其中γ0表示液体表面的背景张力,γs表示液体表面上的表面张力。
表面张力公式有很多应用,它可以用来计算液体的表面张力,可以用于液体的流动模拟,也可以用于研究液体的表面特性。
它还可以用于研究纳米尺寸的液体滴,以及液体表面与其他环境的相互作用。
此外,表面张力公式还可以用来研究表面活性剂的性质,以及表面活性剂与其他液体的相互作用。
表面张力公式在物理学中有着重要的作用,它可以用来研究液体表面的特性,以及液体表面与其他环境的相互作用。
它可以帮助我们更好地理解液体的表面特性,并有助于改善液体在工业应用中的利用。
渗透压与张力

在液体治疗中,液体的渗透压与张力是很重要的概念,是我们了解、认识液体特点的基础一.定义1.液体渗透压(Fluid osmolality):当两种不同浓度溶液用一种理想的半透膜隔开时,则溶剂从低浓度溶液向高浓度溶液中渗透,这种溶剂渗透的力,通常称为渗透压,可简单理解为溶质分子对溶剂分子产生的吸引力,反映的是单位体积溶液中溶质微粒的数目液体渗透压的计算摩尔浓度(mmol/L)=1000×ρ×A%÷摩尔质量×1000备注:ρ为溶剂密度(水密度为1);A%为质量百分比浓度;上式计算结果数值与渗透压(单位mOsm/L)的数值相等2. 液体张力(Fluid tonicity):指溶液进入到体内后能够维持渗透压的能力,是指溶液中电解质产生的渗透压与血浆渗透压正常值的比值,是一个没有单位的数值液体张力计算:电解质渗透压/血浆渗透压说明:葡萄糖进入体内后很快被代谢,只剩自由水,渗透液压就消失了。
因此说葡萄糖溶液是无张力的3. 等渗液(iso-osmotic solution):渗透压与血浆相等或相似的溶液是一个物理化学观念4. 等张液(isotonic solution)与红细胞张力相等或相似的溶液是一个生物学概念在等张液中红细胞既不肿胀也不皱缩,维持原有形态等张溶液是由不能自由透过细胞膜的溶质形成的等渗溶液二.一些治疗液体的渗透压与张力液体渗透压(mOsm/L)张力0.45%氯化钠154 1/25%葡萄糖252 00.9%氯化钠308 1复方氯化钠305 1乳酸钠林格273 15%葡萄糖0.9%氯化钠560 12.5%葡萄糖0.45%氯化钠280 1/22.5%葡萄糖1/2张林格278.5 1/22.5%葡萄糖1/2张乳酸林格262.5 1/210%葡萄糖504 03%氯化钠1026 3.45%碳酸氢钠1190 4说明:5%葡萄糖液中的葡萄糖是水合葡萄糖(分子式为C6H12O6·H2O ;分子量为198)。
液相平均表面张力计算公式

液相平均表面张力计算公式
液相平均表面张力计算公式是指通过实验测量液体在不同温度下的表面张力,然后计算出平均表面张力的公式。
该公式的具体表达式如下:
γ = 1/n × Σγi
其中,γ表示平均表面张力,n表示实验测量的温度数目,
Σγi表示在不同温度下测量的表面张力之和。
该公式的计算过程包括以下几个步骤:
1. 在不同温度下分别测量液体的表面张力,记录每个温度下的数据。
2. 将所有温度下测得的表面张力值相加,得到总和。
3. 将总和除以实验测量的温度数目,得到平均表面张力值。
4. 将计算得到的平均表面张力值进行验证,确保其准确性和可靠性。
通过该公式计算出的平均表面张力值可以用于分析液体的表面性质和应用于工业生产中的润滑、表面处理等方面。
- 1 -。
补液张力计算

补液张力计算液体疗法是儿科最常用的治疗方法之一,是儿科学的重要内容,也是每位临床医学生必需掌握的基本技能。
液体张力计算与配制则是液体疗法的基础,如对此不理解、不掌握,则将难以学习和运用液体疗法。
现有多种教材对液体张力的计算与配制,阐述均较为复杂而含糊,教师按教材授课,学生按课本学习,其结果是大多数学生难于理解与掌握。
通过五个步骤,即使所有学生很快便能理解与掌握。
过程如下:1、首先出一道简单的数学算术题例1、将10%NaCL10ml稀释至100ml,请问稀释后溶液百分比浓度。
学生很快便能列出算式:10%×10=X×100,X=1%。
稀释定律:稀释前浓度×稀释前体积=稀释后浓度×稀释后体积。
即:C1×V1=C2×V2。
并且强调但凡涉及物质浓度的换算,均遵循此定律。
2、问题:能够用来表达物质浓度的有A.百分比浓度 B.摩尔浓度 C.张力张力亦是物质浓度的一种表达方式。
3、阐述溶液张力的概念及计算张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
判断某溶液的张力,是以它的渗透压与血浆渗透压正常值(280~320mosm/L,计算时取平均值300mosm/L)相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能离解的离子数)/分子量。
如0.9%NaCL溶液渗透压=(0.9×10×1000×2)/58.5=308mosm/L(794.2kPa)该渗透压与血浆正常渗透压相比,比值约为1,故该溶液张力为1张。
又如5%NaHCO3溶液渗透压=(5×10×1000×2)/84=1190.4mosm/L(3069.7kPa)该渗透压与血浆正常渗透压相比,比值约为4,故该溶液张力为4张。
液体表面张力系数测定实验报告

液体表面张力系数测定实验报告一、实验目的。
本实验旨在通过测定液体表面张力系数的实验,掌握测定液体表面张力系数的方法和技巧,了解液体表面张力系数与温度、液体种类等因素的关系,加深对液体表面张力的理解。
二、实验原理。
液体的表面张力是指在液体表面上的一层分子受到的合力,使得表面上的液体分子呈现出对内聚力的表现。
液体的表面张力系数可以用下式表示:γ = F / L。
其中,γ为液体的表面张力系数,F为液体表面张力的大小,L为液体表面的长度。
实验中,我们将通过测定液体表面张力系数的实验来求得液体的表面张力系数。
三、实验仪器与试剂。
1. 二号烧瓶。
2. 纯水。
3. 毛细管。
4. 电子天平。
5. 温度计。
6. 实验台。
四、实验步骤。
1. 将烧瓶内装满纯水,并在水面上插入毛细管。
2. 用电子天平测定毛细管上升的质量m。
3. 用温度计测定水的温度T。
4. 根据实验数据,计算出液体表面张力系数γ。
五、实验数据记录与处理。
实验数据如下:水的质量m = 0.05g。
水的温度T = 25℃。
根据实验数据,我们可以计算出水的表面张力系数γ如下:γ = (2 m g) / (π d h)。
其中,g为重力加速度,取9.8m/s²;d为毛细管的直径,取0.5mm;h为毛细管上升的高度。
经过计算,我们得到水的表面张力系数γ约为0.072N/m。
六、实验结果与分析。
通过实验测定,我们得到水的表面张力系数γ约为0.072N/m。
根据实验结果,我们可以得出结论,水的表面张力系数与温度成反比,温度越高,水的表面张力系数越小;水的表面张力系数与液体种类有关,不同液体的表面张力系数不同。
七、实验总结。
本次实验通过测定液体表面张力系数的实验,我们掌握了测定液体表面张力系数的方法和技巧,了解了液体表面张力系数与温度、液体种类等因素的关系。
通过实验,我们加深了对液体表面张力的理解,为今后的学习和科研工作打下了坚实的基础。
八、参考文献。
1. 《物理化学实验指导》,XXX,XXX出版社,200X年。
液体表面张力系数测定实验报告

液体表面张力系数测定实验报告1. 了解液体表面张力的概念和测量方法;2. 掌握液体表面张力系数的测量方法。
实验仪器:1. 六轴电子天平;2. 红外线电子温度计;3. 倍频光源。
实验原理:液体表面张力指在液体表面上任意一点单位长度上所作用的拉力,单位为N/m。
液体表面张力系数是液-气界面的表面张力,这个系数也可以称为液体的表面张力。
液体表面张力的测量方法:干法法和湿法法。
其中湿法法包括皮革法、浸水法和滴下法。
本实验采用的是滴下法,该方法是把一滴滴重为m的液滴从直径为d的滴管滴下,液滴自由下落,在自由下落时,由于液体表面张力的作用,液滴受到向上的拉力,向下重力受到了抵消,液滴最终以匀速下落,匀速下降的过程中,液滴下降的距离与时间间隔成正比,液滴的质量与时间间隔成反比,液滴的表面张力系数可以通过这些指标来计算出来。
实验过程:1. 在天平上量出60度左右的开口角的玻璃滴管的质量m1,D=1mm,L=50mm。
2. 用红外线电子温度计测量滴管内壁和外壁的温度。
3. 用甲醇、乙醇、正丁醇和去离子水分别进行实验,分别滴出10滴,记录时间和滴重。
4. 通过实验数据计算表面张力系数。
实验数据:样品温度(℃) 室温(℃) 滴管重量(m1)(g) 滴重(m2)(g) 滴下时间(t)(s)甲醇24.4 21.4 0.2723 0.0271 30.47乙醇24.7 21.4 0.2742 0.0276 39.37正丁醇24.8 21.4 0.2720 0.0272 80.86 去离子水24.7 21.4 0.2726 0.0272 29.50天平的量程:500g,分度值:0.001g计算:1. 测量液体表面张力的计算公式:γ=(4mg)/(πd^2t^2ρ)其中:γ:液体表面张力系数,单位:mN/m;m:液滴重量(g);g:重力加速度(9.8 m/s^2);d:液滴等效半径(直径)(m);t:液滴落下的时间(s);ρ:液体的密度(g/cm^3)。
测量表面张力系数
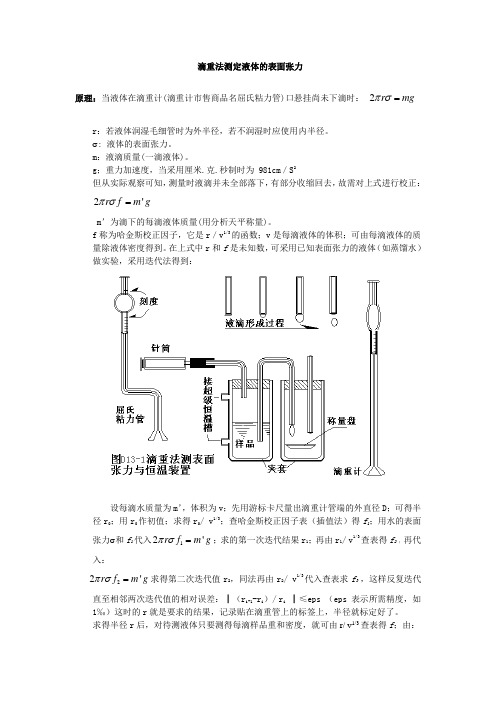
滴重法测定液体的表面张力原理:当液体在滴重计(滴重计市售商品名屈氏粘力管)口悬挂尚未下滴时: 2r mg πσ=r :若液体润湿毛细管时为外半径,若不润湿时应使用内半径。
σ: 液体的表面张力。
m :液滴质量(一滴液体)。
g ;重力加速度,当采用厘米.克.秒制时为 981cm /S 2但从实际观察可知,测量时液滴并未全部落下,有部分收缩回去,故需对上式进行校正:2'r f m g πσ=m ’为滴下的每滴液体质量(用分析天平称量)。
f 称为哈金斯校正因子,它是r /v 1/3的函数;v 是每滴液体的体积;可由每滴液体的质量除液体密度得到。
在上式中r 和f 是未知数,可采用已知表面张力的液体(如蒸馏水)做实验,采用迭代法得到:设每滴水质量为m ’,体积为v ;先用游标卡尺量出滴重计管端的外直径D ;可得半径r 0;用r 0作初值;求得r 0/ v 1/3;查哈金斯校正因子表(插值法)得f 1;用水的表面张力σ和f 1代入12'r f m g πσ=;求的第一次迭代结果r 1;再由r 1/ v 1/3查表得f 2 ;再代入:22'r f m g πσ=求得第二次迭代值r 2,同法再由r 2/ v 1/3代入查表求f 3 ,这样反复迭代直至相邻两次迭代值的相对误差:┃(r i-1-r i )/ r i ┃≤eps (eps 表示所需精度,如1‰)这时的r 就是要求的结果,记录贴在滴重管上的标签上,半径就标定好了。
求得半径r 后,对待测液体只要测得每滴样品重和密度,就可由r/ v 1/3查表得f ;由:2'r f m g πσ= 就可求得样品的表面张力。
最大泡压法测定溶液的表面张力实际上,最大泡压法测定溶液的表面张力是毛细管上升法的一个逆过程。
其装置如图所示,将待测表面张力的液体装于表面张力仪中使毛细管的端面与液面相切(这样做是为了数据处理方便,如果做不到相切,每次实验毛细管浸没的深度应保持一致,此时数据处理参见其它文献),由于毛细现象液面即沿毛细管上升,打开抽气瓶的活塞缓缓抽气,系统减压,毛细管内液面上受到一个比表面张力仪瓶中液面上(即系统)大的压力,当此压力差——附加压力(∆p =p大气-p 系统)在毛细管端面上产生的作用力稍大于毛细管口液体的表面张力时,气泡就从毛细管口脱出,此附加压力与表面张力成正比,与气泡的曲率半径成反比,其关系式为拉普拉斯公式:Rp σ2=∆ (4-2) 式中,∆p 为附加压力;σ为表面张力;R 为气泡的曲率半径。
水的表面张力计算公式

水的表面张力计算公式
摘要:
1.水的表面张力概念介绍
2.水的表面张力计算公式推导
3.表面张力的实际应用
正文:
一、水的表面张力概念介绍
表面张力是指液体分子之间的相互作用力,这种力作用在液体的表面,并使液体的表面尽量减小到最低的能量状态。
表面张力是液体的一种特性,它与液体的种类、温度以及液体的表面积有关。
在实际应用中,表面张力的计算和研究具有重要意义,尤其在液体的润滑、洗涤、喷雾等方面。
二、水的表面张力计算公式推导
水的表面张力计算公式是通过实验数据和理论分析推导得出的。
计算公式如下:
γ= (4 * π * ρ * rho) / 3
其中,γ代表表面张力,ρ代表液体的密度,rho 代表液体的摩尔密度,r 代表液体分子的半径。
从公式中可以看出,表面张力与液体的密度、摩尔密度以及液体分子的半径有关。
在实际应用中,可以通过测量液体的密度、摩尔密度和液体分子的半径,然后代入公式计算出表面张力。
三、表面张力的实际应用
表面张力在实际应用中具有广泛的应用,尤其在液体的润滑、洗涤、喷雾等方面。
例如,在润滑方面,表面张力可以影响润滑油的润滑效果,润滑油的表面张力过低或过高都会影响润滑效果。
在洗涤方面,表面张力可以影响洗涤剂的去污能力,洗涤剂的表面张力过低或过高都会影响去污能力。
在喷雾方面,表面张力可以影响喷雾的雾滴大小和分布,表面张力过低或过高都会影响喷雾效果。
综上所述,表面张力是液体的一种特性,它与液体的种类、温度以及液体的表面积有关。
简单张力液体配制法

判断某溶液的张力,是以它的渗透压与血浆渗透压正常值(280~320mosm/L,算时取平均值300mosm/L)相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能离解的离子数)/分子量。
如0.9%NaCl溶液渗透压=(0.9×10×1000×2)/58.5=308mOsm/L(794.2kPa)该渗透压与血浆正常渗透压相比,比值约为1,故该溶液张力为1 张。
又如5%NaHCO3 溶液渗透压=(5×10×1000×2)/84=1190.4mOsm/L(3069.7kPa)该渗透压与血浆正常渗透压相比,比值约为4,故该溶液张力为4 张。
对以上复杂的计算过程,不要求学生掌握,但要记住张力是物质浓度的一种表达方式,其换算自然亦遵循稀释定律:C1×V1=C2×V2。
然后列出课本上已标明相应张力的几种常用溶液:10%(NaCl)11 张(临床上可按10 张计算)0.9%(NaCl)1 张5%(NaHCO3)4 张10%(KCl)9 张10%(GS)0 张(无张力,相当于水)并指出,临床上多数情况下就是用以上几种溶液配制成其它所需的液体进行治疗,只需记住此几种溶液的张力,便可灵活自如地进行配制与计算所需溶液及张力;而不必去追究为什么10%NaCl张力是10 张这一复杂的计算过程。
4、举例说明混合溶液张力的计算例2、10%NaCl(10ml)+10%GS(90ml),请问该组溶液张力。
同学们很快能够根据C1×V1=C2×V2 列出算式:10×10=X×100,X=1 张例3、10%NaCl(20ml)+5%NaHCO3(25ml)+10%GS(255ml),请问该组溶液张力。
10×20+4×25=X×300,X=1 张。
渗透压与张力

在液体治疗中,液体的渗透压与张力是很重要的概念,是我们了解、认识液体特点的基础一.定义1.液体渗透压(Fluid osmolality):当两种不同浓度溶液用一种理想的半透膜隔开时,则溶剂从低浓度溶液向高浓度溶液中渗透,这种溶剂渗透的力,通常称为渗透压,可简单理解为溶质分子对溶剂分子产生的吸引力,反映的是单位体积溶液中溶质微粒的数目液体渗透压的计算摩尔浓度(mmol/L)=1000×ρ×A%÷摩尔质量×1000备注:ρ为溶剂密度(水密度为1);A%为质量百分比浓度;上式计算结果数值与渗透压(单位mOsm/L)的数值相等2. 液体张力(Fluid tonicity):指溶液进入到体内后能够维持渗透压的能力,是指溶液中电解质产生的渗透压与血浆渗透压正常值的比值,是一个没有单位的数值液体张力计算:电解质渗透压/血浆渗透压说明:葡萄糖进入体内后很快被代谢,只剩自由水,渗透液压就消失了.因此说葡萄糖溶液是无张力的3. 等渗液(iso—osmotic solution):渗透压与血浆相等或相似的溶液是一个物理化学观念4。
等张液(isotonic solution)与红细胞张力相等或相似的溶液是一个生物学概念在等张液中红细胞既不肿胀也不皱缩,维持原有形态等张溶液是由不能自由透过细胞膜的溶质形成的等渗溶液二.一些治疗液体的渗透压与张力液体渗透压(mOsm/L)张力0。
45%氯化钠154 1/25%葡萄糖252 00.9%氯化钠308 1复方氯化钠305 1乳酸钠林格273 15%葡萄糖0.9%氯化钠560 12。
5%葡萄糖0.45%氯化钠280 1/22。
5%葡萄糖1/2张林格278.5 1/22.5%葡萄糖1/2张乳酸林格262.5 1/210%葡萄糖504 03%氯化钠1026 3。
45%碳酸氢钠1190 4说明:5%葡萄糖液中的葡萄糖是水合葡萄糖(分子式为C6H12O6·H2O ;分子量为198)。
补液张力计算

小儿补液张力计算“溶液张力计算与配制”液体疗法是儿科最常用的治疗方法之一,是儿科学的重要内容,也是每位临床医学生必需掌握的基本技能。
液体张力计算与配制则是液体疗法的基础,如对此不理解、不掌握,则将难以学习和运用液体疗法。
现有多种教材对液体张力的计算与配制,阐述均较为复杂而含糊,教师按教材授课,学生按课本学习,其结果是大多数学生难于理解与掌握。
通过五个步骤,即使所有学生很快便能理解与掌握。
过程如下:1、首先出一道简单的数学算术题例1、将10%NaCl 10ml稀释至100 ml ,请问稀释后溶液百分比浓度。
学生很快便能列岀算式:10%X 10=XX 100,X =1%。
且强调但凡涉及物质浓度的换算,均遵循此定律。
稀释定律:稀释前浓度X稀释前体积= 稀释后浓度X稀释后体积。
即:c 1XV仁C 2XV 1。
并2、问题:c . 张力能够用来表达物质浓度的有()A .百分比浓度B.摩尔浓度张力亦是物质浓度的一种表达方式。
3、阐述溶液张力的概念及计算张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
判断某溶液的张力,是以它的渗透压与血浆渗透压正常值( 均值280 ~ 320 mosm / L,计算时取平300mosm / L)相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值。
溶液渗透压=(百分比浓度X 10X 1000X每个分子所能离解的离子数) /分子量。
如%NaCl溶液渗透压=(X 10X 1000X 2) /=308 mOsm / L(kPa )该渗透压与血浆正常渗透压相比,比值约为1 ,故该溶液张力为1 张。
又如5%NaHCO 3溶液渗透压=(5X 10X 1000X 2) /84= mOsm / L (kPa) 该渗透压与血浆正常渗透压相比,比值约为4,故该溶液张力为4 张。
对以上复杂的计算过程,不要求掌握,但要记住张力是物质浓度的一种表达方式,其换算自然亦遵循稀释定律:C 1XV 1 = C 2XV 2。
液体的张力

1、液体张力的概念:任何溶液都具有一定的渗透压,亦称为张力。
溶液所含溶质的浓度愈高,溶液的渗透压愈大,渗透压与溶液的浓度成正比。
表达渗透压大小的单位是毫克渗透分子/升,溶液的渗透压是由溶液中溶质的“颗粒”数目决定的,与“颗粒”的性质和大小无关。
对电解质来说,当它溶于水后,能解离成阳离子和阴离子,两种离子的性质不相同,但它们引起的渗透效果是完全相同的,故电解质溶液的张力等于阴阳两种离子浓度的总和。
例如1毫摩尔的NaCl溶于1升蒸馏水中,形成1升NaCl溶液时,其张力为1毫摩尔钠离子和1毫摩尔氯离子的和,其张力为2毫渗分子/升。
而非电解质,1毫摩尔分子/升浓度的溶液,其渗透压即张力就等于1毫渗分子/升。
2 血浆的渗透压(张力):血浆中的阳离子、阴离子、有机酸、蛋白质所产生的总张力为290毫渗分子/升,简记为300毫渗分子/升,其正常范围是280--320毫渗分子/升。
低于280毫渗分子/升的称谓低张(或低渗),高于320毫渗分子/升的称谓高张(或高渗)。
在血浆中钠离子的几乎占总张力的一半,临床上常以检查钠离子量来推测血浆张力。
其方法为:血浆钠离子含量加10乘2即得血浆总张力(加10是代表加入钠以外的阳离子的含量,乘2是把阴阳离子以等量看待)。
血浆的钠离子的正常范围是130--150毫摩尔/升,即血浆钠离子低于130毫摩尔/升时称为低张(低渗),高于150毫摩尔/升时称为高张(高渗)。
3临床上常用液体张力:液体的张力与血浆张力相同则称为1个张力,若为血浆张力的1/2则称为1/2个张力,依此类推。
5%GS 278毫渗分子/升,1个张力,等渗。
10%GS 556毫渗分子/升,2个张力,高渗。
(因葡萄糖进入人体后较快被氧化代谢,故在输液时葡萄糖多不算张力,计算时葡萄糖的张力安0计算,但在糖尿病病人存在高渗或酮症时,一定要注意它的张力。
)0.9%NS 307.7毫渗分子/升,1个张力,等渗。
3%NS 1025.6毫渗分子/升,3.5个张力,高渗。
补液张力计算

小儿补液张力计算“溶液张力计算与配制”液体疗法是儿科最常用的治疗方法之一,是儿科学的重要内容,也是每位临床医学生必需掌握的基本技能。
液体张力计算与配制则是液体疗法的基础,如对此不理解、不掌握,则将难以学习和运用液体疗法。
现有多种教材对液体张力的计算与配制,阐述均较为复杂而含糊,教师按教材授课,学生按课本学习,其结果是大多数学生难于理解与掌握。
通过五个步骤,即使所有学生很快便能理解与掌握。
过程如下:1、首先出一道简单的数学算术题例1、将10%NaCl10ml稀释至100ml,请问稀释后溶液百分比浓度。
学生很快便能列出算式:10%×10=X×100,X=1%。
稀释定律:稀释前浓度×稀释前体积=稀释后浓度×稀释后体积。
即:C1×V1=C2×V1。
并且强调但凡涉及物质浓度的换算,均遵循此定律。
2、问题:能够用来表达物质浓度的有()A.百分比浓度B.摩尔浓度C.张力张力亦是物质浓度的一种表达方式。
3、阐述溶液张力的概念及计算张力是指溶液溶质的微粒对水的吸引力,溶液的浓度越大,对水的吸引力越大。
判断某溶液的张力,是以它的渗透压与血浆渗透压正常值(280~320mosm/L,计算时取平均值300mosm/L)相比所得的比值,它是一个没有单位但却能够反映物质浓度的一个数值。
溶液渗透压=(百分比浓度×10×1000×每个分子所能离解的离子数)/分子量。
如0.9%NaCl溶液渗透压=(0.9×10×1000×2)/58.5=308mOsm/L(794.2kPa)该渗透压与血浆正常渗透压相比,比值约为1,故该溶液张力为1张。
又如5%NaHCO3溶液渗透压=(5×10×1000×2)/84=1190.4mOsm/L(3069.7kPa)该渗透压与血浆正常渗透压相比,比值约为4,故该溶液张力为4张。
液体张力计算

渗透压是溶液的特性,是受半透膜的性质来决定的。
比如细胞膜作为半透膜,仅允许水分子自由通过,通过的量由细胞膜两侧溶质的浓度来控制。
水分子通过细胞膜向溶质高的一侧转移,逐渐达到膜两侧溶质浓度相近,这一现象就叫渗透。
由此,膜两侧容积发生了变化,压力也发生了变化,这种通过渗透维持的溶液的平衡压力就是渗透压。
摩尔浓度通常被用作渗透压的单位。
血液作为一种特殊溶液也有一定的渗透压,通常正常值为:280 - - 320m0Sm / L 。
也就是血浆中的溶质摩尔浓度的总合。
任何溶液有一定的浓度就有一定的渗透压,相对于血液比较,高于血浆渗透压的就叫高渗溶液,低于者就叫低渗溶液,在血浆渗透压正常值范围内的当然就是等渗溶液。
任何溶液在进入血液时都要求是等渗的,比如:0 . 9 %盐水、1 . 4 %碳酸氢钠、1 . 2 %氯化钾、5 %葡萄糖等等。
但是并不是所有的溶液进入血液中都能够维持住本身的渗透压,比如葡萄糖进入体内后很快被代谢掉,渗透压就消失了。
这就引出一个概念:液体的张力。
液体的张力是指溶液进入到体内后能够维持渗透压的能力。
比如 5 %葡萄糖25Oml + 0 . 9 %盐水25Oml ,共计5OOml ,我们叫对半液5OOml ,输液之前是等渗溶液,输到体内后葡萄糖被代谢,仅有0 . 9 % 盐水250ml 维持渗透压,所以说对半液是1 / 2 张力液。
就不一一列举了。
0 . 9 %盐水、1 . 4 %碳酸氢钠、1 .2 %氯化钾、5 %葡萄糖等上述四种液体是我们补液的常用液体,只有葡萄糖被代谢,所以不含张力常用的混合溶液有下列几种:(1)1:1液:是5%葡萄糖溶液1份与0.9%氯化钠1份的混合溶液,其渗透压约为血浆的一半,即1/2张,适合于对单纯性呕吐和继续丢失液量的液体补充。
简便配制方法可用5%葡萄糖500ml加入10%氯化钠溶液20ml即可。
(2)3:2:1液:即3份10%葡萄糖溶液、2份0.9%氯化钠溶液及1份1.87%乳酸钠(或1.4%碳酸氢钠)溶液的混合溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
渗透压是溶液的特性,是受半透膜的性质来决定的。
比如细胞膜作为半透膜,仅允许水分子自由通过,通过的量由细胞膜两侧溶质的浓度来控制。
水分子通过细胞膜向溶质高的一侧转移,逐渐达到膜两侧溶质浓度相近,这一现象就叫渗透。
由此,膜两侧容积发生了变化,压力也发生了变化,这种通过渗透维持的溶液的平衡压力就是渗透压。
摩尔浓度通常被用作渗透压的单位。
血液作为一种特殊溶液也有一定的渗透压,通常正常值为:280 - - 320m0Sm / L 。
也就是血浆中的溶质摩尔浓度的总合。
任何溶液有一定的浓度就有一定的渗透压,相对于血液比较,高于血浆渗透压的就叫高渗溶液,低于者就叫低渗溶液,在血浆渗透压正常值范围内的当然就是等渗溶液。
任何溶液在进入血液时都要求是等渗的,比如:0 . 9 %盐水、1 . 4 %碳酸氢钠、1 . 2 %氯化钾、5 %葡萄糖等等。
但是并不是所有的溶液进入血液中都能够维持住本身的渗透压,比如葡萄糖进入体内后很快被代谢掉,渗透压就消失了。
这就引出一个概念:液体的张力。
液体的张力是指溶液进入到体内后能够维持渗透压的能力。
比如 5 %葡萄糖25Oml + 0 . 9 %盐水25Oml ,共计5OOml ,我们叫对半液5OOml ,输液之前是等渗溶液,输到体内后葡萄糖被代谢,仅有0 . 9 % 盐水250ml 维持渗透压,所以说对半液是1 / 2 张力液。
就不一一列举了。
0 . 9 %盐水、
1 . 4 %碳酸氢钠、
1 .
2 %氯化钾、
5 %葡萄糖等
上述四种液体是我们补液的常用液体,只有葡萄糖被代谢,所以不含张力
常用的混合溶液有下列几种:
(1)1:1液:是5%葡萄糖溶液1份与0.9%氯化钠1份的混合溶液,其渗透压约为血浆的一半,即1/2张,适合于对单纯性呕吐和继续丢失液量的液体补充。
简便配制方法可用5%葡萄糖500ml加入10%氯化钠溶液20ml即可。
(2)3:2:1液:即3份10%葡萄糖溶液、2份0.9%氯化钠溶液及1份1.87%乳酸钠(或1.4%碳酸氢钠)溶液的混合溶液。
其简单配制方法为:5%葡萄糖溶液500ml加入10%氯化钠溶液15ml及11.2%乳酸钠溶液15ml(5%碳酸氢钠溶液24m),其张力为1/2张。
(3)3:4:2液(有的单位将混合液的顺序变动为4:3:2溶液):是3 份10%葡萄糖溶液、4份0.9%氯化钠溶液及2份1.87%(1/6克分子)乳酸钠溶液(或1.4%碳酸氢钠溶液)的混合溶液,总份数为9,其中电解质(有渗透压作用的)占6份,所以是6/9张,简化为2/3张(约相当于血浆渗透压的2/3,即2/3张)。
主要用于补充以丢失的液体量(即累积损失量)。
配制方法:先用总份数9除以丢失的液体总量,求出1份是多少毫升,然后用1份的毫升数分别乘以3、4和2,所得乘积即为各种溶液的毫升数。
例如:一个9kg的小儿,估计已丢失的体液量是体重的10%,则总丢失量为900ml,900ml除以9份,则1份为100ml,那么3份是10%GS,即100ml×3=300ml,依此类推,400ml为生理盐水,200ml为1/6克分子乳酸钠溶液。
简便配制方法:用5%葡萄糖溶液500ml加10%氯化钠溶液20ml及11.2%乳酸钠溶液20ml(或5%碳酸氢钠33ml) 。
(4)6:7:5液(一般称5:6:7液):是6份5%~10%葡萄糖溶液、7份0.9%氯化钠溶液及5份1/6克分子乳酸钠溶液的混合液,总份数是18,其中含电解质的占12份,所以是12/18,简化为2/3张,它与4:3:2液有相同的张力,所不同的是5:6:7液中乳酸钠含量较4:3:2液为高,故纠正酸中毒时,以5:6:7液为佳,配制方法与4:3:2液相似(不含简便配制法)。
(5)6:3 :1 液:是6份5%葡萄糖溶液、2份0.9%氯化钠溶液及1份1.87%乳酸钠(或1.4%碳酸氢钠)溶液的混合溶液,为1/3张液。
简便配制方法:用5%葡萄糖500ml,加入10%氯化钠溶液10ml与11.2%乳酸钠溶液9ml(或5% 碳酸氢钠溶液16ml)。
(6)生理维持液:即4份10%葡萄糖溶液,1份0.9%氯化钠溶液,再加10%氯化钾溶液15ml的混合溶液,张力为1/3张。
(7)3:1或4:1溶液:是3份或4份10%葡萄糖溶液与1份0.9%氯化钠溶液的混合溶液,总份数是4或5,即为1/4张或1/5张(约相当于血浆渗透压的1/4或1/5)。
多作为婴儿时期维持生理需要的维持液。
因新生儿肾功能尚不健全,对氯化钠的负荷量较小,故用1/5张溶液为佳。
用于新生儿的4:1溶液亦可称基本液。
4:1液的简便配制方法:5%葡萄糖溶液500ml加入10%氯化钠溶液10ml。
(8)2:1等张含钠液:即2份0.9%氯化钠溶液与1份 1.8 7%乳酸钠(或1.4%碳酸氢钠)溶液的混合溶液。
2:1等张含钠液简单配制方法:5%葡萄糖溶液500ml加10%氯化钠溶液30ml及11.2%乳酸钠溶液30ml(或5%碳酸氢钠溶液47ml)。
