二氧化碳的制备性质及相对分子量的测定课件
二氧化碳的制取和性质-说课课件 (1)

反应原理:CO2+Ca(OH)2=CaCO3↓+H2O
CO2能使澄清的石灰水变浑浊。
长丰县城关中学 缪康杰
(检验CO2的常用方法)
吹水变“牛奶”
26
二氧化碳的制取和性质
二 氧 化 碳 的 制 取 和 性 质 实 验 .mp4
长丰县城关中学 缪康杰
27
二氧化碳的制取和性质
根据实验台上的仪器和药品 进行二氧化碳制取及性质的实验验证
检验方法
长丰县城关中学
12
二氧化碳的制取和性质
六、过程设计 1、实验室制取气体的思路和方法 2、实验室制取二氧化碳的原理 3、实验室制取二氧化碳的装置 4、收集二氧化碳的方法 5、实验室制取和收集二氧化碳的步骤 6、二氧化碳气体性质的检验
长丰县城关中学 缪康杰
13
二氧化碳的制取和性质
方案实践
长丰县城关中学 缪康杰
18
二氧化碳的制取和性质
收集装置:
气体的物理性质
密度
溶解性
a
b
c
d
缪康杰
e
19
长丰县城关中学
二氧化碳的制取和性质
六、过程设计 1、实验室制取气体的思路和方法
2、实验室制取二氧化碳的原理
3、实验室制取二氧化碳的装置 4、收集二氧化碳的方法 5、实验室制取和收集二氧化碳的步骤 6、二氧化碳气体性质的检验
二氧化碳的制取和性质
长丰县城关中学
缪康杰
1
二氧化碳的制取和性质
一、教材分析、学情分析 二、教学目标制定 三、实验内容设计 四、实验环境设计
五、教法学法设计
六、过程设计
七、实验评价
八、教学反思
长丰县城关中学 缪康杰
二氧化碳的实验室制取与性质PPT课件2(2份) 人教版
• 满意答案 • ~因为可乐雪碧属于碳酸饮料,长期喝的
话会倒至钙的流失,从而使牙齿缺钙.所以 你现在牙齿咬不动很硬的东西.我建意你 最好不要再喝这些饮料了!!赶快补钙吧~
•
25、你不能拼爹的时候,你就只能去拼命!
•
26、如果人生的旅程上没有障碍,人还有什么可做的呢。
•
27、我们无法选择自己的出身,可是我们的未来是自己去改变的。励志名言:比别人多一点执着,你就会创造奇迹
现象
蜡烛熄灭了
二氧化碳不燃烧也不支持燃烧
分析
且比空气密度大
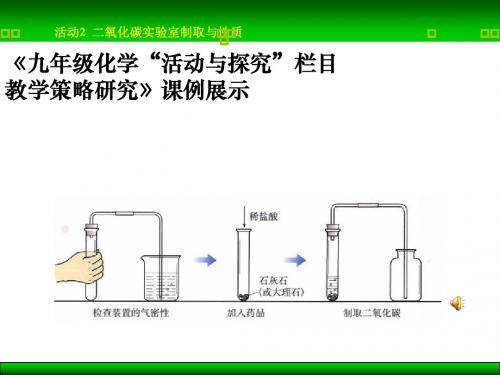
活动2 二氧化碳实验室制取与性质
4.溶解性实验
现象 分析
软塑料瓶变瘪了.
因为二氧化碳能溶于水,使瓶内的气体减少, 压强变小,所以瓶子变瘪。
活动2 二氧化碳实验室制取与性质
试一试
• 怎样用实验证明碳酸型饮料(如汽水)中 含有二氧化碳?请试一试。
• 为什么说常喝雪碧对牙齿不好?
活动2 二氧化碳实验室制取与性质
• 满意答案 • ~因为可乐雪碧属于碳酸饮料,长期喝的
话会倒至钙的流失,从而使牙齿缺钙.所以 你现在牙齿咬不动很硬的东西.我建意你 最好不要再喝这些饮料了!!赶快补钙吧~
活动2 二氧化碳实验室制取与性质
活动2 二氧化碳实验室制取与性质
通入澄清石灰水,变白色浑浊
CO2 + Ca(OH) 2
H2O +CaCO3
2.向两支试管中分别加入约2mL蒸馏水,然后各滴 活动2 二氧化碳实验室制取与性质 入1~2滴石蕊溶液,观察试管中溶液的颜色。将
其中一支试管静置。向另一只试管中通入二氧化
碳,观察现象,并与静置的试管中溶液的颜色进
行对比。将通入二氧化碳的试管放在酒精灯的火
《二氧化碳的制取和性质》教学课件

H2 无色 无味
无色
比空气小得多 难溶于水
CO2 无色 无味 无色 比空气大 微溶于水
世界闻名的“杀狗洞”
在意大利的那不勒斯附近,有个世界闻名的“ 杀狗洞”,这个山洞是肓肠结构、洞口在上。任 何一只健壮的狗走进去,过不多久,就会倒毙在 洞中,而人走进去却安然无恙?这是什么原因?
二氧化碳密度比空气 大,不能供给呼吸.
D、二氧化碳→光合作用→有机物→动植物残体 →地下漫长反应→煤、石油、天然气→燃烧→ 二氧化碳
冷藏食品 人工降雨 5.制汽水: 微溶于水
温室效应原理
二氧化碳气体具有吸热和 隔热的功能。它在大气中 增多的结果是形成一种无 形的玻璃罩,使太阳辐射 到地球上的热量无法向外 层空间发散,其结果是地 球表面变热起来。因此, 二氧化碳也被称为温室气 体。
讨论:温室效应有什么利弊?
适度的温室效应能保 证地球上的气温衡定,适 于动植物生存。但由环境 污染引起的温室效应是指 地球表面变热的现象。 它会带来以下列几种严重 恶果: 1) 地球上的病虫 害增加; 2) 海平面上升; 3) 气候反常,海洋风暴 增多; 4) 土地干旱,沙 漠化面积增大。
界
中
你能得到
的
死亡的生物
哪些信息?
碳 循
CO2 光合作用
呼吸
水生植物
环
腐败生物
煤 石油和天然气
3.碳循环主要的几种形式(主要通过CO2来进行)
A、二氧化碳→光合作用→有机物→植物呼吸 作用→二氧化碳
B、二氧化碳→光合作用→有机物→动物吸收 →体内氧化→二氧化碳
C、二氧化碳→光合作用→有机物→动植物残体 →微生物分解作用→二氧化碳
二:二氧化碳的化学性质
既不能燃烧,也不能支持燃烧;不能供给呼吸。
浙教版科学二氧化碳二氧化碳的制取和性质研究教学PPT(精选)课件

归纳提升:
科学探究永无止境!敢于思考、勇于探索
甲装置
乙装置
丙装置
装置评价:
操作简单 不便于添加药品 不能控制反应停止
装置评价:
操作简单 便于添加药品 不能控制反应停止
装置评价:
节约药品 取用方便
实验讨论: 图3-61是某学生设计的实验室制取并收集二 氧化碳气体的装置图。指出图中的错误之处, 并说明原因。
①长颈漏斗下端伸入太短, 没有伸入液面以下,导 致 气体从漏斗中逸出。
②集气瓶中的导管伸入太 短,没有接近底部,导致收 集的气体不纯。
二、二氧化碳的性质研究
学生分组实验二:试验二氧化碳性质 4. 车迟国三妖和唐僧斗法,(虎力大仙 )要和唐僧比赛求雨,(鹿力大仙)要和唐僧比赛坐禅,(洋力大仙 )和唐僧比试隔板猜枚
二氧化碳的性质
1、二氧化碳的物理性质
二氧化碳是一种无色无味的气体。
能溶于水,通常 1体积水中能溶解1体积的 CO2 密度比空气大。
低温下可液化成无色液体,也可凝固成雪状固体。
2、二氧化碳的化学性质
一般情况下,二氧化碳不能支持燃烧,也不能燃烧。
不能供给呼吸。
CO2 + Ca(OH)2 CO2 + H2O
正确组合 :CDBA 1、语境表达:话题统一,句序合理,注意过渡、衔接和呼应。还要适应语言环境,注意场合、注意说话对象、注意文明礼貌。格式:
礼貌用语+表达内容+询问 题目就是文章的眼睛,归纳这类文章的主要内容,就可以借助文章的标题。 要点概括:
D
学生分组实验一:利用乙装置制取并收集两瓶二氧化碳
思考:收集满两瓶二氧化碳后, 反应还在进行,怎么办?
1.反应原理 CaCO3+2HCl=CaCl2+H2O+CO2↑
浙教版科学二氧化碳的制取、性质与用途PPT(精选)课件

用酒精灯加热颜色呈红色的那支试管,颜色 如何变化?
现象:红色的溶液又变成了紫色
解释:碳酸很不稳定,很容易分解。
H2CO3
CO2 + H2O
通过以上的活动,你能总结出了二氧化碳 的化学性质了吗?
2、二氧化碳的化学性质
①. 一般情况下,二氧化碳不能支持燃烧,也 不能燃烧。
肢体语言是舞台呈现的组成部分,并且是舞台呈现中不可或缺的部分。肢体语言与任何道具和设备等辅助措施都不一样,它是舞台呈
就凝结成雾。 现的途径和必要手段。舞台呈现的效果从肢体语言的应用开始就发生了巨大的变化。在整个呈现过程中,肢体语言的表现方式、程度
等要素的任何细微变化都会对效果产生极大的影响。肢体语言也是表演者获得自我角色认同和观众共鸣的重要途径。 案件定性:冤案 8.用农民服饰的简朴盛赞他们性格的淳厚质朴。 全文翻译 16. 在车迟国,国王受到了妖精的蛊惑,受苦的是(和尚 ),在比丘国,国王受到妖精的迷惑,受苦的是(幼儿 )。 2、一张为都市所折磨而成的白脸,同一件称身软料细毛衣服,在一个小家碧玉心中所能引起的是一种如何幻想。 作者是冰心,原名谢婉莹,中国现代文学史上第一位著名女作家。这两作品是在受到了印度诗人泰戈尔的《飞鸟集》的影响下写成的。 包括三方面的内容: 《一个爱惜鼻子的朋友》:民国十年,那是一个激进的时代,“两湖青年”中弥漫着一种“对革命的狂热”。旧地重游,三个同乡的 面容逐渐显影。这三个朋友,一个姓杨,一个姓韩,一个姓印,都是野性环境和狂飙时代陶冶下的青年人。此篇的主人公就是这个 “印瞎子”: 1、秋天的树叶就是这样五彩缤纷,黄的如金,绿的如玉,红的如火等等,把秋姑娘打扮得格外妖娆。一阵凉风拂过,金黄的树叶,摇 拽着一把把小扇子,从空中飘飘而下,似乎在诉说着一个美丽的童话。
实验项目 二氧化碳的制备及其相对分子质量的测定

实验项目二氧化碳的制备及其相对分子质量的测定二氧化碳(CO2)为空气中常见化合物之一,被认为是造成温室效应的主要来源。
常温下CO2是一种无色无味气体,密度略大于空气,能溶于水,并生成碳酸。
液态CO2和超临界CO2均可作为溶剂,其超临界比液体状态具有更高的溶解性(具有与液体相近的密度和高溶解性,并兼备气体的低粘度和高渗透力)。
液体CO2可作为织物的清洗剂,洗涤后液体CO2可通过减压变成气体很容易和织物分离,完全省去了用传统溶剂清洗带来的复杂后处理过程。
液态CO2蒸发时会吸收大量的热,当它释放大量的热则凝成固体CO2,俗称干冰。
干冰的使用范围很广,在食品、卫生、工业、餐饮及人工降雨等领域都有应用。
本实验由大理石和稀盐酸在启普气体发生器中反应制得二氧化碳,然后根据阿伏伽德罗定律的基本原理测定其相对分子质量。
一、实验目的1. 学习气体相对密度法测定相对分子质量的原理和方法。
2. 加深理解理想气体状态方程式和阿佛加德罗定律。
3. 巩固启普气体发生器的使用,熟练掌握气体的发生、净化、干燥和收集等基本操作。
二、实验原理阿伏伽德罗定律:同温、同压、同体积的气体含相同的分子数,即摩尔数相同。
根据阿伏伽德罗定律,对于p、V、T相同的A、B两种气体,若以m A、m B分别代表体积的A、B两种气体的质量,M A、M B分别代表A、B两种气体的相对分子质量。
其理想气体状态方程式分别为:对于气体A: p V=m A/M A RT对于气体B: p V=m B/M B RT由以上两式整理得:m A/ m B =M A /M B通过上式可知,利用相同温度、体积、压强下的二氧化碳质量(m CO2)、空气质量m空气和已知的空气平均相对分子质量可计算出二氧化碳的相对分子质量(M CO2)。
先根据实验时测得的大气压(p)和室温(T)由理想气体状态方程计算得到体积为V的空气质量m空气,再利用实验测得的(CO2 + 瓶+ 塞)的平均总质量及(空气+ 瓶+ 塞)的总质量G1(g)差值即m CO2﹣m空气,计算得到同体积的二氧化碳气体质量m CO2。
《二氧化碳的实验室制取与性质》PPT课件

与水的反应等。
二氧化碳的应用
03
介绍了二氧化碳在工业生产、灭火、制冷等领域的应用。
课程收获与感悟
掌握了二氧化碳的实验室制取方法和性质
通过本次课程,我深入了解了二氧化碳的实验室制取方法和性质,对二氧化碳有了更加全面 的认识。
提高了实验技能
通过实验操作,我提高了自己的实验技能,包括实验设计、操作规范、数据记录等方面。
说是非常重要的基础知识。
本课程旨在通过实验操作和理论 学习相结合的方式,帮助学生深 入了解二氧化碳的制取和性质。
课程目的
01
02
03
04
掌握二氧化碳的实验室制取方 法,包括反应原理、实验步骤
和注意事项等。
了解二氧化碳的物理性质和化 学性质,如颜色、气味、密度、
溶解性、化学稳定性等。
培养学生的实验技能和动手能 力,提高学生的实践能力和创
化工原料
二氧化碳是许多化工产品 的原料,如尿素、碳酸钠 等。
医学应用
呼吸刺激剂
在急救医学中,二氧化碳可作为呼 吸刺激剂,用于刺激呼吸中枢,促 进患者呼吸。
造影剂
二氧化碳可用于医学影像学中的造 影剂,帮助医生更清晰地观察患者 体内结构。
农业应用
气肥
二氧化碳是植物光合作用的原料之一,适量增加大气中二氧化 碳的浓度可以促进植物生长,提高产量。因此,在温室大棚等 封闭环境中,常使用二氧化碳作为气肥。
探索创新应用
我将积极探索二氧化碳的创新应用, 寻找更多的利用途径,为可持续发 展做出贡献。
THANKS
感谢观看
高压、高温等危险源的识别与 防护:使用耐压、耐高温设备, 确保操作安全。
废气、废液、废渣的处理:分 类收集,妥善处理,防止污染 环境。
二氧化碳的性质和制法第1课时二氧化碳的性质和用途ppt课件

澄清石灰水变 ______浑__浊______
______________
二氧化碳能与澄清 石灰水反应
5.3 二氧化碳的性质和制法
互动探究
探究点一 二氧化碳的性质
[情景展示] 1.二氧化碳的物理性质
5.3 二氧化碳的性质和制法
[问题探究] 二氧化碳的物理性质是什么呢?
[思考交流]
5.3 二氧化碳的性质和制法
5.3 二氧化碳的性质和制法
[归纳总结] 用途:(1)化工原料:用于制造汽水、纯碱、化肥;(2)干冰易升 华吸热,可用作制冷剂和用于人工降雨;(3)灭火:因为二氧化 碳不燃烧也不支持燃烧,且密度比空气的大;(4)气体肥料:是 植物进行光合作用的基本原料,是保证人类氧气和食物循环供 给的重要物质。影响:二氧化碳排放量增多,会使人窒息,引 起温室效应。温室效应会引起地球的气温上升,导致冰川融化, 海平面升高,淹没沿海城市,引起气候反常,生态环境恶化,
1.CO2的产生途径:_动__植__物_的__呼__吸_作__用__、_含__碳_燃__料__的_燃__烧__、________ _____微__生__物_的__分__解_作__用_______________。 2.CO2的消耗途径:_绿__色_植__物__的_光__合__作_用_______。 [注意] CO2 不是空气污染物。CO2会参与大气中的碳循环,是 氧气的间接来源。
7.如图31-4为自然界中碳循环示意图。
5.3 二氧化碳的性质和制法
(1)海洋能够吸收二氧化碳,其原因之一是二氧化碳可以跟水反应, 请写出该反应的化学方程式:__CO_2_+_H_2O_=_=_=H_2_CO_3_______________。 (2)请验证人和动物呼出的气体中含有二氧化碳: ______C_a_(O_H__)2_+_C_O__2=_=_=_C_a_C_O_3↓__+__H_2O___(用化学方程式表示)。 (3)请据图简述二氧化碳对生活和环境的影响(各写出一条即可)。 利:_光__合_作__用__(或__化_工__产__品_)_的_原__料__________________________。 弊:__过__多__会_引__起_“_温__室_效__应_”_(_合_理__即_可__)______________________。
《二氧化碳的制取和性质》教学课件

普利斯特里实验
英国科学家普利斯特曾做过如下实验:在甲、乙两个 密闭的玻璃容器内,甲中放一只小白鼠,乙内放了一盆绿 色植物和一只小白鼠。分别给予足够的光照,发现小白鼠 在乙容器中比在甲容器中的存活时间长许多。
问题: 植物光合作用释放氧气 (1)此实验说明了植物 。 (2)实验中甲是乙的对照。为使实验更为可靠,这两容器
甲
A
照 光 小 时 2
检 查 淀 粉
B 乙 甲、乙两套装置有什么主要区别? 甲中A内放的是氢氧化钙溶液 ,乙中B内放的是 清水。 随着时间的延长,甲、乙装置的空间内,空气成 分会发生什么变化?
甲装置内空气中的二氧化碳比乙内二氧化碳量大 大减少。
(1)A中叶片检查淀粉时,叶片___ _______; 不显蓝色 显蓝色 B中叶片检查淀粉时,叶片____。
以后,他每天只用纯净的雨水浇灌树苗。为防止灰尘落入 ,他还专门制作了桶盖。五年以后,柳树增重80多千克, 而土壤却只减少了100g。因此,海尔蒙特作出何种推断? ——水分是植物体自身制造的原料。 但是当时他却没有考虑到空气的作用。是谁首先想到 植物的生长与空气的作用有关的呢?是一位英国科学家普
利斯特利。
4. CO2固体叫干冰:作致冷剂
冷藏食品 人工降雨 5.制汽水: 微溶于水
光合作用与呼吸作用的关系
项目 ①部位 光合作用 含叶绿体的 细胞 呼吸作用 活 细胞
区 ②与光的关系 在 光 下才能进行 有光无光 都能进行 别 ③气体变化 吸收 CO2 放出 O2 吸收 O2 放出 CO.2 制造 有机物 分解有机物 ④物质变化 贮藏 能量 释放能量 ⑤能量变化 ⑥呼吸作用所分解的 有机物 ,正是光合作用的产物; 联 呼吸作用所释放的 能量 ,正是光合作用贮藏在有 系 机物中的 化学能 ,植物进行光合作用所需要的能量 正是呼吸作用所 释放 的能量。
实验4二氧化碳相对分子质量的测定.pptx

• 14、Thank you very much for taking me with you on that splendid outing to London. It was the first time that I had seen the Tower or any of the other famous sights. If I'd gone alone, I couldn't have seen nearly as much, because I wouldn't have known my way about.
同数目的分子。因此 ,在同温同压下,同 体积的两种气体的质量之比等于它们的相 对分子质量之比,即
M1/M2=W1/W2=d
(2)本实验中把同体积的二氧化碳气体与空气(其 平均相对分子质量为29.0)相比。这样二氧化碳 的相对分子质量可按下式计算:
M co2=Wco2×M空气/W空气=d空气 ×29.0
▪ 最后在瓶内装满水,塞好塞子(注意塞子的位置),在台秤上称重,精 确至0.1g。记下室温和大气压。
五、数据记录和结果处理
室温t(℃) ____ ,T(K) ____ 气压p(Pa) ____ (空气+瓶+塞子)的质量A ____ g (二氧化碳气体+瓶+塞子)的质量B____ g (水+瓶+塞子)的质量C____ g 瓶的容积V=(C-A)/1.00____ mL
• 17、一个人如果不到最高峰,他就没有片刻的安宁,他也就不会感到生命的恬静和光荣。上午8时47分46秒上午8时47分08:47:4620.8.1
谢谢观看
二氧化碳相对分子质量的测定
H 2SO4
二氧化碳的性质和制法ppt课件

精选ppt课件
32
知识网络: ①C
②
烧完 全
燃
CO
点燃 O2
高温 C CO2
解不
H2O
稳 定
分
Ca(OH)2
HCl 或高温
CaCO3
H2CO3
精选ppt课件
33
CO
(两个反应)②
C
④
③ CO2
①
⑦ CaCO3
⑧ (两个反应) ⑤
⑥ H2CO3
点燃
① C+O2
CO2
② 2C+O2 点燃 2CO C+CO2 高温 2CO ③ 2CO+O2 点燃 2CO2
8、把二氧化碳气体通过__紫__色石蕊试液,石
蕊试液变 __红__色,该反应的化学方程式是 __CO_2+_H2_0 =_H_2C_O3_ ,将溶液加热又变成 _紫__色,反应方程式为_H_2C_O_3 =_H_2O_+C_O_2。
精选ppt课件
21
9、久盛石灰水的试剂瓶的内壁往往形成 一层
白色不溶于水的物质,该物质是__C_a_C__O_3_, 有关化学方程式是_CO_2+_Ca_(O_H)_2=_Ca_CO_3_+H_2O。
1、二氧化碳的制取
• 在实验室里,二氧化碳常用稀盐酸和大理石或石灰石反 应制得,化学方程式如下:
CaCO3 + 2HCl====CaCl2 + H2O + CO2↑ 碳酸钙 盐酸 氯化钙 水 二氧化碳
精选ppt课件
43
一、药品及反应原理的探究:
实验 编号
1
2
3
4
实验药品
碳酸钠和 稀盐酸
二氧化碳的制备性质及相对分子量的测定ppt课件

精选课件ppt
2
实验药品:
凡士林、大理石、稀盐酸(6mol/L) 、石蕊试液、石灰水、镁条、铁丝、 小蜡烛、氢氧化钠、无水氯化钙、、饱和碳酸氢钠溶液、浓硫酸
实验器具:
250毫升启普发生器 1个 木夹(或竹夹)1个 注射器 1只 锥形瓶1个 100毫升烧杯 1只 集气瓶4个 酒精灯 1个 铁架台1架 剪刀1把 托盘天平 1台
相对误差:
精选课件=ppt___________
29
数据记录与结果处理 第一次测定: 用250 ml 碘量瓶收集,温度:25.0℃,大气压:606.5 mmHg
实验次数
1
2
3
4
5 平均值
瓶+空气质量 A 75.6527 75.6527 75.6527 75.6527 75.6527 75.6527
MCO2=(mCO2/m空气)×29.0 因此,在实验中只要测出一定体积二氧化碳的质量,计算
出实验条件下同体积空气的质量,即可得到二氧化碳的相对分 子量。
精选课件ppt
28
数据记录和结果处理
室温T:______________
气压P:______________
(空气+瓶子+塞)的质量A:________g
精选课件ppt
4
一、二氧化碳的制备 1 启普发生器装置实验步骤:
从启普发生器的气体出口加入大理石,加入量 不超过中间球体积的1/3,关闭气体出口,再从球 形漏斗加入6mol/L的盐酸。打开旋塞,盐酸即从底 部通过狭缝上升与大理石作用,产生二氧化碳气体。
由于大理石中含有硫,所以制备的二氧化碳气 体中,常含有硫化氢、酸雾、水汽等杂质,此时, 通过KMnO4(1mol/L)、浓H2SO4除去。
二氧化碳的制取和检验课件

是什么类型?采用这些装置的原因是什么?
实验室制取二氧化碳发生装置是固液常温型, 收集装置是向上排空气法;因为反应是固体与液 体常温下发生的,二氧化碳可溶于水且密度比空 气大。
发生装置
收集装置
3、如何检验集气瓶中收集的气体是二氧化碳?如何 检验二氧化碳气体已经集满? 向集气瓶中倒入少量澄清的石灰水,振荡,石灰水 变浑浊,证明气体是二氧化碳;用燃烧的木条放在 集气瓶口,如果木条熄灭,说明气体已经集满。
4、实验室制取二氧化碳的实验步骤有哪些?请用最 简单的字或词语表达出来。 步骤包括连接仪器、检查气密性、装入药品、固 定仪器、收集气体、验满、气体检验、整理仪器。 可简单表示为:连、检、装、定、集、验。
二、实验探究
三、评价和总结
通过本节实验,你学得了什么知识和技能呢?
二氧化碳的制取和检验
实验目的
实验技能:掌握二氧化碳的实验室制法;练 习仪器连接、气密性检查、药品取 用、气体收集、二氧化碳检验等实 验基本操作。
过程方法:讨论归纳,实验探究,交流提高 情感目标:获得成功喜取二氧化碳气体的原理是什么?
实验室用大理石或石灰石与稀盐酸反应制取二氧 化碳; 化学方程式表示为
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验室制取二氧化碳原理: 2HCl+CaCO3 → CaCl2+ CO2↑ +H2O
二氧化碳的制备性质及相对分子量的测定
一、二氧化碳的制备 1 启普发生器装置实验步骤:
从启普发生器的气体出口加入大理石,加入量 不超过中间球体积的1/3,关闭气体出口,再从球 形漏斗加入6mol/L的盐酸。打开旋塞,盐酸即从底 部通过狭缝上升与大理石作用,产生二氧化碳气体。
加入反应物后,盖紧塞子,塞子外加上适量水 作密封,静置反应一定时间后,慢慢打开塞子,让 密封水沿瓶塞流入锥形瓶,再用水将瓶口及塞子上 的碘液洗入瓶中。
二氧化碳的制备性质及相对分子量的测定
碘量瓶
二氧化碳的制备性质及相对分子量的测定
称量瓶(weighing bottle) 带有磨口塞的筒形的玻璃瓶,用于差减法称量试样
实验3 二氧化碳的制备、 性质及相对分子量的测定
二氧化碳的制备性质及相对分子量的测定
实验目的: 1.熟练掌握制取和收集二氧化碳的方法及 性质实验的规范操作。 2.实习二氧化碳制取及化学性质演示实验 的讲解方法。 3.学会测定二氧化碳相对分子量的实验方 法。学习气体密度法测定气体相对分子量 的原理和方法,学习启普发生器的使用和 称量的操作,了解气体净化和干燥的方法。
由于大理石中含有硫,所以制备的二氧化碳气 体中,常含有硫化氢、酸雾、水汽等杂质,此时, 通过KMnO4(1mol/L)、浓H2SO4除去。
二氧化碳的制备性质及相对分子量的测定
2 简易装置实验步骤:
(1)按图安装好制取二氧化碳的实验装置。
(2)锥形瓶中加入10克左右块状大理石,塞紧带 有长颈漏斗和导管的橡皮塞。
制取实验仪器和装置:
二氧化碳的制备性质及相对分子量的测定
二氧化碳的制备性质及相对分子量的测定
二氧化碳测定
二氧化碳的制备性质及相对分子量的测定
要点:
(1)实验室制取二氧化碳,如选用大理石为原料, 则不能选用稀硫酸。 因为生成的碳酸钙是微溶性物 质,它包裹在大理石表面,使酸液不能与大理石接 触, 从而使反应中止。
二氧化碳的制备性质及相对分子量的测定
实验药品:
凡士林、大理石、稀盐酸(6mol/L) 、石蕊试液、石灰水、镁条、铁丝、 小蜡烛、氢氧化钠、无水氯化钙、、饱和碳酸氢钠溶液、浓硫酸
实验器具:
250毫升启普发生器 1个 木夹(或竹夹)1个 注射器 1只 锥形瓶1个 100毫升烧杯 1只 集气瓶4个 酒精灯 1个 铁架台1架 剪刀1把 托盘天平 1台
取约10cm长的镁条,用砂纸或小刀把它一端的氧化膜除尽,用 坩埚钳夹持另一端,放在酒精灯上点燃后,随即伸入盛有二氧 化碳的集气瓶内,镁条会继续燃烧,并发出耀眼白光。燃烧后, 集气瓶的瓶壁特别是瓶底出现有白色粉末,同时还有黑色斑点。 〔备注〕 1.氧化镁的生成热是612.4kJ/mol,二氧化碳的生成热是 393.4kJ/mol,因此在二氧化碳中燃烧镁,可以把二氧化碳还原 成碳。 2.除净镁带表面的氧化物和通入足量的二氧化碳是本实验的 成败关键。 3.燃烧产物白色粉末是氧化镁,黑色固体是单质碳。
为了测定碘量瓶的容积,可在瓶内装满水,塞好 塞子,(注意:要求瓶内没有气泡,瓶外没有水珠)。 在台秤上称重并记录C。
二氧化碳的制备性质及相对分子量的测定
碘量瓶: 在锥形瓶口上使用磨口塞子,并且加一水封槽。
用于碘量分析,盖塞子后以水封瓶口。 碘量瓶的用途:
一般为碘量法测定中专用的一种锥形瓶。也可 用作其他产生挥发性物质的反应容器。 用法:
(2)收集二氧化碳气体也可用排水法,但水槽中 的液体最好选用饱和的碳酸氢钠溶液, 它不会使二 氧化碳损失。
(3)注意气密性;
(4)导管口要在瓶底处,因为二氧化碳的比重大 于空气。
二氧化碳的制备性质及相对分子量的测定
二、二氧化碳性质实验
1二氧化碳通入滴加过石蕊试剂纯净水中,观察 试剂颜色变化。
2二氧化碳通入澄清石灰水,观察澄清石灰水的 变化。
3 把充满二氧化碳的集气瓶中的二氧化碳倒入放 有点燃的蜡烛的烧杯里,观察蜡烛火焰变化。
4 点燃用坩埚钳夹住的镁条,放入盛满二氧化碳 的集气瓶中,观察集气瓶内的现象。
2Mg+CO2 → 2MgO+C 二氧化碳的制备性质及相对分子量的测定
镁在二氧化碳中燃烧 〔用品〕 二氧化碳发生装置、集气瓶、坩埚钳、酒精灯、砂纸、小刀。 〔操作〕
二氧化碳的制备性质及相对分子量的测定
三、二氧化碳分子量的测定 取一只洁净而干燥的碘量瓶,盖好瓶塞,在电子
天平上称量并记录空气、瓶子、塞子的质量A。 拔去塞子,把启普发生器装置上的导气管插入瓶
底,等4-5分钟后,轻轻取出导气管,盖好瓶塞,在 原来的天平上称重并记录B1。为了保证瓶内空气完 全被二氧化碳排出,重复通入二氧化碳和称量的操作 并记录B2,直至两次称量结果相差不超过2毫克为 止。记录二氧化碳、瓶子、塞子的质量B。
(3)气体导出管放入集气瓶中,导管口应处在集 气瓶的瓶底处。
(4)通过长颈漏斗加入适量的稀盐酸,锥形瓶中 立刻有气体产生。
(5)片刻后,划一根火柴,把燃着的火柴放到集 气瓶口的上方, 如果火柴很快熄灭说明集气瓶中 已经受集满 二氧化碳气体,盖好毛玻璃片, 将集 气瓶口向上放在桌子上备用。
二氧化碳的制备性质及相对分子量的测定
脱脂棉 1袋
洗瓶 2只(带塞)
试管 2只
锥形瓶 一个
平底烧瓶1只
长颈漏斗 1只
长颈漏斗1只
干燥管 1个
50毫升烧杯1只 100mL塑料集气瓶 1只
玻璃导管 2 段
水槽 1个
分液漏斗 1个
矿泉水瓶底1个
托盘天平 1台
毛玻片4片
玻璃导管1段
洗气瓶2个
电子天平(分析天平) 1台
二氧化碳的制备性质及相对分子量的测定
的容器。因有磨口塞,可以防止瓶中的试样吸收空气中 的水分和CO2等,适用于称量易吸潮的试样。
称量瓶是一种常用的实验室玻璃器皿,一般用于准 确称量一定量的固体。又称称瓶。精确称量分析试样所 用的小玻璃容器。一般是圆柱形,带有磨口密合的瓶盖。
称量瓶的规格以外径×高(cm)表示,分为扁形、筒形 两种外形。根据材料有普通玻璃称量瓶和石英玻璃称量 瓶。
