高中化学常见离子检验(可以直接打印)
高中化学离子检验(全)

高中化学离子检验(全)高中化学离子检验H+的检验使用试剂:石蕊试液,Na2CO3溶液或pH试纸。
操作步骤和反应现象:将含有H+的溶液取出放入试管中,滴加Na2CO3溶液,会产生气泡。
将溶液用玻璃棒蘸取少量滴到蓝色石蕊试纸或pH试纸上,会呈现红色。
离子方程式:2H++CO32- CO2↑+H2O。
Na+、K+的检验使用试剂:XXX、HCl。
操作步骤和反应现象:取含钠离子的溶液,用烧过的铂丝蘸溶液或固体少许在酒精灯焰上灼烧,观察会出现黄色火焰。
用蘸HCl溶液烧铂丝进行清洗,直到看不出黄色为止,再取K+盐或其溶液在酒精灯焰上灼烧,透过钴玻璃片观察会出现紫色火焰。
NH4+的检验使用试剂:浓HCl、NaOH溶液、红色石蕊试纸。
操作步骤和反应现象:取含NH4+的盐或溶液加入浓NaOH溶液后加热,会产生气体,接触湿润红色石蕊试纸会变蓝。
或者用玻璃棒蘸上浓HCl挨近上述气体时冒大量白烟。
离子方程式或化学方程式:NH4++OH- NH3↑+H2O,NH3+H2O NH3•H2O,NH3+HCl NH4Cl。
Mg2+检验使用试剂:NaOH溶液。
操作步骤和反应现象:将含Mg2+的溶液中加入NaOH溶液,会生成白色不溶于过量NaOH的沉淀。
离子方程式:Mg2++2OH- Mg(OH)2↓。
Al3+的检验使用试剂:NaOH溶液,HCl溶液。
操作步骤和反应现象:在含有Al3+的溶液中滴加少量NaOH溶液,会产生白色絮状沉淀。
过量NaOH溶液沉淀会溶解,白色状沉淀也会溶于盐酸。
离子方程式:Al3++3OH-Al(OH)3↓,Al(OH)3+OH- AlO2-+2H2O,Al(OH)3+3H+Al3++3H2O。
Cu2+的检验使用试剂:NaOH溶液,NH3•H2O。
操作步骤和反应现象:取含Cu2+的蓝色溶液加入NaOH 溶液,会生成蓝色的沉淀。
再加NH3•H2O振荡,会呈现深蓝色溶液。
离子方程式:Cu2++2OH- Cu(OH)2↓,Cu(OH)2+4NH3 Cu(NH3)4(OH)2.Fe2+的检验使用试剂:NaOH溶液。
高中化学常见离子检验大全(精品范文).doc

【最新整理,下载后即可编辑】(一)常见阳离子的检验方法
2Fe2++ Cl
2Fe3++
2
2Cl-
Fe3++3SCN-=
Fe(SCN)
3
即显红色。
-+8H+
5Fe2+ + MnO
4
5Fe3+ +Mn2++4 H
O
2
(二)常见阴离子的检验方法
【最新整理,下载后即可编辑】 注意:
1.若SO 42-与Cl-同时检验,需注意检验顺序。
应先用Ba(NO 3)2溶液将SO 42-检出,并滤去BaSO 4,然后再用AgNO 3检验Cl-。
2.检验SO 32-的试剂中,只能用盐酸,不能用稀硝酸。
因为稀硝酸能把SO 32-氧化成SO 42-。
3.若Ag +和Ba 2+同时检验,也需注意检验顺序,应先用盐酸将Ag +检验出并滤去沉淀,然后再用稀硫酸检验Ba 2+。
4.若Ag +和Ba 2+同时检验,也需注意检验顺序,应先用盐酸将Ag +检验出
5.若CO 32-和HCO 3-同时检验,应先用足量的BaCl 2溶液将CO 32-检出,静置,取上层清夜用Ba(OH)2或Ca(OH)2检出HCO 3-。
高中化学常见离子检验 可以直接打印

高中化学常见离子检验可以直接打印----5e692b94-7166-11ec-9782-7cb59b590d7d高中化学常见离子检验可以直接打印高中化学常见离子测试(您可以打印&rPar;(一)常见阳离子的检验方法(二)常见阴离子的试验方法1.若so42-与cl-同时检验,需注意检验顺序。
应先用ba(no3)2溶液将so42-检出,并滤去baso4,然后再用agno3检验cl-。
2.在测试SO32-的试剂中,只能使用盐酸,不能使用稀硝酸。
因为稀硝酸可以将SO32-氧化为SO42-。
3.若ag+和ba2+同时检验,也需注意检验顺序,应先用盐酸将ag+检验出并滤去沉淀,然后再用稀硫酸检验ba2+。
4.如果同时测试Ag+和Ba2+,还需要注意测试顺序。
Ag+应首先用盐酸进行测试5.若co32-和hco3-同时检验,应先用足量的bacl2溶液将co32-检出,静置,取上层清夜用ba(oh)2或ca(oh)2检出hco3-三:常见气体的检查物质检验的一般程序及答题要领通常分两步进行。
第一步是取少量样品(如果样品是固体)体的要先配制成溶液)放入容器(通常用试管)。
第二步各取少许溶液,根据要求在试样中加入已知成分和性质的试剂,并根据所发生的现象,进行分析、判断,作出结论。
① 请勿使用原装瓶子进行操作:标识的目的是供将来使用。
如果使用原瓶操作,原瓶试剂会被污染。
应该有“每人吃一点”的字样。
②不许“指名道姓”:结论的得出,来自实验现象,在加入试剂之前,该物质是未知的,应该叙述为“若……(现象),则证明有……”,叙述时不可出现“取某某物质加入某某试剂……”的字样,一般间答顺序为:各取少许→溶解→加入试剂→描述现象→得出结论。
气体检验方法和思路:(1)气体检测的想法一般从以下几个方面考虑①气体的颜色和气味;② ② 水溶液的酸碱度;③③助燃、可燃及燃烧现象和产物;④ ④ 空气的变化;⑤⑤其它特性。
高中化学常见离子检验方法一览表
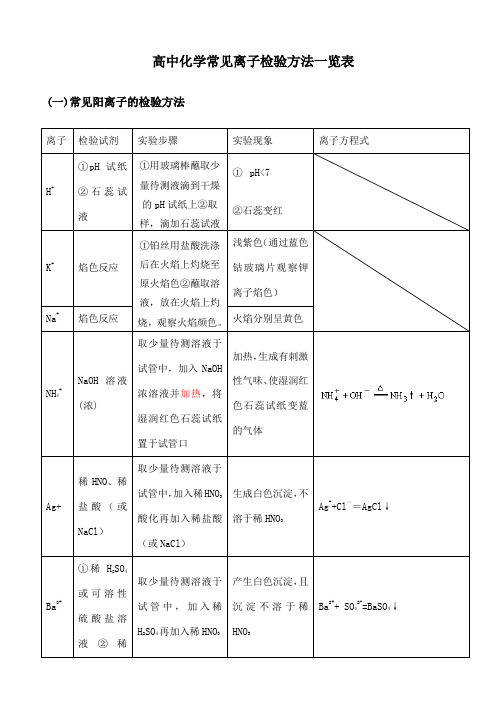
高中化学常见离子检验方法一览表(一)常见阳离子的检验方法离子检验试剂实验步骤实验现象离子方程式H+①pH试纸②石蕊试液①用玻璃棒蘸取少量待测液滴到干燥的pH试纸上②取样,滴加石蕊试液①pH<7②石蕊变红K+焰色反应①铂丝用盐酸洗涤后在火焰上灼烧至原火焰色②蘸取溶液,放在火焰上灼烧,观察火焰颜色。
浅紫色(通过蓝色钴玻璃片观察钾离子焰色)Na+焰色反应火焰分别呈黄色NH4+NaOH溶液(浓)取少量待测溶液于试管中,加入NaOH浓溶液并加热,将湿润红色石蕊试纸置于试管口加热,生成有刺激性气味、使湿润红色石蕊试纸变蓝的气体Ag+稀HNO、稀盐酸(或NaCl)取少量待测溶液于试管中,加入稀HNO3酸化再加入稀盐酸(或NaCl)生成白色沉淀,不溶于稀HNO3Ag++Cl-=AgCl↓Ba2+①稀H2SO4或可溶性硫酸盐溶液②稀取少量待测溶液于试管中,加入稀H2SO4再加入稀HNO3产生白色沉淀,且沉淀不溶于稀HNO3Ba2++ SO42-=BaSO4↓HNO3Fe3+KSCN溶液取少量待测溶液于试管中,加入KSCN溶液变为血红色溶液Fe3++3SCN-=Fe(SCN)3加苯酚取少量待测溶液于试管中,加苯酚溶液显紫色淀粉KI溶液滴加淀粉KI溶液溶液显蓝色2Fe3++2I-=2Fe2++ I2加NaOH溶液加NaOH溶产生红褐色沉淀Fe3++3OH-=Fe(OH)3↓离子检验试剂实验步骤实验现象离子方程式Fe2+①KSCN溶液,新制的氯水①取少量待测溶液于试管中,加入KSCN溶液,新制的氯水①加入KSCN溶液不显红色,加入少量新制的氯水后,立即显红色。
2Fe2+ + Cl22Fe3+ + 2Cl-Fe3++3SCN-=Fe(SCN)3②加NaOH溶液②取少量待测溶液于试管中,加入NaOH溶液并露置在空气中②开始时生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀。
Fe2++2OH —=Fe(OH)2↓4Fe(OH)2十O2+2H2O=4Fe(OH)3(二)常见阴离子的检验方法注意:1.若SO42-与Cl-同时检验,需注意检验顺序。
高中化学中常见离子检验方法总结

高中化学中常见离子检验方法总结高中化学中常见离子检验方法总结一、常见阴离子的检验1.阴离子的初步检验①与稀H2SO4作用,试液中加入稀H2SO4并加热,有气泡产生,可能有CO32-、SO32-、S2-、NO2-或CN-存在,再根据气体的特性不同,再进行判断。
②与BaCl2的作用。
试液中加入BaCl2溶液,生成白色沉淀,可能有SO42-、SO32-、PO43-、S2O32-根据沉淀性质不同进行检验。
③与AgNO3HNO3作用。
试液中加入AgNO3再加入稀HNO3若为白色沉淀为Cl-黄色沉淀可能有I-、Br-和CN-存在,若有黄色沉淀很快变橙、褐色,最后变为黑色,表示有S2O32-存在,Ag2S 为黑色沉淀。
④氧化性阴离子的检验试液用H2SO4酸化后,加入KI溶液和淀粉指示剂,若溶液变蓝,说明有NO2-存在。
⑤还原性阴离子检验a、强还原性阴离子与I2的试验,试液用H2SO4酸化后,加含0.1%KI的I2-淀粉溶液,若其蓝色褪去,可能有SO32-、C2O42-、S2O32-、S2-和CN-等离子存在。
b、还原性阴离子与KMnO4的试验,试液用H2SO4酸化后,加入0.03%KMnO4溶液,若能褪色,可能有SO32-、S2O32-、S2-、C2O42-、Br-、I-、NO2-等离子。
2.个别鉴定反应⑴SO42-加入BaCl2溶液生成BaSO4白色沉淀,该沉淀不溶于稀HCl或稀HNO3Ba2SO42-===BaSO4↓⑵SO32-a、加入BaCl2溶液生成BaSO3白色沉淀,加入稀HCl,沉淀溶解并放出有刺激性气味的气体SO2Ba2SO32-===BaSO3↓BaSO32H===Ba2H2O SO2↑b、加入少量I2-淀粉溶液,蓝色褪去SO32-I2H2O===SO42-2I-2H⑶Cl-加入AgNO3生成AgCl白色沉淀,该沉淀不溶于稀HNO3或稀HCl,但溶于浓NH3·H2OAgCl2NH3·H2O===[Ag(NH3)2]Cl-2H2O⑷Br-a、加入AgNO3生成淡黄色AgBr沉淀,该沉淀不溶于HCl或HNO3中,微溶于浓NH3·H2O。
高中化学中各种离子的检验方法

高中化学中各种离子的检验方法
K+:焰色反应紫色
Na+:焰色反应黄色
加入SO42-产生不溶于稀硝酸的白色沉淀。
Ca2+:焰色反应砖红色,加入Na2CO3后产生白色沉淀
加入NaOH后先产生白色沉淀,后沉淀溶解。
Fe3+:加入KSCN变为血红色或加苯酚变为紫色。
先检验原溶解液无Fe3+,先加强氧化剂(K2Cr2O7、
HNO3、H2O2酸性KMnO4、HClO……)然后检验有没有Fe3+。
一般为蓝色溶液,加入OH-产生蓝色沉淀。
Ag+:加入Cl-产生不溶于稀HNO3的白色沉淀。
NH4+:加入OH-,加热产生无色气体,可使紫色石蕊试纸变蓝。
NO3-:加入H+、Fe产生红棕色气体,或无色气体与O2反应后显红棕色。
CL-:加入Ag+产生不溶于稀HNO3的白色沉淀。
Br-:加入Ag+产生不溶于稀HNO3的浅黄色沉淀。
I-:加入Ag+产生不溶于稀HNO3的黄色沉淀。
SO42-:加入Ba2+产生不溶于稀HNO3的白色沉淀。
加入Ca2+产生白色沉淀,加入H+产生气体,能使品红褪色。
HSO3-:加入Ca2+产生白色沉淀,加入H+产生气体,能使品红褪色。
CO32-:加入Ca2+产生白色沉淀,加入H+产生气体,
不能使品红褪色。
HCO3-:加入Ca2+不产生白色沉淀,加入H+产生气体,不能使品红褪
S2-:加入Cu2+产生黑色沉淀。
高中常见离子的检验完整版

实验现象 ①变红 ②产生无色无味的气体 产生黄色火焰 产生紫色火焰(透过蓝色钴玻璃观察) 产生白色沉淀且沉淀不溶解在过量的 NaOH 溶液中 先产生白色沉淀,后沉淀溶解在过量的 NaOH 溶液中 白色沉淀→灰绿色→红褐色沉淀 先无明显变化,再变红色 产生蓝色沉淀 产生红褐色沉淀 溶液呈血红色 产生蓝色沉淀,加热则沉淀变黑 产生白色沉淀且不溶于稀 HNO3 产生白色沉淀 产生能使湿润的红色石蕊试纸变蓝的气体 ①无色酚酞试液变红 ②紫色石蕊试液变蓝 产生白色沉淀 产生淡黄色沉淀 ①产生黄色沉淀 ②淀粉溶液变蓝 ①产生无色无味能使澄清石灰水变浑浊的气体 ②产生白色沉淀且溶于稀盐酸 ①产生无色无味能使澄清石灰水变浑浊的气体 ②产生白色沉淀且溶于稀盐酸 产生白色沉淀且沉淀不溶于稀 HNO3 ①有气体产生,品红溶液褪色 ②产生白色沉淀且溶于稀 HCl 中,产生刺激性气味的气体 ①生成无色有臭鸡蛋气味的气体 ②产生黑色沉淀 产生红棕色气体,溶液变蓝 ①产生黄色沉淀,溶于稀 HNO3 ②产生白色沉淀,溶于稀 HNO3 先生成白色沉淀,后沉淀溶解
2+ 2+ +
+
HCO3CO32SiO32-
HCO3 SO4 SO3 S
2-
-
2-
2-
NO3 PO4
-
铜屑,浓 H2SO4,加热 ①AgNO3 溶液,稀 HNO3 ②Ba(NO3)2 溶液,稀 HNO3 稀盐l Fe Fe
+
+
Na+
Mg2+
3+
2+
3+
Cu Ba
2+ +
Ag
2+ +
NH4
OHCl I
常见离子的检验方法(表格整理版)
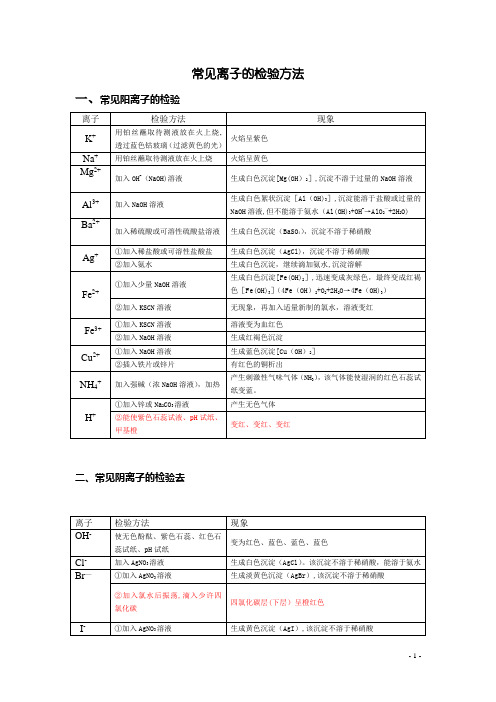
加入稀硫酸或可溶性硫酸盐溶液
生成白色沉淀(BaSO4),沉淀不溶于稀硝酸
Ag+
①加入稀盐酸或可溶性盐酸盐
生成白色沉淀(AgCl),沉淀不溶于稀硝酸
②加入氨水
生成白色沉淀,继续滴加氨水,沉淀溶解
Fe2+
①加入少量NaOH溶液
生成白色沉淀[Fe(OH)2],迅速变成灰绿色,最终变成红褐色[Fe(OH)3](4Fe(OH)2+O2+2H2O→4Fe(OH)3)
②加入Pb(NO3)2溶液或CuSO4溶液
生成黑色的沉淀(PbS或CuS)
CO32—
①加入CaCl2或BaCl2溶液
生成白色沉淀(CaCO3或BaCO3),将沉淀溶于强酸,产生无色、无味的气体(CO2),该气体能使澄清的石灰水变混浊
②ห้องสมุดไป่ตู้入盐酸
产生无色、无味的气体,该气体能使澄清的石灰水变浑浊;向原溶液中加入CaCl2溶液,产生白色沉淀
生成淡黄色沉淀(AgBr),该沉淀不溶于稀硝酸
②加入氯水后振荡,滴入少许四氯化碳
四氯化碳层(下层)呈橙红色
I-
①加入AgNO3溶液
生成黄色沉淀(AgI),该沉淀不溶于稀硝酸
②加入氯水后振荡,滴入少许四氯化碳
四氯化碳层(下层)呈紫红色
③加入氯水和淀粉试液
溶液变蓝
SO42-
先加入HCl再加入BaCl2溶液(加H+防CO32—干扰;加HCl防Ag+干扰;不用HNO3防 SO32—干扰)
生成白色沉淀(BaSO4),该沉淀不溶于稀硝酸
SO32—
①加入盐酸或硫酸
产生无色、有刺激性气味的气体(SO2),该气体可使品红溶液褪色
高中化学——离子检验

高中化学——离子检验1.常见阳离子的检验(1)Fe2+➢与NaOH(少量)生成白色的Fe(OH)2沉淀,迅速变成灰绿色,然后变成沉淀。
红褐色的Fe(OH)3➢往亚铁盐溶液里面加入KSCN溶液,无明显变化,再往里面滴加氯水,溶液变为血红色。
➢往亚铁盐溶液K3[Fe(CN)6]溶液,生成深蓝色沉淀(Fe3[Fe(CN)6]2 (2)Fe3+➢滴加KSCN溶液,溶液变为血红色➢滴加NaOH溶液,生成红褐色的沉淀➢滴加苯酚溶液,溶液变为紫色(3)Ag+➢与可溶性氯盐可产生白色的AgCl沉淀,且该沉淀不溶于稀硝酸。
(氯化银沉淀可溶于氨水,形成银氨溶液)➢与NaOH溶液可生成白色沉淀(不稳定),迅速变成黑色(Ag2O)(4)Al3+➢与NaOH(少量)生成白色沉淀(Al(OH)3),继续滴加,沉淀消失。
➢与氨水反应,生成的沉淀不溶解(5)K+➢通过焰色试验,透过蓝色钴玻璃,火焰呈紫色。
2.常见阴离子的检验(1)Cl-➢先加HNO3酸化,加入AgNO3溶液,生成白色沉淀(AgCl)(2)Br-➢与硝酸银溶液反应,生成浅黄色沉淀(AgBr),且不溶于稀硝酸(3)I-➢与硝酸银溶液反应,生成黄色沉淀(AgI),且不溶于稀硝酸(4)SO42-➢先加盐酸酸化,再加入BaCl2溶液,产生白色沉淀(BaSO4)2-等)注意:酸化是为了排除干扰离子(Ag+、CO32-(5)CO3➢与BaCl2溶液反应,生成白色沉淀(BaCO3),且可溶于稀酸(放出的气体能使澄清石灰水变浑浊)2-(6)SO3➢与BaCl2溶液反应,生成白色沉淀(BaSO3),且可溶于稀酸(生成有刺激性气味的气体)(7)S2-➢与硝酸铅溶液反应,生成黑色沉淀(PbS)➢滴加稀盐酸或稀硫酸,生成有臭鸡蛋气味的气体(H2S)。
高中化学常见离子检验篇

高中化学常见离子检验篇WTD standardization office【WTD 5AB- WTDK 08- WTD 2C】常见物质性质小结之离子检验篇下面这些,完全可以在化学推断题、实验设计题中直接使用。
像亚铁离子这种有多种检验方法的,一般情况下选用第一种,有时候可用第二种,第三种等(如实验条件限制,原溶液中所含离子颜色干扰等)一、阳离子1.氢离子(H+):取少量溶液,滴加紫色石蕊试液或甲基橙试液,溶液显红色,则可证明溶液中含有氢离子。
2.钠离子(Na+):焰色反应,火焰呈黄色。
3.钾离子(K+):焰色反应,透过蓝色钴玻璃观察,火焰呈蓝色。
4.钡离子(Ba2+):取少量溶液,加稀盐酸酸化,无明显现象(排除Ag+),再滴加稀硫酸,析出不溶于稀硝酸的白色沉淀,则可证明溶液中含有钡离子。
5.镁离子(Mg2+):取少量溶液,滴加NaOH溶液,析出白色沉淀且沉淀溶于NH4Cl溶液,则可证明溶液中含有镁离子。
6.铝离子(Al3+):取少量溶液,逐滴滴加NaOH溶液,先析出白色絮状沉淀,然后沉淀消失,则可证明溶液中含有铝离子。
7.银离子(Ag+):取少量溶液,滴加稀盐酸,析出不溶于稀硝酸的白色沉淀,则可证明溶液中含有银离子。
8.铵离子(NH4+):取适量溶液,加入浓的NaOH溶液并加热,放出能使湿润的红色石蕊试纸变蓝的刺激性气味气体,则可证明溶液中含有铵离子。
9.亚铁离子(Fe2+):①取少量浅绿色溶液,滴加NaOH溶液,先生成白色沉淀,迅速变为灰绿色,最后沉淀变为红褐色,则可证明溶液中含有亚铁离子。
(请注意“先”“迅速”“最后”,不要更改) ②取少量浅绿色溶液,加入KSCN溶液,不显红色,滴加少量新制氯水,溶液立即显红色(或血红色),则可证明溶液中含有亚铁离子。
10.三价铁离子(Fe3+):①取少量黄色溶液,滴加KSCN溶液,溶液变为血红色,则可证明溶液中含有三价铁离子。
②取少量黄色溶液,滴加NaOH溶液,生成红褐色沉淀,则可证明溶液中含有三价铁离子。
高一常见离子检验

6、OH-:
试剂: 无色酚酞试液
方法: 向待检物中滴加无色酚酞试 液,若酚酞试液变红,证明未 知物中含OH-。
小结:离子的检验:
离子 使用的试剂 石蕊试液 、锌粉 石蕊、酚酞试液 化学反应 发生的现象 的方程式
常见离子检验
几种重要离子的检验:
1、CO32-:
用试管取少量待检物质,滴加稀盐酸, 若有无色无味的气体放出,则将该气体 通入澄清石灰水,若石灰水变浑浊,则 该物质中含有CO32-或HCO3-
2、SO42-:
H2SO4+ Ba(NO3)2=2HNO3+BaSO4
Na2SO4+ Ba(NO3)2=2NaNO3+BaSO4 K2SO4+ Ba(NO3)2 = 2KNO3+BaSO4
2、如何证明某溶液是NaCl溶液?
3、某溶液中只含有NaOH和Na2CO3两种溶 质,如何设计实验证明CO32-和OH-确实 存在?
练习:
√
有一瓶溶液,可能含Na+、Ba2+、H+、Cl-、 CO32-、SO42-、OH- 中的几种, 现进行如下实验: (1)取试样溶液加入试管中,滴入BaCl2溶 液,有白色沉淀产生,过滤; (2)在滤液中滴入酚酞试液,溶液呈红色; (3)在沉淀中加入稀硝酸,白色沉淀全部溶 解,并产生气泡。 则溶液中一定含有的离子是: Na+、 CO32-、 OH- ; 2+、H+、SO 2- Ba 一定没有的离子是________________ 4 ; Cl- 可能有的离子是: 。
高中化学15种离子鉴定

高中化学几种常见离子的鉴定1、铵根(NH4+)检验用浓NaOH 溶液,现象:有刺激性气味气体产生离子反应式:NH4(++OH(-=NH3 ↑+H2O2、钾离子(K+)试剂:使其盐溶液在无色火焰中灼烧,现象:透过蓝色的钴玻璃看见火焰是紫色,方程式:无(焰色反应是物理变化)3、钠离子(Na+)方法同上,火焰呈黄色4、亚铁离子(Fe2+试剂:氢氧化钠溶液,现象:产生白色沉淀,之后变为灰绿色,最后变成红褐色。
方程:Fe(2++2OH(-==Fe(OH2↓4Fe(OH2 + O2 +H2O==4Fe(OH3↓5、铁离子(Fe3+)试剂:氢氧化钠溶液,现象:红褐色沉淀生成,方程:Fe(3++3OH(-==Fe(OH3↓6、铝离子(Al3+)方法一:加氨水,现象产生白色沉淀,方程:Al(3++3NH3-H2O=Al(OH3↓+3NH4(+ 方法2:加氢氧化钠溶液,现象:产生白色沉淀,加入过量NaOH 溶液后沉淀溶解方程:Al(3++3OH(-=Al(OH3↓Al(OH3+NaOH==NaAlO2+2H2O7、铜离子(CU2+)方法一:加氨水,现象产生蓝色沉淀,方程:Cu(2++4NH3-H2O=[Cu(NH34](2++4H2O方法2:加氢氧化钠溶液,现象:产生BLUE 色沉淀,方程:CU(2++2OH(-=CU(OH2↓8、氯离子(Cl-)试剂:稀硝酸和硝酸银,现象:白色沉淀生辰,方程:Ag(++Cl(-=AgCl↓9、溴离子Br(-试剂同上,浅黄色沉淀生成,方程Br(++Cl(-=AgBr↓10、硫离子S(2-试剂硝酸铅,现象:黑色沉淀,方程:Pb(2++S(2-=PbS↓或者用稀盐酸,现象:臭鸡蛋气味气体放出,气体可以使乙酸铅、硝酸铅试纸变黑方程:2H(++S(2-=2H2S↑S(2-+Pb(2+=PbS↓11、硝酸根NO3(-试剂:浓硫酸和铜单质现象:产生红棕色气体,方程:Cu+2NO3(-+4H(+=CU(2++NO2↑+2H2O12、碳酸根CO3(2-试剂:稀盐酸,现象,声称使澄清石灰水变浑浊的气体方程:2H(++CO3(2-=H20+CO2↑C02+CA(0H2=CACO3↓+H2O13、硫酸根(SO42-试剂:稀盐酸和氯化钡,现象:白色沉淀生成,方程:Ba(2++SO4(2-=BaSO4↓此沉淀不溶于盐酸和稀硝酸14、磷酸根PO4(3-试剂:稀硝酸和硝酸银现象:黄色沉淀,方程:3Ag(++PO4(3-=Ag3PO4↓15、氟离子(F-)加入氯化钙溶液,产生白色的CaF2沉淀2F-+Ca(2+=CaF2↓。
高中化学常见离子检验(可以直接打印)
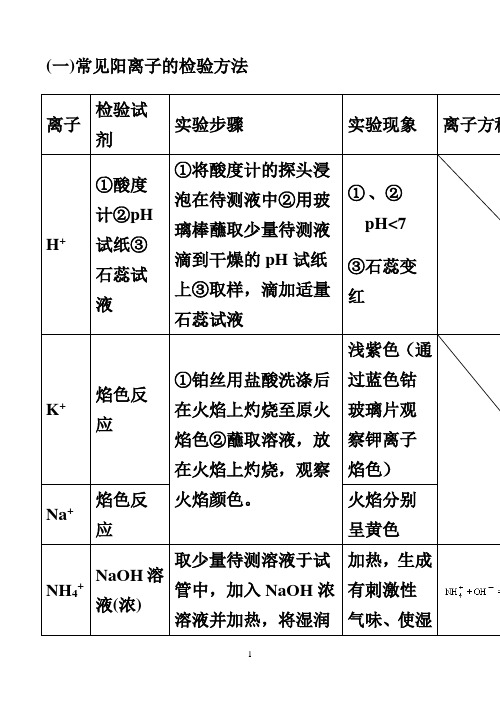
(一)常见阳离子的检验方法(二)常见阴离子的检验方法注意:1.若SO42-与Cl-同时检验,需注意检验顺序。
应先用Ba(NO3)2溶液将SO42-检出,并滤去BaSO4,然后再用AgNO3检验Cl-。
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。
因为稀硝酸能把SO32-氧化成SO42-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
4.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出5.若CO32-和HCO3-同时检验,应先用足量的BaCl2溶液将CO32-检出,静置,取上层清夜用Ba(OH)2或Ca(OH)2检出HCO3-三:常见气体的检验物质检验的一般程序及答题要领⑴实验操作:通常分两步进行,第一步取少量试样(如试样是固体的要先配制成溶液)放入容器(通常用试管)。
第二步各取少许溶液,根据要求在试样中加入已知成分和性质的试剂,并根据所发生的现象,进行分析、判断,作出结论。
⑵答题要领:①不许用原瓶操作:鉴别的目的是为了以后的使用,若用原瓶操作,污染了原瓶中的试剂。
要有“各取少许”字样。
②不许“指名道姓”:结论的得出,来自实验现象,在加入试剂之前,该物质是未知的,应该叙述为“若……(现象),则证明有……”,叙述时不可出现“取某某物质加入某某试剂……”的字样,一般间答顺序为:各取少许→溶解→加入试剂→描述现象→得出结论。
气体检验方法和思路:⑴检验气体的思路一般从以下几个方面考虑①气体的颜色和气味;②②水溶液的酸碱性;③③助燃、可燃及燃烧现象和产物;④④遇空气的变化;⑤⑤其它特性。
⑵方法:①观察法:对于有特殊颜色的气体如Cl2(黄绿色)、NO2(红棕色)、I2蒸汽(紫色)科举颜色辨别。
②溶解法:根据溶于水现象不同区分。
如NO2和Br2蒸汽均为红棕色,但溶于水后NO2形成无色溶液,Br2形成橙色溶液。
③退色法:如SO2和CO2克用品红溶液区分。
高中化学常见离子检验大全

Cu2+
NaOH溶液
取少量待测溶液于 试管中,加入
NaOH溶液
加入话量NaOH
溶液后生成蓝色 沉淀
Cu2++2OH J Cu(OH)2J
2+
NaOH溶液
取少量待测溶液于 试管中,加入
NaOH溶液
加入话量NaOH
溶液后生成白色 沉淀,该沉淀不
溶于过量NaOH
生成不溶于稀 盐酸的白色沉 淀
Ba2++ SO42-=BaSO4J
SO32-
①稀盐酸、 品红溶液
取少量待测溶液 于试管中,加入 稀盐酸后放出的 气体通入品红溶 液
加入稀盐酸后 放出的气体使 品红溶液褪色
SO32-+2H+=H2O+SO2?
②BaCl2溶
液、稀盐酸
取少量待测溶液 于试管中,加入BaCl2溶液再向沉 淀中加入稀盐 酸。
浅紫色(通过蓝 色钴玻璃片观察 钾离子焰色)
Na+
焰色反应
火焰分别呈黄色
NH4+
NaOH溶液
(浓)
取少量待测溶液于 试管中,加入NaOH浓溶液并加 热,将湿润红色石 蕊试纸置于试管口
加热,生成有刺 激性气味、使湿 润红色石蕊试纸 变蓝的气体
WH;+0H-十也0
Ag+
稀HNO3、
稀盐酸(或
NaCl)
取少量待测溶液于 试管中,加入稀HNO3再加入稀盐
溶液中
Mg2++2OH—=Mg(OH)2J
(仅用于鉴别Mg2+和Al3+)
(二)常见阴离子的检验方法
高中化学常见离子检验大全
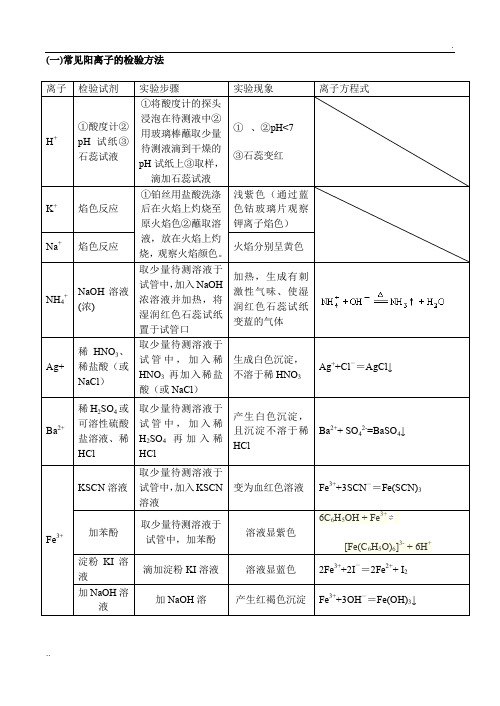
①AgNO3溶液、稀硝酸
①生成不溶于稀硝酸的黄色沉淀
Ag++I-=AgI↓
②新制氯水,淀粉溶液
取少量待测溶液于试管中,加入新制氯水,再加入淀粉溶液
②滴入新制Cl2,振荡后再滴入淀粉溶液,变蓝
Ag++I-=AgI↓
2I-+Cl2=I2+2Cl-
I2遇淀粉变蓝
ClO-
HCl、淀粉-KI
取少量待测溶液于试管中,加入HCl溶液,然后加入淀粉-KI溶液
2.加入稀盐酸后放出无色无味气体,通入澄清的Ca(OH)2溶液变浑浊
CO32-+2H+=H2O+CO2↑
Ca2++2OH-+CO2=CaCO3↓+H2O
SO42-
BaCl2溶液、稀盐酸
取少量待测溶液于试管中,加入BaCl2溶液再向沉淀中加入稀盐酸。
生成不溶于稀盐酸的白色沉淀
Ba2++ SO42-=BaSO4↓
SO32-+2H+=H2O+SO2↑
离子
检验试剂
实验步骤
实验现象
离子方程式
Cl-
AgNO3溶液、稀硝酸
取少量待测溶液于试管中,加入AgNO3溶液,再向沉淀中加入稀盐酸。
生成不溶于稀硝酸的白色沉淀
Ag++Cl-=AgCl↓
Br-
AgNO3溶液、稀硝酸
生成不溶于稀硝酸的浅黄色沉淀
Ag++Br-=AgBr↓
SO32-
①稀盐酸、品红溶液
取少量待测溶液于试管中,加入稀盐酸后放出的气体通入品红溶液
加入稀盐酸后放出的气体使品红溶液褪色
高中化学常见离子检验方法一览表
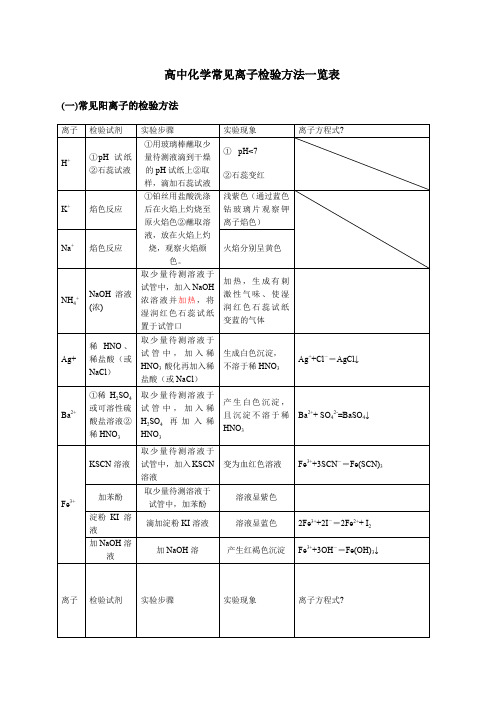
高中化学常见离子检验方法一览表(一)常见阳离子的检验方法
2(二)常见阴离子的检验方法
注意:
1.若SO
42-与Cl-同时检验,需注意检验顺序。
应先用Ba(NO
3
)
2
溶液将SO
4
2-检出,并滤
去BaSO
4,然后再用AgNO
3
检验Cl-。
2.检验SO
32-的试剂中,只能用盐酸,不能用稀硝酸。
因为稀硝酸能把SO
3
2-氧化成
SO
4
2-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
4.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出
5.若CO
32-和HCO
3
-同时检验,应先用足量的BaCl
2
溶液将CO
3
2-检出,静置,取上层清夜用
Ba(OH)
2或Ca(OH)
2
检出HCO
3
-。
高中的关于化学常见离子检验大全精选

(一 )常有阳离子的查验方法离子 查验试剂 ①酸度计②H +pH 试纸③ 石蕊试液K +焰色反响Na+焰色反响实验步骤实验现象①将酸度计的探头浸泡在待测液中② ① 、② pH<7 用玻璃棒蘸取少许待测液滴到干燥的 ③石蕊变红pH 试纸上③取样,滴加石蕊试液①铂丝用盐酸清洗浅紫色(经过蓝后在火焰上灼烧至 色钴玻璃片察看原火焰色②蘸取溶 钾离子焰色)液,放在火焰上灼 火焰分别呈黄色烧,察看火焰颜色。
取少许待测溶液于 加热,生成有刺试管中,加入 NaOH离子方程式NH 4 +NaOH 溶液 (浓 )激性气味、使湿浓溶液并加热,将 润红色石蕊试纸润湿红色石蕊试纸 变蓝的气体置于试管口取少许待测溶液于 稀 HNO 3、Ag+ 稀盐酸(或NaCl )试 管 中 , 加 入 稀 生成白色积淀, HNO 3 再加入稀盐 不溶于稀 HNO 3酸(或 NaCl )Ag + +Cl - = AgCl ↓稀 H 2SO 4 或 取少许待测溶液于产生白色积淀,可溶性硫酸 试 管 中 , 加 入 稀Ba2+且积淀不溶于稀盐溶液、稀 H 2SO 4 再 加 入 稀HClHClHCl取少许待测溶液于KSCN 溶液试管中,加入 KSCN 变为血红色溶液溶液加苯酚取少许待测溶液于 溶液显紫色Fe3+试管中,加苯酚淀粉 KI 溶 溶液显蓝色液 滴加淀粉 KI 溶液加 NaOH 溶产生红褐色积淀液加 NaOH 溶Ba 2++ SO 42-=BaSO 4↓Fe 3++3SCN -=Fe(SCN) 36C 6 H 5OH + Fe 3+ ?[Fe(C 6H 5O)6]3- + 6H+2Fe 3++2I - = 2Fe 2++ I 2Fe 3++3OH -= Fe(OH) 3↓离子查验试剂①KSCN 溶液,新制的氯水②NaOH 溶液Fe2+③酸性高锰酸钾(无其它复原性物质)④铁氰化钾K3[Fe(CN) 6]3+Al NaOH 溶液Cu2+NaOH 溶液Mg 2+NaOH 溶液实验步骤取少许待测溶液于试管中,加入 KSCN溶液,新制的氯水取少许待测溶液于试管中,加入 NaOH溶液并露置在空气中取少许待测溶液于试管中,加入酸性高锰酸钾溶液取少许待测溶液于试管中,加入铁氰化钾溶液取少许待测溶液于试管中,逐滴加入NaOH 溶液至过度取少许待测溶液于试管中,加入 NaOH溶液取少许待测溶液于试管中,加入 NaOH溶液实验现象加入 KSCN 溶液不显红色,加入少许新制的氯水后,立刻显红色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(一)常见阳离子的检验方法
离子检验试剂实验步骤实验现象离子方程式
H+①酸度计②
pH试纸③石
蕊试液
①将酸度计的探头浸
泡在待测液中②用玻
璃棒蘸取少量待测液
滴到干燥的pH试纸上
③取样,滴加石蕊试液
①、②pH<7
③石蕊变红
K+焰色反应①铂丝用盐酸洗涤后
在火焰上灼烧至原火
焰色②蘸取溶液,放在
火焰上灼烧,观察火焰
颜色。
浅紫色(通过蓝色钴玻璃
片观察钾离子焰色)
Na+焰色反应火焰分别呈黄色
NH4+NaOH溶液
(浓)
取少量待测溶液于试
管中,加入NaOH浓溶
液并加热,将湿润红色
石蕊试纸置于试管口
加热,生成有刺激性气
味、使湿润红色石蕊试纸
变蓝的气体
Ag+ 稀HNO3、稀
盐酸(或
NaCl)
取少量待测溶液于试
管中,加入稀HNO3再
加入稀盐酸(或NaCl)
生成白色沉淀,不溶于稀
HNO3
Ag++Cl-=AgCl↓
Ba2+①稀H2SO4
或可溶性硫
酸盐溶液②
稀HNO3
取少量待测溶液于试
管中,加入稀H2SO4
再加入稀HNO3
产生白色沉淀,且沉淀不
溶于稀HNO3
Ba2++ SO42-=BaSO4↓
Fe3+KSCN溶液
取少量待测溶液于试
管中,加入KSCN溶液
变为血红色溶液Fe3++3SCN-=Fe(SCN)3加苯酚
取少量待测溶液于试
管中,加苯酚
溶液显紫色
淀粉KI溶液滴加淀粉KI溶液溶液显蓝色2Fe3++2I-=2Fe2++ I2
加NaOH溶
液
加NaOH溶产生红褐色沉淀Fe3++3OH-=Fe(OH)3↓
离子检验试剂实验步骤实验现象离子方程式
Fe2+ ①KSCN溶
液,新制的氯
水
①取少量待测溶液于
试管中,加入KSCN溶
液,新制的氯水
①加入KSCN溶液不显
红色,加入少量新制的氯
水后,立即显红色。
2Fe2+ + Cl22Fe3+ + 2Cl-
Fe3++3SCN-=Fe(SCN)3
②加NaOH
溶液
②取少量待测溶液于
试管中,加入NaOH溶
液并露置在空气中
②开始时生成白色
Fe(OH)2沉淀,迅速变成
灰绿色,最后变成红褐色
Fe(OH)3沉淀。
Fe2++2OH —=Fe(OH)2↓
4Fe(OH)2十O2+2H2O=4Fe(OH)3
③(无其它还
原性物质如
SO32-)酸性高
锰酸钾
取少量待测溶液于试
管中,加入酸性高锰酸
钾溶液
加入酸性高锰酸钾溶液
紫色褪去
1.若SO42-与Cl-同时检验,需注意检验顺序。
应先用Ba(NO3)2溶液将SO42-检出,并滤去BaSO4,然后再用AgNO3检验Cl-。
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。
因为稀硝酸能把SO32-氧化成SO42-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
4.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出
5.若CO32-和HCO3-同时检验,应先用足量的BaCl2溶液将CO32-检出,静置,取上层清夜用Ba(OH)2或Ca(OH)2检出HCO3-。
