小儿急救——儿科脓毒症
小儿脓毒症注意事项

小儿脓毒症注意事项
小儿脓毒症是一种严重的感染性疾病,常见于婴幼儿和幼儿期。
脓毒症的主要表现为高热、意识障碍、呼吸困难、皮疹等症状,如果不及时治疗,可能会导致严重后果甚至死亡。
因此,对于脓毒症患儿,家长需要特别注意以下几点。
首先,家长应保持冷静并及时就医。
一旦孩子出现高热、皮疹、呼吸困难等明显症状,家长应该第一时间就医,并告诉医生孩子的病史、发病情况和家族史等。
家长不要自行处理,以免耽误治疗。
其次,家长应当做好孩子的护理工作。
脓毒症患儿的体温通常很高,家长应当给孩子解热,可以使用物理降温方法如冷敷,也可以服用适当的解热药物,但需遵医嘱使用。
家长还需给孩子提供充足的水,保持室内空气清新,并注意孩子身体的清洁和换洗。
再次,家长要密切观察孩子的病情。
脓毒症患儿常常有意识障碍、呼吸困难等严重症状,家长应时刻注意孩子的表情、呼吸和意识状态,如有异常立即报告医生。
如果医生安排了住院治疗,家长要积极配合医生,按时给孩子进行各项治疗和检查。
最后,家长应注重孩子的营养和休息。
脓毒症患儿身体虚弱,容易产生营养不良和疲劳,家长应给予孩子高能量、易消化的食物,并适当增加营养摄入量。
同样重要的是,家长要给孩子提供足够的休息时间,避免过度劳累,保证睡眠质量。
总之,小儿脓毒症是一种严重的感染性疾病,对于患儿来说是一次严峻的生命考验。
家长要冷静应对,及时就医,并做好护理工作。
此外,家长还应注意观察孩子的病情变化,提供适当的营养和休息。
只有这样,孩子才能尽快康复,恢复健康。
儿科感染性休克(脓毒性休克)诊疗推荐方案解读

感染性休克(脓毒性休克)代偿期(早期):
3、外周动脉搏动细弱,心率、脉搏增快; 4、毛细血管再充盈时间≥ 3秒(除外环境温度影 响); 5、尿量 <1 ml / (kg . h) ; 6、代谢性酸中毒(除外其他缺血缺氧及代谢因 素)。
诊疗推荐方案简介---概念
感染性休克(脓毒性休克)失代偿期:
一、定义 脓毒症(Sepsis)是指感染引起的全身 炎症反应综合征(SIRS)。 脓毒症出现循环功能障碍称感染性休克 或脓毒性休克(Septic Shock)
诊疗推荐方案简介---概念
全身炎症反应综合征(SIRS) 至少出现下列四项标准的两项,其中一项为体温或白细胞计数异 常: 中心温度> 38.5℃ 或 < 36.0 ℃。 心动过速,平均心率> 同年龄组正常值2个标准差以上(无外界刺 激、慢性药物或疼痛刺激),或不可解释的持续性增快超过0.5~ 4 h; 或< 1岁出现心动过缓,平均心率< 同年龄组值第10百分位以下 (无外部迷走神经刺激及先天性心脏病,亦未使用β阻滞剂药物), 或不可解释的持续性减慢超过0.5小时。 平均呼吸频率> 各年龄组正常值2个标准差以上,或因急性病程需 机械通气(无神经肌肉疾病也与全身麻醉无关)。 白细胞计数升高或下降(非继发于化疗的白细胞减少症),或未 成熟嗜中性粒细胞>10%。
诊疗推荐方案---治疗
纠正凝血障碍: 早期可给予小剂量肝素 5-10 IU/kg 皮下注射或静脉输注(注意 肝素钠不能皮下注射),每6 h 1次。若 已明确有DIC,则应按DIC常规治疗。
诊疗推荐方案---治疗
其他治疗: 1)保证氧供及通气,充分发挥呼吸代偿作用。 应用NCPAP,小婴儿更需积极气管插管及 机械通气。儿童肺保护策略与成人相似。 2)注意各脏器功能支持,维持内环境稳定 3)保证能量营养供给,注意监测血糖、血电解 质。
儿科脓毒症诊断标准解读

儿科脓毒症诊断标准解读儿科脓毒症患病率高,死亡率高,治疗费用昂贵。
在国际儿科脓毒症共识会议上,权威专家制定了儿科全身炎症反应综合征(SIRS)、脓毒症定义和器官功能障碍的诊断标准,并经美国儿科学会核准公布。
该标准将儿科脓毒症诊断作了具体而明确的规定,澄清了一些概念。
现请专家作一介绍。
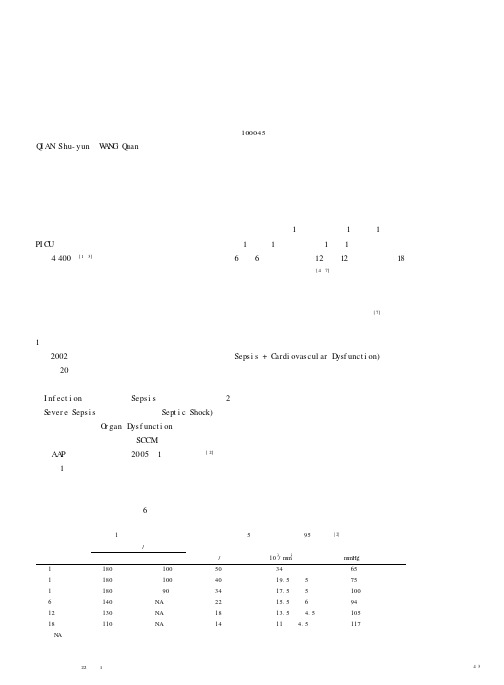
脓毒症专家组根据不同年龄儿童生理值范围、感染风险度的差异及抗生素治疗选择的不同,将儿童分为6个年龄段,即初生儿(0天~1周)、新生儿(~1月)、婴儿(~1岁)、幼儿及学龄前儿童(~5岁)、学龄儿童(~12岁)、青少年(~18岁)。
五个概念需明确1. SIRS 符合以下四项标准中至少两项,其中一项必须是体温异常或白细胞计数异常:●中心体温>38.5℃或<36℃。
●心动过速,平均心律>同年龄组正常值±两个标准差,并且无外界**、慢性药物或疼痛**的影响;或不可解释的持续性增快超过0.5~4 h;或●平均呼吸频率>同年龄组正常值2SD(标准差)或需机械通气的急性疾病(与神经肌肉疾病或全身麻醉无关)。
●白细胞计数升高或降低(非继发于化疗的白细胞减少症)或幼稚中性粒细胞>l0%。
2. 感染可疑存在或已证实感染(细菌培养、组织涂片或PCR);或与感染高度相关的临床综合征。
感染的证据包括临床体检、影像学或实验室的阳性结果。
3. 脓毒症SIRS出现在可疑或已证实的感染中或为感染的结果。
4. 严重脓毒症脓毒症+以下情况之一:心血管功能障碍;急性呼吸窘迫综合征、两个或两个以上心、肺以外的器官功能障碍。
5. 脓毒症休克脓毒症+心血管功能障碍。
液体复苏最重要1. 气道支持(机械通气)对脓毒症患儿,首先应保持气道通畅,高流量吸氧,如液体复苏达40ml/kg后休克仍不能纠正或意识状况恶化,应行气管插管和机械通气。
儿童肺保护策略与成人相似,高浓度给氧时应避免早产儿氧中毒。
2.液体复苏小儿脓毒症休克时多存在相对或绝对循环量不足,心输出量下降,因此,液体复苏最为重要。
小儿脓毒症
继续医学教育 第 22 卷第 1 期
45
专家讲 堂
学习 提 纲 1 .掌握小儿脓毒症定义。 2 .掌握小儿脓毒症的治
进行液体复苏时可以选择晶体或胶体液。有随 机对照临床研究显示,用胶体液或晶体液复苏登革 热休克患儿时,其死亡率无显著性差异,但用乳酸 林格氏液复苏的患儿其恢复时间有所延长。胶体液 可能更适于脉压差小的患儿。
由于脓毒症患儿的毛细血管渗透性增加,可出 现持续渗漏,其增加的液体需求量可持续数天。因 此对该类患儿应该继续和维持补液。此时注意监测 血 气、生化等,保持内环境稳 定。红细胞比积< 3 0 %时, 可以适当输血,以尽量维持 血红蛋白在 1 00 g / L以上。在该阶段仍需评估循环情况,以判 定液体性质及量是否合适。 2 . 2 血管活性药物
2
◆ 证明需要高氧或 FI O ≥ 0. 5 才能维持血氧饱和度≥ 92% 2
◆ 需紧急侵入或非侵入性机械通气 神经 ◆ Gl a s gow昏迷评分≤ 11 分 ◆ 精神状态急性改变伴 Gl as gow昏迷评分从基线下降≥ 3 分 血液 ◆ 血小板计数< 80 00 0/ mm3 或在过去 3 天内从最高值下降 50%(适用于慢性血液或肿瘤患儿) ◆ 国际标准化比值> 2(标准化的 PT) 肾脏 血清肌酐为各年龄组正常值上限的 2 倍及以上,或较基线增加 2 倍 肝脏 ◆ 总胆≥ 4 mg/ dl (新生儿不适用) ◆ ALT为同年龄正常值上限 2 倍及以上
去甲肾 上腺 素 ◆ 具备下列中2 项:
儿科脓毒症诊断标准

儿科脓毒症诊断标准
儿科脓毒症是一种严重的感染性疾病,对儿童的健康造成严重
威胁。
脓毒症的诊断标准通常是根据患儿的临床表现和实验室检查
结果来进行判定。
以下是一般情况下用于诊断儿科脓毒症的标准:
1. 临床表现,典型的脓毒症症状包括发热、心率加快、呼吸急促、皮肤发红、血压下降、意识改变等。
婴儿和幼儿可能表现为食
欲不振、烦躁不安、呕吐等。
2. 实验室检查,血液培养是诊断脓毒症的关键实验室检查之一,通过血液培养可以检测出是否存在细菌感染。
其他实验室检查可能
包括白细胞计数、C反应蛋白测定、凝血功能检查等。
3. 炎症指标,脓毒症患儿的炎症指标通常会升高,包括白细胞
计数、中性粒细胞计数、C反应蛋白水平等。
4. 临床评分系统,儿科脓毒症的诊断也可以借助临床评分系统,如儿童全身性感染症状评分(PRISM)或小儿全身性感染症状评分(PELOD),来评估患儿的病情严重程度。
总的来说,诊断儿科脓毒症需要综合考虑患儿的临床表现和实
验室检查结果,以及可能的病因和感染部位。
及早诊断和治疗对于
儿童脓毒症的预后至关重要,因此医生在面对疑似脓毒症的患儿时,需要及时进行全面的评估和诊断。
儿童脓毒性休克诊治专家共识

➢ 切断SIRS连锁反应:
➢
肾上腺皮质激素:小剂量、长疗程(2004)
➢
内பைடு நூலகம்素抗体,抗自由基,血浆超滤
➢ 改善微循环、保护肾功能
小儿脓毒症 (Sepsis)
定义
脓毒症(Sepsis) 是指感染(可疑或证实)引起的全身炎症反应综合征(SIRS) 严重脓毒症(Severe Sepsis) 是指脓毒症导致的器官功能障碍或组织低灌注 脓毒性休克(Septic shock) 是指脓毒症诱导的组织低灌注和心血管功能障碍.
内毒素(LPS)启动SIRS过程
LPS:脂多糖;
LBP:脂多糖结合 蛋白;
TLR4:Toll样受体 4;
MyD88:骨髓分化 因子88;
IRAK:IL-1受体相 关激酶;
TRAF6:TNF 受 体相关因子;
SRF:血清反 应因子;
AP-1:活化子 蛋白1;
ATF2:活化转 录因子。
炎症细胞活化(Activation of inflammatory cells) 炎症细胞 Mo-M、NG、噬酸性粒细胞、VEC、PLT
3、持续高代谢:高氧耗,BMR(基础代谢率)明显升高,耗能异常,对 外源性营养底物反应差,蛋白营养不良,伪神经介质
诊断标准
1、1991年8月ACCP/SCCM: T>38℃或<36℃ HR>90次/分 RR>20次/分或PaCO2<4.3kPa (32mmHg) WBC>12×109/L或<4×109/L或未成熟细胞>0.10
临床治疗
•
抗炎症介质、抗内毒素抗体治疗
•
NOS阻断剂
•
活化蛋白C(APC) :儿科不用
•
激素的治疗
•
非甾体类药物如布洛芬等的治疗
儿科脓毒症、脓毒性休克ppt课件

治疗
如仍无效或存在毛细血管渗漏或低蛋白血症可给予等量5%白蛋白。接 近成人体重的患儿液体复苏量为:每次等渗晶体液500—1000ml或5% 白蛋白300—500ml,30min内输入。
治疗
液体复苏期间严密监测患儿对容量的反应性,如出现肝大和肺部啰音( 容量负荷过度)则停止液体复苏并利尿。如有条件可同时监测CVP数值 的动态变化,当液体复苏后CVP升高不超过2mmHg时,提示心脏对容量 的反应性良好,可以继续快速输液治疗;反之,机体不能耐受快速补 液。也可采用被动抬腿试验评估患儿的容量反应。第1小时液体复苏不 用含糖液,若有低血糖可用葡萄糖0.5~1g/kg纠正。
CRT延长(≥3s)或花斑
脓毒症诊断:发热(肛温>38.5℃)或低体温(肛温<35℃)、心动过速(低体温者可以无心动过
速),伴以下至少一个脏器功能异常:意识改变、低氧血症、血清乳酸增高或洪脉
严重脓毒症诊断:脓毒症诱导的组织低灌注或器官功能障碍
脓毒性休克诊断
表3(不同年龄儿童低血压标准 )
年龄
收缩压(mmHg)
国内指南
脓毒症:指感染(可疑或证实)引起的全身炎症反应综合征(SIRS) ;
严重脓毒症:指脓毒症导致的器官功能障碍或组织低灌注; 脓毒性休克:指脓毒症诱导的组织低灌注和心血管功能障碍;
SIRS
全身炎症反应综合征(SIRS) 符合以下四项标准中至少二项,其中一项必须是体温异常或白细胞计
数异常
病理生理
在“指南”中成人脓毒性休克定义为:脓毒症在给予液体复苏后仍无 法纠正的持续低血压。
儿童脓毒性休克不能以血压为衡量标准,以低灌注组织状态更能早期 识别,即出现意识状态改变、周围脉搏减弱、毛细血管再充盈时间>2 S、皮肤花纹、肢端发冷、尿量减少等就考虑休克的存在,而低血压是 休克晚期和失代偿的表现。
《2024年国际共识标准:儿童脓毒症和脓毒性休克》解读PPT课件

02
维持适宜的温度和湿度 ,注意保暖,避免孩子 受凉。
03
确保家庭环境安全,避 免孩子接触到尖锐物品 、电器等危险源。
04
为孩子提供安静、舒适 的休息环境,保证充足 的睡眠时间。
营养支持和心理关爱重要性
01
02
03
04
提供高热量、高蛋白、易消化 的饮食,以满足孩子康复期的
营养需求。
注意补充维生素和矿物质,如 维生素C、锌等,有助于增强
肾脏系统并发症处理
对于出现肾脏系统并发症的患儿, 应给予连续性肾脏替代治疗( CRRT)等,同时优化液体管理和 电解质平衡。
神经系统并发症处理
对于出现神经系统并发症的患儿, 应给予降颅压治疗、抗惊厥治疗等 ,同时加强神经系统监测和评估。
06 家庭护理与康复期管理建 议
家庭环境优化建议
01
保Байду номын сангаас室内空气清新,定 期开窗通风,避免烟雾 、香水等刺激性气味。
免疫治疗与营养支持
针对不同器官功能障碍,采取相应的支持 治疗措施,如机械通气、血液净化等。
根据患者病情和免疫状态,给予免疫调节剂 、营养支持等治疗措施,以促进康复。
03 儿童脓毒症早期诊断方法
临床表现及体征识别
发热或低体温
儿童脓毒症早期常伴有 发热,体温可高于38℃
或低于36℃。
心率增快
脓毒症时,心率通常增 快,与体温升高不成比
02 2024年国际共识标准内 容
诊断标准更新与解读
新的诊断标准
强调早期识别和及时干预,包括临床 表现、实验室检查和影像学检查等多 方面的综合评估。
诊断标准的适用范围
适用于所有年龄段儿童,包括新生儿 和婴幼儿,为临床医生提供了统一的 诊断依据。
小儿脓毒症诊治进展

• 儿科今后应在推广应用方面下功夫。
循证医学为基础的指南-责任 回归到最基本-循证指导临床实践
•
:2008 2008,36:296-327.
• 抗生素应用及病灶清除
• 液体复苏、血管活性药(目标导向治疗)
• 其他脏器支持治疗
• 。。。。。。。。。。。
• 采用循证医学为基础的综合治疗( ) 病死率明显下降(4923<0.05) 2005,9(6)764-70
感性和耐药情况(如肺炎)。 • 明确病灶:感染部位确定有助于判断感染的病原。此外病灶的清除对感染的控制非常重要,
如果有阑尾炎、腹膜炎、脓胸等要尽早行外科手术或引流。 • 院内或院外感染:是判断病原的重要参考,比如社区获得性肺炎和院内获得性肺炎常见病原
是不同的,细菌耐药性也不一致,在选择药物时决策也不同。 • 年龄:是考虑病原的重要参考,不同的年龄可能感染的病原是不同的
病死率* 40% 60%
80%
100 %
; 2003
抗生素在脓毒症治疗中的作用
早期发现、早期明确病原,早期适当的抗生素治疗(细菌与真菌)及病灶的清除起到关键作用 即使重症脓毒症恰当抗生素治疗也是抢救成功的基础(虽然有时不能完全挽救生命) 抗生素每延迟1小时 病死率增加7.6%( 2006; 34:1589–1596) 肺炎病死率也明显增加(等在一个前瞻性多中心超过14000例患者参与的研究中强调了首剂抗生素使用时
脓毒症增加的趋势 ❖ . J 2003; 167:695–701
儿童脓毒症-死亡的主要原因
• 美国:年发病率0.56/1000(1995年,婴儿5.6/1000)
• 住院的重症脓毒症病死率为10.3%.全国6.2/10万儿童死于脓毒症,
小儿脓毒血症诊断标准

小儿脓毒血症诊断标准小儿脓毒血症是一种严重的感染性疾病,需要及时准确地诊断和治疗。
本文将为读者提供小儿脓毒血症诊断标准的参考,主要包括以下四个方面:感染指标、炎症指标、组织损伤指标和病原学检查。
1.感染指标感染指标是指那些能够反映机体感染状况的指标。
在小儿脓毒血症的诊断中,常见的感染指标包括血常规、C反应蛋白(CRP)和降钙素原(PCT)。
血常规是一种常规的血液检查,可以反映机体的白细胞计数、红细胞计数和血小板计数等基本情况。
在脓毒血症时,白细胞计数通常会升高,同时伴有中性粒细胞比例增加。
C反应蛋白是一种敏感的急性时相反应蛋白,当机体发生感染时,CRP水平会明显升高。
在小儿脓毒血症中,CRP通常会升高至正常值的数倍至数十倍。
降钙素原是一种蛋白质,当机体发生严重感染时,PCT水平也会明显升高。
在小儿脓毒血症中,PCT的升高通常早于其他感染指标,具有较高的早期诊断价值。
2.炎症指标炎症指标是指那些能够反映机体炎症反应状况的指标。
在小儿脓毒血症的诊断中,常见的炎症指标包括体温、血氧饱和度和白细胞计数等。
体温是反映机体感染和炎症反应的重要指标。
在小儿脓毒血症中,患儿通常会出现发热,体温通常会高于38.5℃。
血氧饱和度可以反映机体的氧合状态和呼吸功能。
在脓毒血症中,由于感染导致机体缺氧和呼吸功能受损,血氧饱和度通常会降低。
白细胞计数可以反映机体的免疫状况。
在小儿脓毒血症中,白细胞计数通常会升高,同时伴有中性粒细胞比例增加。
3.组织损伤指标组织损伤指标是指那些能够反映机体组织损伤状况的指标。
在小儿脓毒血症的诊断中,常见的组织损伤指标包括肝肾功能、心肌酶谱和胸片检查等。
肝肾功能是反映机体代谢和解毒功能的重要指标。
在小儿脓毒血症中,由于感染导致机体代谢紊乱和毒素积累,肝肾功能通常会受到影响。
心肌酶谱是反映心肌损伤状况的指标。
在小儿脓毒血症中,由于感染导致机体缺氧和代谢紊乱,心肌也容易受到损伤。
胸片检查可以反映肺部和胸膜的病变情况。
儿科脓毒症脓毒性休克ppt课件

提高免疫力
合理饮食、加强锻炼、接种疫苗等 措施可以提高儿童的免疫力,减少 感染的发生。
早期诊断和治疗
对疑似脓毒症休克的患儿应尽早进 行诊断和治疗,以降低死亡率。
PART 03
儿科脓毒症脓毒性休克的 治疗
早期识别与诊断
早期识别
关注患儿的全身症状,如发热、寒战 、呼吸急促、心率加快等,以及局部 感染病灶,如皮肤化脓性病灶、肺炎 等。
能性,为脓毒症患者提供个性化治疗方案。
制
深入研究脓毒症和脓毒性休克的病理生理机制, 了解其发生、发展的分子机制和细胞生物学过程 。
微生物学研究
对引起脓毒症的病原微生物进行深入研究,了解 其致病机制和耐药性,为抗生素治疗提供依据。
3
免疫学研究
研究脓毒症患者的免疫状态和免疫应答,了解免 疫细胞在脓毒症中的作用,为免疫调节治疗提供 理论支持。
液体复苏与血管活性药物应用
液体复苏
通过补充血容量,维持正常的组织灌注和氧合。
血管活性药物
在液体复苏的基础上,使用血管活性药物如多巴 胺、去甲肾上腺素等,以改善组织灌注。
监测指标
密切监测患儿的生命体征、尿量、中心静脉压等 指标,以评估治疗效果。
支持治疗与器官功能保护
01
02
03
04
呼吸支持
对于呼吸衰竭的患儿,给予机 械通气辅助呼吸。
临床表现与诊断标准
临床表现
脓毒症和脓毒性休克的临床表现多样,包括发热、寒战、呼 吸急促、心率加快、血压下降等。此外,还可能出现意识障 碍、少尿、皮肤湿冷、四肢厥冷等症状。
诊断标准
根据临床表现和实验室检查,脓毒症和脓毒性休克的诊断标 准包括体温、白细胞计数、呼吸频率、心率、血压等指标。 同时,还需要排除其他可能导致类似症状的疾病。
儿童脓毒症课件

儿童脓毒症。
虽然脓毒症的诊断门槛并不 高,但除重症医学专科(ICU )外,其他医护人员使用脓 毒症概念诊断的机会仍较低 。
MODS诊断标准不统一。
脓毒性休克诊疗 指南存在争议
2020年实现5项关键指标
脓毒症发生率下降20%. 力争将儿童和成人脓毒症患者 的存活率较2010年提升100% 公众及专业人员对脓毒症的认知水平进 一步提升,让脓毒症成为家喻户晓的一 个专 有名词,并成为感染紧急干预的代名。 所有脓毒症患者都能制定最适当的康复治疗计划。 对全球脓毒症负担的评估和对脓毒症控制及管理措 施的影响力显著改善,建立起全球及地区性的 脓毒症疾病管理系统
全身炎症反应综合征(SIRS) 脓毒症(Sepsis) 严重性脓毒症(Severe Sepsis)
脓毒症休克(Septic shock) 多器官功能不全综合征(MODS)
救活或死亡
脓毒症是一个异质性很大的临床综合征
机体对各种微生物感染所产生的全身性炎症反应即为Sepsis,它不是独立 的疾病概念,而是一个复杂临床综合征,具有很大的异质性,但殊途同归 。
3、呼吸加快 4、白细胞升高或下降
平均呼吸频率>同年龄组正常值25%,或因急性病程需 机械通气的(无神经肌肉疾病,也与全身麻醉无关)
白细胞计数升高或降低(非继发于化疗的白细胞减少) 或者未成熟中性粒细胞>10%(不同年龄标准不同)
感染(Infection)
1、存在任何病原体引起的已证实或高度怀疑的感染:即存在与感染 高度相关的临床综合征.
脓毒症休克的定义
1、脓毒症休克(Septic shock),是发生在各种严重感染的基础上,由致病微 生物(如细菌、病毒、真菌等)及其产物所引起的急性循环功能衰竭,有效循环 血量减少,使全身细胞和重要器官血流灌注不足,不能提供足够的氧和营养物质 满足细胞代谢需要,从而导致一系列代谢紊乱、细胞受损及脏器功能障碍的急性 综合征。 2、Sepsis+急性循环功能衰竭障碍(如顽固性组织低灌注,伴或不伴低血压)即 为脓毒性休克(Septic shock)。 3、在脓毒性休克病程的不同阶段,有不同的矛盾特点:早期时有效循环血容量 减少、心输出量减少,微循环障碍为主;晚期则以细胞损害、代谢紊乱和脏器功 能衰竭为主,最后发展至MODS,直至死亡。
脓毒症

(六)连续血液净化
脓毒性休克常因组织低灌注导致AKI或急性肾衰竭。 在下列情况行连续血液净化治疗(CBP)[10]:①AKI Ⅱ期; ②脓毒症至少合并一个器官功能不全时;③休克纠正后 存在液体负荷过多经利尿剂治疗无效,可予以CBP,防止 总液量负荷超过体重的10%。
(七)抗凝治疗 脓毒性休克患儿因内皮细胞损伤常诱发凝血功能异常,尤其 易导致深静脉栓塞。儿童深静脉血栓的形成往往与深静脉置管 有关,肝素涂层的导管可降低导管相关性深静脉血栓的发生风 险。对高危患儿(如青春期前)可应用普通肝素或低分子肝素预防 深静脉血栓的发生[11]。如出现血栓紫癜性疾病(包括弥散性血 管内凝血、继发性血栓性血管病、血栓性血小板减少性紫癜)时 ,给予新鲜冰冻血浆治疗。
(二)脓毒性休克分期
1.代偿期:儿童脓毒性休克的诊断与成人不同之处 在于不一定具备低血压[7]。当患儿感染后出现上述3 条或以上组织低灌注表现,此时如果血压正常则诊断 脓毒性休克代偿期。 2.失代偿期:代偿期灌注不足表现加重伴血压下降 ,则进展为失代偿期。不同年龄低血压标准参考表3 。
(三)休克分型
(五)控制血糖 脓毒性休克可诱发应激性高血糖,如连续2次血糖 超过10 mmol/L(180 mg/dl),可予以胰岛素静脉输注,剂 量0.05~0.10 U/(kg· h),血糖控制目标值≤10 mmol/L。胰 岛素治疗过程中需严密监测血糖以防止低血糖的发生, 根据血糖水平和下降速率随时调整胰岛素剂量。开始每1 ~2小时监测血糖1次,达到稳定后4 h监测1次。小婴儿由 于糖原储备及肌肉糖异生相对不足,易发生低血糖,严 重低血糖者可给予25%葡萄糖2~4 ml/kg静脉脓毒症(sepsis)是指感染(可疑或证实)引起的全身 炎症反应综合征(SIRS);严重脓毒症(severe sepsis)是指 脓毒症导致的器官功能障碍或组织低灌注;脓毒性休 克(septic shock)是指脓毒症诱导的组织低灌注和心血 管功能障碍[1,4]。脓毒性休克主要为分布异常性休克, 在儿童常同时伴低血容量性休克。儿童脓毒性休克早 期可以表现为血压正常,休克晚期呈难治性低血压[5]。
新生儿脓毒血症

一般表现如精神即可进入不吃、不哭、 不动、面色不好、神萎、嗜睡。体壮儿常 发热,体弱儿、早产儿常体温不升。
实验室检查
1.外周血培养:应在用抗生素前取周围血做培养, 关键是需严格无菌。采血时间越长,污染机会越多。
2.外周血像:新生儿白细胞总数正常波动范围太大, 尤其是 48 小时内可高达 38×109/L,一周后 5~ 21×109/L。白细胞数<5×109/L 或 100 个中性粒 细胞中杆状核(包括晚幼粒细胞等)≥20 是辅助诊断 本症最简便的方法。
病原学
国内多年来以葡萄球菌最多,其次为大肠 埃希菌等肠道细菌,机会菌感染有所增加, 链球菌一直很少见。但在美国则以链球菌 最多,依次为大肠埃希菌、克雷伯菌,肠 杆菌属、葡萄球菌等。
感染途径
一般新生儿脓毒血症发生于产后和产时, 虽然临产前产妇可有多种细菌的菌血症, 如肺炎链球菌菌血症,但其胎儿通常未被 感染,主要由于母亲的免疫功能及胎盘屏 障对胎儿有一定的保护作用。
发病机制
1、皮肤粘膜屏障功能较差。 2、淋巴结发育不全
缺乏吞噬细菌的过滤作用,常不能将病 原菌局限于局部淋巴结。
3、非特异性免疫功能不足:
补体、调理素、溶菌酶水平低于成人。 产生γ干扰素(INF-γ), 肿瘤坏死因子(TNFα), 白介素(IL)-3、 -4、 -6, 胰岛素生长 因子-1(IGF-1)明显低于年长儿和成人。 中 性粒细胞、单核-吞噬细胞系统、自然杀伤 (NK)细胞的杀菌能力明显低于成人。
3.C 反应蛋白(cRP)≥15μg/ml、微量法++~+++或乳 胶 CRP>8μg/ml 提示败血症。
4、深部脓液、穿刺液涂片和培养更加可靠。最好 能从耻骨上穿刺做碌液涂片及培养。
儿童脓毒症ppt课件

定义
脓毒症(Sepsis) SIRS出现在可疑或已证实的感染中或为 感染的结果 即 SIRS诊断+感染诊断
Shanghai Children’s Medical Center
定义
全身炎症反应综合症(SIRS)
• 中心温度> 38.5C 或 < 36.0C • 心动过速,平均心率>同年龄组正常值2 个标准差以上(无外界刺激、慢性药物或 疼痛刺激),或不可解释的持续性增快超 过0.5-4.0小时;或< 1岁出现心动过缓,
The Epidemiology of Sepsis in the United States from 1979 through 2000. N Engl J Med 2003;348:1546-54.
Shanghai Children’s Medical Center
流行病学资料
美国儿童严重脓毒症 发病率 0.56/1000 (婴儿5.16/1000, 年长儿0.2/1000)
定义
多脏器功能不全综合症(MODS)
神经功能障碍 • Glasgow昏迷评分≤11 或 • 精神状态急性改变伴Glasgow昏迷评分从异常基 线下降≥3分
Shanghai Children’s Medical Center
定义
多脏器功能不全综合症(MODS)
血液功能障碍 • 血小板计数<80,000/mm3或在过去3天内从最高 值下降50%(适用于慢性血液/肿瘤患儿) • 国际标准化比值>2(标准化的PT)
Crit Care Med. 2005 Jul;33(7):1538-48
Shanghai Children’s Medical Center
感染
新生儿脓毒血症早期诊断及治疗

脓毒症的新进展
EGDT(early goal-dirted therapy) 理论依据:
严重脓毒血症时组织低灌注或低血压的发生、发展导
致氧输送不足。 EGDT的核心内容即为如何提高组织对氧 的输送。通过提高心输出量和动脉血氧含量能增加对组织 的氧的输送,而心输出量的的增加主要通过液体复苏达到 最佳心脏负荷、正性肌力药物应用以增加心肌收缩力、升 压药以达到适宜的心脏后负荷。动脉血氧含量的增加主要 通过输注红细胞提高血红蛋白浓度、提供高动脉氧饱和度 来达到。
新生儿脓毒症(sepsis)指新生儿期 发生的、各种病原菌感染导致的、 伴有SIRS表现的临床综合征,其中, 细菌或真菌血行感染导致的新生 儿脓毒症称为新生儿败血症。
2005年国际儿科脓毒症共识会议组成员根据不同 年龄儿童的生理特点,提出了儿科(出生至18岁) SIRS、感染、脓毒症、严重脓毒症、脓毒性休克 的定义及诊断标准.
虽然在初始治疗 及时,但未能在6 小时内达标。如 医师操作经验欠 缺,不能尽快完 成完成PICC,影 响液体复苏及 CVP/ScvO2的监 测。由于监测手 段的受限,液体 复苏时临床医师 害怕导致心功能 衰竭
治疗过程中缺乏 团队协作精神, 医护人员之间合 作不紧密。应该 加强科室医护协 作,培训专业的 重症监护的医师 和护理队伍。同 时规范流程,结 合自身医院的实 际情况,建立相 应的切实可行的 操作规范。
2.肝肾功、血乳酸、血培养 3.经皮血氧饱和度、血压、血糖
4.尿量、毛细血管再充盈时间
脓毒血症的治疗:
3.换血 治疗
1.抗菌 药物的 应用
3.保持机体 内外环境的 稳定及对症
治疗
2.清除 感染灶
脓毒性休克的早期目标导向治疗 (EGDT):
2005年首次公布的国际儿科脓毒症相关概念和定义的专家共识

2005年首次公布的国际儿科脓毒症相关概念和定义的专家共识[1]已得到全世界儿科界广泛认可;2006年我国儿科重症医学专家制定的"儿科感染性休克(脓毒性休克)诊疗推荐方案" [2],对国内儿科医师具有积极指导意义。
2012年"拯救脓毒症战役"之严重脓毒症、脓毒性休克国际指南加入了血流动力学、组织灌注、器官功能不全等量化指标,使脓毒症、严重脓毒症、脓毒性休克的诊断和治疗更具客观性[3]。
基于国际指南,结合中国实际情况,对我国儿科脓毒性休克诊治推荐方案进行部分修订,提出更新的专家共识。
此次修订参考的文献范围包括:PubMed、Medline、中文相关数据库(万方数据库、清华同方、维普中文科技期刊数据库)中包括成人和儿童的资料,检索时间截至2015年3月。
此次修订先后举行了多次专家讨论会,并征求了儿科重症医学资深专家的意见和建议,经反复多次修改后形成此共识。
脓毒症(sepsis)是指感染(可疑或证实)引起的全身炎症反应综合征(SIRS);严重脓毒症(severe sepsis)是指脓毒症导致的器官功能障碍或组织低灌注;脓毒性休克(septic shock)是指脓毒症诱导的组织低灌注和心血管功能障碍[1,4]。
脓毒性休克主要为分布异常性休克,在儿童常同时伴低血容量性休克。
儿童脓毒性休克早期可以表现为血压正常,休克晚期呈难治性低血压[5]。
脓毒症、严重脓毒症及脓毒性休克是机体在感染后出现的一系列病理生理改变及临床病情严重程度变化的动态过程,其实质是全身炎症反应不断加剧、持续恶化的结果。
2012年严重脓毒症/脓毒性休克国际指南有关儿童脓毒症、严重脓毒症诊断相关的指标参考表1[3]。
(一)脓毒性休克诊断脓毒症患者出现组织灌注不足和心血管功能障碍即可诊断为脓毒性休克[2,3,6],表现为:1.低血压:血压<该年龄组第5百分位,或收缩压<该年龄组正常值2个标准差以下。
儿童脓毒血症标准

儿童脓毒血症标准儿童脓毒血症是一种严重的全身感染性疾病,其诊断标准包括以下几个方面:一、临床表现1.发热或低体温:儿童脓毒血症患者通常会出现发热,体温大多在38.3℃以上,但也有可能出现低体温。
2.寒战:患者可能会出现寒战,这是由于炎症反应所引起的。
3.少尿症:由于肾功能受损,患者可能会出现少尿或无尿的情况。
4.头痛、躁动、困倦:这些症状是由于感染引起的神经系统和代谢紊乱所导致的。
5.休克:严重感染可能导致休克,表现为血压下降、面色苍白、四肢厥冷等。
二、体格检查1.体温过低或过高:儿童的体温低于36℃或高于38℃。
2.心率加快:心率超过90次/分。
3.呼吸急促:呼吸频率大于30次/分。
4.神志改变:出现精神萎靡、嗜睡或烦躁不安等症状。
5.局部症状:在受伤或手术部位发现明显的感染灶,如红肿、压痛等。
三、实验室检查1.血常规检查:白细胞计数升高,通常大于10×10⁹/L,中性粒细胞比例增加,但也有可能出现白细胞计数降低的情况。
2.血生化检查:血尿素氮和肌酐水平升高,血乳酸水平升高,C反应蛋白(CRP)和降钙素原(PCT)等炎症指标明显升高。
3.血流动力学检查:出现休克时,收缩压低于90mmHg,心脏指数降低等。
4.其他检查:病原学检查如血培养、尿培养等有助于明确病原菌。
四、其他诊断方法1.超声检查:通过超声检查可以发现深部组织感染、脓肿等病变。
2.X线检查:肺部感染时行X线检查有助于发现肺部病变。
3.CT检查:对于某些深部组织和器官的感染,CT检查可以提供更准确的诊断信息。
综上所述,儿童脓毒血症的诊断标准主要包括临床表现、体格检查、实验室检查和其他诊断方法。
当孩子出现发热、寒战、少尿症等症状时,家长应立即带孩子就医,并告知医生孩子的症状和体征。
医生会根据孩子的具体情况进行体格检查和必要的实验室检查,以明确诊断并制定合适的治疗方案。
同时,家长应该注意孩子的饮食和卫生习惯,增强孩子的免疫力,预防脓毒血症的发生。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
小儿急救——儿科脓毒症【概述】严重感染的患者不断增加,每1000个人中就有3人患严重感染性疾病。
在美国,成人严重感染是第10位的致死原因。
严重感染或感染性休克患者的死亡人数超过乳腺癌、直肠癌、结肠癌、胰腺癌和前列腺癌致死人数的总和。
脓毒症也是世界范围内造成婴儿和儿童死亡的最常见原因之一。
在发达国家,如美国每年有4万多名严重脓毒症患儿,分别是婴儿和儿童死因的第4和第2位。
肺炎等严重感染性疾病始终是我国儿童健康的最大威胁。
脓毒症是指感染引起的全身炎症反应综合征(SIRS)。
过去临床常用的术语,如败血症、菌血症、毒血症等,现统一称脓毒症(sepsis)。
引起感染的病原体可以是细菌,也可以是病毒、真菌、支原体、立克次体等,其中以细菌占多数。
儿童脓毒症最常见的感染部位是肺部和血流感染。
<1岁以血流感染最多见,其次是肺部感染,而>1岁则是肺部感染最多,其次是血流感染。
其他常见感染源有泌尿系统、腹腔、创伤和软组织等。
致死率最高的是心内膜炎和中枢神经系统感染。
值得注意的是不同国家、地区及医院的病原种类可能存在较大差别。
【诊断标准】(一)脓毒症有炎症的症状和体征加上发热或低体温(肛温>38.5℃或<35℃),心率快(低体温患儿可能不存在)同时存在以下至少1个器官功能改变的指证:精神状况改变,低氧血症,血乳酸水平升高,或有洪脉。
(二)严重脓毒症脓毒症出现心血管功能障碍,急性呼吸窘迫征,2个或更多其他器官功能障碍时,称为重症脓毒症。
(三)感染性休克(脓毒性休克)分为2期:1. 代偿期(早期) 临床表现符合下列6项中3项。
①意识改变,烦躁不安或萎靡,表情淡漠。
意识模糊,甚至昏迷、惊厥(多见于失代偿休克);②皮肤改变面色苍白发灰,唇周、指趾紫绀,皮肤花纹,四肢凉。
如有面色潮红,四肢温暖,皮肤干燥为暖休克;③心率脉搏外周动脉搏动细弱,心率、脉搏增快;④毛细血管再充盈时间≥3 s(需除外环境温度影响);⑤尿量<1ml/(kg·h);⑥代谢性酸中毒(除外其他缺血缺氧及代谢因素)。
2. 失代偿期代偿期临床表现加重伴血压下降。
收缩压<该年龄组第5百分位或<该年龄组正常值2个标准差。
即:1~12个月<70 mmHg(1mmHg=0.133 kPa),1~10岁<70 mmHg+[2×年龄(岁)],≥10岁<90 mmHg。
(四)临床分型1. 暖休克为高动力性休克早期,可有意识改变、尿量减少或代酸等,但面色潮红,四肢温暖,脉搏无明显减弱,毛细血管再充盈时间无明显延长。
此期容易漏诊,且可很快转为冷休克。
心率快,血压低,过度通气,中心静脉压高,心输出量低多为失代偿表现。
2. 冷休克为低动力性休克,皮肤苍白、花纹,四肢凉,脉搏快、细弱,毛细血管再充盈时间延长,儿科以冷休克为多。
学术上对感染性休克有不同的定义,针对发展中国家的情况,WHO提出3项诊断标准:①手发凉;②毛细血管再充盈时间大于3s;③脉搏弱快。
为条件有限的地方提供了一个方便快捷的判断方法。
有学者提出,患者1小时内静脉输入等张液体40 ml/kg仍有血压下降或需用血管活性药物始能维持血压在正常范围时,才够诊断标准。
这一标准可用于科研,不利于识别早期休克并及时治疗,欧美国家临床也未普遍采用。
(五)实验室炎症指标1. 白细胞增多(>12×109/L),白细胞减少(<4×109/L),自细胞计数正常,有超过10%的不成熟白细胞。
2. 血浆C反应蛋白(CRP)水平超过正常值的2个标准差。
3. 血浆前降钙素(PCT)水平超过正常值的2个标准差。
【治疗】(一)初始治疗对存在呼吸窘迫及低氧血症的患儿,给予面罩吸氧,必要时也可给予高流量鼻导管或鼻咽持续气道正压通气(CPAP)。
中心静脉通路难以建立时,可先建立外周血管通路或骨髓通路进行液体复苏及使用正性肌力药物。
若必须行插管机械通气治疗,先进行适当的心血管复苏支持,以免在插管过程中出现心血管系统不稳定。
1. 液体复苏:对感染性休克患儿,充分液体复苏是逆转病情,降低病死率最关键的措施。
①第1 h快速输液常用0.9%氯化钠,首剂20 ml/kg,10—20 min推注。
然后评估循环与组织灌注情况(心率、血压、脉搏、毛细血管再充盈时间等)。
若循环无明显改善,可再予第2剂、第3剂,每剂均为10-20 ml /kg。
总量最多可达40-60 ml/kg。
第1 h输液既要避免液量不足,又要注意心肺功能(如肺部罗音、奔马律、肝大、呼吸作功增加等常示心动能衰竭、肺水肿)。
条件允许应监测中心静脉压。
第1 h液体复苏不用含糖液,若有低血糖可用葡萄糖0.5-1 g/kg纠正,婴儿输液时葡萄糖的摄取糖速在4~6 mg/kg·min,新生儿在6~8 mg/kg·min;血糖应控制在≤180mg/dl,当血糖大于200 mg/dl时,可静脉输注胰岛素0.05 u/kg·h。
②继续和维持输液由于血液重新分配及毛细血管渗漏等,感染性休克的液体丢失和持续低血容量可能要持续数日。
因此要继续和维持输液。
继续输液可用l/2-2/3张液体,可根据血电解质测定结果进行调整,6-8 h内输液速度5-10 mL/kg·h。
维持输液用1/3张液体,24h内输液速度2-4 ml/kg·h,24 h后根据情况进行调整。
③休克纠正后,若液体负荷过大超过体重的10%,应使用利尿剂减轻液体过负荷,若无效,可使用持续静脉滤过治疗。
继续及维持输液阶段也要动态观察循环状态,评估液体量是否恰当,随时调整输液方案。
2. 血管活性药物在液体复苏基础上休克难以纠正,血压仍低或仍有明显灌注不良表现,可考虑使用血管活性药物以提高血压、改善组织灌注。
①正性肌力药物:包括中等剂量的多巴胺5-10ug/kg·min、多巴酚丁胺5-10ug/kg·min、小剂量肾上腺素0.05-0.3ug/kg·min,主要增加心肌收缩力,用于血压正常而心肌收缩功能降低(心输出量降低)的严重脓毒症或脓毒性休克患儿。
②扩血管药物:当心输出量降低、外周血管阻力增加、血压尚正常时(即低排高阻型休克)应给予正性肌力药物加用扩血管药物,可降低心室后负荷,有利于心室射血和心输出量增加。
正性肌力药物可选用多巴酚丁胺或多巴胺。
扩血管药物一般用短效制剂,如硝普纳0.5-8ug/kg·min,应从小剂量开始,避光使用。
磷酸二酯酶抑制剂(如氨力农、米力农、依诺昔酮等)具有增加心肌收缩力和扩血管作用,也可用于此类低排高阻休克患儿。
目前临床常用剂量:米力农负荷量25-50μg/kg(>10min,IV),维持量0.25-1.0μg/kg min持续静脉输注;氨力农负荷量0.75-1.0mg/kg(>5min,IV),维持量3-10μg/kg⋅min持续静脉输注。
③升压药物:当心输出量增加、外周血管阻力降低(即高排低阻型休克)时首选去甲肾上腺素输注0.05-0.3ug/kg·min,当需要增加药物以维持血压时,建议加用肾上腺素或肾上腺素替换去甲肾上腺素。
当心输出量、外周血管阻力均降低时(即低排低阻型休克)给予多巴胺(≥10ug/kg·min)或肾上腺素(≥0.3-2.0ug/kg·min)或多巴酚丁胺加去甲肾上腺素。
在治疗过程中进行动态评估,适时调整药物剂量及药物种类,使血流动力学指标达到治疗目标。
切勿突然停药,应逐渐减少用药剂量,必要时小剂量可持续数天。
3. 初始治疗目标在第一个6小时内达到:CRT≤2s,血压正常(同等年龄),外周及中央动脉搏动均正常,肢端温暖,尿量>1ml/kg·h,意识状态正常,中心静脉血氧饱和度(ScvO2)≥70%,心脏指数(CI)3.3-6.0L/min/m2。
(二)抗感染治疗和感染源控制1. 抗微生物制剂治疗诊断严重脓毒症和脓毒性休克后的1小时内应静脉使用有效抗微生物制剂。
需依据流行病学和地方病原流行特点选择覆盖所有疑似病原微生物的经验性药物治疗,如粒细胞缺乏症、难治性或多重耐药菌感染等可联合用药治疗。
如诊断病毒感染所致的严重脓毒症,应尽早抗病毒治疗。
尽可能在应用抗生素前获取血培养(外周、中央或深静脉置管处各1份)或其它感染源培养(如尿、脑脊液、呼吸道分泌物、伤口、其他体液等),但也不能因获取感染源培养困难而延误抗生素治疗。
每日评估抗微生物治疗方案,经验性治疗 3~5天。
一旦明确病原应降阶梯到恰当的单药治疗。
疗程一般7~10天,如果患者病情改善缓慢、存在不能引流的脓腔、金黄色葡萄球菌血症、真菌与病毒混合感染、免疫缺陷,可延长疗程。
2. 感染源控制积极寻找感染源,可选择合适的影像学检查,尽快确定和去除感染灶,如采取清创术、引流、冲洗、修补、感染装置去除等极其重要。
(三)肾上腺皮质激素:无休克的脓毒症患者不推荐使用糖皮质激素,对重症休克疑有肾上腺皮质功能低下(如流脑)、长期使用激素或出现儿茶酚胺抵抗性休克时可以使用。
目前主张小剂量、中疗程。
可用氢化可的松3~5 mg/(kg·d)或甲泼尼龙2~3 ms/(kg·d),分2~3次给予。
有人建议低剂量的氢化可的松持续输注,而不是重复推注。
(四)纠正凝血障碍:早期可给予小剂量肝素5~10 IU /kg皮下注射或静脉输注(注意肝素钠不能皮下注射),每6 h 1次。
若已明确有DIC,则应按DIC常规治疗。
(五)严重脓毒症或脓毒性休克常伴有消化道出血或应激性溃疡,可给予H2受体阻滞剂或质子泵抑制剂治疗。
对机械通气患儿常需要H2受体阻滞剂或质子泵抑制剂预防应激性溃疡。
(六)其他辅助支持治疗1. 血液制品应用:严重脓毒症或脓毒性休克患儿在初始复苏期间,当中心静脉血氧饱和度<70%时,需要保持血红蛋白目标值10g/dl。
当病情稳定后或休克和低氧血症纠正后,则血红蛋白目标值>7g/dl即可。
严重脓毒症患儿血小板<10⨯109/L(没有明显出血)、或血小板<20⨯109/L(有明显出血倾向),应预防性输血小板;当活动性出血、侵入性操作或手术,需要维持较高血小板(≥50⨯109/L)。
2. 丙种球蛋白输注:对严重脓毒症患儿可应用静脉丙种球蛋白输注治疗。
3. 镇痛镇静应用:严重脓毒症机械通气患儿应给予适当镇静治疗,可降低氧耗和有利于维持血流动力学稳定。
脓毒性休克的患儿需避免或谨慎使用依托咪酯或右美托咪啶,因其分别影响肾上腺轴及交感神经系统,不利于血流动力学的稳定。
4. 营养支持治疗:能耐受肠道喂养的严重脓毒症患儿及早予以肠内营养支持,如不耐受可予以肠外营养。
10%葡萄糖(通常是葡萄糖氯化钠溶液)维持输注提供了新生儿和儿童的葡萄糖输送要求,脓毒症时糖的输送要求提高。
