各种条件下多种螯合剂对钙离子和铁离子螯合值数据
螯合剂种类总结及其在不同pH下的对金属离子的螯合能力比较

螯合剂种类总结及其在不同pH下的对金属离子的螯合能力比较螯合剂的种类及其在不同pH值条件下螯合剂的螯合常数一、螯合剂与螯合物具有可供配位孤电子对的分子、原子或离子的化合物能够与具有空轨道的金属离子形成配位键,该化合物称为络合物,如能与配位金属离子形成环状结构的化合物称为螯合剂,形成的络合物称为螯合物。
螯合剂中至少含有一对孤电子对,而金属离子必须有空的价电子轨道,孤电子对填充入金属离子空轨道,电子对属2个原子共享,形成配位键,中心金属离子空轨道杂化。
不同的提供孤电子对的配位体分别与不同金属离子形成正四面体、正六面体、正八面体的螯合物。
1.类型1.1无机类螯合剂聚磷酸盐螯合剂:主要是三聚磷酸钠(STPP)、六偏磷酸钠、焦磷酸钠为主,含磷酸基空间配位基团。
特点:高温下会发生水解而分解,使螯合能力减弱或丧失。
而且其螯合能力受pH值影响较大,一般只适合在碱性条件下作螯合剂。
1.2有机类螯合剂形态分析表明螯合剂提取的重金属主要来源于可交换态或酸溶态、还原态和氧化态。
1.21羧酸型(1)氨基羧酸类:含羧基和胺(氨基)配位基团,如乙二胺四乙酸(EDTA),氨基三乙酸(又称次氮基三乙酸NTA),二亚乙基三胺五乙酸(DTPA )及其盐等。
如:EDTA的4个酸和2个胺(一NRR )的部分都可作为配体的齿,两个氮原子和四个氧原子可提供形成配位键的电子对。
特点:络合能力强,络合稳定常数大,耐碱性好,但分散力弱且不易被生物降解。
(2)羟基羧酸类含羟基、羧基配位基团这类羧酸主要是柠檬酸(CA)、酒石酸(TA)和葡萄糖酸(GA)。
特点:可生物降解,在酸性条件下羟基与羧基不会离解为氧负离子,因而络合能力很弱,不适宜在酸性介质中应用。
(3)羟氨基羧酸类这类酸用作螯合剂的典型代表是羟乙基乙二胺三乙酸(HEDTA)和二羟乙基甘氨酸(DEG)。
特点:大多易于生物降解,在pH=9的弱碱性条件下可螯合铁离子,但对其他离子螯合能力较差。
1.22有机多元膦酸羟基亚乙基-1,1-二膦酸(HEDP )、氨基三亚甲基膦酸(ATMP)、二乙烯三胺五亚甲基膦酸(HTPMP)、三乙烯四胺六亚甲(TETHMP)、双(1,6-亚己基)三胺五亚甲基膦酸(BNHMTPMP)、多氨基多醚基四亚甲基膦酸(PAPEMP)。
螯合剂种类总结及其在不同pH下的对金属离子的螯合能力比较

螯合剂的种类及其在不同pH值条件下螯合剂的螯合常数一、螯合剂与螯合物具有可供配位孤电子对的分子、原子或离子的化合物能够与具有空轨道的金属离子形成配位键,该化合物称为络合物,如能与配位金属离子形成环状结构的化合物称为螯合剂,形成的络合物称为螯合物。
螯合剂中至少含有一对孤电子对,而金属离子必须有空的价电子轨道,孤电子对填充入金属离子空轨道,电子对属2个原子共享,形成配位键,中心金属离子空轨道杂化。
不同的提供孤电子对的配位体分别与不同金属离子形成正四面体、正六面体、正八面体的螯合物。
1.类型1.1无机类螯合剂聚磷酸盐螯合剂:主要是三聚磷酸钠(STPP)、六偏磷酸钠、焦磷酸钠为主,含磷酸基空间配位基团。
特点:高温下会发生水解而分解,使螯合能力减弱或丧失。
而且其螯合能力受pH值影响较大,一般只适合在碱性条件下作螯合剂。
1.2有机类螯合剂形态分析表明螯合剂提取的重金属主要来源于可交换态或酸溶态、还原态和氧化态。
1.21羧酸型(1)氨基羧酸类:含羧基和胺(氨基)配位基团,如乙二胺四乙酸(EDTA),氨基三乙酸(又称次氮基三乙酸NTA),二亚乙基三胺五乙酸(DTPA)及其盐等。
如:EDTA的4个酸和2个胺(—NRR′)的部分都可作为配体的齿,两个氮原子和四个氧原子可提供形成配位键的电子对。
特点:络合能力强,络合稳定常数大,耐碱性好,但分散力弱且不易被生物降解。
(2)羟基羧酸类含羟基、羧基配位基团这类羧酸主要是柠檬酸(CA)、酒石酸(TA)和葡萄糖酸(GA)。
特点:可生物降解,在酸性条件下羟基与羧基不会离解为氧负离子,因而络合能力很弱,不适宜在酸性介质中应用。
(3)羟氨基羧酸类这类酸用作螯合剂的典型代表是羟乙基乙二胺三乙酸(HEDTA)和二羟乙基甘氨酸(DEG)。
特点:大多易于生物降解,在pH=9的弱碱性条件下可螯合铁离子,但对其他离子螯合能力较差。
1.22有机多元膦酸羟基亚乙基-1,1-二膦酸(HEDP)、氨基三亚甲基膦酸(A TMP)、二乙烯三胺五亚甲基膦酸(HTPMP)、三乙烯四胺六亚甲(TETHMP)、双(1,6-亚己基)三胺五亚甲基膦酸(BNHMTPMP)、多氨基多醚基四亚甲基膦酸(PAPEMP)。
螯合剂种类总结及其在不同pH下的对金属离子的螯合能力比较

螯合剂的种类及其在不同pH值条件下螯合剂的螯合常数一、螯合剂与螯合物具有可供配位孤电子对的分子、原子或离子的化合物能够与具有空轨道的金属离子形成配位键,该化合物称为络合物,如能与配位金属离子形成环状结构的化合物称为螯合剂,形成的络合物称为螯合物。
螯合剂中至少含有一对孤电子对,而金属离子必须有空的价电子轨道,孤电子对填充入金属离子空轨道,电子对属2个原子共享,形成配位键,中心金属离子空轨道杂化。
不同的提供孤电子对的配位体分别与不同金属离子形成正四面体、正六面体、正八面体的螯合物。
1.类型1.1无机类螯合剂聚磷酸盐螯合剂:主要是三聚磷酸钠(STPP)、六偏磷酸钠、焦磷酸钠为主,含磷酸基空间配位基团。
特点:高温下会发生水解而分解,使螯合能力减弱或丧失。
而且其螯合能力受pH值影响较大,一般只适合在碱性条件下作螯合剂。
1.2有机类螯合剂形态分析表明螯合剂提取的重金属主要来源于可交换态或酸溶态、还原态和氧化态。
1.21羧酸型(1)氨基羧酸类:含羧基和胺(氨基)配位基团,如乙二胺四乙酸(EDTA),氨基三乙酸(又称次氮基三乙酸NTA),二亚乙基三胺五乙酸(DTPA )及其盐等。
如:EDTA的4个酸和2个胺(一NRR )的部分都可作为配体的齿,两个氮原子和四个氧原子可提供形成配位键的电子对。
特点:络合能力强,络合稳定常数大,耐碱性好,但分散力弱且不易被生物降解。
(2)羟基羧酸类含羟基、羧基配位基团这类羧酸主要是柠檬酸(CA)、酒石酸(TA)和葡萄糖酸(GA)。
特点:可生物降解,在酸性条件下羟基与羧基不会离解为氧负离子,因而络合能力很弱,不适宜在酸性介质中应用。
(3)羟氨基羧酸类这类酸用作螯合剂的典型代表是羟乙基乙二胺三乙酸(HEDTA)和二羟乙基甘氨酸(DEG)。
特点:大多易于生物降解,在pH=9的弱碱性条件下可螯合铁离子,但对其他离子螯合能力较差。
1.22有机多元膦酸羟基亚乙基-1,1-二膦酸(HEDP )、氨基三亚甲基膦酸(ATMP)、二乙烯三胺五亚甲基膦酸(HTPMP)、三乙烯四胺六亚甲(TETHMP)、双(1,6-亚己基)三胺五亚甲基膦酸(BNHMTPMP)、多氨基多醚基四亚甲基膦酸(PAPEMP)。
各种螯合剂的螯合值对照表
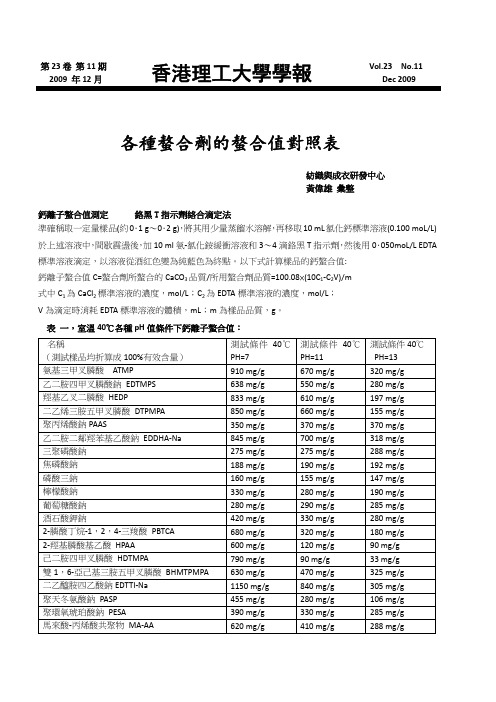
第23卷第11期2009 年12月香港理工大學學報 Vol.23 No.11 Dec 2009各種螯合劑的螯合值對照表紡織與成衣研發中心黃偉雄彙整鈣離子螯合值測定------鉻黑T指示劑絡合滴定法準確稱取一定量樣品(約0.1 g~0.2 g),將其用少量蒸餾水溶解,再移取10 mL氯化鈣標準溶液(0.100 moL/L)於上述溶液中,間歇震盪後,加10 ml氨-氯化銨緩衝溶液和3~4滴鉻黑T指示劑,然後用0.050moL/L EDTA 標準溶液滴定,以溶液從酒紅色變為純藍色為終點。
以下式計算樣品的鈣螯合值:鈣離子螯合值C=螯合劑所螯合的CaCO3品質/所用螯合劑品質=100.08×(10C1-C2V)/m式中C1為CaCl2標準溶液的濃度,mol/L;C2為EDTA標準溶液的濃度,mol/L;V為滴定時消耗EDTA標準溶液的體積,mL;m為樣品品質,g。
表一,室溫40℃各種pH值條件下鈣離子螯合值:名稱(測試樣品均折算成100%有效含量)測試條件40℃PH=7測試條件40℃PH=11測試條件40℃PH=13氨基三甲叉膦酸ATMP 910 mg/g 670 mg/g 320 mg/g 乙二胺四甲叉膦酸鈉EDTMPS 638 mg/g 550 mg/g 280 mg/g 羥基乙叉二膦酸HEDP 833 mg/g 610 mg/g 197 mg/g 二乙烯三胺五甲叉膦酸DTPMPA 850 mg/g 660 mg/g 155 mg/g 聚丙烯酸鈉PAAS 350 mg/g 370 mg/g 370 mg/g 乙二胺二鄰羥苯基乙酸鈉EDDHA-Na 845 mg/g 700 mg/g 318 mg/g 三聚磷酸鈉275 mg/g 275 mg/g 288 mg/g 焦磷酸鈉188 mg/g 190 mg/g 192 mg/g 磷酸三鈉160 mg/g 155 mg/g 147 mg/g 檸檬酸鈉330 mg/g 280 mg/g 190 mg/g 葡萄糖酸鈉280 mg/g 290 mg/g 285 mg/g 酒石酸鉀鈉420 mg/g 330 mg/g 280 mg/g 2-膦酸丁烷-1,2,4-三羧酸PBTCA 680 mg/g 320 mg/g 180 mg/g 2-羥基膦酸基乙酸HPAA 600 mg/g 120 mg/g 90 mg/g 己二胺四甲叉膦酸HDTMPA 790 mg/g 90 mg/g 33 mg/g 雙1,6-亞己基三胺五甲叉膦酸BHMTPMPA 630 mg/g 470 mg/g 325 mg/g 二乙醯胺四乙酸鈉EDTTI-Na 1150 mg/g 840 mg/g 305 mg/g 聚天冬氨酸鈉PASP 455 mg/g 280 mg/g 106 mg/g 聚環氧琥珀酸鈉PESA 390 mg/g 330 mg/g 285 mg/g 馬來酸-丙烯酸共聚物MA-AA 620 mg/g 410 mg/g 288 mg/g第23卷第11期2009 年12月香港理工大學學報 Vol.23 No.11 Dec 2009馬來酸-丙烯酸共聚物MA-AA 620 mg/g 410 mg/g 288 mg/g二乙烯三胺五乙酸五鈉DTPA5Na 420 mg/g 180 mg/g 85 mg/g次氮基三乙酸NTA 480 mg/g 330 mg/g 260 mg/g亞氨基二乙酸IDA 460 mg/g 190 mg/g 70 mg/g矽酸鈉模數=1 270 mg/g 280 mg/g 320 mg/g矽酸鈉模數=3 380 mg/g 335 mg/g 360 mg/g鐵離子螯合值----磺基水楊酸顯色測定待測樣品溶液配製:準確稱取待測樣品5.000 g,加去離子水溶解,移至500mL容量瓶中定容至刻度,搖勻備用待測。
螯合铁ph

螯合铁ph螯合铁是指通过配位键结合,将铁元素和一些有机化合物形成一个稳定的配合物,称为螯合铁。
由于铁是生命体内必需的元素之一,因此螯合铁在生物领域中具有重要的应用价值。
本文将介绍螯合铁在不同ph条件下的性质及其在生物领域中的应用。
1.在中性条件下的性质在中性条件下,螯合铁具有稳定性强、相对不易水解以及抗氧化等优点。
常见的中性螯合剂有EDTA(乙二胺四乙酸)和DFO(除铁酸)。
这两种螯合剂与铁离子形成的配合物非常稳定,可用于医学上的铁摄取和铁的治疗。
例如,EDTA可用于治疗中毒性铁过量和铜过量引起的中毒,DFO则可用于治疗化疗引起的铁过量。
在酸性条件下,螯合铁的性质发生了较明显的改变。
由于酸性条件下容易发生配位键的水解反应,使得螯合铁的稳定性降低。
另外,在酸性条件下,铁的还原性增强,容易发生氧化还原反应。
这些因素导致螯合铁在酸性条件下的应用相对较少。
但是,在某些特殊情况下,例如需要在人体胃酸下使用铁补充剂时,铁需要形成酸性条件下的可溶性盐,此时可使用了一些特殊的螯合剂。
在碱性条件下,螯合剂容易被质子化,在形成配合物时和铁离子会发生较为明显的静电作用。
由于静电力的作用,碱性螯合铁的稳定性相对较低。
同时,碱性条件下的螯合铁还容易被氧化,这主要是由于氢氧根离子的方向性使得氧化剂更易接近螯合铁分子。
但是,由于碱性条件下的生理环境相对较少,因此碱性螯合铁的应用相对较少。
4.在生物领域中的应用螯合剂在生物领域中应用相对不多,但是它们在一些重要的生物过程中扮演着重要的角色。
例如,血红蛋白和肌红蛋白中的铁均以螯合物形式存在。
铁和螯合剂还可用于检测和治疗缺铁性贫血,这是因为低铁血红蛋白经铁补充剂治疗后,它需要形成铁的可溶性盐以被吸收。
此外,螯合铁在医学中也有广泛的应用。
例如,DFO可用于治疗黑色素瘤(一种肿瘤),这是因为黑色素细胞中存在大量的铁质。
EDTA也可用于治疗铅中毒等疾病。
总的来说,螯合铁在生物领域中具有重要的应用价值,但它的性质和应用还需要进一步研究和探索。
纺织印染助剂+螯合剂+螯合能力的测定

ICS 71.100.40G 70囝目中华人民共和国国家标准GB/T 2 1 884--2008纺织印染助剂螯合剂螯合能力的测定Textile auxiliaries--Chelating agents—Determination of the capability of chelating2008-05-15发布2008—11—01实施宰瞀徽鬻瓣警糌瞥翼发中GB/T 21884--2008刖舌本标准附录A为规范性附录。
本标准由中国石油和化学工业协会提出。
本标准由全国染料标准化技术委员会(SAC/TC 134)归口。
本标准起草单位:浙江传化股份有限公司、沈阳化工研究院。
本标准主要起草人:赵梅、陈红梅、沈淑英、姬兰琴。
GB/T 21884--2008纺织印染助剂螯合剂螯合能力的测定1范围本标准规定了纺织印染助剂中螯合剂螯合能力的测定方法。
本标准适用于纺织印染助剂中有机多元膦酸盐、高分子聚羧酸及其盐类螯合剂螯合能力的测定;也适用于乙二胺四乙酸(EDTA)、N-羟基乙二胺四乙酸(HEDTA)、二乙基四胺五乙酸(DTPA)及其盐类的螯合剂螯合能力的测定。
2规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB/T 601化学试剂标准滴定溶液的制备GB/T 603化学试剂试验方法中所用制剂及制品的制备(GB/T 603--2002,ISO 6353—1:1982,NEQ)GB/T 6792002化学试剂乙醇(95Yo)GB/T 6368 1993表面活性剂水溶液pH值的测定电位法(neq ISO 4316:1977)GB/T 6682分析实验室用水规格和试验方法(GB/T 6682 2008,ISO 3696:1987,MOD)3术语下列术语和定义适用于本标准。
螯合能力 钙镁离子 铁离子
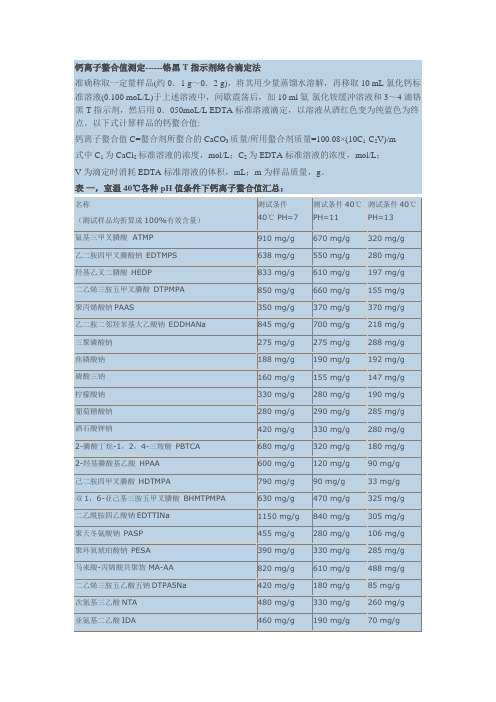
钙离子螯合值测定------铬黑T指示剂络合滴定法
准确称取一定量样品(约0.1 g~0.2 g),将其用少量蒸馏水溶解,再移取10 mL氯化钙标准溶液(0.100 moL/L)于上述溶液中,间歇震荡后,加10 ml氨-氯化铵缓冲溶液和3~4滴铬黑T指示剂,然后用0.050moL/L EDTA标准溶液滴定,以溶液从酒红色变为纯蓝色为终点。
以下式计算样品的钙螯合值:
钙离子螯合值C=螯合剂所螯合的CaCO3质量/所用螯合剂质量=100.08×(10C1-C2V)/m
式中C1为CaCl2标准溶液的浓度,mol/L;C2为EDTA标准溶液的浓度,mol/L;
V为滴定时消耗EDTA标准溶液的体积,mL;m为样品质量,g。
表一,室温40℃各种pH值条件下钙离子螯合值汇总:。
螯合剂铁螯合值测定方法简介及评价_洪焱根

洪焱根,王魁,冯彬,马俊,栾志乾(黎明化工研究院,河南洛阳471001)摘要:介绍了目前常用螯合剂铁螯合值测定方法[络合滴定法、Fe(OH)3沉淀法、碘量法]及原理;采用这3种方法测定乙二胺四乙酸二钠(EDTA-2Na)铁螯合值,并对测定结果与理论值进行比较.结果表明:络合滴定法精密度及准确度均最高,操作简便,不受放置时间、溶液颜色的影响,且测定结果与理论值相符.Fe(OH)3沉淀法和碘量法误差大、准确度低,测定结果随样品质量变化而变化.因此,络合滴定法是测定螯合剂铁螯合值的最适宜方法.关键词:铁螯合值;络合滴定法;Fe(OH)3沉淀法;碘量法中图分类号:TQ317文献标识码:C文章编号:1004-0439(2010)10-0053-04螯合剂铁螯合值测定方法简介及评价Introduction and assessment on measurement methods ofFe(III)chelation value of chelating agentHONG Yan -gen,WANG Kui,FENG Bin,MA Jun,LUAN Zhi -qian(Liming Research Insitute of Chemcial Industry,Luoyang 471001,China)Abstract :The methods (complexometric titration method,ferric hydroxide precipitation method and iodo -metric method)commonly used to determine Fe(III)chelation value and the measurement mechasim were intro -duced.The three methods were used to test Fe(III)chelation values of disodium edta (EDTA-2Na),and the mea -sured values were compared with theoretical values.The results showed that complexometric titration method had the highest precision and accuracy.And this method was simple,convenient and was not influenced by the placing time and sample color,and the measured value was in accord with the theoretical value.Both ferric hy -droxide precipitation method and iodometric method had big system error and low accuracy.And their measured values varied with the sample weight.Therefore,complexometric titration method was the most feasible method to determine Fe(III)chelation value of chelating agents.Key words :Fe(III)chelation value;complexometric titration method;ferric hydroxide precipitation method;iodometry method收稿日期:2009-12-24作者简介:洪焱根(1981-),男,江西景德镇人,工程师,学士,主要从事过氧化氢生产工艺技术和造纸助剂开发工作近年来,随着科学技术日益发展,螯合剂已得到广泛的应用,特别是在印染、造纸、纺织、工业清洗、水处理等方面.造纸工业中螯合剂常用作过氧化氢稳定剂,可减少过氧化氢发生无效催化分解,降低漂白成本,提高漂白效率.[1]在染整加工时金属螯合剂用作硬水软化剂,也可在过氧化氢漂白中用作稳定剂.[2]螯合剂一般为多种有效成分(如氨基羧酸盐、有机磷酸盐、无机磷酸盐、有机高分子聚合物等)的复配物,具有较强螯合Ca 2+、Mg 2+、Fe 3+的能力,能有效去除溶液中金属离子,获得较好的使用效果.螯合力是指1g 螯合剂可螯合多少mg 金属离子的能力.螯合容量越高,其螯合能力越强.目前,测定螯合剂钙螯合值和镁螯合值的方法较成熟[3],但测定铁螯合值的方法较多,依测定原理,可分为EDTA 络合滴定法、碘量法、Fe(OH)3沉淀法[4-6]、磺基水杨酸显色分光光度法[7]等.这些方法测定结果不尽相同[4,7],存有争印染助剂TEXTILE AUXILIARIES Vol.27No.10Oct .2010第27卷第10期2010年10月印染助剂27卷议.本文主要叙述络合滴定法、碘量法、Fe(OH)3沉淀法的测定原理,并以工业上最常用的乙二胺四乙酸二钠(EDTA-2Na)作为螯合剂样本,分别对它们的测定结果进行分析与评价.1测定原理1.1络合滴定法在酸性条件下,Fe3+可与磺基水杨酸反应形成红色配合物.故可在酸性溶液中,以磺基水杨酸作指示剂,用Fe3+标准溶液滴定螯合剂样品溶液,当螯合剂反应完全后,微过量的Fe3+即可与磺基水杨酸反应生成红色配合物,此即为滴定终点.1.2Fe(OH)3沉淀法在碱性条件下,Fe3+可与OH-反应形成稳定红褐色Fe(OH)3沉淀.因此,控制螯合剂样品溶液的pH值较高,用Fe3+标准溶液进行滴定,过量的Fe3+与OH-反应致溶液中出现红褐色絮状沉淀即为滴定终点.1.3碘量法Fe3+具有氧化性,可将I-氧化成I2.利用这一性质,用间接碘量法进行铁螯合值测定,即向一定质量螯合剂溶液中加入过量硫酸铁铵溶液,螯合剂与Fe3+作用,向剩余的Fe3+溶液中加入过量KI,生成的I2以淀粉作指示剂用Na2S2O3溶液滴定.为消除Fe3+水解对测定结果的影响,滴定反应溶液pH≤2.2.铁离子与碘化钾氧化还原反应式如下:硫代硫酸钠与碘反应式如下:2试验2.1试剂及仪器试剂:乙二胺四乙酸二钠(EDTA-2Na)、磺基水杨酸、淀粉、氢氧化钠、硫酸铁铵、碘化钾、硫代硫酸钠等均为分析纯;螯合剂HPC-1(黎明化工研究院).仪器:电子天平,精度0.0001g;PHS-25型pH计,分辨率0.01pH,配有复合电极.2.2滴定溶液配制EDTA-2Na样品溶液(0.01mol/L):按GB/T601-2002《化学试剂标准滴定溶液的制备》制备0.1mol/L 标准溶液,用移液管准确吸取25mL于250mL容量瓶中,用去离子水定容.Fe3+滴定溶液(0.01mol/L):参考GB/T602-2002《化学试剂杂质测定用标准滴定溶液的制备》,准确称取4.822g(精确至0.0001g)硫酸铁铵[FeNH4(SO4)2·12H2O]溶于水中,加1mL98%浓硫酸后,移至1000mL容量瓶中,定容.Na2S2O3滴定溶液(0.01mol/L):按GB/T601-2002中所示方法制备0.1mol/L标准溶液,用移液管准确吸取25mL于250mL容量瓶中,用去离子水定容.2.3铁螯合值表示方法铁螯合值为1g螯合剂螯合Fe3+的质量,以Y表示,单位为mg/g.2.4铁螯合值测定2.4.1络合滴定法用移液管准确移取20mL EDTA-2Na样品溶液于250mL三角瓶中,用去离子水稀释至100mL,滴加2mL磺基水杨酸指示剂(5%),用Fe3+滴定溶液进行滴定,至黄色变成淡红色为滴定终点.滴定在60℃恒温水浴中进行.铁螯合值计算如式(1):式(1)中,c为Fe3+滴定溶液浓度,mol/L;V为滴定消耗的Fe3+标准溶液体积,mL;M为样品质量,g;56为铁原子摩尔质量,g/moL.2.4.2Fe(OH)3沉淀法用移液管准确移取20mL EDTA-2Na样品溶液于250mL三角瓶中,加去离子水稀释至100mL,用20% NaOH溶液调pH=12,然后用Fe3+滴定溶液进行滴定,至溶液中出现絮状沉淀即为终点.滴定过程中用NaOH 溶液维持试样pH=12.铁螯合值计算同式(1).2.4.3碘量法用移液管准确移取20mL EDTA-2Na样品溶液于250mL碘量瓶中,加入50mL Fe3+滴定溶液,反应一段时间以后,加入5mL0.1mol/L的KI溶液,封盖,于暗处放置0.5h后,用Na2S2O3滴定溶液进行滴定.至溶液呈浅黄色时加入5滴淀粉指示剂(0.5%),继续滴定至溶液蓝色消失变成无色为终点.铁螯合值计算如式(2):式(2)中,C1为加入的Fe3+滴定溶液浓度,mol/L;V1为加入的Fe3+滴定溶液体积,mL;C2为Na2S2O3滴定溶液浓度,mol/L;V2为滴定消耗的Na2S2O3滴定溶液体积,mL; 56为铁原子摩尔质量,g/moL.3结果与讨论3.1EDTA-2Na理论铁螯合值乙二胺四乙酸二钠(EDTA-2Na)摩尔质量为3362Fe3++2I-→2Fe2++I2 I2+2S2O32-→2I-+S4O62-(1) Y=56×c×V/m(2) Y=56×(C1V1-C2V2)/m5410期g/mol,分子式为C 10H 14N 2Na 2O 8,与Fe 3+可以生成稳定的螯合物(螯合物的稳定常数[8]146:lg β=24.23),螯合反应[n (EDTA-2Na)∶n (Fe 3+)=1∶1],据此可计算出EDTA-2Na 理论铁螯合值:式(3)中,56为铁原子摩尔质量,g/mol.3.2精密度不同方法测定结果及相对标准偏差(RSD)见表1.由表1可知,络合滴定法相对标准偏差(RSD)最小,精密度最高,测定结果与理论值相符;Fe(OH)3沉淀法精密度最差,原因是其沉淀物在试样溶液中形成较慢,且受溶液本身颜色影响而不易观察.3.3放置时间如图1所示,络合滴定法和Fe(OH)3沉淀法测定结果基本不受放置时间的影响.碘量法测定值随放置时间延长而逐渐减小,原因是在碘量法测定过程中,过量的I -在酸性条件下逐渐被空气氧化生成I 2;同时体系中生成的Fe 2+在酸性条件下被空气氧化成Fe 3+,继续氧化溶液中过量的I -,导致测定结果随放置时间延长逐渐减小.3.4准确度由图2可知,络合滴定法测定结果不受样品质量影响,准确度较高;Fe(OH)3沉淀法和碘量法测定结果均与样品质量的倒数呈线性关系,且与所测平均值(表1)相对误差太大,准确度较差,故均不适合作为铁螯合值测定方法.其原因:(1)Fe(OH)3沉淀法,EDTA 与Fe 3+所生成配合物稳定常数lg K =24.23,在pH 值为12时EDTA 酸效应系数[8]149:lg α(H)=0.01、Fe 3+水解副反应系数[9]482:lg αM(OH)=17.7,故其条件稳定常数lg K ′=lg K -lg α(H)-lg αM(OH)=6.52;OH -与Fe 3+所生成配合物Fe(OH)的累积稳定常数[8]142:lg β1=11.87,大于前者的条件稳定常数,故OH -先于EDTA 与Fe 3+发生络合反应.滴定时,为保持试样溶液pH 值不变而不断补加OH -,即溶液中OH -浓度始终保持不变,则加入的Fe 3+不与EDTA 发生络合反应(或相对于OH -,发生络合反应的EDTA 太少,可忽略不计).因此,在滴定过程中,Fe 3+只与OH -进行络合反应生成Fe(OH)3胶体,继续滴定,溶液中Fe(OH)3胶体浓度逐渐增大,至一定浓度时凝聚成沉淀,从而到达滴定终点.三角瓶中试样溶液初始体积不变(100mL),即溶液中OH -数量不变,且EDTA 对Fe(OH)3胶体凝聚成沉淀的浓度影响不大,故滴定消耗的Fe 3+溶液体积保持不变,依据铁螯合值计算式(1),测定结果与所取样品质量的倒数呈线性关系.当螯合剂本身性质对Fe(OH)3胶体凝聚成沉淀的浓度有影响时,铁螯合值测定结果与样品质量的倒数就会偏离线性关系.(2)碘量法,在酸性溶液中,用淀粉作指标剂进行碘量法滴定,在滴定完成后蓝色重现的原因:溶液中存在痕量Fe 3+,促进了I -被空气氧化[10](即痕量Fe 3+起催化作用),引起蓝色重现的最低Fe 3+质量浓度为0.1mg/75mL.文献[11]进一步证实了水中Fe 3+为碘量法的干扰物质(催化I -被空气氧化),并求出了出现滴定终点“重蓝”现象的最低Fe 3+质量浓度0.11mg/70mL.2.4.3所述碘量法中,碘量瓶中试样溶液Fe 3+质量浓度垌0.11mg/70mL,故滴定过程中,与Na 2S 2O 3反应的I 2是溶液Y ==166.67mg/g1g ×56g/mol ×1000336g/mol(3)表1不同方法测定结果及RSD测定方法铁螯合值/(mg ·g -1)测定值络合滴定法168.75373.17378.19平均值167.73RSD/%与理论值相对误差/%0.330.64375.58375.10213.33碘量法377.03375.820.46125.49213.75212.50Fe(OH)3沉淀法210.42212.600.5527.56213.33167.42167.17167.50167.83放置时间/min■—络合滴定法;●—Fe(OH)3沉淀法;▲—碘量法图1放置时间对测定结果的影响铁螯合值/(m g ·g -1)40425400375350225200175150302010●▲■●▲■●▲■●▲■●▲■洪焱根,等:螯合剂铁螯合值测定方法简介及评价55印染助剂27卷中I -在Fe 3+催化作用下被空气氧化生成,而并非被Fe 3+氧化生成,即滴定结果与溶液中Fe 3+质量浓度无关,只与空气氧化时间(即试样溶液在滴定前放置时间)有关.放置时间越长,I -被空气氧化生成的I 2越多(直至I -被全部氧化),消耗Na 2S 2O 3滴定溶液体积也相应增多,测定结果就越小,这与3.3试验结果一致.当放置时间一定时,滴定消耗Na 2S 2O 3滴定溶液体积为一定值,依据铁螯合值计算公式(2)可知,测定结果与样品质量的倒数呈线性关系.因滴定消耗Na 2S 2O 3滴定溶液体积只与试样溶液放置时间有关,而与试样溶液种类无关,故不同螯合剂在样品质量相同时测定结果相同.3.5准确度验证采用有机膦酸复配型螯合剂HPC-1,按2.4所述方法,对3.4结果进行验证,并与EDTA-2Na 进行对比.结果见图3、图4.由图3~4可以看出,试验结果符合3.4推论,即对于Fe(OH)3沉淀法,测定结果受样品质量影响,若不同螯合剂对Fe(OH)3胶体凝聚成沉淀的浓度影响程度不同,则其测定结果受样品质量的影响程度也不同;对于碘量法,放置时间相同时,不同螯合剂测定结果与样品质量的倒数呈同一线性关系,与螯合剂本身性质无关.3.6测定方法综合比较(1)络合滴定法操作简单、快速,滴定终点突跃明显,精密度及准确度均最高,测定结果与理论值相符.(2)Fe(OH)3沉淀法滴定突跃不明显,终点不易观察,且易受样品本身颜色影响,平行测定相对误差大;因pH=12时Fe 3+与OH -形成Fe(OH)配合物的累积稳定常数比与EDTA-2Na 形成配合物的条件稳定常数大,且在滴定时溶液OH -浓度保持不变,故测定结果随样品质量变化而变化,方法误差大,准确度低.(3)碘量法滴定突跃明显,平行测定相对误差较小;但在酸性条件下,与Na 2S 2O 3反应的I 2是溶液中的I -在Fe 3+催化作用下被空气氧化生成,而并非被Fe 3+氧化生成,故放置时间一定时,测定结果与样品质量的倒数呈线性关系,方法误差大,准确度低.4结论(1)在3种方法中,络合滴定法精密度及准确度均最高,测定结果不受放置时间及样品质量的影响,且与理论值相符,是测定螯合剂铁螯合值最适宜的方法.(2)Fe(OH)3沉淀和碘量法方法误差大、准确度低,测定结果随样品质量变化而变化,均不适合作为螯合剂铁螯合值的测定方法.参考文献:[1]李海明,杨立宏.制浆和漂白技术的进展[J].国际造纸,2004,23(6):22-24.[2]叶金鑫.应用于染整加工的金属螯合剂[J].现代纺织技术,2002,10(1):46-50.[3]俞英珍,金鲜花,傅佳亚.钙离子螯合力测试方法及比较[J].印染助剂,2006,23(12):40-42.[4]沈淑英,魏艳,赵梅,等.螯合铁离子能力测定方法比较[J].印染助剂,2009,26(7):50-52.[5]邢富强,刘学.新型螯合分散剂的研制与应用[J].印染助剂,2006,23(6):43-46.[6]蒲宗耀,黄玉华,蒲实.无磷耐碱高效螯合分散稳定剂的研制及应用[J].纺织科技进展,2006(6):20-24.[7]魏艳,沈淑英,赵梅,等.磺基水杨酸显色分光光度法测定螯合剂螯合铁能力的研究[J].清洗世界,2009,25(3):23-26.[8]李梦龙.化学数据速查手册[M].北京:化学工业出版社,2003.[9]华东理工大学分析化学教研组等.分析化学[M].北京:高等教育出版社,2001.[10] B.曼努兴等著,王子云摘译.碘量法滴定终点的改进[J].化学世界,1956(7):314.[11]李秀珍.碘量法滴定终点为什么出现“重蓝”现象[J].大学化学,1998,3(4):46-47.样品质量的倒数/g -1■—HPC-1;●—EDTA-2Na图3Fe(OH)3沉淀法测定不同螯合剂的铁螯合值铁螯合值/(m g ·g -1)6020005000300●■●■●■1509012010001500■样品质量的倒数/g -1■—HPC-1;●—EDTA-2Na图4碘量法测定不同螯合剂的铁螯合值铁螯合值/(m g ·g -1)602500500020●■80100100020001500■■●●■40样品质量的倒数/g -1■—络合滴定法;●—Fe(OH)3沉淀法;▲—碘量法图2取样质量不同样品测定值铁螯合值/(m g ·g -1)401500120090060030003020●▲■●▲■●▲■10605056。
各种螯合剂的螯合值对照表

第23卷第11期2009 年12月香港理工大學學報 Vol.23 No.11 Dec 2009各種螯合劑的螯合值對照表紡織與成衣研發中心黃偉雄彙整鈣離子螯合值測定------鉻黑T指示劑絡合滴定法準確稱取一定量樣品(約0.1 g~0.2 g),將其用少量蒸餾水溶解,再移取10 mL氯化鈣標準溶液(0.100 moL/L)於上述溶液中,間歇震盪後,加10 ml氨-氯化銨緩衝溶液和3~4滴鉻黑T指示劑,然後用0.050moL/L EDTA 標準溶液滴定,以溶液從酒紅色變為純藍色為終點。
以下式計算樣品的鈣螯合值:鈣離子螯合值C=螯合劑所螯合的CaCO3品質/所用螯合劑品質=100.08×(10C1-C2V)/m式中C1為CaCl2標準溶液的濃度,mol/L;C2為EDTA標準溶液的濃度,mol/L;V為滴定時消耗EDTA標準溶液的體積,mL;m為樣品品質,g。
表一,室溫40℃各種pH值條件下鈣離子螯合值:名稱(測試樣品均折算成100%有效含量)測試條件40℃PH=7測試條件40℃PH=11測試條件40℃PH=13氨基三甲叉膦酸ATMP 910 mg/g 670 mg/g 320 mg/g 乙二胺四甲叉膦酸鈉EDTMPS 638 mg/g 550 mg/g 280 mg/g 羥基乙叉二膦酸HEDP 833 mg/g 610 mg/g 197 mg/g 二乙烯三胺五甲叉膦酸DTPMPA 850 mg/g 660 mg/g 155 mg/g 聚丙烯酸鈉PAAS 350 mg/g 370 mg/g 370 mg/g 乙二胺二鄰羥苯基乙酸鈉EDDHA-Na 845 mg/g 700 mg/g 318 mg/g 三聚磷酸鈉275 mg/g 275 mg/g 288 mg/g 焦磷酸鈉188 mg/g 190 mg/g 192 mg/g 磷酸三鈉160 mg/g 155 mg/g 147 mg/g 檸檬酸鈉330 mg/g 280 mg/g 190 mg/g 葡萄糖酸鈉280 mg/g 290 mg/g 285 mg/g 酒石酸鉀鈉420 mg/g 330 mg/g 280 mg/g 2-膦酸丁烷-1,2,4-三羧酸PBTCA 680 mg/g 320 mg/g 180 mg/g 2-羥基膦酸基乙酸HPAA 600 mg/g 120 mg/g 90 mg/g 己二胺四甲叉膦酸HDTMPA 790 mg/g 90 mg/g 33 mg/g 雙1,6-亞己基三胺五甲叉膦酸BHMTPMPA 630 mg/g 470 mg/g 325 mg/g 二乙醯胺四乙酸鈉EDTTI-Na 1150 mg/g 840 mg/g 305 mg/g 聚天冬氨酸鈉PASP 455 mg/g 280 mg/g 106 mg/g 聚環氧琥珀酸鈉PESA 390 mg/g 330 mg/g 285 mg/g 馬來酸-丙烯酸共聚物MA-AA 620 mg/g 410 mg/g 288 mg/g第23卷第11期2009 年12月香港理工大學學報 Vol.23 No.11 Dec 2009馬來酸-丙烯酸共聚物MA-AA 620 mg/g 410 mg/g 288 mg/g二乙烯三胺五乙酸五鈉DTPA5Na 420 mg/g 180 mg/g 85 mg/g次氮基三乙酸NTA 480 mg/g 330 mg/g 260 mg/g亞氨基二乙酸IDA 460 mg/g 190 mg/g 70 mg/g矽酸鈉模數=1 270 mg/g 280 mg/g 320 mg/g矽酸鈉模數=3 380 mg/g 335 mg/g 360 mg/g鐵離子螯合值----磺基水楊酸顯色測定待測樣品溶液配製:準確稱取待測樣品5.000 g,加去離子水溶解,移至500mL容量瓶中定容至刻度,搖勻備用待測。
edta螯合比

edta螯合比
EDTA,即乙二胺四乙酸,是一种广泛应用于分析化学和医学领域的多用途螯合剂。
它能与许多金属离子形成稳定的水溶性络合物。
关于EDTA的螯合比,我们可以从以下几个方面进行探讨:
首先,EDTA的分子结构使其具有很强的螯合能力。
分子中有两个氨氮原子和四个羧氧原子,这使得EDTA分子能够与金属离子形成多个配位键,从而形成稳定的螯合物。
其次,EDTA与金属离子的螯合比通常为1:1。
这是由于EDTA分子中的配位原子数量与大多数金属离子的配位数相匹配。
这种1:1的螯合比意味着每一个EDTA分子可以与一个金属离子形成稳定的络合物。
然而,实际情况中,由于溶液的pH值、离子强度、络合物稳定常数等因素的影响,EDTA与金属离子的具体螯合比可能会发生变化。
在某些条件下,EDTA分子可能会与两个或更多的金属离子形成络合物,或者在某些情况下,一个金属离子可能会与多个EDTA分子形成络合物。
此外,值得一提的是,尽管EDTA通常与金属离子形成1:1的螯合物,但在某些特定条件下,也可能形成其他比例的螯合物。
例如,在某些高浓度的金属离子溶液中,EDTA 可能会与两个或更多的金属离子形成多齿螯合物。
综上所述,EDTA的螯合比是一个相对复杂的概念,受到多种因素的影响。
尽管通
常为1:1,但在实际应用中应考虑各种因素对螯合比的影响。
螯合剂种类

螯合剂种类螯合剂是一种化学物质,可以与金属离子形成稳定的络合物,从而改善金属离子的稳定性、降低金属离子的毒性或增加金属的可溶性。
螯合剂可以广泛应用于医学、农业和工业等领域。
以下是常用的螯合剂种类:1. EDTA(乙二胺四乙酸)EDTA是一种常用的螯合剂,能够络合和稳定多种金属离子,如钙、镁、锰、铁、铜和锌等元素。
EDTA还可以用于垃圾处理和水处理等领域。
2. DTPA(二异丙基三胺五乙酸)DTPA是一种能够络合稀土元素和铁离子的螯合剂,广泛应用于农业和医学领域。
它还可以用于石油开采、污水处理和金属清洗等工业领域。
3. EGTA(四乙二胺四乙酸)EGTA是一种专门用于螯合钙离子的螯合剂,可以被用来研究细胞内的钙离子通路。
EGTA也被应用于医学领域,如心脏手术中的心脏停跳。
4. CDTA(半胱氨酸)CDTA是一种钙螯合剂,能够在中性条件下络合和稳定钙离子。
它可以用于处理含有钙的污水,增强防腐剂的稳定性,以及帮助染料的溶解等领域。
5. NTA(乙二胺四乙酸)NTA是一种可以络合和稳定铁、锰、铜、镍和钴等金属离子的螯合剂。
NTA在医学领域已经被用于治疗重金属中毒。
6. 1,10-菲啰啉1,10-菲啰啉可以络合和稳定铁、钴、镍、铜和锌等金属离子,广泛应用于电池制造、染料制造和金属清洗等工业领域。
7. HEEDTA(羟乙基乙二胺三乙酸)HEEDTA是一种具有高螯合能力的螯合剂,可以络合稀土金属、铁和锰等金属离子。
HEEDTA在化妆品制造中被用作防腐剂。
8. EDDHA(乙二胺二(羟基苯甲酸))EDDHA是一种钙螯合剂,能够提高土壤中铁的可溶性,增加植物根系对铁的吸收率。
EDDHA广泛应用于农业领域,用于防治铁缺乏症和改善植物生长。
9. IDA(亚硝基二乙酸)IDA是一种用于治疗缺铁性贫血的药物,它能够将铁离子转移进入人体细胞,从而增加血红蛋白的合成。
10. DFO(除铁胺)DFO是一种用于治疗铁过载症的药物,能够络合和稳定体内的自由铁离子,改善铁过量引起的神经系统损害。
螯合剂使用说明书

螯合剂使⽤说明书产品说明螯合剂产品介绍近年来,随着废弃物处理处置相关法律的完善以及政府对污染物排放的严格管制,相应的垃圾焚烧等产⽣的飞灰污染问题也急需解决,特别是飞灰·焚烧灰中重⾦属污染问题。
根据垃圾成分的不同,产⽣的飞灰的性状也会相应产⽣变化,重⾦属的存在也不同,因此不能采取相同划⼀的处理⽅法⽤于固化飞灰中的重⾦属。
对于重⾦属的固化、减容化以及在操作上的不同,本公司进⾏了充分的探讨与研究,引进⽇本三好⽯油有限公司的在飞灰螯合剂上的技术。
通过数年的研发形成了独特的、更⾼效、更环保的⾼性价⽐螯合剂。
“螯合chelate”⼀词来源于希腊语“蟹钳”⼀词,因S-C-S 的三⾓形部分具有良好的化学稳定性,能像蟹钳夹物⼀样将⾦属离⼦紧紧钳制⽽得名。
⽽本公司的系列螯合重⾦属⽣成的是环保型聚硫类聚合物,稳定性更佳(螯合机理如图所⽰)。
图螯合剂螯合机理如上图所⽰,本公司的螯合剂通过三个氮原⼦,三个硫原⼦,共3 个配位原⼦与重⾦属结合形成稳定的四原⼦环状螯合物,3 个配位原⼦与重⾦属离⼦螯合,效率⾼。
⽔溶性的螯合剂具有与重⾦属离⼦有选择性地进⾏反应,⾼效结合⽣成不溶于⽔的⾦属配们络合体。
这种性质被利⽤到飞灰中重⾦属离⼦的固定化(不溶化)的处理。
如下⾯的分⼦式所⽰,含有DTC 的⾦属固定化剂和⾦属离⼦(M2 +)反应,形成了不溶于⽔的⼤分⼦螯合体。
⼀般常规的螯合剂可以100%的使铅、镉、汞固定化,但其他的⾦属如六价铬、砷、氟、硒等不能进⾏固定化,锌⾦属化合物及其它⾦属碳酸盐类化合物也存在固化效果差的问题。
这就需要通过其它的专项添加剂对螯合剂进⾏辅助处理,以期降低某些重⾦属离⼦在酸性条件下的溶出能⼒。
表 1 螯合剂物理性质产品优点:◆产品本⾝环保,⽆毒,不易燃易爆螯合剂1618 本⾝属于环保产品:产品本⾝⽆毒、⽓味接近⽆味,螯合重⾦属时也接近⽆味。
不会分解和排放有毒物质,螯合时不会排放有毒刺激性⽓体,不易燃易爆,保障了现场操作⼈员的⼈⾝安全。
钙螯合值的测定

精心整理
精心整理
钙螯合值的测定
1、方法提要
在螯合剂的溶液中,加入过量的碳酸根离子,在溶液PH 值为11时,慢慢加入钙标准溶液至溶液出现清晰、永久的轻微浑浊。
2、试剂和溶液
钙-3a 、 b 、 氢氧
c 、 以mg/ml 表示的Ca 2+的浓度(C 1)按式(1)计算
C 1==(1)
式中V----滴定中消耗的乙二胺四乙酸二钠标准溶液的体积,ml
C----乙二胺四乙酸二钠标准溶液[C (EDTANa 2)=0.05mol/L ]的实际浓度。
0.04008----与1.00ml 乙二胺四乙酸二钠[C (EDTANa 2)=0.05mol/L ]相当的以克
精心整理
精心整理
表示的钙的质量。
4、仪器和设备
酸度计:配有饱和甘汞参比电极和玻璃电极或复合电极的酸度计。
电磁搅拌器
5、分析步骤
称取约2g 试样(精确至0.0002g ),于250ml 烧杯中,加入100ml 水,置于PH 至在。
不同pH值条件下螯合剂对铁、钙、镁等离子的螯合常数

不同pH值条件下螯合剂对铁、钙、镁等离子的螯合常数一,螯合分散剂用途纺织工业:1,退浆在退浆液中添加螯合剂,不管使用哪种退浆方法,可使退浆效率大大提高。
这是因为它把与浆料反应的金属离子络合以后,提高了浆膜的可溶胀性,也提高了浆料与退浆剂的可反应性,从而很容易从织物上去除。
2,前处理主要用作双氧水漂白的稳定剂,控制双氧水缓慢平稳的分解,提高双氧水利用率;同时防止金属离子导致的局部剧烈分解,引起织物纤维断裂形成破洞。
3,染色染色过程使用的水、芒硝、纯碱、氯化钠等都含有一定的杂质,在杂质的影响下,染料会引起沉淀。
特别是鲜艳的色系染色时,加入螯合剂可使色泽更加鲜艳,而对染料的磨擦牢度及匀染没有不良影响。
在染硫化染料时,更可防止起铜镜面的效果出现。
造纸工业:金属离子在纸浆漂白过程中引起的反应沉淀结垢,漂白剂无效分解,纸浆返黄等不良后果,纸浆漂白工艺中也需要使用螯合剂减少漂白的副作用,避免Fe3+离子与纸浆中的酚基团反应形成深颜色的复合物,保护纤维,提高纸浆白度,减少纸浆返黄。
循环水阻垢:在水处理中需要螯合剂用作循环冷却水和锅炉水的阻垢缓蚀剂,特别是针对含碳酸钡高的油田注水和冷却水、锅炉水的阻垢缓蚀剂。
清洗领域:无论是在工业清洗还是民用洗衣粉等日化产品,都需要螯合剂改善水质,提高净洗效果。
二,螯合剂的选用螯合剂种类繁多,如何选择适合的螯合剂则是我们最头疼和迷惑的地方,螯合力-稳定系数K是重要的参考指标,稳定系数K值越大,表明螯合剂对该离子的螯合能力越大。
下图为不同螯合剂对铁、钙、镁离子的螯合常数K值。
酸碱(pH值)对螯合剂螯合力影响在大多数使用螯合剂的工艺里面,工作液往往为酸性或碱性,因此pH值对螯合剂的影响对于螯合剂的选择与应用,尤为重要。
因此绘制出不同pH值条件下的螯合力曲线图,具有重要的实际意义,从而可以根据实际应用工艺条件,选择适合的螯合剂。
图表1铁离子螯合值(螯合值K)与pH曲线图表2钙离子螯合值(螯合值K)与pH曲线图表3镁离子螯合值(螯合值K)与pH曲线三,几种螯合剂的综合应用评价无机磷酸盐类:三聚磷酸钠以及焦磷酸钠是常用的螯合剂,自身带有弱碱性质,多用于洗衣粉添加剂。
各种水处理药剂单体螯合值
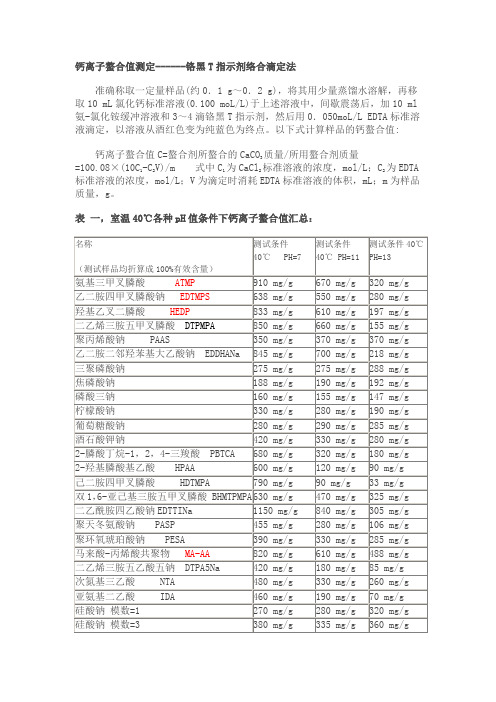
钙离子螯合值测定------铬黑T指示剂络合滴定法准确称取一定量样品(约0.1 g~0.2 g),将其用少量蒸馏水溶解,再移取10 mL氯化钙标准溶液(0.100 moL/L)于上述溶液中,间歇震荡后,加10 ml 氨-氯化铵缓冲溶液和3~4滴铬黑T指示剂,然后用0.050moL/L EDTA标准溶液滴定,以溶液从酒红色变为纯蓝色为终点。
以下式计算样品的钙螯合值:钙离子螯合值C=螯合剂所螯合的CaCO3质量/所用螯合剂质量=100.08×(10C1-C2V)/m 式中C1为CaCl2标准溶液的浓度,mol/L;C2为EDTA标准溶液的浓度,mol/L;V为滴定时消耗EDTA标准溶液的体积,mL;m为样品质量,g。
表一,室温40℃各种pH值条件下钙离子螯合值汇总:铁离子螯合值----磺基水杨酸显色测定待测样品溶液配制:准确称取待测样品5.000 g,加去离子水溶解,移至500mL 容量瓶中定容至刻度,摇匀备用待测。
Fe3+滴定法(磺基水杨酸显色)移取配制好的样品溶液2 mL于250 mL锥形瓶中,加30 mL水和5滴2%磺基水杨酸,用0.01 mol/L硫酸铁铵标准溶液滴定至溶液由无色变成微红色为终点.计算公式如下: X=Vcx159.6 x250/m式中,V为样品消耗硫酸铁铵溶液的体积(mL);c为硫酸铁铵溶液的浓度(mol/L);m为样品质量(g).表二,100℃各种pH值条件下铁离子螯合值汇总:增稠剂:(1)无机增稠剂(气相法白炭黑、钠基膨润土、有机膨润土、硅藻土、凹凸棒石土、分子筛、硅凝胶)。
(2)纤维素醚(甲基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠、羟乙基纤维素)。
(3)天然高分子及其衍生物(淀粉、明胶、海藻酸钠、干酪素、瓜尔胶、甲壳胺、阿拉伯树胶、黄原胶、大豆蛋白胶、天然橡胶、羊毛脂、琼脂)。
(4)合成高分子(聚丙烯酰胺、聚乙烯醇、聚乙烯吡咯烷酮、聚氧化乙烯、卡波树脂、聚丙烯酸、聚丙烯酸钠、聚丙烯酸酯共聚乳液、顺丁橡胶、丁苯橡胶、聚氨酯、改性聚脲、低分子聚乙烯蜡)。
钙镁离子螯合值 铁离子螯合值 金属离子捕捉剂
己二胺四甲叉膦酸HDTMPA
1280mg/g
460 mg/g
60mg/g
双1,6-亚己基三胺五甲叉膦酸BHMTPMPA
1530 mg/g
670mg/g
130mg/g
二乙酰胺四乙酸钠EDTTINa
1180 mg/g
775mg/g
140mg/g
聚天冬氨酸钠PASP
930 mg/g
280 mg/g
1150 mg/g
840 mg/g
305 mg/g
聚天冬氨酸钠PASP
455 mg/g
280 mg/g
106 mg/g
聚环氧琥珀酸钠PESA
马来酸-丙烯酸共聚物MA-AA
820 mg/g
610 mg/g
488 mg/g
二乙烯三胺五乙酸五钠DTPA5Na
680 mg/g
320 mg/g
180 mg/g
2-羟基膦酸基乙酸HPAA
600 mg/g
120 mg/g
90 mg/g
己二胺四甲叉膦酸HDTMPA
790 mg/g
90 mg/g
33 mg/g
双1,6-亚己基三胺五甲叉膦酸BHMTPMPA
630 mg/g
470 mg/g
325 mg/g
二乙酰胺四乙酸钠EDTTINa
197 mg/g
二乙烯三胺五甲叉膦酸DTPMPA
850 mg/g
660 mg/g
155 mg/g
聚丙烯酸钠PAAS
350 mg/g
370 mg/g
370 mg/g
乙二胺二邻羟苯基大乙酸钠EDDHANa
845 mg/g
700 mg/g
软水剂对金属离子的螯合能力的测定方法

软水剂对金属离子的螯合能力的测定方法软水剂对金属离子的螯合能力的测定方法1 方法来源染整专业书籍。
2适用范围适用于助剂中对金属离子有螯合要求的所有助剂。
3测试方法3.1 对钙离子螯合能力的测定方法3.1.1 试剂3.1.1.1 NH4Cl-NH3(pH=10)的缓冲溶液称取20g NH4Cl(分析纯),溶于适量的蒸馏水中,加入100mL 25%的氨水(分析纯),再用蒸馏水稀释至1L。
此缓冲溶液pH=10。
3.1.1.2 0.1mol/L乙酸钙标准溶液准确称取乙酸钙Ca(CH3COO)2·H2O)17.618g,用蒸馏水溶解后移入1L容量瓶中,稀至刻度。
3.1.2 测定用蒸馏水将待测助剂配成原液的1%(即将原液稀释100倍),取50.00mL于250ml 锥形瓶中,加入0.5mL的1%草酸钠(Na2C2O4)溶液和5mL pH=10的NH4Cl-NH3缓冲溶液,摇匀,用(3.1.1.2)0.1mol/L乙酸钙标准溶液滴定至溶液产生永久性的白色沉淀物为终点。
注:如终点难以出现,可考虑适当增加草酸钠的量,并在报告中说明。
3.1.3 计算钙螯合值(以CaCO3表示,mg/g),计算公式如下:钙螯合值= 0.1×V×100W (1)式中0.1————乙酸钙标准溶液的摩尔浓度;V————滴定样品时消耗乙酸钙标准溶液的体积,mL;100————CaCO3的相对克分子质量;W————滴定时所取样品的重量;g(此时为0.5g)。
3.2 对镁离子螯合能力的测定方法3.2.1 试剂3.2.1.1 0.5mol/L Mg2+标准溶液准确称取结晶氯化镁(MgCl2·6H2O)101.5g,用蒸馏水溶解,移入1L容量瓶中,稀至刻度。
3.2.1.2 NH4Cl-NH3(pH=11)的缓冲溶液用蒸馏水溶解6g分析纯NH4Cl和414mL分析纯NH4OH(比重=0.89)使成1L溶液,该缓冲溶液pH=11。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
各种条件下多种螯合剂对钙离子和铁离子螯合值数据
钙离子螯合值测定------铬黑T指示剂络合滴定法
准确称取一定量样品(约0.1 g~0.2 g),将其用少量蒸馏水溶解,再移取10 mL氯化钙标准溶液(0.100 moL/L)于上述溶液中,间歇震荡后,加10 ml氨-氯化铵缓冲溶液和3~4滴铬黑T指示剂,然后用0.050moL/L EDTA标准溶液滴定,以溶液从酒红色变为纯蓝色为终点。
以下式计算样品的钙螯合值:
钙离子螯合值C=螯合剂所螯合的CaCO3质量/所用螯合剂质量=100.08×(10C1-C2V)/m
式中C1为CaCl2标准溶液的浓度,mol/L;C2为EDTA标准溶液的浓度,mol/L;
V为滴定时消耗EDTA标准溶液的体积,mL;m为样品质量,g。
表一,室温40℃各种pH值条件下钙离子螯合值汇总:
名称
(测试样品均折算成100%有效含量)测试条
件40℃
PH=7
测试条
件40℃
PH=11
测试条
件40℃
PH=13
氨基三甲叉膦酸 ATMP 910 mg/g 670 mg/g 320 mg/g 乙二胺四甲叉膦酸钠 EDTMPS 638 mg/g 550 mg/g 280 mg/g 羟基乙叉二膦酸 HEDP 833 mg/g 610 mg/g 197 mg/g 二乙烯三胺五甲叉膦酸 DTPMPA 850 mg/g 660 mg/g 155 mg/g 聚丙烯酸钠PAAS 350 mg/g 370 mg/g 370 mg/g 乙二胺二邻羟苯基大乙酸钠
EDDHANa
845 mg/g 700 mg/g 218 mg/g
三聚磷酸钠275 mg/g 275 mg/g 288 mg/g 焦磷酸钠188 mg/g 190 mg/g 192 mg/g 磷酸三钠160 mg/g 155 mg/g 147 mg/g 柠檬酸钠330 mg/g 280 mg/g 190 mg/g 葡萄糖酸钠280 mg/g 290 mg/g 285 mg/g 酒石酸钾钠420 mg/g 330 mg/g 280 mg/g 2-膦酸丁烷-1,2,4-三羧酸 PBTCA 680 mg/g 320 mg/g 180 mg/g 2-羟基膦酸基乙酸 HPAA 600 mg/g 120 mg/g 90 mg/g 己二胺四甲叉膦酸 HDTMPA 790 mg/g 90 mg/g 33 mg/g
630 mg/g 470 mg/g 325 mg/g 双1,6-亚己基三胺五甲叉膦酸
BHMTPMPA
840 mg/g 305 mg/g 二乙酰胺四乙酸钠EDTTINa 1150
mg/g
聚天冬氨酸钠 PASP 455 mg/g 280 mg/g 106 mg/g 聚环氧琥珀酸钠 PESA 390 mg/g 330 mg/g 285 mg/g 马来酸-丙烯酸共聚物 MA-AA 820 mg/g 610 mg/g 488 mg/g 二乙烯三胺五乙酸五钠DTPA5Na 420 mg/g 180 mg/g 85 mg/g 次氮基三乙酸NTA 480 mg/g 330 mg/g 260 mg/g 亚氨基二乙酸IDA 460 mg/g 190 mg/g 70 mg/g 硅酸钠模数=1 270 mg/g 280 mg/g 320 mg/g 硅酸钠模数=3 380 mg/g 335 mg/g 360 mg/g
铁离子螯合值----磺基水杨酸显色测定
待测样品溶液配制:准确称取待测样品 5.000 g,加去离子水溶解,移至500mL容量瓶中定容至刻度,摇匀备用待测。
Fe3+滴定法(磺基水杨酸显色)
移取配制好的样品溶液2 mL于250 mL锥形瓶中,加30 mL水和5滴2%磺基水杨酸,用0.01 mol/L硫酸铁铵标准溶液滴定至溶液由无色变成微红色为终点.计算公式如下:
X=Vcx159.6 x250/m式中,V为样品消耗硫酸铁铵溶液的体积(mL);c 为硫酸铁铵溶液的浓度(mol/L);m为样品质量(g).
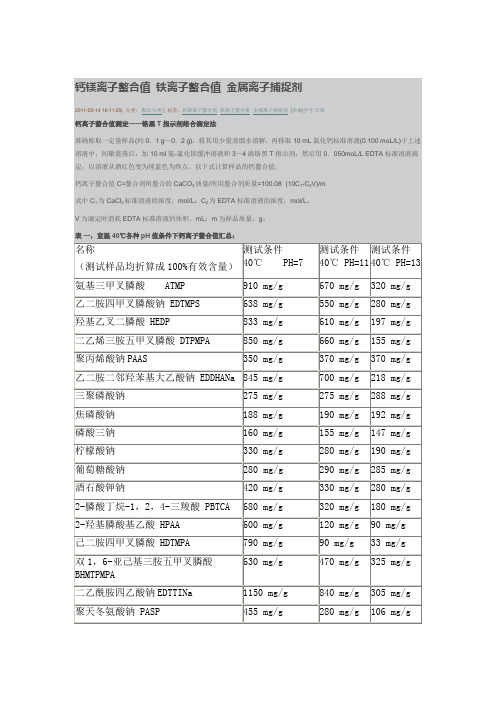
表二,100℃各种pH值条件下铁离子螯合值汇总:
名称
(测试样品均折算成100%有效含量)测试条件
100℃
PH=7
测试条件
100℃
PH=11
测试条
件100℃
PH=13
氨基三甲叉膦酸 ATMP 1200
mg/g
450mg/g 270 mg/g
乙二胺四甲叉膦酸钠 EDTMPS 1800mg/g 990 mg/g 177 mg/g 羟基乙叉二膦酸 HEDP 1800
mg/g
1300mg/g 280mg/g
二乙烯三胺五甲叉膦酸 DTPMPA 1700
mg/g
660 mg/g 155 mg/g 聚丙烯酸钠PAAS 445 mg/g 120 mg/g 65mg/g
乙二胺二邻羟苯基大乙酸钠EDDHANa 2200mg/g 1550
mg/g
230mg/g
三聚磷酸钠440 mg/g 360 mg/g 130mg/g 焦磷酸钠575mg/g 410 mg/g 165mg/g 磷酸三钠330 mg/g 280 mg/g 145mg/g 柠檬酸钠780mg/g 620mg/g 440mg/g 葡萄糖酸钠940mg/g 980 mg/g 820mg/g 酒石酸钾钠880 mg/g 555mg/g 380 mg/g 2-膦酸丁烷-1,2,4-三羧酸 PBTCA 1300mg/g 820 mg/g 330 mg/g 2-羟基膦酸基乙酸 HPAA 1420mg/g 650 mg/g 319mg/g 己二胺四甲叉膦酸 HDTMPA 1280mg/g 460 mg/g 60mg/g
双1,6-亚己基三胺五甲叉膦酸BHMTPMPA 1530
mg/g
670mg/g 130mg/g
二乙酰胺四乙酸钠EDTTINa 1180
mg/g
775mg/g 140mg/g 聚天冬氨酸钠 PASP 930 mg/g 280 mg/g 106 mg/g 聚环氧琥珀酸钠 PESA 880mg/g 650 mg/g 180 mg/g 马来酸-丙烯酸共聚物 MA-AA 1900mg/g 1100mg/g 660 mg/g 二乙烯三胺五乙酸五钠DTPA5Na 1400
mg/g
995mg/g 270mg/g 次氮基三乙酸NTA 680 mg/g 185 mg/g 70mg/g 亚氨基二乙酸IDA 550 mg/g 225mg/g 105mg/g
硅酸钠模数=1 480 mg/g 180 mg/g 55mg/g 硅酸钠模数=3 665mg/g 210 mg/g 125 mg/g。
