不同种类的元素周期表
元素周期表

元素周期表1、元素周期表:把电子层数相同的各种元素,按原子序数递增的顺序从左到右排成横行,再把不同横行中最外层电子数相同的元素,按电子层数递增的顺序由上至下排成纵行,这样得到的一个表叫做元素周期表。
2、周期:具有相同的电子层数的元素按原子序数递增的顺序排列而成的一个横行,叫做一个周期。
(1)元素周期表中共有7个周期,其分类如下:短周期(3个):包括第一、二、三周期,分别含有2、8、8种元素周期(7个)长周期(3个):包括第四、五、六周期,分别含有18、18、32种元素不完全周期:第七周期,共26种元素(1999年又发现了114、116、118号三种元素)(2)某主族元素的电子层数=该元素所在的周期数。
(3)第六周期中的57号元素镧(La)到71号元素镥(Lu)共15种元素,因其原子的电子层结构和性质十分相似,总称镧系元素。
(4)第七周期中的89号元素锕(Ac)到103号元素铹(Lr)共15种元素,因其原子的电子层结构和性质十分相似,总称锕系元素。
在锕系元素中,92号元素铀(U)以后的各种元素,大多是人工进行核反应制得的,这些元素又叫做超铀元素。
3、族:在周期表中,将最外层电子数相同的元素按原子序数递增的顺序排成的纵行叫做一个族。
(1)周期表中共有18个纵行、16个族。
分类如下:①既含有短周期元素同时又含有长周期元素的族,叫做主族。
用符号“A”表示。
主族有7个,分别为I A、ⅡA、ⅢA、ⅣA、VA、ⅥA、ⅦA族(分别位于周期表中从左往右的第1、2、13、14、15、16、17纵行)。
②只含有长周期元素的族,叫做副族。
用符号“B”表示。
副族有7个,分别为I B、ⅡB、ⅢB、ⅣB、VB、ⅥB、ⅦB族(分别位于周期表中从左往右的第11、12、3、4、5、6、7纵行)。
③在周期表中,第8、9、10纵行共12种元素,叫做Ⅷ族。
④稀有气体元素的化学性质很稳定,在通常情况下以单质的形式存在,化合价为0,称为0族(位于周期表中从左往右的第18纵行)。
元素周期表

折叠元素表顺口溜我是氢,我最轻,火箭靠我运卫星;我是氦,我无赖,得失电子我最菜;我是锂,密度低,遇水遇酸把泡起;我是铍,耍赖皮,虽是金属难电离;我是硼,电子穷,我和本族大不同;我是碳,反应慢,既能成链又成环;我是氮,我阻燃,加氢可以合成氨;我是氧,不用想,离开我就憋得慌;我是氟,最恶毒,抢个电子就满足;我是氖,也不赖,通电红光放出来;我是钠,脾气大,遇酸遇水就火大;我是镁,最爱美,摄影烟花放光辉;我是铝,常温里,浓硫酸里把澡洗;我是硅,色黑灰,信息元件把我堆;我是磷,害人精,剧毒列表有我名;我是硫,来历久,沉淀金属最拿手;我是氯,色黄绿,金属电子我抢去;我是氩,活性差,霓虹紫光我来发;我是钾,把火加,超氧化物来当家;我是钙,身体爱,骨头牙齿我都在;我是钪,耐温广,高温合金我来帮;我是钛,过渡来,航天飞机我来盖;我是钒,酸碱烦,如虎添翼钢加钒;我是铬,正六铬,酒精过来变绿色;我是锰,价态广,七氧化物爆炸猛;我是铁,多用也,不锈钢喊我叫爷;我是钴,蓝色母,癌症要用六十钴;我是镍,无锈铁,镍钛合金能记忆;我是铜,色紫红,投入硝酸气棕红;我是锌,人必需,体内我立大功勋;我是镓,易熔化,六十七镓是奇葩;我是锗,可晶格,红外窗口能当壳;我是砷,颜色深,三价元素夺你魂;我是硒,补人体,口服液里有玄机;我是溴,挥发臭,液态非金我来秀;我是氪,很耐克,通电就显橘红色;我是铷,碱金属,沾水烟花钾不如;我是锶,天青石,八十七锶帮医师;我是钇,难分离,我在特种合金里;我是锆,熔点高,石头里面很多锆;我是铌,能吸气,网络让我当NB;我是钼,像石墨,提高再结晶温度;我是锝,能放射,地壳里面我没得;我是钌,量很少,王水我也应得了;我是铑,光泽好,抗腐蚀性我很好;我是钯,把氢拉,吸氢我就破裂啦;我是银,不是人,只有硝酸氟化溶;我是镉,污染的,当年日本痛痛得;我是铟,软如金,轻微放射宜小心;我是锡,五金里,与铅熔合成焊锡;我是锑,非SB,虽说锑锅那是铝;我是碲,毒性低,又是金属又非金;我是碘,升华烟,遇到淀粉蓝点点;我是氙,很陌生,太阳灯啊我来填;我是铯,金黄色,入水爆炸容器破;我是钡,硫酸钡,可以用来检查胃;我们是镧系,个个都很稀;镧!铈!镨!工业维生素;钕能用来造磁铁;钷有放射性;钐!铕!钆!铽!合金很奇特;还有镝钬铒铥镱镥;我是铪,笑哈哈,我和锆矿是一家;我是钽,能抗酸,我遇强酸比金懒;我是钨,高温度,其他金属早呜呼;我是铼,催化爱,我把氢气吸过来;我是锇,和铱合,保持百年很耐磨;我是铱,做钢笔,只有千万分之一;我是铂,很贵重,含量比金还淡薄;我是金,很稳定,扔进王水影无形;我是汞,吸入痛,温度高低我能懂;我是铊,能脱发,投毒出名看清华;我是铅,能储电,子弹头里也出现;我是铋,半衰期,大于宇宙的年纪;我是钋,核能破,α粒子我有很多;我是砹,极少在,要找到我很难哎;我是氡,放射中,三天我就造真空;我是钫,人造上,廿三分钟我就亡;我是镭,千年累,我把癌细胞变没;我们是锕系,个个会放粒;锕!钍!镤!航飞做热源;铀造原子弹很牛;镎也造炸弹;钚!镅!锔!锫!做核反应堆;还有锎锿镄钔锘铹;我们超锕系,我们都超重;鑪,钅杜,钅喜,钅波,钅黑,钅麦,鐽,錀,鎶,Uut,鈇,Uup,鉝,Uus,Uuo。
化学元素 元素周期表

• • • • •
指出下列符号的意义 N 4Si F 4Zn
考点1
元素
1、概念:元素就是具有相同 相同核电荷数(即核 内 质子数 )的一类原子的总称。元素的种类 质子数 由 决定。 O,Si,Al,Fe 2、地壳中含量居前四位的元素是: ; 人体中含量最多的元素是 O ,含量最多的金属 元素是 Ca 。 金属 非金属 3、元素分类:可分为 元素, 元素和稀 有气体元素。
表示方法→ 元素符号
表示一个原子
元素周期表
原子序数=核电荷数 元素周期表的信息
化学变化中元素种类不变
元素分类与最外层电子数之间的关系
元素分类
金属元素
非金属元素
稀有气体元素
原子最外 一般小于 层电子数 4个电子
一般大于等于 4个电子
8个电子 (He为2)
• • • • • •
用元素符号表示: 氧元素 一个氧原子 三个氧原子 氢元素 一个氢原子 5个氢原子 碳元素 氯元素 镁元素 铁元素 铜原子 4个硫原子 氩气 一个氦原子 5个钾原子 钙元素 磷元素的3个原子
4.某原子的结构示意图如下, 有关它的说法正 确的是 A最外层电子数是8 B.质子数为12 C.该元素的原子化学性质稳定 D.该元素属于非金属元素
5. 下表是元素周期表的一部分,请你根据下表回答问题: 3 Li 锂 6.941 11 Na 钠 22.99 4 Be 5B 6C 7N 8O 9 F 10 Ne 铍 硼 碳 氮 氧 氟 氖 9.012 10.81 12.01 14.01 16.00 19.00 20.18 12 Mg 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar 镁 铝 硅 磷 硫 氯 氩 24.31 26.98 28.09 30.97 32.06 35.45 29.95
元素周期表及应用

根据元素周期表预言新元素的存在
• 类铝(镓)的发现:
❖ 1875年,法国化学家布瓦博德朗在分析比里牛 斯山的闪锌矿时发现一种新元素,命名为镓, 测得镓的比重为4.7,不久收到门捷列夫的来 信指出镓的比重不应是4 .7,而是5.9~6.0, 布瓦博德朗是唯一手里掌握金属镓的人,门捷 列夫是怎样知道镓的比重的呢?经重新测定镓 的比重确实是5.94,这结果使他大为惊奇,认 真阅读门捷列夫的周期论文后,感慨地说“我 没有什么可说的了,事实证明了门捷列夫理论 的巨大意义”。
C.Cs+具有很强的氧化性
D.CsHCO3受热不易分解
1869年 门捷列 夫发表 的第一 张元素 周期表
★粒子半径大小比较的规律
1 同一主族元素的原子和离子, 电子层数越多的,其半径越 大. r(Na)<r(K) r(F)<r(Cl)
r(Na+)<r(K+) r(F-)<r(Cl-)
2同周期元素的原子,核电荷数越大的,
K Br 得电子能力减弱,非金属性减弱。
Si I
Cs
一般地,元素单质密度逐渐增大;
金属熔沸点逐渐减小,非金属熔沸
点逐渐增大
(二)元素在周期表中的位置与性质的关系
11Na 12Mg 13Al 14Si 15P 16S 17Cl
Li F 从左往右,核电荷增大,半径减小
Na Cl 失电子能力减弱,金属性减弱; K Br 得电子能力增强,非金属性增强。
1、 学习和研究化学的规律和工具
2、研究发现新物质
预言新元素,研究新农药,寻找半导 体材料、催化剂、耐高温耐腐蚀材料。
元素周期表(带详细解析)

第一章物质结构元素周期律第一节元素周期表重难点一元素周期表1.构成原子(离子)的微粒间关系(1)原子序数=核电荷数=核内质子数=核外电子数(原子中)。
(2)离子电荷数=质子数-核外电子数。
(3)质量数(A)=质子数(Z)+中子数(N)。
(4)质子数(Z)=阳离子的核外电子数+阳离子的电荷数。
(5)质子数(Z)=阴离子的核外电子数-阴离子的电荷数。
2.元素周期表的结构(3)过渡元素元素周期表中从ⅢB到ⅡB共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
特别提醒族序数为Ⅱ、Ⅲ的地方是主族和副族的分界线,第一次分界时主族在副族的前面,第二次分界时副族在主族的前面。
“第一次”指ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ依次排列。
“第二次”指ⅠB ⅡB ⅢA ⅣA ⅤA ⅥA ⅦA 0依次排列。
重难点二 零族定位法确定元素的位置 1.2.比大小定周期比较该元素的原子序数与0族元素的原子序数大小,找出与其相邻近的两种0族元素,那么该元素就和序数大的0族元素处于同一周期。
3.求差值定族数(1)若某元素原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA 族或ⅡA 族。
(2)若比相应的0族元素少1~5时,则应处在同周期的ⅢA ~ⅦA 族。
(3)若差其他数,则由相应差值找出相应的族。
重难点三 元素的性质与原子结构 1.碱金属单质的相似性和递变性 (1)相似性①与O 2反应生成相应的氧化物,如Li 2O 、Na 2O 等。
②与Cl 2反应生成RCl ,如NaCl 、KCl 等。
③与H 2O 反应,能置换出H 2O 中的氢,反应通式为2R +2H 2O===2ROH +H 2↑。
④与非氧化性酸反应,生成H 2,反应通式为2R +2H +===2R ++H 2↑。
(R 表示碱金属元素)(2)递变性从Li 到Cs ,随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱,失电子能力逐渐增强,金属性逐渐增强。
元素周期表

即:氯的相对原子量为35.453。
原子结构
已知:H有三种同位素H、D、T,则氢分子有几种? 其相对分子质量有几种?
课堂活动:
元素的种类比核素的()
课堂活动:
实际存在的 1H、2H、3H、H+、H ,他们是 2
A、H的5种同位素 B、五种氢元素 C、H的5种核素 D、氢元素的五种不同微粒
课堂活动:
F2 Cl2 Br2 I2,都有较强氧化性。 且氧化性依次增强,元素非金属 性依次增强。
小结: 同主族元素都具有相似性和递变性, 同一主族,从上至下, 元素的金属性在增强, 非金属性在减弱。
原子结构 原子核
质子
中子
核外电子
核电荷数=质子数
原子结构
已知:对于一个原子而言
原子序数=质子数=电子数 又∵核电荷数=质子数
∴原子序数=核电荷数=质子数=电子数
原子结构
构成原子的 粒子
质量/kg 相对质量
电子
质子 9.109×10-31 质子质量的 1/1836
原子核
中子
1.673×10-27 1.675×10-27 1.007 1.008
课堂活动:
A、B、C是周期表中相邻的三种元素,其中A、B是 同周期,B、C是同主族。此三种元素原子最外层电 子数之和为17,质子数之和为31,则A、B、C分别 为什么元素? A是氮元素 B是氧元素
C是硫元素
课堂活动:
元素X的原子获得3个电子或元素Y的原子失去2个电子后, 它们的电子层结构与氖原子的电子层结构相同。 元素X、Y在周期表中的位置是___ 。
如果用各核素的质量数A1、A2……代替 其相对原子质量,计算得到的是元素的 近似相对原子质量
原子结构
第三节 元素周期表
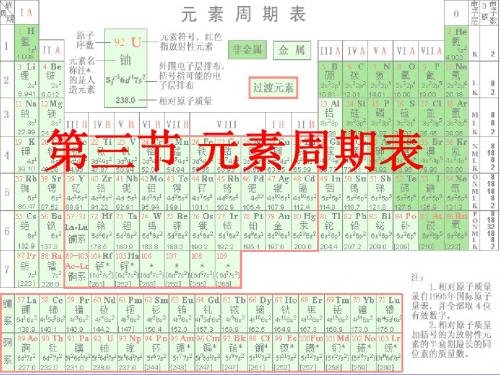
(1)主族:由短周期元素和长周期元素共 同构成的族。 表示方法:在族序数后面标一“A” 字。ⅠA、ⅡA、ⅢA、…ⅦA (2)副族:完全由长周期元素构成的族。 表示方法:在族序数后标“B”字。 如ⅠB、ⅡB、ⅢB、…ⅦB (3)第VⅢ族: (“8、9、10” 三个纵行) (4) 0族:稀有气体元素
米奇利还分析了其它的一些规律, 最终,一种全新的致冷剂CCl2F2终 于应运而生了。 80年代,科学家们发现氟里昂会破 坏大气的臭氧层,危害人类的健康 的气候,逐步将被淘汰。人们又将 在元素周期表的指导下去寻找新一 代的致冷剂。
氟里昂的发现与元素周期表
在第三周期中,单质的易燃性是 Na>Mg>Al,在第二周期中,CH4比 NH3易燃,NH3双比H2O易燃,再比较 氢化物的毒性:AsH3>PH3>NH3 H2S>H2O,根据这样的变化趋势,元 素周期表中右上角的氟元素的化合物 可能是理想的元素,不易燃的致冷剂。
氟里昂的发现与元素周期表
> HCl > HBr > HI NH3 < HF NH3 > PH3
HF 2.碱性强弱: KOH
>
NaOH HNO3
3.酸性强弱: HClO4
> > >
Mg(OH)2 HBrO4 H3PO4
三、元素化合价与元素在周期表中 位置的关系
价电子——元素原子的最外层电子或
某些元素的原子的次外层或倒数第三层的 部分电子。 (1)最高正价= 主族序数 = 最外层电子数
2
10
K
2
4
12 20 38 III B 21 39 IV B 22 40 V B 23 41 VI B 24
化学元素周期表,元素周期律 精读笔记!!

一.元素周期表1。
原子序数=核电荷数=核内质子数=核外电子数2.主族元素最外层电子数=主族序数3。
电子层数=周期序数4。
碱金属元素:密度逐渐增大,熔沸点逐渐变大,自上而下反应越来越剧烈银白色金属,密度小,熔沸点低,导电导热性强5.判断元素金属性强弱的方法:单质与水(酸)反应置换出氢的难易程度最高价氧化物的水化物(氢氧化物)的碱性强弱单质间的置换6。
卤族元素:密度逐渐增大,熔沸点逐渐升高与氢气反应剧烈程度越来越弱,生成氢化物稳定性渐弱7.判断元素非金属性强弱的方法:与氢气生成气态氢化物的难易程度以及氢化物的稳定性最高价氧化物的水化物的酸性单质间的置换8。
质量数:核内所有质子和中子的相对质量取近似整数相加9。
核素:具有一定数目质子和一定数目的中子的一种原子10。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素天然稳定存在的同位素,无论是游离态还是化合态各同位素所占的原子个数百分比一般是不变的在相同状况下,各同位素的化学性质基本相同(几乎完全一样),物理性质有所不同12。
原子相对原子质量=1个原子的质量/(1/12 C12的原子质量)13。
原子的近似相对原子质量=质量数14。
元素的相对原子质量=各同位素的相对原子质量的平均值=A·a%+B·b%…15.元素的近似相对原子质量=各同位素质量数的平均值=A·a%+B·b%…二.元素周期律1.K、L、M、N、O、P、Q(1,2,3,4,5,6,7,)层数越大,电子离核越远,其能量越高2.能量最低原理3.各电子层最多容纳电子数:2n^24.最外层不超过8,次外层18,倒数第三层325.原子半径:同周期主族元素,原子半径从左到右逐渐减小同主族元素,元素原子半径从上到下逐渐增大6.元素性质的周期性变化是元素原子的核外电子排布的周期性变化的结果(实质)7.同一周期元素,电子层数相同,从左到右,核电荷数增多,原子半径减小,失电子的能力逐渐减弱,得电子的能力逐渐增强8.同一主族,自上而下,元素的金属性逐渐增强,非金属性逐渐减弱,最外层电子数相同,电子层数增多,原子半径增大9.最高正价=最外层电子数最低负价=8—最外层电子数10.各周期元素种类:2,8,8,18,32,3211.稀有气体原子序数;2,10,18,36,54,8612.同族上下相邻的原子序数差:2,8,18,3213.同周期IIA族与IIIA族原子序数相差:1,1,11,11,2514.电子层数不同,原子序数(核电荷数)均不同时,电子层数越多,半径越大15.电子层数相同,原子序数(核电荷数)不同时,原子序数(核电荷数)越大,半径越小16.电子层数,原子序数(核电荷数)均相同时,核外电子数越多,半径越大17.电子排布相同的离子,离子半径随核电荷数递增而减小选修三.原子结构与性质1.原子轨道(能级即亚层):处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动,分别用s、p、d、f表示不同形状的轨道,s轨道呈球形、p轨道呈纺锤形,d 轨道和f轨道较复杂.各轨道的伸展方向个数依次为1、3、5、7。
元素周期表

补充:粒子半径的大小比较规律
1、不同元素的粒子半径比较: (1)同一周期元素的原子,从左到右,原子半径依次 减小(稀有气体除外)。 (2)同一主族元素的原子,从上到下,原子半径依次增大, 离子半径也依次增大。 (3)电子层相同的不同粒子,核电荷数越大(或正电荷越 多),粒子半径越小。 2、同种元素的离子半径比较: (1)同一元素的阳离子半径小于对应的原子半径;同一 元素的阴离子半径大于对应原子半径。 (2)变价金属的低价态阳离子半径大于对应的高价态阳离 子半径。
元素周期表的框架结构:
族 周 期
1 2 3 4 5 6 7
…
小结:
一、元素周期表的几个数量关系:
1、周期序数===电子层数 2、主族序数===最外层电子数
3、元素最高正价===原子最外层电子数 6、主族或副族的族序数==元素 所在纵行的个位数 5、主族中非金属元素的种类===∣主族序数-2∣
4、元素负价===最外层电子数﹣8
3、元素周期表和元素周期律的关系:
元素周期律是编排元素周期表的理论基础,元素周 期表是元素周期律的具体表现形式。
பைடு நூலகம்
二、元素周期表的结构:
1、周期:一个横行称做一个周期。 周期序数==电子层数 三短周期(1、2、3) 7个横行(7个周期) 三长周期(4、5、6) 一不完全周期(7周期)
表5-11 元素周期表的有关知识
C
D
2、相似规律: (1)同主族元素性质相似; (2)位于斜对角规则的元素性质相似。
补:元素金属性、非金属性强弱的判断:
1、主族金属元素与非金属元素的判断:主族序数/周期序数﹥1,则为非 金属元素;若主族序数/周期序数≤1,则为金属元素(H除外)。 2、元素金属性、非金属性的强弱判断: (1)根据在周期表中的位置判断: ①同一主族,从上到下,金属性逐渐增强,非金属性逐渐减弱;
第一节元素周期表(共40张PPT)
第ⅦA 族
与水缓慢反应
(2)原子结构特点 Cl2+H2O=HCl+HClO
静置后,液体分为两层。
通一过个以 12上C相质比量较同×,1点/思12考:钠和钾最的外性质层有 7个电子
静置后,液体分为两层。
和递变性。 (氧化性:Cl2 >I2)
核电荷数依次增多
不同点: 电子层数依次增多 上层无色,下层分别呈橙红色、紫红色
第一章 物质结构、元素周期律
第一节 元素周期表 一、元素周期表的结构
原子序数:依原子核电荷数由小到大的顺序给元素编号,这种
编号叫原子序数。
原子序数=核电荷数=质子数=核外电子数 (一)元素周期表的编排原则
1、横行: 把电子层数相同的各种元素按原子序数递增顺序
从左到右排列。
2、纵行: 把最外层电子数相同的各种元素按电子层数递增顺序 从上而下排成。
性逐渐增强,非金属性逐渐减弱。
2. 元素性质与原子结构有有密切的关系,主要与原子
核外的排布,特别是最外层电子数有关。原子结构
相似的一族元素,它们在化学性质上表现出相似性 和递变性。
1、砹(At)原子序数85,与F、Cl、Br、I同族,推测砹或
砹的化合物不可能具有的性质是( B)
A、砹易溶于某些有机溶剂 B、砹能与水剧烈反应
应越来越
,剧生烈成的氧化物越来越
。
最高复价杂氧化物对应水化物的碱性越来越 。
强
讨论1:Li与K 应如何保存? Li封存于固体石蜡中, 少量K保存于煤油中。
讨论2:碱金属与盐酸: 2R+2H+= 2R++H2 ↑ 讨论3:碱金属与盐溶液: 先与水反应
讨论4:Li+、Na+、K+、Rb+、Cs+也具有强还原性吗? 没有。 有较弱的氧化性。 氧化性: Li+ > Na+ > K+ > Rb+ > Cs+
元素及元素周期表

针对训练3 右图是铝的结构示意图和在周期表 中的位置图,下列说法错误的是(C ) A.铝原子的核电荷数是13 B.铝元素的相对原子质量是26.98 C.铝离子核外有3个电子层 D.铝原子最外层有3个电子
【火眼金睛】 易错点1 对元素概念的理解不清晰 例 下列有关元素的说法正确的是( D ) A.质子数相同的粒子属于同一种元素 B.相同元素组成的化合物一定是同种物质 C.一种元素只能组成一种单质 D.水是由氢、氧两种元素组成的
(3)元素周期表中氟元素的有关信息如下图所示, 下列说法正确的是 B (填字母)。 氟属于金属元素 氟的原子序数是9 氟的相对原子质量是19.00g (4)氟原子结构示意图为 ,氟原子在化学 反应中易 得到 (填“得到”或“失去”)电子, 由钠元素和氟元素组成的化合物氟化钠的化学式 为 NaF 。
例3 (2016·枣庄)如图是元素周期表的一部分,请 回答
:
(1)①处元素和②处元素形成常见化合物的化学 式为 ,该化合物中②处元素的化合价为 ( 2) 表示如表中 (填表中序号) 的原子结构示意图,该原子易 (填“得”或 “失”)电子,形成的离子符号为 .
【解析】(1)①是氧元素,在化合物中常 显﹣2价,②是铝元素,常显+3价;二者组成 的化合物氧化铝的化学式为Al2O3;故填: Al2O3;+3; (2)由原子结构示意图可知,这是17号元 素氯原子的结构示意图,元素位于元素周期 表的④位置;其最外层有7个电子,在化学反 应中易得到1个电子,而形成带一个单位负电 荷的氯离子;故填:④;得;Cl﹣.
(6)主族元素原子的最外层电子数等于主族序数;
(7)主族元素原子的最外层电子数等于其最高正化合价。
3.元素周期表中的信息 原子序数 (核电荷数) 1H 元素符号 元素名称
元素周期表

9.2 元素周期表知识要点一、元素周期表编排原则1、把电子层数相同的元素,按原子序数递增顺序从左到右排成一个横行,称为一个周期;2、把最外层电子数目相同的元素按电子层数递增的顺序由上到下排列成一个纵行,称为一个族。
注意:元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
二、元素周期表的结构非金属区(22种,包含6种稀有气体元素)区金属区(包含所有主族金属及过渡金属元素)周期数=电子层数(除钯)七个周期:3个短周期、4个长周期构成周期掌握前三周期元素符号、元素名称和原子序数掌握各周期起止元素原子序数与名称了解镧系元素、锕系元素主族序数=原子最外层电子数族十六个族:7个主族、7个副族、1个零族、1个Ⅷ族掌握周期表中从左到右的族排列序数掌握各主族元素的价电子数(最外层电子数)1、周期将具有相同电子层数而又按照原子序数递增的顺序排列的一系列元素称为一个周期。
这样,周期数即是该周期元素原子的电子层数,元素周期表中有七个横行,即七个周期。
短周期:一、二、三周期,元素种类2、8、8。
长周期:四、五、六、七周期,元素种类18、18、32、32。
2、族把最外层电子数相同的元素按电子层数递增的顺序从上到下排成的纵行称为一个族。
周期表中有十八个纵行,但第8、9、10三个纵行为一族,所以共十六个族。
主族:由长周期和短周期元素共同构成的族,共七个纵行。
副族:仅由长周期元素构成的族,共七个纵行。
Ⅷ族:包括第8、9、10三个纵行的元素。
零族:稀有气体元素,一个纵行。
三、元素的性质递变规律1、元素性质2、递变规律3、对角线规则:Li与Mg,Be与Al,B与Si这三对元素在周期表中处于对角线位置:Li Be B CNa Mg Al Si相应的两元素及其化合物的性质有许多相似之处。
这种相似性称为对角线规则。
如:★锂和镁在过量的氧气中燃烧均生成正常氧化物,而不是过氧化物。
★ 锂、镁都能与氮气直接化合而生成氮化物。
元素周期表

反 应 越 来 越 难 以 发 生
【实验】
1
氯水
CCl4
振荡
NaBr溶液 氯水
试管中溶液由无色变为橙 黄色,加CCl4后,分层,上层无 色,下层橙红色.
2
KI溶液
CCl4
振荡
试管中溶液由无色变为棕 黄色,加CCl4后,分层,上层无 色,下层紫红色.
溴水
3
KI溶液
CCl4
振荡
试管中溶液由无色变为棕 黄色,加CCl4后,分层,上层无色, 下层紫红色.
例3. A、B、C均为短周期元素,它们在周期表中 的位置如右图。B、C元素的原子序数之和是A元 素原子序数的4倍,则A、B、C所在的一组元素 是( D ) A.Be、Na、Al B.B、Mg、Si C.C、Al、P D.O、P、Cl
元素周期表
第二课时
元素性质与原子结构
二、
碱金属元素
碱金属元素包括哪些元素?
右图有三种原子,核内 都只有一个质子、中子数 为0、1、2,核外有一个电 子,质量数为1、2、3,可 表示为:11H 、12H、13H 。 属质子数相同的同一类原 子(总称为氢元素),但 中子数不同。
核素 : 具有一定数目的质子和一定数目的中子的一 种原子。如 1H(H、氕 ) 、 2H(D 、氘 ) 、 3H(T 、氚 ) 就各 为一种核素。 同位素:具有相同核电荷数(即质子数)不同中子数 同一元素的(核素)原子。
探究实验2:钾和钠与水反应
②与水的反应 2Na + 2H2O = 2NaOH + H2↑ 2K + 2H2O = 2KOH + H2↑
通式:2R +2H2O = 2ROH + H2↑
结论: Li Cs,与水反应趋于容易与剧烈; 都生成碱和氢气;
元素周期表
越来越困难
稳定性↓ 还原性↓
三、位、构、性的关系
质子数Z 电子层数 最外层电子数
电子层数
=周期序数
决
定
最外层电子数
=主族序数
原子结构
元素性质由最
外层电子数和
决 电子层数共同
反
反
定
决定。主要由 原子最外层电
映
映 子数决定。
周期表中位置
相似性,递变性
元素性质
推断
7个周期 16个族
同一周期 同一主族
1 H →He 2
1
2 Li→Ne 8
2
3 Na→Ar 8
3
4 K →Kr 18
4
5 Rb→Xe 18
5
6 Cs→Rn 32
6
7 Fr→… 26
7
(2)族:
①概念:元素周期表共有18列。周期表中的第8、
9、10三个纵列是一个族,叫做第Ⅷ族,其余15
个纵列,每个纵列成为一族。共16个族。 ②族的分类及表示:七主七副一零族一Ⅷ族
M L k
8 8 2
4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
5 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54
57
6 55 56 - 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
4、下表是元素周期表的一部分,针对所给的10种元素, 完成下列各小题。
主族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 周期
2
①② ③
化学元素周期表(学生版)

化学元素周期表和周期律一.完成下列元素周期表1.并标明元素性质变化趋势、非金属性最强和金属性最强元素。
12.、完成氢化物周期表并标明氢化物稳定性趋势、氢化物最稳定的物质23.、完成最高价氧化物对于水化物周期表并标明最高价氧化物对于水化物性质变化趋势、最强酸和最强碱3第一周期:氢氦---- 侵害第二周期:锂铍硼碳氮氧氟氖---- 鲤皮捧碳蛋养福奶第三周期:钠镁铝硅磷硫氯氩---- 那美女桂林留绿牙(那美女鬼流露绿牙)第四周期:钾钙钪钛钒铬锰---- 嫁改康太反革命铁钴镍铜锌镓锗---- 铁姑捏痛新嫁者砷硒溴氪---- 生气休克二.熟悉元素周期表的结构,熟记前36号元素及主族和零族元素的名称及符号。
1.记住7个横行,即个周期(短、长)。
2.记住18个纵行,包括个主族(ⅠA~ⅦA)、个副族(ⅠB~ⅦB)、1个第族(第8、9、10纵行)和1个族(即稀有气体元素)。
3.记住金属与非金属元素的分界线(氢、硼、硅、砷、碲、砹与锂、铝、锗、锑、钋之间)。
三、特殊元素集锦1、最活泼的金属元素、最高价氧化物对应的水化物碱性最强的元素、阳离子氧化性最弱的元素是铯()。
2、最活泼的非金属元素、无正价的非金属元素、无含氧酸的非金属元素、无氧酸(或氢化物)可腐蚀玻璃的元素、气态氢化物最稳定的元素、阴离子的还原性最弱的元素是氟()。
3、最强的碱是()最强的含氧酸是()最高价氧化物的水化物能与其气态氢化物发生化合反应的短周期元素是()最高价氧化物的水化物能与其气态氢化物发生氧化还原反应的短周期元素是(())气态氢化物和它的氧化物在常温下生成该元素的单质的元素是()3、最稳定的气态氢化物是()气态氢化物中含氢质量分数最大的是()最小的是()4、形成化合物种类最多的元素是()、单质是自然界中硬度最大的物质的元素、气态氢化物中氢的质量分数最大的元素是碳()。
空气中含量最多的元素是()或气态氢化物的水溶液呈碱性的元素是氮()。
地壳中含量最多的元素是()地壳中含量最多的金属元素是()5、焰色反应呈黄色的元素是()透过蓝色钴玻璃观察焰色反应呈紫色的元素是()46、常温下单质呈液态的元素是()常温下单质呈液态的非金属元素是()7、无氧酸能腐蚀玻璃的元素是()最易着火的非金属单质的元素是()8、既能与酸反应又能与碱溶液反应可产生H2的金属元素为铝(),与碱溶液反应可产生H2的非金属元素为(),Al2O3和Al(OH)3都有两性。
物质结构 元素周期表

第一章 物质结构 元素周期表专题一:元素周期表一、元素周期表1、元素周期表的排列原则:横行:电子层数相同,从左到右原子序数依次递增纵行:最外层电子数相同,自上而下电子层数依次递增2、周期结构:三短(1、2、3周期)、三长(4、5、6周期)、一不全(7周期)3、族的构建巧记:18纵行16族;八九十列成VIII 族;每逢二三分主副,镧系锕系各十五,都在III 副里边住。
第I A 族(除氢):碱金属元素 第VII 族:卤族元素 0族:稀有气体元素4、关系式(1)原子序数=核电荷数=质子数=核外电子数(2)质量数=中子数=质子数二、碱金属1、碱金属元素的原子结构规律周期类别 周期序数 元素种类 短周期 1 2 2 8 3 8 长周期 4 18 5 18 6 32 不完全周期 7 32 列数 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 类别 主族 副族 VIII 族 副族 主族名称 IA II A IIIB IV B V B VI B VII B VIII 族 I B II B III A IV A V A VI A VII A 0族碱金属元素元素名称 元素符号 核电荷数 原子结构示意图 最外层电子数 电子层数 锂 Li 3 钠 Na 11 钾 K 19 铷 Rb 37 铯 Cs 55按Li、Na、K、Rb、Cs顺序,密度依次升高;熔点、沸点依次降低。
2、K、Na性质实验对比与O2反应与水反应钠剧烈燃烧,色火焰熔成小球,浮于水面,四处游走,发出嘶嘶的声音钾更剧烈,色火焰熔成小球,浮于水面,四处游走,轻微爆炸声结论K比Na的活动性强3、碱金属元素原子结构与性质的关系(1)原子结构特点相同点:最外层都只有一个电子不同点:随核电荷数增加,原子半径增大(2)化学性质特点A、相似性:原子都易失去最外层的一个电子,与非金属单质及水反应。
Li、Na、K在O2中燃烧反应,Na、K与H2O反应,B、差异性:随着核电荷数的增加,原子核对最外层电子的引力逐渐减弱。
完整版元素周期表详解

元素周期表中元素及其化合物的递变性规律1原子半径(1)除第1 周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而减小;(2 )同一族的元素从上到下,随电子层数增多,原子半径增大。
注意:原子半径在VIB 族及此后各副族元素中出现反常现象。
从钛至锆,其原子半径合乎规律地增加,这主要是增加电子层数造成的。
然而从锆至铪,尽管也增加了一个电子层,但半径反而减小了,这是与它们对应的前一族元素是钇至镧,原子半径也合乎规律地增加(电子层数增加)。
然而从镧至铪中间却经历了镧系的十四个元素,由于电子层数没有改变,随着有效核电荷数略有增加,原子半径依次收缩,这种现象称为“镧系收缩”。
镧系收缩的结果抵消了从锆至铪由于电子层数增加到来的原子半径应当增加的影响,出现了铪的原子半径反而比锆小的“反常”现象。
2元素变化规律(1 )除第一周期外,其余每个周期都是以金属元素开始逐渐过渡到非金属元素,最后一稀有气体元素结束。
(2 )每一族的元素的化学性质相似3元素化合价(1)除第1 周期外,同周期从左到右,元素最高正价由碱金属+1 递增到+7 ,非金属元素负价由碳族-4 递增到-1 (氟无正价,氧无+6 价,除外);(2 )同一主族的元素的最高正价、负价均相同(3)所有单质都显零价4单质的熔点(1 )同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔点递减;(2 )同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增5元素的金属性与非金属性(1 )同一周期的元素电子层数相同。
因此随着核电荷数的增加,原子越容易得电子,从左到右金属性递减,非金属性递增;(2 )同一主族元素最外层电子数相同,因此随着电子层数的增加,原子越容易失电子,从上到下金属性递增,非金属性递减。
6最高价氧化物和水化物的酸碱性元素的金属性越强,其最高价氧化物的水化物的碱性越强;最高价氧化物的元素的非金属性越强,水化物的酸性越强。
元素周期表(带拼音)

元素周期表(带拼音)元素周期表是以原子或离子的符号作为标准号,以元素符号来表示元素种类或含量的化学符号,以及元素符号所代表的意义,可以反映元素特性的化学符号。
元素符号,是由原子排列顺序表示。
在原子排列中,每个原子或离子排列构成一个元素序列。
所有在排列中的原子按其分子个数表示为每个原子中分子所占组成单位,元素符号的大小就表示了所代表元素序号和该序号在化学上的意义,以及该序列对应分子之间的区别,也代表了元素之间互相影响而又相互独立的一个系统在一定程度上说明这个系统是否稳定和连续。
在化学性质上,元素都是平衡态,这也是我们要强调必须保持同一性的原因之一:原子形成过程不可能同时完全相同,但是它们之间不可能完全相同。
因此原子或离子之间并没有绝对紧密相联,即原子或离子能够存在于同一个空间中。
一、为什么要以原子命名?从化学角度看,元素在地球上存在的时间比地球上现有的原子的生命还早。
而目前最有可能用得上原子理论的就是原子族的相关元素(如铀、镭、铌、钽、锂、钡、钴、锆、硅、铂、镭)和元素族的所有原子核组成的有机金属元素。
我们知道,化学元素周期表中所列元素周期表所用原子或离子序号用一种特定形式表示。
如元素周期表中第一个原子按其序号可称为第 I元素第IV元素。
这些元素的序号一般就可以代表它们在化学上的含义。
因此,以原子命名可以避免用原子概念对原子现象作出概括描述,从而使化学元素周期表不会过于死板(例如只用原子名称)。
1、取其首字为元素名的依据在化学方面,有一种公认的元素命名原则,那就是尽量不用首字)来命名。
如在元素周期表中:第 I、 II、 III、 IV这四个数字为首字,其他每一个数字都要对应第一个字母:如第 I 对应1 (这四个数字是按首字第一英文字母排序而来)、第 II、 IV对应1 (这四个数字是按首字第二英文字母排序而来)。
但如果把这四个数字拆开来看则不存在这种说法或现象,如取1 (这个数字是按照首字“一”这一英文字母排序而来)来命名这四个数字则是不合理行为。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
不同种类的元素周期表
2015级六班甘浩弘1.扇形元素周期表
2.四棱锥形元素周期表
3.工程图式环形元素周期表
4.圆形元素周期表
5.圆环形元素周期表6
6.树式元素周期表
7.螺旋式立体元素周期表
8.塔式元素周期表
9.螺旋时钟式元素周期表
11.零件式元素周期表
12.太极八卦式元素周期表
规律:1.原子序数依次递增
2.不同种类的元素周期表都显示出元素性质与其位置之间的联系。
3.元素的最外层电子数显示出周期性的变化特征
4.在同一方向上的元素其性质往往有一定的相似性
5.元素相对原子质量随原子序数增加。
