乙烯-优质课件
化学课件《乙烯》优秀ppt 通用

加成反应
加聚反应
作业设计:
1.工业上的乙烯主要来源于
,它是
一种
色、
味的气体,
法收集。
溶于水。实验室制取乙烯时用
2.可以用来鉴别甲烷和乙烯,还可以用来除 去甲烷中乙烯的操作方法是( )。
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气 瓶
点燃
C2H4+3O2 → 2CO2+2H2O
b.乙烯使酸性高锰酸钾(aq)褪色的 反应说明乙烯能被氧化剂氧化
利用这个反应可以鉴别甲烷和乙烯
乙烯与高锰酸钾的反应
2.乙烯的加成反应:
乙烯使溴的四氯化碳溶液褪色.
加成反应:有机物分子中的不饱
和键(双键或三键)两端的碳原子 与其它原子或原子团直接结合生成 新的化合物的反应叫做加成反应。
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
节来自石油和煤的两种基本化工原料
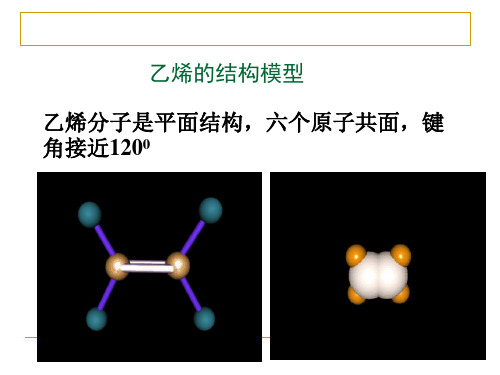
6个原子共平面,键角120°,平面型分子。
比较: “=”和” —”所表现出
的化学性质相同吗?
乙烯的物理性质
无色 稍有气味的气体 密度比空气小 难溶于水
乙烯的化学性质:
1.乙烯的氧化反应:
a.乙烯在空气中燃烧,火焰明亮且 伴有黑烟,生成CO2和H2O
乙烯教学资料PPT

中国乙烯存在巨大的市场缺口和消费增
长空间,国产乙烯的市场占有率一直较低。 为缓解国内乙烯供应紧张,满足国内经济 发展需求,虽然中国石油、中国石化和中 海油加快实施乙烯扩能计划,但中国乙烯 当量消费供需仍将存在缺口。从整体情况 看,中国乙烯工业还有较大的发展空间。
我国未来乙烯需求预测
万吨 4500 4000 3500 3000 2500 2000 1500 1000 500
采用裂解法生产乙烯的原料,主要来源 于原油直接蒸馏产物、馏分油二次加工, 以及天然气和油田气等。以原油直接蒸馏 得到的乙烯原料,主要是直馏石脑油(轻 油)、直馏轻柴油、直馏减压柴油;还有 烯烃生产、芳烃生产的副产乙烷、丙烷、 丁烷、芳烃抽余油等,以及油田轻烃和天 然气凝析液等。
1.石油制乙烯:
乙烯是石油化工的基本有机原料,约有 75%的石油化工产品由乙烯生产,它主要 用来生产聚乙烯、聚氯乙烯、环氧乙烷/乙 二醇、二氯乙烷、苯乙烯、聚苯乙烯、乙 醇、醋酸乙烯等多种重要的有机化工产品, 实际上,乙烯产量已成为衡量一个国家石 油化工工业发展水平的标志。
CH2=CH2 + H-H → CH3-CH3
(3)加聚反应
说明:a.相关概念:
n
催化剂 CH2=CH2
-CH2-CH2-n
单体
高分子化合物
b.聚乙烯无固定熔沸点,为混合物。
聚合反应:
由相对分子质量小的化合物分子 互相结合成相对分子量大的高分子化合物 的反应叫做聚合反应。
不饱和分子发生的聚合反应同时也 是加成反应所以又称为加成聚合反应,简称 加聚反应。
CO2 H 2 HCOOH HCOOH CH3OH HCOOCH3 H 2O
d.甲醇制烯烃
甲醇制烯烃是指以煤或天然气合成的甲 醇为原料,借助类似催化裂化装置的流化 床反应形式,生产低碳烯烃的化工技术。
乙烯PPT课件15(7份打包) 人教课标版

以必修二第三章 乙烯为例
一、情境导入 三天后
在微课中提两个问题: 1熟苹果可以大大缩短青橘 时间,你知道为什么吗?
2天猫超市华南店,买到的 水果箱中放入一些用0.2% 液浸泡过的纸,封严,能 保质期,你知道原因吗?
四天后
设计意图:从生活中的情境导
设计意图:体会,结构决定性质,性质决定用
反思
• 微课视频用途广泛,有机化学中,用于实验现象的对比, 构(空间),习题讲解,定位精准。但是制作需要费工夫 验微课,实验要成功,拍摄技术,视频剪辑等。
• 学生对微课肯定态度,而且学生们也很感兴趣,考虑让学 与进来。
• 丙烯和溴的四氯化碳、氢气、氯化氢、水、次氯酸的加成反应。
• (介绍马尔科夫尼科夫规则,用信息的方式,让他们阅读,不同的催化剂得到马
马氏规则:俄国化学家马尔夫尼科夫在1870年提出:当发生亲电加成反应(如卤化氢和烯烃的反应 (如氢)总是加在连氢最多(取代最少)的碳原子上,而负电基团(如卤素)则会加在连氢最少(取 不对称烯烃与极性试剂加成时,试剂中正离子或带部分正电荷部分加到重键中带有部分负电荷的碳原 而试剂中负离子或带部分负电荷部分加到重键中带有部分正电荷的碳原子上。 反马氏规则:过氧化物催化,丙烯和溴化氢加成,氢加到含氢较少的碳原子上。
•
17、没有一件事情可以一下子把你打垮,也不会有一件事情可以让你一步登天,慢慢走,慢慢看,生命是一个慢慢累积的过程。
•
18、努力也许不等于成功,可是那段追逐梦想的努力,会让你找到一个更好的自己,一个沉默努力充实安静的自己。
•
19、你相信梦想,梦想才会相信你。有一种落差是,你配不上自己的野心,也辜负了所受的苦难。
• 除了微课视频,有机分子球棍模型也非常直观,方便,建 构的时候用实物模型更好。
人教版高中化学必修2-乙烯(共33张PPT)

Br Br CH2CH2 1,2-二溴乙烷
——可用于鉴别或除杂。 Br Br (CH2BrCH2Br) 无色油状液体, 密度比水大,
不溶于水,易溶于CCl4 。
迁移应用
试写出乙烯与H2 、HCl 、H2O发生加成反应 的化学方程式。
催化剂
CH2=CH2 + H-H △
CH3-CH3 乙烷
催化剂
CH2=CH2 + H-Cl
石油裂解气: 主要成分是乙烯, 还含有丙烯、异丁 烯、甲烷、乙烷、 异丁烷、硫化氢和 碳的氧化物等。
一、乙烯的分子结构
分子式
C2H4
球棍模型
电子式
结构式 结构简式 CH2= CH2
CH2CH2
比例模型
空间构型: 平面型分子 6个原子共平面
( 键角约120° )
六个原子共面
约120°
约120°
约120°
研究表明,石蜡油分解的产物 主要是烯烃和烷烃的混合物
资料卡片 石油的裂化、裂解
催化剂
CC168HH3146
△
催化剂
C8CH81H8 16
△
C4H10 C4H10
催化剂
△
催化剂
△
CC8H4H1810++CC8H4H168 辛烷 辛烯
C4H10 + C4H8 丁烷 丁烯
C2H4 + C2H6 乙烯 乙烷 CH4 + C3H6 甲烷 丙烯
• 8、普通的教师告诉学生做什么,称职的教师向学生解释怎么做,出色的教师示范给学生,最优秀的教师激励学生。上午10时55分 53秒上午10时55分10:55:5324.3.4
实验 通入酸性高锰酸钾溶液中
人教版-必修二-化学乙烯课件ppt
火灾袭来时要迅速疏散逃生,不可蜂 拥而出 或留恋 财物, 要当机 立断, 披上浸 湿的衣 服或裹 上湿毛 毯、湿 被褥勇 敢地冲 出去
注意问题:
(1)浓硫酸:浓硫酸与乙醇的体积比为3:1 (2)对反应温度的要求:170℃以下及170 ℃以上不能 有效脱水,故必须迅速将温度升致170℃并保持恒温。 140 ℃时分子间脱水生成乙醚和水 170℃以上浓硫酸使乙醇脱水炭化
现象、 用途
CH2=CH2 +H-Cl →CH3CH2Cl
CH2=CH2
+
H-OH
催化剂 加热、加压
CH3CH2OH
加成反应:
有机物分子中双键或叁键两端的碳原子与其他原 子或原子团直接结合生成新的化合物的反应。
火灾袭来时要迅速疏散逃生,不可蜂 拥而出 或留恋 财物, 要当机 立断, 披上浸 湿的衣 服或裹 上湿毛 毯、湿 被褥勇 敢地冲 出去
△
C2H5OH+2H2SO4(浓)==2C+2SO2↑+5H2O
△
C2H5OH+4H2SO4(浓)==2CO↑+4SO2↑+7H2O
△
C2H5OH+6H2SO4(浓)==2CO2↑+6SO2↑+9H2O
火灾袭来时要迅速疏散逃生,不可蜂 拥而出 或留恋 财物, 要当机 立断, 披上浸 湿的衣 服或裹 上湿毛 毯、湿 被褥勇 敢地冲 出去
4、烯烃的命名
(1)在分子中含有多个双键时,选择满 足有尽可能多的双键的最长的碳链的为主 链,并命名为某烯; (2)从最靠近双键的这一端开始编号; (3)其它命名同烷烃。
《乙烯》精品课件

二、乙烯的结构
物质
乙烷
乙烯
结构简式
CH3-CH3
CH2=CH2
键的类别
C—C
C=C
空间
2C和6H不在同 2C和4H在同一
各原子的位置 一平面上
平面上
乙烯分子中含有碳碳双键,在组成和结构上与只含碳碳 单键和碳氢键的烷烃有较大差异,因此在性质上也有很 多不同。碳碳双键使乙烯表现出较活泼的化学性质。
【典型例题】 例:下列关于乙烯和乙烷的说法中错误的是( C ) A.乙烯是不饱和结构,乙烷是饱和结构。 B.乙烯分子中的两个碳原子在同一条直线上,乙 烷分子中的两个碳原子也在同一条直线上。 C.乙烯分子中含有碳碳双键,乙烯比乙烷稳定。 D.乙烯分子为平面结构,乙烷分子为立体结构。
加成聚合反应,简称加聚反应。
【典型例题】 例:下列过程中发生了加成反应的是( B )
A.C2H4使酸性高锰酸钾溶液褪色 B.C2H4使溴的CCl4溶液褪色 C.C2H4燃烧生成二氧化碳和水 D.CH4和Cl2的混合气体在光照条件下逐渐褪色
【解析】A项,酸性高锰酸钾溶液与C2H4发生氧化反应; B项,C2H4与溴发生加成反应; C项,C2H4燃烧属于氧化反应; D项,属于取代反应。
《乙烯》
一、乙烯的物理性质
乙烯是一种无色,稍有气味的气体 密度比空气略小 难溶于水 用排水法收集
二、乙烯的结构
分子式 C2H4
结构式
H H C=C
H H
电子式 结构简式
H.. H.. H : C :: C : H CH2 = CH2
CH2 CH2
乙烯分子为平面结构,两个碳原子和 四个氢原子在同一平面上。分子中有 碳碳双键,碳原子的价键没有全部被 氢原子“饱和”。
乙烯优质课ppt课件

乙烯分子结构特点乙烯分子式为C2H4,是最简单的烯烃。
乙烯分子为平面结构,所有原子在同一平面上。
乙烯分子中存在碳碳双键,是烯烃的官能团。
乙烯难溶于水,易溶于有机溶剂。
乙烯用途广泛,可用于合成塑料、橡胶、纤维等高分子化合物,也可用作植物生长调节剂和水果催熟剂等。
乙烯为无色、稍有气味的气体,密度比空气略小。
乙烯物理性质及用途乙烯易被氧化剂氧化,如高锰酸钾溶液、臭氧等。
氧化反应乙烯中的碳碳双键可与氢气、卤素单质等发生加成反应。
加成反应在特定条件下,乙烯可发生聚合反应生成聚乙烯等高分子化合物。
聚合反应乙烯分子中的α-氢原子比较活泼,可发生取代反应和消去反应等。
α-氢原子的反应乙烯化学性质分析原料选择与预处理过程原料选择通常采用石脑油、轻柴油等作为裂解原料,要求原料中烷烃含量高,环烷烃和芳烃含量低。
预处理过程原料需要经过预分馏、预加氢等预处理步骤,以去除杂质、调整烃类组成,提高裂解效率和产品质量。
裂解反应原理及条件控制裂解反应原理在高温(750-950℃)和极短停留时间(0.1-0.2秒)的条件下,原料中的大分子烃类发生断链和脱氢反应,生成小分子的烯烃和烷烃。
条件控制裂解温度、停留时间和原料组成是影响裂解效果的主要因素,需要精确控制以确保产品质量和收率。
产品分离纯化方法分离方法通过精馏、萃取、吸附等分离技术,将裂解气中的乙烯、丙烯等目标产品与甲烷、乙烷等轻组分以及重组分进行分离。
纯化方法采用催化加氢、精馏等技术,去除乙烯中的微量杂质,如乙炔、硫化物等,提高乙烯的纯度。
03采用辐射传热方式,具有结构简单、操作方便、投资少等优点,但热效率低、能耗高。
管式裂解炉采用辐射和对流传热相结合的方式,具有热效率高、能耗低等优点,但结构复杂、投资大。
梯台式裂解炉采用流化床技术,使原料在炉内均匀分布并快速裂解,具有热效率高、产品质量好等优点,但操作难度较大。
流化床裂解炉裂解炉类型及特点介绍关键设备结构和工作原理阐述裂解气压缩机用于将裂解气压缩至所需压力,以便进行后续分离和精制。
乙烯说课PPT精品文档(2024)

2024/1/26
安全设施配备
完善安全设施,如安全阀、压力表 、温度计等,确保生产过程安全可 控。
21
废弃物处理和环境影响评估
分类收集
对生产过程中产生的废弃物进行分类收集,便于后续处理。
2024/1/26
资源化利用
通过技术手段将废弃物转化为有用资源,如回收再利用或生 产其他产品。
22
废弃物处理和环境影响评估
甲烷氧化偶联路线
以甲烷为原料,通过氧化 偶联反应得到乙烯,此路 线具有原子经济性但催化 剂活性有待提高。
12
绿色合成路线创新点介绍
生物质转化路线
利用生物质资源,通过生物或化学方 法转化为乙烯,此路线具有可再生性 和环保性。
甲烷无氧芳构化路线
在无氧条件下,通过催化剂作用将甲 烷转化为乙烯,此路线原子经济性高 且无需外源氧化剂。
• 无害化处理:对无法资源化利用的废弃物进行无害化处理 ,确保不对环境和人体造成危害。
2024/1/26
23
废弃物处理和环境影响评估
评估内容
对乙烯生产过程中的废气、废水、噪声等环境因素进行评估。
评估方法
采用定量和定性评估方法,综合考虑环境因素的各个方面。
2024/1/26
评估结果
根据评估结果采取相应的环保措施,降低乙烯生产对环境的影响 。
15
作为原料参与各类有机反应
乙烯与卤素反应
生成卤代烃,是有机合成 中引入卤素原子的重要方 法。
2024/1/26
乙烯与氢气反应
生成乙烷,是工业上制备 乙烷的主要途径。
乙烯与水反应
在酸催化下生成乙醇,是 工业上制备乙醇的方法之 一。
16
作为催化剂促进反应进行
高一化学1《乙烯》课件(新人教版必修2)

A. CO C. C2H4
B. CO2 D. C2H6
4. 乙烯发生的下列反应中,不属于加成反应 的是 ( D )
A. 与氢气反应生成乙烷 B. 与水反应生成乙醇 C. 与溴水反应使之褪色 D. 与氧气反应生成二氧化碳和水
例题选讲:
[例1]某气态烃在密闭容器中与氧气混合,用电火 花点燃,完全燃烧前后容器内压强保持不变(温 度为120℃),则该烃为( AC)
3. 聚合反应
催化剂
nCH2=CH2
[ CH2- CH2 ]n
定义:由相对分子质量小的化合物分子互 相结合成相对分子质量大的高分子的反应 叫做聚合反应
在聚合反应中,由不饱和的相对分子质量 小的化合物分子结合成相对分子质量大的 化合物的分子,这样的聚合反应同时也是加 成反应,所以这种聚合反应又叫做加成聚合 反应,简称加聚反应.
4、能否用排空法收集乙烯? 不能,因为乙烯的密度与空气的密度接近。
5பைடு நூலகம்实验结束是先撤酒精灯还是先撤导管? 先撤导管,防止倒吸。
6、加热过程中混合液颜色如何变化?
溶液由无色变成棕色最后变成黑色。
原因是浓硫酸使酒精脱水碳化
△
2H2SO4+C2H5OH
2SO2↑+2C+5H2O
7、加热时间过长,还会产生有刺激性气味的气体, 为什么?
1、关于乙烯分子结构的说法中,错误的是
(C)
A.乙烯分子里含有C=C双键;
B.乙烯分子里所有的原子共平面;
C.乙烯分子中C=C双键的键长和乙烷分 子中C-C单键的键长相等。
D.乙烯分子里各共价键之间的夹角为 120。
2、除去乙烷中混有的少量乙烯的方法,正确
化学乙烯课ppt课件

乙烯还可与其他单体(如丙烯、苯 乙烯等)共聚,生成各种共聚物, 广泛应用于包装、建筑、汽车等领 域。
05
乙烯在工业上的应用
聚乙烯的生产与应用
聚乙烯的生产
通过乙烯的聚合反应得到聚乙烯 ,反应条件包括高温高压、催化
剂等。
聚乙烯的种类
根据聚合方法和分子结构的不同 ,聚乙烯可分为低密度聚乙烯( LDPE)、高密度聚乙烯(HDPE
废水排放
乙烯生产还会产生大量的废水,其中含有许多有机物和重金属离子等污染物。这 些废水如果未经处理直接排放到水体中,会对水生生物和人类造成危害。
降低乙烯生产对环境的影响
采用清洁生产技术
通过改进生产工艺和设备,减少废气、废水的产生和排放。例如,采用高效催化剂、优化 反应条件等。
加强废气、废水处理
对产生的废气、废水进行严格的处理,确保达到国家排放标准后再进行排放。例如,采用 活性炭吸附、生物处理等废气处理技术;采用化学沉淀、膜分离等废水处理技术。
安全防护措施
在生产和使用乙烯的过程中,必须采取严格的安全防护措施 。例如,穿戴防护服、戴防毒面具、保持通风等。此外,还 应定期进行安全检查和培训,提高员工的安全意识。
乙烯生产过程中的环保问题
废气排放
乙烯生产过程中会产生大量的废气,其中含有许多有害物质,如二氧化碳、硫化 氢等。这些废气如果未经处理直接排放到大气中,会对环境造成严重的污染。
技术成熟度与产量
石油裂解法技术成熟,产量高;天然 气转化法技术也在不断发展完善,产 量逐渐提高。
环境保护与可持续性
石油裂解法在生产过程中会产生一定 的环境污染;天然气转化法相对较为 环保,且原料来源广泛,具有更好的 可持续性。
适用场景与选择建议
化学课件《乙烯》优秀ppt12(4份打包) 人教课标版

分子式
通式
结构
燃烧
通入酸性 KMnO4溶液 通入Br2水或 Br2的CCl4溶 液
小结
CH4 (烷烃)
CnH2n+2
(n≥1整数)
C2H4 (烯烃)
CnH2n
(n≥2整数)
烷烃只含碳碳单键 含有C=C
淡蓝色火焰
生成CO2和 H2O
火焰明亮并伴有黑 烟,生成CO2和H2O
不反应,无现象 褪色,发生氧化反应
A. 乙烷和氯气反应
B. 乙烯和氯气反应
C. 乙烯和氯化氢反应
D. 乙烯和氢气反应
85.每一年,我都更加相信生命的浪费是在于:我们没有献出爱,我们没有使用力量,我们表现出自私的谨慎,不去冒险,避开痛苦,也失去了快乐。――[约翰·B·塔布] 86.微笑,昂首阔步,作深呼吸,嘴里哼着歌儿。倘使你不会唱歌,吹吹口哨或用鼻子哼一哼也可。如此一来,你想让自己烦恼都不可能。――[戴尔·卡内基]
不反应,无现象 褪色,发生加成反应
练1:能用于鉴别甲烷和乙烯的试剂是 ( AB )
A. 溴水
B.酸性高锰酸钾溶液
C. NaOH溶液 D.四氯化碳溶液
练2下:列物质不可能是乙烯加成产物的是(B)
A.CH3CH3
B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
练3制:取一氯乙烷的最好方法是( C)
94.对一个适度工作的人而言,快乐来自于工作,有如花朵结果前拥有彩色的花瓣。――[约翰·拉斯金] 95.没有比时间更容易浪费的,同时没有比时间更珍贵的了,因为没有时间我们几乎无法做任何事。――[威廉·班] 96.人生真正的欢欣,就是在于你自认正在为一个伟大目标运用自己;而不是源于独自发光.自私渺小的忧烦躯壳,只知抱怨世界无法带给你快乐。――[萧伯纳]
乙烯教学完整ppt课件

,耗氧量最大的是哪个?CH4
精选编辑ppt
54
类型一: 等物质的量和等质量的烃完全燃烧比较耗氧量
(1)等物质的量的烃(CxHy)完全燃烧时耗氧 量多少决定于(x+y/4)的数值,其值越大,耗氧 越多,反之越少。
(2)等质量的烃完全燃烧时,耗氧量的多少决定 于CHy/x中y/x(含氢量)的数值,y/x值越大耗氧 越多,反之耗氧越少。
溶液褪色的气体有 ( AC)
A. SO2 C. C2H4
B. CO2 D. C2H6
精选编辑ppt
46
4、下列反应属于加成反应的是( D ) A. 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑ B.
C.
D.
精选编辑ppt
47
5、某烯烃和氢气加成后的产物如图:
⑤ CH3 C①H3—②C—C③H2—CH④ 3
CH3CH2Cl(一氯乙烷)
H—OH
CH2=CH2 + H2O
催化剂 △
CH3CH2OH(乙醇)
工业上乙烯水化法制酒精的原理
精选编辑ppt
28
思考:
⑴实验室制取氯乙烷, 是采取CH3-CH3与Cl2取代
反应好, 还是采用CH2=CH2与HCl加成反应好?
CH3-CH3 +Cl2 光 CH3-CH2Cl+HCl
条件
常温、标况下,水是液态 >100℃,水是气态
例4:在压强一定,温度150 ℃ 条件下,某有机物 完全燃烧,反应前后压强不发生变化,该有机物 可能是(AC)
A、CH4 B、C2H6 C、C2H4 D、C2H2
乙烯ppt课件免费

乙烯
CATALOG
DATE
ANALYSIS
SUMMARY
目录
CONTENTS
• 乙烯的简介 • 乙烯的生产 • 乙烯的应用 • 乙烯的市场分析 • 乙烯的储存与运输 • 乙烯的环保与安全
REPORT
CATALOG
DATE
ANALYSIS
SUMMAR Y
01
乙烯的简介
乙烯的化学性质
乙烯是一种有机化合物,化学 式为C2H4,是最简单的烯烃。
乙烯的废弃物处理与利用
废气处理
乙烯生产过程中产生的废气需要进行处理,以减少对环境 的污染。常见的废气处理方法包括洗涤、吸附和催化燃烧 等。
固体废弃物处理
乙烯生产过程中产生的固体废弃物需要进行处理,以减少 对环境的污染。常见的固体废弃物处理方法包括填埋、焚 烧和资源化利用等。
废水处理
乙烯生产过程中产生的废水需要进行处理,以满足排放标 准。常见的废水处理方法包括沉淀、过滤和生物处理等。
医学
乙烯可以用于生产医用材料和器械,如医用塑料、医疗器械等,具 有良好的生物相容性和耐腐蚀性。
化学工业
乙烯是许多化学反应的原料,可以用于生产溶剂、油漆、涂料等化 学品,同时还可以用于生产燃料添加剂和润滑油等。
REPORT
CATALOG
DATE
ANALYSIS
SUMMAR Y
04
乙烯的市场分析
全球乙烯市场分析
全球乙烯产能
全球乙烯产能持续增长,主要集中在中国、美国、中东和欧洲等 地。
全球乙烯需求
乙烯主要用于生产塑料、化学品和燃料等,市场需求稳步增长。
全球乙烯贸易
全球乙烯贸易活跃,主要出口国为中国、美国和中东等地,进口 国主要为欧洲和亚洲国家。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
加成反应同时又是聚合反应,简称加聚反应。
小结:
分子式 结构
燃烧
通入酸性 KMnO4溶液 通入Br2水或 Br2的CCl4溶液
CH4 (烷烃)
只含碳碳单键 淡蓝色火焰 生成CO2和H2O 不反应,无现象
不反应,无现象
C2H4 (乙烯)
含有C=C
火焰明亮并伴有黑烟 生成CO2和H2O 褪色,发生氧化反应
(乙烯的还原性,被氧化成CO2)
应用:鉴别乙烯和甲烷(烷烃)
(2). 加成反应:
现象:溴水或溴的四氯化碳溶液褪色
应用:鉴别乙烯和甲烷(烷烃);
除去甲烷(烷烃)中的混有乙烯气体
HH
HH
H C C H + Br – Br H C C H
反应实质
Br Br
1,2-二溴乙烷,无色油状液 体,难溶于水
注意:①乙烯与卤素分子常温条件下进行
吗?
CH2 = CH2 + Cl2→ CH2ClCH2Cl
乙烷
催化剂
CH2=CH2 + H2 ▲
CH3CH3
催化剂
CH2=CH2 + HCl ▲ CH3CH2Cl
催化剂
CH2=CH2 + H-OH 加热加压CH3CH2OH
氯乙烷 乙醇
CH2=CHCH3 + HCl
已知AgBr是难溶于水的淡黄色沉淀, HBr是一元强酸,试证明乙烯与Br2 的反应是加成反应而不是取代反应?
试一试:回顾乙烷的分子结构和化学性质, 根据乙烯分子式C2H4和C原子的成键特点, 对比乙烷的分子结构推测乙烯的结构?
HH
∣∣
→
H - C- C-H
∣∣
HH
乙烷
?
乙烯
6
1、乙烯的结构:
分子式
C2H4
电子式 结构式 结构简式
: :
HH H
H
H:C::C:H C=C
CH2 = CH2
H
H
空间构型: 平面型分子--6个原子在同一平面上,
②分子空间构型发生了改变
迁移
③产物相对较纯净
12
难点突破
有机物分子中双键(或三键)两端的碳原子与其他原子或原 子团直接结合生成新的化合物的反应叫做加成反应。
加成反应特点:断一加二,只上不下, 产物相对较纯净
乙烯 溴分子
1,2-二溴乙烷
返回
迁移应用
在一定条件下,乙烯还可以与Cl2、H2、HCl 、H2O等 发生加成反应,你能写出有关反应的化学方程式
8
2、乙烯的物理性质:
乙烯是 无 色
稍气有味的气体
, 溶于难水;密度较空气
。 略小
收集方法 : 排水法
2020/3/19
(1).氧化反应: ①在空气中燃烧
CH2= CH2 + 3O2 点燃 2CO2 +2 H2O 现象:火焰明亮并伴有黑烟 (乙烯含碳量大,燃烧不充分)
10
②使酸性KMnO4溶液褪色
2020/3/19
键角120º
分子式
键长(10-10m )
键能(kJ/mol)
键角
乙烯 C2H4
1.33 615 120°
乙烷 C2H6 1.54 348
109°28’
思考:1.“C=C”的键长和键能是否是“C-C”的2倍? 2.根据“C-C”的性质推测“C=C”有什么特征?
C=C双键中有一个键不ຫໍສະໝຸດ 定,易断裂操作:滴加AgNO3溶液 或 测溶液的pH
15
聚乙烯
(3). 加聚反应:
n
催化剂 CH2=CH2
-CH2-CH2-n
乙烯
(聚乙烯)
1、聚乙烯无固定熔沸点。
2、聚乙烯等白色塑料废弃物,微生物
不能降解,是白色污染物。
由不饱和的相对分子质量小的化合物分子结合成
相对分子质量大的化合物的分子,这样的反应是
乙烯
如果把青桔子和熟苹果放在同一个 塑料袋里,系紧袋口,这样一段时间后青 桔子就可以变黄、成熟。
乙 烯 这是谁的功劳?
来源:乙烯主要来自石油化工
如何衡量石油化工发展水平
科学探究
教材P67石蜡油的分解实验
① 石蜡油:17个C以 上的烷烃混合物 ②碎瓷片:催化剂 ③加热位置:碎瓷片
④将生成气体通人酸 性高锰酸钾溶液中。
⑤生成的气体通入溴的四氯化碳溶液
⑥点燃气体
科学探究:石蜡油分解实验
实验
现象
结论
通入酸性 KMnO4溶 液 通入Br2的 CCl4溶液
点燃
溶液褪色 乙烯可被酸性KMnO4氧化
溶液褪色 乙烯可与Br2发生反应
火焰明亮,
有黑烟
乙烯中C含量较高
从上面的现象可以看出,生成的气体中含有与 烷烃性质不同的烃。
5
H2
Ni
CH3—CH3
加成
Br2
CH2Br—CH2Br
HCl
催化剂、加温、加压
CH3—CH2Cl
H2O
CH3—CH2OH
加聚
[ CH2—CH2]n
4、用途:
(1) 有机化工原料,制聚乙烯塑料、乙醇等
(2) 植物生长调节剂,水果的催熟剂
2020/3/19
褪色,发生加成反应
2020/3/19
取代反应与加成反应的比较
意义 归属 断键规律
产物特点
取代反应
取而代之,一上一下 烷烃的特征反应 C-H 断裂
产物复杂, 为混合物
加成反应
加之而成,断一加二 烯烃等的特征反应
C-C断裂 产物相对较纯净
总结乙烯的化学性质
氧化
使酸性高锰酸钾溶液褪色
CH2=CH2
2CO2+2H2O
