配位化合物
第五章配位化合物

[Ag(S2O3)2]3-, [Fe(CN)6]4-, [Fe(SCN)6]3-, [HgI4]2- , [Fe(CN)6]3-等 或原子)和一定数目 配位单元:由中心离子(或原子 配位单元:由中心离子 或原子 和一定数目 的中性分子或阴离子以配位键结 合而成的中性分子或复杂离子。 合而成的中性分子或复杂离子。 [Ni(CO)4], [Co(NH3)3F3], [Pt(NH3)2Cl2], K3[Fe(SCN)6], [Ag(NH3)2]NO3。 配合物: 含配位单元的化合物。 配合物 含配位单元的化合物。
6
{
多齿配体数≠( ) 多齿配体数 (<) 配位数 中心离子的配位数一般等于其电荷数的二倍 如:M+——2、M2+——4、M3+——6 、 、 ④.配离子的电荷数 a. 配离子的电荷数等于中心原子的氧化数 和配体总电荷数的代数和。 和配体总电荷数的代数和。 b. 外层电荷数的相反数。 外层电荷数的相反数。 K3[Fe(SCN)6] [Ag(NH3)2]NO3 中心离子的电荷数: 中心离子的电荷数 +3(Ⅲ) +1(Ⅰ) [Pt(NH3)2NO2NH2 Cl2] +4(Ⅳ) Ⅳ
13
[Co(NH3)5(ONO)]Cl2 氯化亚硝酸根•五氨合钴 Ⅲ) 氯化亚硝酸根 五氨合钴(Ⅲ 五氨合钴 六氯合铂( 六氯合铂(Ⅳ)酸 H2[PtCl6] Na3[Ag(S2O3)2] [Cu(NH3)4](OH)2 K3[Fe(SCN)6] 二硫代硫酸根合银(Ⅰ 酸钠 二硫代硫酸根合银 Ⅰ)酸钠 氢氧化四氨合铜(Ⅱ 氢氧化四氨合铜 Ⅱ) 六硫氰合铁(Ⅲ 酸钾 六硫氰合铁 Ⅲ)酸钾
12
首页 上页 下页 返回
[Ag(S2O3)2]3[Cr(NH3)5(H2O)]3+ [Cu(NH3)4]2+ [Fe(NH3)2(en)2]3+ [Co(NH3)5(ONO)]2+ [Cr(NH3)3Cl3]
配位化合物
8.2 配合物的空间结构和异构现象
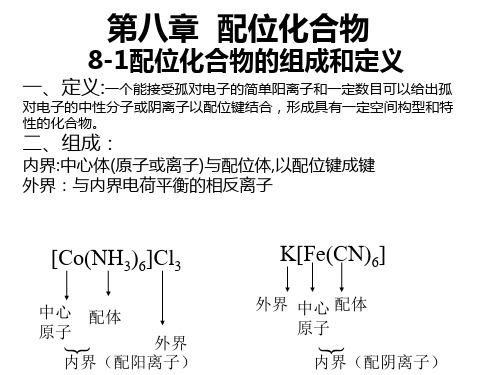
1、配合物的空间结构 空间构型
配位数 2 杂化轨道 sp 空间构型 直线型 实例 [Ag(NH3)2]+
3
4
sp2
sp3
平面三角形
平面正方形
[HgI3][Ni(CN)4]-、[PdCl4]2-
四面体
5 dsp3或d3sp d2sp2 6 d2sp3或sp3d2 三角双锥 正方锥形 正八面体
配位数(不一定是配体数)
与中心原子直接以配位键结合的配位原子的数目 称为中心原子的配位数。中心原子的配位数一般可为 2-12,以配位数2,4,6最为常见。 中必原子的配位数与配体的齿数有关,
配体是单齿,那么中心原子的配位数就是配体的数目; 配体是多齿,那么中心原子的配位数则是配体的数目 与其齿数的乘积。 例如: [Co Br(NH3)5] (SO4),
1.62×107=(0.02-x)/4x3
x=6.8×10-4
二、配位解离平衡移动
1. 与弱电解质平衡的竞争
M+ + L+ + OHH+ [ML]
当Ka, Kb越小,配离子越易解离 平衡向生成弱酸、弱碱方向移动 MOH HL
[ Fe(C2O4 )3 ]3
Fe3 3C2O4 2
+ 6H+
→
3. 杂化轨道形式与配合物的空间构型
配 位 数 2 3
空间构型
直线形 平面三角形
杂化轨 道类型 sp sp2
实例
Ag(NH3)2+ , Ag(CN)2– Cu(CN)32 – ,HgI3–
4 4 5
5 6
正四面体 四方形 三角双锥
四方锥 八面体
配位化合物

• 配位反应与氧化还原反应的关系 配位离解平衡与氧化还原平衡的关系,主 要体现在配位化合物的生成对电极电势的影 响。
根据能斯特方程: 若氧化型生成配位化合物,浓度减小,则E减小; 若还原型生成配位化合物,浓度减小,则E增大。
中心原子(阳离子或原子)与一定数目的配体(离子或 中性分子) ,通过配位键结合,并按一定组成和空间 构型形成的复杂离子称为配离子
例如, [Cu(H2O)4] 2+
含有配离子的化合物以及中性配位分子统称为 配合物。 例如, H[AuCl4] 、[Co(NH3)Cl3]
配位键 配体 中心原子
[Cu (NH3)4]SO4 [Cu (NH3)4]2+
• 当配位体接近中心离子时,为了增强成键 的能力,中心离子用能量相近的空轨道进 行杂化,形成数目相同,能量相等的具有 一定方向性的杂化空轨道,以容纳配位体 提供的电子形成配位键。配离子的空间构 型、配位数及稳定性等主要取决于杂化轨 道的数目和类型。 • M :L(L代表配位体)
第三节 配位化合物的离解平衡
中 心 离 子 配 位 配 体 位 原 子 配 位 数 离 子 电 荷
内界(配离子)
外界 SO42-
内界
在配合物化学式中用方括号表示内界。 配合物的内界能稳定地存在于晶体及水溶液中。 它是配合物的特征部分,它的结构和性质与其他离 子不同。 如: [ Cu (NH3) 4 ]2+
外界
不在内界的其他离子,如SO42- 构成配合物的外界。 写在方括号外,
单齿配体:一个配体中只有一个配位原子 例如: Ag+ 与NH3 结合
第七章 配位化合物

1 1.73
2 2.83
3 3.87
4 4.90
5 5.92
如:实验测出 [FeF6]3﹣的µ= 5.9 → n = 5 可知它是外轨型配合物 再如: 再如:实验测出 [Fe(CN)6]3﹣的µ= 1.9 → n = 1 可知它是内轨型配合物 外轨型,中心离子电子结构未变, 外轨型,中心离子电子结构未变,单电子数未变 内轨型,中心离子电子结构改变, 内轨型,中心离子电子结构改变,单电子个数改变
配
配
4
7.1.2 配位化合物的组成
[Cu(N 配 [Cu(NH3)4] SO4
中 心 离 子 配 位 原 子 界 位 体
配 离 子 电 荷
2+
配 位 数
外 界
配位化合物
5
中心离子(原子) ① 中心离子(原子):位于配位化合物的中心位置的离子 或原子,是配合物的核心, 或原子,是配合物的核心, 通常是某些金属阳离子或金属原子以及高 氧化态的非金属元素
和中心离子配合的负离子或分子, ② 配位体: 和中心离子配合的负离子或分子,简称配体
③ 配位原子:直接与中心原子配位的原子。配位原子上均 配位原子:直接与中心原子配位的原子。
有孤对电子, 有孤对电子,N、O、S、Cl、C、F、Br、I等 Cl、 Br、 直接与中心离子(或原子) ④配位数:直接与中心离子(或原子)结合成键的配位原子 数目,常见的为2 数目,常见的为2、4、6。
14
§7.2 配合物的化学键理论
中心离子和配位体之间是怎样结合的? 中心离子和配位体之间是怎样结合的? 关于配合物的化学键理论主要有: 关于配合物的化学键理论主要有: 价键理论√ 晶体场理论 配位场理论 分子轨道理论
15
配位化合物

Ni2+可以利用丁二肟在氨溶液中与Ni2+配位生成桃红 色絮状螯合物沉淀物来鉴定。
首页
上一页
下一页
末页
32
利用硫氰根负离子可以与Co2+形成蓝紫色的四硫氰 根 合 钴 ( II ) [Co(SCN)4]2- 来 检 验 Co2+ 的 存 在 。 与 Fe3+形成血红色配合离子可供检验Fe3+的存在。
K4[Fe (CN)6]
六氰合铁(Ⅱ)酸钾
H4[Fe (CN)6]
六氰合铁(Ⅱ)酸
[Co(NH3)5H2O]Cl3
氯化五氨·水合钴(Ⅲ)
首页
上一页
下一页
末页
18
配合物的类型
(1)简单配合物 由单齿配体与中心原子直接配位而成的配位化合 物。
例:[Ag(NH3)2]+ BF4[Fe(H2O)6]Cl3 [CoCl3(NH3)3] 等
28Ni 3d84s2 3d
Ni2+
4s 4p
[Ni(CN)4]2-
dsp2杂化
CN- CN- CN-CN-
首页
上一页
下一页
末页
24
[NiCl4]2-的空间构型为四面体。
28Ni 3d84s2
3d
Ni2+
4s 4p
[NiCl4]2-
3d sp3杂化
4s
4p
Cl- Cl- Cl- Cl-
首页
上一页
下一页
首页
上一页
下一页
末页
38
配合物与配位作用用于医学
什么是配位化合物

什么是配位化合物?配位化合物是指由一个或多个配位体(ligand)与一个中心金属离子(或原子)通过配位键(coordination bond)结合形成的化合物。
在配位化合物中,配位体通过共用电子对与中心金属离子形成配位键,将其固定在配位体的周围形成配位球形结构。
1. 配位体:配位体是能够提供一个或多个电子对给中心金属离子的分子或离子。
配位体通常是具有孤对电子的原子或分子,包括有机分子如胺、醇和酸以及无机分子如氨、水和卤素离子等。
配位体通过配位键与中心金属离子结合,形成稳定的配位化合物。
2. 配位键:配位键是指配位体与中心金属离子之间的共用电子对。
配位键通常是通过配位体中的孤对电子与中心金属离子中的空轨道形成。
这种共用电子对的形成使得配位体与中心金属离子之间形成了较强的化学键。
配位键可以是单个配位体提供一个电子对形成的单配位键,也可以是多个配位体提供多个电子对形成的多配位键。
根据配位键的数量,配位体可以分为单齿配位体、多齿配位体和桥配位体等。
3. 配位球形结构:配位化合物中的配位体通过配位键与中心金属离子结合,形成了一个稳定的配位球形结构。
在这个结构中,中心金属离子被配位体包围,形成一个多面体的结构。
配位球形结构的形状和几何构型取决于配位体的种类和数量,以及中心金属离子的电子构型。
常见的配位球形结构包括八面体、四方体、正方形平面、三角双锥等。
这些不同的结构对于化合物的性质和反应有重要影响。
配位化合物具有许多特点和性质。
首先,配位化合物通常具有良好的溶解性和热稳定性,因为配位键是较强的化学键。
其次,配位化合物的颜色通常取决于中心金属离子的电子结构和配位体的取代情况。
这使得配位化合物在催化、荧光和生物活性等领域具有重要应用。
此外,配位化合物还可以通过改变配位体的种类和数量来调节其性质和功能,如选择性吸附、储能和分子识别等。
配位化合物是化学中的重要概念,对于理解过渡金属化学、配位化学和配位聚合物等领域具有重要意义。
配位化合物

[Cu(NH3)2]Ac + CO + NH3 ===== [Cu(NH3)2]Ac.CO
减压加热
H = -35kJ
Cu2+ + 5CN- = Cu(CN)43- + 0.5(CN)2 K稳 =2×1030 (极为稳定,加入H2S也无沉淀,Ksp=2.5×10-50))
Cu(CN)4 3 - + e == Cu + 4CNE = -1.27V Zn(CN)42- + 2e == Zn + 4CNE = -1.26V 这两个电对的电势值相近,所以镀黄铜(Cu-Zn合金)所 用的电镀液为上述混合物.
[AlCl4][BF4][AgI4]2- 从这些配离子你看出配位数有什么规律? 从这些配离子你看出配位数有什么规律?
二,化学键理论
维尔纳(Werner.A):Nobel Prize提出三点: 维尔纳( 提出三点: 提出三点 1,主价和副价 , 主价指氧化数,副价指配位数. 主价指氧化数,副价指配位数. 2,倾向于既要满足主价,又要满足副价. ,倾向于既要满足主价,又要满足副价. 3,副价指向空间的确定位置. ,副价指向空间的确定位置. 1,价键理论:中心离子和配位原子都是通过杂化了的共价配位键 ,价键理论: 结合的. 结合的. (1)配位键的本质: )配位键的本质: a,σ配位键: 配位键: , 配位键
2,复盐 ,
CsRh(SO4)2.4H2O + BaCl2 无沉淀出现. 无沉淀出现. [Rh(H2O)4(SO4)2]-(二硫酸根四水合铑(III)) 二硫酸根四水合铑( )) 二硫酸根四水合铑 KCl.MgCl2.6H2O不是配合物 不是配合物
3,组成 ,
(1)配位体:是含有孤电子对的分子和离子 )配位体:
配位化合物知识总结

VS
磁性配合物在磁学、磁记录、信息存 储和分子基磁体等领域有广泛的应用 前景。
Part
04
配位化合物的应用
在化学反应中的作用
催化反应
配位化合物可以作为催化剂,通 过与反应物结合,改变反应途径,
降低反应活化能,从而加速化学 反应的进行。
分离和提纯
利用配位化合物的独特性质,如选 择性络合、稳定性差异等,可以实 现化学物质的分离和提纯。
配位化合物的稳定性取决于多个因素 ,包括中心离子的性质、配位体的类 型和数量、以及配位环境等。
稳定性规律
一般来说,中心离子的电荷数越高、 半径越小,配位化合物的稳定性越强 ;配位体的电子给予能力越强、数目 越多,稳定性也越高。
配位化合物的合成方法
有机合成
通过有机合成方法,可以制备出结构复杂、功能多样的配 位化合物。常见的合成方法包括重氮化反应、氧化还原反 应等。
配位化合物的分类
按中心原子分类
根据中心原子的种类,可以将配位化合物分为金属配位化合物和非金属配位化合物。金属配位化合物是指中心原 子为金属元素的配位化合物,如铜、钴、铁等;非金属配位化合物是指中心原子为非金属元素的配位化合物,如 硫、氮、磷等。
按配位数分类
根据配位数的大小,可以将配位化合物分为低配位数(2-4)和高配位数(≥6)的配位化合物。低配位数配位化 合物是指中心原子周围参与配位的配位体数目较少的配位化合物;高配位数配位化合物是指中心原子周围参与配 位的配位体数目较多的配位化合物。
02
动态配位化合物
03
超分子配位化合物
具有可逆的结构变化和反应性, 可用于传感器、分子机器等领域。
由多个分子或离子通过非共价相 互作用形成的复杂结构,具有独 特的物理和化学性质。
配位化合物

(二)配位体
在配合物中与形成体结合的离子或中性分子称为配位体, 简称配体,如[Co(NH3)4]2+中的NH3、在配体中提供孤对电
子与形成体形成配位键的原子称为配位原子,如配体NH3中
的N。常见的配位原子为电负性较大的非金属原子C、N、P、 O、S和卤素等原子。
根据一个配体中所含配位原子数目的不同,可将配体分为 单齿配体和多齿配体。 单齿配体:一个配体中只有一个配位原子,如NH3,OH-,X-,
第三节 螯 合 物
乙二胺分子是多齿配体,两个乙二胺分子与一 个Cu2+形成具有两个五元环的配位个体[Cu(en)2]2+:
H 2C H 2C H2N
NH 2
CH 2 CH 2
2
Cu
H2N
NH 2
由中心原子与多齿配体所形成的具有环状结构 的配位个体称为螯合个体。螯合个体为离子时称为 螯合离子,螯合离子与外界离子所组成的化合物称 为螯合物。不带电荷的螯合个体就是螯合物,通常 把螯合离子也称为螯合物。 能与中心原子形成螯合个体的多齿配体称为螯 合剂。
O H2N H3C N N N Co
+
O NH2 O
CH3
N N
CH3 CH3
CH3 O
Vitamin B12
(钴的配合物)
NH
O
NH2 CH3 CH3
O N P O HO N O H H H O H
HO
Co
Vitamin B12
的结构模型
K s{[Zn(NH 3 ) 4 ]2+ }
ceq {[Zn(NH 3 ) 4 ]2+ }/ c
[ceq (Zn 2+ ) / c ] [ceq (NH 3 ) / c ]4 1 8 5.0 10 (6.7 103 ) 4
配位化合物

总解离反应: [Ag(NH3)2]+(aq) 总解离常数(不稳定常数):
Ag+(aq)+2NH3(aq) Kd
{c(Ag )}{c( NH3 )}2 Kd Kd1Kd 2 {c(Ag(NH3 ) 2 )}
无机及分析化学
显然,Kd 越大, 配合物越不稳定。
西南科技大学
13
2. 配位平衡
• 稳定
•
加热不放出氨气
[Co(NH3)6]Cl3
2. 特征: 有[内界]外界,如:[Ag(NH3)2]Cl;
外层 内层
从溶液中析出配合物 时,配离子常与带有相反 电荷的其他离子结合成盐, 这类盐称为配盐。
K3 [Fe ( C N )6 ]
形 成 体
配配 配 位体 位 原 数 子
西南科技大学
2
无机及分析化学
无机及分析化学
西南科技大学
14
在溶液中,配离子的生成一般是分步进行的,因此溶液中 存在着一系列的配位平衡,每一步都有相应的稳定常数,称为 逐级稳定常数。 c Ag+(aq)+NH3(aq)
(1)简单配合物
单基配位体和中心原子所形成的配合物,如 [Ag(NH3)2]Cl。
(2)螯合物
多基配位体以一个或两个配位原子与同一中 心原子配位所形成的环状化合物, 如[Zn(en)2]2+,en:NH2CH2CH2NH2 (乙二胺)。
(3)多核化合物
由配位体与多个中心原子所形成的配合物, 如[(H20)4Fe(OH)2Fe(H2O)4]4+。
(4)羰合物
以羰基配位体与金属形成的一类化合物,如 Ni(CO)4。
无机及分析化学 西南科技大学
8
配位化合物
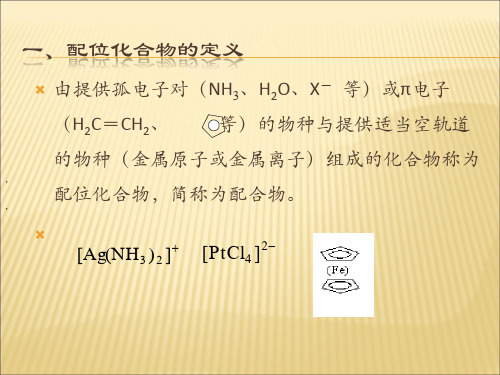
配位数
2 3 4 4 5 5 6 6
中心 杂化方式
构型
实例
sp sp2 sp3 dsp2 dsp3 sp3d sp3d2 d2sp3
直线形 [ Ag( NH3)2 ]+ 三角形 [ Cu(CN)3 ]2- 四面体 [ Zn(NH3)4 ]2+ 正方形 [ N(i CN)4 ]2-
三角双锥 [ F(e CO)5 ] 三角双锥 [ Fe(SCN)5 ]2-
2 溶剂合异构
当溶剂分子取代配位基团而进入配离子的内界所
产生的溶剂合异构现象。与电离异构极为相似, 最熟悉 的例子是:
[Cr(H2O)6]Cl3 [Cr(H2O)5Cl]Cl2·H2O [Cr(H2O)4Cl2]Cl·2H2O 在配合物的内界,各含有6、5、4个配位水分子 和0、1、2个配位氯离子, 在配合物的外界各含有0、1 、2个溶剂合水分子和3、2、1个可电离的氯离子。这 些异构体在物理和化学性质上有显著的差异,如它们的 颜色分别为绿、蓝绿、蓝紫。
4p 4s
dsp2杂化
Ni(CN)24
八面体构型
对于F-,H2O等配体而言,配位原子F,O的电负性大, 不易给出孤对电子对,所以对中心体的3d轨道上的 电子不发生明显的影响,因此3d轨道上的电子排布 情况不发生改变 ,形成外轨型配合物。
对于CN-,CO等配位体而言,配位原子C的电负性小, 较易给出孤对电子对,对中心体的3d轨道发生重大 影响,从而使3d发生了电子重排,腾出能量较低的 内层(n-1)d轨道与ns,np轨道杂化,形成内轨型配合 物。
en
en
AACoe Nhomakorabea enCo
en
en
[Co(en)3])
A M
配位化合物

配位化合物一、配位化合物的定义往CuSO4的稀溶液滴加6mol/L的氨水不断振摇,开始时有天蓝色Cu(OH)2沉淀,继续再加氨水时,沉淀消失。
在溶液中检查不到Cu2+却只能检测到SO42-,推测生成了一种新物质,用酒精沉淀,再经结构分析:该物质为[Cu(NH3)4]SO4·H2O。
物质[Ag(NH2)]NO3,K2[HgI4]……,在水溶液中形成离子[Cu(NH3)4]2+,[Ag(NH2)]+,[HgI4]2-。
金属离子(或原子)与一定数目的中性分子或负离子结合成不易离解的复杂离子称为配离子。
含有配离子及配位分子的化合物统称为配合物。
配合物与复盐如明矾[KAl(SO4)2]12H2O不一样,不能相混。
二、配合物的组成以[Cu(NH3)4] SO4为例其组成可表示配位离子1.中心原子:一般为金属阳离子(原子),特别是过渡金属离子,Fe、Co、Ni、Cu、Ag、Au等。
2.配体:中心原子周围的分子或离子(可以是阴离子,也可以是中性分子)。
3.配位原子:配体中能向中心原子提供孤对电子的原子如NH3中的N原子,H2O中的O原子,CN-中的C原子,以N、P、O、S、C等原子居多。
配体又分:4.配位数:直接与中心原子相结合的配位原子总数。
以2、4、6较为多见。
在[Pt(en)2]Cl其配位数为4。
5.配离子电荷:中心原子和配位体电荷的代数和。
如[Cu(NH3)4]2+、[Fe(CN)6]4-。
三、配位化合物的类型1.简单配位化合物单齿配位体与单个中心离子(或原子)所形成的配合物K2[PtCl6][Fe(H2O)6]Cl5[Cr(H2O)6]Cl3Na[AlF6]2.螯合物由中心离子和多齿配体结合而成的环状配合物。
思考题:在制剂中作为金属离子络合剂使用的是A.NaHCO3B.NaClC.焦亚硫酸钠D.NaOHE.依地酸二钠【正确答案】E四、配位平衡Ks(K稳)称为配离子的稳定常数,Ks越大,说明生成配离子的倾向越大,配合物越稳定。
配位化合物
第二节 配位化合物的化学键理论
一、价键理论 (一)价键理论的基本要点 1.中心原子与配位体以配位键结合。配位 体的配位原子提供孤对电子,中心原子提供 空轨道容纳这些电子,形成配位键。
配位键 :M L
2. 成健过程中,中心原子外层能量相近 的轨道首先要进行轨道杂化,形成数 目相等、能量相同、具有一定伸展方 向的杂化轨道。
对价键理论的评价:
• 很好地解释了配合物的空间构型、
磁性、稳定性。
• 直观明了,使用方便。
• 无法解释配合物的颜色(吸收光谱)。
• 无法解释 [Cu (H2O)4 ]2 的稳定性。
Cu 2 (3d9 )
3d
4s
4p
[Cu (H2O)4 ]2
dsp2
第三节 配位平衡
一、配位平衡常数 配合物生成反应的平衡常数,称为配 合物的稳定常数 Ks (stability constant)。
inner sphere and outer sphere
中心原子和配位体组成配合物的内界, 用方括号表示内界,内界多为带电荷的配 离子,也有不带电荷地配位分子。配离 子以外的部分称为外界。
内外界之间以离子键结合 。
配合物的组成
配位键 配位原子 离子键
例:[ Cu ( N H 3 ) 4 ]
中心原子 配位体 配体数
第十二章 配位化合物
配位化合物简称配合物,是 一类非常广泛和重要的化合物。
在植物生长中起光合作 用的叶绿素,是一种含镁的 配合物;
叶绿素
含镁的 配合物
人和动物血液中起着输 送氧作用的血红素——含亚 铁的配合物;
血红素
含铁的 配合物
维生素B12——含钴的配 合物;
配位化合物大全

配位化合物配位化合物(coordination compound)定义简称配合物,为一类具有特征化学结构的化合物,由中心原子或离子(统称中心原子)和围绕它的称为配位体(简称配体)的分子或离子,完全或部分由配位键结合形成。
组成配合物由中心原子、配位体和外界组成,例如硫酸四氨合铜(Ⅱ)分子式为〔C u(NH3)4〕SO4,其中Cu2+是中心原子,NH3是配位体,SO4 2-是外界。
中心原子可以是带电的离子,如〔Cu(NH3)4〕SO4中的Cu2+,也可以是中性的原子,如四羰基镍〔Ni(CO)4〕中的Ni。
周期表中所有的金属元素都可作为中心原子,但以过渡金属最易形成配合物。
配位体可以是中性分子,如〔Cu(NH3)4〕SO4中的NH3,也可以是带电的离子,如亚铁氰化钾K4〔Fe(CN)6〕中的CN-。
与中心原子相结合的配位体的总个数称为配位数,例如K4〔Fe(CN)6〕中Fe2+的配位数是6 。
中心原子和配位体共同组成配位本体(又称内界),在配合物的分子式中,配位本体被括在方括弧内,如〔Cu(NH3)4〕SO4中,〔Cu(NH3)4〕2+就是配位本体。
它可以是中性分子,如〔Ni(CO)4〕;可以是阳离子,如[Cu(NH3)4〕2+ ;也可以是阴离子,如〔Fe(CN)6〕4-。
带电荷的配位本体称为配离子。
命名方法①命名配离子时,配位体的名称放在前,中心原子名称放在后。
②配位体和中心原子的名称之间用“合”字相连。
③中心原子为离子者,在金属离子的名称之后附加带圆括号的罗马数字,以表示离子的价态。
④配位数用中文数字在配位体名称之前。
⑤如果配合物中有多种配位体,则它们的排列次序为:阴离子配位体在前,中性分子配位体在后;无机配位体在前,有机配位体在后。
不同配位体的名称之间还要用中圆点分开。
根据以上规则,〔Cu(NH3)4〕SO4称硫酸四氨合铜(Ⅱ),〔Pt(NH3)2Cl2〕称二氯·二氨合铂(Ⅱ),K〔PtCl3(C2H4)〕称三氯·(乙烯)合铂(Ⅱ)酸钾。
配位化合物名词解释

配位化合物名词解释
配位化合物是一种金属与分子或原子间的稳定化合物,它们之间形成
复杂的化学键。
它们经常用作催化剂、抗生素、药物,以及工业催化
剂和电子装置。
1. 钴卟啉配位化合物:钴卟啉配位化合物是一种以钴为核心,同时有
四个卟啉分子构成的配位化合物。
它有着类似碳酸钴的结构,但它的
化学结构更加复杂。
它可以用作催化剂,可以加速苯酚的氧化。
它也
可以作为杀菌剂,可以对对霉菌和细菌有效抑制作用。
2. 氨基酸配位化合物:氨基酸配位化合物是金属和氨基酸结合的复杂
化合物,它通常把金属离子和氨基酸结合起来。
它们结构相似于金属键,并作为金属离子复合物的组成部分。
它们有助于金属离子在生物
体内被正确转移或保存,并参与金属离子催化酶(MEC)活性化。
3. 螺环配位化合物:螺环配位化合物是一种利用配位作用将金属和硫
衍生物配位成复杂结构的化合物。
它有以下特点:它具有超依赖性。
它高度稳定,不容易分解。
配位化合物具有独特的电磁性现象,这对材
料的性质有着重要作用。
螺环配位化合物常用于组装和检测生物物质,也可以用作药物作用的基础,能有效降低药物作用效率。
4. 氯酞配位化合物:氯酞配位化合物是氯酞分子和金属离子结合形成
的复合物。
它们结构类似磷酸盐,金属离子与氯酞分子的结合被称为配位作用。
氯酞配位化合物的性质类似于碳酸盐,它可以起到自组装作用,形成多孔和结构优美的复合材料,这些材料可以用于储存、催化剂和量子传输设备。
此外,它还可以用于光学传感器、磁性材料和绝缘材料等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(2) 形成配位键的必要条件是:配体L至少含有一
对孤对电子对,而中心体M必须有空的价轨道。
(3) 在形成配合物(或配离子)时,中心体所提 供的空轨道(s、p,d、s、p或s、p、d)必须首 先进行杂化,形成能量相同的与配位原子数目 相等的新的杂化轨道。 (4)轨道的杂化类型决定了配离子的空间构型、 配位数和稳定性。
B A B A A 面 式 B B A B B A A
经式(子午式)
[M(AB)3]也有面式和经式的两种异构体:
A B A B B 面 式 A B A A B A B 经 式
[MA3(BC)D](其中BC为不对称二齿配体)也有面式 和经式的区别。在面式的情况下三个A处于一个三角面 的三个顶点, 在经式中, 三个A在一个四方平面的三个顶 点之上。
4 配位异构
在阳离子和阴离子都是配离子的化合物中, 配体的 分布是可以变化的, 这种异构现象叫配位异构。如 [Co(NH3)6][Cr(CN)6]和[Cr(NH3)6][Co(CN)6]
[Cr(NH3)6][Cr(SCN)6]和Cr(SCN)2(NH3)4][Cr(SCN)4(NH3)2]
[PtII(NH3)4][PtⅣCl6]和[PtⅣ(NH3)4Cl2][PtIICl4]
NO2 en Co NO2 en en en NO2 O2N Co NO2 O2N en Co en
反式-[Co(en)2(NO2)2], 无旋光对映体
顺式-[Co(en)2(NO2)2] 有旋光对映体
2 配位化合物的化学键理论
一、价键理论 1.价键理论的基本内容: (1) 配合物的中心体M与配体L之间的结合,一般 是靠配体单方面提供孤对电子对与M共用,形成 配键M ←∶L,这种键的本质是共价性质的,称 为σ配键。
外界为简单离子,配合物可以无外界,但不可以无内
界。例如:Fe(CO)5 Pt(NH3)2Cl2
• 2.内界由中心体和配位体组成。
(1) 中心体:提供适当的空轨道的原子或离子, 绝大部分是d区或ds区元素。用M表示。 (2) 配位体 (L)(简称配体):提供孤对电子对 或π 电子的离子,离子团或中性分子。
看作带负电的点电荷,两者靠静电作用结合。
(2)过渡金属的中心离子的5个d 轨道在假想 的球形场(均匀电场) 中能量是简并的,中心离子和 配位体成键时,配体的静电场对中心离子的d 轨道 电子的不同排斥作用力,使d 轨道能级发生了分裂
(3)中心离子的d电子在分裂后的d轨道上重新排布,
优先占据能量低的轨道,进而获得额外的稳定化能,
②八面体配合物
在八面体配合物中, MA6和MA5B两种异构体:
A A A A A B 顺式 B A A B B A 反式
MA3B3型配合物也有两种异构体、一种是三个A占据八面体 的一个三角面的三个顶点, 称为面式;另一种是三个A位于正方 形平面的三个顶点, 称为经式
5 6 6
sp3d sp3d2 d2sp3
三角双锥 八面体 八面体
(5)内外轨型
用(n 1)d、ns、np杂化形成的配合物,称为内轨型配 合物。 用ns、np、nd杂化形成的配合物,称为外轨型配合物 。 稳定性:内轨型>外轨型
Ni 的sp 杂化:3d
2+ 3 8
Ni 的dsp 杂化
2+
2
4p 4s 3d
称为晶体场稳定化能(CFSE)
2.中心体d轨道的角度分布图
2
3、分裂能() : d轨道分裂后,最高d轨道的能量与最低d轨 道的能量差,称为分裂能()
o:(O: octahedral)八面体场d轨道的能级分裂能 o = 10 Dq
eg轨道 的能量为E eg , t2g轨道的能量为E t2g E eg - E t2g = 10 Dq = o (1) 2E eg + 3E t2g = 0 (2) 解得: E eg = 6 Dq E t2g = - 4 Dq (记住)
未成对电子数n与磁矩μ的关系
未成对 电子数 μ/B.M 0 0 1 1.73 2 2.83 3 3.88 4 4.90 5 5.92
Fe(CN)63+
[FeF6]3– sp3d2杂化, 八面体构型, 外轨型配合物
价键理论的局限性
(1) 只能解释配合物基态的性质,不能解释其 激发态的性质,如配合物的颜色。 (2) 不能解释离子为什么是平面四方几何构 型而Cu2+离子不是采取dsp2杂化?
3 键合异构
有些单齿配体可通过不同的配位原子与金属结合 , 得到不同键合方式的异构体, 这种现象称为键合异构。 如 [Co(NO2)(NH3)5]2+ 和 [Co(ONO)(NH3)5]2+ 前者叫硝基配合物, 是通过N进行配位的;后者叫 亚硝酸根配合物, 是通过O进行配位的。类似的例子还 有SCN-和CN-, 前者可用S或N进行配位, 后者可用C 和N进行配位。 从理论上说, 生成键合异构的必要条件是配体的两 个不同原子都含有孤电子对。如, :N≡C-S:-, 它的N 和S上都有孤电子对, 以致它既可以通过N原子又可以 通过S原子同金属相联结。
小,较易给出孤对电子对,对中心体的3d轨道发生
重大影响,从而使3d发生了电子重排,腾出能量较 低的内层(n-1)d轨道与ns,np轨道杂化,形成内轨型 配合物 。 • 注:形成内轨型配合物,d电子的排布违反洪特规则
•
(6)中心离子采取内外轨杂化的判据 - 磁矩 s n (n 2) n为未成对电子数
• 3、配位体
(1) 单基(齿)配体:配体中只含有一个配位原子; 例如:NH3、H2O、X- (2) 多基(齿)配体:配体中含有两个或两个以上 的配位原子。由单齿配体组成的配合物,称为简单 配合物;由多齿配体组成的配合物,称为螯合物 例如:en (乙二胺) H2NCH2CH2NH2
草酸根(ox2 )
A B A A D C 面式 B A D A A C 经式
2 光学异构
① 旋光异构现象 H 光学异构又称旋光异构。旋光异 H3C C* COOH 构是由于分子中没有对称因素(面和对 称中心)而引起的旋光性相反的两种不 OH 同的空间排布。当分子中存在有一个 不对称的碳原子时 , 就可能出现两种 COOH HOOC 旋光异构体。旋光异构体能使偏振光 C C 左旋或右旋 , 而它们的空间结构是实 OH HO H 物和镜象不能重合 , 尤如左手和右手 H H3 C CH3 的关系, 彼此互为对映体。 具有旋光性的分子称作手性分子。 数学上已经严格证明, 手性分子的必要和充分条件是不具 备任意次的旋转反映轴Sn。
3d 4s
4p
dsp 杂化
2
Ni(NH3 ) 2 4
Ni(CN)2 4
八面体构型
• 对于F-,H2O等配体而言,配位原子F,O的电负性大, 不易给出孤对电子对,所以对中心体的3d轨道上的 电子不发生明显的影响,因此3d轨道上的电子排布
情况不发生改变 ,形成外轨型配合物。
• 对于CN-,CO等配位体而言,配位原子C的电负性
2 溶剂合异构
当溶剂分子取代配位基团而进入配离子的内界所产 生的溶剂合异构现象。与电离异构极为相似, 最熟悉的 例子是: [Cr(H2O)6]Cl3 [Cr(H2O)5Cl]Cl2· H 2O [Cr(H2O)4Cl2]Cl· 2H2O 在配合物的内界,各含有6、5、4个配位水分子和 0、1、2个配位氯离子, 在配合物的外界各含有0、1、2 个溶剂合水分子和3、2、1个可电离的氯离子。这些异 构体在物理和化学性质上有显著的差异,如它们的颜色 分别为绿、蓝绿、蓝紫。
间完全靠静电作用结合,中心离子处在配体的包
围之中,两者的相互作用与离子晶体中正负离子 间的相互作用极为相似,因此把配体产生的电场 叫做晶体场。因为作为配体的负离子或极性分子 的负端指向中心离子,所以晶体场是负电场,他
对中心离子d轨道产生推斥作用,从而使其能量升
高。
1.理论要点
(1)把中心离子Mn+看作带正电的点电荷,配位体L
二、σ配键和反馈π键 Pauling电中性原理—在形成一个稳定的分子 或配离子时,其电子结构总是竭力设法使每 个原子的净电荷基本上等于零。 配位键是极性共价键,带有部分离子性。
反馈π键
反 馈 d π 键 σ
M C O
π*
Cr 3d6
d2sp3
d2sp3杂化 空轨道
协同效应
二、晶体场理论
• 晶体场理论认为:配合物中,中心离子和配体之
配位数
2 3 4 4 5
中心 杂化方式 sp sp2 sp3 dsp2 dsp3
构型 直线形 三角形 四面体 正方形 三角双锥
实例
+ [ Ag (NH3) 2] 2- [ Cu (CN) 3] 2+ [ Zn ] (NH3) 4 2- [ Ni (CN) 4] [ Fe (CO) 5] 2- [ Fe (SCN) 5] 2+ [ Co ] (NH3) 6 3- [ Co ] (CN) 6
含有四个不同配体的[MABCD]配合物有三种异构体, 这是因为B、C、D都可以是A的反位基团。
A M D B
记作 [M<AB><CD>]
C
A M
B
A M C
B D
D C [M<AC><BD>]
[M<AD><BC>]
其中的角括弧表示相互成反位。 不对称双齿配体的平面正方形配合物 [M(AB)2] 也有 几何异构现象, 如式中(AB)代表不对称的双齿配体。 A A A B M 顺式 M 反式 B B B A
[M(AA)3](如[Co(en)3])和[M(AA)2X2]型的六配位螯合物有 很多能满足上述条件, 其不对称中心是金属本身。
en Co en Co en
A A X M A X A X X
