新诊断及复发胶质母细胞瘤病例分享
脑胶质瘤放射治疗的体会

150-200mg/m2,口服,d1-5,治疗6周期。
以术前MRI T1强化像上显示的肿瘤区及术后MRI上显示的残留灶外放2.5cm为CTV1,外扩 3mm为PTV1,以术前MRI T1强化像上显示的肿瘤区及术后MRI上显示的残留灶外放1cm为 CTV2,外扩3mm为PTV2,给予PTV1 95%等剂量线6MVX DT5040cGY/28Fx后给予PTV2 95%等
病例3
患者,男,33岁,于2012.3.24在外院 诊断“左额叶实性占位”,行“左额开 颅肿瘤切除术”,术后病理:“左额叶” 间变型胶质细胞瘤, WHO III级;免疫 组化:GFAP(+)、Vim(+)、Ki-67标记指 数约10%。转我院,诊断:左额叶间变 型胶质细胞瘤(WHOIII级)术后。
侧额叶片状低密度影,低代谢,考虑治疗后改变。
进展后治疗
2013.3.6在福建省立医院行开颅左额叶 复发胶质瘤切除术,术后病理示:1.左 额叶肿瘤:胶质母细胞瘤(WHO IV级), 伴大片坏死。2.左额叶肿瘤表面脑组织: 送检组织中未见肿瘤细胞浸润。
术后行替莫唑胺密集方案化疗2周期。
目前第3周期化疗中。
MRI示:右额部硬膜下见新月形T1、T2双高信号影
MRS示:受出血影响,MRS基线不稳,未见明显 Cho峰升高和NAA峰降低
FLT-PETCT示:"右额叶胶质瘤术后"1、考虑术区前外侧切缘多 发残留。2、考虑肿瘤鞍区、鞍左旁及小脑幕播散。3、考虑术后
出血、积气并轻度大脑镰下疝。4、右额部硬膜下出血可能。
2. 同步化放疗结束后予替莫唑胺巩固化疗,替莫唑 胺150-200mg/m2,口服,d1-5,计划6周期。
胶质瘤病历分享

放疗联合PCV化疗(2级证据)
参加可行的临床试验(2级证据)
对于具有1p/19q联合缺失的间变性少突胶质细胞瘤,推荐进行放疗和PCV方案化疗(1级证据)
放疗加同步或者辅助TMZ辅助化疗(2级证据),或接受可行的临床试验(2级证据)
对于KPS<60的间变性脑胶质瘤,推荐进行放疗(短程放疗和常规分次放疗)(2级证据)
5
以人为本 以德为先 科学发展 追求卓越
对于低级别脑胶质瘤的化疗存在一定争议,主要包括:化疗的时机、化疗方案的选择 、化疗与放疗次序的安排等。
根据目前的循证医学证据,对于有高危因素(1.年龄>40岁,2.年龄<40岁,但伴有颅
高压、神经功能症状、术后残留、癫痫未控、未关注1p/19q)的低级别脑胶质瘤患者
以人为本 以德为先 科学发展 追求卓越
该患者预期预后差,若出现肿瘤进展
1.推荐再次手术 2.手术风险大者,可重复放疗,但要考虑相 关风险可考虑联合贝伐单抗+TMZ 3.弥漫或多灶复发,推荐化疗,但若有明显 占位效应的大病灶推荐手术
复发后化疗方 案选择
低级别脑胶质瘤复发后可选方案:①放疗加辅助PCV治疗;②放疗加TMZ辅 助治疗;③同步放化疗加TMZ辅助治疗;④对于以往没有使用过TMZ的患者 还可以使用TMZ;⑤洛莫司汀或卡莫司汀单药治疗;⑥PCV联合方案治疗; ⑦以卡铂或者顺铂为基础的化疗方案
MGMT启动子区甲基化者,建议接受TMZ治疗(2级证据),也可以采用姑息治疗
7
以人为本 以德为先 科学发展 追求卓越
对于WHO IV 级胶质瘤 年龄≤70岁 对于KPS≥60的患者,若存在MGMT启动子区甲基化, 推荐进行常规放疗加同步和辅助TMZ化疗(1级证据)、常规放疗加同步和辅助TMZ化疗加电场治疗(1级证据), 或接受可行的临床试验(2级证据) 对于MGMT启动子区非甲基化和甲基化情况不明确者,推荐进行放疗同步并辅助TMZ化疗(I级证据)、常规放 疗加同步和辅助TMZ化疗加电场治疗(1级证据)、单纯标准放疗(2级证据)或接受可行的临床试验(2级证据) 对于KPS<60的患者,推荐在短程放疗的基础上,加或者不加同步和辅助TMZ化疗(2级证据) 存在MGMT启动子区甲基化的患者,也可单独采用TMZ化疗(2级证据),或姑息治疗(2级证据) 年龄>70岁 推荐应用短程放疗(40 Gy/15 f/3 w)联合TMZ化疗(1级证据) 对于KPS<60分,建议采用短程放疗,MGMT启动子区甲基化者建议采用TMZ单药化疗,或姑息治疗
脑胶质瘤1例病例分享

ቤተ መጻሕፍቲ ባይዱ
头颅磁共振增强扫描
头颅磁共振增强扫描
头颅增强磁共振
三脑室区占位,考虑脑胶质瘤? 双侧丘脑异 常信号,水肿?脑胶质瘤?(三脑室区病变可 见轻度斑片状强化,病变边界不清)
病例分享
2019.10.25
基本情况
姓名:某 职业:务农 入院日期:2019-09-01
年龄:70岁 性别:男
主诉:认知障碍半月余,加重6小时余(代)
现病史
半月余前无明确诱因出现认知障碍,主要表现 为远期、近期记忆力差,出门不认路,无发热, 无头痛,无恶心呕吐,无言语不利、肢体活动障 碍、无意识障碍,至当地卫生院行头颅CT检查提 示:脑萎缩。给予拜阿司匹林肠溶片 每日1片治 疗,无明显好转。
文献复习
胶神经质瘤起源于神经上皮细胞组织内的胶质 细胞,是脑内最常见的原发肿瘤,占中枢神经 系统肿瘤的40%-50%,按照WHO中枢神经系 统肿瘤的分类,脑胶质瘤分为低级别胶质瘤( I、II级)和高级(III、IV级)两类。
大多数情况下脑胶质瘤随着肿瘤级别的增高, 肿瘤新生血管的通透性逐渐增加,因而肿瘤的 强化程度也逐渐增加;此外由于高级别胶质瘤 内新生血管分布不均匀,增强扫描常不均匀强 化。文献报道显示,有近30%的高级别胶质瘤 无明显强化或轻微强化。而约10%的低级别胶 质瘤表现为明显强化。
双侧侧脑室扩张并间质性脑水肿 左侧侧脑室旁点片状DWI高信号,考虑急性脑
梗死。 双侧基底节区腔隙性脑梗死,双侧额顶叶白质
脱髓鞘。 MRV未见明显异常
术后头颅CT
脑神经胶质瘤病历模板范文

脑神经胶质瘤病历模板范文英文回答:Nerve glioma, also known as brain glioma, is a type of tumor that originates from the glial cells in the brain. It is a relatively rare condition, but it can be quite serious and require immediate medical attention.In my case, I was experiencing persistent headaches and dizziness, which prompted me to seek medical help. After a series of tests, including a CT scan and an MRI, I was diagnosed with a brain glioma. The doctors explained that the tumor was located in a critical area of my brain and needed to be removed surgically.I underwent surgery to remove the tumor, which was a complex and delicate procedure. The doctors successfully removed the tumor, but they also had to remove a small portion of healthy brain tissue to ensure complete removal. The surgery was followed by a course of radiation therapyto target any remaining cancer cells.During my recovery, I experienced various side effects, such as fatigue, loss of appetite, and difficulty concentrating. However, with the support of my medical team and loved ones, I was able to overcome these challenges and gradually regain my strength.Despite the successful treatment, I still need to undergo regular check-ups and monitoring to ensure that the tumor does not recur. The doctors have informed me that there is a possibility of long-term side effects, such as cognitive impairment or neurological deficits, but they are closely monitoring my condition and providing necessary support.Overall, my experience with nerve glioma has been a challenging journey, but I am grateful for the medical advancements and the support I have received. It has taught me the importance of early detection and seeking medical help promptly. I am now more aware of the fragility of life and strive to make the most of every day.中文回答:脑神经胶质瘤,也被称为脑胶质瘤,是一种源自脑部胶质细胞的肿瘤。
脑胶质瘤诊断及鉴别

病例 2
讨论
病例 3
讨论
? ?
病例 4
患者刘国芬,女,53岁。 病 史 : 患 者 2 月 前 无 明 显 诱 因 出 现 阵 发 性 头
晕、头痛,为胀痛,以左侧颞顶部为重,并伴 左耳鸣,记忆力下降,无恶心及抽搐,无意识 言语障碍,对症治疗无好转,外院 MR 示颅内 占位。
MRI: T1等、低信号,T2高信号,50%单发、
多发强化
大脑胶质瘤病
(dysembryoplastic neuroepithelial tumor, DNET)
概述
胚胎发育不良性神经上皮肿瘤
皮质发育不良基础上良性局限性皮质内肿块(I级) 占20岁以下原发脑瘤的1~2%,局限癫痫发病
病理
脑、 下丘脑
病理
局限无包膜、膨胀无浸润生长,多有结节的
囊,25%钙化
影像学
结节的囊性肿块,结节、壁强化
毛细胞型星形细胞瘤
毛细胞型星形细胞瘤
毛细胞型星 形细胞瘤
成人型毛细胞型星形细胞瘤
男,70岁 [鉴别诊断] •淋巴瘤 •转移瘤 [误诊原因] •年龄 •部位
一、神经上皮组织肿瘤
少突胶质细胞肿瘤
T2WI
T1WI
FLAIR
DWI
增强
矢状位 冠状位
讨论
1、胶质瘤 2、淋巴瘤 3、转移瘤 4、肉瘤 5、其他
病例 5
CT平扫
病理
(右额顶叶)胶质肉瘤 (WHO Ⅳ)
中枢神经系统肿瘤组织学分类(1993年)
1.神经上皮组织肿瘤 2.颅神经和脊神经肿瘤 3.脑膜肿瘤 4.淋巴和造血组织肿瘤 6.囊肿和瘤样病变
多中心性胶质瘤
a~c 混合性少突—星形细胞瘤II级 d 纤维型星形细胞瘤II级
神经内科疑难病例讨论范文

神经内科疑难病例讨论范文
患者男性,50岁,近期出现头晕、头痛、呕吐等症状,体检发
现颅内压升高,进行脑CT检查发现右侧颅内有一颗直径约2cm的肿瘤。
患者接受手术切除后,病理检查结果为胶质母细胞瘤。
后续随访发现患者出现了多发性肺结节和骨转移病灶。
讨论:
胶质母细胞瘤是一种恶性肿瘤,通常出现在大脑的深部,如胼胝体、嗅球和第三脑室区域等。
患者的症状与颅内压升高相关,因此手术切除是必要的治疗手段。
然而,一旦出现多发性转移病灶,患者的预后大大降低。
胶质母细胞瘤的治疗通常包括手术切除、放疗和化疗等综合治疗。
对于多发性肺结节和骨转移病灶的治疗,一般建议采用放疗和化疗相结合的方式。
此外,针对转移病灶的具体位置和病情,也可以考虑局部手术切除等治疗手段。
总结:
胶质母细胞瘤是一种恶性肿瘤,患者的治疗需要综合考虑多种治疗手段。
对于多发性转移病灶的处理,需要根据患者的具体情况制定个体化的治疗方案。
需要注意的是,患者的预后通常与转移病灶的位置、数量和治疗效果等相关,因此需要加强随访和管理。
- 1 -。
胶质瘤误诊的真实案例

胶质瘤误诊的真实案例
以下是一位真实的胶质瘤误诊案例:
患者为一名30岁的女性,她开始感到头痛,失眠和精神恍惚。
她最
初看了家庭医生,被诊断为慢性头痛并给予了止痛药物。
然而,她的症状
没有改善,她开始觉得愈来愈疲倦和处理问题变得困难。
她前往眼科诊所,眼科医生诊断为视神经炎并推荐一名神经学家。
神经学家进行了全面的神
经学检查,但没有发现异常,并确认患者确实有头痛和视觉障碍。
然而,
他们认为这是由于艰苦的工作和家庭压力造成的,继续推荐让患者继续休
息和减轻压力。
随着时间的推移,患者的症状变得越来越严重。
她突然发生了癫痫发作,这提示医生进行头颅CT扫描。
扫描结果显示她患有胶质瘤,需要立
即手术切除。
患者接受了手术,并接受化疗和放疗治疗。
尽管治疗过后她
的症状得到缓解,但她的神经系统损害已经无法完全恢复。
这个案例凸显了胶质瘤误诊的问题和危害。
患者多次就医,但始终没
有得到正确的诊断和治疗。
建议患者和医生一起关注任何不寻常的症状,
并确保进行适当的检查和诊断,以便尽早发现和治疗潜在的神经系统问题。
胶质瘤病历

胶质瘤病历
患者:李先生
年龄:32岁
性别:男
诊断:胶质瘤
病历描述:
李先生于半年前开始出现头痛和头晕等症状,但一开始并没有太在意,以为是因为工作太忙的缘故。
但是症状越来越明显,开始出现视力模糊、恶心呕吐等症状。
去医院检查后发现他患了胶质瘤。
李先生被安排了手术来切除肿瘤,术后进行了放疗和化疗。
然而,他
的病情并没有得到有效的控制,尽管医生们尽了最大努力,但是肿瘤
仍在继续扩散。
胶质瘤是一种较为常见的脑部肿瘤,在治疗上相对困难。
李先生的案
例也说明了这一点。
他已经接受了不少次手术和治疗,但是仍然需要
继续接受医疗干预,以便在保持舒适的同时,延长生命。
如果癌细胞继续扩散,那么他的生活质量将会继续受到影响。
他将需
要更多的支持,包括医疗和社交支持,来帮助他度过这个难关。
同时,作为医护人员,他们需要尽最大努力来为他提供治疗和支持。
这可能包括与家人、病人本人和医疗团队交流,以帮助制定更好的治
疗计划和康复方案。
总而言之,李先生的案例是胶质瘤治疗上的一个难题。
但是,他的生命依然如我们每个人一样,有着不可估量的价值和意义。
我们应该通过不断创新和努力,尽最大努力为他和他的家庭提供支持,同时希望他能够度过这个难关,开启新的生命旅程。
颅内胶质母细胞瘤的影像诊断与鉴别诊断

女,72岁,反复头痛1年,加重2月余;3年前因“卵巢癌”行卵巢肿瘤切除术。
鉴别诊断-脑脓肿
• 有发热、意识障碍等症状;可有其他部位炎症性病变。 • 脓腔:DWI呈明显高信号。 • 强化区弥散不受限。 • 脑膜炎:软脑膜强化。 • 可见卫星灶(子灶)。
男,38岁,左上肢麻木1天余,不自主抖动2小时
早期表现。 • 病灶实性部分呈明显高灌注,rCBV、rCBF值增高。
SWI序列
• 利用磁敏感度差异和血氧依赖效应成像。 • 无需对比剂即可无创显示瘤体内出血和静脉
结构。 • 病灶内增生血管多,但不成熟,易出血。
1H-MRS波谱分析
• 活体内无创地评价胶质母细胞瘤的细胞代谢活动及生物能量学 情况,从分子水平对病变进行评估:
小结
• 中枢神经系统中最常见的恶性上皮性肿瘤,好发于45-75岁。 • WHO IV级肿瘤,进展快,易复发,预后差。 • 临床表现为颅压增高及非特异性的神经症状。 • 影像上病灶浸润生长,占位效应明显,常伴水肿,可跨中线;
坏死囊变多见;显著强化。
谢谢
节。
病理分型
• IDH-野生型: 巨细胞型胶质母细胞瘤。 神经胶质肉瘤。 上皮样胶质母细胞瘤。
• IDH-突变型。 • NOS:未能全面评价。
病理
• 瘤组织弥漫分布,细胞密度较高。 • 瘤细胞形态多样,异型性明显,核深染,分裂象多见。 • 伴大片坏死,坏死灶周围瘤细胞排列成栅栏状。 • 肿瘤间质内小血管、血管内皮细胞和血管平滑肌细胞明显增生,
颅内胶质母细胞瘤的影像 诊断与鉴别诊断
概述
• 又称多形性胶质母细胞瘤,是中枢神经系统中最常见的 恶性上皮性肿瘤,约占颅内恶性肿瘤的12-15%。
• WHO IV级肿瘤,进展快,易复发,预后差。 • 发病高峰年龄45-75岁,平均61.3岁,男性多见。 • 好发于额叶、颞叶、顶叶,还可见于枕叶、丘脑和基底
胶质母细胞瘤演示课件

02
诊断方法与标准
影像检查
1 2 3
计算机断层扫描(CT)
CT扫描可以显示肿瘤的位置、大小和形态,以及 与周围组织的毗邻关系。
磁共振成像(MRI)
MRI是诊断胶质母细胞瘤的首选影像学检查方法 ,能够更清晰地显示肿瘤及其与周围脑组织的关 系。
正电子发射断层扫描(PET)
PET扫描可以用于评估肿瘤的代谢活性和恶性程 度,有助于制定治疗方案和评估预后。
化学治疗
化疗药物选择
针对胶质母细胞瘤的化疗药物主要有 替莫唑胺等,可单独使用或联合其他 药物治疗。
化疗副作用管理
化疗可能导致恶心、呕吐、骨髓抑制 等副作用,需采取相应的预防和治疗 措施。
化疗方案制定
根据患者的具体情况制定个性化的化 疗方案,包括药物剂量、给药途径、 治疗周期等。
免疫治疗及靶向治疗
开颅手术活检
对于需要手术治疗的患者 ,可以在手术过程中获取 肿瘤组织样本进行病理学 检查。
免疫组化染色
利用特异性抗体对肿瘤组 织进行染色,有助于鉴别 不同类型的胶质母细胞瘤 和评估患者的预后。
03
治疗策略与方案
手术治疗
手术切除
通过开颅手术尽可能完全切除肿瘤,减少肿瘤负荷,为后续 治疗创造条件。
手术并发症
颅内出血
术后严密监测患者生命体征,及 时发现并处理颅内出血,必要时
行手术治疗。
脑水肿
术后给予脱水、降颅压等药物治 疗,减轻脑水肿症状。
感染
加强术后护理,保持伤口清洁干 燥,预防感染发生。
放疗和化疗相关并发症
放射性脑病
放疗过程中需严密监测患者神经系统症状,发现异常及时处理。
化疗药物毒性反应
根据化疗药物的不同,患者可能出现恶心、呕吐、脱发等毒性反 应,需给予相应的对症治疗。
胶质瘤复发与放射性坏死鉴别(优质医学)

精制课件
13
MRS
例1:马某某,术后18月增强
例1:马某某,术后18月MRS
精制课件
患侧:Cho/NAA: 0.799 Cho/Cr: 1.58 对侧:Cho/NAA: 0.822 Cho/Cr:1.39
放射性坏死 14
19
DWI
• 表观弥散系数(ADC)描述水分子的活动度,水分子弥散 受限的的部分,ADC值低。
• 放射性坏死、假性进展水分子运动弥散,在DWI上呈现低 信号(边缘高信号或者没有高信号)、ADC值高,而肿瘤由于 水分子在细胞内活动受限制,DWI高信号,ADC值低。
• ADC:1.49*10-3mm2/s,敏感性73.7%,特异性70%。 • 正常脑灰质ADC: (0.76±0.13)*10-3mm2/s • 正常脑白质ADC: (0.77±0.18)*10-3mm2/s
肿瘤复发
16
例4:张某某
2020/1/6
患侧:Cho/NAA: 0.828 Cho/Cr: 1.53 对侧:Cho/NAA:0.604 Cho/Cr:0.854
不典型波普 17
MRS
• 其中Cho,NAA,Cho/NAA,Cho/Cr为诊断胶质瘤复发最重要的 指标。
• 优点:无创,通过图像就能知道脑组织代谢变化。 • 缺点:对于肿瘤残留伴有坏死MRS鉴别较困难。 • 对于MRS不典型的病例,应前后对比MRS变化,观察Cho,
例2:韩某某,术后14月MRI
例2:韩某某,术后14月MRS
2020/1/6
患侧:Cho/NAA: 2.53 Cho/Cr: 2.58 对侧:Cho/NAA: 0.611 Cho/Cr: 0.957
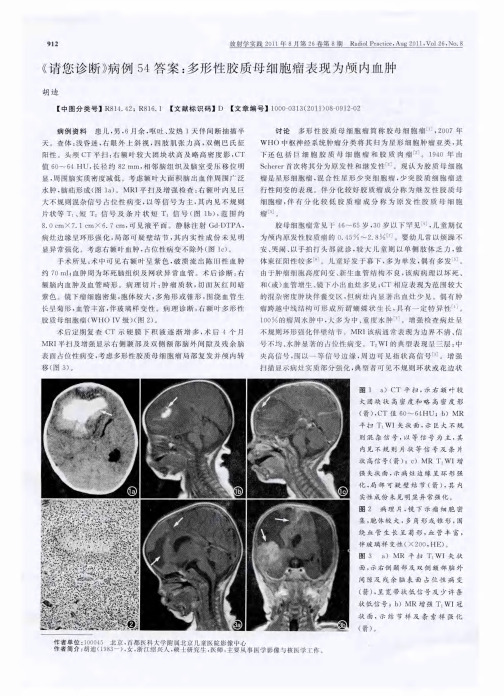
《请您诊断》病例54答案:多形性胶质母细胞瘤表现为颅内血肿
Rail rci , g2 1 , l2 , . பைடு நூலகம்do at e Au 0 1 Vo 6 No8 P c
91 3
边 缘 强 化 ]囊 变坏 死 区 无 强 化 。 , t 综 合 分 析本 例 患 儿 6月 余 , 灶 位 于 幕 上 , 血 肿 为 主 体 , 病 以 占位 效 应 明 显 , 水 肿 并 不 显 著 。C 表 现 为 典 型 高 密 度 病 灶 , 但 T MRI 扫 呈 现 不 同 时期 血 肿 信 号 , 强 后 仅 于 病 灶 边 缘 可 见 环 平 增
现 脑 积 水 或 硬膜 下 积 液 不 断 增 多 亦 可 作 为 脑 脊 液 转 移 的 间 接
般为 2 3 病灶 , 死常 见 , 出血少 见。临床表 现为颅 内 ~ 个 坏 但
压 增 高 和 局 灶 性 脑 功 能 障碍 。病 理 上 肿 瘤 质 软 、 面 灰 白或 粉 切
红 , 囊变 、 血 和坏死 小灶 。镜下 瘤 细胞 密集 、 体 较 大、 有 出 胞 呈 多 角 形 或 锥 形 、 绕 血 管 生 长 形 成 菊 形 , 有 短 粗 突 起 伸 入 血 围 并 管 内 ; 管 丰 富 , 壁 厚 薄 不 一 , 有 玻 璃 样 变 性 。免 疫 组 织 化 血 管 常
形 强 化 , 内 血 肿 坏 死 区无 强 化 。 因其 发 病 年 龄 、 位 、 像 学 其 部 影
[ 1 张贵祥 , 京龙 , 1] 赵 胡运 胜 , 颅 内肿瘤 手术 后 经脑 脊液播 散 的 等.
MRI 点 E] 中 国 医 学影 像 技术 ,0 6 2 () 3 43 7 特 J. 2 0 ,2 3 :8 —8 .
术后综合治疗高级别胶质瘤89例分析

多种 生物 学 功 能
生索 D类 似物, 如帕立 骨化醇 [, 5 临床 研究可 能更具 生存 优 ] 势。 维生素 D类似物与 R S抑制剂联用治疗 D A N还需大型临 床研究的肯定 . 此治疗模式值得期待。 参 考 文 献 [] 王海燕 肾脏病学.版. 1 3 北京: 人民卫生出版辛 ,08 12. t20 :43
本研究结果 支持以上讨论 ,活性维生 素 D联 合 A E 、 CI A B治疗 D R N可有效减少尿 蛋 白, 延缓 肾损 害 , 影响血压 不 时改善低 钙血症 , 防骨质 疏松 , 预 但对于 临床无低钙血症 的
患者 , 骨化 l 醇有 引起 高钙血症 的不 良反应 , 一 对于此类 患者 可考虑 使用对钙代谢影 响小而保 留了对 肾素抑 制作用 的维
[] G t H, ki K m t d t 1 Rnl l a cn -: 2 o Wau H,o auaA e a o s t . ea a h— t i4 p a in prao adu m e a i ne md—i i p pr ・ uci i t n npr yi mn ui ie n n o n o e b d g r ey o t Nprn x eh,069 ()2_5 eho pN pl 0 ,31:73・ E 2 [] 陈升, 3 于青・ R S A B 和活性维生素 D在糖尿病肾病治疗中的新
者经手术治疗 后采用不同术后治疗策 略的高级别胶质瘤 8 9
ESMO临床实践指南:新诊断和复发性套细胞淋巴瘤(MCL)的诊断、治疗及随访(2014)

内部资料仅供医学药学专业人士参考,禁止翻印及外传
MCL的分期
治疗根据疾病分期而不同,因此开始需进行彻底分期,特别是无肿块的Ⅰ和Ⅱ期少见病例
Ann Arbor 分期
分期
累及区域
Ⅰ(ⅠE) Ⅱ(ⅡE) Ⅲ(ⅢE, ⅢS) Ⅳ
巴瘤中占6%-9%。 • 近年来,该病的年发病率增加到最近的 1-2 / 100 000。 • MCL在男性中更常见,男女发病比例为3:1。
内部资料仅供医学药学专业人士参考,禁止翻印及外传
目录
• MCL的发生率与流行病学 • MCL的诊断、分期与预后 • MCL的治疗与疗效评估 • 个体化药物与随访
单个淋巴结区域或淋巴外部位Ⅰ(ⅠE)
膈膜同侧2个或更多淋巴结区域或至少1个淋巴结区域加单个 局部淋巴外部位(ⅡE) 膈膜两侧多个淋巴结区域或淋巴结构(如胸腺,韦氏环), 可伴随局部淋巴结外部位(ⅢE)或脾脏(ⅢS)
弥散性或广泛淋巴外器官受累
A 无症状;B不明原因的发热>38℃,夜间盗汗;或6个月内体重下降>10%
6.700-9.999
2
60-69
2-4
1.00-1.49
10.000-14.999
3
>70
-
≥1.50
≥15.000
每项预后因素每位患者可给0-3分,分数总计最高为11分。总分为0-3的患者为低危,4–5分的患者为中危, 6-11分的患者为高危。如果患者无法工作或卧床不起,ECOG 表现状态为2分(ECOG 2–4)。LDH 根据相 对于正常值上限的比例而评分。因此正常值上限为240 U/l, 分数界限为180, 240 及360 U/l。
胼胝体多形性胶质母细胞瘤1例

( 胼胝 体 ) 合 型 胶 质 瘤 。 混
讨 论
都 是骨质破 坏 或骨 质增 生和 破坏 。MR S 显 示 胆 碱/ 酸 比例 升 高 , 见 脂 肪 酸 族 肌 可
代谢 。
胶 质 母 细 胞 瘤 在 神 经 上 皮 性 肿 瘤 中 占 2 . % , 报 告 占颅 内肿 瘤 的 1. % 。 23 有 02 仅 次 于 星 形 细 胞 瘤 而 后 第 2位 。本 病 主 要发生于成人 , 尤其 3 0~5 0岁多见 , 男性 明显 多 于 女 性 , 发 年 龄 为 4 好 0~4 5岁 。 胶 质 母 细 胞 瘤 位 于 皮 质 下 , 浸 润 性 生 呈 长, 常侵 犯 几 个 脑 叶 , 侵 犯 深 部 结 构 , 并 还 可 经 胼 胝 体 波 及 对 侧 大 脑 半 球 。发 生 部
漫性 浸润性生 长 , 恶性程 度高 , 界卫 生 世 组 织 ( O) 级 属 4级 , 于 瘤 细 胞 高 WH 分 由 度 间变 和 不成 熟 性 , 上 血 管 新 生 赶 不 上 加
肿 瘤 迅 速 生 长 的需 要 , 以瘤 内 常有 广 泛 所 坏 死 、 变 及 出血 。发 生 部 位 以额 叶 最 多 囊
图 1
M I 扫及 增强 : 平 扫示 : 胝体 R平 ① 胼 膝 部 及 体 前 部 见 大 片 状 略 长 、 长 1 略 、 2
混 杂信号 , 边界 不清 , 围伴有 大 片状水 周 肿 , 向 后 突 入 双 侧 脑 室 体 部 , 侧 脑 室 并 双 对 称 性 扩 大 。② 增 强 示 : 信 号 影 呈 厚 壁 该 囊 状 显 著 强 化 , 壁 不 规 则 , 见 壁 结 节 囊 未 强化 , 该处 大 脑 镰 及 双 侧 侧 脑 室 前 角 壁 亦
肿瘤电场治疗联合多柔比星及放化疗治疗复发胶质母细胞瘤1例报道

doi:10.3971/j.issn.1000-8578.2023.22.1475肿瘤电场治疗联合多柔比星及放化疗治疗复发胶质母细胞瘤1例报道李宏博,蒋念,李学军Tumor-treating Fields Combined with Doxorubicin and Chemoradiotherapy in Treatment of Recurrent Glioblastoma Multiforme: A Case Report LI Hongbo, JIANG Nian, LI XuejunDepartment of Neurosurgery, Xiangya Hospital, Central South University, Changsha 410008, ChinaCorrespondingAuthor:LIXuejun,E-mail:****************.cnFunding: National Natural Science Foundation of China (No. 82270825, 81770781)Competing interests: The authors declare that they have no competing interests.关键词:肿瘤电场治疗;多柔比星;替莫唑胺;Li -Fraumeni 综合征;胶质母细胞瘤中图分类号: R739.41 开放科学(资源服务)标识码(OSID): 收稿日期:2022-12-13;修回日期:2023-04-12基金项目:国家自然科学基金(82270825, 81770781)作者单位:410008 长沙,中南大学湘雅医院神经外科通信作者:李学军(1972-),男,博士,主任医师,主要从事颅底肿瘤相关研究,E-mail: ****************.cn ,ORCID: 0000-0001-6406-4423作者简介:李宏博(1997-),男,硕士在读,住院医师,主要从事神经肿瘤的临床研究,ORCID: 0000-0002-0720-6744·病例报道·0 引言Li-Fraumeni 综合征是一种罕见的常染色体显性遗传肿瘤综合征,以多种肿瘤发病高风险为特征。
脑胶质瘤病例分享

Chang SM提出的一个判定是否是放射治疗诱发的肿瘤 的一个标准:
新发肿瘤起源于原发肿瘤的放射治疗区域。
在放射治疗前并未出现该新肿瘤,且放射治疗与新发肿瘤的 发现之间有一段合理的间期,一般为数年。
原发肿瘤和新发肿瘤之间存在着组织学差异。
问题:
无症状的海绵状血管(瘤)畸形(CCM)是否需要手术治疗? 何时手术?
大脑半球海绵状血管畸形(CCM)选择伽马刀治疗合适吗? 效果如何?
伽马刀治疗是否为脑胶质瘤发生的诱因?
海绵状血管畸形(CCM)是否是胶质瘤前病变?部分CCM 是否可转变成胶质瘤?
手术的刺激是否会诱发脑胶质瘤?
无症状的CCM是否需要手术,何时手术
其中有两例间变性胶质瘤是 发生于CCM切除之后的术区。
∆两种肿瘤同时发生的原因,据猜测可能有:
共同的发病因素(如基因易感性CCM1,CCM2, CCM3,放射线 暴露,病毒感染。)
CCM可以引起附近脑实质的胶质增生反应,引起出血、胶质 细胞去分化、增生等。
畸形血管会分泌产生生长因子、细胞因子,可能导致胶质瘤 发生。CCM高表达VEGF,而VEGF在胶质瘤的发生、发展中 有促进作用。
文章推论:
M的基因如:CCM 、KRIT1在gamma knife作用下发生
突变,为胶质瘤的形成创造可能性
M为突变的胶质细胞增殖创造了内环境(如表皮生长 因子EGF的分泌),有学者报道发现了CCM中可见少突胶 质细胞增殖的现象
3.并非所有CCM在gamma knife等放射治疗作用下都转变成 胶质瘤,故应假设是部分CCM的亚型更容易转变
瓣,手术顺利,术后肿瘤标本送病理检查
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2011-1-31转回当地医院继续治疗。
术后11个月再次入院时头颅MRI-----左侧枕叶胶质瘤术 后复发,右侧小脑多发转移灶。
复发肿瘤切除术后第5天复查头颅CT ---左侧颞角囊肿较术前明显缩小
同步放化疗5年生存率 明显高于单纯放疗
讨论
替莫唑胺对年轻患者,尤其是MGMT基因启动子甲基化的患者疗效更为显著。
MGMT甲基化(+)
MGMT甲基化(-)
讨论
目前对于复发恶性胶质瘤的治疗尚无定论。
大约有20%~25%的复发患者可以再内压情况以及患者基 本情况综合考虑。
2011-1-31转回当地医院继续对症支持治疗,于???去世。
讨论
恶性胶质瘤诊断的“Gold Standard”------病理学诊断 分子生物学标记对恶性胶质瘤的治疗、疗效观察及预后判断都有积极作用 如:MGMT,1p/19q,IDH
讨论
对于年龄≤70岁,身体状况允许的胶质母细胞瘤患者,术后应常规行放射治
目前在许多国家,包过美国和瑞士,贝伐珠单抗已经被批准用于临床治 疗复发胶质母细胞瘤。
结论
放疗是胶质母细胞瘤的主要辅助 放疗 治疗,行替莫唑胺同步放化疗及
后续辅助化疗效果更佳。
化疗
综合治疗
化疗是胶质母细胞瘤治疗的重要补 充, MGMT基因启动子甲基化的患 者疗效更为显著。
手术
手术治疗是胶质母细胞瘤 的首选手段,其基本原则 是在保护脑功能的前提下, 尽可能彻底地切除肿瘤组 织。
; 疗+替莫唑胺同步及辅助化疗
Roger Stupp, Monika E Hegi, Warren P Mason,et,al. Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial. Lancet Oncol 2009; 10: 459–66.
瘤切除术,术中发现肿瘤供血丰富。术中冰冻提示:胶质 瘤IV级。术中将肿瘤近全切除。术后予止血、抗炎、补液 、脱水降颅压、预防癫痫发作、护胃、激素抗脑水肿等对症 支持治疗。2010.2.2术后病理报告:(左枕叶)胶质细胞 瘤(WHO:IV级)。 患者术后恢复良好,于2010-2-4头部切口拆线,2010-2-8始 接受泰道同步放化疗(泰道140mg/日*42天,病灶放射 30*2Gy)。 2010-3-31复查头颅MRI提示“ 左侧枕顶叶胶质瘤术后改变 ,未见明确复发及转移灶。”
2010-1-22头颅MRI增强:左侧枕叶占位,胶质瘤首先考虑,肉瘤不能除外。
头颅MRI平扫---左侧枕叶见片状异常信号影,T1呈混杂等低信号,
T2呈混杂高信号,中线结构稍右偏。
头颅MRI增强------可见病灶呈多发环形明显强化
入院诊断:左侧枕叶占位性病变,胶质瘤首先考虑 治疗经过:排除手术禁忌症后于2010.1.27全麻下行左枕叶肿
2.排除手术禁忌症后于2010-12-28全麻下行左枕叶复发胶质瘤切除+囊肿 内Ommaya囊埋置术,手术经过顺利,术后神志较术前明显好转,复查 头颅CT提示左侧颞角囊肿较术前明显缩小。
术后病理提示:弥漫胶质细胞增生,灶区可见瘤巨细胞形成伴星状肿 瘤性坏死形成,病理诊断:左枕叶胶质细胞瘤(IV级)。 3.术后一周左右患者神志再次恶化,呈嗜睡状,复查头颅CT(2011-1-10) 提示脑室增大。
新诊断及复发胶质母细胞瘤病例分享 ------诊断与治疗探讨
浙江大学医学院附属第一医院神经外科 俞建波
病例简介
患者,男,56岁,因“头晕伴记忆力下降1月 ”于2010.01.22入院。 入院查体:无明显阳性体征。 辅助检查: 2010-1-21头颅MRI平扫: 左侧枕叶占位,胶质瘤首先考虑,建议增强扫描。
2010-4-1病愈出院,门诊随访。
术后头颅CT平扫
放化疗后(术后2个月)复查头颅MRI平扫+增强 ------未见明确复发及转移灶
门诊随访(术后4个半月)头颅MRI平扫+增强+FLAIR ------术区周围水肿,未见异常强化
门诊随访(术后6个月)头颅MRI平扫+增强+FLAIR ---病灶边缘环形强化,肿瘤复发待排。
2010.12.23患者因“胶质瘤术后11月余,右侧肢体活动障碍3月”再次入院。
病史:3月前患者出现右侧肢体活动障碍,至丽水市中心医院就诊,查头颅MRI (2010.9.28)示:“左侧颞枕叶胶质瘤术后改变,复发可能”。予以甘露 醇、激素等脱水降颅压治疗后病情未见明显好转,并逐渐出现神志淡漠。为 求进一步治疗转我院。
复发肿瘤切除术后第12天复查头颅CT ------脑室增大
复发肿瘤切除术后第17天,右侧脑室腹腔分流 +左侧囊腔穿刺引流术后第3天复查头颅CT
病例分析
新诊断胶质母细胞瘤:2010-01-22 患者术前有神经系统功能缺失伴颅内压增高症状; 头颅MRI检查提示左枕叶占位性病变(T1混杂等低信号,T2混杂高信号, 增强可见多发环形明显强化); 开颅手术切除病灶,病理检查提示(左枕叶)胶质细胞瘤(WHO:IV级)。 术后第12天开始接受泰道同步放化疗(泰道140mg/日×42天,病灶放射
30 × 2Gy)。 术后恢复良好,门诊随访。
复发胶质母细胞瘤:2010-12-23 患者术后第8月出现肢体功能障碍症状; 头颅MRI提示:左侧枕叶胶质瘤术后复发,右侧小脑多发转移灶; 再次行复发胶质瘤切除+囊肿内Ommaya囊埋置术,术后出现脑积水, 行V-P 分流术。 术后病理提示(左枕叶)胶质细胞瘤(WHO:IV级)。
入院查体:神志淡漠,右侧肢体肌力0级,左侧肢体肌力III级,右侧肌张力减 退。
辅助检查:
当地医院头颅MRI(2010.9.28):“左侧枕叶胶质瘤术后改变,复发可能”。
入院诊断:左侧枕叶胶质瘤术后复发 诊治经过: 1.入院后复查头颅MRI(2010-12-25)提示:左侧枕叶胶质瘤术后复发,
病灶累及三角区后角伴左侧颞角扩大;右侧小脑多发转移灶。
