2016年药品不良反应分析报告
医疗安全不良事件分析报告
2016年度医疗(安全)不良事件分析报告XXXXXX人民医院质控科随着人们法律观念和维权意识日益增强,对医护人员的职业道德、技术水平及服务质量提出了更高的要求。
为进一步加强医疗安全管理,促进医疗质量的持续改进,保障医疗安全,进一步明确以“病人安全”为导向,自从2014年我院制定了非处罚性的《医疗安全不良事件报告制度及工作流程》以来,各科室严格监控和管理,按规定及时、主动上报,2016年度各科室上报不良事件及药品不良反应312例,未发生重大安全事件。
现将各科室报告医疗安全不良事件进行分析,以利于消除安全隐患,防范医疗事故及纠纷,不断提高医疗质量。
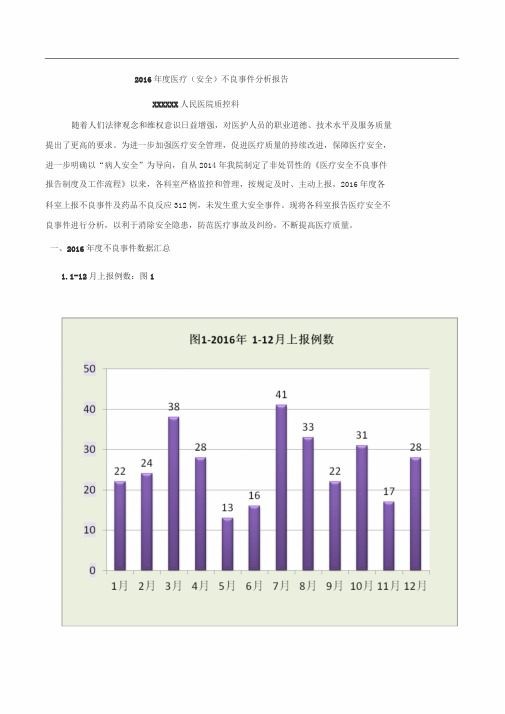
一、2016年度不良事件数据汇总1.1-12月上报例数:图12.医疗安全不良事件科室分布:图23.不良事件分类:4.2016年与2015年不良事件对比,见图4图42016年与2015年各类不良事件对比4.各类不良事件1-12月趋势,见图5图5—2016年1-12月趋势图5.不良事件发生场所,见图6二、2016年各类不良事件汇总分析(一)医疗安全不良事件1.医疗不良事件分类:图7—-医疗不良事件分类柏拉图2.医疗不良事件分级:3.医疗安全不良事件小结:医疗安全不良事件中,由医生上报7例,护士上报19例。
绝大多数属于Ⅳ级事件,占73%,主要是医嘱事件,Ⅲ级事件占27%,主要有医疗处置事件、用药错误等。
医嘱事件16例,其中录错药物数量5例、录错药物剂量4例、漏录电脑4例、录错患者3 例;医疗处置事件4例,包括胸腔闭式引流操作2例,导尿操作2例;用药错误2例,包括用法错误、提前用药各1例;跌倒事件2例,均为脑血管疾病患者夜间坠床;意外事件1例,为住院处录入身份信息错误;输液反应1例。
(二)护理安全不良事件1.护理不良事件分类:2.护理不良事件分级3.2016年与2015年护理不良事件对比,见图11图11—2016年与2015年护理不良事件对比4.护理不良事件小结:从图9、图11中看出:用药错误共发生27例,比2015年增加8例,增长率42%;坠床/跌倒事件23例,比2015年增加11例,增长率91%;管路事件13例,比2015年减少9例,降低40%;意外事件15例,包括:床档致皮肤挫裂伤、皮肤烫伤、手术物品不齐全、服药伤害、患者走失等;操作处置事件12例,包括静脉输液操作4例、导尿操作2例、输液泵操作不当2例、肾透析操作2例;标本采集事件9例,包括用错试管、血标本溶血、试管错误、血标本送检延误等。
热毒宁注射液不良反应38例报告分析
热毒宁注射液不良反应38例报告分析发表时间:2016-06-16T15:41:06.090Z 来源:《医师在线》2016年3月第5期作者:王鹏军1,曲韶丽2[导读] 热毒宁注射液是一种纯中药制剂,其功效为清热,疏风,解毒。
王鹏军1,曲韶丽2(1.烟台市牟平区检验检测中心 264100;2.烟台市牟平区高陵镇中心卫生院 264100)【摘要】目的:对热毒宁注射液不良反应(ADR)38例报告进行分析,探讨其ADR的特征,为临床安全用药提供参考。
方法:收集4家公立医院2013年1月至2015年9月的门诊发热患者应用热毒宁注射液6900例,对发生的ADR特征进行分析。
结果:应用热毒宁注射液6900例患者中发生ADR 38例,占0.55%,主要表现为发热(体温升高或不降)、药物过敏性性皮疹、恶心、腹痛、腹泻等症状,临床症状一般较轻,未见严重的ADR发生,38例患者中男性18例,女性20例。
结论:静脉注射热毒宁注射液时,要严格控制静滴速度,严密观察患者反应,以避免或减少ADR的发生,保证临床用药安全。
【关键词】热毒宁注射液;不良反应;用药安全热毒宁注射液是一种纯中药制剂,其功效为清热,疏风,解毒。
临床上用于呼吸道感染(外感风热证)所致的高热、微恶风寒、头痛身痛、咳嗽、痰黄等症。
由于该制剂在临床上的广泛应用,ADR的报道也日益增多【1】。
笔者收集2013年1月至2015年9月4家医院(烟台毓璜顶医院,烟台业达医院,烟台市蓬莱市人民医院,烟台市烟台山医院)发热门诊使用热毒宁注射液发生ADR的病人38例,对发生的ADR 特征及其原因进行分析,现报告如下。
1、一般资料1.1 患者基本情况收集2013年1月至2015年9月4家医院应用热毒宁注射液治疗的发热患者6900例,发生ADR 38例。
其中男性患者18例,女性患者20例。
发生ADR的患者年龄为3.3-61.2岁,平均年龄为43.5岁,就诊原因均为发热,体温范围为38.3-39.4℃。
26例热毒宁注射液不良反应报告

热毒宁是一种中成药制剂,主要是由青蒿、栀子、金银花三味中药提取精制而成,具有清热解毒、疏风的作用,可快速退热,具有较强的抗病毒作用,在外感风热引起的咳嗽、感冒、急性支气管炎、上呼吸道感染等疾病中应用十分普遍[1]。
近些年来,随着中成药制剂的不断应用与推广,热毒宁注射液应用日益普遍,其抗病毒功效受到了临床的认可与青睐,但相应的不良反应也随之出现。
热毒宁注射液中含有青蒿素、黄酮类、绿原酸等化学物质,可能引起机体过敏反应,引发一系列不良反应,降低患者治疗效果。
本研究选取26例于医院应用中成药制剂热毒宁注射液治疗后出现不良反应的患者,探讨热毒宁注射液不良反应发生情况及预防措施,现报道如下。
1 病例特征以2016年1月- 2021年9月在医院应用中成药制剂热毒宁注射液治疗后出现不良反应的患者26例为观察对象,其中女性患者8例,男性患者18例;年龄在1~64岁,年龄均值11.04±1.65岁;原患疾病:呼吸道感染7例,发热4例,支气管炎4例,上呼吸道感染3例,口腔感染2例,扁桃体炎1例,抽搐1例,呕吐1例,腹痛1例,带状疱疹1例,会厌溃疡1例。
2 结果26例不良反应中,皮疹、瘙痒9例,占有比率34.62%;皮疹7例,占有比率26.92%;寒战3例,占有比率11.54%;瘙痒1例,占有比率3.85%;荨麻疹1例,占有比率3.85%;恶心、呕吐1例,占有比率3.85%;咳嗽1例,占有比率3.85%;心悸1例,占有比率3.85%;心悸、胸闷1例,占有比率3.85%;头晕、胸闷1例,占有比率3.85%。
26例患者经停药、换药等处理后均好转,无死亡病例。
3 体会热毒宁注射液成分主要为青蒿、栀子、金银花,其中青蒿为君药,作用为透散肌表、清热凉血,对风热邪毒、入里热邪等疾病治疗的效果确切;栀子为佐【摘要】 目的 研究分析临床中应用中成药制剂热毒宁注射液的不良反应发生情况及预防措施。
方法 选取2016年1月- 2021年9月于医院应用中成药制剂热毒宁注射液治疗后出现不良反应的患者26例为研究对象,总结分析患者不良反应发生情况,制定切实可行的预防措施。
护理不良事件错误给药RCA分析
精品文档考试教学资料施工组织设计方案七例给药错误不良事件根本原因(RCA)分析2016年1月至6月共上报护理不良事件共33例,其中给药相对不良事件共7例,占21.2%,均无造成后果事件。
为了尽可能减少用药失误,现对7例给药错误事件进行RCA分析,为安全、有效、合理地使用药物,保障患者药物治疗安全。
一、RCA前的准备1、成立RCA小组督导:杨毅华组长:彭雪金组员:缪燕灵曹齐凤陈慧郭素云桂辉琼迈进张友根谢福丽王蕾杨燕妮2、问题定义:2016年上半年7例给药错误不良事件二、事件资料1、一般资料(见表1)2、事件过程资料(见表2)3、给药事件相关因素资料三、资料分析对7例给药不良事件的:药品类型(图1),给药途径进行分类(图2),参与护士层级(图3),工作总年资(图4),该科室工作年资(图5),发生时间段(图6),发放患者错误(图7)给予统计分析。
图1分析结果示:中药占57.1%,中药外包装欠规范,用法及姓名等标识不够明显,导致外用中药误为口服;护理人员未能严格落实查对制度,无用二种以上有效识别核对方法进行查对,导致发放错误。
图2分析结果示:口服给药途径占74.1%,护理人员在给药前未严格执行查对制度,未能严格落实床边工作制度,未能监督服药到口。
图3图4图5图3、4、5分析结果:1、发生不良事件护士主要分布在N1级及N2级护士中。
2、从中可见发生不良事件护士在该科室工作年资在半年以上占57.1%。
我院正处在业务发展期,截止6月21日,上半年住院病人数达5191人,比去年同期增加2032人,增长64.32%。
今年4月新开疼痛科,原有分增科室(内三病区、骨伤科及外妇病区)床护比平均1:0.26,护理部从2016年1月至6月共新聘人员48人。
在新入职护士人员多且护理人力资源紧缺,住病人数过度饱和的情况下,科室只能完成基本的护理工作,对新入职人员未接触的新业务、新技术的临床带教、培训都存在落实不到位,容易发生不良事件。
398例精神类药物不良反应报告分析

3 4 ADR 主要的临床表现 本统计结果显示ꎬ抗菌药物不
21 23% ) ꎻADR 累及系统以消化系统居多( 占 49 以上(57 49% ) ꎬ主要临床表现为皮疹、瘙痒、斑丘
导临床用药提供参考ꎮ
良反应累及多个系统或器官ꎬ但皮肤及其附件位居首位ꎬ占总
况ꎬ促进精神类药物的临床合理应用ꎮ 方法 收集我院 2016 年 10
月至 2018 年 10 月上报的与精神药品相关的 ADR 报告 398 例ꎬ分别
从患者的性别、年龄、相关药物品种、临床表现及转归情况等进行统计
和分析ꎮ 结果 发生 ADR 患者中ꎬ女性患者居多ꎻ年龄在 18 ~ 30 岁
的患者较多ꎻ共涉及相关药品 41 种ꎬ以奥氮平引起的 ADR 最多( 占
极遵循世卫组织“ 能口服不肌注ꎬ能肌注不静脉” 的用药原
则ꎮ
398 例精神类药物不良反应报告分析
陈思思1 ꎬ钱丽梅2 ꎬ王 俊1 (1 湖州市第三人民医院
药剂科ꎬ浙江湖州 313000ꎻ2 杭州市第七人民医院
药剂科ꎬ浙江杭州 310013)
摘要:目的 分析精神病专科医院药物不良反应( ADR) 的发生情
品在正常用法用量下出现的与用药目的无关的或意外的有害
明书用药ꎬ密切监测患者病情和用药情况ꎮ 作为药学工作者ꎬ
反应 〔1〕 ꎬ而药师对于把控患者的用药安全有着不可推卸的责
ADR 的危害性和监测意义ꎮ 加强对患者的用药交代和用药
理性有着至关重要的作用ꎮ 本文将对湖州市第三人民医院
我们 应 该 做 好 ADR 的 宣 传 和 培 训 工 作ꎬ 使 医 护 人 员 了 解
〔6〕 董迪ꎬ崔蔚ꎬ陈宁ꎬ等 我院头孢菌素相关用药安全问题分析〔 J〕
中国药师ꎬ2017ꎬ20(1) :121 ̄123
药品质量信息20162016药品质量信息收集

药品质量信息20162016药品质量信息收集药品质量信息2016:2016年药品质量管理自查报告2016年度药品质量管理自查报告根据药监局领导下发的2016年医疗机构药品安全专项整治工作的通知,我院按照师药监局培训的各项内容进行了自查,现将自查结果汇总如下:一、领导重视,管理组织健全我院成立了医院药事管理委员会,负责监督、指导本机构科学管理药品和合理用药。
药剂科设立了了药品质量管理人员负责人具体负责药品质量管理的管理工作,确定各岗位职能,并建立健全药品质量管理各环节制度。
二、药品的管理1.我院药品采购目录根据《国家基本药物目录》及结合临床实际使用确定,并经医院药事管理委员会审核通过,由药剂科按照目录进行采购。
2.建立供货单位档案,严格审核供货单位及销售人员的资质。
确保从有合法资格的企业采购合格药品。
3. 根据《药品管理法》及相关药品法律法规并结合我院实际制定了相关的药品质量管理制度:包括药品的购进、验收、养护制度、处方的调配及处方管理制度、近效期药品管理制度、特殊药品管理制度、药品不良反应报告制度等。
4.我院按照医院的规模分别设立了门诊药房与药库,库房卫生整洁、布局合理,按照药品的储存要求将药品进行分库储存,配备了温湿度计、鼠药等养护设施。
5.药库按照药品GSP的管理规定划分为待验区、退货区、不合格区、合格区等。
库房分为常温库、阴凉库、按照药品的储存要求将药品进行分库分柜进行储存。
6.按照药品的储存要求分别储存于相应的库中,保证了药品的质量。
冷藏柜2-8℃、阴凉库不高于20℃、常温库为0-30℃、各库房的相对湿度保持在45%-75%之间。
7.不合格药品存放在不合格区内,并登记好不合格台账。
8.在库药品按照批号远近集中存放、药品堆垛与屋顶、墙壁之间的间距不小于30CM、与地面间距不小于10CM、药品垛间有一定距离。
9.实行药品效期储存管理,对效期不足6个月的药品挂牌警示。
报各使用科室进行促用。
10.药库每日上午、下午定时对在库药品进行巡查与养护,进行温湿度检测并做好记录,如超出规定范围,及时采取调控措施。
4例中药配方颗粒不良反应报告及分析

4例中药配方颗粒不良反应报告及分析梅安存;孙静;严学玲;朱瑞琳;朱亚宁;张鹏【摘要】目的:正确认识中药饮片的安全性,减少不良反应的发生.方法:对2016年6月-12月某院发生的4例中药配方颗粒引起的不良反应进行分析.结果:中药配方颗粒可引起胃肠道不良反应,主要以不同程度的腹痛、腹泻为临床表现.结论:关注中药饮片不良反应,加强用药交待,提高用药安全性.【期刊名称】《山西中医学院学报》【年(卷),期】2017(018)006【总页数】2页(P70-71)【关键词】中药配方颗粒;不良反应;用药安全【作者】梅安存;孙静;严学玲;朱瑞琳;朱亚宁;张鹏【作者单位】安康市中医医院,陕西安康725000;陕西省人民医院,陕西西安710021;陕西省人民医院,陕西西安710021;陕西省人民医院,陕西西安710021;陕西省人民医院,陕西西安710021;陕西省人民医院,陕西西安710021【正文语种】中文【中图分类】R288近几年,中药配方颗粒作为一种新剂型进入大众视野,它弥补了传统中药饮片体积大、携带不方便、需要煎煮的缺点,同时也继承了中医药特色和优势。
中药配方颗粒是以炮制规范的单味传统中药饮片为原料,根据临床用药要求经现代制药工艺加工制成的可以即冲即饮的颗粒剂。
早在2001年《中药配方颗粒暂行规定》中就已正式将中药配方颗粒纳入中药饮片管理。
目前,因其质量可控、使用方便、疗效可靠在临床上大受欢迎。
据报道,2009年我国中药配方颗粒销售量超10.9亿[1]。
中药配方颗粒由中药饮片加工而成,那么中药饮片有的不良反应,配方颗粒也可能有。
虽说中药相对于西药不良反应小,但也不乏严重不良反应。
在2016年国家药品不良反应监测年度报告中就显示全国药品不良反应/事件(ADR/ADE)呈数量增长趋势。
按怀疑药品类别统计,中药占到16.9%。
其中中药注射剂53.7%,口服制剂38.6%。
而据查阅文献,目前对于中药配方颗粒的不良反应报道较少[2-3],本文旨在对医院4例由中药配方颗粒引起的不良反应进行分析,以便引起人们的关注。
62例中药不良反应分析 谢江生

62例中药不良反应分析谢江生发表时间:2016-10-28T15:04:48.350Z 来源:《名医》(学术版)2016年4期作者:谢江生[导读] 药品不良反应(Adverse drug reaction,ADR)报告和监测是指药品不良反应的发现、报告、评价和控制的过程。
甘肃省静宁县深沟卫生院 743409[摘要] 目的:分析我院的中药使用状况和不良反应发生的特点、探讨不良反应发生的相关因素。
方法:采用回顾性分析方法,对我院20091月-2014年12月上报的62中药不良反应报告进行统计分析。
结果:不良反应可以发生在任何年龄阶段, 62例中药不良反应病例报告中,男性27例,占总数43.55%;女性35例,占总数的56.45%,女性的比例高于男性]。
62例不良反应报告中年龄最小的0.8岁,最大的表77岁,说明中药不良反应可发生在任何年龄阶段,其中61岁以上的患者占38.71%。
其发生率可因该药的剂型不同有很大的差异,其中以注射剂为首位(61.29%),片剂次之。
结论:加强中药不良反应的监控力度,慎重选择静脉滴注给药治疗,提高临床合理用药水平,以减少临床不良反应发生,保障患者安全合理用药。
【关键词】中药 ;不良反应;合理用药药品不良反应(Adverse drug reaction,ADR)报告和监测是指药品不良反应的发现、报告、评价和控制的过程。
按照WHO国家药物检测合作中心的规定,ADR指正常测量的药物用于预防、诊断、治疗疾病或调节生理机能时出现的有害的与用药目的无关的反应。
它不包括无意或者故意超剂量用药引起的反应以及用药不当引起的反应。
在临床上对药品的要求不仅仅局限于对疾病的治疗作用,也要求在治疗疾病的同时所使用的药品应当尽可能少的出现ADR。
在我国每年约500万的患者因为ADR而入住医院治疗,有19.2万人死于ADR[1]。
近年来,随着中药新品种,新剂型的不断研发及其在临床中的广泛应用,其不合理应用现象日益严重,但一般认为,中药不良反应的发生率与严重程度均低于西药,使许多人对中药的不良反应问题有所忽视。
抗感冒药的不良反应与合理应用

抗感冒药的不良反应与合理应用摘要】目的:探讨抗感冒药的不良反应与合理应用。
方法:此次调查对象随机选自我院2015年7月至2016年7月收治的感冒患者300例,将所有研究对象的临床资料和处方信息进行整理分类,针对患者的一般病情、处方中用药情况等展开回顾性分析,分析其处方信息、不良反应及药理成份分布。
结果:在300张处方中,不合理处方占12.50%,药物成分重复处方占10.00%,药物使用不对症占1.67%;出现不良反应为9.67%,其中胃部不适者51.72%,过敏者35.58%,血压升高或心跳加快者27.59%,恶心呕吐者31.03%;300张处方中涉及的抗感冒药物包括复方盐酸伪麻黄碱缓释胶囊、咖酚伪麻片、复方氨酚伪麻片、氨咖黄敏溶液等。
结论:抗感冒药引起不良反应可涉及各个器官系统,使用抗感冒药前应仔细阅读说明书,并遵医嘱用药,注意用药间的相互作用,避免药物的滥用,最大程度降低不良反应的发生。
【关键词】抗感冒药;不良反应;合理应用【中图分类号】R373.1+4 【文献标识码】A 【文章编号】1007-8231(2016)34-0075-02前言感冒属于临床上较普遍发生的一种疾病,是一种常见病,多发病,主要是因病毒感染而引起的一种上呼吸道疾病,属于自限性疾病,在患者得到充分的休息,注意保暖,饮食清淡并饮用大量的水的情况下,大多症状在几日后可自行缓解甚至消失[1]。
感冒目前临床上还没有特效药,大多采取抗病毒治疗及自身免疫调节治疗。
在日常生活中大多患者都将感冒当成小病,没有引起足够的重视,自行备一些不同类型的感冒药,且多数患者缺少足够的医药知识,急于求成,往往会服用多种抗感冒药物或自行增大药物的剂量,导致出现一系列不良的反应,造成严重后果。
为此及时了解各种抗感冒药的不良反应,是保证合理用药的关键。
1.资料与方法1.1 一般资料此次调查对象随机选自我院2015年7月至2016年7月收治的感冒患者300例,其中男165例,女135例;年龄3~77岁,平均(36.7±6.5)岁;儿童57例,青少年59例,中年51例,老年133例。
使用利巴韦林注射液30例药品不良反应分析

使用利巴韦林注射液30例药品不良反应分析摘要]目的;分析利巴韦林注射液不良反应发生情况及相关因素。
方法:选取我院2013年6月—2016年6月的30例患者,对患者的不良反应进行总结归纳。
结果:利巴韦林注射液不良反应临床表现复杂多样,可累及血液系统、神经系统、呼吸系统、消化系统、皮肤及粘膜,大多数不良反应经对症治疗,减慢滴速及停药都能恢复正常。
结论:利巴韦林注射液静脉滴注时要密切观察病情,防止发生不良反应。
[关键词]利巴韦林注射液;不良反应;分析研究利巴韦林注射液具有广谱抗病毒性能,体外具有抵制呼吸道合胞病毒、流感病毒、甲型肝炎病毒、腺病毒等多种病毒生长的作用,在临床上广泛应用,用于呼吸道合胞病毒引起的病毒性肺炎与支气管炎。
临床用于各种病毒引起的感染,随着临床的广泛使用,其副作用明显增加,尤其是一些罕见反应的报道不断增加。
根据我院2013年6月—2016年6月的30份不良反应病例研究,现总结如下:1资料与方法1.1临床资料选取我院2013年6月—2016年6月的30份病例,其中男18例,女12例,年龄18—68岁,平均年龄43岁。
其中呼吸道感染6例,其他疾病合并呼吸系统感染4例,支气管肺炎3例,流感2例,疱,5例,扁桃体炎3例,其他疾病7例,既往有过敏史4例,其中青霉素过敏1例,利巴韦林2例,庆大霉素1例。
1.2方法从注射利巴韦林注射液后的患者情况、用药情况、不良反应情况等方面对病例进行统计分析,内容涉及原发病、给药剂量、方法及溶媒、不良反应症状及预后情况。
统计方法:统计结果通过统计软件APSS22.0对资料数据进行统计分析,处理数据采用卡方检验。
P<0.05表明具有统计学意义。
2结果2.1过敏不良反应一例患者因化脓性扁桃体炎给予利巴韦林注射液200mg,加入5%葡萄糖溶液100ml中,静脉滴注,当用药30分钟时,患者出现寒战、高热、呼吸急促等不良反应,立即停止用药,给予异丙嗪、地塞米松、安痛定注射液等对症处理,症状得到缓解。
我院药品不良反应漏报情况调查及原因分析

我院药品不良反应漏报情况调查及原因分析目的分析我院药品不良反应ADR出现漏报情况,将会对患者造成伤害,需要针对其进行全面有效的控制和管理,以此降低药品不良反应的发生率、促进临床合理用药。
方法采用回顾性调查研究方法对我院2015~2016年上报ADR 124例和漏报的ADR 230例进行统计分析。
结果漏报的230例ADR报告中以静脉给药引发的ADR最多,其中又以调节免疫药物方面引发的ADR最多,达到41.28%。
门诊耳鼻喉科ADR的漏报率最高,达到84.88%。
结论临床应加强ADR的监测,如实上报ADR的发生率,避免或减少药品不良反应发生。
[Abstract] Objective To explore the adverse drug reactions (ADR)missing report in our hospital,which would cause harm to the patient. Comprehensive and effective control and management was required. In order to reduce the incidence of adverse drug reactions,and to promote rational use of drugs in clinical practice. Methods Retrospective investigation and research method was used to statistically analyze the 124 cases report ADR and 230 cases of missed report ADR in our hospital in 2015 -2016. Results Among the 230 cases of missing report ADR,the most was ADR caused by intravenous administration. Among them,ADR caused the regulation of immune drugs was the most,up to 41.28%. The outpatient department of ENT,had the highest false negative rate of ADR,reaching 84.88%. Conclusion We should strengthen the monitoring of ADR and truthfully report the incidence of ADR to avoid or reduce adverse drug reactions.[Key words] Adverse drug reactions ADR;Adverse drug reaction monitoring;Clinical rational use of drugs;Reason analysis药品不良反应(adverse drug reactions),主要是指合格药品在正常用法用量下出现的与用药目的无关或意外的有害反应。
2016年某院蔗糖铁注射液临床使用评价及分析

2016年某院蔗糖铁注射液临床使用评价及分析倪寂;冯伟民;范赟婷【摘要】目的为临床合理应用蔗糖铁注射液提供参考.方法选取医院信息系统(HIS)2016年1月至12月所有使用蔗糖铁注射液的住院病例,对患者一般情况、临床诊断、用法用量、注意事项等资料进行回顾性分析.结果 429例患者蔗糖铁注射液使用基本合理,其中不合理应用主要为贫血类型未明确诊断、用法用量不当及溶剂品种选择不适宜等情况.结论医院临床使用蔗糖铁注射液时,需强化血清铁、血清铁蛋白等的监测,甄别贫血类型,对明确诊断为缺铁性贫血的患者方可使用该药.%Objective To provide a reference for clinical rational application of Iron Sucrose Injection. Methods All of the hospitalized patients used Iron Sucrose Injection were selected from HIS in our hospital from January to December in 2016,the general situation, clinical diagnosis,usage and dosage,precautions and other data of the patients were retrospectively analyzed. Results In 429 patients,the use of Iron Sucrose Injection was basically rational,among them,the irrational use was not clear in the diagnosis of the anemic types, usage and dosage,selection of the solvent varieties and so on. Conclusion When Iron Sucrose Injection is used in clinic,it is necessary to strengthen the detection of serum iron and serum ferritin,examine and distinguish the anemia types. The drug can only be used in the patients with definite diagnosis of iron-deficiency anemia.【期刊名称】《中国药业》【年(卷),期】2017(026)022【总页数】4页(P89-92)【关键词】蔗糖铁注射液;住院患者;用药分析;合理用药【作者】倪寂;冯伟民;范赟婷【作者单位】上海市第十人民医院崇明分院药剂科,上海 202157;上海市第十人民医院崇明分院药剂科,上海 202157;上海市第十人民医院崇明分院药剂科,上海202157【正文语种】中文【中图分类】R969.3;R954;R973+.3蔗糖铁注射液为静脉用铁剂,为多核氢氧化铁(Ⅲ)-蔗糖复合物溶液,适用于口服铁剂效果不好而需静脉铁剂治疗的患者。
我院191例药品不良反应分析报告及临床药师作用探讨
Strait Ph-ma/utW—Joti—Vol32No.0426204结论本研究结合工作实际,对儿科医院急诊取药等候这一环节进行分析,发现急诊药房取药等候时间符合要求,其中药品数量(处方难易度、、拆零、给药途径对取药等候时间影响大,通过改进仍可以提升急诊药房服务质量。
参考文献〔2张乃文,孟莉,杨军,等•优化我院门诊药房工作流程的研究3-.中国药房401102(2)21710175.〔2〕王晓玲0长艳菊,郭春彦•我国儿童常用药品现状分析5〕2015,10(50):26-22.〔5〕王春婷,李玉基,夏东胜,等.儿童用药现状及对策5-.中国药物警戒46209(08):492O96900.5〕许晶晶,姚平立,宋海宁,等•我院门诊药房药品拆零管理存在的问题与改进措施5〕中国医药导报061805(22):156055.〔5〕张晶晶,李琪,曹荣娟,等•某院门诊西药房60例退药原因分析与对策5-.海峡药学00199211):221024.5〕李杨•门诊西药房退药情况分析与改进措施探讨5-4中国药事, 201995(08):956-904.-药物不良反应•我院21例药品不良反应分析报告及临床药师作用探讨许娟娟,袁秀芝*(华中科技大学同济医学院附属梨园医院药剂科,湖北武汉032077)摘要:目的探讨我院药品不良反应(ADR)发生的特点和规律,特别是严重的,罕见的不良反应。
为临床安全用药提供参考。
方法采用回顾性分析方法,对我院2012〜202年上报国家ADR监测中心的191例药品不良反应报告,从ADR患者的年龄与性别、给药途径、药品种类、ADR涉及的器官或系统等方面进行统计分析。
结果191例ADR报告中,女性略高于男性,以鼻65岁这个年龄段人群最多,为105例(54.07%);以静脉滴注方式引发的ADR最多,65例(74.87%);抗感染药物引起的ADR最多,71例(57.17%);ADR表现以皮肤及附件损伤最为常见,65例(34.05%)。
47例钆喷酸葡胺注射液不良反应的文献分析_李信华

333中南药学 2016年3月 第14卷 第3期 Central South Pharmacy. March 2016, Vol. 14 No.347例钆喷酸葡胺注射液不良反应的文献分析李信华 (武汉市汉口医院,武汉 430010)摘要:目的 了解钆喷酸葡胺致不良反应的情况,分析其特点及相关因素,促进临床合理用药。
方法 采用文献学计量方法,对国内公开报道的47例钆喷酸葡胺致不良反应进行总结性分析。
结果 钆喷酸葡胺所致不良反应中,中度过敏反应11例,重度过敏反应28例(包含6例死亡),非过敏反应8例。
结论 钆喷酸葡胺注射液的不良反应发生率虽低,但重度不良反应可危及生命,应引起临床重视。
关键词:钆喷酸葡胺;不良反应;文献分析中图分类号:R981 文献标识码:B 文章编号:1672-2981(2016)03-0333-03doi:10.7539/j.issn.1672-2981.2016.03.029Literature analysis of 47 adverse reactions of gadopentetate dimeglumineLI Xin-hua (Hankou Hospital of Wuhan, Wuhan 430010)Abstract: Objective To understand the adverse reactions caused by gadopentetate dimeglumine (Gd-DTPA), analyze its characteristics and related factors, and promote the clinical rational use of drugs. Methods Through the method of literature study, 47 adverse reactions of reported Gd-DTPA and acid were summarized. Results Elevel moderate allergic reactions, 28 heavy reactions (including 6 deaths) and 8 non allergic reactions were induced by Gd-DTPA. Conclusion The incidence of adverse reactions of Gd-DTPA acid injection is low, but severe adverse reactions can be life-threatening, and attention should be paid to. Key words: gadopentetate dimeglumine ; adverse reaction ; literature analysis作者简介:李信华,男,主管药师,主要从事医院药学研究,Tel :(027)51139149,E-mail :498073056@ 钆喷酸葡胺(Gd-DTPA )是一种顺磁性物质,系离子型非特异性细胞外液对比剂,虽然安全性较高,但仍有一些严重甚至致死的报道出现,本文通过钆喷酸葡胺公开发表的不良反应(ADR )文献,综合分析其一般规律、特点及相关因素,给临床用药提供参考。
临床DM公告-总局关于发布药物临床试验数据管理与统计分析的计划和报告指导原则的通告(2016年第113号)

附件药物临床试验数据管理与统计分析的计划和报告指导原则一、前言规范的数据管理计划有助于获得真实、准确、完整和可靠的高质量数据;而详细的统计分析计划则有助于保证统计分析结论正确和令人信服。
为保证临床试验数据的质量和科学评价药物的有效性与安全性,必须事先对数据管理工作和统计学分析原则制定详细的计划书。
在试验完成时,对试验中的数据管理和统计分析工作进行全面完整的总结至关重要,通过数据管理报告真实反映临床试验过程中的数据质量和试验样本特征,通过统计分析报告为临床试验总结报告的内容和研究结论提供主要依据。
因此,在药物上市注册时,监管部门将数据管理计划和报告与统计分析计划和报告视为评价临床试验结果的重要文件和依据。
虽然我国《药物临床试验质量管理规范》(Good Clinical Pr actice,GCP)中对药物临床试验数据管理与统计分析进行了原则要求,且国家食品药品监督管理总局已发布的有关药物临床试验及其统计学的相应技术指南也涉及数据管理和统计分析工作的主要环节,但针对数据管理计划和报告、统计分析计划和报告却没有详细的技术规范和指导性建议。
因此,本技术指导原则对此进行了较为详细的介绍和阐述,并提出具体要求,旨在为临床试验的数据管理和统计分析人员提供技术指导,帮助其更好地完成相关工作以达到监管要求。
二、数据管理的计划和报告(一)一般考虑数据管理计划(Data Management Plan, DMP)是由数据管理人员依据临床试验方案书写的一份动态文件,它详细、全面地规定并记录某一特定临床试验的数据管理任务,包括人员角色、工作内容、操作规范等。
数据管理计划应在试验方案确定之后、第一位受试者筛选之前定稿,经批准后方可执行。
通常数据管理计划需要根据实际操作及时更新与修订。
数据管理工作涉及多个单位或业务部门,包括数据管理、临床研究者、统计分析、医学事务、临床监查、临床稽查等单位或部门。
数据管理的职责可分为负责、参与、审核、批准、告知等,各单位/部门在数据管理各步骤的职责不尽相同。
2015-2016年我院药品不良反应报告Pareto最优分析

2015-2016年我院药品不良反应报告Pareto最优分析摘要】目的:了解我院药品不良反应(ADR)发生的规律及特点,为临床合理用药提供参考。
方法:采用Pareto最优分析,对2015-2016年上报的374例ADR报告进行整理,对患者年龄、药物品种、抗菌药物品种、给药途径以及ADR临床表现进行分析和归纳。
结果:374例ADR中,45~64岁这个年龄段较易发生ADR (43.9%),在所有药物中抗菌药物发生ADR的比例最大(30.7%),其中头孢菌素发生例数最多(45例,39.1%),发生ADR的主要给药途径为静脉滴注(52.4%),ADR主要表现为皮肤及其附件损害(31.0%)。
结论:依据ADR出现的特征与规律,合理掌握用药方式,并强化监护环节,运用有效的措施加以监测和管理,以降低ADR的发生。
【关键词】药品不良反应;Pareto最优分析【中图分类号】R197.324 【文献标识码】A 【文章编号】2095-1752(2017)19-0383-02药品不良反应(Adverse drug reaction,ADR)是指合格药品在正常用法用量下出现的有害反应[1]。
近年来随着我国人均用药率、群体用药频度和数量的大幅增加,由此产生的药品不良反应问题也越来越严重。
笔者采用帕累托图法分析我院374例ADR报告,了解我院ADR发生的特征,为临床合理用药提供参考。
1.资料与方法1.1 一般资料通过我院局域网“药物不良反应监测管理系统”收集2015年1月1日-2016年12月31日ADR报告,共计417例,其中合格报告374例,合格率89.69%,经审核后上报全国药品不良反应监测中心。
1.2 研究方法利用Excel 2007对374例ADR报告分别按照患者年龄、药物类别、给药途径、不良反应表现进行分类和Pareto图分析。
“Pareto”最优法则也称为80/20法则,指资源分配的一种状态。
Pareto图分析法将影响因素分为三类:A类为关键的少数,是主要因素,其影响程度的累计百分数在0~80%范围内;B类是一般因素,其影响程度的累计百分数在80%~90%范围内;C类为次要因素,其影响程度的累计百分数仅在90%~100%范围内。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2016年药品不良反应分析报告
一、药品不良反应类型统计:
2016年我院共上报药品不良反应/事件报告179例,其中严重报告3例,占1.68%;新的严重报告2例,占1.12%;一般报告120例,占67.04%;新的一般报告54例,占30.16%。
二、按药品种类统计
化学药品不良反应上报166例,占92.7%;中成药品不良反应上报13例,占7.3%。
详见见表1:
表1 按药品种类上报情况表
药品种类上报例数占比
化学药品166 92.7%
中成药品13 7.3%
三、按药理作用统计
抗感染药品不良反应上报112例,占62.57%;非抗感染药品不良反应上报67例,占37.43%。
见表2:
表2 按药理作用上报情况表
四、抗感染药品不良反应报告:
硝基咪唑类上报6例,占5.36%;头孢菌素类上报36例,占32.14%;青霉素类上报1例,占0.89%;其他B-内酰胺类上报5例,占4.46%;喹诺酮类上报54例,占48.12%;大环内酯类上报3例,占2.68%;其他抗生素上报6例,占5.36%;抗病毒药品上报1例,占0.89%。
见表3:
表3 抗感染药品ADR上报情况表
五、报告科室分布
药品不良反应报告来自全院18科室,其中住院患者162例,门急诊患者17例。
详见表4:
表4 ADR科室上报情况表
六、药品不良反应报告性别和年龄分布
在报告的179例ADR中,男性75例,女性104例。
年龄分布区间为1-90岁,具体情况见表5:
表5 患者年龄分布情况
七、用药途径情况分析:
用药途径包括静脉给药及口服、皮下注射等。
最常见仍为静脉滴注,占%。
详见表6
表6 给药途径情况表
八、药物不良反应涉及的系统、器官及表现情况分析
上报的ADR涉及的系统损害多为皮肤及其附件损害,常见症状为皮疹、瘙痒等,具体内容见表7:
表7 药物不良反应所涉及的系统、器官及临床表现情况
九、统计ADR报表中发现的问题
1.上报药品不良反应类型单一:由表7可见,我院上报的药品不良反应多局限为各种药物致皮疹,且均为轻微皮疹,停药后多自行消散,所涉及药物无上市5年内的新药。
医务人员应对不良反应类别的定义严格掌握,临床应鼓励医务人员积极发现新的、严重的不良反应,对于造成器官损害、致残、致畸、致死、导致住院治疗甚至延长住院时间的药物不良反应,要在规定时限内准确上报。
2.药物不良反应报表书写不规范:本次回顾分析发现,本院ADR 报表书写虽比往年有很大提高,但仍存在部分不规范的情况,如填写漏项、不良反应发生经过描述不详、阐述内容无逻辑关系等,导致这一现象的主要原因是上报人对于表格各项目的要求理解不到位。
3.抗菌药物使用的安全隐患:与国内文献报道一致,我院2016年收集到的ADR病例怀疑由抗菌药物引起的不良反应所占比例最大,其中以喹诺酮类抗菌药物为主,由此提示临床科室在用药过程中应告知患者,如感觉不适应立即反馈。
4.开展ADR监测工作需要医务人员的共同努力,全面配合。
做好药物不良反应事件的管理工作是医务人员的责任,与医疗安全息息相关,希望我院医务人员提高对ADR监测工作的积极性和主动性,进一步推进此项工作,促进临床安全合理用药。
