测量气体体积方法(精编课件).ppt
气体体积的测量及读数

气体体积随气压变化而变化,如果测 量时气压与标准气压不一致,会导致 测量结果出现误差。
人为误差
操作不当
测量过程中,如果操作人员操作不当,如读数不准确、操作顺序错误等,会导致测量结果出现误差。
主观判断误差
在某些情况下,操作人员的主观判断可能影响测量结果,如对异常数据的筛选、对仪器状态的判断等 ,这些主观判断可能存在误差。
气体体积的测量及读 数
目录
• 气体体积测量的基础知识 • 气体体积测量的方法 • 气体体积测量仪器的使用与维护
目录
• 气体体积测量的误差分析 • 气体体积读数的注意事项
01
气体体积测量的基础知识
气体体积测量的定义
总结词
气体体积测量是指通过一定的方法和技术,对气体所占的空间进行量化的过程。
详细描述
02
气体体积测量的方法
直接测量法
定义
直接测量法是通过使用量筒、量杯等直接测量气 体体积的工具进行测量。
优点
直接测量法简单易行,不需要复杂的设备和技术, 适用于小量气体体积的测量。
缺点
由于气体的可压缩性和可流动性,直接测量法在 高压或低温条件下误差较大。
间接测量法
定义
01
间接测量法是通过测量气体的质量、温度和压力等参数,再利
仪器误差
仪器精度
仪器的精度决定了测量结果的准确性 ,如果仪器精度不高,会导致测量结 果偏离真实值。
仪器校准
仪器在使用前需要进行校准,以确保 测量结果的准确性,如果仪器未经过 校准,则测量结果可能存在误差。
环境误差
温度影响
气体体积随温度变化而变化,如果测 量时温度与标准温度不一致,会导致 测量结果出现误差。
量程范围
物质的量气体摩尔体积PPT课件

解析 (1)①22 g 二氧化碳的物质的量为442g2/mg ol=0.5 mol; ②8 g 氢气的物质的量为2 g8/mg ol=4 mol; ③1.204×1024 个氮气分子的物质的量为6.012.×210042×31m02o4l-1=2 mol,质量为
2 mol×28 g/mol=56 g; ④4 ℃时 18 mL 水,其质量为 18 mL×1 g/mL=18 g,物质的量为181g8/mg ol= 1 mol;
A.1.5NA 2 mol C.3.01×1023 4 mol
Hale Waihona Puke B.1.5NA 32 g D.NA 64 g
【对点练2】 (平均摩尔质量的计算)根据相关量的关系,完成下列填空:
(1)由8 g O2和28 g N2组成的混合气体的平均摩尔质量是________。 (2)在空气中N2、O2、Ar的体积分数分别约为78%、21%、1%,则空气的平均 摩尔质量为________。
同压下,同质量的三种气体,密度和相对分子质量成正比,三种气体密度最小的是
X,故 C 正确;同温同体积气体物质的量之比等于压强之比,Y、Z 气体的压强比 m(Y)
为pp((YZ))=nn((YZ))=Mmr((ZY))=mm( (YZ))··MMrr((YZ))=2×12=4∶1,故 D 错误。 Mr(Z)
解析 (2)1 mol Na2R 中含 2 mol Na+,题目中有 Na+ 0.4 mol,则有 0.2 mol Na2R。 运用公式 M=mn 得mn((NNaa22RR))=01.22.m4 gol=62 g·mol-1。Mr(Na2R)=62,求得 Mr(R) =62-2×23=16。根据 n=Mm,得 n(R)=0.1 mol,则 n(Na2R)=0.1 mol。
测定1mol气体的体积PPT学习教案

气体摩尔 体积的 测定装 置应该 有几部 分组成 ?
测定气体摩尔体积的装置
气体发生装置 根据制气反应的反应物状态和反应条件选择装置
气体收集装置 量体积装置
如果把气体收集与量体积结合起来的装置设计 通过测定被气体从广口瓶中压出来的水的体积 来测得气体的体积,或用量气管,使生成的气 体直接通入原本装满水的管中,水被排向另一 管,从另一管的刻度可读出气体的体积。以上 两种装置在读取气体体积时都应使两边的水面 保持同一水平面。
定量测定技术的进步推动了现代化学的发展。 定量测定是现代化工生产中控制生产的必要条件。 定量测定中“准确性”极其重要。
第2页/共38页
化学的定量测 定:
定量测定方法:
称量、量出体积、确定温度的变化数等
• 电子天平、量筒、滴定管、温度计 、秒表 等
定量仪器 :
第3页/共38页
10.1 测定1mol气体的体积
录数据。 第20页/共38页
10.1 测定1mol气体的体积
【实验部分】
3、加料(镁带) ——从A瓶出气口处除下胶管, 托盘中移出A瓶,用小烧杯加入 20毫升的水,再加入称量后的 镁带,加料口塞上橡胶塞,将A 瓶置于A托盘第21内页/共3,8页 出气口接上胶 管。
10.1 测定1mol气体的体积
8、针筒读数时要看平端所对的刻度 9、复原时用水冲洗气体发生器是为了降温,将其
恢复到室温
第31页/共38页
实验误差的来源及处理办法
1、系统误差
来源于仪器装置和药品自身的误差 仪器的精密度高、试剂品质好,误差就小 系统误差有专门的方法来处理
2、偶然误差
来源于测定时的某些偶然因素
如测定时,环境温度的变 化 偶然误差可用多次平行实验求平均值来减小
气体体积质量的测定ppt正式完整版

装置E:直接测量固液反应产生气体的体积, 注 意应恢复至室温后再读取注射器中气体的体积。 (一般适合滴加液体量比较少的气体体积测量)。
(2)间接测量法。如F装置是通过测量气体排出 的液体体积来确定气体体积。读数时,应先冷 却至室温,再上下移动量筒,使量筒中液面和 广口瓶内的液面相平后再读数。
气将操体稀质 H2作量SO的4方测加量入法一气般球是为前用,吸关_关收_闭剂闭_K1将_和气b_K体2_,,吸_打收_打开,_K然3_开,后_反再_a应称_,结量_束。_缓时_气_缓球_膨_通胀_的_体入_积与_空量_筒_气Ⅰ_中_,所_接_直收_的_至水_的_a体_处积_相_出等_,_来此_为_的CO_2_空与_O2_气的体
2.气体质量的测量装置 气体质量的测量一般是用吸收剂将气体吸收,然后再称量。 常见的吸收装置:
测定气体的质量时,要防止空气中相关气体的干扰。
题组一 气体体积的测定
递进题组
1.为了测定已部分变质的过氧化钠样
品的纯度,设计如图所示的实验装置,
图中Q为弹性良好的定
知识 梳理
递进 题组
定量实验中常测定3种数据:温度、质量和体积。
温度——用温度计测量
固体——用天平称量
液体——在器皿中用天平称量
质量气体——用天平称出吸收装置吸收气体前后
的质量后求差值
知识梳理
液体——用量筒、滴定管或容量瓶 体积气体——用各种组合仪器见下面讲解
1.气体体积的测定装置 既可通过测量气体排出的液体体积来确定气体的体积(二者 体积值相等),也可直接测量收集的气体体积。 直接测量气体体积的常用装置
气体摩尔体积课件(共28张PPT)高中化学沪科版(2020)必修第一册

= .
.
= .
.
= .
.
= .
.
【结论1】同温同压下,1 mol气体的体积远大于1 mol固体或液体的体积。
【思考】计算1 mol各物质的体积,并寻找规律。
NaCl
Fe
C2H5OH
H2SO4
H2(273 K)
He(273 K)
CH4(273 K)
固
固
液
液
气
气
气
1
1
1
1
1
1
1
58.5
56
46
98
2
4
16
2.17
7.86
0.789
1.84
0.000 088
0.000 176
0.000 716
【结论2】同温同压下,1 mol气体的体积近似相等。
V=
V=
V=
V=
V=V=V=
L。
V(O2) = n(O2) × Vm = 0.8 mol × 22.4 L·mol-1 = 17.92 L
2. 标准状况下,56 L CO2的物质的量为 2.5
n(CO2) =
V(CO2)
56 L
=
= 2.5 mol
Vm
22.4 L·mol−1
mol。
【资料卡片】
分子直径/
(nm)
分子间的平均距离/
(nm)
0.35
0.36
0.33
3.3
3.3
3.3
注:均为常温常压下的测量值
气体物质分子间的平均距离远大于分子本身大小,在分子数
目相同的情况下,气体的体积主要由分子间的距离大小决定。
气体的质量和体积的测定PPT教学课件

答案 Ⅰ.②酸式滴定管 Ⅱ.(1)254)氢离子浓度不同 镁与铜易形成原电池,加快 反应速率,干扰实验的测定
2.气体质量的测定 (1)原理:气体的质量一般采用间接的方法来 测定,对一些可用试剂直接吸收的气体根据气 体的某些性质(如酸碱性或溶解性)采用合适的 吸收剂(如浓硫酸、碱石灰)和实验装置(如洗 气瓶、干燥管)来吸收,通过吸收装置吸收前后
出甲管内气体体积数。这套装置的好处是成功的 避免了装置(a)的不足,利用反应前装置内外的气 压相等,反应后上下移动乙管,使甲、乙两管内 的液面保持相平,从而保持反应后装置内外的气 压相等,这样测得的结果才比较准确。但这套装 置也有不足,操作复杂。 (3 读数时注意:①冷却至室温;②调节两液面相平;
250 mL 0.5 mol/L的H2SO4溶液,所需要的主
要仪器有
、
、烧杯、玻璃
(2)以下是读取量筒内水的体积时必须包括的
几个步骤:①使乙、丙中液面相平;②将装置
冷却至室温;③读取量筒内水的体积。这三步
操作的正确顺序是
(3)读取量筒内水的体积时,若丙中液面高于
乙中液面,使乙、丙中液面相平的操作是
(4)简述速率不等的原因是
量取10.00 mL 0.5 mol/L
H2SO4和H2C2O4 ③分别称取除去表面氧化膜的镁条并系于铜
④检查装置的气密性,在广口瓶中装满水,按 图连接好装置; ⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不 与酸接触),至反应完全,记录 ⑥反应结束后,读取量筒中水的体积为y mL。
Ⅱ.
(1)用密度为1.84 g/cm3 98%的浓H2SO4配制
(2)测量装置
【实验探究2】 碳酸钠样品中往往含有少量NaCl, 现欲测定样品中Na2CO3的质量分数,某探究性 学习小组分别设计了如下实验方案。请回答下
气体摩尔体积公开课课件

PPT,a click to unlimited possibilities
汇报人:PPT
添加目录标题
气体摩尔体积 的定义与意义
气体摩尔体积 的公式与计算
气体摩尔体积 的实验测定
气体摩尔体积 的应用
气体摩尔体积 的注意事项
气体摩尔体积 的拓展知识
添加章节标题
气体摩尔体积的定义与 意义
气体摩尔体积的 概念和计算方法
气体摩尔体积在 物理变化中的应 用
气体摩尔体积在 化学变化中的应 用
气体摩尔体积在 不同温度和压力 下的变化规律
在工业生产中的应用
计算气体的质量:通过气体摩尔体积可以计算出气体的质量,从而控制生产过程中的原料用量。
确定气体的体积:气体摩尔体积可以用来确定气体的体积,从而控制生产过程中的气体流量。
气体摩尔体积的概念
定义:气体摩尔体积 是指单位物质的量的 气体所占有的体积, 数值是本节课需要重 点掌握的内容。
单位:气体摩尔体 积的单位是升/摩尔, 符号为L/mol。
意义:气体摩尔体积 是气体宏观量与微观 量之间的桥梁,可以 帮助我们更好地理解 气体的性质和行为。
影响因素:温度、压 强是影响气体摩尔体 积的主要因素,不同 条件下,气体摩尔体 积会有所不同。
添加标题
气体摩尔体积的应用:气体摩尔体积在化学、物理、工程等领域都有广泛的应 用。例如,在化学反应中,气体摩尔体积可以用来计算反应物和生成物的比例; 在工程中,气体摩尔体积可以用来计算气体的流量和压力等参数。
气体摩尔体积的理论基础
阿伏伽德罗定律:在同温同压下,相同体积的任何气体都含有相同数目的分子。
气体摩尔体积的注意事项
气体摩尔体积的概念和计算方法 气体摩尔体积与温度、压强的关系 气体摩尔体积的适用范围和限制条件 气体摩尔体积与其他物理量的关系
气体摩尔体积-完整版PPT课件精选全文

2.气体摩尔体积 (1)定义:单位物质的量的气体所占的体积。 (2)符号:Vm。 (3)单位:L/mol或L·mol-1。 (4)气体摩尔体积概念的要点。 ①物质的聚集状态,必须是气体,不适用于固体、液体。 ②物质的量必须为1_mol。 ③必须指明气体所处的外界条件,即温度、压强。
3.标准状况下的气体摩尔体积
三、气体摩尔体积
1.决定物质体积大小的因素
(1)决定固体、液体物质体积大小的因素主要是粒子数目的多少和粒子 本身的大小。
(2)决定气体体积大小的因素是粒子数目的多少和气体分子间的平均距 离。影响气体间距离的因素是温度和压强,对于一定量的气体,当压强一 定时,温度升高,气体体积要增大,当温度一定时,增大压强,气体体积 会减小。
判断有关概念要注意其指向性——粒子的具体化;恒久性——相对分子 质量,摩尔质量不随微粒的增多而变化;一致性——物理单位与指代物质要
一致。
(2011 年潍坊模拟)设 NA 为阿伏加德罗常数,下列说法中正确的是 ()
A.1 mol Na2SO4 溶于水,所得溶液中 Na+个数为 NA B.H2、O2、N2、CO2 组成的混合气体 1 mol 在标准状况下的体积 约为 22.4 L C.1 L 0.3 mol·L-1 Na2SO4 溶液中含有 Na+和 SO24-总数为 0.6NA D.NA 个氢气分子(H2)的质量为 1 g
【答案】 B
考点2 跨越阿伏加德罗常数判断的“七个陷阱” 陷阱一:忽视气体摩尔体积适用的条件。22.4 L·mol-1指在标准状况 下(0℃,101 kPa)的气体摩尔体积。若题中出现物质的体积,需考虑所给物 质的状态是否为气体,条件是否为标准状况。
陷阱二:忽视物质的聚集状态。气体摩尔体积适用的对象是气体(包 括苯状混况常合下作气为为体气干体)扰。。因一素些迷在惑标考准生状。况另下外是注液意体烃或的固衍体生的物物中质C,H3如Cl、CCHl4C、HSOO等3、在己标烷准、
高频考点-气体体积的测定专项突破PPT2021届高考化学二轮复习

天平上称量,得质量为mg,并将其投入试管B中的带孔隔板上; 微泛黄的旧水墨画,自在飞花、无边丝雨之中,一个长发披肩的女子,从雨巷中袅袅走来,携着一缕丁香花的幽香,载着一怀嫣然极致的心事,有叹息,但不哀伤,有顾盼,但不
凄然。 6.《离骚》中表明自己遭到不公正对待的原因之一是在上位者的荒唐的两句:
1.以“白衣冠”送荆轲,为易水送别,创造悲壮、凄怆的气氛。
字母表示)。 期”,“易水送别”,秦廷行刺等情节,塑造了荆轲这位敢于扶危济困、助弱御强、有勇有谋、视死如归的古代侠士形象。荆轲刺秦王并不能真正挽救燕国的危亡。荆轲千百年来,被
受压迫的人们敬仰的原因,在于他站在了斗争的最前列,去反对秦国对山东六国的进攻和挽救燕国的危亡,本文揭示了弱小燕国和强大秦国之间的尖锐矛盾和激烈斗争,从一个侧 面反映了战国时期秦燕之间的兼并与反兼并的斗争。
强敌压境,燕国危在旦夕,燕太子丹访得荆轲,即尊为上卿,然后派他到秦国行刺,其目的是要荆轲“劫秦王,使悉返诸侯侵地”,如不成,使“因而刺杀之”。荆轲具有义侠的性格, 又受太子丹的厚遇重任,明知身入不测之秦是极其危险的事,还是毅然前往,当事败后,荆轲身被八创却“倚柱而笑,箕踞以骂”壮烈而死。本文记的就是这件史事。通过“私见樊於
。
②擦掉镁条表面的氧化膜,将其置于 四、理清层次
⑵ 从文中可看出,他对国家大事了解得很透彻。既然烛之武一直不被用,他了解得那么透彻想干什么?
宋人秦观又在词中这样描绘春雨:“自在飞花轻似梦,无边丝雨细如愁。”春雨也是一个惹人闲愁几许的经典意象。(板书:春雨)而《雨巷》则把文人对雨的喜爱推向了极至:象一幅微
这一复杂的事件,作者不但写得精彩、生动,而且文字十分洗练,有很强的感染力。 第四段:迫晋退兵面对风云突变的局势,晋侯没有感情用事,而表现了清醒的头脑和理智的判断。这种隐忍不发、随机应变的胸怀和谋略,正是晋文公终成霸业的根本原因。 二、要历史地看待古人,看待英雄人物,要实事求是地分析评价。
排水法测定气体体积实验装置PPT课件
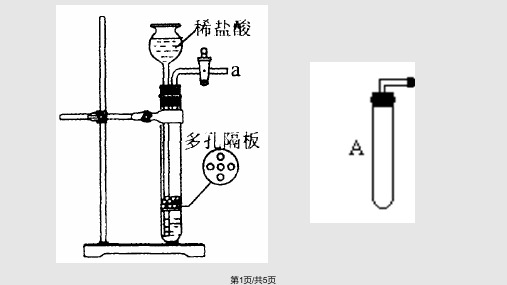
第1页/共5页
第2页/共5页
高度相同 ⑤再次读取量气管液面刻度
(3)反应完毕,每间隔1分钟读取气体体积,气体体积逐渐减 小,直至不变,气体体积逐次减小的原因是_________
(排除仪器和实验操作的因素)
第3页/共5页
第4页/共5页
感谢您的观看!
第5页/共5页
橡胶管
用左图装置来测定残余清液与Zn反应放 出气体的体积。 (1)使Y形管中的残余清液与锌粒反应的 正确操作是将____转移到____中。 (2)整个实验的操作顺序是_________ ①调整橡胶管右端装置使两边液面
高度相同 ②使量气管及反应装置内气体都冷却至
室温 ③读取量气液面刻度 ④再次调整橡胶管右端装置使两边液面
测量气体体积的方法

测量气体体积的方法(总3页) -CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除测量气体体积的方法文/巩庆凯胡贵和测量气体体积是一项基本的实验技能,因此学生需要掌握正确的测量方法。
测量方法可分为直接测量法和间接测量法两种。
现结合有关试题加以说明。
一、直接测量法直接测量法就是将气体通入带有刻度的容器中,直接读取气体的体积。
根据所用测量仪器的不同,直接测量法可分为倒置量筒法和滴定管法两种。
1.倒置量筒法将装满液体(通常为水)的量筒倒放在盛有液体的水槽中,气体从下面通入,实验结束,即可读取气体的体积。
1998年高考27题和2001年“3+2”高考20题均用到这一装置,现以2001年“3+2”高考20题为例说明。
例1 某学生利用氯酸钾分解制氧气的反应测定氧气的摩尔质量,实验步骤如下:①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为ag。
②装好实验装置(如图1)。
图1实验装置③检验装置气密性。
④加热开始反应,直到产生一定量的气体。
⑤停止加热(如图,导管出口高于液面)。
⑥测量收集到气体的体积。
⑦准确称量试管和残留物的质量为bg。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。
回答下列问题:(1)如何检查装置的气密性(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。
这三步操作的正确顺序是:________(请填写步骤代号)。
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同________。
(4)如果实验中得到的氧气体积是cL(25℃、1.01×105Pa),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简):M(O2)=________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
测量气体体积的方法
测量方法可分为直接测量法和间接测量法两种
精品课件,下载后可编辑
一、直接测量法 直接测量法就是将气体通入带有刻度的容器中, 直接读取气体的体积。根据所用测量仪器的不 同,直接测量法可分为针筒法、倒置量筒法、 和滴定管法。
精品课件,下载后可编辑
二、间接测量法 间接测量法是指利用气体将液体(通常为 水)排出,通过测量所排出液体的体积从而得 到气体体积的测量方法。 常用的测量装置为:用导管连接的装满液 体的广口瓶和空量筒
精品课件,下载后可编辑
排水量气时在读数之前,必须保证气 体的温度、压强均与外界相同,为此要注
意 1、:反应结束恢复至室温才能读数 2、调整内外(左右)液面相平才能读数 3、读数时视线和凹液面最低处相平
精品课件,下载后可编辑连接,检查装置的气密性。 ⑵、向酸式滴定管中注入一定量的无水乙醇,调整液面到“0” 处,然后向圆底烧瓶中加入一定量的金属钠,塞紧瓶塞。 ⑶、向由碱式滴定管组装的量气管中注入一定量的蒸馏水,调 整两边液面相平,记下读数V1。 ⑷、慢慢打开酸式滴定管的活塞,向圆底烧瓶中滴入无水乙醇。 ⑸、待反应结束,冷却到室温后,进行读取酸式滴定管的数据, 记为V醇。调整量气装置两边液面相平,读数,记为V2。
精品课件,下载后可编辑
