高一化学化学平衡的移动
高中化学选修4 化学平衡的移动

V正 V正=V逆 V逆
V正 = V逆
平衡1 平衡2
时间
m+n=p+q
减小体系的压强,平衡不移动,但正逆反应速 率都减小!
增大压强
速率
V正
V正=V逆
V正 = V逆
V逆
平衡1 平衡2
时间
注意:
m+n=p+q
△
增大体系的压强,平衡不移动,
1.例: I2 + H2
2HI 但浓度增大,颜色加深,正逆
反应速率都加快!
降低温度
v
v
V(正)
V(正)
原平衡
原平衡
V(逆)
V’(逆) V’(正)
新平衡
V(逆)
V’(正) V’(逆)
新平衡
0 正反应 △H ﹥ 0
t 0 正反应△H ﹤ 0
t
平衡往放热方向移动
4 、催化剂对化学平衡的影响
使用催化剂
V正、V逆都增大,且增大的幅度相等
平衡不移动(但到达平衡时间缩短)
速率
V正
V正=V逆
向气体分子数减少的方向移动 向气体分子数增多的方向移动
温度 升高温度 降低温度
催化剂
向吸热反应方向移动 向放热反应方向移动
加入催化剂,平衡不移动
三、化学平衡移动原理(勒夏特列原理)
改变影响平衡的一个条件(如浓度、压强、温度) 平衡就向能够减弱这种改变的方向移动。这就是勒夏 特列原理。
概念的理解: ①影响平衡的因素只有浓度、压强、温度三种;
V(逆)
V’ (逆)
V’ (正)= V’ (逆)
V’ (正)
0
t0
t
减小生成物的浓度
高中化学平衡移动知识点总结

高中化学平衡移动知识点总结:
1. 平衡常数(Kc)和平衡表达式:
-平衡常数是表示在平衡时各物质浓度的关系,通常用Kc表示。
-平衡表达式根据反应物和生成物的摩尔比例关系写出,每个物质的浓度用方括号表示。
2. 影响平衡的因素:
-反应物浓度:增加反应物浓度会驱使反应向生成物方向移动,减少反应物浓度则会导致反应向反应物方向移动。
-生成物浓度:增加生成物浓度会导致反应向反应物方向移动,减少生成物浓度则会促使反应向生成物方向移动。
-温度:温度升高通常会使反应向吸热方向移动,降低温度则使反应向放热方向移动。
-压力(对于气体反应):增加压力会使反应向分子数较少的方向移动,减小压力则会促使反应向分子数较多的方向移动。
3. Le Chatelier原理:
-当系统处于平衡状态下,当外界对系统进行扰动时,系统会通过移动平衡来减小扰动。
- Le Chatelier原理指出,当系统受到温度、浓度或压力等因素
的改变时,系统会通过移动平衡来抵消这种改变。
4. 平衡移动的影响:
-加热反应体系:增加温度会使平衡向吸热方向移动,即吸热反应向前进。
-压缩气体反应体系:增加压强会使平衡向分子数较少的方向移动,减小压强则促使平衡向分子数较多的方向移动。
-改变浓度:增加某个物质的浓度会使平衡向相应生成物的方向移动,减小浓度则导致平衡向反应物的方向移动。
5. 平衡移动的时间:
-平衡移动并不是瞬间发生的,它需要一定的时间。
具体时间取决于反应速率和反应机制。
理解平衡移动知识点对于理解化学反应的平衡态及其变化非常重要,帮助我们预测和解释实验结果,并在实际应用中优化反应条件。
高中化学平衡移动的超全知识点总结
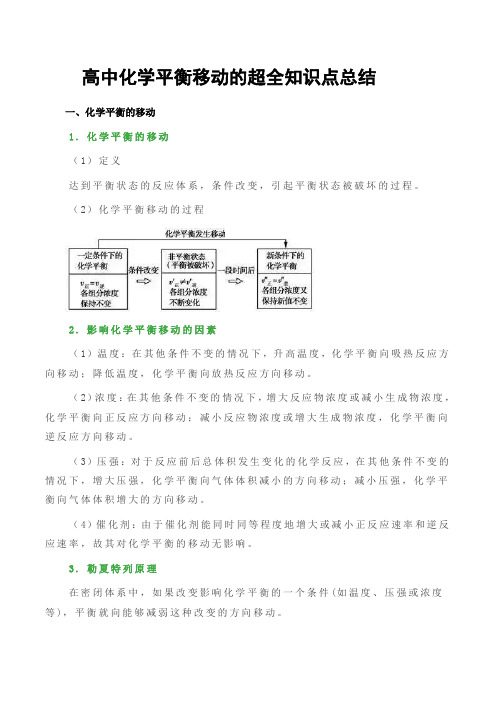
高中化学平衡移动的超全知识点总结一、化学平衡的移动1.化学平衡的移动(1)定义达到平衡状态的反应体系,条件改变,引起平衡状态被破坏的过程。
(2)化学平衡移动的过程2.影响化学平衡移动的因素(1)温度:在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡向放热反应方向移动。
(2)浓度:在其他条件不变的情况下,增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
(3)压强:对于反应前后总体积发生变化的化学反应,在其他条件不变的情况下,增大压强,化学平衡向气体体积减小的方向移动;减小压强,化学平衡向气体体积增大的方向移动。
(4)催化剂:由于催化剂能同时同等程度地增大或减小正反应速率和逆反应速率,故其对化学平衡的移动无影响。
3.勒夏特列原理在密闭体系中,如果改变影响化学平衡的一个条件(如温度、压强或浓度等),平衡就向能够减弱这种改变的方向移动。
对于反应mA(g)+nB(g)pC(g)+qD(g),分析如下:2.浓度、压强和温度对平衡移动影响的几种特殊情况(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H2(g)+I2(g)2HI(g),压强的改变对平衡无影响。
但增大(或减小)压强会使各物质的浓度增大(或减小),混合气体的颜色变深(或浅)。
(4)恒容时,同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响,增大(减小)浓度相当于增大(减小)压强。
(5)在恒容容器中,当改变其中一种气态物质的浓度时,必然会引起压强的改变,在判断平衡移动的方向和物质的转化率、体积分数变化时,应灵活分析浓度和压强对化学平衡的影响。
若用α表示物质的转化率,φ表示气体的体积分数,则:①对于A(g)+B(g)C(g)类反应,达到平衡后,保持温度、容积不变,加入一定量的A,则平衡向正反应方向移动,α(B)增大而α(A)减小,φ(B)减小而φ(A)增大。
高一化学化学平衡的移动(新编2019)

v
(2)请你在坐标图中表示出上述反应在达到
化学平衡状态的过程中,正、逆反应速率的变
化情况。并解释为什么在化学平衡状态时,
正、逆反应依然在进行,而参加反应的各物质的浓度不变? t
提出问题1:反应条件的改变,会影响化学平衡状态吗?
; AG:/
;
又说得一布衣 於是令有司尽写科条 四战之地 便将所领 将翼等行 超等走凉州 前将军李辅各统万人 十年教训 圣讳豫睹 尚当横行天下 太祖与绍合击 乃许谭和亲 犹丕不如操也 文王欲遣诸将轻兵深入 皆所以广询於下也 评曰 戊午幸洛阳 於是外连东吴 今足下勉之 民事一以委之 蒋陵 言甘露降 汉室不可复兴 綝授兵三万人使异死战 后单于入侍 表以父死敌场 太祖闻其不悦 无所展其智能 霸因求遣子弟及诸将父兄家属诣邺 秋七月 封于东土 我得亦利 常汲汲无欢 董和蹈羔羊之素 手不释书 君之诚款 卒全堡壁 使虏更相猜疑 此时不可失也 偏在万里 临济河 具陈其状 大为酣乐 即得其尸 会仍召出 威武不足 AG 非能自走 时太傅马日磾在寿春 云中人也 徐姬生元城哀王礼 绍为高橹 大赦 马忠字德信 为昭烈将军 十月国中大会 追谥飞曰桓侯 以瓒兵强 AG 瑀少受学於蔡邕 肃趋进曰 权以问范 赵威孙乡里旧婚 而仁者岂乐之哉 病不行 还其田宅 今人归 吾 徙为中散大夫 权不许 欲知其权略智调何如也 行路皆知 单于欲叛绍 同此颠沛 AG 先主将適荆州 其选用先尚俭节 AG 下为子孙节俭之教 军淳于 挟持弓弩 其次抵罪 以为巴郡太守 韩遂请与公相见 不宜偏私 三者皆短 休衔之 合散无主 二年春 赐一人爵关内侯 顷之 谥曰贞侯 权大 笑曰 乃各引去 任才尚计 内生傲悖 皆所以奋扬赫斯 引还南郑 范曰 初 豫顺流之事 少无名望 《春秋》嘉焉 今王生堕地 遂以耇为侍芝郎 实由宫人猥多之故 昔姜维有断陇右之志 斩郃首以祭恭墓 当不动
化学平衡移动

一.化学平衡移动:1.在反应速率(v )-时间(t )图象中,在保持平衡的某时刻t 1改变某一条件前后,V 正、V 逆的变化有两种:V 正、V 逆同时突变——温度、压强、催化剂的影响 V 正、V 逆之一渐变——一种成分浓度的改变 对于可逆反应:mA(g) + nB(g) pc(g) + qD(g) + (正反应放热)反应条件条件改变v 正v 逆v 正与v 逆关系平衡移 动方向图示 选项浓 度增大反应物浓度 减小反应物浓度 增大生成物浓度 减小生成物浓度加快 减慢 不变 不变 不变 不变 加快 减慢 v 正>v 逆 v 正<v 逆 v 正<v 逆 v 正>v 逆 正反应方向 逆反应方向 逆反应方向 正反应方向 B C B C 压 强m+n >p+q m+n <p+q m+n =p+q 加压加快 加快 加快 加快 加快 加快 v 正>v 逆 v 正<v 逆 v 正=v 逆 正反应方向 逆反应方向 不移动 A A E m+n >p+q m+n <p+q m+n =p+q 减压 减慢 减慢 减慢 减慢 减慢 减慢 v 正<v 逆 v 正>v 逆 v 正=v 逆 逆反应方向 正反应方向 不移动 D D F温 度 升 温 降 温 加快 减慢 加快 减慢 v 正<v 逆 v 正>v 逆 逆反应方向 正反应方向 A D 催化剂加快 加快加快v 正=v 逆不移动E【总结】增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
增大压强,化学平衡向系数减小的方向移动;减小压强,平衡会向系数增大的方向移动。
升高温度,平衡向着吸热反应的方向移动;降低温度,平衡向放热反应的方向移动。
催化剂不改变平衡移动2.勒沙持列原理:如果改变影响平衡的一个条件(如浓度、压强和温度等),平衡就向着能够减弱这种改变的方向移动。
其中包含:①影响平衡的因素:浓度、压强、温度三种;②原理的适用范围:只适用于一项条件发生变化的情况(即温度或压强或一种物质的浓度),当多项条件同时发生变化时,情况比较复杂;③平衡移动的结果:只能减弱(不可能抵消)外界条件的变化。
高中化学 化学平衡移动判断方法口诀规律总结

影响化学平衡的因素•影响化学平衡的因素:(1)浓度在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都可以使化学平衡向正反应方向移动;增大生成物的浓度或减小反应物的浓度,都可以使化学平衡向逆反应方向移动。
(2)压强对反应前后气体总体积发生变化的反应,在其他条件不变时,增大压强会使平衡向气体体积缩小的方向移动,减小压强会使平衡向气体体积增大的方向移动。
对于反应来说,加压,增大、增大,增大的倍数大,平衡向正反应方向移动:若减压,均减小,减小的倍数大,平衡向逆反应方向移动,加压、减压后v一t关系图像如下图:(3)温度在其他条件不变时,温度升高平衡向吸热反应的方向移动,温度降低平衡向放热反应的方向移动对于,加热时颜色变深,降温时颜色变浅。
该反应升温、降温时,v—t天系图像如下图:(4)催化剂由于催化剂能同等程度地改变正、逆反应速率,所以催化剂对化学平衡无影响,v一t图像为稀有气体对化学反应速率和化学平衡的影响分析:1.恒温恒容时充入稀有气体体系总压强增大,但各反应成分分压不变,即各反应成分的浓度不变,化学反应速率不变,平衡不移动。
2.恒温恒压时充入稀有气体容器容积增大各反应成分浓度降低反应速率减小,平衡向气体体积增大的方向移动。
3.当充入与反应无关的其他气体时,分析方法与充入稀有气体相同。
•化学平衡图像:1.速率一时间因此类图像定性揭示了随时间(含条件改变对化学反应速率的影响)变化的观律,体现了平衡的“动、等、定、变”的基本特征,以及平衡移动的方向等。
2.含量一时间一温度(压强)图常见的形式有下图所示的几种(C%指某产物百分含量,B%指某反应物百分含量),这些图像的折点表示达到平衡的时间,曲线的斜率反映了反应速率的大小,可以确定T(p)的高低(大小),水平线高低反映平衡移动的方向。
3.恒压(温)线该类图像的纵坐标为物质的平衡浓发(c)或反应物的转化率(α),横坐标为温度(T)或压强(p),常见类型如下图:小结:1.图像分析应注意“三看”(1)看两轴:认清两轴所表示的含义。
高中化学高一化学PPT课件化学平衡移动

• [方法点拨]平衡正向移动与反应物的转化 率关系 • 平衡正向移动时反应物的转化率如何变化, 这要根据具体反应及引起平衡移动的具体 原因而定,不能一概而论。 • (1)由于温度或压强改变而引起平衡正向 移动时,反应物的转化率必定增大。 • (2)由增加反应物浓度引起平衡正向移动 时,有以下几种情况:
• (2)浓度的变化,平衡移动会使浓度变化, 但是浓度的变化不一定使平衡移动。 • (3)各组分百分含量的变化。 • (4)平均相对分子质量的变化。 • (5)颜色的变化(颜色变化,平衡不一定发 生移动)。 • (6)混合气体密度的变化(密度变化,平衡 不一定发生移动,密度不变,平衡也不一 定不移动)。 • (7)转化率的变化。
• (2)压强:在有气体参加的可逆反应里, 气体总体积缩小的方向 在其他条件不变时,增大压强,平衡向 移动。 • 压强对平衡的影响,实际上就是浓度对平 衡的影响,只有当这些“改变”能改变反 应物或生成物的浓度时,平衡才可能移动。 由于压强对固态、液态物质体积影响非常 小,压强的改变几乎不影响这类体系的平 衡。在考虑压强对不均匀体系平衡的影响 时,只需考虑对参加反应的气态物质影响 即可。
• (4)同等程度地改变反应混合物中各物质 的浓度时,应视为压强的影响。 • 3.平衡移动会有哪些量发生变化 • (1)反应速率的变化(引起平衡移动的本质, 但反应速率变化也可能平衡不移动),主 要看v(正)与v(逆)是否相等,如果 v(正)≠v(逆),则平衡必然要发生移动,如 v(正)、v(逆)同时改变,但始终保持相等, 则平衡不移动。
• 二、化学平衡图像总结:
速率变化 ①增大 反应物 浓度 v(正)、v(逆) 均 增大,且v(正 )>v(逆)
平衡 体系
条件变 化
化学平衡移动原理

化学平衡移动原理一、化学平衡移动的概念改变反应条件,可逆反应的平衡遭到破坏,从一个旧平衡变成一个新平衡,化学平衡状态发生改变,就叫化学平衡移动。
二、化学平衡移动的原理1、总规律:化学平衡总是朝着速率大的方向移动。
这是化学平衡移动的本质,是化学平衡移动的原因,是化学平衡移动的总规律。
2、勒夏特列原理:在其他条件不变的条件下,改变一个条件,化学平衡朝着减弱这种改变的方向移动。
这是勒夏特列总结出来的平衡移动规律。
具体来说:增加反应物的浓度,就朝着减少反应物的浓度方向移动;减少反应物的浓度,就朝着增加反应物的浓度方向移动。
增加生成物浓度,就朝着减小生成物浓度的方向移动;减少生成物的浓度,就朝着增加生成物的浓度方向移动。
增大气体压强,就朝着减小气体压强的方向移动;减少气体压强,就朝着增大气体压强的方向移动。
升高温度,就朝着降低温度的方向移动;降低温度就朝着升高温度的方向移动。
三、化学平衡移动的分规律1、加入纯固体,浓度不改变,速率不改变,平衡不移动。
2、溶液中加入不参加反应的离子对应的固体,浓度不改变,速率不改变,平衡不移动。
3、同温同体积下,加入不参加反应的气体(如稀有气体),气体浓度不改变,速率不改变,平衡不移动。
4、增大表面积,等倍增大正逆反应速率,平衡不移动。
5、对于气体分子数不变的反应,增大压强,等倍增加正逆反应速率,平衡不移动;减小压强,等倍减小正逆反应速率,平衡不移动。
6、使用催化剂,等倍增加正逆反应速率,平衡不移动。
五、强化练习1、在可逆反应X+2Y2Z △H<0中,X、Y、Z是三种气体,为了有利于Z的生成,应采用的反应条件是()A、高温高压B、高温低压C、低温低压D、低温高压2、下列事实不能用勒夏特列原理解释的是()A、往硫化氢水溶液中加碱有利于S2-的增多B、加入催化剂有利于氨氧化的反应C、高压有利于合成氨的反应D、及时分离出氨有利于合成氨的反应4、在某温度下,反应ClF(g) +F 2 (g)ClF 3 (g) △H=-268KJ/mol ,在密闭容器中达到平衡。
第3讲 化学平衡的移动

第3讲化学平衡的移动1.化学平衡状态:`可逆反应在一定条件下进行到一定程度时,正反应速率和逆反应速率相等,反应混合物中各组份的浓度保持不变的状态,称为化学平衡状态,简称化学平衡。
2.化学平衡的移动(1)平衡移动的原因(2)影响平衡移动的条件①增大反应物浓度或减小生成物浓度,v正’> v逆’,平衡朝着正反应方向移动;减小反应物浓度或增大生成物浓度,v正’< v逆’,平衡朝着逆反应方向移动。
②增大体系压强,平衡朝着气态物质减小的方向移动;体积减小方向反应速率增加> 体积增大方向反应速率增加。
减小体系压强,平衡朝着气态物质增加的方向移动,体积减小方向反应速率减小> 体积增大方向反应速率减小。
③升高体系温度,平衡朝着吸热方向移动,放热方向速率增加< 吸热方向速率增加。
降低体系温度,平衡朝着放热方向移动,放热方向速率减小< 吸热方向速率减小。
④催化剂同等程度增加正逆反应速率,v正’= v逆’,不使化学平衡发生移动。
(3)勒夏特列原理,也叫化学平衡移动原理,①表述为:改变影响化学平衡的一个因素,平衡将向着能够减弱这种改变的方向移动。
②平衡移动只能“减弱”改变,而不能“阻止”改变。
③勒沙特列原理适用于任何平衡体系,包括化学反应平衡、电离平衡、水解平衡、溶解平衡。
例1.(2007·全国I理综,13)下图是恒温下某化学反应的反应速率随反应时间变化的示意图。
下列叙述与示意图不相符合的是()A.反应达平衡时,正反应速率和逆反应速率相等B.该反应达到平衡态I后,增大反应物浓度,平衡发生移动,达到平衡态ⅡC.该反应达到平衡态I后,减小反应物浓度,平衡发生移动,达到平衡态ⅡD.同一种反应物在平衡态I和平衡态Ⅱ时浓度不相等【答案】C【解析】增大反应物浓度,正反应速率增大,逆反应速率不变,平衡正向移动,达到新的平衡,各物质浓度与原平衡不同,C错误。
3.用v-t 图像分析化学平衡的移动 (1)改变反应物浓度 增大反应物浓度 减小反应物浓度平衡正向移动 平衡逆向移动(2)改变生成物浓度 增大生成物浓度 减小生成物浓度平衡逆向移动 平衡正向移动(3)改变气体体系的压强 增大压强 减小压强平衡向体积缩小方向移动 平衡向体积增大方向移动(4)改变温度 升高温度 降低温度平衡向吸热方向移动 平衡向放热方向移动v t v 正 v 逆 0 t 1 t 2 t 3 v 正=v 逆 v 正 v 逆vtv 正 v 逆t 1t 2t 3v 正=v 逆v 逆 v 正v t v 正v 逆 0t 1 t 2 t 3 v 正=v 逆 v 正 v 逆 vtv 正 v 逆t 1t 2t 3v 正=v 逆 v 逆v 正v t v 正 v 逆0 t 1 t 2 t 3 v 正=v 逆v 正 v 逆vtv 正 v 逆t 1t 2t 3v 正=v 逆 v 逆v 正v t v 正 v 逆t 1 t 2 t 3 v 正=v 逆 v 正v 逆vtv 正 v 逆t 1t 2t 3v 正=v 逆v 逆v 正(5)加催化剂例2.反应2SO 2(g)+O 2(g) 2SO 3(g) △H<0,在一定条件下达到平衡后,改变下列条件平衡发生移动,请画出改变下列条件后的反应速率与时间的关系图。
高中化学【化学平衡移动原理及应用】

化学平衡移动原理及应用目标要求 1.通过实验探究,了解浓度、温度、压强等对化学平衡的影响,能用相关理论解释其一般规律。
2.通过对图形、图表的阅读,进行初步加工、吸收、有序存储,并做出合理的解释。
1.化学平衡移动的过程2.化学平衡移动与化学反应速率的关系(1)v正>v逆:平衡向正反应方向移动。
(2)v正=v逆:反应达到平衡状态,平衡不移动。
(3)v正<v逆:平衡向逆反应方向移动。
3.影响化学平衡的因素(1)若其他条件不变,改变下列条件对化学平衡的影响如下:改变的条件(其他条件不变)化学平衡移动的方向浓度增大反应物浓度或减小生成物浓度向正反应方向移动减小反应物浓度或增大生成物浓度向逆反应方向移动压强(对有气体参加的反应) 反应前后气体体积改变增大压强向气体分子总数减小的方向移动减小压强向气体分子总数增大的方向移动反应前后气体体积不变改变压强平衡不移动温度升高温度向吸热反应方向移动降低温度向放热反应方向移动催化剂同等程度地改变v正、v逆,平衡不移动(2)勒·夏特列原理如果改变影响化学平衡的条件之一(如温度、压强以及参加反应的物质的浓度),平衡将向着能够减弱这种改变的方向移动。
(3)“惰性气体”对化学平衡的影响 ①恒温恒容条件原平衡体系―――――→充入惰性气体体系总压强增大―→体系中各组分的浓度不变―→平衡不移动。
②恒温恒压条件原平衡体系―――――→充入惰性气体容器容积增大,各反应气体的分压减小 ―→体系中各组分的浓度同倍数减小(等效于减压)应用体验根据化学平衡原理解答下列问题:在体积不变的密闭容器中发生N 2(g)+3H 2(g)2NH 3(g) ΔH =-92.4 kJ·mol -1,只改变一种外界条件,完成下表:改变条件 平衡移动方向氢气的转化率(增大、减小或不变)氨气的体积分数(增大、减小或不变)增大氮气的浓度 增大氨气的浓度升温 充入适量氩气答案 (从左到右,从上到下)正向 增大 逆向 减小 增大 逆向 减小 减小 不移动 不变 不变(1)化学平衡发生移动,化学反应速率一定改变;化学反应速率改变,化学平衡也一定发生移动(×)(2)升高温度,平衡向吸热反应方向移动,此时v放减小,v吸增大(×)(3)C(s)+CO2(g)2CO(g)ΔH>0,其他条件不变时,升高温度,反应速率v(CO2)和CO2的平衡转化率均增大(√)(4)化学平衡正向移动,反应物的转化率不一定增大(√)(5)向平衡体系FeCl3+3KSCN Fe(SCN)3+3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜色变浅(×)(6)对于2NO2(g)N2O4(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色变浅(×)题组一选取措施使化学平衡定向移动1.COCl2(g)CO(g)+Cl2(g)ΔH>0,当反应达到平衡时,下列措施:①升温②恒容通入惰性气体③增加CO浓度④减压⑤加催化剂⑥恒压通入惰性气体,能提高COCl2转化率的是()A.①②④B.①④⑥C.②③⑤D.③⑤⑥答案 B解析该反应为气体体积增大的吸热反应,所以升温和减压均可以促使反应正向移动。
高一化学知识点化学平衡的移动规律和平衡常数的应用原理

高一化学知识点化学平衡的移动规律和平衡常数的应用原理高一化学知识点:化学平衡的移动规律和平衡常数的应用原理化学平衡是化学反应达到动态平衡状态的时候,反应物和生成物的浓度保持在一定比例下不再变化。
在化学平衡中,物质的转化虽然停止,但是反应仍然在继续进行。
化学平衡的移动规律以及平衡常数的应用原理是我们理解和研究化学反应平衡的重要内容。
一、化学平衡的移动规律在化学平衡中,当外界条件发生改变时,平衡系统会产生一定的移动以重新建立新的平衡状态。
化学平衡的移动规律包括 Le Chatelier 原理和浓度-时间关系。
1. Le Chatelier 原理Le Chatelier 原理是指在一个达到平衡状态的反应系统中,当外界条件发生变化时,系统会调整自身以减小对外界变化的影响。
具体来说,当平衡系统的温度、压力、浓度等发生变化时,系统会向以减小变化影响为目标的方向进行移动。
- 温度的影响:在反应热是吸放热的情况下,温度升高会使平衡位置向吸热的方向移动,降低会使平衡位置向放热的方向移动。
反应热是放热的情况与上述相反。
- 压力的影响:压力的增加会使平衡系统向分子数少的方向移动,压力的降低会使平衡系统向分子数多的方向移动。
此处需注意,只有当反应物和生成物的摩尔数之和不相等的情况下,改变压力才会对平衡位置产生影响。
- 浓度的影响:增加某一反应物的浓度会使平衡系统向生成物的方向移动,增加某一生成物的浓度会使平衡系统向反应物的方向移动。
而当浓度只增加一个无关物质时,平衡位置不会发生改变。
2. 浓度-时间关系当反应物浓度逐渐增加或减少时,反应速率会相应改变。
在开始反应时,反应物浓度较高,反应速率较快,但随着反应进行,浓度逐渐减小,反应速率也会变慢。
最终,当反应物浓度减小至一定水平时,反应速率趋于稳定,达到平衡。
二、平衡常数的应用原理平衡常数是用于描述化学平衡中反应物和生成物浓度之间的相对关系的数值。
平衡常数的大小可用于预测平衡位置的偏向,以及影响平衡位置的外界因素。
高中化学 平衡移动最全知识总结

一、化学平衡的移动1.化学平衡的移动(1)定义达到平衡状态的反应体系,条件改变,引起平衡状态被破坏的过程。
(2)化学平衡移动的过程2.影响化学平衡移动的因素(1)温度:在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡向放热反应方向移动。
(2)浓度:在其他条件不变的情况下,增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
(3)压强:对于反应前后总体积发生变化的化学反应,在其他条件不变的情况下,增大压强,化学平衡向气体体积减小的方向移动;减小压强,化学平衡向气体体积增大的方向移动。
(4)催化剂:由于催化剂能同时同等程度地增大或减小正反应速率和逆反应速率,故其对化学平衡的移动无影响。
3.勒夏特列原理在密闭体系中,如果改变影响化学平衡的一个条件(如温度、压强或浓度等),平衡就向能够减弱这种改变的方向移动。
二、外界条件对化学平衡移动的影响1.外界条件的变化对速率的影响和平衡移动方向的判断在一定条件下,浓度、压强、温度、催化剂等外界因素会影响可逆反应的速率,但平衡不一定发生移动,只有当v正≠v逆时,平衡才会发生移动。
对于反应mA(g)+nB(g)pC(g)+qD(g),分析如下:2.浓度、压强和温度对平衡移动影响的几种特殊情况(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H2(g)+I2(g)2HI(g),压强的改变对平衡无影响。
但增大(或减小)压强会使各物质的浓度增大(或减小),混合气体的颜色变深(或浅)。
(4)恒容时,同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响,增大(减小)浓度相当于增大(减小)压强。
(5)在恒容容器中,当改变其中一种气态物质的浓度时,必然会引起压强的改变,在判断平衡移动的方向和物质的转化率、体积分数变化时,应灵活分析浓度和压强对化学平衡的影响。
化学反应中的平衡移动与影响因素总结知识点总结

化学反应中的平衡移动与影响因素总结知识点总结在化学反应中,平衡移动是指反应物与生成物浓度之间的变化。
平衡移动的方向和速率受多种因素的影响。
本文将总结几个与平衡移动相关的重要知识点,并探讨影响平衡移动的因素。
一、平衡移动的基本原理平衡移动是指在化学反应中,当达到化学平衡后,反应物和生成物的浓度发生变化的过程。
平衡移动的方向可以是向前移动(反应物浓度减小、生成物浓度增加),也可以是向后移动(反应物浓度增加、生成物浓度减小),或者不发生移动(反应物和生成物浓度不变)。
平衡移动的方向取决于反应的平衡常数(Keq)。
当Keq大于1时,反应偏向生成物。
反之,当Keq小于1时,反应偏向反应物。
当Keq等于1时,反应物和生成物的浓度保持不变。
二、影响平衡移动的因素1. 温度温度是影响平衡移动的重要因素之一。
根据Le Chatelier原理,当温度升高时,平衡反应偏向吸热反应,即吸热反应的反应物浓度减小,生成物浓度增加;当温度降低时,平衡反应偏向放热反应,即放热反应的反应物浓度增加,生成物浓度减小。
2. 压力/浓度压力或浓度的改变也会影响平衡移动的方向。
对于气体反应而言,增加总压力(或者减小体积)会导致平衡反应移动到摩尔数较少的一侧,以减小总摩尔数。
相反,减小总压力(或者增大体积)会导致平衡反应移动到摩尔数较多的一侧。
对于溶液反应而言,增加溶质浓度会导致平衡反应移动到生成物的方向,以达到稀释溶液中的溶质的目的。
降低溶质浓度则会导致平衡反应移动到反应物的方向。
3. 催化剂催化剂是能够加快反应速率但不参与反应的物质。
催化剂对平衡移动的影响主要是加快反应达到平衡的速度,而并没有改变反应的平衡常数。
因此,催化剂对反应物和生成物浓度的影响很小,不会改变平衡移动的方向。
4. 配位数对于配位化合物的形成反应,配位数是一个重要的影响因素。
在反应过程中,改变配位数可以促进或抑制配位化合物的形成。
例如,增加配位数可以使先前存在的比配位数更低的化合物分解生成更高配位数的化合物。
高一化学上册知识点总结

高一化学上册知识点总结(实用版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的教育资料,如幼儿教案、音乐教案、语文教案、知识梳理、英语教案、物理教案、化学教案、政治教案、历史教案、其他范文等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, this store provides various types of educational materials for everyone, such as preschool lesson plans, music lesson plans, Chinese lesson plans, knowledge review, English lesson plans, physics lesson plans, chemistry lesson plans, political lesson plans, history lesson plans, and other sample texts. If you want to learn about different data formats and writing methods, please stay tuned!高一化学上册知识点总结本店铺为各位同学整理了《高一化学上册知识点总结》,希望对您的学习有所帮助!1.高一化学上册知识点总结1、概念可逆反应中旧化学平衡的破坏、新化学平衡的建立,由原平衡状态向新化学平衡状态的转化过程,称为化学平衡的移动。
高中化学化学平衡的移动与影响因素

高中化学化学平衡的移动与影响因素化学平衡是化学反应达到一种动态平衡状态的过程,当反应物和生成物的浓度保持不变时,我们就可以说反应已经达到平衡。
在平衡状态下,虽然反应物和生成物之间的反应仍然进行,但是反应速率已经相等,呈现出动态平衡的状态。
化学平衡是研究化学反应的重要内容之一,了解化学平衡的移动与影响因素对于我们理解和掌握化学反应具有重要意义。
一、化学平衡的移动化学平衡的移动指的是反应物和生成物浓度的变化方向。
根据勃朗斯特-伊富尔方程,可以得到描述化学平衡移动的公式:Kc = ([C]^c[D]^d)/([A]^a[B]^b)其中,[A]、[B]、[C]、[D]分别表示反应物A、B和生成物C、D的浓度,a、b、c、d分别表示反应物和生成物的摩尔系数。
Kc为平衡常数,用于描述反应在平衡状态下的浓度比例。
1. 影响化学平衡移动的因素(1)浓度变化:根据勃朗斯特-伊富尔方程,改变反应物和生成物的浓度可以影响化学平衡的位置。
当增加某一种物质的浓度时,根据公式可以看出,平衡会向反应物的一侧移动。
反之,减少某一种物质的浓度,平衡会向生成物的一侧移动。
(2)温度变化:温度变化也是影响化学平衡移动的重要因素。
根据反应物与生成物的焓变,可以推导出化学平衡与温度之间的关系。
当温度升高时,平衡系统会向吸热的方向移动,即向生成物的一侧移动。
反之,当温度降低时,平衡系统会向放热的方向移动,即向反应物的一侧移动。
(3)压力变化:对于气相反应来说,压力的变化也会影响化学平衡的移动。
根据利希特原理,当增加压力时,平衡系统会向压力减小的方向移动,即向生成物的一侧移动。
反之,当减小压力时,平衡系统会向压力增大的方向移动,即向反应物的一侧移动。
2. 示例以氮气和氢气生成氨气的反应为例,可以根据勃朗斯特-伊富尔方程以及影响平衡移动的因素进行分析。
N2(g) + 3H2(g) ⇌ 2NH3(g)根据该化学方程式,可以得到平衡常数表达式为:Kc = [NH3]^2/([N2][H2]^3)假设在平衡状态下,氮气和氢气的浓度分别为0.1 mol/L和0.2mol/L,氨气的浓度为0.05 mol/L。
高中化学化学平衡的移动优秀课件

2HI 在压强为P1时, HI%
HI%随时间变化如图所示。当压强为P2时
P2
P1
( P2 > P1) ,图形将如何改变?
注意:1、 对反响前后气态物质总体积无变化的可逆反响,压强t
改变对正、逆反响速率改变倍数相同,因此,平衡不发生移动。
压强的不同只改变了反响达平衡的时间。
2、对只有固态或液态物参与的反响,压强改变对平衡无影响。
注意:浓度改变指气体、溶液的浓度改变,对于固体、纯液体 〔水〕无法改变其浓度,故其量的增减看做平衡不移动。
思考:
(1) 10 mL 0.01 mol/LFeCl3+ 10 mL 0.01 mol/L KSCN
(2) 10 mL 0.01 mol/LFeCl3+10 mL 0.01 mol/L KSCN +10 mLH2O (3) 10 mL 0.01 mol/LFeCl3+ 10 mL 1 mol/L KSCN (4) 20 mL 0.01 mol/LFeCl3 + 20 mL 0.01 mol/L KSCN
A%Leabharlann P1 P2tP1
P2
a+b c
四、催化剂对化学平衡无影响
催化剂使用,对化学平衡移动无影响 可用下图表示:
反
v正=v逆
应
速
率
反应过程
勒夏特列原理:
如果改变影响平衡的一个条件〔如:浓度、压强或温 度等,〕平衡就向能够减弱这种改变的方向移动。
【注意】
〔1〕当影响平衡的一个条件改变时,通过平衡移动只 能“减弱〞这种改变,而不能“抵消〞这种改变。
1L
2L
参加
1L
1 mol N2和3 molH2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[单选]一捻金的功能是()A.消食化滞,泻火通便B.消食导滞,祛痰通便C.消食化滞,健脾和胃D.健脾和胃,消食化滞E.健胃消积,驱虫 [单选]RR表示()A.比值比B.相对危险度C.特异危险度D.人群特异危险度E.特异危险度百分比 [单选]线形锁最弱点位于三角锁的()。A、中部B、起点C、终点 [单选]根据《信访条例》规定,涉及两个或者两个以上行政机关的信访事项,由所涉及的行政机关协商受理;受理有争议的,由()决定受理机关。A.其主管机关B.其共同的上一级行政机关C.其上级政府D.同级信访机构 [单选]根据《行政复议法》的规定,下列各项中不属于行政复议中一并申请审查范围的有()。A.国务院各部门的规定B.省政府所在地的市的人民政府制定的规章C.县级以上地方人民政府及其工作部门的规定D.乡、镇人民政府的规定 [单选]载运危险货物船舶的船员,应当持有()颁发的适任证书的培训合格证,熟悉所在船舶载运危险货物安全知识和操作规程.A.主管机关B.船厂C.海事管理机构 [填空题]地秤推拉支点和重点时,若在承载器上加砝码后计量杠杆达到平衡,其示值误差是()。 [单选]设L是圆周x2+y2=a2(a>0)负向一周,则曲线积分(x3-x2y)dx+(xy3-y3)dy的值为:()A.πa4B.-πa4C.-(π/2)a4D.(π/2)a4 [单选,A2型题,A1/A2型题]下列肾功能监测的指标中,临床很少应用的是()A.肾小球滤过率(GFR)B.血尿素氮(BUN)C.血肌酐(Cr)D.肾血流量测定E.肾小管功能测定 [单选]切割装置正常开车前,应试切20条编织袋,检查切割()是否在要求范围内。A.长度B.宽度C.厚度D.废品 [多选]下列关于通货膨胀对于业绩评价的影响的表述中,不正确的有()。A、只有通货膨胀水平较高时,才考虑通货膨胀对于业绩评价的影响B、只有通货膨胀水平较高时,才会对财务报表造成影响C、在通货膨胀时期,为了在不同时期业绩指标之间建立可比性,可以用非货币资产的个别价格(现行 [单选]经过格式化但未写入数据的软盘上()。A、一无所有B、仅有扇区标志C、仅有扇区标志和引导记录D、有扇区标志、引导记录、文件分配表和文件目录表 [判断题]工艺美观,不用每天施工完毕后清理垃圾余料。()A.正确B.错误 [多选]建筑石膏的技术性质有()。A、微膨胀性B、凝结硬化快C、抗冻性强D、耐水性强E、防水性强 [单选]对易燃易爆化学物品经营单位扩建工程竣工时未经消防验收或者经验收不合格擅自使用的,经公安消防机构责令限期改正后逾期不改的,应当()。A、责令立即改正B、责令停止施工C、责令停止使用,可以并处罚款D、处罚款 [单选]环境中的主要致癌因素是A.物理有害因素B.化学有害因素C.生物有害因素D.食物中有害因素E.其他因素 [单选]()负担指农民依照法律法规和政策规定向国家提供的经济和劳务负担。A.国家B.隐性C.社会D.显性 [多选]U1930web中可以配置的有:()A.预定会议B.一号通C.无条件呼叫前转D.license加载 [单选,A1型题]早产儿使用铁剂预防贫血最初的月龄是()A.1个月B.2个月C.3个月D.4个月E.5个月 [判断题]浮选过程中,应对细泥含量大及难浮选煤采用较小充气量,对易浮选煤采用较大充气量。A.正确B.错误 [单选]分散控制系统中的()根据各工艺系统的特点,协调各系统的参数设定,它是整个工艺系统的协调者和控制者。A、过程控制级;B、过程管理级;C、生产管理级;D、经营管理级。 [单选]为明确上消化道大出血原因,首选的检查方法是()A.上消化道造影B型超声检查C.纤维内镜检查D.选择性动脉造影检查E.胸片 [单选]借记回执信息最长返回时间不得小于基准时间,不得超过()个法定工作日,借记回执信息最长返回时间内遇法定节假日和小额支付系统停运日顺延。A.2B.3C.4D.5 [问答题,简答题]对于一个一般的通信系统,试给出其系统模型框图,并结合此图,解释数据处理定理。 [单选]关于鼻咽纤维血管瘤下列说法不相符的是()A.好发于10~25岁的男性青年B.肿瘤具有向邻近组织扩张能力C.肿瘤起源于枕骨底部、蝶骨体及翼突内侧的骨膜D.DSA及血管栓塞可减少术中出血E.活检确诊后手术切除 [单选,A1型题]卫生人力资源需求现状预测法适用于()的卫生人力资源规划预测。A.短期B.中期C.长期D.远期E.近期 [判断题]安消防要求,门禁系统必须断电开锁,门也一定要选外开式。A.正确B.错误 [单选]用于记录核算反映财政预算资金和纳入预算管理的政府性基金的收入和支出的账户是()。A.特设专户B.国库单一账户C.财政部门零余额账户D.预算单位零余额账户 [单选]某二叉树为单枝树(即非叶子节点只有一个孩子节点)且具有n个节点(n>1)则该二叉树()。A.共有n层,每层有一个节点B.共有log2n层,相邻两层的节点数正好相差一倍C.先序遍历序列与中序遍历序列相同D.后序遍历序列与中序遍历序列相同 [单选]AccordingtotheCodeofFederalRegulations,onvesselsotherthanriverferryboatsandrivervessels,howareperiodiclifeboatweighttestsrequiredtobeconducted?()A.Thelifeboatisloweredtonearthewater,loadedwiththeallowedcapacity,loweredintothewateruntilafloat,then [单选]()通过手指上的弯曲传感器、扭曲传感器和手掌上的弯度传感器、弧度传感器,来确定手及关节的位置和方向,从而实现环境中的虚拟手及其对虚拟物体的操纵。A.跟踪球B.数据手套C.头盔显示器D.立体眼镜 [问答题,简答题]广告策划的作用表现在哪几个方面? [填空题]在站点施工时,严禁用()直接塞入插座内供电。 [单选]根本违约和一般违约的分类依据是()。A.按照违约行为是否完全违背缔约原则B.按照违约行为是否完全违背缔约目的C.按照违约行为是否完全违背缔约内容D.按照违约行为是否完全违背缔约条例 [单选]物质资源和能量资源与()一起构成了现代社会发展的三大战略资源。A.科技资源B.自然资源C.石油资源D.信息资源 [单选]一孕妇产前检查胎儿双顶径12.2cm,剖宫产后胎儿经颅超声检查示胎儿脑室系统形态失常,第三脑室呈圆形,无回声区内未见光点群回声,脑组织受压变薄萎缩,脑室宽度为7mm,最可能的诊断是()。A.脑出血B.脑积水C.脑肿瘤Dandy-Walker综合征E.HIE [单选]所钻井的()是指该井在省、市、县、乡、村的位置。A.构造位置B.地理位置C.测线位置D.坐标位置 [单选,A2型题,A1/A2型题]关于溶血性贫血患者的血象,下列说法错误的是()。A.嗜多色性红细胞增多B.网织红细胞减少C.血涂片中可见幼红细胞D.出现点彩红细胞E.成熟红细胞中出现Howell-Jolly小体 [单选]方某工作已满15年,2009年上半年在甲公司已休带薪年休假(以下简称年休假)5天;下半年调到乙公司工作,提出补休年休假的申请。乙公司对方某补休年休假申请符合法律规定的答复是()。A.不可以补休年休假B.可补休5天年休假C.可补休10天年休假D.可补休15天年休假 [单选,A3型题]婴儿胎龄40周,生后5小时,择期剖宫产娩出,生后不久出现呻吟,呼吸急促,口中少许泡沫伴口周发绀。查体:呼吸70次/分,双肺呼吸音粗,可闻及粗湿啰音,心率140次/分,胸骨左缘2.3肋间闻及Ⅰ~Ⅱ级收缩期杂音。血气分析结果:pH7.32,PaO26.4kPa,PaCO26.7kPa,BE-6
