国家药品抽验发出质量风险提示的品种
关于2023年高预警药物的分类目录

关于2023年高预警药物的分类目录高预警药物是指那些具有潜在严重不良反应、药物相互作用风险高、用药错误风险高、或有特殊使用要求的药物。
为了确保患者安全,医疗机构和药品监督管理部门通常会对这类药物进行特别的监管。
本文档旨在概述2023年高预警药物的分类目录,以及相关的使用和管理建议。
高预警药物分类高预警药物分为以下几类:1. 抗凝血药物- 肝素类- 华法林- 新型口服抗凝剂(如达比加群、沙库巴曲等)2. 抗小板药物- 阿司匹林- 氯吡格雷- 替格瑞洛3. 糖皮质激素- 泼尼松- 甲泼尼龙- 地塞米松4. 抗肿瘤药物- 蒽环类抗生素(如阿霉素)- 靶向治疗药物(如伊马替尼)- 生物制剂(如利妥昔单抗)5. 心血管药物- β受体阻滞剂- 钙通道阻滞剂- ACE抑制剂/ARBs6. 神经精神类药物- 抗抑郁药(如选择性5-羟色胺再摄取抑制剂)- 抗精神病药(如奥氮平、喹硫平)- 镇静催眠药(如苯二氮卓类药物)7. 抗生素- β-内酰胺类(如头孢菌素、氨曲南)- 氨基糖苷类(如庆大霉素、阿米卡星)- 氟喹诺酮类(如莫西沙星、左氧氟沙星)8. 抗病毒药物- 抗HIV药物(如奈韦拉平、利托那韦)- 抗乙型肝炎病毒药物(如恩替卡韦、替诺福韦)使用和管理建议1. 处方审核:对于高预警药物,药师在审核处方时应特别注意药物的适应症、剂量、用药频率和时间,以及可能的药物相互作用。
2. 患者教育:患者在使用高预警药物时,应充分了解药物的用途、不良反应、正确的用药方法和可能的药物相互作用。
3. 用药监测:对于需要监测血药浓度、肝肾功能等指标的药物,应定期进行相关检查,以确保药物在安全范围内使用。
4. 药物相互作用评估:在使用高预警药物时,应评估与其他药物的相互作用,必要时调整剂量或更换药物。
5. 特殊人群用药:针对孕妇、哺乳期妇女、老年人、儿童和肝肾功能不全等特殊人群,应谨慎使用高预警药物,并根据实际情况调整剂量。
6. 紧急情况处理:在使用高预警药物过程中,如出现不良反应或其他突发情况,应立即停药并寻求医生帮助。
高预警药品分类目录2023

高预警药品分类目录2023
背景介绍:
高预警药品是指那些潜在存在较高风险,容易引发不良反应或意外事件的药物。
为了保障公众的用药安全,制定高预警药品分类目录具有重要意义。
目的:
本文档的目的是提供2023年的高预警药品分类目录,帮助医疗机构和患者更好地识别和管理高风险药物。
分类目录:
1. 特定人群禁用药:包括孕妇、哺乳期妇女、儿童等特定人群禁用的药物,可能对特定人群产生严重的不良反应。
2. 高度致敏药物:包括常见致敏反应较高的药物,例如青霉素类抗生素等,使用过程中需特别注意过敏风险。
3. 高危药物:包括治疗疾病所必需但潜在危险性较高的药物,例如抗凝剂和免疫抑制剂等,使用过程中需密切监测和管理。
4. 预防慎用药物:包括具有潜在严重不良反应但对某些疾病可能有预防效果的药物,例如糖尿病治疗药物等,应在严密监测下使用。
5. 交互作用药物:包括与其他药物存在严重相互作用的药物,可能增加药物效果或产生不良反应的风险,需谨慎搭配使用。
6. 安全用药提示药物:包括虽然使用相对安全但需特别注意使用技巧和注意事项的药物,例如麻醉药物等,需遵循医疗专业人员的指导使用。
备注:
本分类目录仅供参考,医疗机构和患者在使用药品时仍应遵循医生或药师的建议,并严格遵守药品使用说明书中的指导。
参考文献:
1. [麻省理工学院医院药物安全手册,2022年]
2. [国家药品监督管理局药品安全通报,2022年]
3. [中国药学会药物临床监测指南,2021年]。
关于2023年高预警药物的分类目录

关于2023年高预警药物的分类目录根据2023年高预警药物的分类,以下是该药物的分类目录:
类别一:危险药物
这一类别包括那些具有潜在危险性的药物。
这些药物可能会导致严重的副作用或依赖性,并且需要特别小心和谨慎地使用。
1. 麻醉药物:包括鸦片类药物、苯二氮䓬药物等。
2. 精神活性药物:包括抗精神病药物、抗抑郁药物等。
3. 镇痛药物:包括强效镇痛药物、非甾体抗炎药物等。
类别二:潜在风险药物
这一类别包括那些具有潜在风险的药物。
这些药物可能引起轻微的副作用或可能与其他药物产生相互作用。
1. 抗生素类药物:包括广谱抗生素、强力抗生素等。
2. 抗凝血药物:包括华法林、肝素等。
3. 免疫抑制药物:包括环孢素、甲氨蝶呤等。
类别三:限制使用药物
这一类别包括那些需要限制使用的药物。
这些药物可能在特定人群中产生不良反应或需要特别的监测和控制。
1. 儿童用药:包括儿童专用药物、儿童剂量药物等。
2. 孕妇用药:包括孕妇禁用药物、孕期限制药物等。
3. 老年人用药:包括老年人专用药物、用药注意事项等。
以上是关于2023年高预警药物的分类目录。
请根据实际情况和具体药物的安全性进行使用和管理。
高警示药品目录2023的最新版本

高警示药品目录2023的最新版本1. 什么是高警示药品目录?高警示药品目录是国家药品监督管理部门发布的一份重要清单,列出了一些具有较高风险和潜在危害的药品。
这些药品在使用过程中可能会引发严重的不良反应或者药物相互作用,因此需要特别谨慎使用。
2. 为什么需要更新高警示药品目录?随着药物研究和临床实践的不断发展,药品的安全性和风险性也在不断变化。
因此,为了及时提醒医务人员和患者,监管部门需要定期对高警示药品目录进行更新,以确保其中包含最新的信息和风险评估结果。
3. 高警示药品目录2023的更新内容根据最新公布的高警示药品目录2023,主要更新如下:(1) 新增药物1.药品A - 新增至高警示药品目录,因其在临床使用中出现了严重不良反应的报道。
2.药品B - 由于最新研究表明其与另一类药物存在严重的相互作用,被列入高警示药品目录。
(2) 药品调整1.药品C - 由于部分患者出现了新的不良反应,将其风险等级从中等调整至高警示。
(3) 警示提示1.针对某些高警示药品,明确了特定人群禁忌或慎用的提示,提醒临床医生和患者注意。
4. 如何正确使用高警示药品目录?在使用高警示药品目录时,医务人员和患者应当密切关注目录中的各类药品信息,了解药品的特点、潜在风险及禁忌情况。
在临床实践中,应遵循医疗指引,谨慎选择使用高警示药品,并密切观察患者的反应情况,在必要时及时调整治疗方案。
高警示药品目录的更新目的在于提高药物使用安全性,保障患者的健康。
因此,在日常临床实践中,应根据最新的高警示药品目录,结合患者的具体情况,科学合理地选择药物治疗方案,避免不必要的风险和不良反应发生。
综上所述,高警示药品目录2023的最新版本对于医疗行业和患者来说具有重要意义,希望广大医务人员和患者能够重视这份清单,加强药物安全应用意识,保障用药安全,最终实现更好的治疗效果。
结语高警示药品目录是一份重要的药品安全参考清单,及时了解和遵循目录中的相关信息对于确保患者用药安全和实现良好疗效至关重要。
专业发布:高警示药品高危药品推荐目录(2019版)

高警示药品推荐目录(2019版)目录高警示药品推荐目录(2019版) (1)一、高警示药品 (1)二、2019版高警示药品目录发布 (2)三、22个药品种类被列入高警示药品 (2)静脉途径给药的茶碱类 (2)生殖毒性药品 (3)四、13种药品被列入高警示药品 (3)阿托品注射液 (3)高锰酸钾外用制剂 (3)凝血酶冻干粉 (4)注射用三氧化二砷 (4)一、高警示药品高警示药品,即通常所说的高危药品,是指若使用不当或发生用药错误会对患者造成伤害/死亡的药品。
美国用药安全研究所(ISMP)的一项研究表明,大多数致死或造成严重伤害的用药错误案例仅涉及少数较特殊的药物;高警示药品引起的差错可能不常见,但一旦发生则后果非常严重。
由于高警示药品是近些年才逐渐从国外引入并引起关注的概念。
目前我国高警示药品的管理存在医务人员认知程度有待提高、不同医疗机构管理水平参差不齐、管理模式亟待统一等问题。
二、2019版高警示药品目录发布近日,中国药学会医院药学专业委员会发布了《中国高警示药品推荐目录(2019版)》。
与2015版目录相比,本次更新删除了腹膜和血液透析液、心脏停博液和依前列醇,加注了硫酸阿托品注射液的规格,并将加压素骨内注射的给药途径规范为骨髓腔内注射。
三、22个药品种类被列入高警示药品中国高警示药品推荐目录(2019版),将22个药品种类列入,包括口服降糖药、抗血栓药、氯化钠注射液、镇痛药/阿片类药物等。
静脉途径给药的茶碱类静脉途径给药的茶碱类包括茶碱、氨茶碱、二羟丙茶碱、多索茶碱等,主要用于急性哮喘、慢性阻塞性肺病急性发作及心源性哮喘的平喘治疗,但因其不良反应较多,治疗窗窄,在国内外的相关疾病诊治指南中,均不作为一线推荐。
静脉茶碱类国外应用较少,国内由于价格相对便宜,在一些基层医院仍应用较多。
生殖毒性药品生殖毒性药品是指可对雌性和雄性生殖系统和生殖过程造成损害的药品。
美国食品与药物管理局药品妊娠安全A~X分级中,D级和X级均具有生殖毒性,如沙利度胺、异维A酸、阿维A、来氟米特、维胺酯、甲氨蝶呤、利巴韦林、化疗药物、镇静催眠药物、他汀类药物等。
国家药监局关于7批次药品不符合规定的通告

国家药监局关于7批次药品不符合规定的通告文章属性•【制定机关】国家药品监督管理局•【公布日期】2021.10.09•【文号】国家药品监督管理局通告2021年第78号•【施行日期】2021.10.09•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家药监局通告2021年第78号关于7批次药品不符合规定的通告经湖南省药品检验研究院等4家药品检验机构检验,标示为中山万汉制药有限公司等5家企业生产的奥利司他胶囊等7批次药品不符合规定。
现将相关情况通告如下:一、经湖南省药品检验研究院检验,标示为中山万汉制药有限公司生产的3批次奥利司他胶囊不符合规定,不符合规定项目为鉴别和溶出度;标示为湖南迪诺制药股份有限公司生产的1批次奥利司他胶囊不符合规定,不符合规定项目为鉴别。
经大连市药品检验检测院检验,标示为三才石岐制药股份有限公司生产的1批次磷酸氯喹片不符合规定,不符合规定项目为含量测定。
经武汉药品医疗器械检验所检验,标示为青海宝鉴堂国药有限公司生产的1批次复方甘草口服溶液不符合规定,不符合规定项目为含量测定。
经江苏省食品药品监督检验研究院检验,标示为芜湖张恒春药业有限公司生产的1批次小儿止咳糖浆不符合规定,不符合规定项目为含量测定。
二、对上述不符合规定药品,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。
三、国家药品监督管理局要求相关省级药品监督管理部门依据《中华人民共和国药品管理法》,组织对上述企业和单位涉嫌生产销售假劣药品的违法行为立案调查,并按规定公开查处结果。
特此通告。
附件:1.7批次不符合规定药品名单2.不符合规定项目的小知识国家药监局2021年10月9日。
高预警药品分类2023年详解

高预警药品分类2023年详解引言本文旨在对2023年的高预警药品分类进行详细解释。
高预警药品是指那些在使用过程中可能引发严重不良反应或有潜在风险的药品。
了解这些分类对于药品监管和使用者十分重要。
分类说明根据2023年的最新规定,高预警药品被分为以下几类:1. 类别一:在使用过程中可能引发严重不良反应的药品。
这些药品对人体有潜在的危害,可能导致严重的副作用或不可逆转的损害。
2. 类别二:在使用过程中需要特殊监测和控制的药品。
这些药品可能对某些人群或特定疾病有较高的风险,需要严格的监测和控制措施。
3. 类别三:在使用过程中可能与其他药物或物质发生相互作用的药品。
这些药品可能会干扰其他药物的疗效或加剧其副作用,需要特别注意潜在的相互作用。
4. 类别四:在使用过程中可能引发滥用或依赖的药品。
这些药品可能具有成瘾性或潜在的滥用风险,需要特别注意合理使用和监测。
监管措施为了确保高预警药品的安全使用,相关监管机构采取了以下措施:1. 严格审批:高预警药品的上市审批过程更为严格,需要充分评估其安全性和有效性。
2. 警示标签:高预警药品的包装上会标注明显的警示标签,提醒使用者注意潜在风险和副作用。
3. 监测和报告:医疗机构和药品生产企业需要积极监测高预警药品的使用情况,并及时报告任何不良反应或意外事件。
4. 宣传和教育:相关监管机构会通过宣传和教育活动向医生、药剂师和患者传达高预警药品的正确使用方法和注意事项。
结论2023年的高预警药品分类对于保障药品使用者的安全至关重要。
了解这些分类和相关监管措施可以帮助医疗机构和患者做出明智的决策,减少药品使用过程中的风险和不良反应。
请注意,本文所提供的内容仅供参考,具体的高预警药品分类和监管措施可能因地区和时间而有所不同。
建议在实际应用中,参考当地的法律法规和权威机构的指导意见。
药品使用中的风险

药品使用中的风险管理内容药品使用中的风险、原因及风险管理措施合理用药与用药错误药品风险管理的2项技术(制度)药品风险来源、组成、起因及影响因素风险与风险管理的概念灾难!被称为20世纪最大的药物己烯雌酚致子代少女阴道腺癌(>300例)阴道腺癌己烯雌酚(1933-1972)苯甲醇—臀肌挛缩2004年湖北恩施州鹤峰县某乡495人(2-29岁)表现:跛行、八字腿、蛙行腿、难翘“二郎腿”、下蹲受限、皮肤凹陷手术费每人3000元/人,一个乡148.5万元千手观音21位演员中18人因药致聋氨基甙类抗生素耳聋耳毒性药物致听力残疾听力残疾60-80%系药源性伤害可避免的药物已知不良反应罗非昔布(万络)与心血管不良事件2004年默沙东宣布万络全球撤市齐二药“亮菌甲素”假药造成9人死亡有毒胶囊发古人云“是药三分毒”。
药物是“双刃剑”,不仅能治病,也能致病。
药品是一种高风险的物质。
药品13风险与风险管理14风险:可能发生的危险;遭受损失、伤害、不利或毁灭的可能性。
风险与之相对的是安全、获益(收益、利益)风险管理(risk management):人们对风险进行识别、分析、估计和处理的过程风险管理---研究风险发生规律和风险控制技术的一门管理科学。
通过有效组合各种相关技术(系统的、有计划的操作过程),有效防范并控制风险,妥善处理风险所致损失的后果,以期以最低成本,获得最大安全保障的管理方法。
《风险管理与保险》威廉斯(1964)风险管理目的是使风险最小化……预先评估风险的性质、危害的程度、发生的条件、发展的趋势,从而预置管理的机制制度。
对已经发生的风险事件进行评估,确认性质、程度、条件、趋势,从而采取针对性的管控措施,防止蔓延和重复发生。
不断地检讨已有的机制与制度,分析其存在的漏洞,及时予以弥补。
风险管理内容16对于不同的药品风险,应予不同的风险干预措施。
根据《中华人民共和国药品管理法》,在我国对于发现或发生药品风险时可以采取的措施有:暂停上市前研究和审批;开展分析、评价,发起有关研究; 修改药品说明书;限制使用;进行质量抽验;提高质量标准;召回、撤市风险控制和干预措施17美国:2003年《上市前风险评估指南》《风险最小化执行方案的制定与应用指南》 《药物警戒管理规范与药物流行病学评价指南》 欧盟:2005年《促进欧盟实施风险管理策略实施特别工作组进展报告》 《人用药品风险管理指南》人用药品注册技术要求国际协调会(ICH):2005年风险管理指导原则(Q9)国外药物风险管理现状18192000年苯丙醇胺(PPA)事件2001年西伐他汀(拜斯亭)事件2001年马兜铃酸(关木通等)事件2004年罗非昔布(万络)事件2005年泗县甲肝疫苗事件2005年吉林亚泰药业卡介菌多糖核酸制剂事件 2006年加替沙星(天坤)事件2006年“齐二药”亮菌甲素注射剂事件202006年鱼腥草素(钠)注射液事件2006年克林霉素磷酸酯注射液(欣弗)事件2007年广东佰易静注人免疫球蛋白事件2007年注射用甲氨蝶呤及阿糖胞苷注射液事件 2008年刺五加注射液事件(3人死亡)2008年茵栀黄注射液事2008年江西(博雅)注射用人免疫球蛋白事件2009年双黄连注射液事件(2人死亡)2010年阿伐斯汀(贝伐珠单抗)眼科门事件2012年4月有毒胶囊事件药品风险的多源性21药物的不良反应(已知的或非预期的) 假、劣药物应用所致伤害药物治疗错误所致伤害药物的急性、慢性中毒药物滥用所致伤害超说明书用药所致的药物不良事件药品风险的特征22成因的多源性客观性:其发生是不以人的主观意志为转移偶然性:风险的发生并非经常,受偶发因素的影响可变性:随着科技进步和社会经济结构的变动,风险发生可能性会随之改变突发性:无征兆突然发生,陷人于重大危机药品质量问题(缺陷产品):我国2005-2008年药品风险导致危机的主要成因由药品管理当局批准的药品=安全?“安全”:对拟用的人群而言,该药的效益大于风险,并非保障一定不发生损害。
全面解读2023年高预警药品分类

全面解读2023年高预警药品分类高预警药品是指在使用过程中可能对人体产生严重不良反应或危害的药品,这类药品需要特别注意管理和使用。
为了保障公众用药安全,我国药监局对高预警药品进行了分类管理。
本文档将对2023年高预警药品分类进行详细解读。
一、高预警药品分类根据2023年药监局的规定,高预警药品分为以下六类:1. 激素类药品:包括甾体类激素和非甾体类激素,如泼尼松、地塞米松等。
2. 抗凝血药品:如华法林、肝素等,这类药品用于预防和治疗血栓性疾病,但过量使用可能导致严重出血。
3. 抗肿瘤药品:包括细胞毒药物、生物制品等,如阿霉素、紫杉醇等。
这类药品对人体有一定的毒副作用,使用时需严格控制剂量和疗程。
4. 精神类药品:如地西泮、氯氮平等,这类药品具有成瘾性和依赖性,需在医生指导下使用。
5. 抗生素类药品:如头孢、氟喹诺酮等。
滥用抗生素可能导致细菌耐药性增强,影响治疗效果。
6. 其他类药品:包括心血管系统用药、呼吸系统用药、消化系统用药等,如硝酸甘油、沙丁胺醇等。
这类药品在使用过程中可能出现不良反应,需谨慎使用。
二、高预警药品管理措施为了确保高预警药品的安全使用,我国药监局采取了以下管理措施:1. 严格审批:高预警药品的上市需经过严格的审批程序,确保药品的安全性和有效性。
2. 说明书和标签管理:高预警药品的说明书和标签需明确警示药品的风险,指导医生和患者合理使用。
3. 处方权和调配管理:高预警药品的处方权应由具有相应资质的医生行使,药房在调配高预警药品时需严格核对处方和患者信息。
4. 监测和报告:医疗机构需对高预警药品的不良反应进行监测,发现疑似不良反应及时报告药监局。
5. 宣传教育:加强对医生、患者和公众的宣传教育,提高对高预警药品的认识和安全用药意识。
三、总结2023年高预警药品分类和管理措施的制定,旨在保障公众用药安全,降低药品不良反应发生的风险。
医疗机构、医生和患者都应共同参与高预警药品的管理,合理、安全地使用高预警药品。
2023年度高风险药品分类名录

2023年度高风险药品分类名录1. 引言本名录旨在为医疗机构、药品生产和经营企业、以及监管机构提供一份关于高风险药品的详细指南。
高风险药品是指在使用过程中可能对患者造成严重伤害或死亡的药品。
本名录根据药品的特性、用途、以及潜在风险进行分类,以帮助各类医疗机构和药品使用者更好地识别和管理高风险药品。
2. 高风险药品分类根据药品的特性、用途、以及潜在风险,我们将高风险药品分为以下几类:2.1 抗凝血药包括华法林、肝素、低分子肝素、磺达肝癸钠等。
这类药品在使用过程中需密切监测患者的凝血功能,以防出血风险。
2.2 抗肿瘤药包括化疗药物、靶向治疗药物等。
这类药品可能引起严重的骨髓抑制、肝肾功能损害等,需谨慎使用。
2.3 免疫抑制剂包括环孢素、他克莫司、雷公藤总苷等。
这类药品可能降低患者的免疫功能,增加感染风险。
2.4 麻醉药品包括吗啡、芬太尼、杜冷丁等。
这类药品具有强烈的成瘾性和潜在的滥用风险。
2.5 精神药品包括地西泮、氯硝西泮、阿普唑仑等。
这类药品可能引起依赖、成瘾、以及严重的戒断症状。
2.6 生物制品包括重组蛋白、抗体、疫苗等。
这类药品可能引起过敏反应、感染等。
2.7 血液制品包括浓缩血小板、白蛋白、免疫球蛋白等。
这类药品需严格筛查病原体,以防传播疾病。
2.8 药物浓度监测药品包括地高辛、锂盐、氨基糖苷类抗生素等。
这类药品的疗效与血药浓度密切相关,需定期监测。
2.9 植入性医疗器械包括心脏起搏器、支架、人工关节等。
这类医疗器械可能存在故障、感染等风险。
2.10 遗传性疾病的基因治疗药物包括针对罕见遗传病的基因治疗药物。
这类药品可能引起未知的风险,需谨慎评估。
3. 总结本名录提供了2023年度高风险药品的分类指南,以帮助各类医疗机构和药品使用者更好地识别和管理高风险药品。
请注意,本名录仅供参考,具体使用时请遵循相关法规、指南和临床实践。
---以上内容仅供参考,具体使用时请遵循相关法规、指南和临床实践。
2023年高预警药品类别清单

2023年重点监控药品分类索引为了加强对药品使用的管理,提高药品使用的合理性和安全性,我国药品监管部门根据药品的疗效、安全性、价格等因素,对药品进行了分类管理。
本索引列举了2023年重点监控的药品分类及其相关信息,以供参考。
一、目录1. 抗感染药物2. 心血管系统药物3. 神经系统药物4. 内分泌系统药物5. 肿瘤药物6. 免疫系统药物7. 呼吸系统药物8. 消化系统药物9. 肾脏疾病药物10. 血液系统药物11. 抗过敏药物12. 抗凝血药物13. 抗高血压药物14. 抗糖尿病药物15. 抗精神病药物16. 抗抑郁药物17. 抗癫痫药物18. 抗风湿药物19. 眼病治疗药物20. 皮肤病治疗药物二、详细信息1. 抗感染药物- 分类说明:抗感染药物是指用于治疗各种病原微生物(包括细菌、病毒、真菌等)引起的感染的药物。
- 包括但不限于:青霉素类、头孢菌素类、大环内酯类、喹诺酮类、硝基咪唑类等。
2. 心血管系统药物- 分类说明:心血管系统药物主要用于治疗心脏病、高血压等心血管疾病。
- 包括但不限于:ACE抑制剂、ARB、β受体阻滞剂、钙通道阻滞剂、抗血小板药物等。
3. 神经系统药物- 分类说明:神经系统药物是指用于治疗神经系统疾病(如癫痫、帕金森病、阿尔茨海默病等)的药物。
- 包括但不限于:抗癫痫药物、抗帕金森病药物、抗抑郁药物、镇静催眠药物等。
4. 内分泌系统药物- 分类说明:内分泌系统药物主要用于治疗内分泌系统疾病(如糖尿病、甲状腺疾病等)。
- 包括但不限于:胰岛素、口服降糖药物、甲状腺激素类药物等。
5. 肿瘤药物- 分类说明:肿瘤药物是指用于治疗各种癌症的药物。
- 包括但不限于:化疗药物、靶向药物、免疫检查点抑制剂等。
6. 免疫系统药物- 分类说明:免疫系统药物是指用于治疗免疫系统相关疾病(如风湿性关节炎、系统性红斑狼疮等)的药物。
- 包括但不限于:生物制剂、免疫抑制剂等。
7. 呼吸系统药物- 分类说明:呼吸系统药物主要用于治疗各种呼吸系统疾病(如哮喘、慢性阻塞性肺病等)。
2023年度高预警药品类型目录

2023年度高预警药品类型目录背景根据国家药品监督管理局的要求,制定2023年度高预警药品类型目录,旨在加强对高风险药品的监管和预警,保障公众的用药安全。
目标本目录的主要目标是识别和分类高预警药品,确保这些药品的生产、流通和使用符合法规要求,并及时预警和处理可能存在的风险。
策略为了实现目标,我们将采取以下策略:1. 系统化的药品评估:建立一套系统的评估程序,对药品进行全面评估,包括其疗效、安全性、副作用等因素,以确定高预警药品的类型。
2. 风险监测和预警:建立风险监测系统,定期收集和分析药品的安全性数据和不良反应报告,及时发现潜在风险,并预警相关部门和用户。
3. 严格的供应链管理:加强对药品生产和流通环节的监管,确保药品的质量和安全性,防止假冒伪劣药品的流入市场。
4. 宣传和教育:开展药品安全宣传和教育活动,提高公众对高预警药品的认识和警惕,引导合理用药,减少不良事件的发生。
目录内容根据以上策略,我们将制定2023年度高预警药品类型目录的内容如下:1. 高风险药物类别:列出被评估为高风险的药物类别,包括但不限于抗生素、抗肿瘤药物、心血管药物等。
2. 药品安全提示:针对每个高风险药物类别,提供相关的药品安全提示和预防措施,以帮助医生、药师和患者正确使用这些药物。
3. 不良反应报告和处理:介绍如何报告药品的不良反应和处理措施,以促进及时处理和预警。
4. 监管措施:明确相关部门对高预警药品的监管措施,包括生产许可要求、流通管理要求等。
实施计划1. 制定目录:在2022年底前,制定完整的2023年度高预警药品类型目录。
2. 宣传推广:2023年初,向医疗机构、药店和公众推广目录内容,提高相关人员对高预警药品的认识和重视程度。
3. 监管执行:加强对高预警药品的监管执行力度,确保相关政策和措施得到有效执行。
结论通过制定2023年度高预警药品类型目录,并采取相应的策略和措施,我们将能够更好地监管和预警高风险药品,保障公众的用药安全。
高度危险药品目录

高度危险药品目录
目前,我国药品管理部门已经制定了一份高度危险药品目录,
以便对相关药品进行统一管理和控制。
以下是该目录中一些应列入
的高度危险药品:
1. 麻醉类药品:包括各种全身麻醉药物,如丙泊酚、咪达唑仑等。
这些药品对于使用者来说具有较高的风险,需要特别的操作和
监控。
2. 毒性药品:包括具有毒性和剧毒性的药物,如氰化物类药品、放射性药物等。
这些药品在使用过程中需要特别小心,以免造成危险。
3. 高风险药物:包括那些存在严重副作用或潜在风险的药物,
如抗癌药物、免疫抑制剂等。
这些药物需要特别谨慎使用,以免对
患者的健康造成损害。
4. 爆炸性药物:包括那些具有爆炸性质的药品,如硝化甘油等。
这些药品在制备、存储和使用过程中需要采取特殊的安全措施,以
防止事故发生。
高度危险药品的目录需要定期更新,以适应新药的开发和药品
的评估。
药品管理部门应当加强监督和执法,确保高度危险药品的
安全使用。
> 注意:以上内容为简要概述,具体高度危险药品目录请参考
相关药品管理部门发布的正式文件。
以上是关于高度危险药品目录的简要说明。
该目录的制定和管
理对于保障公众的安全和健康具有重要意义。
我们应当高度重视,
并加强对高度危险药品的管理和控制。
食药局通报中药材及饮片不合格名单 中心医院在列

食药局通报中药材及饮片不合格名单中心医院在列责任编辑:紫苏发布时间:2014-09-23 15:36:00导读]国家食品药品监督管理总局开展了中药材及饮片专项抽验。
共从全国31个省(区、市)有关中药材及饮片的生产、经营和使用10个品种772批样品,经检验发现93批不合格。
国家食品药品监督管理总局近期组织开展了中药材及饮片专项抽验。
共从全国31个省(区、市)有关中药材及饮片的生产、经营和使用单位抽取蒲黄、柴胡、川贝母、血竭、薄荷、木通、苍术、附子、制川乌和制草乌等10个品种772批样品,经检验发现93批不符合标准规定。
总体上看,抽验的中药材及饮片的质量状况不容乐观,染色、增重、掺伪、掺杂等问题仍然比较突出。
除薄荷、木通和制川乌外,其余7个中药材及饮片均检出不符合标准规定产品。
其中,蒲黄的不合格率最高,发现存在染色、增重及掺杂等问题;川贝母发现存在掺伪问题;血竭发现存在掺杂问题。
对中药材及饮片进行染色、增重、掺伪、掺杂等违法行为,严重危害公众用药安全,欺骗消费者,必须严厉打击。
总局已组织相关省(区、市)食品药品监督管理局对不符合标准规定的中药材及饮片及时采取相应控制措施,对相关单位依法查处,并要求各省(区、市)局结合本行政区域的实际情况,有针对性地加强对有关中药材及饮片的质量监管,切实保障公众用药安全。
不符合标准规定的中药材及饮片名单品种生产批号检品来源抽样省份不符合规定项目检验依据检验机构发现的主要问题苍术120415483 天津市保寿堂药店天津[鉴别]((2)薄层色谱) 《中国药典》2010年版一部中国食品药品检定研究院主要化学成分差异大1302001 栾城县医药药材公司河北110315488 长春经济技术开发区嘉宁大药房吉林20121103 内蒙古自治区中蒙医医院内蒙古130113 福州榕参医药连锁有限公司连江店福建120501 国药控股重庆有限公司重庆20111202 云南富民医药有限责任公司云南柴胡20130126 辽宁中正堂医药连锁有限公司辽宁[性状];[鉴别](薄层色谱) 《中国药典》2010年版一部中国食品药品检定研究院掺杂或掺伪121123 上海中医药大学附属龙华医院上海130201 巢湖中辰大药房有限公司团结东路店安徽120601 武汉国泰君安大药房有限公司湖北2011120703 湖南养天和大药房企业集团有限公司和强店湖南130301 海口琼山医药公司药品总汇海南20121101 重庆市南岸区人民医院重庆120504 黔东南苗族侗族自治州中医医院贵州130401 双城市德康医药药材商店黑龙江[性状]20121207 浙江省中医院浙江121215 连江县宜又佳医药商店福建120901 新乡市中心医院河南20121101 南宁市茂诚药品零售连锁有限责任公司宁康药店广西130102 海南寿南山参业有限公司海南12040117 海南菁华药业有限公司海南120219 榆中县第一人民医院甘肃20111205 西宁市中医院青海川贝母20110301 沈阳市天桥中医院辽宁[性状];[鉴别]((3)聚合酶链式反应-限制性内切酶长度多态性方法) 《中国药典》2010年版第一增补本中国食品药品检定研究院掺伪20130226 厦门市聚德堂药业有限公司新阳分店福建2012年10月01日江西远东药业有限公司江西110826 大冶市金康药店湖北20120901 南宁市茂诚药品零售连锁有限责任公司宁康药店广西130108 儋州那大好药林药店海南20121201 青海东大肛肠医院有限公司青海12041401 吉木乃县人民医院新疆101210 上海中医药大学附属龙华医院上海[鉴别]((3)聚合酶链式反应-限制性内切酶长度多态性方法)121217 上海药房股份有限公司上海YT2012110106 上海华宇药业有限公司上海20130301 福建中医药大学附属人民医院福建121101 贵溪市中医院江西12050201 长沙市雨花区洞井医院湖南120902 海口市中医院海南120301 西安市中医医院陕西附子(淡附片) YPA1K0001广东友邦医药有限公司广东[鉴别](薄层色谱) 《中国药典》2010年版一部中国食品药品检定研究院炮制不当,有效成分下降附子(黑顺片) 110804 沈阳市华鸿大药房连锁有限公司千源店辽宁蒲黄120701 浙江瑞人堂医药连锁有限公司椒江开元店浙江[性状];[检查](杂质)、(总灰分)、(金胺O(1)、(2)) 《中国药典》2010年版一部及国家食品药品监督管理局药品检验补充检验方法和检验项目批准件(批准件编号:2007007) 中国食品药品检定研究院掺杂、染色或增重120426 合肥中山医院安徽110801 贵溪市中医院江西20121106 浠水县清泉大药房连锁有限公司清泉大药房湖北130101 南宁生源中药饮片有限责任公司广西121101 广西南宁金恩药业有限公司广西110901 海南广益药业连锁经营有限公司海口南宝分店海南110701 海南源安隆药品超市连锁有限公司儋州东坡路超市海南121002 海南寿南山参业有限公司海南20111205 西宁市中医院青海20100302 阜康市中医医院新疆130101 焦作市第二人民医院河南[性状];[检查](总灰分)、(金胺O(1)、(2))120106 银川仁安堂大药房有限公司宁夏201204574 湖南楚仁堂医药连锁经营有限责任公司锦源店湖南[检查](杂质)、(总灰分)、(金胺O(1)、(2))121101 泸州本草堂医药有限公司四川2012601 贵阳市第二人民医院贵州121106 贵州中草医医院贵州110602 湟中县鲁沙尔益寿堂药房青海20120701 漳州市芗城祝安堂药店福建[检查](杂质)、(总灰分)、(金胺O(1))130108 青岛市中心医院山东[检查](总灰分)、(金胺O(1))、(2))100923 宁夏古方中医医院宁夏20121201 天津北辰北门医院天津[检查](杂质)、(金胺O(1)、(2))) 掺杂、染色20120801 武汉市中医医院湖北2008年6月29日察右中旗中安医药有限责任公司内蒙古[检查](杂质)、(总灰分) 掺杂或增重121102 东北制药集团供销有限公司辽宁110313 哈尔滨市灵峰大药房黑龙江20091030 长沙市雨花区华药堂大药房湖南1206043 西宁市城中区真壹堂药店青海20110301 沈阳铁西姚氏中医院辽宁[检查](总灰分)YP20120701 健之佳连锁健康药房有限公司博仁堂诊所云南130101 河北省中医院河北[性状];[检查](杂质)、(总灰分)1211075 北京海升堂大药房有限责任公司北京[检查](杂质) 掺杂11080421 山西仁和大药房连锁有限公司平阳二部山西13031401 上海中医药大学附属龙华医院上海120827 绍兴市震元堂药店浙江121128 无为县中医医院安徽130202 福州市中医院福建20110601 武汉初开堂药业有限公司六渡桥分店湖北130101 广州市天河区中医医院广东20120801 海口琼山医药公司中山药店海南13022707 阿克苏市百福大药房新疆生蒲黄120101 北京百姓康宁大药房有限公司北京[检查](总灰分)、(金胺O(1)、(2)) 《中国药典》2010年版一部及国家食品药品监督管理局药品检验补充检验方法和检验项目批准件(批准件编号:2007007) 中国食品药品检定研究院掺杂、染色或增重120701 哈尔滨市中医医院黑龙江[检查](杂质) 掺杂121001 西安市中医医院陕西080925 甘肃众友健康医药连锁有限公司银川分公司宁夏[性状];[检查](杂质)炒蒲黄120312156 天津市保寿堂药店天津[性状];[检查](金胺O(1)、(2)) 《天津市中药饮片炮制规范》2012年版及国家食品药品监督管理局药品检验补充检验方法和检验项目批准件(批准件编号:2007007) 中国食品药品检定研究院掺杂、染色20121016 南昌市第五医院江西血竭090626 山西益源大药房连锁有限责任公司柳巷分店山西[检查]((1)薄层色谱、(2)高效液相色谱) 《中国药典》2010年版一部及国家食品药品监督管理局药品检验补充检验方法和检验项目批准件(批准件编号2008004) 中国食品药品检定研究院掺杂110313 哈尔滨市灵峰大药房黑龙江制草乌11121046 福建省尤溪医药有限责任公司福建[鉴别](薄层色谱) 《中国药典》2010年版一部中国食品药品检定研究院炮制不当,有效成分下降12121074 广东仁乐药业有限公司广东。
药品质量风险反馈函

药品质量风险反馈函XXX食品药品监督管理局药品生产监管处:我公司在2019年6月22日收到“XXX食品药品监督管理局关于通报国家药品抽检品种质量风险的函”:提示我公司生产的XXX(批号18000101)在国家药品抽检中,经XXX省药品检验检测研究院检验发现存在潜在的质量风险(检出矮壮素),要求开展排查,降低质量风险。
得知此情况后,公司领导高度重视,成立了由质保部、采购部、生产部、物流部组成的调查小组,对问题进行了分析研究、开展了针对性的调查,并列出了相关的预防措施。
一、针对“矮壮素”问题,我公司在网上查阅了有关资料,对其用途及危害阐述如下:矮壮素抑制作物生长,属于一种用途很广的植物生长调节剂,主要用于生长期较长的农作物,使苗期的农作物长得矮壮,不倒伏,多结果。
到作物结果时,“矮壮素”已没了毒性。
蔬菜生长期短,如使用了“矮壮素”,到收割时还有一定毒性,对人体有害。
XXX从种植到采收共7个月。
矮壮素有以下几点危害:(一)作物危害:如果施用过量,会导致植物无法正常生长,表现为植株矮缩、生长停滞,影响生长及产量。
(二)人体危害:家里有小孩和孕妇的不能用,矮壮素类药物低毒性,成人影响不大,不敢保证对小孩和怀孕期人群是否有影响。
(三)坏境污染:用了矮壮素类似药物后,如果坏境适宜的地方,衰减期长达两年,也就是说你不换土,两年内种植物都长不大。
目前有关部门只对农药残留作检测,对“生长素”之类的检测还没作要求。
二、调查小组从物料采购方面、生产管理、及原料、产品的质量检验方面开展了调查分析,我公司生产的XXX在采购、生产和检验环节严格按照规定进行,无违规操作行为,且符合GMP规范要求,可以排除采购、生产和检验环节的因素,初步判断检出矮壮素的原因是农户在种植过程中施用的各类肥料中残留的生长调节剂所致。
三、结合以上的调查分析并根据我公司的具体情况,启动纠正和预防措施。
(一)纠正措施:1、公司已于2017年7月7日对该批XXX进行了召回处理,杜绝不合格产品在市场上继续流通。
高风险药品分类

高风险药品分类
引言
本文档旨在对高风险药品进行分类,并提供相应的说明。
高风
险药品是指使用和管理过程中存在较高风险的药品。
分类标准
根据药品的特点、风险和使用要求,我们将高风险药品分为以
下几类:
1. 麻醉药品:这包括各种麻醉用药,如全身麻醉药、局部麻醉
药和镇痛药物。
由于麻醉药品使用时直接影响病人安全和手术成功率,因此属于高风险药品。
2. 抗癌药品:这些药品用于治疗各种癌症,通常具有较高的毒
性和副作用。
由于使用抗癌药品可能引发严重的不良反应和并发症,所以被归类为高风险药品。
3. 抗凝药品:这些药品用于预防和治疗血栓形成。
由于抗凝药品使用时需要严密的监测和调整剂量,使用不当可能导致出血等风险,因此属于高风险药品。
4. 免疫抑制药品:这些药品用于降低免疫系统的功能,常用于器官移植术后和自身免疫性疾病的治疗。
由于免疫抑制药品会增加感染和其他副作用的风险,所以归类为高风险药品。
监管要求
针对高风险药品,监管机构通常有严格的要求和规定。
这些要求可能包括:
- 高风险药品的存储和配送要求;
- 开具和使用高风险药品的合规性要求;
- 使用高风险药品时的安全措施和监测要求。
医疗机构和相关从业人员需要遵守这些监管要求,以确保高风险药品的安全使用。
总结
高风险药品的分类对医疗机构和从业人员非常重要。
通过对高风险药品的分类和监管要求的遵守,可以减少药品使用过程中的风险,保障病人的安全和效果。
以上是对高风险药品分类的简要说明,希望对您有所帮助。
中国高警示药品目录最新版
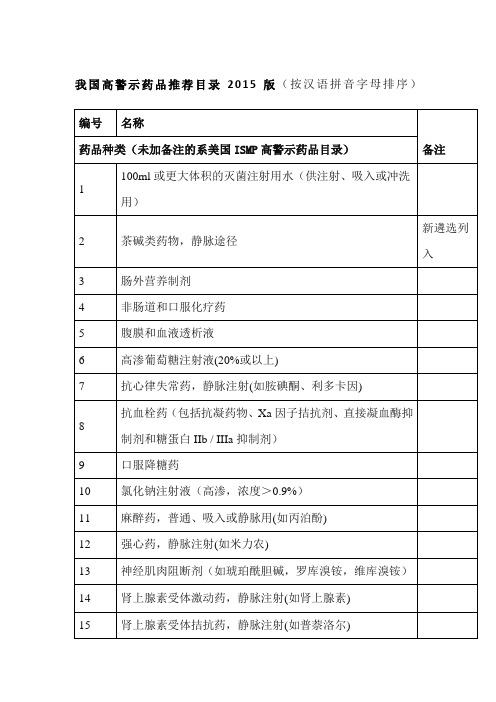
我国高警示药品推荐目录2015版(按汉语拼音字母排序)
附注:
1、基于遵从英文原文(High-Alert Medications)语义、切合管理文化以及方便对患者进行用药交代、避免歧义等多方面考虑,对于在我国近年沿用的“高危药品”,更名为“高警示药品”。
2、通过由全国23家医疗机构医务人员参与的“高警示药品目录遴选调研项目”,借鉴美国用药安全研究所(ISMP)高警示药品目录,同时结合我国国情,增加了对育龄人群有生殖毒性的药品(如阿维A等)、静脉途径给药的茶碱类两类及阿托品注射液(5mg/ml)、高锰酸钾外用制剂、凝血酶冻干粉和注射用三氧化二砷四种药品。
3、中国药学会医院药学专业委员会用药安全专家组正在研究拟定高警示药品分级管理目录以及管理SOP,相关结果将会适时发布。
3、关于中药饮片和中成药的高警示目录,相关学会正在组织研究中。
欢迎全国同行提出宝贵的意见和建议!
联系邮箱:
中国药学会医院药学专业委员会
用药安全专家组2015年6月5日。
2023药品高预警分类手册
2023年高预警药品种类明细
高预警药品是指在使用过程中可能对人体产生严重不良反应、危害人体健康的药品。
为确保患者安全,减少药品不良反应的发生,我国药品监管部门对高预警药品实行了严格的管理制度。
本文档详细列出了2023年高预警药品的种类,以便医疗机构、药品经营企业和患者了解并遵守相关规定。
一、高预警药品种类
以下为2023年高预警药品的种类,包括药品名称、生产厂家、规格等信息。
二、高预警药品管理要求
1. 医疗机构应当建立健全高预警药品管理制度,明确高预警药品的品种、使用范围、使用剂量、使用频率等,并加强对医生的培训和指导。
2. 药品经营企业应当建立健全高预警药品销售管理制度,明确高预警药品的品种、销售范围、销售剂量、销售频率等,并加强对销售人员的培训和指导。
3. 患者在使用高预警药品时,应当严格遵守医生的用药指导和药品说明书,不得擅自增减剂量、停药或更换药品。
4. 医疗机构、药品经营企业和患者应当密切关注高预警药品的不良反应信息,发现疑似不良反应应当及时报告药品监管部门。
5. 药品监管部门应当加强对高预警药品的监管,及时收集和分析不良反应信息,采取有效措施减少药品不良反应的发生。
三、总结
本文档详细列出了2023年高预警药品的种类和管理要求,旨在提高医疗机构、药品经营企业和患者对高预警药品的认识和关注度,确保患者用药安全。
如有疑问,请及时与药品监管部门联系。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附件3
国家药品抽验发出质量风险提示的品种
药品名称可能存在的质量风险和问题
红参通过新建方法发现总糖超出拟定的标准限度,疑存在掺糖情况。
蒲黄(生蒲黄)参照药材补充方法检出金胺O染色,疑在生产过程中存在人为染色情况
醋乳香总灰分大于6.0%,醇水不溶物大于10%,疑掺杂泥沙或树皮过多。
制乳香总灰分大于6.0%,醇水不溶物大于10%,疑掺杂泥沙或树皮过多。
跌打红药片对跌打红药片中红花质量的考察:以红花的特征成分羟基红花黄色素A为对照,采用高效液相法定性鉴别红花。
结果羟基红花黄色素A未检出。
分析造成药品羟基红花黄色素A含量低的原因可能为:1、生产工艺中的60% 乙醇加入量过低,导致提取不完全;
2、原药材的质量存在问题。
沉香含树脂少,有效成分低,疑原药材质量不佳。
没药(醋没药)探索性研究发现HPLC特征图谱异常,疑存在未按标准炮制或非法添加的情况。
妇科止带片1.阿胶、龟甲的高效液相色谱-质谱法限量检查不符合拟定标准规定,疑存在少投料或不投料的情况;2.存在南五味子、五味子混用情况;3、检出黄柏、五味子显微特征,疑在生产过程中存在生粉投料的情况。
胃康灵胶囊显微鉴别未见白及显微特征,特征图谱未检出白及特征峰,白及含量测定结果未检出,疑存在未投原料白及的情况。
黄连总灰分、二氧化硫超标,含量测定不符合拟定标准规定,疑存在过分熏硫或掺杂情况,检出金胺O。
安神补心丸1.按照新标准草案拟定的限量判定,丹参酮ⅡA、隐丹参酮和丹参酮Ⅰ成分总含量不符合拟定标准规定,疑使用丹参质量较差或投料不足;2.按照新标准草案拟定的限量判定,特女贞苷含量不符合拟定标准规定,疑使用女贞子(蒸)质量较差或投料不足;或安神膏处方量制成总量不固定,导致女贞子在制成安神膏后再到制剂含量难以控制。
银翘解毒颗粒疑使用山银花投料。
小儿咳喘灵颗粒探索研究含量测定及制剂中山银花检查补充检验方法结果表明,既检出金银花特征成分木犀草苷,且检出山银花3个特征成分灰毡毛忍冬皂苷乙、灰毡毛忍冬皂苷甲川续断皂苷乙,疑在金银花中掺混山银花投料。
