生物大分子.ppt
合集下载
生物大分子的分离与制备(共89张PPT)

2022/9/24
2022/9/24 7
生物分子的结构与功能分析:
1. 蛋白质结构分析
2. 酶活力检测
3. 蛋白质组学分析
4. DNA序列分析
5. 聚合酶链反应(PCR)6. 分子杂交
7. 基因克隆8. 基因组构建9. cDNA构建
10. 筛选11. 报告基因检测12. 基因芯片
13. 基因敲除
➢ 核酸是遗传信息的携带者,在生物体中指导各种蛋 白质的合成。
2022/9/24
生物化学分离方法与一般的化学分离方法相比,有下列
几个特点: • 生物材料组成非常复杂。其中包括数百种甚至数千种化
合物,并且在分离过程中,这些化合物仍在发生代谢 变化,如蛋白质和核酸的水解。
有些化合物的含量极微,如激素等。 许多具有生物活性的物质一旦离开活体,很易变 变性破坏,因此常选用比较温和的条件进行制备。
• 功能或分子生物化学阶段(1950 年至今)。研究生命的本质和奥秘: 运动、神经、内分泌、生长、发育、繁殖等的分子机理 。
2022/9/24
2022/9/24
3
生物化学研究技术方法
❖ 生物化学研究的方法:
– 观察:生命现象
– 分离:未知蛋白组分,新基因片段,新的次生代谢物。 (抽提、过 滤、离心、色谱)
立了一系列研究核酸及蛋白质相互作用的技 确定要制备的生物大分子的目的和要求,是进行科研、开发还是要发现新的物质。
盐析的发生在于盐浓度增高到一定数值时,使水活度降低,进而导致蛋白质分子表面电荷逐渐被中和,水化膜逐渐被破坏,最终引起蛋白质分子之 间相互聚集并从溶液中析出。 其他化学性质:如对各种蛋白酶、水解酶的稳定性和对各种化学试剂的稳定性。
脂溶性的有机溶剂(丙酮,乙醚)中脱脂;采用快速加热 (50℃左右),快速冷却的方法,使溶化的油滴冷却后 凝聚成油块而被除去。
2022/9/24 7
生物分子的结构与功能分析:
1. 蛋白质结构分析
2. 酶活力检测
3. 蛋白质组学分析
4. DNA序列分析
5. 聚合酶链反应(PCR)6. 分子杂交
7. 基因克隆8. 基因组构建9. cDNA构建
10. 筛选11. 报告基因检测12. 基因芯片
13. 基因敲除
➢ 核酸是遗传信息的携带者,在生物体中指导各种蛋 白质的合成。
2022/9/24
生物化学分离方法与一般的化学分离方法相比,有下列
几个特点: • 生物材料组成非常复杂。其中包括数百种甚至数千种化
合物,并且在分离过程中,这些化合物仍在发生代谢 变化,如蛋白质和核酸的水解。
有些化合物的含量极微,如激素等。 许多具有生物活性的物质一旦离开活体,很易变 变性破坏,因此常选用比较温和的条件进行制备。
• 功能或分子生物化学阶段(1950 年至今)。研究生命的本质和奥秘: 运动、神经、内分泌、生长、发育、繁殖等的分子机理 。
2022/9/24
2022/9/24
3
生物化学研究技术方法
❖ 生物化学研究的方法:
– 观察:生命现象
– 分离:未知蛋白组分,新基因片段,新的次生代谢物。 (抽提、过 滤、离心、色谱)
立了一系列研究核酸及蛋白质相互作用的技 确定要制备的生物大分子的目的和要求,是进行科研、开发还是要发现新的物质。
盐析的发生在于盐浓度增高到一定数值时,使水活度降低,进而导致蛋白质分子表面电荷逐渐被中和,水化膜逐渐被破坏,最终引起蛋白质分子之 间相互聚集并从溶液中析出。 其他化学性质:如对各种蛋白酶、水解酶的稳定性和对各种化学试剂的稳定性。
脂溶性的有机溶剂(丙酮,乙醚)中脱脂;采用快速加热 (50℃左右),快速冷却的方法,使溶化的油滴冷却后 凝聚成油块而被除去。
《生物大分子分离纯》PPT课件

(2)物理法: 1) 反复冻融法:将待破碎的细胞冷至-15℃到-20℃,然后放于室温(或40℃) 迅速融化,如此反复冻融屡次,由于细胞内形成冰粒使剩余胞液的盐浓度增高 而引起细胞溶胀破碎。 2) 超声波处理法:此法是借助超声波的振动力破碎细胞壁和细胞器。破碎微生 物细菌和酵母菌时,时间要长一些。 3) 压榨法:这是一种温和的、彻底破碎细胞的方法。在1000×105Pa~ 2000×105Pa 的高压下使细胞悬液通过一个小孔突然释放至常压,细胞将彻 底破碎。 4) 冷热交替法:从细菌或病毒中提取蛋白质和核酸时可用此法。在90℃左右 维持数分钟,立即放入冰浴中使之冷却,如此反复屡次,绝大局部细胞可以被 破碎。
⑴ 水溶液提取:蛋白质和酶的提取一般以水 溶液为主。稀盐溶液和缓冲液对蛋白质的稳 定性好,溶解度大,是提取蛋白质和酶最常 用的溶剂。 ⑵ 有机溶剂提取:一些和脂类结合比较结实 或分子中非极性侧链较多的蛋白质和酶难溶 于水、稀盐、稀酸、或稀碱中,常用不同比 例的有机溶剂提取。
别离纯化
• 刚提取得到的大分子物质,往往是粗制品, 含有许多杂质,必须进一步别离纯化。别 离提纯各种生物大分子,主要根据各种物 质的分子大小、溶解度、带电性、亲和力 大小等差异,选用有机溶剂沉淀,等电点 沉淀,盐析,层析,电泳,超离心,吸附, 结晶等方法
《生物大分子分离纯》 PPT课件
本课件PPT仅供大家学习使用 学习完请自行删除,谢谢! 本课件PPT仅供大家学习使用 学习完请自行删除,谢谢! 本课件PPT仅供大家学习使用 学习完请自行删除,谢谢! 本课件PPT仅供大家学习使用 学习完请自行删除,谢谢!
一、生物大分子的别离与纯化技 术
二、肝酶提取
• ⑶许多生物大分子一旦离开了生物体内的环境 时就极易失活,因此别离过程中如何防止其失活, 就是生物大分子提取制备最困难之处。
高三生物一轮复习:细胞中的生物大分子一ppt课件

糖类、脂质的种类和作用 1.糖类的两大分类标准 (1)按化学性质分:
还原性糖:葡萄糖、果糖、麦芽糖、乳糖等。 非还原性糖:多糖、蔗糖。
(2)按功能分:
①参与构成细胞的 重要组成成分
纤维素:植物细胞壁的主要成分。 脱氧核糖:DNA的组成成分之一。 核糖:RNA的组成成分之一。
②细胞生命活动的主要能源物质:葡萄糖。
斐林试剂 双缩脲试剂 苏丹Ⅲ/Ⅳ染液 丙酮、层析液
作用 检测、鉴定淀粉 检测、鉴定还原性糖 检测、鉴定蛋白质 检测、鉴定脂肪 提取、分离色素
现象 淀粉遇碘变蓝
砖红色沉淀 紫色
橘黄色/红色 形成四条色素带
实验常用的试剂或指标物 Ca(OH)2溶液
作用 检测、鉴定CO2
现象
CO2使Ca(OH)2溶液 变浑浊
1.淀粉是植物体内的一种储能物质,构成淀粉的基本单位与下
列哪种物质的基本单位不同( )
A.纤维素
B.肝糖原
C.肌糖原
D.核糖
【解析】选D。淀粉的基本单位是葡萄糖;纤维素与糖原的基
本单位也是葡萄糖;而核糖是一种单糖。
2.(2012·海安模拟)纤维素和性激素的化学本质分别是( )
A.糖类和脂质
B.糖类和蛋白质
C.蛋白质和脂质
D.脂质和蛋白质
【解析】选A。纤维素是多糖属于糖类;性激素是固醇类物质属
于脂质。
3.下列叙述与选项中糖类对应正确的是( ) ①存在于DNA而不存在于RNA中的糖类 ②植物细胞主要的能源物质 ③存在于叶绿体而不存在于线粒体内的糖类 ④存在于植物细胞而不存在于肝脏细胞中的糖类 A.核糖、纤维素、葡萄糖、糖原 B.脱氧核糖、葡萄糖、葡萄糖、纤维素 C.核糖、葡萄糖、脱氧核糖、糖原 D.脱氧核糖、纤维素、葡萄糖、蔗糖
生物大分子结构与功能ppt课件

氨基酸部分 ➢ 多肽主链(main chain):由肽键连接各氨基酸残基形成的
长链骨架 ➢ 多肽侧链(side chain):蛋白质多肽链中的各氨基酸侧链基团
肽的书写格式
NH2-甘-丙-谷-……-组-蛋-COOH NH2-Gly-Ala-Glu-……His-MetCOOH NH2-GAE……HM-COOH GAE……HM
子量(MW)30,000-45,000 ➢ 一个含有100个氨基酸组成的蛋白质可存在20100
种不同的形式 ➢ E. coli约含有3,000种蛋白质,人体约含有100,000种
蛋白质的基本组成单位——氨基酸
➢编码氨基酸:20 种 , 除Gly外,均为L-氨基酸, Pro为 环状亚氨酸 ➢非编码氨基酸:胱氨酸、碘代酪氨酸、羟脯氨酸与 羟赖氨酸等
Trp
光 密 度
Tyr Phe
0 240 250 260 270 280 290 300 310 波 长 ( nm )
芳香族氨基酸的紫外吸收
化学性质
亚硝酸反应:测定产生的N2可计算氨基酸的含量, 为Van Slyke定 氮法的基础。
甲醛反应: 氨基酸与甲醛反应生成二羟甲基氨基酸, 为中和法测 定氨基酸含量的依据, 称甲醛滴定法, 两性氨基酸在与 甲醛反应后使氨基封闭而酸性增强, 可用强碱滴定。
➢ 寡肽(oligopeptide): 十个以下氨基酸缩合成的肽统称为寡肽
➢ 多肽链(polypeptide chain) : 十个以上氨基酸形成的肽,
典型的多肽MW<104 ➢ 蛋白质: 由一条或几条多肽链组成的生物大分子 ➢ 氨基酸残基(amino acid residues):蛋白质肽链中的每个
(2) R为羟基和硫: Ser、Thr含羟基,Ser有极性可形成氢键, 大多数酶的活性中心有
长链骨架 ➢ 多肽侧链(side chain):蛋白质多肽链中的各氨基酸侧链基团
肽的书写格式
NH2-甘-丙-谷-……-组-蛋-COOH NH2-Gly-Ala-Glu-……His-MetCOOH NH2-GAE……HM-COOH GAE……HM
子量(MW)30,000-45,000 ➢ 一个含有100个氨基酸组成的蛋白质可存在20100
种不同的形式 ➢ E. coli约含有3,000种蛋白质,人体约含有100,000种
蛋白质的基本组成单位——氨基酸
➢编码氨基酸:20 种 , 除Gly外,均为L-氨基酸, Pro为 环状亚氨酸 ➢非编码氨基酸:胱氨酸、碘代酪氨酸、羟脯氨酸与 羟赖氨酸等
Trp
光 密 度
Tyr Phe
0 240 250 260 270 280 290 300 310 波 长 ( nm )
芳香族氨基酸的紫外吸收
化学性质
亚硝酸反应:测定产生的N2可计算氨基酸的含量, 为Van Slyke定 氮法的基础。
甲醛反应: 氨基酸与甲醛反应生成二羟甲基氨基酸, 为中和法测 定氨基酸含量的依据, 称甲醛滴定法, 两性氨基酸在与 甲醛反应后使氨基封闭而酸性增强, 可用强碱滴定。
➢ 寡肽(oligopeptide): 十个以下氨基酸缩合成的肽统称为寡肽
➢ 多肽链(polypeptide chain) : 十个以上氨基酸形成的肽,
典型的多肽MW<104 ➢ 蛋白质: 由一条或几条多肽链组成的生物大分子 ➢ 氨基酸残基(amino acid residues):蛋白质肽链中的每个
(2) R为羟基和硫: Ser、Thr含羟基,Ser有极性可形成氢键, 大多数酶的活性中心有
生物大分子的分离纯化技术(共34张PPT)
范围. 以1×10-13s 为一个单位,称为斯韦德贝格单位(Svedberg) ,用S(大写)表示.
离心(3)
最大速度方法:
移动界面(Moving Boundary)超 速离心法
移动区带(Moving Zone)超速离心法
等密度方法(Isodensity):
样品的类型、采集与保存 酶样品的准备
亲和色谱
琼脂糖的溴化氰活化法
6-氨基己酸-琼脂糖和,1,6-己二胺-琼脂糖
层析柱短 配基-与大分子间以氢键离子键或疏水相互作用结合
透析 微过滤 盐析 冷冻干燥 离心
透析
透析膜:
材料: 火棉胶(Collodion), 玻璃纸(Cellophane), 纤维素 (Cellulose)
纤维透析管的处理: 1%乙酸水溶液 1h, 碱性EDTA (1% Na2CO3, 1 mM EDTA) 煮1h, 纯水清洗,保存.
透析液:
离心(2)
(Relative centrifugal force):
F=mω2r;
Fcf=(1.119×10-5)(rpm)2r
F摩擦=fv
F净=(Mp-Ms)ω2r-fv
沉淀速度与离心力的比率(单位离心场中颗粒的沉降速度 ), 蛋白质\核酸\病毒等的沉降系数介于1×10-13到200×10-13秒的
紫外-可见吸收法 荧光检测法
电化学检测法
质谱法
高效毛细管电泳
电泳淌度 电渗流
淌度和迁移时间 分离效率 分离度
高效毛细管电泳分离模式
毛细管区带电泳
以1×10-13s 为一个单位,称为斯韦德贝格单位(Svedberg),用S(大写)表示.
(Capillary Zone Electrophoresis, CZE) 纤维透析管的处理: 1%乙酸水溶液 1h, 碱性EDTA (1% Na2CO3, 1 mM EDTA) 煮1h, 纯水清洗,保存.
离心(3)
最大速度方法:
移动界面(Moving Boundary)超 速离心法
移动区带(Moving Zone)超速离心法
等密度方法(Isodensity):
样品的类型、采集与保存 酶样品的准备
亲和色谱
琼脂糖的溴化氰活化法
6-氨基己酸-琼脂糖和,1,6-己二胺-琼脂糖
层析柱短 配基-与大分子间以氢键离子键或疏水相互作用结合
透析 微过滤 盐析 冷冻干燥 离心
透析
透析膜:
材料: 火棉胶(Collodion), 玻璃纸(Cellophane), 纤维素 (Cellulose)
纤维透析管的处理: 1%乙酸水溶液 1h, 碱性EDTA (1% Na2CO3, 1 mM EDTA) 煮1h, 纯水清洗,保存.
透析液:
离心(2)
(Relative centrifugal force):
F=mω2r;
Fcf=(1.119×10-5)(rpm)2r
F摩擦=fv
F净=(Mp-Ms)ω2r-fv
沉淀速度与离心力的比率(单位离心场中颗粒的沉降速度 ), 蛋白质\核酸\病毒等的沉降系数介于1×10-13到200×10-13秒的
紫外-可见吸收法 荧光检测法
电化学检测法
质谱法
高效毛细管电泳
电泳淌度 电渗流
淌度和迁移时间 分离效率 分离度
高效毛细管电泳分离模式
毛细管区带电泳
以1×10-13s 为一个单位,称为斯韦德贝格单位(Svedberg),用S(大写)表示.
(Capillary Zone Electrophoresis, CZE) 纤维透析管的处理: 1%乙酸水溶液 1h, 碱性EDTA (1% Na2CO3, 1 mM EDTA) 煮1h, 纯水清洗,保存.
细胞中的生物大分子——蛋白质ppt

n条肽 链
a
m
m-n
ma- 至少 m-n 18(m-n)
n个
至少 n个
蛋白质的功能
多种多样的蛋白质执行各种特定的生理功能
细胞膜
蛋白质的空间结构和多样性
蛋白质的空 间结构
由于组成蛋白 质多肽链的氨基酸 在种类、数目、排 列顺序上的不同, 以及构成蛋白质的 多肽链在数目和空 间结构上的不同, 因此,细胞中的蛋 白质具有多样性。
D]
COOH
思考:氨基酸与氨基酸之间是如何反应 的呢?
R1 H R2 H2N C C OH H N C COOH H H O H2O 肽键 脱水缩合
R1 H2N C C H O
H R2 N C COOH H 二肽
二肽 多肽 肽链 H2O H2O
例1:在一条由100个氨基酸分子形成的多肽链 中,应含有的肽键数目是----------[ C ] A.101 B.100 C.99 D.98 例2:血红蛋白含有四条多肽链,共由574个氨基 酸分子构成,那么,该分子中含有的肽键数 目应是--------------------------[ B ] A.574 B.570 C.578 D.573
(4)一条肽链中至少含有氨基和羧基的数目为 1、1 ;x条肽链组成的蛋白质分子中,至 • 少含有氨基和羧基的数目为 x、x 。
总结
AA 相对 分子 质量 1条肽 链
AA 个数
肽键 个数
脱去 水分 子个 数
多肽 相对 分子 质量
氨基 数目羧基 数目a Nhomakorabeam
m-1
ma- m-1 18(m-1) 至少
1个
至少 1个
蛋白质知识点小结
约20种 元素组成 C、 H、 O、 N 类 种 氨基酸 R I
02章生物大分子

核酸。
在生物体系中,除了蛋白质和核酸外, 碳水化合物、脂等生物大分子也含有可与 金属发生作用的含氧基团,但是,到目前 为止,有关它们与金属离子相互作用的了 解还很少。
第一节 蛋白质及其组成与结构 第二节 核酸与其他生物分子
第一节 蛋白质及其组成与结构
蛋白质是生命体系中最重要的一类生 物大分子,是生命活动的主要承载者以 及生命现象的主要物质基础。据统计, 到目前为止所发现的蛋白质中大约有三 分之一为金属蛋白。
第二章 生物大分子 的结构及性质
生物无机化学的主体部分由金属元素的 配位化合物所构成。在生命体系中,金属中 心常常被给电子的各种配体所“包围”。
生物体系中的配体可分为两类: 1、简单的无机小分子或阴离子,如H2O、
S2-、O2-、OH-、PO43-、Cl-、HCO3-等; 2、生物大分子,如蛋白质(或多肽)和
鸟嘌呤、腺嘌呤的N7位置电负性最低, 是金属离子结合的主要位点。
二、其他生物分子
1、三磷酸腺苷 三磷酸腺苷(ATP)是生物体内广泛
存在的辅酶,是体内组织细胞所需能量的 主要来源。蛋白质、脂肪、糖和核苷酸的 合成都需要ATP的参与。
三磷酸腺苷中磷脂基可以和一系列金 属离子,尤其是硬金属离子结合。具估计, 细胞内大约超过90%的ATP与Mg2+结合, Mg2+-ATP是许多酶的底物或辅因子。
酶的催化特性:
1、高效性; 2、高度专一性; 3、反应条件温和;
第二节 核酸与其他生物分子
一、核酸
核酸分为脱氧核糖核酸(DNA)和核
糖核酸(RNA)两种。 磷酸
核酸 核苷酸
核苷
戊糖 碱基
脱氧核糖核酸(DNA)是染色体的主 要成分,真核生物的线粒体和叶绿体中也 含有DNA,原核生物的质粒全由DNA构成。 除了RNA病毒和噬菌体外,DNA是所有生 物的遗传物质基础。生物体的遗传信息都 储存在DNA分子中。
在生物体系中,除了蛋白质和核酸外, 碳水化合物、脂等生物大分子也含有可与 金属发生作用的含氧基团,但是,到目前 为止,有关它们与金属离子相互作用的了 解还很少。
第一节 蛋白质及其组成与结构 第二节 核酸与其他生物分子
第一节 蛋白质及其组成与结构
蛋白质是生命体系中最重要的一类生 物大分子,是生命活动的主要承载者以 及生命现象的主要物质基础。据统计, 到目前为止所发现的蛋白质中大约有三 分之一为金属蛋白。
第二章 生物大分子 的结构及性质
生物无机化学的主体部分由金属元素的 配位化合物所构成。在生命体系中,金属中 心常常被给电子的各种配体所“包围”。
生物体系中的配体可分为两类: 1、简单的无机小分子或阴离子,如H2O、
S2-、O2-、OH-、PO43-、Cl-、HCO3-等; 2、生物大分子,如蛋白质(或多肽)和
鸟嘌呤、腺嘌呤的N7位置电负性最低, 是金属离子结合的主要位点。
二、其他生物分子
1、三磷酸腺苷 三磷酸腺苷(ATP)是生物体内广泛
存在的辅酶,是体内组织细胞所需能量的 主要来源。蛋白质、脂肪、糖和核苷酸的 合成都需要ATP的参与。
三磷酸腺苷中磷脂基可以和一系列金 属离子,尤其是硬金属离子结合。具估计, 细胞内大约超过90%的ATP与Mg2+结合, Mg2+-ATP是许多酶的底物或辅因子。
酶的催化特性:
1、高效性; 2、高度专一性; 3、反应条件温和;
第二节 核酸与其他生物分子
一、核酸
核酸分为脱氧核糖核酸(DNA)和核
糖核酸(RNA)两种。 磷酸
核酸 核苷酸
核苷
戊糖 碱基
脱氧核糖核酸(DNA)是染色体的主 要成分,真核生物的线粒体和叶绿体中也 含有DNA,原核生物的质粒全由DNA构成。 除了RNA病毒和噬菌体外,DNA是所有生 物的遗传物质基础。生物体的遗传信息都 储存在DNA分子中。
人教版高中化学《生物大分子》完整版PPT1

题点(一) 糖的性质
1.(2021年1月新高考8省联考·江苏卷)葡萄糖的银镜反应实验如下:
步骤1:向试管中加入1 mL 2% AgNO3溶液,边振荡边滴加2%氨水,观察 到有白色沉淀产生并迅速转化为灰褐色。
步骤2:向试管中继续滴加2%氨水,观察到沉淀完全溶解。 ②图乙是我国自行研制的氢动力概念跑车.氢气作为最清洁燃料的原因是
解析:(1)制镜工业和热水瓶胆镀银都利用了葡萄糖中含有醛基,与银氨溶液反 应还原出单质银,所以反应为反应④。
△ 答案:(1)④ (2)CH2OH(CHOH)4CHO+2Cu(OH)2――→CH2OH(CHOH)4COOH +Cu2O↓+2H2O (3)C6H12O6+6O2―→6CO2+6H2O
[题点全盘查]
D.Cr2O72-可将葡萄糖氧化而不能共存,故D错误;
D.
工业炼铁、从海水中提取镁、制玻璃、水泥过程中都需要用到石灰石
(2) 淀 粉 和 纤 维 素 的 分 子 式 可 以 表 示 为 (C H O ) , 也 可 以 表 示 为 D.离子方程式不一定表示的是一类反应,如2CH3COOH+CaCO3═2CH3COO﹣+Ca2++H2O+CO2↑,该反应只表示醋酸和碳酸钙的反应,故D错误;
实验步骤
实验现象
试管壁上有 银镜出现
②与新制氢氧化铜溶液反应
实验步骤
实验现象
试管中出现 红色沉淀
③实验结论:
葡萄糖对银氨溶液、氢氧化铜等弱氧化剂表现出还原性,属于还原糖。
(5)应用 ①葡萄糖在食品和医药工业中有广泛应用。
②葡萄糖易于被人体吸收,经酶的催化发生氧化反应,放出热量,提供了维持生
命活动所需要的能量。反应形式表示如下: C6H12O6+6O2―― 酶→6CO2+6H2O。 葡萄糖
第二节 细胞中的生物大分子.ppt

核糖核酸(RNA) 碱基:A、U、G、C。
分布:细 胞质中。
增强对食物的了解, 让我们做一个优秀的 营养师吧!
单糖是指不能水解的糖,即糖类的最小单位。
葡萄糖、果糖、半乳糖。 (C6H1206) 核糖、 脱氧核糖。 (C5H1005)(C5H1004) 五碳糖 六碳糖
单 糖
分子式(C12H22O11)
2、二糖
二糖是指水解后能生成两个单糖的糖。
二糖必须水解成单糖才能被生物体吸收。
二 糖
麦芽糖 蔗糖 乳糖
水
葡萄糖 + 葡萄糖 果 糖 + 葡萄糖 半乳糖 + 半乳糖
解
分子式(C6H10O5)n
3、多糖
多糖是指水解后能生成多个单糖的糖。
多糖必须水解成单糖才能被生物体吸收。
多 糖
淀 粉:植物细胞内。 纤维素:植物细胞壁的成分之一。 糖 元:分肝糖元和肌糖元。
4、糖类鉴定
还原性糖 + 斐林试剂
△
砖红色 沉淀
还原性糖:单糖、麦芽糖、乳糖;
非还原性糖:淀粉、蔗糖。
概念
学习目标: 概述糖类、蛋白质的种类和功能; 举例说出脂质的种类和功能; 简述核酸的结构和功能。
一、生物大分子的基本骨架
—O
播放
—H
C
C原子
—S
—N
碳链
你知道什么叫做营养均衡吗? 我们所吃的食物中含有哪些物质?
水稻、甘蔗主要含( 糖类 ),
大豆、油菜主要含( 脂质 ),
蛋、奶主要含( 蛋白质 )。
肥胖影响健康
2、类脂
磷脂是构成细胞 膜和多种细胞器 膜的重要成分。
存在于:人和动物 的脑、卵细胞、肝 脏以及大豆的种子 中。磷脂分子3固醇胆固醇固醇
【高中生物】生物大分子ppt
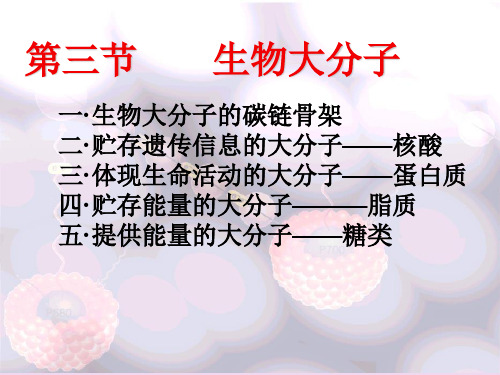
(一)、生物小分子和生物大分子的关系
小分子 大分子 单体
多聚体
单糖 · · · · · · · · · · · · · · · · · · · · · · · · · · · · · 多 糖 氨基酸 · · · · · · · · · · · · · · · · · · · · · · · · · 蛋白 质 (由小分子到大分子 ) 核苷酸 · · · · · · · · · · · · · · · · · · · · · · · · · 核酸
第三节
生物大分子
一· 生物大分子的碳链骨架 二· 贮存遗传信息的大分子——核酸 三· 体现生命活动的大分子——蛋白质 四· 贮存能量的大分子———脂质 五· 提供能量的大分子——糖类
一、生物大分子以碳链为骨架
生物大分子: 指的是作为生物体内 主要活性成分的各种分子量达到上万 或更多的有机分子。
常见的生物大分子包括: 蛋白质、核酸、脂质、糖类。
另外12种氨基酸是人体细胞能够合成的, 叫做非必需氨基酸。
我们应该注意及时补充必需氨基酸!
H NH2 C
O
C OH NH2
H C
O
C OH
H
H NH2 C
甘氨酸
O
C OH NH2
CH
缬氨酸
CH3 CH3 H C CH3 O C OH
CH2 亮氨酸
CH CH3 CH3
丙氨酸
试一试,能不能推导出氨基酸的结构通 式?
H
H C
N
H
C R2
||
O
_ OH
缩合
H
N
H
C R3
COOH
2H2O+
以此类推,三个氨基酸分子缩合而成的化 合物叫做三肽;四个氨基酸分子缩合而成 的化合物叫做四肽……。由三个或者三个 以上的氨基酸分子缩合而成的含有多个肽 键的化合物通称为多肽。 氨基酸
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
刮下结晶,蘸取少量接种到待结晶溶液,搅拌
(三)晶体的生长
晶体生长:在过饱和溶液中已有晶核形成或加 入晶种后,以过饱和度为推动力,晶核或晶种 将长大,这种现象称为晶体生长。
晶体生长速度也会影响晶体产品粒度大小。
晶核形成后立即开始生长成晶体,同时新的晶 核还在继续形成
晶核形成速度 > 晶体生长速度:细小晶体,甚至无定形 晶核形成速度 < 晶体生长速度:粗大而均匀晶体
溶液浓度
浓度高:结晶收率高 浓度过高:分子在溶液中析出
的速度太快,超过形成晶核的 速率,得不到晶体,只获得无 定形固体颗粒;杂质浓度增大, 易生成纯度差的粉末结晶。
样品纯度 纯度越高,越容易结晶
溶剂 溶剂不能和结晶物质发生化学反应
晶体形成
pH
等的一般方法
盐析法
主要用于大分子如蛋白质、酶、多肽等的结晶 原因:不耐热, 对pH变化及有机溶剂十分敏感 用中性盐作为沉淀剂, 操作安全简单
金属配合物法原理:
利用不同多糖能与金属离子形成配合物而沉淀下 来,使用多种配位剂沉淀多糖。
结晶 最先析出的微小颗粒是以后结晶的中心,称 为晶核。
只有达到一定的过饱和度时晶核才存在。
晶核形成并不是结晶的完成,还需要继续扩散 成长为晶体。
结晶
过饱和溶液的形成 晶核的形成 晶体的生长
(一)过饱和溶液的形成 结晶的首要条件是溶液的过饱和。
理论曲线
成 核 速 度
实际曲线
过饱和度
晶体生长速度和所需晶体大小
(2)温度
成 核 速 度
温度
温度
成核速度 过饱和度
温度与过饱和度 相互消长速度
(3)溶质种类
无机盐类: 阳离子或阴离子的化合价越低,越不容易成核 相同化合价下,含结晶水越多,越不容易成核
有机物质: 结构越复杂,相对分子质量越大,成核速度越慢
设计实验报告
*生物大分子分离
纯化及肝酶提取
*⑴ 乃至生几物千材种料化的合组物成。极其复杂,常常包含有数百种 *分离⑵纯许化多的生步物骤大繁分多子,在流生程物长材。料中的含量极微, * ⑶许多生物大分子一旦离开了生物体内的环境
时 就就 是生极物易大失分活子,提因取此制分备离最过困程难中之如处何。防止其失活,
制备如下:
脱脂→去杂→浓缩→再次去杂→脱色 →浓缩 →冷却 →结晶 (→进一步纯化)
*
多糖原料可从动植物器官、菌类及微生物发酵产物中得到。 一般多糖的分离纯化工艺: 一、分离提取方法 (extraction) (1)脱脂 由于多糖被脂质包围,通常用醇或醚回流脱脂。
(2)提取
①稀碱提取法:适合用此方法的多糖主要是不溶性胶类,用冷水浸 润0.5mol/L NaOH提取,提取液用酸中和后浓缩,再加乙醇沉淀 即得到多糖。甘露聚糖、半乳糖等利用此法可得到相当纯的物质。
制备
蒸发法 冷却法 化学反应结晶法 盐析结晶法 等电点法 复合法
(二)晶核的形成
晶核:过饱和溶液中最先析出的微小颗粒,是 以后结晶的中心。
成核速度:单位时间内在单位体积溶液中生成 的新晶核数目。是决定晶体产品粒度分布的首 要因素。
1.成核速度的影响因素:
溶液的过饱和度、温度、溶质种类
(1)过饱和度
*的 各种,⑷组温生成度物的、大综p分H合值子影、的响离制,子备很强几难度乎准等都确各是估种在计参溶和数液判对中断溶进。液行中
*
*
*前期准备
初级提取分离
生物材料的选择 及预处理
组织与细胞破碎
精细分离纯化
纯度鉴定
产物处理
糖类制品的分离及纯化 Isolation and depuration of sugar
盐析法原理:
利用不同多糖与金属离子成盐后在水溶液中的特 异性沉淀作用,用硫酸铵、乙酸钾、氯化钾等盐 析剂,将不同的多糖逐步析出。
季铵盐沉淀法原理:
长链季铵盐是碱性表面活性剂,酸性多糖在溶液 中以聚阴离子形式存在,它就与季铵盐或其碱形 成不溶性配合物沉淀,又由于多糖分子酸性越强、 相对分子质量越大越易沉淀出来,这样控制 季铵 盐浓度即可以分离出不同的酸性多糖。
影响晶体生长的因素: 杂质、搅拌、温度和过饱和度 ① 杂质:制止、促进、改变外形 ② 搅拌:促进扩散,加速晶体生长、晶核形成。 以试验为基础,确定适宜的搅拌速度 ③ 温度:升高有利于扩散,使结晶速度增快 ④ 过饱和度: 增高—使结晶速度增大 增高—引起黏度增加,结晶速度受阻
影响结晶析出的主要条件
2. 晶核的诱导 加晶种能诱导结晶 晶种可以是同种物质或相同晶形的物质,有时惰 性的无定形物质也可作为结晶的中心,如尘埃。
添加晶种诱导晶核形成的方法: (1)有现成晶体:取少量研碎,加溶剂,离心去 除大颗粒,稀释,悬浮液中有小晶核,倒入待结晶 溶液,搅拌,放置一段时间
(2)无现成晶体: ① 取1-2滴待结晶溶液置于表面玻璃皿上,缓慢 蒸发除去溶液,可得少量晶体 ② 取少量溶液置于试管中,旋转试管,使溶液 在管壁上形成薄膜,溶剂蒸发,冷却试管,管壁 上可形成一层结晶。
二、纯化方法( depuration) 由因于此提需取要液进还一含步有纯多化种。组其分方的法多有糖:混合物,
➢(1)沉淀法(常用乙醇沉淀法) ➢(2)盐析法 ➢(3)季铵盐沉淀法 ➢(4)纤维素柱层析法 ➢(5)离子交换层析法 ➢(6)金属配合物法
沉淀法原理:
由于不同相对分子质量的多糖在不同浓度的低级 醇或低级酮中溶解性不同,可以逐步提高溶液中 醇或酮的浓度以使不同组分的多糖依相对分子质 量由大到小的顺序沉淀,最终达到分离的目的。
纤维素柱沉淀法原理:
它利用的是不同多糖浓度乙醇中溶解性不同,先 用4倍V的乙醇将多糖混合液沉淀在惰性的多孔纤 维素柱上,再用不同浓度的乙醇洗脱,使不同多 糖分离开来。
离子交换层析法原理: 多糖分子带有电荷,可以 与离子交换剂中的
离子或基团结合,亲和力随多糖结构与电离性 的不同而不同,一般随分子中酸性基团的增加 而增强,然后用不同浓度的盐溶液进行洗脱。
②温水提取法:对于易溶于温水、难溶于冷水和乙醇的多糖采用这 种方法。材料需要先用冷水浸过,再用热水提取,必要时可加热 至80~90℃,搅拌提取,提取液用正丁醇与氯仿混合液除去杂蛋 白,离心除去杂蛋白的清液,透析后用乙醇沉淀即得到多糖。
*
除杂
Seveg法 三氟三氯乙烷法 三氯乙酸法 酶法 等电点沉淀法
(三)晶体的生长
晶体生长:在过饱和溶液中已有晶核形成或加 入晶种后,以过饱和度为推动力,晶核或晶种 将长大,这种现象称为晶体生长。
晶体生长速度也会影响晶体产品粒度大小。
晶核形成后立即开始生长成晶体,同时新的晶 核还在继续形成
晶核形成速度 > 晶体生长速度:细小晶体,甚至无定形 晶核形成速度 < 晶体生长速度:粗大而均匀晶体
溶液浓度
浓度高:结晶收率高 浓度过高:分子在溶液中析出
的速度太快,超过形成晶核的 速率,得不到晶体,只获得无 定形固体颗粒;杂质浓度增大, 易生成纯度差的粉末结晶。
样品纯度 纯度越高,越容易结晶
溶剂 溶剂不能和结晶物质发生化学反应
晶体形成
pH
等的一般方法
盐析法
主要用于大分子如蛋白质、酶、多肽等的结晶 原因:不耐热, 对pH变化及有机溶剂十分敏感 用中性盐作为沉淀剂, 操作安全简单
金属配合物法原理:
利用不同多糖能与金属离子形成配合物而沉淀下 来,使用多种配位剂沉淀多糖。
结晶 最先析出的微小颗粒是以后结晶的中心,称 为晶核。
只有达到一定的过饱和度时晶核才存在。
晶核形成并不是结晶的完成,还需要继续扩散 成长为晶体。
结晶
过饱和溶液的形成 晶核的形成 晶体的生长
(一)过饱和溶液的形成 结晶的首要条件是溶液的过饱和。
理论曲线
成 核 速 度
实际曲线
过饱和度
晶体生长速度和所需晶体大小
(2)温度
成 核 速 度
温度
温度
成核速度 过饱和度
温度与过饱和度 相互消长速度
(3)溶质种类
无机盐类: 阳离子或阴离子的化合价越低,越不容易成核 相同化合价下,含结晶水越多,越不容易成核
有机物质: 结构越复杂,相对分子质量越大,成核速度越慢
设计实验报告
*生物大分子分离
纯化及肝酶提取
*⑴ 乃至生几物千材种料化的合组物成。极其复杂,常常包含有数百种 *分离⑵纯许化多的生步物骤大繁分多子,在流生程物长材。料中的含量极微, * ⑶许多生物大分子一旦离开了生物体内的环境
时 就就 是生极物易大失分活子,提因取此制分备离最过困程难中之如处何。防止其失活,
制备如下:
脱脂→去杂→浓缩→再次去杂→脱色 →浓缩 →冷却 →结晶 (→进一步纯化)
*
多糖原料可从动植物器官、菌类及微生物发酵产物中得到。 一般多糖的分离纯化工艺: 一、分离提取方法 (extraction) (1)脱脂 由于多糖被脂质包围,通常用醇或醚回流脱脂。
(2)提取
①稀碱提取法:适合用此方法的多糖主要是不溶性胶类,用冷水浸 润0.5mol/L NaOH提取,提取液用酸中和后浓缩,再加乙醇沉淀 即得到多糖。甘露聚糖、半乳糖等利用此法可得到相当纯的物质。
制备
蒸发法 冷却法 化学反应结晶法 盐析结晶法 等电点法 复合法
(二)晶核的形成
晶核:过饱和溶液中最先析出的微小颗粒,是 以后结晶的中心。
成核速度:单位时间内在单位体积溶液中生成 的新晶核数目。是决定晶体产品粒度分布的首 要因素。
1.成核速度的影响因素:
溶液的过饱和度、温度、溶质种类
(1)过饱和度
*的 各种,⑷组温生成度物的、大综p分H合值子影、的响离制,子备很强几难度乎准等都确各是估种在计参溶和数液判对中断溶进。液行中
*
*
*前期准备
初级提取分离
生物材料的选择 及预处理
组织与细胞破碎
精细分离纯化
纯度鉴定
产物处理
糖类制品的分离及纯化 Isolation and depuration of sugar
盐析法原理:
利用不同多糖与金属离子成盐后在水溶液中的特 异性沉淀作用,用硫酸铵、乙酸钾、氯化钾等盐 析剂,将不同的多糖逐步析出。
季铵盐沉淀法原理:
长链季铵盐是碱性表面活性剂,酸性多糖在溶液 中以聚阴离子形式存在,它就与季铵盐或其碱形 成不溶性配合物沉淀,又由于多糖分子酸性越强、 相对分子质量越大越易沉淀出来,这样控制 季铵 盐浓度即可以分离出不同的酸性多糖。
影响晶体生长的因素: 杂质、搅拌、温度和过饱和度 ① 杂质:制止、促进、改变外形 ② 搅拌:促进扩散,加速晶体生长、晶核形成。 以试验为基础,确定适宜的搅拌速度 ③ 温度:升高有利于扩散,使结晶速度增快 ④ 过饱和度: 增高—使结晶速度增大 增高—引起黏度增加,结晶速度受阻
影响结晶析出的主要条件
2. 晶核的诱导 加晶种能诱导结晶 晶种可以是同种物质或相同晶形的物质,有时惰 性的无定形物质也可作为结晶的中心,如尘埃。
添加晶种诱导晶核形成的方法: (1)有现成晶体:取少量研碎,加溶剂,离心去 除大颗粒,稀释,悬浮液中有小晶核,倒入待结晶 溶液,搅拌,放置一段时间
(2)无现成晶体: ① 取1-2滴待结晶溶液置于表面玻璃皿上,缓慢 蒸发除去溶液,可得少量晶体 ② 取少量溶液置于试管中,旋转试管,使溶液 在管壁上形成薄膜,溶剂蒸发,冷却试管,管壁 上可形成一层结晶。
二、纯化方法( depuration) 由因于此提需取要液进还一含步有纯多化种。组其分方的法多有糖:混合物,
➢(1)沉淀法(常用乙醇沉淀法) ➢(2)盐析法 ➢(3)季铵盐沉淀法 ➢(4)纤维素柱层析法 ➢(5)离子交换层析法 ➢(6)金属配合物法
沉淀法原理:
由于不同相对分子质量的多糖在不同浓度的低级 醇或低级酮中溶解性不同,可以逐步提高溶液中 醇或酮的浓度以使不同组分的多糖依相对分子质 量由大到小的顺序沉淀,最终达到分离的目的。
纤维素柱沉淀法原理:
它利用的是不同多糖浓度乙醇中溶解性不同,先 用4倍V的乙醇将多糖混合液沉淀在惰性的多孔纤 维素柱上,再用不同浓度的乙醇洗脱,使不同多 糖分离开来。
离子交换层析法原理: 多糖分子带有电荷,可以 与离子交换剂中的
离子或基团结合,亲和力随多糖结构与电离性 的不同而不同,一般随分子中酸性基团的增加 而增强,然后用不同浓度的盐溶液进行洗脱。
②温水提取法:对于易溶于温水、难溶于冷水和乙醇的多糖采用这 种方法。材料需要先用冷水浸过,再用热水提取,必要时可加热 至80~90℃,搅拌提取,提取液用正丁醇与氯仿混合液除去杂蛋 白,离心除去杂蛋白的清液,透析后用乙醇沉淀即得到多糖。
*
除杂
Seveg法 三氟三氯乙烷法 三氯乙酸法 酶法 等电点沉淀法
