PCT质控品产品介绍
降钙素原PCT2015524

出生后时间(h) PCT[ng/mL]
0-6
2
脓
6-12
8
毒
12-18
15
症 新
18-30
21
生
30-36
15
儿
36-42
8
42-48
2
新生儿的正常范围(覆盖所有测量值的95%)
3. PCT在内科的使用
2. PCT判断细菌感染的灵敏指标
项目
细菌感染检 测阳性率
细菌感染 特异性
细菌培养 60-70%
高(95-100%)
WBC计数 50-70%
稍高(70-85%)
CRP检测 88-95%
较低(20-35%)
PCT测定
G+:70-85% G_:80-95%
高(88-98%)
临床意义
特殊作用
培养阳性:细菌感染诊断的金指标 加做药敏试验,指导抗生素使用
CRP C反应蛋白延迟释放,下降
1. 哪些情况下 PCT 会升高?
全身性细菌感染; 严重休克、SIRS和MODS等。 真菌、寄生虫、立克次体、结核等感染; 病毒感染、肿瘤、过敏、自身免疫性疾病及
局部感染患者中,PCT水平可轻度升高;
二. PCT临床意义
细菌感染的初筛 动态监测病人感染状态、治疗效果及指 导抗生素的使用 预测预后
391± 648 (20 – 3200)
CSF protein levels (g/l) 2.3 ± 1.2 (0.4-
4.74)
0.62± 0.47 (0.12-2.72)
CRP levels (g/l)
14.4± 69 (28-311)
降钙素原(PCT)质控品产品技术要求mairui

2性能要求
2.1外观和性状
2.1.1颜色性状
质控品复溶前应为浅黄色冻干粉末,复溶后应为清澈浅黄色液体,无沉淀、悬浮物和絮状物。
2.1.2包装
试剂瓶应无泄漏;盒贴、瓶贴、标签标识应完整、清晰。
2.2装量
质控品质量(含瓶重)均应不少于18 g。
2.3均一性
2.3.1瓶内均一性
质控品瓶内均一性应不大于表 2 的要求(SD 和CV 值满足其一即可)。
表 2 质控品瓶内均一性要求
2.3.2瓶间均一性
质控品瓶间均一性应不大于表3 的要求(SD 和CV 值满足其一即可)。
表3 质控品瓶间均一性要求
2.4参考值及参考范围
每批质控品均应提供本批产品的参考值表。
经迈瑞校准品校准的BS 系列生化分析仪及配套试剂对质控品进行测定,测定结果应在给定的参考范围内。
2.5生物安全性
质控品使用国家权威管理机构认可的、且不低于我国法定用于血源筛查体外诊断试剂
灵敏度的检测试剂,HBsAg、HIV 抗体、HCV 抗体、梅毒螺旋体TP 抗体检测应为阴性。
1。
降钙素原(PCT)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求runnuosi
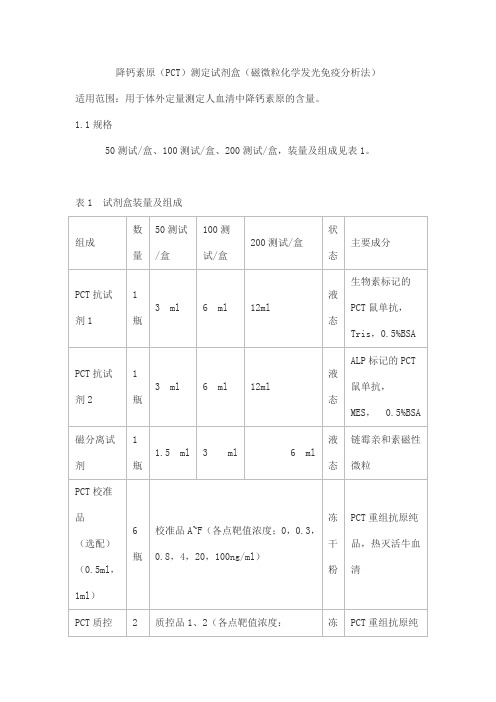
降钙素原(PCT)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血清中降钙素原的含量。
1.1规格50测试/盒、100测试/盒、200测试/盒,装量及组成见表1。
表1 试剂盒装量及组成2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后为均匀悬浊液,无明显凝集;2.1.3 液体组分应澄清,无沉淀或絮状物;2.1.4 包装标签应清晰,无磨损。
2.2准确度将已知浓度的PCT抗原加入到样本中,其回收率应在(85%~115%)范围内。
2.3空白检测限应不大于0.02ng/ml。
2.4线性在(0.02,100)ng/ml的测量范围内,试剂盒的相关系数r应≥0.99。
2.5重复性变异系数(CV)应不大于10%。
2.6质控品测值测值应在质控范围内。
2.7批间差批间变异系数(CV)应不大于15%。
2.8校准品瓶间差校准品的瓶间变异系数(CV)应不大于10%。
2.9分析特异性2.9.1 浓度不低于5000pg/ml白介素(IL-6)的零浓度PCT样本,在本试剂盒上测定结果应不高于0.03ng/ml。
2.9.2 浓度不低于10ng/ml降钙素(CT)的零浓度PCT样本,在本试剂盒上测试结果应不高于0.02ng/ml。
2.10稳定性2.10.1效期稳定性:试剂盒在2℃~8℃贮存,有效期为12个月,到效期后的试剂盒检测外观、准确度、空白检测限、线性、重复性和质控品测值,应符合2.1~2.6的要求。
2.10.2复溶稳定性:校准品与质控品复溶后,在2℃~8℃环境下保存3天后进行以下检测:a)校准品:进行准确度、质控品测值的检测,结果应符合2.2,2.6的要求。
b)质控品:进行质控品测值的检测,结果应符合2.6的要求。
降钙素原(PCT)质控品产品技术要求万孚生物

降钙素原(PCT)质控品
性能指标
1外观检查
质控品复溶前为白色或类白色疏松饼状结构,应在30秒内完全复溶,复溶后为澄清、透明液体,无沉淀、悬浮物和絮状物。
2包装
包装瓶为棕色玻璃瓶,盖有橡胶瓶内塞和塑料外盖;盒贴、瓶贴、标签标识应完整、清晰。
橡胶瓶内塞与玻璃配合后应无泄漏;塑料外盖应无明显划痕、崩缺。
3均一性
3.1瓶内均一性
瓶内CV≤15%。
3.2瓶间均一性
瓶间CV≤15%。
4靶值及靶值范围
4.1赋值程序
每批质控品均应提供本批产品的靶值和靶值范围表,并应提供赋值方法程序文件。
4.2赋值的准确性
用校准后的测量程序测定该质控物,检测结果应在其靶值范围内。
人降钙素原(PCT)ELISA试剂盒说明书

人降钙素原(PCT)酶联免疫吸附测定试剂盒使用说明书厦门慧嘉生物科技有限公司本试剂盒仅供体外研究使用、不用于临床诊断!预期应用ELISA法定量测定人血清、血浆或其它相关生物液体中PCT含量。
实验原理用纯化的PCT抗体包被微孔板,制成固相载体,往微孔中依次加入标本或标准品、生物素化的PCT抗体、HRP标记的亲和素,经过彻底洗涤后用底物(TMB)显色。
TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的PCT呈正相关。
用酶标仪在450nm波长下测定吸光度(值),计算样品浓度。
试剂盒组成及试剂配制1、酶标板:一块(96孔)2、标准品(冻干品): 2瓶,请临用前15分钟内配制。
每瓶以样品稀释液稀释至1ml,盖好后室温静置大约10分钟,同时反复颠倒/搓动以助溶解,其浓度为2,000 pg/ml,将其稀释为1,000 pg/ml后,再做系列倍比稀释(注:不要直接在板中进行倍比稀释),分别配制成1,000 pg/ml,500 pg/ml,250 pg/ml,125 pg/ml,62.5 pg/ml,31.2 pg/ml,15.6 pg/ml,样品稀释液直接作为空白孔 0 pg/ml。
如配制500 pg/ml标准品:取0.5ml(不要少于0.5ml )1,000 pg/ml的上述标准品加入含有0.5ml样品稀释液的Eppendorf 管中,混匀即可,其余浓度以此类推。
3、样品稀释液:1×20ml。
4、检测稀释液A:1×10ml。
5、检测稀释液B:1×10ml。
6、检测溶液A:1×120/瓶(1:100)。
临用前以检测稀释液A 1:100稀释(如:10 检测溶液A / 990检测稀释液A),充分混匀,稀释前根据预先计算好的每次实验所需的总量配制(100/孔),实际配制时应多配制 0.1-0.2ml。
7、检测溶液B:1×120/瓶(1:100)。
降钙素原(PCT)测定试剂盒(时间分辨荧光免疫层析法)产品技术要求注册版

医疗器械产品技术要求编号:降钙素原(PCT)测定试剂盒(时间分辨荧光免疫层析法)1.产品型号/规格及其划分说明1.1包装规格25人份/盒。
1.2主要组成成分由PCT测试卡、降钙素原(PCT)质控品、ID卡组成。
其中,PCT测试卡由试纸条、塑料盒组成;试纸条上的主要成分有硝基纤维素膜、吸水纸、样本垫、偶合物垫及PVC板;硝基纤维素膜包被有鼠抗人PCT抗体和羊抗鸡IgY抗体;样本垫上有鼠抗人红细胞抗体;偶合物垫上有荧光标记的鼠抗人PCT抗体和荧光标记的鸡IgY抗体。
降钙素原(PCT)质控品:重组人PCT蛋白。
ID卡:内含校准曲线信息。
1.3适用范围:用于体外定量测定人全血、血浆或血清中降钙素原(PCT)的含量。
临床上主要用于细菌感染性疾病的辅助诊断。
2.产品性能指标2.1试剂盒性能指标2.1.1外观a)试剂盒外观应整洁,文字符号标识清晰,封装无破损,内容物齐全。
b)测试卡外观应平整、色泽均匀、边缘无毛刺,无色斑或污渍,卡固定紧密。
2.1.2膜条宽度膜条宽度应不小于 1.4mm。
2.1.3液体移行速度液体移行速度应不低于10mm/min。
2.1.4准确度测定具有溯源性的PCT工作校准品,测量结果与标定浓度的相对偏差应不超过±10%。
2.1.5空白限应不大于0.04ng/mL。
2.1.6线性范围在0.05ng/mL~100ng/mL区间内,线性相关系数r≥0.9900。
2.1.7批内精密度用同一批次的试剂盒,两个浓度工作校准品测定结果的变异系数CV<10.0%。
2.1.8批间精密度用三个不同批次的试剂盒测试,两个浓度工作校准品测定结果的变异系数CV<15.0%。
2.2质控品性能指标2.2.1外观无色澄清透明液体。
2.2.2装量质控品装量为0.5mL,应不少于标示值。
2.2.3准确度和赋值程序质控品测试结果应在靶值范围之内,赋值程序见附录1。
2.2.4均一性对一瓶质控品重复10次检测,对同一批号的10瓶质控品进行检测,批内瓶间差CV应≤15%。
降钙素原(PCT)测定试剂盒(胶体金免疫层析法)产品技术要求meikang

降钙素原(PCT)测定试剂盒(胶体金免疫层析法)适用范围:用于体外定量检测人血清中的降钙素原,与南京美宁康诚生物科技有限公司生产的Mokosensor-A300型胶体金免疫分析仪配套使用。
1.1 包装规格20人份/盒、100人份/盒。
1.2 主要组成成分由相应人份的检测卡组成,其中,检测卡:检测线包被来源于小鼠的降钙素原单克隆抗体A、质控线包被羊抗鼠IgG多克隆抗体、金标垫上固定胶体金标记来源于小鼠的降钙素原单克隆抗体B。
2.1外观2.1.1外观平整,材料附着牢固,内容齐全,包装标签应清晰;2.1.2膜条宽度为4mm±0.2mm;2.1.3液体移行速度应不低于10mm/min。
2.2 空白限不高于0.10μg/L。
2.3 线性2.3.1试剂盒线性范围为[0.10,100.00]μg/L,线性相关系数r不低于0.9900;2.3.2 [0.10,0.25]μg/L绝对偏差不超过±0.02μg/L,(0.25,100.00]μg/L 线性偏差在±10%范围内。
2.4重复性检测高、低两个浓度的样本,变异系数(CV)应不大于10% 。
2.5准确度回收率在85%~115%。
2.6分析特异性检测浓度为100.00μg/L超敏C反应蛋白中降钙素原的浓度,计算交叉反应率,应小于10%。
2.7批间差检测一个高浓度的样本,相对极差应在±10%范围内。
2.8稳定性:常温(10℃~30℃)保存,有效期12个月,有效期末分别检测2.2~2.5项,其结果应符合各项要求。
2.9 校准品溯源性试剂盒校准信息所用校准品按照GB/T 21415-2008 《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,溯源到本公司工作校准品,工作校准品通过已上市产品试剂盒比对赋值。
降钙素原(PCT)测定试剂盒(荧光免疫层析法)产品技术要求puenguangde

降钙素原(PCT)测定试剂盒(荧光免疫层析法)
适用范围:用于体外定量测定人血清、血浆或全血中降钙素原(PCT)含量。
1.1包装规格
10人份/盒,25人份/盒,50人份/盒。
1.2主要组成成分
试剂盒由PCT荧光免疫层析检测卡、PCT样品稀释液(F)、PCT校准卡组成,各组分及数量见表1。
表1:试剂盒组成成分
2.1外观
外包装盒应完整,无破损;单包铝箔袋应完整,无破损,保持密封包装;液体组分应澄清透明,无沉淀、无渗漏。
2.2物理性状
2.2.1 试纸条的宽度:应不超于(
3.40±0.10)mm 。
2.2.2 液体移行速度:应不低于5mm/min。
2.3空白检出限
空白检出限浓度应不高于0.05ng/ml。
2.4线性范围
在[0.05,40]ng/ml范围内线性相关系数r≥0.990。
2.5精密度
2.5.1 重复性
变异系数CV不超于15%。
2.5.2 批间差
变异系数CV不超于20%。
2.6准确度
回收率应在85%~115%之间。
2.7分析特异性
测试按表2规定浓度范围的降钙素、白介素-6、C反应蛋白的样品,检测结果应不超过0.1ng/ml。
表2:交叉反应物及浓度列表
2.8效期稳定性试验
试剂盒2℃~30℃保存,铝箔袋密封状态下存放,取有效期满后两个月内的产品进行检测,结果应符合2.2、2.3、2.4、2.5.1、2.6项要求。
降钙素原(PCT)测定试剂盒(胶体金免疫层析法)产品技术要求mkjy

降钙素原(PCT)测定试剂盒(胶体金免疫层析法)适用范围:用于体外定量测定人全血中降钙素原的含量。
1.1 包装规格20人份/盒、100人份/盒。
1.2 主要组成成分每人份包括1个检测卡、1包干燥剂、1个铝箔袋,每盒试剂包括1个校准信息U盘,(内含校准曲线、产品批号、生产日期、“有效期至”信息)。
其中,检测卡:硝酸纤维素膜,检测线(T线)包被鼠抗人的降钙素原单克隆抗体A、质控线(C线)包被羊抗鼠IgG多克隆抗体、金标垫(材质:玻璃纤维)上固定胶体金标记的鼠抗人降钙素原单克隆抗体B、金标垫的下端装配有玻璃纤维材质的滤血膜。
2.1 外观2.1.1 外观平整,材料附着牢固,内容齐全,包装标签应清晰;2.1.2 膜条宽度为4mm±0.2mm;2.1.3 液体移行速度应不低于10mm/min。
2.2 空白限不高于0.1μg/L。
2.3 定量限测定0.2μg/L的降钙素原样本,变异系数(CV)应不大于10%。
2.4 线性2.4.1 线性范围为[0.2,100.0]μg/L,线性相关系数r不低于0.9900;2.4.2 [0.2,2.0]μg/L绝对偏差不超过±0.2μg/L,(2.0,100.0]μg/L线性偏差在±10%范围内。
2.5 重复性检测高、低两个浓度的样本,变异系数(CV)应不大于10%。
2.6 准确度将已知浓度的降钙素原加入到人全血基质或其它体液成分中, 回收率在85%~115%。
2.7 分析特异性测定浓度为100.0μg/L C反应蛋白,结果应小于0.2ug/L。
2.8 批间差用3个不同批号的试剂盒检测25.0ug/L高浓度样本,相对极差应在±10%范围内。
2.9量值溯源根据GB/T 21415规定了校准曲线的溯源情况,溯源至公司内部工作校准品,并与已上市产品比对赋值。
2.10稳定性:10℃~30℃保存,有效期12个月。
过有效期后进行检测,应符合2.2、2.3、2.4、2.5、2.6的要求。
降钙素原(PCT)测定试剂(荧光免疫层析法)产品技术要求梓健

2.性能指标
2.1外观和性状
外观和性状应符合表2要求。
表2试剂盒中各组分的外观性状组分外观性状
测试卡
铝箔袋外观平整无破损,封口严密,标签文字清晰
卡壳无明显污点,条码等标记清晰、准确
测试条无明显划痕、破损、外观平整、材料附着牢固缓冲液无絮状物及沉淀、文字和标记清晰、准确ID芯片文字和标识清晰、准确、无污痕
2.2膜条宽度
膜条宽为 4.0mm,允许偏差为±0.1mm;
2.3液体移行速度
以企业参考品作为样本,加样后,液体移行速度应不低于10mm/min。
2.4液体装量
每管样本缓冲液中液体的体积应在0.27ml±0.03ml范围之内。
2.5准确度
用已溯源的企业参考品作为样本进行检测,其测量结果的相对偏差(Bias%)不应超过±15%。
2.6最低检测限
应不大于0.1ng/mL。
2.7线性范围
试剂在[0.1~100]ng/mL的范围内,线性相关系数r≥0.990。
2.8精密度
2.8.1批内精密度
检测2个不同浓度的PCT企业参考品,批内精密度应不大于15%。
2.8.2批间精密度
检测2个不同浓度的PCT企业参考品,批间精密度应不大于15%。
罗氏诊断降钙素原(PCT)中文说明书

05056888 200 100测试主要用途用于体外定量检测人体血清或血浆中的PCT (procalcitonin)。
Elecsys BRAHMS PCT检测可辅助临床早期诊断相关的细菌感染。
Elecsys和cobas e 免疫分析仪的工作原理是电化学发光免疫分析“ECLIA”。
临床应用降钙素原(PCT)是由116个氨基酸组成的激素原,分子量大约为12.7kD。
PCT由神经内分泌细胞(包括甲状腺、肺和胰腺组织的C细胞)表达,经酶切分解为(未成熟)降钙素、羧基端肽和氨基端肽。
健康人血中仅含有少量的PCT1,2。
细菌感染后PCT会明显升高。
动物模型试验显示机体发生脓毒血症时,多组织均能表达PCT3。
脓毒血症患者体内的PCT只含有114个氨基酸,缺少氨基末端的Ala-Pro4。
PCT水平升高见于细菌性脓毒血症,尤其是重症脓毒血症和感染性休克5,6,7,8,9,10。
PCT可作为脓毒血症的预后指标8,11,12,13,也是急性重症胰腺炎及其主要并发症的可靠指标14,15。
对于社区获得性呼吸道感染和空调诱导性肺炎患者,PCT可作为抗生素选择以及疗效判断的指标。
检测原理双抗体夹心法,总检测时间:18分钟●第一次孵育:30μl样本、生物素化的单克隆PCT抗体以及钌复合物标记a的单克隆PCT抗体一起孵育,形成抗原抗体夹心复合物。
●第二次孵育:添加包被链霉亲和素的磁珠微粒进行孵育,复合体与磁珠通过生物素和链霉素的作用结合。
●将反应液吸入测量池中,通过电磁作用将磁珠吸附在电极表面。
未与磁珠结合的物质通过ProCell被去除。
给电极加以一定的电压,使复合体化学发光,并通过光电倍增器测量发光强度。
●Elecsys软件自动通过定标曲线计算得到检测结果。
a)Tris(2,2’-bipyridyl)ruthenium(II)-co mplex (Ru(bpy){23}三联吡啶钌试剂-工作溶液M 包被链霉亲和素的磁珠微粒(透明瓶盖),每瓶6.5ml;包被链霉亲和素的磁珠微粒,0.72mg/ml;防腐剂。
降钙素原(PCT)测定试剂盒(荧光免疫层析法)产品技术要求sz

批间变异系数(CV)应≤15%。
2.6准确度
回收率应在 85%~115%范围内。
1
2.1.3膜条宽度
膜条宽度为 4.00±0.40mm。
2.1.4液体移行速度
液体移行速度应不低于 25mm/min。
2.2线性范围
试剂的线性范围为0.2ng/ml~60ng/ml,在此线性范围内:线性相关系数r应不小于0.990。
2.3检测限
检测限应不大于 0.2ng/ml。
2.4批内精密度
变异系数(CV)应≤15%。
产品适用范围/预期用途
本试剂盒用于体外定量测定人血清、血浆和全血样本中降钙素原(PCT)的含量。临床上主要用于细菌感染性疾病的辅助诊断。
2,材料附着牢固;
样本稀释液为无色透明液体,无悬浮物及沉淀物。
2.1.2样本稀释液净含量
样本稀释液净含量偏差不大于标示量的±10%。
产品名称
降钙素原(PCT)测定试剂盒(荧光免疫层析法)
型号、规格
20人份/盒, 40人份/盒,60人份/盒
结构及组成
试剂盒由检测卡、稀释液和ID卡组成;检测卡主要组成成分有硝酸纤维素膜,玻璃纤维素膜,吸水纸,PVC板,红细胞抗体(RBC);其中硝酸纤维素膜在特定的位置上包被有PCT单克隆抗体和兔IgG,玻璃纤维素膜上喷有荧光微球标记的PCT单克隆抗体和兔IgG抗体。稀释液组分:PB缓冲液;Proclin300。ID卡包含校准曲线和批号。
PCT质控品产品介绍

质控品使用目的与方法
质控结果如何看?
举例 CRP 水平2:靶值 25mg/L,范围20mg/L~30mg/L 只要测试结果落在20~30mg/L之间,就认为产品合格,受控,不存在测到20.1mg/L就是 偏低,29.9mg/L就是偏高的说法
总结回顾
谢谢大家! 欢迎提出宝贵意见,增强相互交流!
• WST253-2005 参考物质的描述
体外诊断医学器具 生物源样品中量的测量
质控品使用目的与方法
什么情况需要做质控? A、装机及培训 B、客户投诉测试值不准 C、客户要求定期做质控
质控品使用目的与方法
怎么做质控?
从公司申请 CRP、PCT 质控品:经过客服或公司技术支持
公司需严格按照冷藏发货要求发货:至少加 6 块冰 现场开始质控测试前,把试剂条、缓冲液都平衡至室温:最佳温度为 22~27℃
质控品概述——关于校准品和质控品
校准品(Calibrator):预期用于制造商最终产品的校准品。
质控品(Control):用于体外诊断的质量控制物质,是一种旨在用于 医学用途的检测系统中使用的物质、材料、物品或设备,其目的是评 价或验证测量精密度、由于试剂或分析仪器的变化检测系统可能产生 的分析偏差等性能特征。
Wondfo质控品—— PCT质控品说明书
[检验方法的局限性]
1. 本质控品仅适用于广州万孚生物技术股份有限公司 的降钙素原(PCT)定量检测试剂盒(免疫荧光层析 法)。 2. 本产品不是校准品,不能用于仪器的校准。
[产品性能指标]
1. 开盖复溶后室温稳定8小时。 2. 准确性:在校准后的检测系统上检测该质控品,检 测值应在其标定的参考值范围内。
免疫层析法
广州万孚生物技术股份有限公司
降钙素原(PCT)测定试剂盒(胶乳免疫比浊法)产品技术要求百奥泰康

降钙素原(PCT)测定试剂盒(胶乳免疫比浊法)适用范围:该产品用于体外定量测定人血清中降钙素原(PCT)的浓度。
1.1 产品规格1.2 组成成分1.2.1 试剂组成试剂1:Tris缓冲液 100mmol/L试剂2:抗人降钙素原抗体包被的胶乳悬浊液<0.5%1.2.2 校准品的组成五个水平的校准品,校准品为冻干品,校准品组成是在牛血清(50g/L)中加入含不同浓度的降钙素原抗原,稳定剂<5%。
定值范围:(0.2-2)ng/mL;(2-5)ng/mL;(8-18)ng/mL;(15-32)ng/mL;(30-70)ng/mL。
1.2.3质控品的组成两水平冻干质控品,在牛血清(30g/L)中加入降钙素原纯品,稳定剂<5%。
目标浓度:(0.3-3)ng/mL、(5-25)ng/mL之间。
2.1 外观试剂1为无色澄清液体;试剂2为乳白色液体;校准品为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体;质控品为无色或浅黄色粉末状物质,复溶后为无色或浅黄色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 空白吸光度试剂空白吸光度应≤2.0。
2.4 分析灵敏度浓度为10ng/mL时,吸光度差值≥0.03。
2.5 线性在(0.15,60]ng/mL线性范围内,线性相关系数r应≥0.990;在(0.15,20]ng/mL 范围内绝对偏差不超过3.5ng/mL;在(20,60]ng/mL范围内的相对偏差不超过±15%。
2.6 精密度试剂盒测试项目精密度 CV≤10%。
2.7 批间差不同批号之间测定结果的相对极差应≤15%。
2.8 准确度回收实验:回收率在90%-110%。
2.9 质控品赋值有效性测定值在质控靶值范围内。
2.10 瓶间重复性(均一性)校准品、质控品瓶间重复性CV≤5%。
2.11校准品溯源性要求根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品控制物质赋值的计量学溯源性》及有关规定提供降钙素原校准品的来源、赋值过程以及测量不确定度等内容。
C反应蛋白(CRP)_降钙素原(PCT)质控品产品技术要求万孚

质控品复溶前为白色或类白色疏松饼状结构,复溶后为澄;
浮物和絮状物。
2.2包装
包装瓶为棕色玻璃瓶,盖有橡胶瓶内塞和塑料外盖;盒贴、瓶贴、标签标识应完整、清晰。
橡胶瓶内塞与玻璃配合后应无泄漏;塑料外盖应无明显划痕、崩缺。
2.3均一性 2.
3.1瓶内均一性
瓶内CVW15%。
2.3.2瓶间均一性
瓶间CVW15%。
2.4靶值及靶值范围
2.4.1赋值程序
每批质控品均应提供本批产品的靶值单,并应提供赋值方法程序文件。
2.4.2赋值的准确性
用校准后的测量程序测定该质控品,检测结果应在其靶值范围内。
人降钙素原(PCT)酶联免疫分析试剂盒产品说明书

人降钙素原(PCT) 酶联免疫分析试剂盒使用说明书【产品名称】通用名称:人降钙素原(PCT)酶联免疫分析试剂盒英文名称:PCT Quantitative Enzyme-linked Immunosorbent Assay Kit【包装规格】96人份/盒【预期用途】本试剂盒采用ELISA双抗体酶联免疫夹心法定量检测人血清、血浆及相关液体样本中降钙素原(PCT)含量。
适用于严重感染或脓毒血症的早期诊断;全身性感染与非细菌性炎症反应(如自身免疫性疾病)的鉴别诊断;全身性细菌性感染与病毒感染的鉴别诊断;全身性细菌/真菌感染与器官移植排斥和移植后病毒感染的鉴别诊断;作为高危患者(如ICU、器官移植术后或接受免疫抑制治疗的患者)感染性疾病的监测指标。
【临床意义】人降钙素原(PCT)是人降钙素的前体物,无激素活性,其在健康人血清中水平极低,但在全身性细菌感染患者血清中含量迅速升高,感染后两个小时即可检测到,且持续时间长,其在血清中的水平与感染性疾病的严重程度呈正相关,经有效抗生素治疗后,PCT水平可迅速下降,而病毒感染、肿瘤、自身免疫性疾病、外伤(多创伤或手术创伤)、临床用药、慢性炎症以及局部感染者,PCT水平维持在正常范围内或者有轻度升高。
因此,PCT是细菌感染所致重症全身性炎症反应的良好指标,在全身性细菌感染和脓毒症辅助鉴别诊断、预后判断、疗效观察等方面有很高的临床价值。
在局限性感染、病毒感染、自身免疫性疾病、手术创伤和慢性炎症时,其血浆浓度正常或轻度升高;严重细菌感染或霉菌、寄生虫感染(如腹膜炎、软组织感染、蜂窝组织炎、吻合口漏、肺炎、ARDS)时大量上升,特别是脓毒性休克时PCT时浓度成倍升高。
因此,利用它能有效地评估感染和炎症的严重程度及进展情况,还能监测药物疗效,指导外科围手术期的处理以及抗生素正确应用。
作为高危患者(如ICU、器官移植术后或接受免疫抑制治疗的患者)感染性疾病的监测指标;早期预测脓毒性休克、多器官功能不全综合征(MODS)、成人呼吸窘迫综合征(ARDS)及多器官功能障碍(MOF)的发生及判断疾病预后等。
降钙素原(PCT)测定试剂盒(胶乳免疫比浊法)产品技术要求北京赛诺浦生物

降钙素原(PCT)测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人体血清降钙素原的含量。
1. 产品型号/规格及其划分说明1.1试剂盒包装规格试剂1:1×15mL,试剂2:1×5mL;试剂1:2×30mL,试剂2:2×10mL;试剂1:2×54mL,试剂2:2×18mL;试剂1:3×45mL,试剂2:3×15mL;试剂1:4×54mL,试剂2:4×18mL;试剂1:2×300mL,试剂2:1×200mL;试剂1:1×9L,试剂2:1×3L。
校准品(选配,冻干品):6×0.5mL(六水平),6×1mL(六水平)。
质控品(选配,冻干品):1×0.5mL,1×1mL。
1.2试剂盒主要组成成分注:校准品和质控品存在批特异性,具体浓度见对应批次产品标签。
2.1 外观试剂1:无色澄清液体;试剂2:乳白色悬浊液。
校准品:淡黄色至黄褐色冻干品。
质控品:淡黄色至黄褐色冻干品。
2.2 净含量净含量不得低于标示体积。
2.3 检出限检出限 0.2ng/mL。
2.4 线性在(0.3,20)ng/mL范围内,线性相关系数r不小于0.990。
2.5 重复性重复测试(0.5±0.1)ng/mL和(10±1)ng/mL的样本,所得结果的变异系数(CV%)应不大于10%。
2.6 批间差重复测试(0.5±0.1)ng/mL和(10±1)ng/mL的样本,所得结果的批间变异系数(CV%)应不大于15%。
2.7 准确度回收率在(85~115)%范围内。
2.8 质控品赋值有效性测定结果在靶值范围内。
2.9 瓶间差(均一性)校准品和质控品瓶间变异系数(CV%)应不大于8%。
2.10 校准品溯源性依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,提供试剂盒内校准品的来源、赋值过程及测量不确定度。
降钙素原(PCT)测定试剂盒(荧光免疫层析法)产品技术要求普菲

降钙素原(P C T)测定试剂盒(荧光免疫层析法)产品技术要求普菲本页仅作为文档封面,使用时可以删除This document is for reference only-rar21year.March降钙素原(PCT)测定试剂盒(荧光免疫层析法)结构组成:预期用途:用于体外定量测定人血清、血浆样本中降钙素原的含量。
2.1.物理性状2.1.1.外观试剂卡外观平整,材料附着牢固;样本稀释液为无色透明液体,无悬浮物及沉淀物;2.1.2.净含量样本稀释液净含量应在标示值的90%~110%之间。
2.1.3.膜条宽度膜条宽度应不小于3.9mm。
2.1.4.液体移行速度液体移行速度应不低于25mm/min。
2.2.空白限空白限≤0.1ng/mL。
2.3 .线性范围试剂的线性范围为 [0.1,60] ng/mL,在此线性范围内,线性相关系数r应不小于0.990。
2.4.测量精密度2.4.1.重复性用质控品重复测试,所得结果的变异系数(CV)≤15%;2.4.2.批间差用质控品重复测试3个批号的试剂盒,所得结果的变异系数(CV)≤15%。
2.5.准确度回收率在85%~115%之间。
2.6 .稳定性试剂在4℃~30℃密封避光保存,原包装存放的试剂有效期为12个月;取效期末的样品检测外观、膜条宽度、液体移行速度、空白限、线性范围、重复性、准确度,应分别符合2.1.1、2.1.3、2.1.4、2.2、2.3、2.4.1、2.5的要求。
2.7.溯源性根据GB/T21415-2008的要求,本产品标准曲线可溯源至企业工作校准品。
降钙素原质控品产品技术要求yuepu

降钙素原质控品
适用范围:与本公司生产的试剂配套使用,用于降钙素原项目的室内质量控制。
1.1 规格
本产品为冻干粉,产品规格如下:
规格1:质控水平I 1×1mL,质控水平II 1×1mL,质控水平III 1×1mL;
规格2:质控水平I 3×1mL,质控水平II 3×1mL,质控水平III 3×1mL;
规格3:质控水平I 6×1mL,质控水平II 6×1mL,质控水平III 6×1mL。
1.2 主要组成成分
表1 质控品主要组成成分
表2 质控品的靶值范围
质控品的质控范围批特异性,详见瓶签。
2.1外观
标签清晰,质控品为淡黄色冻干品,用蒸馏水复溶后应为淡黄色液体。
2.2重复性
重复性CV(%)应不高于15%。
2.3瓶间差
瓶间差CV(%)应不高于15%。
2.4赋值有效性
测定结果应在质控范围内。
2.5稳定性
2.5.1复溶稳定性
质控品复溶后在2℃~25℃条件下4h后,产品性能应符合2.1、2.2、2.4规定的要求。
2.5.2效期稳定性
质控品在2℃~25℃的环境中保存18个月后,产品性能应符合2.1、2.2、2.4规定的要求。
降钙素原(PCT)检测试剂盒(化学发光法)产品技术要求tx

降钙素原(PCT)检测试剂盒(化学发光法)适用范围:用于体外定量测定人血清或血浆中降钙素原(PCT)的含量。
1.1包装规格48人份/盒、96人份/盒1.2主要组成成分表1 试剂盒组成及主要成份2.1外观组分齐全、完整,液体无渗漏,微孔板包装袋无破损、漏气现象;包装标签应清晰,易识别。
2.2装量液体装量应不少于标示值。
2.3准确度用已知浓度的纯品做回收试验,其回收率应在85-115%范围内。
2.4线性用适当的数学模型拟合,在线性范围内[0.05ng/ml,50ng/ml],剂量反应曲线相关系数(r)的绝对值应不低于0.9900。
2.5空白限应不大于0.05ng/ml。
2.6重复性同一次试验中分别重复检测浓度值为(1.03±0.22)ng/ml、(20.83±5.23)ng/ml 样本10次,其变异系数(CV)应不大于10.0%。
2.7批间差用3个批号的试剂盒检测浓度值为(1.03±0.22)ng/ml、(20.83±5.23)ng/ml,3个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.8分析特异性测定浓度为20ng/ml人下钙素(Katacalcin),交叉反应率小于0.5%。
测定浓度为60ng/mL人降钙素(Calcitonin),交叉反应率小于0.5%。
测定浓度为10000ng/ml人降钙素基因相关肽(CGRP,Calcitonin Gene-Related Peptide),交叉反应率小于0.5%。
2.9稳定性产品在2℃~8℃条件下保存有效期为12个月,取到效期产品在二个月内进行检测,检测结果应满足2.1~2.6项要求。
2.10校准品溯源性根据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准和控制物质赋值的计量学溯源性》有关规定提供所用校准品的来源、赋值过程以及不确定度等内容,校准品溯源至公司工作校准品。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
质控品概述——关于校准品和质控品
校准品(Calibrator):预期用于制造商最终产品的校准品。
质控品(Control):用于体外诊断的质量控制物质,是一种旨在用于 医学用途的检测系统中使用的物质、材料、物品或设备,其目的是评 价或验证测量精密度、由于试剂或分析仪器的变化检测系统可能产生 的分析偏差等性能特征。
免疫层析法
广州万孚生物技术股份有限公司
人降钙素原(PCT)检测试纸
胶体金免疫层析法 马鞍山国声生物技术有限公司
人降钙素原(PCT)定量检测试剂盒 胶体金法
天津中新科炬生物制药有限公司
降钙素原测定试剂盒
免疫色谱法
湖南布拉姆斯生物医药有限公司
已上市质控品——质控品需求
不同检测平台上质控品的使用情况
化学发光法 上转发光法 荧光定量法 酶联免疫法 金标法
校准品
√
×
×
√
×
(标准品)
质控品
√
√
√
√
×
已上市质控品——Wondfo PCT定量产品
产品优势 1. 国内唯一发明专利的成熟荧光定量平台
; 2. 全国首家真正实现床旁PCT全定量检测
; 3. 全国唯一具有质控品的PCT全定量检测
; 4. 实现全血样本检测;
Wondfo质控品——PCT质控品生产流程
• WST253-2005 参考物质的描述
体外诊断医学器具 生物源样品中量的测量
质控品使用目的与方法
什么情况需要做质控? A、装机及培训 B、客户投诉测试值不准 C、客户要求定期做质控
质控品使用目的与方法
怎么做质控?
从公司申请 CRP、PCT 质控品:经过客服或公司技术支持
公司需严格按照冷藏发货要求发货:至少加 6 块冰 现场开始质控测试前,把试剂条、缓冲液都平衡至室温:最佳温度为 22~27℃
辅料等
PCT重组蛋白
辅料等检定
PCT重组蛋白评价及配制浓度
冻干稀释液、冻干基质配制
PCT质控工作液配制及分装 预冻
真空冷冻干燥
加塞加盖 按要求装盒,附说明书等
质控品参数检测及赋值
QC成品检定 入库
Wondfo质控品—— PCT质控品说明书
Wondfo质控品—— PCT质控品说明书
[包装规格]
冻干粉型, 水平1:0.5ml ×1; 水平2:0.5ml ×1; 水平3:0.5ml ×1。
质控品概述——标准品、校准品和质控品的比较
提供者 标示值 适用范围
溯源性 是否通用 特点
标准品
校准品
质控品
国际/国家认可 的机构
有明确数值
生产厂家 一定范围区间
生产厂商用试 剂赋值
1、更换批号;2 、异常后校准;3 、修理后校准
1、室间/室内质评 ;
2、更换批号/结果 异常
有要求
无要求
是
否
仅有部分免疫 学标准品
质控品研发参考原则
• GBT 19702-2005 体外诊断医疗器械 生物源性样品中量的测量 参考测量程序的说明
• GBT 19703-2005 体外诊断医疗器械 生物源性样品中量的测量 参考物质的说明
• GBT 21415-2008 体外诊断医疗器械 校准品和控制物质赋值的计量学溯源性
生物样品中量的测量
质控品使用目的与方法
质控结果如何看?
举例 CRP 水平2:靶值 25mg/L,范围20mg/L~30mg/L 只要测试结果落在20~30mg/L之间,就认为产品合格,受控,不存在测到20.1mg/L就是 偏低,29.9mg/L就是偏高的说法
总结回顾
谢谢大家! 欢迎提出宝贵意见,增强相互交流!
Wondfo质控品—— PCT质控品说明书
[检验方法的局限性]
1. 本质控品仅适用于广州万孚生物技术股份有限公司 的降钙素原(PCT)定量检测试剂盒(免疫荧光层析 法)。 2. 本产品不是校准品,不能用于仪器的校准。
[产品性能指标]
1. 开盖复溶后室温稳定8小时。 2. 准确性:在校准后的检测系统上检测该质控品,检 测值应在其标定的参考值范围内。
高精密度
高稳定性
质控品概述——校准品和质控品的实际应用
✓ 大型检验仪器,如化学发光和酶免等,同时提供校准品和质控品, 且国内也在逐渐完善,如四川迈克。 ✓ 对于POCT产品,大多数厂家不提供校准品/质控品,有少数仅提供 质控品。 ✓ 对于床旁检验而言,不需校准步骤更便于使用。
已上市质控品——PCT检测试剂
拿到质控后及时使用:质控平衡到室温后避免反复冷藏再使用
CRP: 用准确量程的移液枪吸取 5μL 质控液血清
PCT: 用准确量程的移液枪吸取 0.5ml 纯化水,使冻干粉充分复融
PCT: 用准确量程的移液枪吸取 30μL/50μL 复融后 质控液加到缓冲液中
把质控液加入缓冲液中, 混匀 1min:混匀时间不多不少,准确掌握 1min 用移液枪准确吸取 75 μL 混匀后的缓冲液,加到测试卡上准点测试
人降钙素原(PCT) 分析试剂盒
酶联免疫
湖南三济生物科技有限公司
降钙素原(PCT)测定试剂盒
化学发光法
深圳市新产业生物医学工程有限公司
降钙素原(PCT)测定试剂盒
免疫增强比浊法 南京诺尔曼生物技术有限公司
血清降钙素原(PCT)测定试剂盒
增强化学发光法 广东虹业抗体科技有限公司
降钙素原(PCT)定量检测试剂盒
试剂盒
法
GmbH 不同浓度的PCT(重组), 同浓度的PCT(重组),浓
浓度具有批特异性。 度具有批特异性。
降钙素原定量 酶联发光法 bioMerieux PCT校准品
测定试剂盒
PCT对照品
已上市质控品——国产PCT产品
产品名称
产品方法
生产厂商
降钙素原(前降钙素,PCT)检测试剂 免疫层析法
武汉明德生物科技有限责任公司
Wondfo质控品—— PCT质控品说明书
[储存条件及有效期]
2 ℃-8 ℃密封避光保存,有效期24个月 。
[检验方法]
1. 质控品使用前先平衡至室温,开盖后,加 0.5ml蒸馏水复溶,轻微震荡并颠倒摇匀,注意不 要用力过大,避免气泡产生。
2. 检验时应按照患者血清标本对待,操作步骤
请参照广州万孚生物技术股份有限公司的降钙素 原(PCT)定量检测试剂盒(免疫荧光层析法) 和免疫荧光检测仪的使用说明书进行。
新型高特异性生化指标 诊断细菌性感染及脓毒症
已上市质控品——进口PCT定量产品
产品名称 产品方法 生产厂商
定标液
质控品
Cal1 PCT定标品1和 PCT质控品1和PCT质控Rocheຫໍສະໝຸດ Cal2 PCT定标品2: 品2:
降钙素原检测电化学发光
Diagnostics 人血清基质中含有两种 人血清基质中含有两种不
降钙素原(PCT)质控品介绍
一. 质控品概述 二. 已上市质控品概况 三. Wondfo质控品 四. 质控品研发参考原则 五. 质控品使用目的与方法
质控品概述——关于标准品
标准品(Reference Material):根据GB/T15000.2-94标准样品工作 导则中的定义,是具有足够均匀的一种或多种化学的、物理的、生物 学的、工程技术的或感官的等性能特征,经过技术鉴定,并附有说明 有关性能数据证书的一批样品。
