药品批准文号,生产批号
院内新进药品申请书模板(3篇)

第1篇尊敬的医院药品管理委员会:随着医疗技术的不断进步和临床需求的日益增长,我院药品品种和规格日益丰富。
为了更好地满足患者需求,提高医疗质量,现申请引进以下新药品。
为确保新药品的引进程序规范、科学,特此提交以下申请书。
一、药品基本信息1. 药品名称:__________2. 商品名称:__________3. 药品剂型:__________4. 药品规格:__________5. 药品批准文号:__________6. 药品生产厂家:__________7. 药品价格:__________8. 药品说明书:__________二、药品引进理由1. 疾病治疗需求:__________近年来,随着我国人口老龄化加剧,__________疾病的发病率逐年上升。
目前我院使用的__________药品在治疗__________疾病方面存在一定的局限性,如疗效不佳、副作用大等。
为提高患者的生活质量,降低疾病复发率,特申请引进__________药品。
2. 药品市场前景:__________根据我国药品市场调研报告显示,__________药品市场需求旺盛,预计未来几年市场增长率将达到__________%。
引进__________药品有利于我院在市场竞争中占据有利地位,提高医院经济效益。
3. 药品安全性:__________经过临床研究证实,__________药品具有以下优点:(1)疗效显著:__________药品在治疗__________疾病方面具有显著疗效,可有效缩短患者病程,提高治愈率。
(2)安全性高:__________药品经过严格的安全性评价,未发现明显不良反应。
(3)适应症广:__________药品适用于多种疾病的治疗,具有广泛的市场前景。
4. 药品经济性:__________引进__________药品后,预计我院药品库存周转率将提高__________%,降低药品库存成本__________%。
新药及药品批准文号格式

《进口药品注册证》、《医药产品注册证》 注册证号格式亦作部分改变
统一换发并规范药品批准文号格式说明(续1)
原文号 国药准(试)字X00000000系列 国药准(试)字(1998)X -0000号系列 国药准(试)字(1999)X –0000号系列 国药准字XF00000000系列 国药准字(1998)XF -0000号系列 国药准字(1999)XF -0000号系列 国药准(试)字(1998)Z -0000号系列 国药准(试)字(1999)Z -0000号系列
药事管理与法规
沈阳药科大学工商管理学院
罗刚
2005年3月19日
办公室: 主楼四楼工商管理教研室
电 话:
23843711-3356
E-mail: yoursluogang@
欢迎同学们拷贝本幻灯!
第二讲 药品注册管理
《药品注册管理办法》简介 药品注册基础知识 新药注册管理 今年工作重点
22药品批准文号格式换发期间国药准字1位字母8位数字国药试字1位字母8位数字23统一换发并规范药品批准文号格式说明000001号换发为国药准字h11020001zz前缀进口药品注册证医药产品注册证注册证号格式亦作部分改变24统一换发并规范药品批准文号格式说明续原文号新文号顺序号国药准字x00000000系列国药准h00000000不变国药准字1998x0000号系列国药准h19980000重新编0000号系列国药准1000起编排国药准字xf00000000系列国药准字h000000003000起编排国药准字1998xf0000系列国药准字h199800003000起编排国药准字1999xf0000系列国药准字h199900004000起编排国药准字1998z0000号系列国药准z19980000不变国药准字1999z0000号系列国药准1000起编排25统一换发并规范药品批准文号格式说明续原文号新文号顺序国药准字zf00000000系列国药准字z000000003000起编排国药准字1998zf0000国药准字z199800003000起编排国药准字1999zf0000国药准字z199900004000起编排国药准字1998厂家s0000号系列国药准s19980000重新编排国药准字1999厂家s0000号系列国药准1000起编排国药准字sf00000000系列国药准字s000000003000起编排国药准字1998sf0000国药准字s199800003000起编排国药准字1999sf0000国药准字s199900004000起编排国药准字年号d0000国药准字t00000000重新编排国药准字年号js0000系列国药准字j00000000重新编排药用新辅料批准文号国药准字f00000000重新编排26通过sda整顿的保健药品进口分包装药品27日以前sda批准药品各省行政区划代码前两位为原各省级卫生行政部门批准的药品28各省市行政区划代码29其他数字的含义位为换发批准文号之年公元年号的后两位数字但来源于卫生部和sda的批准文号仍使用原文号年号的后两位数字位为顺序号30完整含义换发期间原浙江省卫生厅批准原国家药品监督管理局2002年换发批准正式生产的顺序号0224的化学药品31四药品批准文号管理除经sfda批准的药品委托生产和异地加工外同一药品不同生产企业发给不同的药品批准文号药品批准文号进口药品注册证或者医药产
药品的批准文号、批号、效期的识别与意义

药 品 的批 准 文号 、 批 号 和有 效 期 , 是 药 品信 息 的 一项 重 要 内容 , 不 仅涉 及 到药 品的生 产 时 间和 批次 , 还涉 及 到药 品 的销售 . 使 用及药 品的监 督管 理 等多个 环 节 , 所 以掌 握不 同 药 品 的批 准 文号 和效 期 、 批号 对 临床 和 患者 都 有重 要 意义 。 现 将如何 准确判 断药 品批 准文号 、 有 效期与批 号 阐述 如下 :
参考文献
[ 1 ] 尤山. 如何 正确 误别 药 品的有效 期 Ⅱ 】 . 内江科技 , 2 o o 0 ( o 5 ) . [ 2 1 迟利锋 . 关于 药品有 效期 的探 究 U ] . 中国 民族 民间医药 , 2 0 1 1 ( 0 2 )
2 药品的批号
药 品批 号是 生产 单 位 在 药 品生 产 过 程 中 , 将 同 一 次 投 料, 同一次 生 产 工艺 所 生产 的 药 品用一 个 批号 来 表示 , 可由 批号 推 算 药 品的有 效 期 和存 效 时间 的长 短 同 时便 于药 品的 抽 样 检 验 。我 国药 品生 产 批 号 通 常 由 6 或8 位数组成 , 以 6位 数表 示前 两 位 为年 份 , 中 间为 月份 , 后两 位 为 日期 。如 :
药 品的批准文号、批号 、效期 的识别与意义
鼋
( 内蒙古赤峰市敖汉旗贝子府镇 中心卫 生院 ,内蒙古 敖汉 0 2 4 3 0 0 )
药品不良反应报告表 填写示例及填写说明
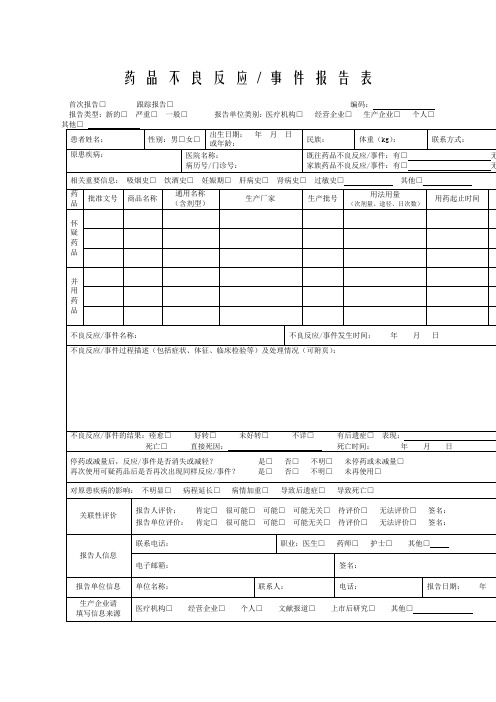
药品不良反应/ 事件报告表首次报告□跟踪报告□编码:报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□药品不良反应/ 事件报告表示例首次报告□跟踪报告□编码:1.《药品不良反应/事件报告表》应填写真实事件,报表所列患者信息及怀疑药品信息项目必须真实、完整、准确。
2.《药品不良反应/事件报告表》填写字迹要清晰,其中选择项画“√”,叙述项应准确、简明,不得有缺漏项。
3. 新的□严重□一般□(1)新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
根据不良反应/事件损害的严重程度,不良反应/事件可能是新的严重的,也可能是新的一般的。
(2)严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:1) 导致死亡;2)危及生命;3)致癌、致畸、致出生缺陷;4)导致显著的或者永久的人体伤残或者器官功能的损伤;5)导致住院或者住院时间延长;6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
(3)一般:指新的、严重的药品不良反应以外的所有不良反应。
4. 单位名称:必须填写单位的完整全称,如日照市人民医院。
5. 部门:应填写科室的标准全称,如:消化内科、普外三科等。
6. 电话:填写报告部门(即科室)的电话。
7. 报告日期:指上交不良反应/事件报告的时间。
新的或严重的药品不良反应/事件应于发现之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应应30日内报告。
有随访信息的,应当及时报告。
8. 患者姓名:填写患者真实全名。
9. 体重:以千克为单位。
如果不知道准确体重,请做一个最佳的估计。
10. 联系方式:最好填写患者的联系电话,也可填写患者的通信地址。
11. 家族药品不良反应/事件及既往药品不良反应/事件情况:请选择正确选项。
如果选择“有”,则在报告的空白处清晰叙述。
药品专业知识与技能培训

5.药品的规格 : 药品的规格是指一定药物制剂单元内所含药物 成分的量。药品规格的表示通常用含量、容量、浓度、质量( 重量)、数量等其中一种方式或几种方式结合来表示。 同一种药品常常不仅有不同的规格,还有各级不同大小的 包装单位。
一般药品包装常可分为最小包装、中包装、大包装 等三到四级 包装单位。
“请仔细阅读药品使用说明书并按说明使用或在药师指导下购买和使用。”
药品经营方式:国家规定有三种形式。一是药品批发经营;一是 药品零售经营,一种是零售连锁经营
药品经营范围:是指经药品监督管理部门核准经营药品的品种类 别。
药品生产企业:是指生产药品的专营企业或者兼营企业。 药品批发企业:是指将购进的药品销售给药品生产企业、药品经
药品。一般多在中药材 放射性药品:是指用于临床诊断或者治疗的放射性核素制剂或者其标记化合物。
因此,凡在分子内或制剂内含有放射性核素的药品都称为放射性药品。 药 材:一般是指未经加工的中药原料药。 中药:是指以中医理论为指导用以预防、诊断和治疗疾病的药用物质。其主要来
源: 天然药及其加工品,包括植物药、动物药、矿物药及部分化学、生物发酵 制品。 中药饮片:是指在中医药理论的指导下,可直接用于调配或制剂的中药材及中药材 的加工炮制品。
电子监管历程
国家局从2006年开始实施药品电子监管工作,至2012年2月底,已分三期将麻 醉药品、精神药品、血液制品、中药注射剂、疫苗、基本药物全品种纳入电子 监管:
2007年11月1日:对麻醉药品、一类精神药品和小包装原料药实行电子监管 2008年10月31日:“四大类”药品:二类精神药品、血液制品、疫苗、中药注射剂 2011年4月1日:基本药物目录307个品种,一律不得参与基本药物招标采购、销售 2012年1月1日:对含麻黄碱类复方制剂、含可待因复方口服溶液、含地芬诺酯复方制剂 2013年11月:基本药物国产药品和在国内分包装的进口药品应于2013年11月底前实行电子监管,进口药品应
药品基本知识一

药品基本知识1、什么是药品?药品是一种特殊商品。
药品,是指用于预防、治疗、诊断人的疾病,有目的地调节人的生理机能并规定有适应症或者功能主治、用法和用量的物质,包括中药材、中药饮片、中成药、化学原料药及其制剂、抗生素、生化药品、放射性药品、血清、疫苗、血液制品和诊断药品等。
2、什么是西药西药即为有机化学药品,无机化学药品和生物制品看其说明书则有化学名,结构式,剂量上比中药精确,通常以毫克计。
3、什么是中成药Traditional Chinese Medicine Patent Prescription中成药是以中草药为原料,经制剂加工制成各种不同剂型的中药制品,包括丸、散、膏、丹各种剂型。
是我国历代医药学家经过千百年医疗实践创造、总结的有效方剂的精华。
生活中人们常说的中成药是指由中药材按一定治病原则配方制成,随时可以取用的现成药品,如各种丸剂、散剂、冲剂等。
优点是现成可用、适应急需、存贮方便、能随身携带、省去了煎剂煎煮过程、消除了中药煎剂服用时特有的异味和不良刺激等。
缺点是药的成分组成、药量配比一成不变,不能灵活多变、随症加减,另外近年来,有关中成药引起的毒性反应及过敏反应也有报道,如朱砂安神丸可引起口腔炎、蛋白尿及严重的药源性肠炎;黑锡丹久服可致严重铅中毒;羚翘解毒丸或银翘解毒丸可引起严重的过敏性休克等。
这些反应虽较少见,一旦发生病情都较严重。
因此有服用某种中成药而发生中毒或过敏反应者,必须牢记以后不可再服同种药。
4、何谓剂型何谓剂型---药品制成适合医疗或预防应用的形式,方便临床使用,充分发挥药物作用,降低或避免不良反应。
如片剂、胶囊剂、软膏剂等,同一种药物,根据临床需要可以的剂型,制成不同的剂型,如尼莫地平有片剂和注射剂,不同剂型有不同的使用特点,同一种药物剂型不同,作用同时也不同。
剂型的种类有:液体剂型、注射剂型、输液剂、眼用剂型、散剂、浸出剂型、片剂、胶囊剂、丸剂剂型、软膏剂型、硬膏剂型、栓剂、气雾剂、长效制剂、膜剂、海绵剂、和微型胶囊、脂质体、贮库制剂等。
药品监督检查要点

6、生化药品:生化药品是指以生物化 学方法为手段从生物材料中分离、纯化、 精制而成的用来治疗、预防和诊断疾病的 药品。比如氨基酸、肽、蛋白质、酶类。
7、放射性药品:放射性药品是指用于 临床诊断或者治疗的放射性核素制剂或者 其标记化合物。放射性药品与其它药品的 不同之处在于,放射性药品含有的放射性 核素能放射出射线。因此,凡在分子内或 制剂内含有放射性核素的药品都称为放射 性药品。
(二)对损伤或者残疾的诊断、治疗、监护、 缓解、补偿;
(三)对解剖或者生理过程的研究、替代、 调节;
(四)妊娠控制。
国家对医疗器械实行分类管理:
第一类:通过常规管理足以保证其安全性、 有效性的医疗器械;
第二类:对其安全性、有效性应当加以控 制的医疗器械;
第三类:植入人体,用以支持、维持生命, 对人体具有潜在危险,对其安全性、有效 性必须严格控制的医疗器械。
药品监督检查要点概述
凤翔县食品药品监督管理局 陈晓龙 2019-12—26
药品基本知识
一、基本概念
药品,是指用于预防、治疗、诊断人的 疾病,有目的地调节人的生理机能并规定 有适应症或者功能主治、用法和用量的物 质,包括中药材、中药饮片、中成药、化 学原料药及其制剂、抗生素、生化药品、 放射性药品、血清、疫苗、血液制品和诊 断药品等。
五、药品的质量标准
质量标准是药品生产、 检验、供应与使用的依 据。国家药品标准包括 《中华人民共和国药 典》、药品注册标准和 其他药品标准。
六、药品的批准文号
药品批准文号是指国家食品药品监督管 理局批准药品生产企业生产药品的文号, 是药品生产合法性的标志。未取得批准文 号而生产的药品按假药论处。
在药品包装或说明书上应标有药品通 用名。药品商品名称不得与通用名称同行 书写,其字体和颜色不得比通用名称更突 出和显著,其字体不得大于通用名称所用 字体的二分之一
药学基本知识

药物基本作用:调节功能、抑制或杀灭病原体、补偿体内必需物质。
给药途径吸收速度顺序:气雾吸收、舌下含服、直肠给药、肌肉注射、皮下注射、口服给药、皮肤贴剂
药品商品名称:系指国家药品监督管理部门批准的特定企业使用的商品名称。药品商品名称须经国家药品监督管理局批准后方可在其包装、标签上使用。
药品注册商标:是由文字、符号及图形等综合组成的。是药品的销售包装及其他宣传品专用的标志,也是药品生产者为把自己的产品与他人的同类产品相区别的标志。
药品批准文号:是药品生产合法性的标志。《药品管理法》规定,生产药品“须经国务院药品监督管理部门批准,并发给药品批准文号”。
药品供上市销售的最小包装必须附有说明书。
药物的作用是指药物与生物体相互作用后呈现的效应。
药物的基本作用:调节功能、抑制或杀灭病原体、补偿体内必需物质
药物的体内过程:吸收、分布、代谢和排泄ADME四个基本过程。
药动学过程:药物的体内过程导致在不同的组织、器官和体液间的药物浓度随时间变化而改变,这种动态的药物转运和转化过程,称为动力学过程。
s.i.d 一日一次 M.D.S. 混合、给予、标明
b.i.d 一日二次 Rp. 取
t.i.d 一日三次 g. 克
q.i.d 一日四次 o.p. 眼用
a.c 饭前 Kg. 公斤(千克)
p.c 饭后 L. 升
a.m 上午 mg. 毫克
p.m 下午 ml. 毫升
Aq.dest 蒸馏水 i.u. 国际单位
生物利用度:是指药物经血管外给药后能被吸收进入人体循环的百分数。
药品购进验收管理制度

应按其特性,采取干燥、降氧、熏蒸等方法进行养护; (三) 药品养护人员应对库存药品根据流转情况定期进
行质量检查,发现问题及时处理并有记录。
第三条 医疗机构应对质量不合格药品进行控制性管理, 并
做到: 发现不合格药品应按规定的要求和程序上报,并及时查 明质量不合格的原因; (二) 不合格药品要单独存放,并有明显标志; 合格药品的确认、报告、报损、销毁应有完善的处 理程序和记录。 第四条 凡有质量问题的药品,不得向病人或患者使用。 第五条 医疗机构库房、药房用于储存和陈列药品的货
第三条 库房、药房工作人员应配戴标明其姓名、职务、 职称的胸牌,精神饱满,穿戴整洁,勤剪指甲,讲究卫生。
第四条 医疗机构直接接触药品的人员每年必须进行一次 健康检查,并建立健康档案,不得有漏检或找人替检的行 为。
第五条 发现患有传染病或其它可能污染药品的疾病,应 及时调离其工作岗位,待身体恢复健康并体检合格后,方 可工作。
6卫生和人员健康管理制度
第一条 为保证药品质量、确保用药安全有效,创造一个 清洁、舒适的工作环境,依据《中华人民共和国药品管理 法》等相关法律法规,制定本制度。
第二条 医疗机构药库和药房应保持干净、整洁,每日坚 持打扫卫生,做到“四无”,即无积水、无垃圾、无烟头、 无污染,保持环境卫生清洁。
第十条 医疗机构应当对麻醉药品和精神药品处方进行专 册登记,加强管理,并按规定将处方留存备查。麻醉药品 处方至少保存3年,精神药品处方至少保存2年。
第十一条 由于破损、变质、过期失效而不可供药用的品 种,应清点登记,单独妥善保管,并列表上报卫生主管部 门,不得擅自处理。
第十二条 不合格品种应按规定的程序办理报告、确认、 报损、销毁,需报损、销毁的特殊管理药品必须报卫生部 门批准后监督销毁,并做好销毁记录。
批准文号

药品批准文号格式2002年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品,采用新的药品批准文号格式1、药品批准文号格式:国药准字+1位字母+8位数字,试生产药品批准文号格式:国药试字+1位字母+8位数字。
进口药品注册证格式:由字母H(Z或S)后接八位阿拉伯数字组成,前四位为公元年号,后四位为顺序编号。
化学药品使用字母“H”,中药使用字母“Z”,通过国家药品监督管理局整顿的保健药品使用字母“B”,生物制品使用字母“S”,体外化学诊断试剂使用字母“T”,药用辅料使用字母“F”,进口分包装药品使用字母“J”。
数字第1、2位为原批准文号的来源代码,其中“10”代表原卫生部批准的药品,“19”、“20”代表2002年1月1日以前国家药品监督管理局批准的药品,其它使用各省行政区划代码(见附件一)前两位的,为原各省级卫生行政部门批准的药品。
第3、4位为换发批准文号之年公元年号的后两位数字,但来源于卫生部和国家药品监督管理局的批准文号仍使用原文号年号的后两位数字。
数字第5至8位为顺序号。
2、每种药品的每一规格发给一个批准文号。
除经国家药品监督管理局批准的药品委托生产和异地加工外,同一药品不同生产企业发给不同的药品批准文号。
3、自2002年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品,一律采用新的药品批准文号格式。
4、自2002年1月1日以后批准发给的化学药品《进口药品注册证》,其注册证号格式亦作部分改变,其中字母“X”改为“H”,其它部分不变。
原已发给的旧格式注册证号在换发《进口药品注册证》时用新格式取代。
5、药品批准文号及化学药品的进口药品注册证号换发后,印有原格式批准文号及注册证号的包装标签在2003年12月31日后禁止流通使用。
6、药品批准文号采用的中华人民共和国行政区划代码例如,“国药准字H11020001”,字母和数字含义依次是:“H”为化学药品,“11”为北京市的行政区划代码前两位,“02”为换发之年2002年的后两位数字,“0001”为新的顺序号。
批准文号及许可证号释义

消毒用品批准文号
• 格式:“卫消字(年份)第xxxx号”、“卫消进 字(年份)第xxxx号”。
• 不得标注无效批准文号,如(1996)×卫消准字 第xxxx号。因为从2006年起消毒剂省级批号上 升为国家级。
• 生产企业卫生许可证号:“(省、自治区、直辖 市简称)卫消证字(发证年份)第xxxx号”
医疗器械批准文号
• 格式:x(x)1(食)药监械(x2)字xxxx3 第 x4xx5xxxx6 号;
• 含义:x1为注册审批部门所在地的简称。境内第 三类医疗器械、境外医疗器械以及台湾、香港、 澳门地区的医疗器械为“国”字。境内第二类医 疗器械为注册审批部门所在的省、自治区、直辖 市简称。境内第一类医疗器械为注册审批部门所 在的省、自治区、直辖市简称加所在设区的市级 行政区域的简称,为xx1(无相应设区的市级行 政区域时,仅为省、自治区、直辖市的简称);
Future Development
致力于成为全球医药行业的优势产业资源整合者! 致力于成为中国医药商业领域整合者及区域领导者!
致力成为中国最大的 OEM 产品生产的领先者!
Global Pharm
Providing for a Healthy Life Every Day!
环球医药,传递健康生活每一天!
Thank You!
化妆品批准文号
• 国产特殊用途化妆品卫生许可批件必须由 国家食品药品监督管理局批准:格式为“ 国妆特字G+4位年度+4位编码”(如:国 妆特字G20100001)。
• 2008年前由原卫生部批准的特殊用途化妆 品,卫生许可批件仍在有效期的,格式为 “卫妆特字+(4位年份)+第××××号” (如卫妆特字[2008]第0001号)。
电子教案与课件:《药品购销技术》第2章药物基础知识 3-3药品的质量要求及包装

(2)非法定标准可以由行业集团乃至制 药公司制定,不能低于法定标准。
2.中华人民共和国药典
• 1953年--首版药典 • 2015年--现用版本,是新中国成立以来的第10版药典。 • 2015年版药典共分为四部 一部:药材和饮片、植物油和提取物、成方制剂和单 味制剂等 二部:化学药品、抗生素、生化药品、放射性药品等 三部:生物制品 四部(总则):通则(制剂通则、通用(检测)方法和 指导原则)、药用辅料
3.国外药典
美国药典(USP) 英国药典(BP) 日本药局(JP) 欧洲药典(EP) 国际药典(Ph.lnt)
三、药品的包装与标识
(一)药品包装的基本要求 1.应适应不同流通条件的需要 2.应和内容物相适应 3.要符合标准化要求
此外,药品包装还有一些具体要求,如药品包装(包括运输包装)必 须加封口、封签、封条或使用防盗盖、瓶盖套等;标签必须贴牢、 贴正,不得与药物一起放入瓶内;凡封签、标签、包装容器等有破 损的,不得出厂和销售。
特殊管理药品、非处方药及外用药品的标签上必须印有规定的标 志。在国内销售的药品的包装、标签、说明书必须使用规范化汉字, 增加其他文字对照的,应当以汉字表述为准。
(二)包装的类别与材料
1.包装的类别 (1)按包装在流通领域中的作用分类 ①销售包装(内包装、零售包装) ②储运包装(外包装) (2)按包装技术与目的分类 ①真空包装 ②充气包装 ③无菌包装 ④条形包装⑤喷雾包装 ⑥儿童安全包装 ⑦危险品包装
国药准字号的定义

关于国药准字号的定义“国药准字”是药品生产单位在生产新药前,经国家食品药品监督管理局严格审批后,取得的药品生产批准文号,相当于人的身份证。
其格式为:国药准字+1位字母+8位数字,其中化学药品使用的字母为“H”,中药使用的字母为“Z”等等。
只有获得此批准文号,药品才可以生产、销售。
由于历史原因,以前省级药品主管部门有权对药品进行审批,一些药品使用的是地方批准文号,如“京卫药准字”、“沪卫药准字”等。
这些药品都是根据各省、直辖市的地方药品标准审批的,不利于国家对药品的统一管理。
为了保证临床用药安全,1999年以后,国家将过去的地方药品标准,提升为国家药品标准,对“X(省)卫药准字”的格式的药品进行清理整顿,对符合国家标准的药品核发“国药准字”的批准文号,对不符合国家标准的药品予以淘汰,同时将新药审批的权限划归为国家食品药品监督管理局。
在现行《药品管理法》中规定,生产药品“需要经过国务院药品监督管理部门批准,并发给药品批准文号”。
所以,现在如果我们在市场上发现“X卫药准字”等非“国药准字”批准文号的药品,因为已经过了国家药监局规定的有效期,均可视为假药。
百姓们在买药时,一定要仔细看好批准文号。
无批准文号,或批准文号有问题的药品,不要购买,以免买到假药。
食品、保健品和药品均使用不同的批准文号,而这些批准文号在近几年又因为审批权限移交、政策调整和法规修订等原因,曾有过更换。
对于药品,现在国家规定统一使用的批准文号是“国药准字”号,即平常所说的“药字号”。
根据国家药监局规定,自2003年6月30日后生产的药品实施新的批准文号,格式是:国药准字+1位拼音字母+8位数字,字母用拼音字头表示药品类别,数字表示批准药品生产的部门、年份及顺序号。
保健品的批准文号则是“卫食健字”或“国食健字()第××号”。
其中2003年以前通过审批的批号是“卫食健字”,2003年以后通过审批的批号是“国食健字”。
而保健品的“药健字”在2004年前已被取消,市场上已不允许这种批号流通。
药品说明书和标签管理规定(说明书样稿)

药品说明书和标签管理规定第一章总则第一条为加强药品监督管理,规范药品说明书和标签的印制,根据《中华人民共和国药品管理法》、《中华人民共和国药品管理法实施条例》(以下分别简称《药品管理法》、《实施条例》),制定本规定。
第二条中华人民共和国境内上市销售的药品,其说明书和标签的印制适用本办法。
第三条药品说明书,是指药品生产企业印制并提供的,包含药理学、毒理学、药效学、医学等药品安全性、有效性重要科学数据和结论的,用以指导临床正确使用药品的技术性资料。
药品标签,是指药品包装上印有或者贴有的内容。
药品说明书和标签由国家食品药品监督管理局根据申请人申报的资料及其他相关信息核准。
第四条药品的每个基本包装单元必须附有说明书并印有或者贴有标签。
药品说明书和标签按照国家食品药品监督管理局规定的内容和格式印制。
第五条药品说明书和标签必须使用国家语言文字工作委员会公布的规范化汉字,药品生产企业根据需要,可以使用外文或者民族文字对照。
第六条药品说明书和标签的文字表述应当规范、准确、简练、通顺。
非处方药说明书还应当使用科学易懂的文字,以便于患者选择和使用药品。
第七条国家食品药品监督管理局根据保护公众健康和指导临床正确用药的需要,可以要求药品生产企业在说明书或标签上标注警示语。
药品生产企业也可以主动提出在药品说明书或标签上标注警示语。
第二章药品说明书第八条药品生产企业应当对药品说明书的正确性与准确性负责,并跟踪药品上市后的安全性、有效性情况,及时对药品说明书进行修订。
第九条国家食品药品监督管理局可以根据药品不良反应监测等情况,要求药品生产企业修改说明书。
第十条药品说明书必须包括以下内容:药品名称、成份、适应症或者功能主治、用法、用量、不良反应、禁忌、注意事项、规格、有效期、批准文号和生产企业。
药品说明书还必须包括孕妇及哺乳期妇女用药、药物相互作用,缺乏可靠的实验或者文献依据而无法表述的,说明书保留该项标题并应当注明“尚不明确”。
药品验收管理规定

药品验收管理规定验收时应按照药品的分类,对抽样药品的外观、包装、标签、说明书以及有关要求的证明文件对每批药品进行逐一抽样检查、核对:5.6.1.验收人员应当对抽样药品的外观、包装、标签、说明书等逐一进行检查、核对,验收结束后,应当将抽取的完好样品放回原包装箱,加封并标示。
出现问题的,交质量管理人员处理;5.6.1.1.应当检查运输储存包装的封条有无损坏,包装上是否清晰注明品名、规格、生产厂商、生产批号、生产日期、有效期、批准文号、贮藏、包装规格及储运图示标示或特殊管理的药品、外用药品、非处方药品的标识等标记。
5.6.1.2.抽取的样品应当具有代表性,同一批号的药品至少检查一个最小包装,但生产企业有特殊质量控制要求或者打开最小包装可能影响药品质量的,可不打开最小包装;破损、污染、渗液、封条损坏等包装异常以及零货、拼箱的,应当开箱检查至最小包装;外包装及封签完整的原料药、实施批签发管理的生物制品,可不开箱检查。
最小包装应当检查封口是否严密、牢固、有无破损、污染或渗液,包装及标签印字是否清晰,标签粘贴是否牢固。
5.6.1.3.每一最小包装的标签、说明书是否符合以下规定:A标签应当有品名、规格、用法用量、批准文号、生产批号、生产厂商等内容。
对注射剂瓶、滴眼剂瓶等因标签尺寸限制无法全部注明上述内容的,至少应标明品名、规格、批号3项;中药蜜丸蜡壳至少注明品名。
B化学药品与生物制品说明书应当列有以下内容:药品名称(通用名称、商品名称、英文名称、汉语拼音)、成分【活性成分的化学名称、分子式、分子量、化学结构式(复方制剂可列出其组分名称)】、性状、适应症、规格、用法用量、不良反应、禁忌、注意事项、孕妇及哺乳期妇女用药、儿童用药、老年用药、药物相互作用、药物过量、临床试验、药理毒理、药代动力学、贮藏、包装、有效期、执行标准、批准文号、生产企业(企业名称、生产地址、邮政编码、电话和传真)。
C中药说明书应当列有以下内容:药品名称(通用名称、汉语拼音)、成分、性状、功能主治、规格、用法用量、不良反应、禁忌、注意事项、药物相互作用、贮藏、包装、有效期、执行标准、批准文号、说明书修订日期、生产企业(企业名称、生产地址、邮政编码、电话和传真)。
药品包装、说明书需要注明内容总结

药品包装、说明书需要注明内容总结1、发运中药材的包装必须注明:品名、产地、日期、调出单位,并附有质量合格的标志。
(药品管理法,P56,53条)2、中药饮片的标签:品名、规格、产地、生产企业、产品批号、生产日期、实施批准文号管理的中药饮片必须注明药品批准文号。
(注意没有:有效期)(药品管理法实施条例,P67,45条)3、标签或说明书药品管理法规定:通用名、成分、规格、生产企业、批准文号、产品批号、生产日期、有效期、适应症或功能主治、用法、用量、禁忌、不良反应和注意事项。
(药品管理法,P56,54条)4、药品内标签:药品通用名称、适应症或功能主治、规格、用法用量、生产日期、产品批号、有效期、生产企业等。
内标签因包装尺寸过小至少应当标注的有:药品通用名称、规格、产品批号、有效期等P220,17条药品外标签:药品通用名称、成份、性状、适应症或功能主治、规格、用法用量、不良反应、禁忌、注意事项、贮藏、生产日期、产品批号、有效期、批准文号、生产企业等。
P220,18条5、运输、储藏的包装标签:药品通用名称、规格、贮藏、生产日期、产品批号、有效期、批准文号、生产企业,可根据需要注明:包装数量、运输注意事项或者其他标记等。
P220,19条运输、储藏包装和原料药标签标示的内容比较(P220,19、20条)①“规格”标示在运输、储藏包装的标签中,而没有标示在原料药标签中。
②“执业标准”没有标示在运输、储藏包装的标签中,而标示在原料药标签中。
③运输、储藏包装标示的是“药品通用名称”;原料药标签标示的是“药品名称”。
6、原料药的标签:药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业,同时还需要注明包装数量、运输注意事项等。
P220。
食字号、健字号、械字号、妆字号、消字号、药字号区别

什么是批文?批文也叫批号、批准文号,是指:药厂生产新药或者已有国家标准的药品的,经国务院药品监督管理部门批准,并在批准文件上规定该药品的专有编号,此编号称为药品批准文号,简称批文或者批号。
从广义上来看,批文可以分为外用产品批文和内服产品批文。
外用产品批文包括:药字号、健字号、消字号、械字号、妆字号。
内服产品批文包括:药字号、健字号、食字号、特医。
药字号:药字号也称为国药准字号,“国药准字”是药品生产单位在生产新药前,经国家食品药品监督管理局严格审批后,取得的药品生产批准文号,相当于人的身份证。
只有获得此批准文号,药品才可以生产、销售。
药字号包含处方药和非处方药。
消毒产品:消毒产品包括消毒剂、消毒器械(含生物指示物、化学指示物和灭菌物品包装物)、卫生用品和一次性使用医疗用品。
消毒剂:用于皮肤、粘膜消毒的消毒剂(其中用于粘膜消毒剂仅限医疗卫生机构诊疗用);用于餐饮具消毒的消毒剂;用于瓜果、蔬菜消毒的消毒剂;用于水消毒的消毒剂;用于环境消毒的消毒剂;用于物体表面消毒的消毒剂;用于空气消毒的消毒剂用于排泄物、分泌物等污物消毒的消毒剂。
消毒器械:用于医疗器械、用品灭菌的灭菌器械;用于医疗器械、用品消毒的消毒器械;用于餐饮具消毒的消毒器械;用于空气消毒的消毒器械;用于水消毒的消毒器械;用于物体表面消毒的消毒器械。
械字号:医疗器械是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件。
妆字号:化妆品是指以涂抹、喷洒或者其他类似方法,散布于人体表面的任何部位,如皮肤、毛发、指趾甲、唇齿等,以达到清洁、保养、美容、修饰和改变外观,或者修正人体气味,保持良好状态为目的的化学工业品或精细化工产品。
食字号:食品分为以下几类固体饮料风味固体饮料;果蔬固体饮料(果汁粉、蔬菜汁、果汁);蛋白固体饮料(含乳蛋白、植物蛋白、复合蛋白);茶固体饮料(速溶茶、研磨茶、调味茶、果汁茶、奶茶);咖啡固体饮料(速溶、研磨)、植物固体饮料(谷物、草本、可可、其他);茶:代用茶、袋泡茶、含茶制品(固态、液态);液体:饮品、植物饮料、配制酒;其他:片剂(压片糖果)、酵素、膏(固元膏、阿胶膏)、蜂蜜制品、食用菌等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
×(×)1(食)药监械(×2)字××××3 第×4××5××××6 号。其中:
×1为注册审批部门所在地的简称:
境内第三类医疗器械、境外医疗器械以及台湾、香港、澳门地区的医疗器械为“国”字;
境内第二类医疗器械为注册审批部门所在的省、自治区、直辖市简称;
了解药品批准文号统一格式识别方法后,让我们一起来识别几种常用药品,如(1)广谱喹诺酮类抗菌药可乐必妥(左氧氟沙星)片的批准文号为国药准字H20000655,表明该药是化学药品,系国家药品监督管理局于2000年批准生产的,顺序号为0655。(2)治疗腹泻的培菲康胶囊的批准文号是国药准字S10950032,表明该药为生物制品,是原卫生部于1995年批准生产的,顺序号为0032。(3)抗血小板聚集药物波立维(硫酸氯吡格雷)片的批准文号为国药准字J20040006,表明该药系进口分装药品,国家食品药品监督管理局于2004年批准生产,顺序号为0006。(4)用于跌打损伤的云南白药胶囊的批准文号是国药准字Z53020799,表明该药是中药,云南省药品监督管理部门于2002年批准生产,顺序号0799。
如何识别药品批准文号《中华人民共和国药品管理法》规定,生产药品须经国家药品监督管理部门批准,并发给药品批准文号方可生产,未经批准生产的药品以假药论处。因此,药品批准文号是指药品生产企业在生产药品前报请国家药品监督管理部门批准后获得的身份证明,是依法生产药品的合法标志。
怎样识别药品批准文号呢?国家药品监督管理局于2001年对药品批准文号和试生产药品批准文号的表达格式作了规定,统一格式为“国药准(试)字+1位汉语拼音字母+8位阿拉伯数字”。其中(1)“准”字代表国家批准正式生产的药品,“试”字代表国家批准试生产的药品。(2)国药准(试)字后的1位汉语拼音字母代表药品类别,分别是H代表化学药品,S代表生物制品,J代表进口分装药品,T代表体外化学诊断试剂,F代表药用辅料,B代表保健药品,Z代表中药。(3)汉语拼音字母后的8位阿拉伯数字中的第1、2位代表批准文号的来源,其中10代表原卫生部批准的药品,19、20代表国家食品药品监督管理局批准的药品,各省、自治区、直辖市的数字代码分别是11-北京市,12-天津市,13-河北省,14-山西省,15-内蒙古自治区,21-辽宁省,22-吉林省,23-黑龙江省,31-上海市,32-江苏省,33-浙江省,34-安徽省,35-福建省,36-江西省,37-山东省,41-河南省,42-湖北省,43-湖南省,44-广东省,45-广西壮族自治区,46-海南省,50-重庆市,51-四川省,52-贵州省,53-云南省,54-西藏自治区,61-陕西省,62-甘肃省,63-青海省,64-宁夏回族自治区,65-新疆维吾尔自治区。8位阿拉伯数字中的第3、4位表示批准某药生产之公元年号的后两位数字,第5、6、7、8位数字(即最后四位数字)为顺序号。
境内第一类医疗器械为注册审批部门所在的省、自治区、直辖市简称加所在设区的市级行政区域的简称,为××1(无相应设区的市级行政区域时,仅为省、自治区、直辖市的简称);
×2为注册形式(准、进、许):
“准”字适用于境内医疗器械;
“进”字适用于境外医疗器械;
“许”字适用于台湾、香港、澳门地区的医疗器械;
掌握了药品批准文号统一格式的识别方法,就能很快判断药品的一些基本情况,有助于对药品真伪或是否合法进行判别,保障用药安全。人们在买药时,要看清药品批准文号,无批准文号或批准文号标注有问题的药,千万不要购买和使用。
《药品注册管理办法》于2007年6月18日经国家食品药品监督管理局局务会审议通过,现予公布,自2007年10月1日起施行。
序号,其中H代表化学药品,Z代表中药,S代表生物制品。对于境内分包装用大包装规格的注册证,其证号在原注册证号前加字母B。
新药证书号的格式为:国药证字H(Z、S)+4位年号+4位顺序号,其中H代表化学药品,Z代表中药,S代表生物制品。
如何读懂医疗器械注册号
械注册证书由国家食品药品监督管理局统一印制,相应内容由审批注册的(食品)药品监督管理部门填写。(2004年8月9曰—现在)
××××3为批准注册年份;
×4为产品管理类别;
××5为产品品种编码;(54—手术室、急救室、诊疗室设备及器具;64—医用卫生材料及敷料)
××××6为注册流水号
其中第一百七十一条
药品批准文号的格式为:国药准字H(Z、S、J)+4位年号+4位顺序号,其中H代表化学药品,Z代表中药,S代表生物制品,J代表进口药品分包装。
《进口药品注册证》证号的格式为:H(Z、S)+4位年号+4位顺序号;
《医药产品注册证》证号的格Байду номын сангаас为:H(Z、S)C+4位年号+4位顺
