药品的批准文号
名称、文号

怎样识别药品批准文号呢?国家药品监督管理局于2001年对药品批准文号和试生产药品批准文号的表达格式作了规定,统一格式为“国药准(试)字+1位汉语拼音字母+8位阿拉伯数字”。
其中,①“准”字代表国家批准正式生产的药品,“试”字代表国家批准试生产的药品。
②国药准(试)字后的1位汉语拼音字母代表药品类别,分别是H代表化学药品,S代表生物制品,J代表进口分装药品,T代表体外化学诊断试剂,F代表药用辅料,B代表保健药品,Z代表中药。
③汉语拼音字母后的8位阿拉伯数字中的第1、2位代表批准文号的来源,其中10代表原卫生部批准的药品,19、20代表国家食品药品监督管理局批准的药品,各省、自治区、直辖市的数字代码分别是11-北京市,12-天津市,13-河北省,14-山西省,15-内蒙古自治区,21-辽宁省,22-吉林省,23-黑龙江省,31-上海市,32-江苏省,33-浙江省,34-安徽省,35-福建省,36-江西省,37-山东省,41-河南省,42-湖北省,43-湖南省,44-广东省,45-广西壮族自治区,46-海南省,50-重庆市,51-四川省,52-贵州省,53-云南省,54-西藏自治区,61-陕西省,62-甘肃省,63-青海省,64-宁夏回族自治区,65-新疆维吾尔自治区。
8位阿拉伯数字中的第3、4位表示批准某药生产之公元年号的后两位数字,第5、6、7、8位数字(即最后四位数字)为顺序号。
了解药品批准文号统一格式识别方法后,让我们一起来识别几种常用药品。
(1)广谱喹诺酮类抗菌药可乐必妥片的批准文号为国药准字H20000655,表明该药是化学药品,系国家药品监督管理局于2000年批准生产的,顺序号为0655。
(2)治疗腹泻的培菲康胶囊的批准文号是国药准字S1*******,表明该药为生物制品,是原卫生部于1995年批准生产的,顺序号为0032。
(3)抗血小板聚集药物波立维片的批准文号为国药准字J20040006,表明该药系进口分装药品,国家食品药品监督管理局于2004年批准生产,顺序号为0006。
药品批准文号的注册要求 流程

药品批准文号的注册要求流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!药品批准文号注册要求。
一、申请主体。
药品生产企业。
药品进口企业。
药品证明文件关系---药品注册证书、注册批件、新药证书、批准文号

新药证书是国产新药批准后发给的证明文件,若生产企业同时申请生产,则同时发给批准文号,从1985年开始实施。
批准文号是国产药品的身份证明,1981年开始施行。
1985年开始以法律形式实施,在生产新药、已有标准国家标准的药品均需获得批准文号。
药品注册批件:2002年开始国家食品药品监督管理局对国产新药申请和仿制药申请,以《药品注册批件》的形式决定是否批准。
药品注册证书是2003年国家食品药品监督管理局在统一换发药品文号后,发给生产企业的证明取得批准文号的文件。
发证范围包括已换发批准文号的全部品种及2002年以后批准生产品种、“国药准字B”型批准文号品种、通过中成药地方标准整顿品种等,凡原发给批准文号时的批件背面未附带再注册登记表者。
”进口药品注册证及医药产品注册证:是进口药品的身份证明,自1999年开始实施。
2002年起对境外进口核发《进口药品注册证》。
中国香港、澳门和台湾地区的制药厂商申请注册的药品,核发《医药产品注册证》。
”再直白一点注册证书1)是2003年换发文号后的药品、2003年前批准的注册批件不带再注册登记表的药品的批准证明文件,相当于2003年以后药品的注册批件(仅指生产批件)。
2)是境外或港澳台地区药品的批准证明文件。
新药证书是所有国产新药的新药证明文件!注册证书及注册批件相当于身份证,批准文号相当于身份证号,新药证书是不是可以相当于独生子女证?新药证书1、1985年卫生部颁发的《新药审批办》中规定:“研制单位在新药临床研究结束后,如需生产,必须向所在省、自治区、直辖市卫生厅(局)提出申请,报送有关资料及样品,经审查同意后转报卫生部,由卫生部审核批准,发给“新药证书”及批准文号。
未取得批准文号的新药一律不得生产”。
2、1999年国家药品监督管理局颁发《新药审批》办法中规定“新药一般在完成Ⅲ期临床试验后经国家药品监督管理局批准,即发给新药证书。
持有《药品生产企业许可证》并符合国家药品监督管理局《药品生产质量管理规范》(GMP)相关要求的企业或车间可同时发给批准文号,取得批准文号的单位方可生产新药。
药品批准文号名词解释

药品批准文号名词解释
药品批准文号是从中国食品药品监督管理总局发布的许可证,用以标
识某类特定产品(包括药品、保健食品、医疗器械、原料药、中药材、中
药饮片、中成药等)的批准文号,(简称“许可证”)。
药品批准文号由
由国家药品监督管理机构在审批通过后发放,是进行药品检验、药品登记
和药品上市的前提条件。
每一种药品的批准文号都有特定的规范,可以由它自身的特征来表示,例如,对西药来说:批准文号一般由山东省食品药品监督局负责发放,其
格式是“山药药字(2015)号”,其中号指批准文号,号包括字母和数字;对于中成药来说,其批准文号则由国家食品药品监督管理总局发放,其格
式是“国药准字H2014号”,其中号包括字母和数字。
药品批准文号是医药行业安全保障的重要证明,也是医疗健康和临床
诊断的重要依据,它是药品经国家药品监督管理机构审批批准后发放,用
以证明药品合法生产、经过安全检验、符合国家标准,并可持续供应市场的,能够有效识别和促进药品的统一管理、指导药品的使用、保护消费者
的权利。
简述药品批准文号的格式

简述药品批准文号的格式
药品批准文号的格式为:国药准字+1位字母+8位数字。
字母是指:H、Z、B、S、T、F、J,依次为:化学药品、中药、保健药品、生物制品、体外化
学诊断试剂、药用辅料、进口分包装药品。
数字是:第1、2位为原批准文
号的来源代码,第3、4位为换发批准文号之年公元年号的后两位数字,第
5至8位为顺序号。
此外,药品批准文号都带有其“药”字样,如“京卫药准字”或“京卫药健字”。
若批准文号以“京健食准字”或“京食准字”为开头,则此产品不属于药品。
请注意,药品批准文号的格式可能因地区和具体规定而有所不同,如有疑问可咨询专业人士或机构。
药品批准文号格式

药品批准文号格式02年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品,采用药品批准文号格式、药品批准文号格式:国药准字+1位字母+8位数字,试生产药品批准文号格式:国药试字+1位字母+字。
进口药品注册证格式:由字母H(Z或S)后接八位阿拉伯数字组成,前四位为公元年号,后四位为编号。
化学药品使用字母“H”,中药使用字母“Z”,通过国家药品监督管理局整顿的保健药品使用字母,生物制品使用字母“S”,体外化学诊断试剂使用字母“T”,药用辅料使用字母“F”,进口分包装药用字母“J”。
数字第1、2位为原批准文号的来源代码,其中“10”代表原卫生部批准的药品,“19”、”代表2002年1月1日以前国家药品监督管理局批准的药品,其它使用各省行政区划代码(见附件一)位的,为原各省级卫生行政部门批准的药品。
第3、4位为换发批准文号之年公元年号的后两位数字,但于卫生部和国家药品监督管理局的批准文号仍使用原文号年号的后两位数字。
数字第5至8位为顺序号。
、每种药品的每一规格发给一个批准文号。
除经国家药品监督管理局批准的药品委托生产和异地加工外药品不同生产企业发给不同的药品批准文号。
、自2002年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品采用新的药品批准文号格式。
、自2002年1月1日以后批准发给的化学药品《进口药品注册证》,其注册证号格式亦作部分改变,其母“X”改为“H”,其它部分不变。
原已发给的旧格式注册证号在换发《进口药品注册证》时用新格式取、药品批准文号及化学药品的进口药品注册证号换发后,印有原格式批准文号及注册证号的包装标签在年12月31日后禁止流通使用。
、药品批准文号采用的中华人民共和国行政区划代码代码省(自治区、直辖市)代码省(自治区、直辖市)11××××北京市42××××湖北省12××××天津市43××××湖南省13××××河北省44××××广东省14××××山西省45××××广西壮族自治区15××××内蒙古自治区46××××海南省21××××辽宁省50××××重庆市22××××吉林省51××××四川省23××××黑龙江省52××××贵州省31××××上海市53××××云南省32××××江苏省54××××西藏自治区33××××浙江省61××××陕西省34××××安徽省62××××甘肃省35××××福建省63××××青海省36××××江西省64××××宁夏回族自治区37××××山东省65××××新疆维吾尔自治区41×××河南省。
2024年药事管理与法规批准文号、色标、时间的总结范文(2篇)

2024年药事管理与法规批准文号、色标、时间的总结范文____年的药事管理与法规中,重要的是药品批准文号、药品色标和药品上市时间。
以下是根据这些方面总结的____字范文。
一、药品批准文号药品批准文号是药品上市时必须具备的标识,用于识别和跟踪药品。
每个药品都有唯一的批准文号,用于表示经过相关审批机构核准上市的药品。
____年,药事管理与法规对药品批准文号的发放和管理工作进一步规范。
在过去的几年里,药品批准文号的发放存在一些问题,如重复发放、乱码等。
因此,在____年,药事管理与法规加强了对药品批准文号的管理,确保每个批准文号的唯一性和准确性。
药事管理与法规还规定了药品批准文号的格式。
根据这些规定,药品批准文号由一串数字和字母组成,可以用于标识药品的各个属性,如药品种类、生产厂家、上市批准日期等。
这样,通过药品批准文号,可以快速准确地了解药品的相关信息。
药品批准文号的管理还涉及到各个环节,包括发放、核查、归档等。
在____年的药事管理与法规中,对这些环节进行了详细规定,以确保药品批准文号的有效管理和使用。
二、药品色标药品色标是一种标识药品的方法,通过不同颜色的标记,可以帮助人们快速识别和区分不同的药品。
药品色标在药品包装上用于表示药品的类型、用途、规格等。
____年的药事管理与法规对药品色标进行了进一步的规范。
在过去的几年里,药品色标的使用存在一些问题,如颜色选择不合理、标识含义不清等。
因此,在____年,药事管理与法规加强了对药品色标的管理,确保色标的准确和统一。
药事管理与法规规定了一套统一的药品色标标准。
根据这些标准,不同颜色的色标用于表示不同类型的药品,如红色表示处方药、黄色表示非处方药等。
这样,通过色标,可以快速准确地判断药品的属性和用途。
药品色标的管理还涉及到生产、包装和销售等环节。
在____年的药事管理与法规中,对这些环节进行了详细规定,以确保药品色标的有效管理和正确使用。
三、药品上市时间药品上市时间是药品正式进入市场销售的时间。
国家药品批准文号查询

国家药品批准文号查询药品批文是国家食品药品监督管理局(NMPA)对药品的审评和批准的证明文件,是药品合法上市的必要条件。
药品批文包括国产药品批准文号和进口药品注册证号,每个批文都有唯一的编号和有效期限。
那么,怎样查询中国药品批文呢?本文将介绍几种常用的查询方法。
一、通过NMPA(国家药品监督管理局)官网查询NMPA官网是国家药品信息查询平台,可以查询到所有在国内批准注册上市的药品,包括已注销或撤销的国产药品与进口药品。
在NMPA官网首页,点击“数据服务”-“数据查询”-“药物数据”,即可进入到“中国上市药物数据库”页面。
在该页面,可以通过以下方式进行检索:1. 智能搜索:在搜索框中输入关键词,如产品名称、商品名、生产企业等,即可显示相关结果。
2. 高级搜索:点击高级搜索按钮,可以选择更多的检索条件,如批准文号、剂型、规格、类别、批准日期等,并可以设置检索方式为模糊查询或精确查询。
3. 分类检索:点击分类检索按钮,可以按照不同的分类标准进行检索,如化学药、生物制品、中成药等。
检索结果包括以下信息:-国产药品:批准文号、原批准文号、产品名称、英文名称、商品名、生产厂家、生产地址、规格、剂型、类别、批准日期等。
-进口药品:注册证号、原注册证号、产品名称(中文)、产品名称(英文)、商品名(中文)、商品名(英文)、剂型(中文)、规格(中文)等。
二、通过药融云-中国药品批文数据库查询(含历史批文数据22万余条)药融云-中国药品批文数据库提供了国内上市药品的药品生产批准信息、药品治疗领域分类、医保药物信息、国家基本药物目录、国家非处方药目录、中药保护品种、药品所属公司信息等一系列相关属性信息查询服务。
并提供更多的查询功能和维度分析。
图片来源:药融云-中国药品批文数据库该数据库旨在帮助用户根据需求筛选出合适的目标产品,详尽地了解某一品种的基本属性及市场竞争态势,以及便于分析企业自身、竞争对手或目标企业的产品结构、产品独特性及产品竞争力,深刻了解医药研发及市场动向,是药企应用最为广泛的数据库之一。
批准文号

药品批准文号格式2002年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品,采用新的药品批准文号格式1、药品批准文号格式:国药准字+1位字母+8位数字,试生产药品批准文号格式:国药试字+1位字母+8位数字。
进口药品注册证格式:由字母H(Z或S)后接八位阿拉伯数字组成,前四位为公元年号,后四位为顺序编号。
化学药品使用字母“H”,中药使用字母“Z”,通过国家药品监督管理局整顿的保健药品使用字母“B”,生物制品使用字母“S”,体外化学诊断试剂使用字母“T”,药用辅料使用字母“F”,进口分包装药品使用字母“J”。
数字第1、2位为原批准文号的来源代码,其中“10”代表原卫生部批准的药品,“19”、“20”代表2002年1月1日以前国家药品监督管理局批准的药品,其它使用各省行政区划代码(见附件一)前两位的,为原各省级卫生行政部门批准的药品。
第3、4位为换发批准文号之年公元年号的后两位数字,但来源于卫生部和国家药品监督管理局的批准文号仍使用原文号年号的后两位数字。
数字第5至8位为顺序号。
2、每种药品的每一规格发给一个批准文号。
除经国家药品监督管理局批准的药品委托生产和异地加工外,同一药品不同生产企业发给不同的药品批准文号。
3、自2002年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品,一律采用新的药品批准文号格式。
4、自2002年1月1日以后批准发给的化学药品《进口药品注册证》,其注册证号格式亦作部分改变,其中字母“X”改为“H”,其它部分不变。
原已发给的旧格式注册证号在换发《进口药品注册证》时用新格式取代。
5、药品批准文号及化学药品的进口药品注册证号换发后,印有原格式批准文号及注册证号的包装标签在2003年12月31日后禁止流通使用。
6、药品批准文号采用的中华人民共和国行政区划代码例如,“国药准字H11020001”,字母和数字含义依次是:“H”为化学药品,“11”为北京市的行政区划代码前两位,“02”为换发之年2002年的后两位数字,“0001”为新的顺序号。
药品批准文号
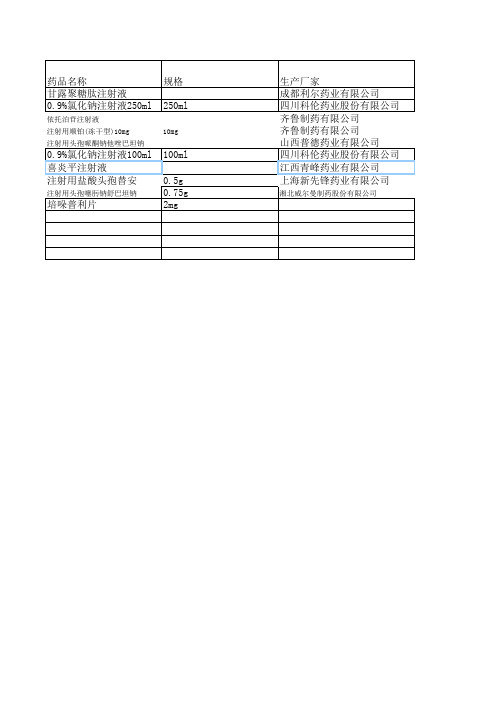
培哚普利片
批准文号 H20003633 H51021157
H37023183 H20023460 H20123099 H51021156
Z20026249 H20056344
H20103369
h20093504
药品名称 甘露聚糖肽注射液 0.9%氯化钠注射液250ml
依托泊苷注射液 注射用顺铂(冻干)10mg 注射用头孢哌酮钠他唑巴坦钠
规格 250ml
10mg
0.9%氯化钠注射液100ml 喜炎平注射液 注射用盐酸头孢替安
注射用头孢噻肟钠舒巴坦钠
100ml 0.5g 0.75g 2mg
生产厂家 成都利尔药业有限公司 四川科伦药业股份有限公司 齐鲁制药有限公司 齐鲁制药有限公司 山西普德药业有限公司 四川科伦药业股份有限公司 江西青峰药业有限公司 上海新先锋药业有限公司
新《药品注册管理办法》中关于药品批准文号的规定

新《药品注册管理办法》中关于药品批准文号的规定药品批准文号的格式第一百七十一条药品批准文号的格式为:国药准字h(z、s、j)+4位年号+4位顺序号,其中h代表化学药品,z 代表中药,s代表生物制品,j代表进口药品分包装.《进口药品注册证》证号的格式为:h(z、s)+4位年号+4位顺序号;《医药产品注册证》证号的格式为:h(z、s)c+4位年号+4位顺序号,其中h代表化学药品,z代表中药,s代表生物制品.对于境内分包装用大包装规格的注册证,其证号在原注册证号前加字母b.新药证书号的格式为:国药证字h(z、s)+4位年号+4位顺序号,其中h代表化学药品,z 代表中药,s代表生物制品.药品批准文号的有效期第一百二十条国家食品药品监督管理局核发的药品批准文号、《进口药品注册证》或者《医药产品注册证》的有效期为5年.有效期届满,需要继续生产或者进口的,申请人应当在有效期届满前6个月申请再注册.第一百二十一条在药品批准文号、《进口药品注册证》或者《医药产品注册证》有效期内,申请人应当对药品的安全性、有效性和质量控制情况,如监测期内的相关研究结果、不良反应的监测、生产控制和产品质量的均一性等进行系统评价.药品批准文号的发给第十九条对他人已获得中国专利权的药品,申请人可以在该药品专利期届满前2年内提出注册申请.国家食品药品监督管理局按照本办法予以审查,符合规定的,在专利期满后核发药品批准文号、《进口药品注册证》或者《医药产品注册证》.第二十五条单独申请注册药物制剂的,研究用原料药必须具有药品批准文号、《进口药品注册证》或者《医药产品注册证》,且必须通过合法的途径获得.研究用原料药不具有药品批准文号、《进口药品注册证》或者《医药产品注册证》的,必须经国家食品药品监督管理局批准.第二十九条申请人获得药品批准文号后,应当按照国家食品药品监督管理局批准的生产工艺生产.第六十五条国家食品药品监督管理局药品审评中心依据技术审评意见、样品生产现场检查报告和样品检验结果,形成综合意见,连同有关资料报送国家食品药品监督管理局.国家食品药品监督管理局依据综合意见,作出审批决定.符合规定的,发给新药证书,申请人已持有《药品生产许可证》并具备生产条件的,同时发给药品批准文号;不符合规定的,发给《审批意见通知件》,并说明理由.第八十一条国家食品药品监督管理局药品审评中心依据技术审评意见、样品生产现场检查报告和样品检验结果,形成综合意见,连同相关资料报送国家食品药品监督管理局,国家食品药品监督管理局依据综合意见,做出审批决定.符合规定的,发给药品批准文号或者《药物临床试验批件》;不符合规定的,发给《审批意见通知件》,并说明理由.第八十二条申请人完成临床试验后,应当向国家食品药品监督管理局药品审评中心报送临床试验资料.国家食品药品监督管理局依据技术意见,发给药品批准文号或者《审批意见通知件》.第一百条国家食品药品监督管理局对报送的资料进行审查,符合规定的,发给《药品补充申请批件》和药品批准文号;不符合规定的,发给《审批意见通知件》,并说明理由.药品批准文号的注销第一百六十九条具有下列情形之一的,由国家食品药品监督管理局注销药品批准文号,并予以公布:(一)批准证明文件的有效期未满,申请人自行提出注销药品批准文号的;(二)按照本办法第一百二十六条的规定不予再注册的;(三)《药品生产许可证》被依法吊销或者缴销的;(四)按照《》第四十二条和《药品管理法实施条例》第四十一条的规定,对不良反应大或者其他原因危害人体健康的药品,撤销批准证明文件的;(五)依法作出撤销药品批准证明文件的行政处罚决定的;(六)其他依法应当撤销或者撤回药品批准证明文件的情形.其它有关“批准文号”的条款第一百零二条进口分包装药品的说明书和标签必须与进口药品的说明书和标签一致,并且应当标注分包装药品的批准文号和分包装药品生产企业的名称.第一百零四条提供药品的境外制药厂商应当对分包装后药品的质量负责.分包装后的药品出现质量问题的,国家食品药品监督管理局可以撤销分包装药品的批准文号,必要时可以依照《药品管理法》第四十二条的规定,撤销该药品的《进口药品注册证》或者《医药产品注册证》.第一百七十五条实施批准文号管理的中药材、中药饮片以及进口中药材的注册管理规定,由国家食品药品监督管理局另行制定.[来源:][来源:][来源:][来源:][来源:][。
药品批准文号格式
药品批准文号格式关于统一换发并规范药品批准文号格式的通知国药监注[2002]33号各省、自治区、直辖市药品监督管理局,解放军总后卫生部:药品批准文号是药品生产合法性的标志。
《药品管理法》规定,生产药品“须经国务院药品监督管理部门批准,并发给药品批准文号”。
由于历史的原因,目前,已上市药品的批准文号的格式不尽相同,这种情况,不利于进行统一管理和监督。
为加强药品批准文号管理,根据国家药品监督管理局《关于做好统一换发药品批准文号工作的通知》(国药监注〔2001〕582号)要求,现又规范了新的药品批准文号格式,并将在近期对全国药品生产企业已合法生产的药品统一换发药品批准文号。
现将有关事项通知如下:一、药品批准文号格式:国药准字+1位字母+8位数字,试生产药品批准文号格式:国药试字+1位字母+8位数字。
化学药品使用字母“H”,中药使用字母“Z”,通过国家药品监督管理局整顿的保健药品使用字母“B”,生物制品使用字母“S”,体外化学诊断试剂使用字母“T”,药用辅料使用字母“F”,进口分包装药品使用字母“J”。
数字第1、2位为原批准文号的来源代码,其中“10”代表原卫生部批准的药品,“19”、“20”代表2002年1月1日以前国家药品监督管理局批准的药品,其它使用各省行政区划代码(见附件一)前两位的,为原各省级卫生行政部门批准的药品。
第3、4位为换发批准文号之年公元年号的后两位数字,但来源于卫生部和国家药品监督管理局的批准文号仍使用原文号年号的后两位数字。
数字第5至8位为顺序号。
有关批准文号的换发说明见附件二。
二、每种药品的每一规格发给一个批准文号。
除经国家药品监督管理局批准的药品委托生产和异地加工外,同一药品不同生产企业发给不同的药品批准文号。
三、自2002年1月1日以后批准生产的新药、仿制药品和通过地方标准整顿或再评价升为国家标准的药品,一律采用新的药品批准文号格式。
四、自2002年1月1日以后批准发给的化学药品《进口药品注册证》,其注册证号格式亦作部分改变,其中字母“X”改为“H”,其它部分不变。
2024年药事管理与法规批准文号、色标、时间的总结

2024年药事管理与法规批准文号、色标、时间的总结截至2024年,药事管理与法规在药品批准文号、色标和时间方面的总结如下:
1. 药品批准文号:药品批准文号是国家药品监督管理局颁发的唯一标识,用于标识批准上市的药品。
根据药事管理与法规,在2024年,药品批准文号的编码规则可能会有所变动,但一般会包含药品的分类、生产单位、批准日期等信息。
2. 药品色标:药品色标是指药品包装上所标识的颜色,用于快速区分不同类型的药品。
根据药事管理与法规,在2024年,药品色标的使用可能会有一定的调整。
一般来说,不同的药品类型会采用不同的色标,比如红色标识中药、绿色标识西药等。
3. 药品上市时间:药品的上市时间是指药品获得批准后开始在市场上销售的时间。
根据药事管理与法规,在2024年,药品上市时间可能会根据不同的情况有所差异。
一般来说,新药的上市时间会需要经过一系列的临床试验、审批等程序,而已上市的药品可能会有不同的更新或变更情况。
需要注意的是,药事管理与法规是根据相关国家法律法规和规章制度进行的,具体的批准文号、色标、时间等规定会随着法规的更新和调整而变化,因此以上总结仅供参考,具体以相关药事管理与法规的最新规定为准。
第 1 页共 1 页。
关于各种批文的说明

关于各种批文的说明一、药品:凭药品经营许可证经营范围及相关经营批件经营,经营范围在营业执照上登记。
一)国产药品批准文号格式:国药准字H(Z、B、j、S、F、T)+4位年数+4位顺序(例:国药准字Z20220023)其中Z:中药;B:保健药品;j:进口药品分包装;S:生物制品;F:药用辅料;H:化学药品;T:体外生物诊断试剂(药品类管理的体外诊断试剂)二)新药证书号批准文号格式:国药证字H(Z、S)+4位年号+4位顺序三)进口药品注册证批文格式:进口药品注册证号:H(Z、S)+4位年号+4位顺序;医药产品注册证号:H(Z、S)C+4位年号+4位顺序四)补充申请批件或补充批件:改变、增加或者取消原批准事项或者内容的,提出补充申请,审批部门同意后,发给补充申请批件,补充申请批件有效期与原注册批件(或再注册批件)有效期一致。
注:进口药品分包装,应当是药品GMP生产企业申请,发给药品批准证明文件。
药品类批文一般有效期为5年二、医疗器械:凭借二类备案凭证或三类许可证经营,一类不需要备案或许可,一、二、三类须在营业执照上登记。
一)二类、三类医疗器械注册证格式:其中审批部门所在地的简称:境内第三类医疗器械、进口第二类、第三类医疗器械为“国”字;境内第二类医疗器械为注册审批部门所在地省、自治区、直辖市简称;注册形式:“准”字适用于境内医疗器械;“进”字适用于进口医疗器械;“许”字适用于香港、澳门、台湾地区的医疗器械;(例:浙械注准20222400434)二)一类医疗器械备案凭证格式:一类医疗器械备案编排格式为:(备案部门所在地简称)+械备+4位年份+4位流水号。
其中:备案部门所在地简称:进口第一类医疗器械为“国”字;境内第一类医疗器械为备案部门所在地省、自治区、直辖市简称加所在地设区的市级行政区域的简称(无相应设区的市级行政区域时,仅为省、自治区、直辖市的简称);(例:浙杭械备20220324号)医疗器械注册证有效期一般为5年,2022年10以前的批文有效期一般为4年,一类备案凭证批文一般无有效期。
所谓“国药准字”是什么意思?

所谓“国药准字”是什么意思?关于统一换发并规范药品批准文号格式的通知国药监注〔2002〕33号 --------------------------------------------------------------------------------各省、自治区、直辖市药品监督管理局,解放军总后卫生部:药品批准文号是药品生产合法性的标志。
《药品管理法》规定,生产药品“须经国务院药品监督管理部门批准,并发给药品批准文号”。
由于历史的原因,目前,已上市药品的批准文号的格式不尽相同,这种情况,不利于进行统一管理和监督。
为加强药品批准文号管理,根据国家药品监督管理局《关于做好统一换发药品批准文号工作的通知》(国药监注〔2001〕582号)要求,现又规范了新的药品批准文号格式,并将在近期对全国药品生产企业已合法生产的药品统一换发药品批准文号。
现将有关事项通知如下:一、药品批准文号格式:国药准字+1位字母+8位数字,试生产药品批准文号格式:国药试字+1位字母+8位数字。
化学药品使用字母“H”,中药使用字母“Z”,通过国家药品监督管理局整顿的保健药品使用字母“B”,生物制品使用字母“S”,体外化学诊断试剂使用字母“T”,药用辅料使用字母“F”,进口分包装药品使用字母“J”。
数字第1、2位为原批准文号的来源代码,其中“10”代表原卫生部批准的药品,“19”、“20”代表2002年1月1日以前国家药品监督管理局批准的药品,其它使用各省行政区划代码(见附件一)前两位的,为原各省级卫生行政部门批准的药品。
第3、4位为换发批准文号之年公元年号的后两位数字,但来源于卫生部和国家药品监督管理局的批准文号仍使用原文号年号的后两位数字。
数字第5至8位为顺序号。
有关批准文号的换发说明见附件二。
二、每种药品的每一规格发给一个批准文号。
除经国家药品监督管理局批准的药品委托生产和异地加工外,同一药品不同生产企业发给不同的药品批准文号。
药品批准文号的注册要求 流程

药品批准文号的注册要求流程下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by theeditor. I hope that after you download them,they can help yousolve practical problems. The document can be customized andmodified after downloading,please adjust and use it according toactual needs, thank you!In addition, our shop provides you with various types ofpractical materials,such as educational essays, diaryappreciation,sentence excerpts,ancient poems,classic articles,topic composition,work summary,word parsing,copy excerpts,other materials and so on,want to know different data formats andwriting methods,please pay attention!药品批准文号是药品生产合法性的标志,是药品身份的证明,是识别真假药的重要依据。
怎样识别药品批准文号

1. 怎样识别药品批准文号?与我们生活密切相关的药品,其实也如同我们每个人一样,都是有一个身份证的,这就是药品的批准文号。
药品批准文号是药品生产企业依法生产药品的合法标志。
我们在买药时,要看清药品批准文号,无批准文号或批准文号标注有问题的药,千万不要购买和使用。
国家药品监督管理局于2001年对药品批准文号和试生产药品批准文号的表达格式作了规定,统一格式为“国药准(试)字+1位汉语拼音字母+8位阿拉伯数字”。
详解如下。
(1)“准”字代表国家批准正式生产的药品,“试”字代表国家批准试生产的药品。
(2)国药准(试)字后的1位汉语拼音字母代表药品类别,分别是H代表化学药品,S代表生物制品,J代表进口分装药品,T代表体外化学诊断试剂,F代表药用辅料,B代表保健药品,Z代表中药。
(3)汉语拼音字母后的8位阿拉伯数字中的第1、2位代表批准文号的来源,其中10代表原卫生部批准的药品,19、20代表国家食品药品监督管理局批准的药品,各省、自治区、直辖市的数字代码分别是11-北京市,12-天津市,13-河北省,14-山西省,15-内蒙古自治区,21-辽宁省,22-吉林省,23-黑龙江省,31-上海市,32-江苏省,33-浙江省,34-安徽省,35-福建省,36-江西省,37-山东省,41-河南省,42-湖北省,43-湖南省,44-广东省,45-广西壮族自治区,46-海南省,50-重庆市,51-四川省,52-贵州省,53-云南省,54-西藏自治区,61-陕西省,62-甘肃省,63-青海省,64-宁夏回族自治区,65-新疆维吾尔自治区。
8位阿拉伯数字中的第3、4位表示批准某药生产之公元年号的后两位数字,第5、6、7、8位数字(即最后四位数字)为顺序号。
例如:某药品的批准文号为国药准字H44021518,表明该药为化学药,原批准文号是广东省药品监督管理部门核发的,2002年统一换后的批准文号,该品种的顺序号为1518。
国药准字Z10890019,表明该药品为中药,原批准文号是卫生部于1989年核发的,顺序号为0019。
批准文号和执行标准

批准文号和执行标准
批准文号是指国家药品监督管理局核准上市的药品所获批准的编号,
这是药品质量的重要保证。
而执行标准是指用于检验药品质量、确保
其安全有效的标准。
这些标准一般由国家药品监督管理局发布,并依
据药品所属类别不同而设有不同的标准。
一般而言,一个药品获得批准之前,需要经过一系列的科研和临床试验,以确保其安全有效,并符合国家法规的规定。
而批准文号的颁布,则意味着该药品已经通过了全部的审核,已经可以正式上市销售。
药品的执行标准则是保证药品质量的重要手段。
这些标准可以包括药
品的物理学、化学和生物学特性,以及药品的产地、生产工艺等方面。
所有符合执行标准的药品,都可以保证其安全、有效,且其含量、成
分都符合药效学要求。
需要指出的是,批准文号和执行标准都是药品质量的重要保障。
对于
患者来说,购买药品时,需要仔细查看药品的批准文号和执行标准,
以确保购买到的药品符合国家监管要求。
同时,对于医生来说,也需
要根据执行标准选择合适的药品,以确保治疗的效果和安全性。
因此,考虑到人民群众的健康,保障药品质量是非常重要的任务。
总之,批准文号和执行标准是保障药品质量的重要措施。
在购买和使用药品时,应该仔细查看药品的批准文号和执行标准,以确保药品符合国家监管要求。
同时,有关部门也应加强监管,进一步提高药品质量。
这是保障人民群众健康的共同责任。
药品批准文号格式举例

药品批准文号格式举例
药品批准文号是指国家药品监督管理局对于药品进行审批后,颁发的唯一标识符号。
它是药品上市销售的必备条件之一,也是保证药品质量和安全性的重要手段之一。
药品批准文号格式举例如下:
1. 化学药品批准文号
化学药品批准文号通常由12位数字组成,其中前两位数字代表省份代码,接下来两位数字代表年份代码,再接下来两位数字代表该年度该省份的第几个申请,最后六位数字为顺序码。
例如:川西制20190001
2. 生物制品批准文号
生物制品批准文号通常由13位数字组成,其中前两位数字代表省份代码,接下来两位数字代表年份代码,再接下来三位数字代表该年度该省份的第几个申请,最后六位数字为顺序码。
例如:川西生201900001
3. 中成药批准文号
中成药批准文号通常由10位字符组成,其中前四个字符为汉字名称缩写(如“桂枝汤”缩写为“GZT”),接下来四个字符为阿拉伯数字
表示的年份和序号,最后两个字符表示该批文号的版本。
例如:GZT2018-01-V1
4. 中药材批准文号
中药材批准文号通常由13位数字组成,其中前两位数字代表省份代码,接下来两位数字代表年份代码,再接下来三位数字代表该年度该省份
的第几个申请,最后六位数字为顺序码。
例如:川西草201900001
总之,药品批准文号格式是根据不同类型的药品而定的,但都遵循一
定的规律和标准。
了解并正确使用药品批准文号对于保障患者用药安全、保证医疗质量具有重要意义。
2023年药事管理与法规批准文号、色标、时间的总结范文

2023年药事管理与法规批准文号、色标、时间的总结范文药事管理与法规对于药品的批准文号、色标以及时间要求是非常重要的。
以下是对于2023年药事管理与法规批准文号、色标、时间的总结范文。
一、批准文号药品的批准文号是国家药品管理部门颁发的唯一标识符号,用于标识药物产品的批准许可。
根据2023年药事管理与法规的要求,批准文号的编制应符合以下规定:1. 批准文号的格式和构成:批准文号应由一定的编码规则构成,通常由字母和数字组成,以便于识别和查询。
在文号的编制中,可以根据药品的类别、用途、剂型等因素进行细分,以便于对药品进行分类管理。
2. 批准文号的颁发和管理:批准文号的颁发应由国家药品管理部门负责,严格按照法律法规和相关规定进行操作。
同时,对于已经获得批准文号的药品,应加强管理和监督,确保药品的质量和安全性。
3. 批准文号的有效期和更新:批准文号应有一定的有效期限,待过期需及时进行更新,以确保药品的信息准确和时效性。
在更新批准文号时,应进行全面的评估和审核,确保药品的适用性和安全性。
二、色标药品的色标是指药物包装上的颜色标识,用于区分药品的性质、用途、剂型等。
根据2023年药事管理与法规的要求,色标的设置应符合以下规定:1. 色标的种类和用途:色标应根据药品的类别和功能进行设置,可以分为不同的颜色和形状,以便于消费者或医务人员识别和使用。
比如,可以使用红色表示处方药,蓝色表示非处方药等。
2. 色标的标识和标示:色标应在药品包装上明确标识和标示,以便于识别和辨认。
同时,应确保色标的清晰度和稳定性,防止色标因长时间暴露于光线或变质导致无法识别。
3. 色标的管理和监督:色标的管理应由国家药品管理部门负责,对于已经设置的色标药品,应进行日常监督和抽检,确保色标的正确性和一致性。
三、时间要求药事管理与法规对于药品的时间要求主要包括以下几个方面:1. 批准时间:药品的审核和批准应在一定的时间内完成,以确保药品能够及时上市和供应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
批准文号什么是药品的批准文号?一共有多少种?
《中华人民共和国药品管理法》规定,生产药品须经国家药品监督管理部门批准,并发给药品批准文号方可生产,未经批准生产的药品以假药论处。
因此,药品批准文号是指药品生产企业在生产药品前报请国家药品监督管理部门批准后获得的身份证明,是依法生产药品的合法标志。
怎样识别药品批准文号呢?国家药品监督管理局于2001年对药品批准文号和试生产药品批准文号的表达格式作了规定,统一格式为“国药准(试)字+1位汉语拼音字母+8位阿拉伯数字”。
其中(1)“准”字代表国家批准正式生产的药品,“试”字代表国家批准试生产的药品。
(2)国药准(试)字后的1位汉语拼音字母代表药品类别,分别是H代表化学药品,S代表生物制品,J代表进口分装药品,T代表体外化学诊断试剂,F代表药用辅料,B代表保健药品,Z 代表中药。
(3)汉语拼音字母后的8位阿拉伯数字中的第1、2位代表批准文号的来源,其中10代表原卫生部批准的药品,19、20
代表国家食品药品监督管理局批准的药品,各省、自治区、直辖市的数字代码分别是11-北京市,12-天津市,13-河北省,14-山西省,15-内蒙古自治区,
第 1 页共3 页
21-辽宁省,22-吉林省,23-黑龙江省,31-上海市,32-江苏省,33-浙江省,34-安徽省,35-福建省,36-江西省,37-山东省,41-河南省,42-湖北省,43-湖南省,44-广东省,45-广西壮族自治区,46-海南省,50-重庆市,51-四川省,52-贵州省,53-云南省,54-西藏自治区,61-陕西省,62-甘肃省,63-青海省,64-宁夏回族自治区,65-新疆维吾尔自治区。
8位阿拉伯数字中的第3、4位表示批准某药生产之公元年号的后两位数字,第5、6、7、8位数字(即最后四位数字)为顺序号。
了解药品批准文号统一格式识别方法后,让我们一起来识别几种常用药品,如(1)广谱喹诺酮类抗菌药可乐必妥(左氧氟沙星)片的批准文号为国药准字H20000655,表明该药是化学药品,系国家药品监督管理局于2000年批准生产的,顺序号为0655。
(2)治疗腹泻的培菲康胶囊的批准文号是国药准字S1*******,表明该药为生物制品,是原卫生部于1995年批准生产的,顺序号为0032。
(3)抗血小板聚集药物波立维(硫酸氯吡格雷)片的批准文号为国药准字J20040006,表明该药系进口分装药品,国家食品药品监督管理局于2004年批准生产,顺序号为0006。
(4)用于跌打损伤的云南白药胶囊的批准文号是国药准字Z53020799,表明该药是中药,云南省药品监督管理部门于2002年批准生产,顺序号0799。
掌握了药品批准文号统一格式的识别方法,就能很快判断药品的一些基本情况,有助于对药品真伪或是否合法进行判别,保障用药安全。
人们在买药时,要看清药品批准文号,无批准文号或批准文号标注有问题的药,千万不要购买和使用。
批准文号有效期:
1、2002年全国统一换发药品批准文号,目前药品已经没有地方文号了(如苏卫药准字、沪卫药准字),全部是国药准字的了。
2、药品管理法实施条例、药品注册管理办法等法规规定,药品批准文号的有效期为5年,这是在借鉴国外经验的同时结合国情而定的,不仅药品批准文号的效期是5年,其他如GMP证书、生产许可证、进口药品注册证、医药产品注册证等效期均为5年,同时制定的效期是一致的目的至少是便于监督管理。
在近效期满6个月前需重新申请办理(换证、复认证、再注册等),也可以称之为续展。
3、在监督管理时,药监局可以让其提供注册证(注册证背面有变更、再注册记录)核查,也可以到国家局网站的数据库查询其有效性。
同时个人认为,药监局作为执法者,也要了解掌握国家及地方政府制定的相关药品管理法规。
