L-色氨酸
L-色氨酸-营养强化剂
L-色氨酸
通用名称:L-色氨酸L-Tryptophan
功能分类:营养强化剂
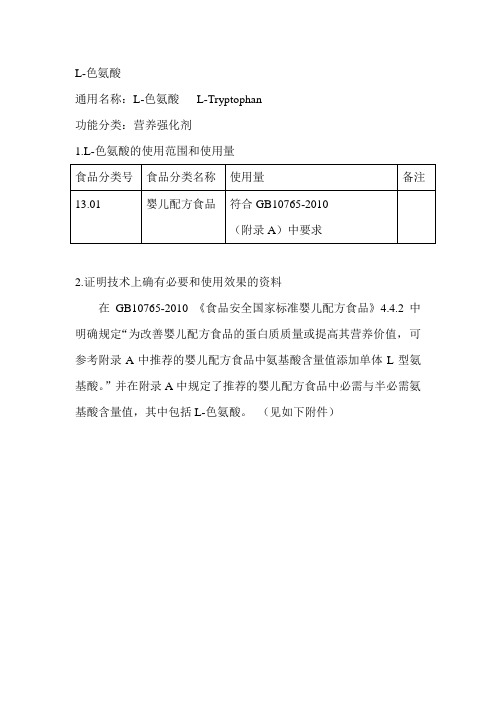
1.L-色氨酸的使用范围和使用量
2.证明技术上确有必要和使用效果的资料
在GB10765-2010 《食品安全国家标准婴儿配方食品》4.4.2中明确规定“为改善婴儿配方食品的蛋白质质量或提高其营养价值,可参考附录A中推荐的婴儿配方食品中氨基酸含量值添加单体L型氨基酸。
”并在附录A中规定了推荐的婴儿配方食品中必需与半必需氨基酸含量值,其中包括L-色氨酸。
(见如下附件)
另外,L-色氨酸在婴儿配方食品中的使用在国内及国外都有相关的法规依据,详细情况见下表:
我公司对添加了L-色氨酸的婴儿配方食品与母乳喂养进行了临床试验对比,试验结果表明120天喂养添加了L-色氨酸的婴儿配方食品的婴儿体重对年龄及体重对身长的Z比分值与母乳喂养婴儿接近。
3.生产工艺和检验方法、食品中L-色氨酸检验方法
3.1生产工艺
以谷氨酸棒状杆菌发酵水解制得。
3.2检验方法
目前L-色氨酸及婴儿配方食品中L-色氨酸的测定没有国标检测方法,使用惠氏营养品公司内部检测方法检测。
4.技术要求
4.1质量规格
1 2 3 4 5 6。
发酵液中L-色氨酸的提取纯化实验指导书
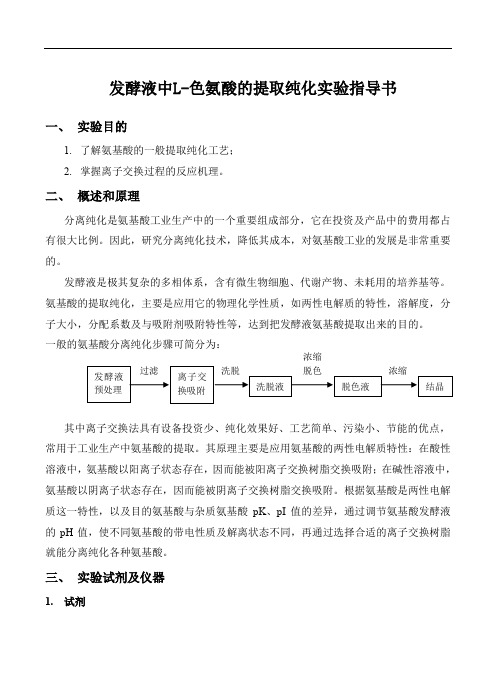
发酵液中L-色氨酸的提取纯化实验指导书一、实验目的1.了解氨基酸的一般提取纯化工艺;2.掌握离子交换过程的反应机理。
二、概述和原理分离纯化是氨基酸工业生产中的一个重要组成部分,它在投资及产品中的费用都占有很大比例。
因此,研究分离纯化技术,降低其成本,对氨基酸工业的发展是非常重要的。
发酵液是极其复杂的多相体系,含有微生物细胞、代谢产物、未耗用的培养基等。
氨基酸的提取纯化,主要是应用它的物理化学性质,如两性电解质的特性,溶解度,分子大小,分配系数及与吸附剂吸附特性等,达到把发酵液氨基酸提取出来的目的。
一般的氨基酸分离纯化步骤可简分为:浓缩其中离子交换法具有设备投资少、纯化效果好、工艺简单、污染小、节能的优点,常用于工业生产中氨基酸的提取。
其原理主要是应用氨基酸的两性电解质特性:在酸性溶液中,氨基酸以阳离子状态存在,因而能被阳离子交换树脂交换吸附;在碱性溶液中,氨基酸以阴离子状态存在,因而能被阴离子交换树脂交换吸附。
根据氨基酸是两性电解质这一特性,以及目的氨基酸与杂质氨基酸pK、pI值的差异,通过调节氨基酸发酵液的pH值,使不同氨基酸的带电性质及解离状态不同,再通过选择合适的离子交换树脂就能分离纯化各种氨基酸。
三、实验试剂及仪器1.试剂L-色氨酸发酵液(由实验一提供);浓硫酸(AR 95.5%);盐酸;氢氧化钠;氨水;冰醋酸;001×7型阳离子交换树脂。
2.仪器离子交换柱,离心机,控温磁力搅拌器,旋转蒸发仪,蠕动泵、真空干燥箱。
四、实验操作步骤1.树脂预处理及装柱先用蒸馏水冲洗001×7型阳离子交换树脂除去杂质,然后用2 mol/L的HCl和NaOH 溶液反复浸泡3次后,再用2 mol/L的HCl转成H+型,最后用去离子水洗至中性备用;离子交换柱用去离子水冲洗干净后,在柱中先装入半柱水,然后将树脂和水一起倒入柱中,让树脂自然沉降。
装柱时应注意柱中的水不能低于树脂界面,否则,树脂间形成气泡,影响交换效率。
色氨酸总结

色氨酸一、产品名称2010018055中文名:色氨酸英文名:tryptophan;tryptophane;简写为Trp二、产品性质:白色或微黄色结晶或结晶性粉末;无臭,味微苦。
熔点281~282℃(右旋体),289℃分解,左旋体。
外消旋体微溶于水(0.4%,25℃)和乙醇,溶于甲酸、稀酸和稀碱,不溶于氯仿和乙醚。
0.2%的水溶液pH 为5.5~7.0。
三、产品用途及作用:L-色氨酸是含有吲哚基的中性芳香族氨基酸,是人体和动物生命活动中必需的氨基酸之一,对人和动物的生长发育、新陈代谢起着重要的作用,被称为第二必需氨基酸,广泛应用于医药、食品和饲料等方面。
在生物体内,从色氨酸出发可合成5-羟基色胺等激素以及色素、生物碱、辅酶、植物激素等生理活性物质,可预防和治疗糙皮病,同时具有消除精神紧张、改善睡眠效果等功效。
色氨酸代谢失凋会引起糖尿病和神经错乱,因此在医学上被用作氨基酸注射液和复合氨基酸制剂。
另外,由于色氨酸是一些植物蛋白中比较缺乏的氨基酸,用它强化食品和做饲料添加剂对提高植物蛋白质的利用率具有重要的作用,它是继蛋氨酸和赖氨酸之后的第三大饲料添加氨基酸。
四、主要产品生产厂家、产品概况及产量:世界上主要生产厂家是日本的昭和电工、协和发酵和三井化学公司,采用发酵法生产色氨酸,赢创德固赛则兼有发酵法和合成法生产色氨酸。
国内具备色氨酸生产能力的企业主要有杭州恒锐生物制品有限公司和浙江东阳市横店集团家园化工有限公司。
杭州恒锐建立于2001年,目前产品有D-色氨酸、DL-色氨酸、L-色氨酸,每月产量均在1吨左右,年产值上千万元。
家园化工研制生产的L-色氨酸被科技部列入2003年度国家重点新产品计划。
该公司与有关科研院所合作,利用基因工程酶法合成生产高纯度L-色氨酸,目前已有商业化产品销售。
另外,上海、武汉、北京等地小规模少量生产气氨酸,用于药品。
但尚无厂家生产饲料添加剂用的色氨酸。
目前该产品生产技术和市场被日本三井化学、美国ADM等几家国际大公司垄断,我国每年要大量进口L-色氨酸,以满足市场所需。
色氨酸 酪氨酸 苯丙氨酸 性质

色氨酸结构式:学名:2-氨基-3-吲哚基丙酸,一种芳香族、杂环、非极性a氨基酸。
L-色氨酸是组成蛋白质的常见20种氨基酸中的一种,是哺乳动物的必需氨基酸和生糖氨基酸。
在自然界中,某些抗生素中有D-色氨酸。
符号:W性能:本品为白色或微黄色结晶或结晶性粉末,无臭,味微苦,密度:1.362g/cm3。
熔点281~282°C (右旋体),289°C分解,左旋体。
外消旋体微溶于水(0.4% , 25C)和乙醇,溶于甲酸、稀酸和稀碱,不溶于氯仿和乙醚。
0.2%的水溶液pH为5.5~7.0。
酪氨酸结构式:学名:2-氨基-3-对羟苯基丙酸,一种含有酚羟基的芳香族极性a 氨基酸,L-酪氨酸是组成蛋白质的20种氨基酸中的一种,是哺乳动物的必需氨基酸,又是生酮和生糖氨基酸。
符号:Y 性能:分子式:C9H11NO3,摩尔质量181.20g/mol,密度1.456g/cm3酪氨酸是一种白色结晶体或结晶粉末,无臭,无味,在水中极微溶解,在无水乙醇、甲醇或丙酮中不溶,易溶于甲酸, 在稀盐酸或稀硝酸中溶解。
【熔点】l:342 〜344 (分解);d:310 〜314(分解);dl:340 (分解)【性状】l-体从水中结晶出来者,无色至白色丝光针状结晶或结晶性粉末;d-体从水中结晶者为无色晶体;dl-体从水中结晶者为有光泽的针状晶体。
为动物体内非必需氨基酸!结构式:H学名:2-氨基-3-苯基丙酸,一种芳香族的非极性的a氨基酸,L-苯丙氨酸是组成蛋白质的20种氨基酸中的一种氨基酸,是哺乳动物的必需氨基酸和生酮生糖氨基酸。
符号:F性能:分子式C9H11NO2摩尔质量165.19 g/mol熔点283 °C沸点295 C密度 1.290g/cm3是a-氨基酸的一种,具有生物活性的光学异构体为L-苯丙氨酸,常温下为白色结晶或结晶性粉末固体,减压升华,溶于水,难溶于甲醇、乙醇、乙醚。
PBS:PBS在医学词汇中表示磷酸盐缓冲液,用于分子克隆及细胞培养,pH=7.4,与人体血液等渗,主要成分为磷酸二氢钾、磷酸氢二钠、氯化钠以及氯化钾。
重组大肠杆菌产 L-色氨酸的补料-分批发酵 实验指导书

重组大肠杆菌产 L-色氨酸的补料-分批发酵实验指导书一、实验目的1.通过对L-色氨酸的发酵,了解L-色氨酸的补料-分批发酵的基本过程;2.初步掌握微生物发酵的基本操作。
二、概述和原理L-色氨酸(L-Trp)是含有吲哚的中性芳香族氨基酸,是人和动物生命活动中不可缺少的必需氨基酸之一。
L-色氨酸不仅在营养代谢中起重要作用,而且还广泛应用于医药、食品、饲料等方面,随着市场需求量的日益增加,L-色氨酸具有广阔的应用前景。
早期的 L-色氨酸的生产方法主要依靠化学合成法和蛋白质水解法,但是由于这些方法存在着材料来源有限、周期长、工艺复杂、产品成分复杂等缺点,因而在上世纪 90年代逐渐被淘汰,随着对微生物法生产 L-色氨酸研究的不断深入,微生物法已经走向实用并且处于主导地位,微生物发酵法具有产酸高、成本低、质量好等优势,将是未来大规模生产 L-色氨酸的首选技术。
该法主要是以葡萄糖、甘蔗糖蜜等廉价原料为碳源,利用优良的 L-色氨酸生产菌种来生产 L-色氨酸。
补料-分批发酵,是指在分批培养过程中,间歇或连续地补加新鲜培养成分的一种发酵方法,现已经广泛应用于发酵工业。
流加操作的主要特点就是能够调节微生物生长反应环境中营养物质的浓度,可以避免营养成分的初始浓度过高而出现的底物抑制现象,同时也能阻止某些限制性营养成分由于在反应过程中被耗尽而影响微生物的生长和产物的形成。
在发酵生产 L-色氨酸过程中,菌体主要以葡萄糖为碳源,由于在高浓度的葡萄糖条件下,大肠杆菌容易产生乙酸,而当发酵液中乙酸浓度积累到 2 g/L时,菌体将停止生长并且抑制外源基因的表达。
因此本实验需采用补料-分批发酵的方式。
补料培养基加入形式可以分为非反馈补料和反馈补料,非反馈补料主要包括恒速补料、指数补料、逐级提速流加等几种流加形式,而反馈补料根据所选反馈指标的不同可分为恒 pH值法、恒溶解氧法、菌体浓度反馈、CER法、DO-stat法等几种补料方法。
反馈补料由于能够根据反馈的信息及时调整补料的速率和策略,从而能够很好地控制系统的营养浓度,防止营养浓度过高,故在大肠杆菌培养中常被广泛采用。
l-色氨酸_企业标准_解释说明

l-色氨酸企业标准解释说明1. 引言1.1 概述引言部分旨在介绍本篇长文的主题——l-色氨酸企业标准,并提供一个概括性的背景说明。
随着社会发展和人们对健康的关注程度不断提升,食品、药品、保健品等行业中对于产品质量和安全的要求也越来越高。
其中,l-色氨酸作为一种重要的营养添加剂,广泛应用于各个领域。
然而,随着l-色氨酸需求的增加,其质量控制与标准化也变得尤为重要。
1.2 文章结构本文将按照以下目录进行阐述:大纲中包含了引言、l-色氨酸的定义、企业标准与l-色氨酸相关性分析、实际案例分析以及结论等五个部分。
通过这样清晰明了的文章结构,读者可以逐步了解到l-色氨酸企业标准的定义、特点、作用与功能,并深入理解企业标准与l-色氨酸之间的关系以及其对质量控制和管理方面所要求的内容。
同时,我们将具体分析一个实际案例,阐述了企业标准下l-色氨酸的品质保障措施。
1.3 目的本篇长文旨在分析解释l-色氨酸企业标准的定义、作用和功能,并深入探讨企业标准与l-色氨酸之间的相关性。
通过对现有企业标准的分析,还将向读者介绍一个实际案例,展示该企业如何在生产过程中采取控制措施来确保产品质量和安全性。
最后,在结论部分将总结l-色氨酸企业标准的重要性,并提供一些关于未来发展该企业标准的思考。
通过本篇文章,希望读者可以更加了解并认识到l-色氨酸企业标准对于产品质量管理和行业发展的重要意义。
2. l-色氨酸的定义2.1 色氨酸介绍色氨酸是一种重要的氨基酸,属于人体必需氨基酸的一种。
它在人体内不能被合成而需要从外部摄入,常见于蛋白质含量较高的食物中,如肉类、奶制品、豆类和谷物等。
色氨酸在人体内可以通过蛋白水解产生,然后经过转化合成为l-色氨酸。
2.2 l-色氨酸特点l-色氨酸是对可溶于水的结晶性粉末,具有一定的疏水性。
它主要存在于动植物细胞中,并且是生命活动中重要的组成部分之一。
l-色氨酸与d-色氨酸相比,在空间构型上有所不同,其中l-色氨酸为左旋构型。
L-色氨酸的性质介绍

品名:L-色氨酸
中文别名:L-2-氨基-3-吲哚基丙酸;(+/-)-2-氨基-3-(3-吲哚基)丙酸;L-2-氨基-3-吲哚基-1-丙酸;L-氨基吲哚丙酸;L-色氨基酸;L-胰化蛋白氨基酸;L-2-氨基-3-吲哚基-丙酸;L-色胺酸
英文名称:L-Tryptophan
CAS: 73-22-3
分子式:C11H12N2O2
性质:L-色氨酸为白色至黄白色晶体或结晶性粉末。
L-色氨酸无臭或微臭,稍有苦味。
熔点289℃,长时间光照则着色。
与水共热产生少量吲哚。
略溶于(1.1g/100ml,25℃)。
L-色氨酸可做营养增补剂;抗氧化剂。
色氨酸是人体重要的神经递质5-羟色胺-的前体,是人体的必需氨基酸之一
L-色氨酸促进动物的采食、削弱应激反应、改善动物睡眠,还可以增加胎儿和幼仔的抗体、提高乳畜泌乳。
L-色氨酸降低日粮优质蛋白用量,节约饲料成本,降低日粮蛋白饲料用量,节约配方空间等。
安泰生物科技有限公司是以销售食品添加剂为主的公司,从事多种食品添加剂产品的销售。
主要产品有:花生四烯酸,甘氨酸钙,花生蛋白粉,亚麻籽油微囊粉,大豆异黄酮,氨基葡萄糖,鱼胶原蛋白肽,辅酶Q10,海藻酸钠,海藻糖,酪蛋白,叶黄素,乳酸亚铁,山梨酸钾,D-甘露糖醇等。
公司坚持"质量为本,科技创新"的宗旨,从原料采购、工艺操作到品质检验,都严格遵守国际质量标准进行管理,竭诚服务于广大新老客户。
L-色氨酸含量和纯度的测定实验指导书

L-色氨酸含量和纯度的测定 实验指导书一、实验目的1.了解对二甲氨基苯甲醛与L-色氨酸的反应机理;2.了解高效液相色谱分析的基本原理;3.掌握L-色氨酸的测定方法。
二、概述和原理L-色氨酸的分析方法主要有氨基酸自动分析仪分析法、高效液相色谱分析法、毛细管电泳法、薄层色谱法和分光光度法等。
本实验主要采用分光光度法进行L-色氨酸含量测定。
分光光度法测定L-色氨酸的基本原理为:在硫酸溶液中,L-色氨酸与对二甲氨基苯甲醛发生缩合反应,生成的希夫碱对二甲氨基苯甲醛缩色氨酸为蓝色,颜色深度在一定范围内与L-色氨酸含量成线性关系,可在分光光度计下定量测定。
高效液相色谱是色谱法的一个重要分支,其系统主要由储液器、泵、进样器、色谱柱、检测器、记录仪等几部分组成,由于该法具有高效、快速和灵敏等特点,不仅可用于L-色氨酸含量的测定,还可用于纯度的测定。
其工作原理为:储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱(固定相)内,由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中作相对运动时,经过反复多次的吸附-解吸的分配过程,各组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器时,样品浓度被转换成电信号传送到记录仪,数据以图谱形式打印出来。
三、实验试剂及仪器1.试剂浓硫酸;对二甲氨基苯甲醛;亚硝酸钠;L-色氨酸标准品;磷酸二氢钾;冰醋酸;甲醇(液相纯);纯净水;乙腈(液相纯)。
2.仪器紫外可见分光光度计,Agilent 1200 Series高效液相色谱仪。
四、发酵液中L-色氨酸含量的测定1.对二甲氨基苯甲醛溶液(3 g/L)制备准确称取0.3 g对二甲氨基苯甲醛,溶于100 mL 1:1浓硫酸中。
2.亚硝酸钠溶液(2%)制备准确称取亚硝酸钠0.2 g于10 mL容量瓶中,以蒸馏水定容,新鲜配制。
3.L-色氨酸标准储备液(100 mg/L)制备准确称取25 mg L-色氨酸标准品,用纯水定容于250 mL棕色容量瓶中,制得浓度为100 mg/L的L-色氨酸标准储备液,于4 ℃冰箱保存备用。
色氨酸工艺流程设计及技术要点

色氨酸工艺流程设计、技术要点及工艺参数前言L-色氨酸是人体和动物生命活动中八种必需氨基酸之一,对人和动物的生长、发育和新陈代谢起着重要作用。
近年来,随着色氨酸在医药、食品和饲料等方面应用的开拓,市场需求量不断增加,色氨酸已成为一种国际市场上发展前景良好,国内市场需求较大的产品,目前生产量远不能满足市场需求。
提高色氨酸发酵产率、降低生产成本、实现工业化生产,已成为目前一个重要课题。
L-色氨酸是人和动物的必需氨基酸,参与机体蛋白质合成和代谢网络调节,广泛存在于自然界。
D-色氨酸则主要存在于微生物和绿色植物中,动物体内含量较少。
D-色氨酸在人体内几乎不发生作用,也无毒性。
L-色氨酸是继蛋氨酸、赖氨酸的3~4倍,具有十分广泛的应用前景,近年来在医药、化妆、食品、保健品等行业也得到广泛的应用。
色氨酸分子式为C11H12N2O2,分子量为204.23,等电点为5.89。
化学名称为α-2氨基2-β-2吲哚丙酸,有L型和D 型同分异构体,此外还有消旋体DL-色氨酸。
本品为L-2-氨基-3(β-吲哚)丙酸。
本品为白色或微黄色结晶或结晶性粉末;无臭,味微苦。
在水中微溶,在乙醇中极微溶解,在氯仿中不溶,在甲酸中易溶,在氢氧化钠试液或稀盐酸中溶解。
比旋度:取本品,精密称定,加水溶解并稀释成每1ml中约含10mg的溶液,依法测定比旋度为-29.0°至-32.8°。
编写《色氨酸生产工艺操作指导书》的目的是为了使生产操作工更好的了解本岗位工艺特性、实际操作方法及理论知识,提高工人技术操作水平,是提高企业产品质量的基础,也是企业能否进一步扩大经济效益的关键;为树立自身良好的操作规范,提高操作水平,提供指导工具,从而不断提高产品质量,提升梅花产品市场竞争力。
目录第一章色氨酸发酵 (1)一、连消岗位 (2)二、二级岗位 (5)三、发酵岗位 (9)第二章色氨酸提取 (14)一、膜过滤岗位 (15)二、离交岗位 (17)三、脱氨岗位 (18)四、板框脱色岗位 (20)五、四效浓缩岗位 (22)六、单效蒸发结晶岗位 (23)七、板框分离岗位 (25)八、烘干、包装岗位 (28)第一章色氨酸发酵发酵工艺流程图一、连消岗位1、主要任务领取发酵二级种子、流加糖、设备设施消毒所需的原辅材料、消泡剂和消毒药品等;根据生产工艺参数规定,准确计量,并按程序配制发酵、二级种子及流加糖培养基;与二楼和三楼人员配合,做好连消设备、管线的空消工作,并负责与主控室人员配合通过自控系统对发酵、二级种子培养基及流加糖的连续灭菌;把好设备、原辅材料和工艺参数控制关,为发酵提供优质无菌的培养基;对空气预处理系统排水,并按工艺参数控制风温;做好各项基础工作,按清洁生产要求,及时对储糖罐、配料罐、维持罐、换热器以及其它设备设施进行清洁生产工作,保证高效、安全、文明生产。
液相分离l-色氨酸和d

液相分离l-色氨酸和d
液相色谱法是一种常用的分离和分析方法,可以用于分离和检测不同的物质。
L-色氨酸和D-色氨酸是两种光学异构体,它们的化学结构相似,但在空间构型上有所不同。
D-色氨酸是L-色氨酸的镜像,因此在生理活性、吸收和代谢方面存在差异。
液相色谱法可以用于分离L-色氨酸和D-色氨酸,主要采用手性固定相拆分法。
这种方法利用手性固定相与流动相的相互作用,使L-色氨酸和D-色氨酸在固定相上的吸附和洗脱速度不同,从而实现分离。
在分离过程中,可以通过调整流动相的组成和流速等参数来优化分离效果。
除了手性固定相拆分法外,还可以采用其他液相色谱技术来分离L-色氨酸和D-色氨酸。
例如,可以采用离子交换色谱法或疏水相互作用色谱法等。
这些方法利用不同的相互作用力来分离L-色氨酸和D-色氨酸,也可以通过调整实验条件来优化分离效果。
在液相色谱分离L-色氨酸和D-色氨酸时,需要注意以下几点:
1. 选用适合的固定相和流动相:根据L-色氨酸和D-色氨酸的性质,选用适合的固定相和流动相,以提高分离效果。
2. 控制实验条件:在分离过程中,需要控制好温度、流速和进样量等实验条件,以保证分离的准确性和稳定性。
3. 进行方法验证:在分离前需要对方法进行验证,以确保方法的可行性和可靠性。
这包括对方法的精密度、准确度、特异性、耐用性和线性范围等进行评估。
4. 注意安全问题:由于L-色氨酸和D-色氨酸具有一定的毒性,因此在分离过程中需要注意安全问题。
建议在专业人员的指导下进行实验操作,并遵循相关的安全规定。
大肠杆菌发酵生产l-色氨酸的研究

大肠杆菌发酵生产l-色氨酸的研究
l-色氨酸是一种重要的有机化合物,具有大量应用价值,即可作为兽药制剂剂型的基础,也可做为磷脂酰肌醇单元来承载细胞激素,同时具有重要的生物有效性,可作为肌肉组织保护剂、抗骨质流失剂等。
为了解决医药工业需求的增长,有效开发生产l-色氨酸的技术方案是迫在眉睫的问题。
近年来,研究人员借助大肠杆菌发酵的方式对l-色氨酸的生产进行了探索。
其中,利用菌株工程技术向大肠杆菌中植入表达l-色氨酸的基因是实现大肠杆菌发酵生产l-色氨酸的关键技术。
另外,研究者们在工艺参数方面也做出了努力,如尝试各种发酵梯度、进步多步次发酵等,以期最大化发酵效率。
此外,加入多种培养液补充剂也非常有助于加速发酵过程,如糖和氨基酸等。
同时,根据电子隐形色谱的结果确定l-色氨酸的产出也是生产过程的关键。
因为一般来说,l-色氨酸产出低于其他相关产物,所以研究者们需要合理操作、改进发酵参数来提高l-色氨酸的产出率。
总之,大肠杆菌发酵生产l-色氨酸是充分考虑发酵参数、改进工艺方案以及利用现有技术,从而实现可持续、可控、高效的新型发酵技术。
只有把这些元素完美结合起来,才能使大肠杆菌发酵生产l-色氨酸的研究取得实效。
l-色氨酸熔点

l-色氨酸熔点
l-色氨酸是一种氨基酸,其熔点约为228-230℃。
这个温度范围可以在常压下进行熔化,但是在高温下可能会发生分解。
l-色氨酸是一种具有重要生理功能的氨基酸,它在蛋白质合成、代谢调节、神经传递等方面都扮演着重要的角色。
因此,l-色氨酸的熔点也具有重要的研究价值。
l-色氨酸的熔点受多种因素的影响,包括纯度、晶体结构、溶剂、温度等。
在实验室中,可以通过差示扫描量热法、动态热机械分析仪等仪器对l-色氨酸的熔点进行测量。
在实际应用中,l-色氨酸的熔点也需要被控制在一定范围内。
例如,在制药工业中,l-色氨酸的熔点需要在生产过程中得到控制,以保证产品的质量和稳定性。
此外,在食品工业中,l-色氨酸的熔点也需要被控制在适宜的范围内,以保证产品的口感和质量。
总之,l-色氨酸的熔点是一个重要的物理化学性质,在科学研究和实际应用中都具有重要的意义。
色氨酸

色氨酸科技名词定义中文名称:色氨酸英文名称:tryptophan;tryptophane;Trp定义:学名:2-氨基-3-吲哚基丙酸。
一种芳香族、杂环、非极性α氨基酸。
L-色氨酸是组成蛋白质的常见20种氨基酸中的一种,是哺乳动物的必需氨基酸和生糖氨基酸。
在自然界中,某些抗生素中有D-色氨酸。
符号:W。
应用学科:生物化学与分子生物学(一级学科);氨基酸、多肽与蛋白质(二级学科)以上内容由全国科学技术名词审定委员会审定公布求助编辑百科名片色氨酸色氨酸β-吲哚基丙氨酸,为白色或微黄色结晶或结晶性粉末;无臭,味微苦。
水中微溶,在乙醇中极微溶解,在氯仿中不溶,在甲酸中易溶,在氢氧化钠试液或稀盐酸中溶解。
色氨酸是植物体内生长素生物合成重要的前体物质,其结构与IAA相似,在高等植物中普遍存在。
简介[1]拼音名:Se'ansuan学名:β-吲哚基丙氨酸英文名:TryptophanCAS号:73-22-3熔点:281~282℃[2]密度:1.362g/cm3书页号:2010年版二部-281C11H12N2O2 204.23本品为L-2-氨基-3(β-吲哚)丙酸。
按干燥品计算,含C11H12N2O2不得少于99%。
结构式球棍模型性能本品为白色或微黄色结晶或结晶性粉末;无臭,味微苦。
熔点281~282℃(右旋体),289℃分解,左旋体。
外消旋体微溶于水(0.4%,25℃)和乙醇,溶于甲酸、稀酸和稀碱,不溶于氯仿和乙醚。
0.2%的水溶液pH为5.5~7.0。
生产方法1、3-吲哚乙腈与氨基脲缩合后,氰加成、水解得到外消旋色氨酸。
2、以3-吲哚甲醛与苯胺缩合,然后与a-硝基乙酸脂缩合,经氢化水解得到DL-色氨酸。
3、丙烯醛-苯肼法:丙烯醛与N-丙二酸基乙酸胺在乙醇钠存在下缩合,然后与苯肼缩合、环化,经水解脱羧得到外消旋产品(此方法是最常用、最具经济的生产方法)。
产品标准中国药典2010版Storage:Preserve in well-closed containers密封保存[3](FCC——1992)含量(%)98.5~101.5干燥失重(105℃,3h,%)≤0.3灼烧残渣(%)≤0.1铅(%)≤0.001重金属(以pb计,%)≤0.004砷(以As计,%)≤0.00015鉴别本品的红外光吸收图谱应与对照的图谱(光谱集156图)一致。
色氨酸的作用及应用是什么

色氨酸的作用及应用是什么【背景及概述】[1][2]色氨酸的化学名称为α-氨基-β-吲哚丙酸,有3 种同分异构体:L 型、D 型和消旋体DL 型。
1825 年,色氨酸首次被发现,1902 年,由Hokinst 首次从酪蛋白中分离获得。
其分子式为C11H12N2O2,分子量为204.23,白色晶体或者微黄色片状晶体或粉末,无味右旋体或有特殊甜味,溶于水或者热乙醇,不溶于氯仿、乙醚,在稀酸或稀碱中稳定。
与水一起加热,会产生少量吲哚,在有NaOH、CuSO4存在的条件下加热,则会分解产生大量吲哚。
若迅速加热至210 ℃时颜色会变黄,290 ℃时发生分解反应,长时间光照则会发生着色反应。
L-色氨酸是人体和动物所必需的8 种必需氨基酸之一,不能通过自身合成。
所以,人和动物只能通过食物来摄取L-色氨酸。
D-色氨酸主要存在于植物和微生物之中,动物中含量极少,而且在人体内几乎不发生代谢作用,也无毒性。
L-色氨酸又被称为第二必需氨基酸,目前广泛应用于医药、食品、饲料添加剂以及农业环境检测等行业。
目前,L-色氨酸的重要性越来越受到人们的重视。
而且现在L-色氨酸的应用不仅局限在传统的医药、食品、饲料添加剂行业,在一些新领域也逐渐有了更多应用,例如氨基酸美白剂逐渐应用到化妆品行业;作为健康饮品的许多氨基酸饮料不仅在欧美等发达国家流行,现在也逐渐开始进入我国的饮料市场,并为大众所接受。
随着科学技术的进步,相信人们对色氨酸的用途会有更多的探究和发现。
而且随着基因工程、代谢工程以及定向进化技术的发展,人们可以更好地了解色氨酸的生物合成途径及调控机制,进一步加强优良的产酸菌株的构建,结合发酵工艺的不断完善,L-色氨酸的市场前景十分广阔。
【生理功能】[3]1.免疫功能色氨酸与畜禽机体的免疫功能密切相关。
例如,在猪发生慢性肺炎时,其血浆色氨酸水平逐渐降低;在饲粮中添加0.04% 的L-色氨酸可显著提高蛋雏鸭的脾脏指数,添加0.06% 的L-色氨酸可显著提高其胸腺指数;在鸡饲粮中添加L-色氨酸可显著提高干扰素和免疫球蛋白G( IgG) 的水平,显著增强机体对传染性法氏囊病的免疫保护;在饲粮中添加0.05% 的L-色氨酸,可显著增加蛋鸭的胸腺、法氏囊和脾脏等免疫器官的重量;在饲粮中添加L-色氨酸,可显著提高扬州鹅的脾脏指数,并通过刺激IgG 和免疫球蛋白M( IgM) 分泌提高其体液免疫能力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
L-色氨酸的生产及其代谢控制育种摘要本文综述了利用微生物生产L-色氨酸的各种方法和L-色氨酸的生物合成途径及其代谢调控机制,并介绍了利用重组DNA技术选育L-色氨酸高产菌的研究现状。
L-色氨酸是含有吲哚基的中性芳香族氨基酸,为白色或略带黄色叶片状结晶或粉末,水中溶解度1.l4g(25℃),溶于稀酸或稀碱,在碱液中较稳定,强酸中分解。
微溶于乙醇,不溶于氯仿、乙醚。
它是人体和动物生命活动中必需的氨基酸之一,对人和动物的生长发育、新陈代谢起着重要的作用,被称为第二必需氨基酸,广泛应用于医药、食品和饲料等方面。
在生物体内,从-色氨酸出发可合成5-羟基色胺等激素以及色素、生物碱、辅酶、植物激素等生理活性物质,可预防和治疗糙皮病,同时具有消除精神紧张、改善睡眠效果等功效。
色氨酸代谢失凋会引起糖尿病和神经错乱,因此在医学上被用作氨基酸注射液和复合氨基酸制剂。
另外,由于色氨酸是一些植物蛋白中比较缺乏的氨基酸,用它强化食品和做饲料添加剂对提高植物蛋白质的利用率具有重要的作用,它是继蛋氨酸和赖氨酸之后的第三大饲料添加氨基酸。
1.色氨酸的生产方法色氨酸的生产最早主要依*化学合成法和蛋白质水解法,但是随着对微生物法生产色氨酸研究的不断深入,这种方法已经走向实用并且处于主导地位。
微生物法大体上可以分为直接发酵法、微生物转化法和酶法。
近年来还出现了将直接发酵法与化学合成法相结合、直接发酵法与转化法相结合生产色氨酸的研究。
另外,重组DNA技术在微生物育种和酶工业上的应用极大地推动了直接发酵法和酶法生产色氨酸的工业化进程。
1.1微生物转化法亦称前体发酵法。
这种方法使用葡萄糖作为碳源,同时添加合成色氨酸所需的前体物如邻氨基苯甲酸、吲哚等,利用微生物的色氨酸合成酶系来合成色氨酸。
这种方法同直接发酵法一样,需要解除生物合成途径中大部分酶所受到的反馈调节,以使色氨酸能够高浓度蓄积。
另外,所添加的前体物大都是抑制微生物生长的,因此添加量不可过高,一般采取分批少量添加的方法。
同时可以筛选前体物的抗性突变株来提高前体物的添加量。
例如采用枯草杆菌的5-FT抗性突变株SD-9在15L含6%葡萄糖的培养基中培养,在培养过程中每次添加少量6%的邻氨基苯甲酸溶液共2L,经120h后可生产色氨酸9.6g/L。
微生物转化法的不足在于当转化液中前体物浓度较高时,转化率有所下降。
另外,前体物的价格比较昂贵,不利于降低成本。
1.2酶法酶法是利用微生物中色氨酸生物合成酶系的催化功能生产色氨酸。
这些酶包括色氨酸酶、色氨酸合成酶、丝氨酸消旋酶等。
根据提供这些酶的微生物种类数,可以分为双酶菌法和单酶菌法两种类型。
该法既可以直接加入细胞壁溶解酶使细胞破壁后再使用,也可以将所需的酶固定化后再使用,一般由酶源菌体的培养、菌体的分离洗涤、固定化和反应几个阶段组成。
例如利用大肠杆菌的色氨酸合成酶和恶臭假单孢菌的丝氨酸消旋酶,以吲哚和DL-丝氨酸为底物,在200L反应罐中反应24h,色氨酸产量可达到28.5g/L。
利用黄杆菌AF39l2的酶系,以DL-5-吲哚甲基乙丙酚脲为底物,同时在反应液中加入适量的苯肼或野芝麻花碱以抑制色氨酸氧化酶的活性而阻止色氨酸的降解,L-色氨酸的产量可达8.8g/L。
酶法能够利用化工合成的前体物为原料,既充分发挥了有机合成技术的优势,又具有产物浓度高、收率高、纯度高、副产物少、精制操作容易的优点,是一种成本较低的生产色氨酸的工业化生产方法。
1.3直接发酵法该法是以葡萄糖、甘蔗糖蜜等廉价原料为碳源,利用优良的色氨酸生产菌种来生产色氨酸。
对这种方法的研究进行的比较早,但在相当长的一段时间内达不到工业化生产的要求。
主要原因是从葡萄糖到色氨酸的生物合成途径比较漫长,其代谢流也比较弱,而且色氨酸的合成需要多种前体物(如PRPP等),若想进一步提高色氨酸的积累量就必需设法增强合成这些前体物的代谢流。
另一方面,色氨酸生物合成途径中的调控机制比较复杂,除了反馈调节这一粗调系统之外,还存在着细调系统-弱化子系统。
随着重组DNA技术在微生物育种中的应用,为优良的色氨酸生产菌株的筛选和产酸水平的提高提供了可*的技术保障,使微生物直接发酵法生产色氨酸成为一种廉价的工业化生产方法。
例如从大肠杆菌EMS4-C25中分离得到抗反馈调节的色氨酸操纵子,并将其克隆到质粒pUCI9和pHSG576中分别得到重组质粒pTC7O1和pTC576。
将pTC576转化到大肠杆菌中,该菌经过17h的分批发酵积累色氨酸l6g/L。
Ikeda等将带有DAHP合成酶(DS)和色氨酸合成酶(F)的质粒引入产色氨酸的谷氨酸棒杆菌KYl0-894中,使色氨酸的产量提高了54%,达到了66g/L。
l.4 其他生产方法的研究这些方法主要是将上述几种方法有机地结合起来进行色氨酸的生产。
主要有直接发酵法与化学合成法、酶法相结合,其特点是利用发酵法廉价提供一种前体物,再结合其它方法的优势进行生产。
例如,利用黄色短杆菌P390直接发酵积累L-谷氨酸-y-半醛(GSA)达13.2g/L,然后将发酵液适当稀释后加入含苯肼的1mol/L H2SO4中加热回流1h之后,48%的CSA可转化为 L-色氨酸。
利用落叶松草AHU9382以5%葡萄糖为碳源发酵3d可积累丙酮酸22-26.5g/L,然后加入吲哚、氯化铵和具有高色氨酸酶活性的产气肠杆菌培养,12h之后可积累L-色氨酸l5g/L。
2.色氨酸发酵的代谢控制育种近年来,色氨酸作为必需氨基酸在输液、健康食品、饲料添加剂上的应用日益广泛,随着蛋氨酸、赖氨酸的大量饲料化应用,价格一直较高的色氨酸更希望有廉价制造的工业化生产方法,以便推进色氨酸的应用饲料化的实施。
在我国对直接发酵法生产色氨酸虽作了一些研究工作,但发酵产酸水平较低,还没有得到可应用于工业化生产的稳定的高产菌株,因此,研究色氨酸的生物合成途径及代谢调节机制,用代谢控制育种和基因工程的方法构建色氨酸高产菌株就十分必要。
2.1出发菌株的选择色氨酸发酵的生产菌种有谷氨酸棒杆菌(C·glutamicum)、黄色短杆菌(B·flavum)、枯草芽孢杆菌(B·subtilis)、大肠杆菌(E·c oli)、产朊假丝酵母(Candida utilis)等。
2.2色氨酸的生物合成途径和代谢调节机制迄今被研究的所有菌株的色氨酸生物合成途径都是一样的,但是其调控方式及trp基因的表达等却有很大的不同。
这些不同点主要有:(1)DS酶所受的调节方式不同。
在大肠杆菌、粗糙脉孢菌等微生物中有3种DS 酶,这些同功酶分别受3种芳香族氨基酸的反馈调节。
在谷氨酸棒杆菌和黄色短杆菌中只有一种DS酶,它受L-Phe和L-Tyr的协同反馈抑制。
枯草芽孢杆菌中的DS酶受顺序反馈抑制。
(2)和色氨酸生物合成有关的基因的顺序和结构不同。
在肠杆菌中对色氨酸的合成进行调控的基因组成一个单一的操纵子,而且它们排列的顺序也都是一样。
在乳糖发酵短杆菌中也是单一的操纵子结构,但在非肠杆菌和真核生物中这种结构却并不多见。
(3)对结构基因表达的调控方式不同。
在大肠杆菌等肠杆菌中,依*阴遏系统和转录的弱化机制来对和色氨酸生物合成有关的结构基因的表达进行调控,在枯草芽孢杆菌中需要RegA和mtrB基因来参与对转录弱化的调控和RNA结合蛋白的调节。
在铜绿假单孢菌中,trpI基因编码的转录激活因子在吲哚甘油磷酸存在时诱导rtpB、trpA基因的表达。
在有些微生物中,只有转录的弱化机制对基因的表达进行调控。
色氨酸的生物合成途径和代谢调节机制(以黄色短杆菌为例),邻氨基苯甲酸合成酶(AS)被色氨酸反馈抑制1.5umol/L的Trp使其活性丧失50%,抑制常数Ki为0.44umol/L,10umol/L的Try 几乎完全抑制其活性,这种抑制作用大大强于大肠杆菌和枯草芽胞杆菌中的AS酶所受的抑制作用。
对于AS酶的底物分支酸来说,抑制是竞争性的,而对于另一种底物谷氨酰胺,抑制是反竞争性的。
邻氨基苯甲酸磷酸核糖移换酶(PRT)不与AS形成复合体,主与大肠杆菌有所不同。
它也受Trp的反馈抑制,其抑制常数Ki为0.26mmol/L。
对于该酶的两个底物邻氨基苯甲酸核糖焦磷酸来说,抑制都是非竞争性的。
TS酶乳受Trp的反馈抑制,其抑制常数为2.0mmol/L,约比PRT的Ki高一个数量级,对于其底物丝氨酸来说,抑制是竞争性的。
此外色氨酸专一合成途径中的所有酶均受到Try的反馈阻遏,但它们的活性系数各不相同,显示出不同程度的阻遏效应。
对于色氨酸操纵子的结构及其阻遏系统和弱化机制已经研究得比较清楚,本文对此不再赘述。
值得注意的是,在色氨酸操纵子内部还存在一个二级启动子,该启动子位于trpC基因的上游、TrpD基在的末端。
为什么trp操纵子需要两个转录起始位置,对这个问题还没有明确的答案,但这很可能是对Trp生物合成进行调节的经济性的需要。
由于Trp对TrpE、TrpD所编码的邻氨基苯甲酸合成酶(AS)和邻氨基苯甲酸核糖移换酶(PRT)的抑制作用远大于对TrpC、TrpB、TrpA所编码的3个酶的抑制作用,因此没有必要使这5个酶的合成具有同步性。
色氨酸操纵子中的两个启动子具有不同的强度,启动作用受不同的因子调控,可使基因表达更加有效、更加协调,而且在不同的生活环境中,不同的启动子精密地调节基因的表达量,对维持细胞的生存起着非常重要的作用。
3.色氨酸生产菌的育种思路如上所述,芳香族氨基酸的生物合成存在着特定的代谢调节机制,因此不可能从自然界中找到大量积累色氨酸的菌株。
但是我们可以以黄色短杆菌、谷氨酸棒杆菌等为出发菌株,设法得到从遗传角度解除芳香族氨基酸生物合成证常代谢调节机制的突变菌株,用微生物直接发酵法,生产色氨酸。
这些方法包括:解除菌体自身反馈调节,切断支路代谢,增加前体物的合成等,下面分别讨论。
3.l切断支路代谢切断由分支酸到预苯酸、Vk、CoQ的代谢支路,可节约碳源,使中间产物分支酸更多地转向合成色氨酸,而且还可以解除苯丙氨酸、酪氨酸对合成途径中DS的反馈调节。
从而有利于色氨酸积累。
例如,有人以谷氨酸棒杆菌为出发菌株,经诱变得到的KY9456(Phe+Tyf)可积累色氨酸0.15g/L。
这个产量是很低的,由此也可看出只选育缺陷型是不够的,还必须解除由色氨酸引起的反馈调节。
3.2解除菌体自身反馈调节根据图1所示的调节机制,对于黄色短杆菌来说,如果解除色氨酸特异途径的调节机制,即使有共同途径上反馈调节的存在,也能大量积累色氨酸。
因此可选育色氨酸结构类似物的抗性突变株,解除其自身的反馈调节来达到积累色氨酸的目的。
对于色氨酸来说,它的结构类似物有:5-甲基色氨酸(5-MT)、5-氟色氨酸(5-FT)、色氨酸氧肟酸盐(TrpHx)、6-氟色氨酸(6-FT)、6-甲基色氨酸(6-MT)、4-甲基色氨酸(4-MT)等。
