临床试验中的样本量计算
临床研究中的样本量估算:临床试验

临床研究中的样本量估算:临床试验在临床研究领域,样本量估算无疑是临床试验设计中至关重要的一环。
它不仅关系到研究结果的可靠性和有效性,还直接影响到研究的成本、时间和可行性。
通俗来讲,样本量估算就是要回答“我们需要多少研究对象才能得出有意义的结论”这个关键问题。
为什么样本量估算如此重要呢?想象一下,如果样本量过小,就好像只从大海中舀了一小杯水来判断海水的成分,结果很可能因为随机性太大而不准确,甚至得出错误的结论。
相反,如果样本量过大,虽然能增加结果的可靠性,但会造成资源的浪费,研究时间延长,成本大幅增加。
所以,找到一个恰到好处的样本量,是每个临床试验设计者都必须面对的挑战。
那么,如何进行样本量估算呢?这可不是拍脑袋就能决定的,而是需要综合考虑多个因素。
首先要考虑的是研究的主要目的和假设。
比如,是要比较两种治疗方法的疗效差异,还是要评估某种药物的安全性?不同的研究目的和假设会对样本量产生不同的要求。
假设我们要比较一种新药物和传统药物治疗某种疾病的效果。
我们的假设是新药物的疗效优于传统药物。
为了能够有足够的把握检测出这种差异,我们需要根据预期的疗效差异大小来确定样本量。
如果预期的差异很小,那么就需要更多的样本才能检测到这种细微的差别;如果预期的差异较大,相对来说所需的样本量就会少一些。
其次,效应大小也是一个关键因素。
效应大小反映了研究中所关注的变量之间的差异程度。
比如,在药物疗效研究中,效应大小可以是新药物和传统药物在治愈率、症状改善程度等方面的差异。
一般来说,效应大小越大,所需的样本量就越小;效应大小越小,所需的样本量就越大。
再者,检验水准和检验效能也不能忽视。
检验水准通常设定为005,它表示在假设检验中,当原假设为真时,错误地拒绝原假设的概率。
而检验效能则是在给定的效应大小和样本量的情况下,正确拒绝原假设的概率,一般要求检验效能不低于 80%。
简单来说,检验水准和检验效能就像是天平的两端,我们需要在它们之间找到一个平衡,以确定合适的样本量。
临床试验样本量的估算30429

临床试验样本量的估算30429
1.实验目标:明确试验的主要目标是什么?是评估治疗的效果、副作用,还是探索新的治疗方法等?不同的目标可能需要不同的样本量。
2.效应大小:效应大小是指治疗或干预与对照组之间的差异有多大。
通常,需要根据预期的效应大小来估算样本量。
如果效应很小,那么需要
更大的样本量才能检测到显著的差异。
3.α和β错误:在样本量估算中,需要考虑到统计显著性水平(α)和统计功效(1-β)。
一般常用的显著性水平为0.05,统计功效为80%。
根据研究的特点和要求,也可以选择不同的显著性水平和统计功效。
4.可接受的误差:在样本量估算中,还需要考虑到可接受的误差范围。
例如,如果试验的目标是评估治疗效果,那么可接受的误差范围是多少?
一般来说,误差范围越小,需要的样本量也越大。
综合上述因素进行样本量估算的计算。
常用的样本量估算方法有多种,如假设检验的样本量估计、置信区间的样本量估计、生存分析中的样本量
估计等。
具体使用哪种方法取决于试验研究的设计和目标。
最后,需要注意的是样本量的估算只是一个大致的估计,并不代表最
终确定的样本量。
在实际进行试验之前,还需要进行实际情况的调查和分析,可能需要进行修正和调整。
临床试验公式

临床试验公式
临床试验公式有很多,以下是一些常见的公式:
1. 样本量计算公式:n=Z²σ²/d²,其中n为样本量,Z为统计量,σ为标准差,d为允许误差。
2. 诊断试验临床灵敏度计算公式:灵敏度=真阳性人数/(真阳性人数+假阴性人数)×100%。
3. 诊断试验临床特异度计算公式:特异度=真阴性人数/(真阴性人数+假阳性人数)×100%。
4. 诊断试验临床准确度计算公式:准确度=(真阳性人数+真阴性人数)/(真阳性人数+真阴性人数+假阳性人数+假阴性人数)×100%。
5. 诊断试验约登指数计算公式:约登指数=灵敏度+特异度-1。
这些公式在临床试验中经常使用,但具体使用哪个公式需要根据试验的目的和设计来确定。
临床试验样本量的估算介绍

临床试验样本量的估算介绍临床试验样本量的估算是一个关键性的步骤,它决定了试验结果的可靠性和统计学上的显著性。
样本量的估算需要考虑多个因素,如预期效应大小、研究设计、统计分析方法以及可接受的错误率等。
本文将详细介绍临床试验样本量估算的基本原理和常用方法。
一、样本量估算的目的和原则样本量估算的主要目的是确保试验具有足够的统计功效,能够检测到预期效应的存在或差异的显著性。
同时,也需要避免过大的样本量,以减少资源的浪费和人体试验的风险。
样本量估算的原则如下:1.统计功效要求:根据研究者的预期效应大小,确定试验能够达到的最小统计功效要求。
通常,我们希望试验能够有80%的功效检测到预期效应。
2.显著性水平:选择统计学上的显著性水平,通常为α=0.053.效应大小的估计:根据已有的文献或专家经验,估计预期效应的大小。
4.变异性的估计:估计所研究的指标的标准差或方差。
5.实用性考虑:考虑到资源和时间的限制,选择可实现的最小样本量。
二、常用的样本量估算方法1.基于效应大小的样本量估算方法这种方法根据研究者希望检测到的最小效应大小来估算样本量。
常用的方法有两组均数差异的估算、比例差异的估算以及相关系数的估算。
对于两组均数差异的估算,可使用t检验或方差分析来进行样本量估算。
对于比例差异的估算,可使用Z检验来进行样本量估算。
对于相关系数的估算,可使用相关系数检验来进行样本量估算。
2.基于统计功效的样本量估算方法这种方法以试验的统计功效为基础,确定对于预期效应的检测,需要多大样本量。
常用的方法有功效检验和样本量递推法。
对于功效检验法,可以通过计算给定样本量下的样本估计效应大小,并判断是否满足统计功效要求。
对于样本量递推法,可以根据初步样本量估计和实际效应大小来修正样本量,直到满足统计功效要求。
3.基于生存分析的样本量估算方法这种方法适用于生存分析或生存率的研究。
常用的方法有Kaplan-Meier方法和Cox比例风险模型。
临床试验样本量估算

临床试验样本量估算在估算样本量时,有几个关键要素需要考虑:1. 效应大小(Effect Size):效应大小是指在两个比较组之间预期的差异大小。
一般来说,效应大小越大,所需的样本量越小。
2. 置信度(Confidence Level):置信度是指研究者对样本调查结果的信任程度。
常用的置信度为95%或99%。
一般来说,置信度越高,所需的样本量越大。
3. 统计显著性(Statistical Significance):统计显著性是指试验结果的显著性水平。
常用的显著性水平为α=0.05或α=0.01、一般来说,显著性水平越低,所需的样本量越大。
4. 效应方向性(Directionality of Effect):效应方向性是指试验是否需要检测两组间的差异。
若只需检测差异是否存在,则样本量较小;若需检测差异的方向,则样本量较大。
5. 控制变量的数量(Number of Control Variables):增加控制变量的数量会增加结果解释的复杂度,从而需要更大的样本量。
6. 数据的可变性(Variability of Data):数据的可变性与样本量呈反比关系。
如果数据变异性大,所需的样本量就会相对较大。
7. 可行性和资源限制(Feasibility and Resource Constraints):实际操作中,样本量可能受到可行性和资源限制的影响。
研究者需要评估可行性因素,并根据实际情况确定样本量。
基于以上要素,常用的样本量估算方法有以下几种:1.参数估计法:通过统计分析来估计试验样本量。
研究者需要提供试验所需的显著性水平、效应大小以及控制变量的数量等参数。
常用的参数估计方法有t检验、方差分析、卡方检验等。
2. 非参数估计法:当样本不满足正态分布或总体参数未知时,可以采用非参数的方法进行样本量估算。
常用的非参数方法有Wilcoxon秩和检验、Mann-Whitney U检验、logistic回归等。
临床试验常用样本量的计算方法

临床试验常用样本量的计算方法临床试验是评价医疗干预措施有效性和安全性的重要方法之一、在进行临床试验时,合理的样本量计算是确保试验具有统计学意义和科学可靠性的重要步骤之一、本文将从试验目的、效应大小、错误类型和统计方法等方面介绍临床试验常用的样本量计算方法。
一、试验目的在进行样本量计算之前,首先需要明确试验的目的是什么。
不同的试验目的对样本量计算有不同的要求。
1.描述性试验:描述性试验是旨在描述和概括人群特征、疾病频率、新技术的性能等,通常不涉及统计检验。
在这种类型的试验中,样本量的计算往往以统计学为基础,根据置信区间长度或精确度来确定。
2.比较试验:比较试验是旨在比较不同干预措施的效果,常见的包括药物疗效的比较、手术效果的比较等。
在这种类型的试验中,需要确定试验的主要效应大小。
二、效应大小效应大小是指试验结果中真实存在的干预效果的大小。
样本量计算中需要考虑到主要效应的大小,以使试验能够检测到具有意义的差异。
1.非劣效(非劣效)试验:非劣效试验是以疗效差异的下限边界(非劣效界)为基础,判断新干预措施是否与已有干预措施相当。
样本量计算需要根据监测期望的非劣效界来确定。
2.等效性试验:等效性试验是旨在证明两种干预措施的疗效相当。
在这种类型的试验中,需要确定非劣效界,并根据非劣效界来计算样本量。
3.优势试验:优势试验是旨在证明新的干预措施是否优于已有干预措施。
样本量计算需要确定所期望的主要效应大小、显著性水平和统计功效,以及预期的丢失率和失败率。
三、错误类型在进行临床试验时,需要考虑两类错误:第一类错误(α错误)和第二类错误(β错误)。
样本量计算需要控制这两类错误的概率。
1.第一类错误(α错误)是指在实际上不存在差异的情况下,错误地拒绝原假设(即错误地得出差异存在的结论)。
控制α错误的概率可以通过选择适当的显著性水平来实现。
2.第二类错误(β错误)是指在实际上存在差异的情况下,错误地接受原假设(即错误地得出差异不存在的结论)。
临床样本量统计

1、样本量计算公式根据统计学原理,经预试验的两组结果,对照组率Pc=100%,治疗组率Pi=99%,两组率差=1%。
根据离散响应变量样本量计算公式(等效性/非劣性),每组样本量N=2(Zα+Z2/β)2×(Pc+Pi)/2×{1-(Pc+Pi)/2}/Δ2。
取α=0.05,β=0.10,按照临床意义的界值Δ(一般为10%),取对照组有效率的10%,即Δ=10%。
根据以上公式和设定值,每组样本量N=2×(1.96+1.645)2×0.995×0.005/0.12=12.9,即至少需要13例。
如果按20%的脱落率计算,即临床样本量为15例。
2、统计分析1、样本数的确定本研究欲考察该产品的临床治愈率不差于对照组产品,即设定为非劣效性试验,试验组与对照组按1:1的比例安排病例数,评价指标采用定性指标,根据以往的该类产品的疗效和统计学的一般要求,取α=0.05,β=0.20,等效标准δ=0.15,平均有效率p=0.95,由传统计算公式N=12.365×P(1-P)/ δ2N:每组的估算例数N1=N2,N1和N2分别为试验组和对照组的例数,P:平均有效率δ:等效标准α显著性水平,也是假阳性率,α=0.05,表示将来自同一总体的两样本可能为来自不同总体的概率为5%β:1-β称为检验效能把握度,β=0.20时表示当两总体确有差异时,按α水准有80%的把握能发现他们有所差别。
根据以往的该类产品的疗效和统计学的一般要求,取α=0.05,β=0.20,等效标准δ=0.15, 平均有效率p=0.95,由上述公式计算得到每组需要完成26例,试验设计每组完成30例。
同时为了弥补传统的样本量估计方法的不足,在非劣效性评价的临床试验中,当疗效指标为离散变量时,可以采用相对率可信区间的方法,SAS下编写宏,由SAS.FREQ过程提供的CMH检验和计算相对率的功能解决。
随机模拟路线:(1)产生若干符合两项分布的随机数,进行CNH检验,估计相对率的可信区间(可信区间下限不低于0.9),并判断是否符合非劣效的标准;(2)重复N 次,以计算得到非劣效结论的次数,从而计算检验效能;(3 )循环使用上述工具K次,用以寻找符合规定检验效能(0.8)的样本量。
临床研究中的样本量估算_1_临床试验

临床研究中的样本量估算_1_临床试验临床研究中的样本量估算一、引言在临床研究设计的过程中,样本量估算是非常重要的一部分。
样本量的大小直接影响到研究结果的可信度和推广性,因此合理的样本量估算对于研究的有效性和准确性至关重要。
本文将介绍在临床试验中进行样本量估算的一般原则和方法。
二、样本量估算的原则1.研究目的和假设:在进行样本量估算之前,需要明确研究的目的和科学假设。
例如,研究目的是评价一种新药物的疗效,科学假设是该新药物相对于对照药物在治疗效果上具有显著差异。
2.效果大小和显著水平:样本量估算需要考虑研究的主要效果大小和研究结果的显著性水平。
主要效果大小通常由预期的效应量来衡量,显著性水平通常设定为0.05.3.统计方法和假设检验:样本量估算需要选择适当的统计方法和假设检验方法。
常用的统计方法包括t检验、χ2检验和生存分析等,根据研究设计和数据类型选择合适的方法。
4.统计功效和样本比例:根据效果大小、显著水平和统计方法,可以计算出研究的统计功效。
统计功效通常设定为80%或90%,根据研究的要求合理选择。
三、样本量估算的方法1.固定效应模型:适用于研究目的明确,效果大小可预期的情况。
根据预期的效应大小、显著水平和统计功效,可以计算出所需的最小样本量。
2.结果模拟法:适用于研究目的不明确,效果大小不确定的情况。
通过模拟多个样本量和效果大小的组合,评估不同样本量下的统计功效和效果大小的关系,从而选择合理的样本量范围。
3.临床合理性法:适用于研究目的和效果大小无法准确估计的情况。
根据研究领域的临床经验和专家意见,结合已有的临床试验结果,进行样本量估算。
四、样本量估算的考虑因素1.预计的失访率和样本无效率:由于各种原因,研究中可能存在部分受试者失访或数据无效的情况。
在样本量估算中需要考虑到这些因素的影响,增加适当的样本量。
2.子组分析和交互效应:如果研究中存在多个子组或交互效应的检验,需要进行适当的样本量调整,以保证对这些效应进行准确的评估。
临床试验中的样本量计算与统计分析

临床试验中的样本量计算与统计分析在临床试验中,样本量计算和统计分析是至关重要的步骤。
正确的样本量计算和合理的统计分析可以提高试验结果的可靠性和准确性,有助于作出科学的结论和决策。
本文将介绍临床试验中样本量计算和统计分析的方法与原则。
一、样本量计算在进行临床试验之前,研究者需要首先确定所需的样本量。
样本量的大小直接影响到试验结果的可靠性和统计分析的准确性。
合理的样本量计算可以提高试验的统计功效,避免对实验性干预或治疗效果的误判。
样本量计算需要考虑以下几个因素:1. 效应大小:试验中所关心的效应大小,即干预措施对结果的影响程度。
效应越大,所需的样本量越小。
2. 显著水平:研究者设置的判断差异是否显著的临界值,通常取α=0.05。
显著水平越高,所需的样本量越大。
3. 统计功效:即在试验中观察到预期效应的可能性。
通常设置为1-β=0.8,表示有80%的概率发现真实效应。
统计功效越高,所需的样本量越大。
4. 效应的变异性:试验个体之间效应的异质性程度。
效应的变异性越大,所需的样本量越大。
二、统计分析完成临床试验后,研究者需要进行统计分析,对试验结果进行解释和推断。
合理的统计分析可以准确评估干预措施的效果,并进行科学性的结论和推广。
常用的统计分析方法包括:1. 描述性统计分析:对试验样本的基本特征进行汇总和描述,例如均值、标准差、频数等。
2. 探索性数据分析:通过图表和分布等方式探索样本数据,寻找数据的规律和趋势。
3. 参数估计和假设检验:通过点估计和区间估计对总体参数进行估计,并利用假设检验对实验组和对照组之间差异的显著性进行判断。
4. 方差分析:用于比较三个或三个以上组别间的差异。
5. 相关分析:评估两个或多个变量之间的相关程度。
6. 生存分析:对生存时间或事件数据进行分析,评估干预措施对生存时间的影响。
根据试验设计和问题的需要,研究者可以选择合适的统计分析方法。
在进行统计分析时,需要注意以下几个方面:1. 数据的可靠性和完整性:尽可能提高数据的质量和完整性,减少因缺失数据而引起的偏差。
临床试验样本量的估算

临床试验样本量的估算临床试验的样本量估算是研究计划中非常重要的一个环节。
样本量的大小会直接影响到试验结果的可靠性和推广性。
本文将介绍一些常用的方法和考虑因素,来进行临床试验样本量的估算。
一、统计学方法1.样本量估算的原则样本量估算的基本原则是保证试验结果的统计学意义和实际应用的可行性,同时控制样本量的大小。
在样本量估算时需要考虑的主要因素包括:研究目的、效应大小、α水平、β水平、检验类型和预估结果的方差。
2.效应大小效应大小(Effect Size)指的是一种观察、试验或实验中的两组之间的差异,并且是研究中最重要的指标之一、效应大小的选择需要基于研究目标和研究领域的实际情况。
常用的效应大小指标包括:风险比、比值比、均值差异等。
3.α水平和β水平α水平和β水平是两种错误假设的概率。
α水平(Type I错误)是拒绝了一个真假设。
通常是将p值设置在0.05以下。
β水平(TypeII错误)是接受了一个错误的假设。
常见的β值是0.2、0.1、0.05和0.01、α和β的选择需要根据实际情况和研究目的进行权衡。
4.检验类型根据研究目的和数据类型的不同,可以选择不同的检验类型。
常见的检验类型包括:t检验、方差分析、卡方检验等。
不同的检验类型需要不同的样本量估算方法。
5.预估结果的方差预估结果的方差是样本量估算的另一个重要因素。
方差的预估可以通过先前的研究结果或者基于临床经验来估算。
二、样本量估算方法1.均值差异的样本量估算方法均值差异的样本量估算方法适用于需要比较两个或多个组之间平均值差异的研究。
常用的方法有:Z检验样本量估算、t检验样本量估算和方差分析样本量估算。
2.分类变量的样本量估算方法分类变量的样本量估算方法适用于比较不同组之间的比率、风险比、比值比等。
常用的方法有:卡方检验样本量估算和Fishers精确检验样本量估算等。
3.生存分析的样本量估算方法生存分析的样本量估算方法适用于评估治疗或干预措施对患者生存时间或复发时间的影响。
临床试验样本量计算小程序使用案例

临床试验样本量计算小程序使用案例一、背景介绍随着临床试验的广泛应用和研究的不断深入,确定合理的样本量成为了保证试验结果可靠性和科学性的重要环节。
为了提高研究者对样本量计算的准确性和效率,开发了临床试验样本量计算小程序。
本文将介绍临床试验样本量计算小程序的使用案例。
二、案例背景某研究团队计划开展一项药物治疗性研究,希望通过比较两种不同治疗方案在治疗效果上的差异。
为了获得可靠的结果,研究人员决定使用临床试验样本量计算小程序来确定合理的样本量。
三、使用案例1. 打开临床试验样本量计算小程序。
2. 选择研究类型:根据研究目的和设计,选择合适的研究类型。
在本案例中,选择“两组平行设计”。
3. 输入效应量:效应量是研究者用来描述两组之间差异程度的指标。
研究人员根据文献资料和先前研究结果,估计了预期的效应量。
4. 输入显著水平:显著水平是用来判断样本量是否足够大以检测出真实差异的概率。
在本案例中,研究人员设置了显著水平为0.05,即5%。
5. 输入功效:功效是用来评估样本量计算的准确性和可靠性的指标。
研究人员预设了80%的功效,以降低类型II错误的概率。
6. 输入其他参数:根据研究设计和具体要求,研究人员可以输入其他相关参数,如推测失效率、相对比例等。
7. 点击“计算”按钮,即可得到计算结果。
8. 解读结果:根据程序给出的计算结果,研究人员可以了解到所需的最小样本量以及建议的总样本量。
同时,程序还提供了多种图表和统计指标,帮助研究人员更直观地了解样本量计算结果。
9. 校核和讨论:研究团队可以根据计算结果进行校核和讨论,是否需要调整样本量或者进行进一步的优化设计。
四、使用案例效果通过使用临床试验样本量计算小程序,研究人员能够准确、高效地确定合理的样本量,从而提高临床试验的科学性和可靠性。
该小程序的使用案例在该研究团队的样本量计算工作中取得了良好的效果,并为后续的数据采集和分析提供了有力支持。
临床试验样本量计算小程序的使用案例为研究人员提供了一种便捷、准确的样本量计算方法。
临床试验公式

临床试验公式
临床试验公式是一种用于评估药物或治疗方法疗效的工具,根据不同的试验目的和研究设计,可能会使用不同的公式。
以下是常见的临床试验公式及其应用范围:
1.样本量计算公式:用于确定临床试验所需的最小样本量,以确保研究结果的统计显著性。
样本量计算公式基于研究假设、统计学原理和实验设计来确定所需的参与者数量。
2.生存分析公式:适用于评估治疗对患者生存时间或无进展生存期的影响。
生存分析公式包括卡普兰-迈尔曲线、库克-默兰公式等,用于计算不同治疗组间的生存曲线的差异和生存率的估计。
3.疾病评分公式:用于评估患者疾病病情的严重程度或治疗效果的变化。
常见的疾病评分系统包括国际白血病骨髓移植联盟(IBMTR)评分、克鲁特克-佩尔森评分等。
4.药物代谢公式:适用于评估药物在体内的代谢速率。
药物代谢公式可以帮助调整药物剂量,以提高治疗效果并降低不良药物反应的风险。
除了以上提到的公式,还有许多其他的临床试验公式,根据具体的研究目的和研究设计而定。
这些公式在临床试验中的应用可以帮助研究人员评估药物或治疗方法的疗效,从而为患者提供更好的治疗选择和医疗决策支持。
临床试验常用样本量的计算方法

临床试验常用样本量的计算方法
临床试验的样本量计算主要涉及到以下几个方法:
1. 根据研究目标和假设:根据试验的目标、研究假设、预计的效应大小和统计显著水平,使用统计方法计算所需的样本量。
常用的统计方法有t检验、卡方检验、方差分析等。
2. 根据统计效应和统计效力:根据已有的研究结果或假设,估计所需的统计效应大小和统计效力(通常选择80%或90%),然后使用相应的统计方法计算样本量。
3. 根据追踪率或失访率:考虑随访率和失访率对样本量的影响。
通常会根据研究经验或类似研究的结果,估计追踪率和失访率,并据此调整样本量。
4. 根据样本量估计的误差:根据研究目标和统计学原理,估计所能接受的误差范围,然后使用统计方法计算所需的样本量。
需要注意的是,样本量计算是一项复杂的工作,需要考虑多个因素,并可能涉及到统计学知识和软件工具的应用。
在实际应用中,可能还需要考虑研究可行性、资源限制和伦理要求等因素。
因此,建议在进行样本量计算时寻求专业统计学家或研究方法学专家的帮助。
临床试验样本量的估算
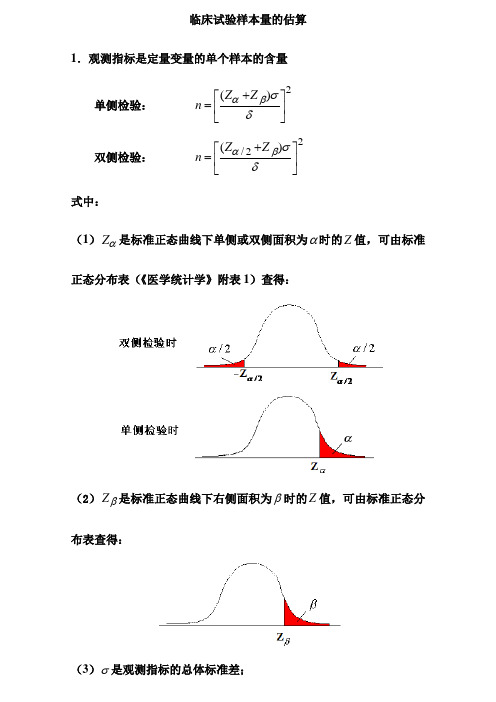
临床试验样本量的估算1.观测指标是定量变量的单个样本的含量单侧检验:2)(⎥⎦⎤⎢⎣⎡+=δσβαZZn双侧检验:22/)(⎥⎦⎤⎢⎣⎡+=δσβαZZn式中:(1)αZ是标准正态曲线下单侧或双侧面积为α时的Z值,可由标准正态分布表(《医学统计学》附表1)查得:(2)βZ是标准正态曲线下右侧面积为β时的Z值,可由标准正态分布表查得:(3)σ是观测指标的总体标准差;(4)δ是容许误差;2.观测指标是定量变量的实验组与对照组的样本含量双侧检验: 22/)(4⎥⎦⎤⎢⎣⎡+⨯=δσβαZ Z n 单侧检验: 2)(4⎥⎦⎤⎢⎣⎡+⨯=δσβαZ Z n 这是两个样本合计的例数,一般,可取21n n =,22n n =。
上式中, (1)αZ 是标准正态曲线下单侧或双侧面积为α时的Z 值,可由附表1查得;(2)βZ 是标准正态曲线下右侧面积为β时的Z 值,可由附表1查得 (3)σ是两个样本所取自的总体标准差的合并值:221σσσ+=;在实际研究时,σ一般是未知的,可以通过预试验或文献确定出1S 与2S ,用221S S S +=估计σ;(4)容许误差||21μμδ-=。
3.观测结果是二分类的单个样本的含量A 方法的阳性率:nb a +=1π B 方法的阳性率:n ca +=2π两种方法结果一致的例数:d a +,其中,阳性例数:a , 两种方法结果一致的阳性率:da a+=π 上述数据在实际中均是未知的,要从小规模的预试验的结果来估计。
样本量的估算公式:221212/)())((22⎥⎥⎥⎥⎦⎤⎢⎢⎢⎢⎣⎡---+=ππππππππβαZ Z n式中,2221ππππ-+=4.观测结果是二分类的实验组与对照组的样本含量双侧检验:22122112/))1()1((2)1(2⎥⎥⎦⎤⎢⎢⎣⎡--+-+-=ππππππππβαZ Z n c c单侧检验: 2212211))1()1((2)1(2⎥⎥⎦⎤⎢⎢⎣⎡--+-+-=ππππππππβαZ Z n c c式中, c π=221ππ+,1π是实验组的阳性率,2π是对照组的阳性率。
非劣效临床试验样本量计算

非劣效临床试验样本量计算非劣效临床试验(Non-inferiority clinical trial)是指在对比两种治疗方案时,试验者预先设定了一定的非劣效边界(non-inferiority margin),试验的目的是证明新的治疗方案与对照方案之间的差异小于这个非劣效边界,从而能够判断新的治疗方案的有效性。
样本量计算通常依赖于以下几个因素:1. 非劣效边界(non-inferiority margin):非劣效边界的设定应该根据临床经验和先前的研究结果来确定。
非劣效边界越小,要求的样本量越大。
因此,在样本量计算中非劣效边界的选择非常重要。
2. 预计的事件率(event rate):试验中需要估计两种治疗方案的事件发生率,即对照方案的事件发生率和新方案的事件发生率。
这可以根据先前的研究结果或者临床经验来估计。
3. 验证所需的统计功效(statistical power):试验者需要设定试验的统计功效,即试验能够检测到非劣效边界之内的差异的概率。
通常情况下,统计功效的设定为80%或90%。
4. 显著性水平(significance level):显著性水平是指试验中拒绝原假设的概率。
常用的显著性水平是0.05根据上述因素,样本量计算可以使用统计学方法,如Z检验、F检验或卡方检验。
在非劣效非劣效临床试验中,样本量计算通常使用Z检验。
样本量计算的公式可以如下表示:n=[(Z1-α/2+Z1-β)×(p1×(1-p1)+p2×(1-p2))]/(p2-p1)²其中n为总样本量,Z1-α/2为1-α/2分位数的Z值,Z1-β为1-β分位数的Z值,p1为对照方案的事件率,p2为新方案的事件率。
通过样本量计算,试验者可以得到所需的总样本量,从而招募足够的患者参与试验。
然而,样本量计算只是试验设计的一部分,还有其他的因素也需要考虑,如试验的可行性、临床实际情况等。
总之,非劣效临床试验样本量计算是一个重要的步骤,它可以帮助试验者确定所需的总样本量,从而保证试验结果的可靠性和准确性。
临床研究样本量计算流程

临床研究样本量计算流程
临床研究样本量计算流程一般包括以下步骤:
1.确定预期效应大小:这是样本量计算的关键步骤,需要基于文献综述、先前的研究结果或临床经验来确定试验中期望观察到的效应大小。
2.确定统计显著性水平(α):这是试验中用来确定效果是否显著的一个阈值。
通常在临床试验中,统计显著性水平设定为0.05,即p值小于0.05时认为效果显著。
3.确定统计功效(1-β):这是试验中检测到真实效应的概率。
通常将统计功效设定为80%或90%,这意味着试验有80%或90%的机会检测到实际效应(如果存在的话)。
4.根据预期效应大小、统计显著性水平和统计功效,使用适当的公式进行样本量计算。
例如,可以使用t检验的样本量计算公式,或者卡方检验的样本量计算公式等。
5.根据计算结果,确定所需的样本量。
如果样本量过大,可能会增加试验成本和时间;如果样本量过小,可能会影响试验的准确性和可靠性。
以上是临床研究样本量计算的一般流程,具体计算方法可能因研究类型、研究目的、研究设计等因素而有所不同。
因此,在进行样本量计算时,建议咨询专业的统计人员或研究人员,以确保计算的准确性和可靠性。
临床研究样本量计算依据

临床研究样本量计算依据
临床研究样本量计算依据通常基于以下几个因素:
1. 效应大小:样本量计算的关键是确定所需的最小效应大小,即研究所要检测的差异必须具有临床或统计学上的重要性。
效应大小可以通过先前的研究、临床经验或专家意见进行估计。
2. 显著性水平(α错误):样本量计算还取决于研究者所设定的显著性水平,即检验某个差异是否真实存在的阈值。
通常常用的显著性水平是0.05或0.01。
3. 功效(β错误):功效是指研究中检测到差异的可能性,也称为1-β。
通常常用的功效水平是0.8或0.9,表示有80%或90%的概率能够检测到真实存在的差异。
4. 方差:样本量计算还需要估计研究中所研究的变量的方差或标准差。
方差的估计可以依据先前的研究结果、文献综述或者小规模的预研究。
上述因素可以通过统计计算方法(如t检验、方差分析、卡方检验等)结合所选的效应大小、显著性水平、功效和方差来进行样本量计算。
此外,还有一些其他因素可能会影响样本量计算,如研究设计(如交叉设计、配对设计等)、可接受的误差率(如可接受的α错误或β错误的水平)以及研究的费用和时间限制等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
临床试验中的样本量计算
在临床试验的设计中,样本量计算是一个关键的环节,它对试验结果的可靠性和推广性起着至关重要的作用。
本文将介绍一些常用的样本量计算方法和相关的原理,以帮助研究人员正确、准确地进行样本量估计。
一、概述
样本量计算是在进行临床试验之前进行的一项基础性工作,它通过科学合理的统计方法来确定所需的参与试验的患者数量。
样本量的大小直接影响到试验结果的可靠性,过小的样本量可能导致结果不具有统计学意义,而过大的样本量则会造成资源的浪费。
二、常用的样本量计算方法
1. 总体比例样本量计算
总体比例样本量计算常用于有两个互补结果的试验,比如药物治疗与安慰剂治疗的对比试验。
通过确定所需的显著性水平、统计功效和预期的疗效差异,可以利用二项分布来计算样本量。
2. 总体均数样本量计算
总体均数样本量计算常用于比较两个治疗组的平均值,比如药物治疗组和对照组的平均生存时间。
在这种情况下,需要确定所需的显著性水平、统计功效、疗效差异和总体的标准差,利用正态分布来计算样本量。
3. 非劣效性与超劣效性试验样本量计算
非劣效性与超劣效性试验样本量计算常用于评估新药物或治疗方法的非劣效性或超劣效性。
在这种情况下,需要确定所需的非劣效或超劣效边界、显著性水平和统计功效,利用二项分布或正态分布来计算样本量。
4. 多组样本量计算
多组样本量计算常用于比较两个以上治疗组的平均值或比例。
在这种情况下,需要确定所需的显著性水平、统计功效、疗效差异和总体标准差,利用方差分析或多项式分布来计算样本量。
三、样本量计算原理
样本量计算的原理基于统计学中的假设检验理论和置信区间理论。
在假设检验中,通过设定显著性水平和统计功效,可以估计出所需的样本量。
而在置信区间中,通过设定置信水平和效应量,可以估计出所需的样本量。
样本量的计算是基于对试验对象总体的假设和对试验结果的预期,并且要求样本具有代表性和随机性。
四、注意事项
在进行样本量计算时,需要注意以下几点:
1. 合理选择显著性水平和统计功效,一般显著性水平取0.05,统计功效取0.8,但也需根据具体研究的目的和研究领域的惯例进行选择。
2. 准确估计总体参数,如总体比例的估计、总体均值的估计以及总体标准差的估计。
3. 需要综合考虑实际可招募的患者数量,以及试验的时间和经费等限制因素。
4. 样本量计算只是一个估计值,实际进行试验时可能会有一定的误差,因此在结果分析和结论的时候需谨慎对待。
五、结语
样本量计算是临床试验设计中的重要环节,它直接关系到试验结果的可靠性和推广性。
正确、准确地进行样本量估计,可以提高试验的科学性和可比性,减少资源的浪费。
研究人员在进行样本量计算时,需根据具体的试验目的和研究内容,选择合适的样本量计算方法,并严格遵守统计学原理和科学伦理要求。
只有这样,才能得到科学、可靠的试验结果,为临床医学的进一步发展作出贡献。
