沉淀理论2
3.沉淀理论

u 与μ成反比,μ随水温上升而下降;即沉速受水 温影响,水温上升,沉速增大。
S
18
四、沉淀池工作原理 为了便于说明沉淀池的工作原理以及 分析水中悬浮颗粒在沉淀池内运动规律, Hazen和Camp提出了理想沉淀池的概念。 理想沉淀池划分为4个区域,即进口区域、 沉淀区域、出口区域及污泥区域。
19
沉淀试验数据
沉淀时间 t,min Pi=ci/c0 表观去 除率 E=1-Pi u=H/t, cm/min η 0 1 15 0.96 30 0.81 45 0.62 60 0.46 90 0.23 180 0.06
31
解:(1)计算各沉淀时间相应的沉速u, 表观去除率E (2)以Pi为纵坐标,u为横纵标作图得沉淀曲线: P-u曲线 (3)图解计算各沉速下的总去率,u0=3.0为例,小 于此沉速的颗粒与全部颗粒之比P0=0.67, 积分项等于各矩形面积之和。
上澄水 自由沉淀带
水深
絮凝干涉沉淀带
B
成层沉淀带
C
时间t
压缩沉淀D
沉淀过程示意图
10
三、自由沉淀及分析 颗粒为球形
分 析 的 假 定
沉淀过程中颗粒的大小、形状、重量 等不变
颗粒只在重力作用下沉淀,不受器壁和 其他颗粒影响。
静水中悬浮颗粒开始沉淀时,因受重力作用 产生加速运动,经过很短的时间后,颗粒的 重力与水对其产生的阻力平衡时,颗粒即成 等速下沉。
作如下假设 (1) 沉淀区过水断面上各点的水流速度均 相同,水平流速为ν; (2) 悬浮颗粒在沉淀区等速下沉,下沉速 度为u; (3) 在沉淀区的进口区域,水流中的悬浮 颗粒均匀分布在整个过水断面上; (4) 颗粒一经沉到池底,即认为已被去除。
20
沉淀的类型和沉淀形成过程

三、沉淀的类型和沉淀形成过程(一)沉淀的类型沉淀可大致分为晶形沉淀和非晶形沉淀两大类。
非晶形沉淀又称为无定形沉淀或胶状沉淀。
BaSO4是典型的晶形沉淀,Fe2O3·nH2O是典型的无定形沉淀。
AgCl 是一种凝乳状沉淀,按其性质来说,介于两者之间。
晶形沉淀与非晶形沉淀之间虽无绝对界限,但仍有明显差异。
晶形沉淀颗粒大,直径约在0.1~ 1 μm之间,内部排列较规则,结构紧密,易于沉淀和过滤;非晶形沉淀颗粒很小,其直径一般小于0.02 μm,没有明显的晶格,排列杂乱,结构疏松,体积庞大,易吸附杂质,难以过滤和洗净。
凝乳状沉淀的颗粒大小介于两者之间。
在重量分析法中,最好能获得晶形沉淀。
(二)沉淀的形成过程沉淀的形成过程是一个非常复杂的过程,目前仍未有成熟的理论,一般认为在沉淀过程中,首先是构晶离子在过饱和溶液中形成晶核,然后进一步成长按一定晶格排列的晶形沉淀。
构晶离子→晶核→沉淀颗粒→晶形沉淀或无定形沉淀晶核的形成有两种情况:均相成核作用和异相成核作用1. Von Veimarn经验公式Von Veimarn(冯·韦曼)经验公式将沉淀生成的速度(用分散度表示)与溶液的相对过饱和度的关系描述为式中Q表示加入沉淀剂瞬间溶质的总浓度;s表示晶体的溶解度;Q-s为过饱和度;(Q-s)/s为相对过饱和度;K为常数,它与沉淀的性质、温度、介质等有关。
溶液的相对过饱和度越小,则晶核形成速度越慢,可望得到大颗粒沉淀。
2. 均相成核的临界(过饱和)比在均匀的液相中,过饱和的溶质自发的产生晶核的均相成核过程决定于体系的过饱和比SR(supersaturation ratio)。
当溶质的过饱和比很小时,只形成很少的晶核,成核过程以异相成核为主;若SR增大,当达到或超过临界过饱和比CSR(critical supersaturation ratio)时,就会自发地产生大量的晶粒,沉淀反应由异相成核作用转化为既有异相成核作用又有均相成核作用。
水污染控制工程理想沉淀池理论(课堂PPT)

1
第四节 理想沉淀池
前面所述沉淀曲线是静止沉淀试验的结果,虽然它比 较真实地反映了废水中不同的悬浮颗粒沉降的特性,但 是并不能反映实际沉淀池中水流运动对悬浮颗粒沉降的 种种复杂影响。
为了分析悬浮颗粒在沉淀池内运动的普遍规律及分离 结果,哈增和坎普提出了一种概念化的沉淀池——理想 沉淀池。
(措施:需要减小流速或减小水力半径R)
14
②水流稳定性:以弗罗德数Fr判断,Fr表示水 流动能与重力能的比值。增大Fr,可克服股流密 度影响。
注:弗罗德数Fr=v2/gR 一般认为平流式沉淀池Fr宜>105. (措施:需要增大流速或减小水力半径R)
在沉淀池中,增大水平流速,一方面提高了雷诺数 Re而不利于沉淀,但另一方面却提高了弗罗德数Fr而 加强了水流稳定性,从而提高沉淀效果。沉淀池的水 平流速宜进行适当的控制,通常为10-25mm/s。
在沉淀池中纵向分格及斜板(管)沉淀池也能 达到上述目的。
实际应用:
由于实际沉淀池受各种因素的影响,采用沉淀 试验数据时,应考虑相应的放大系数。
1 q设1.25~1.75q0
( 平q均 0 ) 1.5
t设(1.5~2)t0 (平均 1.75t0)
17
第五节 沉淀池
按池内水流方向分类 平流式沉淀池 竖流式沉淀池 辐流式沉淀池 斜板式沉淀池
2
理想沉淀池的假定条件:
① 进出水均匀分布在整个横断面,亦即沉淀池中各进 水断面上各点流速均相同;
② 悬浮物在沉淀过程中以等速下沉; ③ 悬浮物在沉降过程中的水平分速度等于水流速度, 水流是稳定的。
④ 悬浮物落到池底污泥区底部,不再上浮,即被除去
。
3
/长度(L) 高H
水质工程学第4章沉淀与澄清3

——沉淀过程中,清水区高度不断增加
A澄清液层、B受阻沉降层、C过渡层、D压缩层
拥挤沉淀试验
——利用沉淀过程线分析: Kynch 法、 Fitch 法
——建立沉速—浓度函数关系v=f(C) (多筒试验):固体通量法、吉冈法
——作用:用于分析静置沉淀;确定水中悬 浮颗粒的沉降特性
1、自由沉淀试验 2、絮凝沉淀 3、拥挤沉淀(高浓度悬浮液的沉淀试验)
自由沉淀试验
自由沉淀一般采用单筒沉淀柱试验确定悬 浮颗粒的沉降特性。
1)试验装置 2)试验方法 3)沉淀效率η的求取
自由沉淀试验
沉淀柱有效水深H,
悬浮物原始浓度为C0。 在时间t1时从水深H处取样测得C1,则认为沉速大于 u1(H/t1)的颗粒均已通过H,残余颗粒必然具有小 于u1的沉速,则沉速小于u1的颗粒与全部颗粒的比 例x1=C1/C0。
——沉淀时间: 絮凝沉淀
因此,设计沉淀池时,除了对表面负荷率有要 求外,还对停留时间、池深、进出水构造、排泥 方式等均有要求。通常,对于静置沉淀得出的试 验结果,在用于设计时还需考虑一定的安全系数。 一般在设计时:
q=q0/1.25~1.75,T=(1.5~2.0)T0
沉淀池
概述
一、平流式沉淀池 (horizontal flow Sedimentation Tank) 二、竖流式沉淀池 (vertical flow ST) 三、斜板(管)沉淀池(tilted-plate ST) 四、澄清池(clarifier,clarification tank)
概述
沉淀池构造根据功能分为五个区:
进水区: 保证进水均匀分布在整个进水断 面上,避免短流,减少死角和紊流影响,提 高容积利用系数。 出水区: 均匀出水(目的同上),阻拦浮渣 沉淀区: 污水与颗粒分离,工作区 污泥区: 污泥贮放、浓缩、排除 缓冲区: 分隔沉淀区,保证沉下的颗粒不 因水流搅动而再次浮起进入沉淀区。
沉淀基础理论

不同水深处去除率与沉降时间的关系数据
表观去除率/%
5 10 20 30 40 50 60 75
不同水深达到去除率所需的时间/min
0.6 m
1.2 m
1.8 m
1.2
2.5
3.7
2.5
5.0
6.5
6.7
11.0
14.5
11.7
3、难点 图解积分法计算ET
二、絮凝沉降试验及沉降曲线
絮凝沉降的特点:
颗粒的形状d、在沉降过程中改变; 浓度上稀下浓;SS浓度随水深度变化而 变化,且呈现非线性变化。
u随d 而增大。
1.絮凝沉降试验
● 装置:φ140~150mm H=2.0~2.5m 4~5个取样口,间距500mm
● 取样: C0由t=0时中间取样口采集 t1、t2、…、ti、…、tn时,同时从各取样口取水样(两份, 求平均浓度),用以确定不同时间、不同水深处残留的SS 浓度C1、C2、…、Ci、…、Cn。 ● 绘图: 例如:0.5m、1.0m、1.5m处各有一取样口,按设定的 时间序列同时取样,并计算Et。
(1)城市污水处理工艺:
污水 格栅 沉砂池 初沉池 好氧 二沉池 排水
消化 浓缩池
(2)高浓度有机废水处理工艺:
废水 沉淀调节池 厌氧 沉淀池 好氧 沉淀池 排水 脱水 浓缩池
(3)含铬废水处理工艺:
药剂
废水 混合反应池 沉淀池 排水 脱水 浓缩池
第一节 沉降过程的基本理论
根据水中悬浮颗粒的凝聚性能和 浓度,沉淀可分成四种类型
E5
=[0.15×(1-0.8)+0.4×(0.8-0.75)+0.84×(0.75-0.6)+1.6×(0.60.45)]/2.0+0.45
《沉淀基础理论》课件

通过沉淀反应可以检测生物体内的离子、酶活性等,用于医学诊 断和检测。
生物成像技术
利用某些沉淀反应产生的荧光、放射性等特性,可以实现生物成 像技术,用于研究生物体内的生理过程。
在环境科学中的应用
污水处理
利用沉淀法可以去除污水中的重 金属离子、悬浮物等有害物质, 使污水得到净化。
土壤修复
详细描述
分离技术是沉淀基础理论的重要应用领域之一,新型分离技术的开发对于提高生产效率 和产品质量具有重要意义。通过研究沉淀反应的动力学和热力学机制,可以开发出新型 的分离技术,如高效沉淀、膜分离、萃取等。这些新技术能够提高分离效率和降低能耗
,有助于推动相关产业的发展。
绿色化学与可持续发展
总结词
绿色化学与可持续发展是沉淀基础理论 的另一个重要发展方向,旨在实现化学 工业的环保和可持续发展。
过滤法
将沉淀通过滤纸或布氏漏 斗等过滤器材,使固体和 液体分离的方法。
离心分离法
利用离心机的高速旋转产 生的离心力使沉淀分离的 方法。
沉淀的洗涤与干燥
洗涤
用适当的溶剂洗涤沉淀,以除去沉淀表面吸附的杂质。
干燥
将洗涤干净的沉淀进行干燥处理,以备后续操作。
沉淀的纯化技术
结晶法
通过控制结晶条件,使杂质与所需物质分离,得到纯化的沉淀。
分类
沉淀可以根据不同的分类标准进行分 类,如根据沉淀的组成、结构、性质 和应用等。
沉淀的形成过程
溶解度
物质在溶液中的溶解度决定了其在一定条件下能否形 成沉淀。
过饱和状态
当溶液中的溶质浓度超过其溶解度时,就会形成过饱 和状态,导致沉淀的形成。
沉淀剂
通过加入沉淀剂,如电解质、有机溶剂等,可以促进 沉淀的形成。
沉淀的基础理论

沉淀类型
4. 压缩沉淀 压缩沉淀发生在高浓度悬浮颗粒的沉降过程 中,由于悬浮颗粒浓度很高,颗粒相互之间互相 接触,互相支承,下层颗粒间的水在上层颗粒的 重力作用下被挤出,使污泥得到浓缩。二沉池污 泥斗中的污泥浓缩过程以及污泥重力浓缩池中均 存在压缩沉淀。
沉淀的基础理论
学号:140210092 姓名:郝国馨
概述
沉淀:利用水中悬浮颗粒和水的密度差,在重力作 用下产生下沉作用,以达到固液分离的一种过程。
沉淀法可用于以下几个方面:
1. 污水处理系统的预处理
2. 污水的初级处理
3. 生物处理后的固液分离
4. 污泥处理阶段的污泥浓缩沉淀类型1. 自由沉淀
自由沉淀是发生在水中悬浮固体浓度不高时 的一种沉淀类型。在沉淀过程中悬浮颗粒之间互 不干扰,颗粒各自独立完成沉淀过程,颗粒的沉 淀轨迹呈直线。整个沉淀过程中,颗粒的物理性 质,如形状、大小及相对密度等不发生变化。沙 粒在沉砂池中的沉淀就属于自由沉淀。
自由沉淀理论基础
水中的悬浮颗粒,都因两种力的作用而发生运动: 悬浮颗粒受到的重力,水对悬浮颗粒的浮力。 假定: 1. 颗粒为球形 2. 沉淀过程中颗粒的大小、形状、重力等不变 3. 颗粒只在重力作用下沉淀,不受器壁和其他颗粒 影响。
沉淀类型
2. 絮凝沉淀
在絮凝沉淀中,悬浮颗粒浓度不高,但沉淀 过程中悬浮颗粒之间有互相絮凝作用,颗粒因相 互聚集增大而加快沉降,沉淀的轨迹呈曲线。沉 淀过程中,颗粒的质量、形状和沉速是变化的, 实际沉速很难用理论公式计算,需通过试验测定。 化学混凝沉淀及活性污泥在二沉池中间段的沉淀 属絮凝沉淀。
第二讲沉淀理论和沉淀试验

第二讲 沉淀理论和沉淀试验李春杰物理处理法 格栅 沉淀 离心 过滤沉淀的类型自由沉淀• • • • • • • • • • • • • 悬浮固体浓度不高 悬浮固体之间互不干扰 颗粒各自单独进行沉淀 颗粒的沉淀轨迹成直线 颗粒的物理性质,如形状、大小及比重等不发生变化 自由沉淀可用牛顿定律及斯托克斯公式描述。
悬浮颗粒浓度不高(约为50~500mg/L) 悬浮颗粒之间相互碰撞产生絮凝作用 颗粒的粒径与质量逐渐加大 沉降速度不断加快 沉淀的轨迹呈直线 实际的沉速很难用理论公式计算,需通过试验测定 化学混凝沉淀,活性污泥在二次沉淀池中的沉淀。
絮凝沉淀(也称干涉沉淀)沉淀的类型 区域沉淀(或成层沉淀,拥挤沉淀)• 悬浮物颗粒浓度较高(大于500mg/l) • 颗粒的沉降受到周围其它颗粒的影响,沉速大的颗粒也无 法超越沉速小的颗粒,颗粒间相对位置保持不变,形成一 个整体共同下沉,与澄清水之间有清晰的泥水界面。
• 二沉池下部的沉淀过程和污泥浓缩池开始阶段。
压缩沉淀• 区域沉淀的继续,即形成压缩。
• 发生在高浓度悬浮颗粒的沉降过程中,由于悬浮颗粒浓度 很高,颗粒间已挤集成团块结构,相互接触、互相支承, 下层颗粒间的水在上层颗粒的重力作用下被挤出,使污泥 得到浓缩。
• 二沉池泥斗中的浓缩过程以及在浓缩池中污泥的浓缩过程。
单独颗粒的沉降规律2 ⎛ ρ u L s Fd = λ' A⎜ ⎜ 2 ⎝⎞ ⎟ ⎟ ⎠Ff = ρl ⋅V ⋅ gFg = mg = ρ s ⋅ V ⋅ g式中:As——运动方向的面积 λ’——牛顿无因次阻力系数: λ’=f(Re)us——颗粒沉降速度当受力平衡时,沉速变为us (最终沉降速度)对于球形颗粒:⎡ 2 g ( ρ s − ρ L ) ⎛ Vs ⎞⎤ us = ⎢ ⎜ ⎟⎥ ' λ ρL ⎝ A ⎠⎦ ⎣1/ 21 V = πd 3 61 A = πd 2 4⎡ 4 g ( ρ s − ρ L )d ⎤ us = ⎢ ⎥ ' 3 λ ρ L ⎣ ⎦1/ 2λ ='K RenRe =du s ρ Lμ① 层流区(stokes区): ② 过渡流区(艾伦区) ③ 紊流区(牛顿区)λ’=24/Reus =1 ρs − ρL gd 2 18 μ1/ 3λ = 10 / Re'0.5⎡ ( ρ s − ρ L )2 g 2 ⎤ u s = 0.26 ⎢ ⎥ μρ ⎥ ⎢ L ⎣ ⎦dλ = 0 .4'⎡ ( ρ − ρ L )g ⎤ u s = 1.82 ⎢ s ⎥ ρ L ⎣ ⎦1/ 2d 1/ 2当ρs> ρL 时,颗粒以us下沉;当ρs= ρL时, us = 0,颗粒在水中呈悬浮状态,不能用沉淀法去除;当 ρs< ρL时,us为负值,颗粒上浮,可用浮上法去除。
沉淀与上浮

沉淀与上浮[Sediment and Floating] (1)一、沉淀的基本理论(一)沉淀的类型按照水中悬浮颗粒的浓度、性质及其絮凝性能的不同,沉淀可分为以下几种类型。
1.自由沉淀。
悬浮颗粒的浓度低,在沉淀过程中呈离散状态,互不粘合,不改变颗粒的形状、尺寸及密度,各自完成独立的沉淀过程。
这种类型多表现在沉砂池、初沉池初期。
2.絮凝沉淀。
悬浮颗粒的浓度比较高(50~500mg/L),在沉淀过程中能发生凝聚或絮凝作用,使悬浮颗粒互相碰撞凝结,颗粒质量逐渐增加,沉降速度逐渐加快。
经过混凝处理的水中颗粒的沉淀、初沉池后期、生物膜法二沉池、活性污泥法二沉池初期等均属絮凝沉淀。
3.拥挤沉淀。
悬浮颗粒的浓度很高(大于500mg/L),在沉降过程中,产生颗粒互相干扰的现象,在清水与浑水之间形成明显的交界面(混液面),并逐渐向下移动,因此又称成层沉淀。
活性污泥法二沉池的后期、浓缩池上部等均属这种沉淀类型。
4.压缩沉淀。
悬浮颗粒浓度特高(以至于不再称水中颗粒物浓度,而称固体中的含水率),在沉降过程中,颗粒相互接触,靠重力压缩下层颗粒,使下层颗粒间隙中的液体被挤出界面上流,固体颗粒群被浓缩。
活性污泥法二沉池污泥斗中、浓缩池中污泥的浓缩过程属此类型。
(二)悬浮物在静水中沉淀的理论1.沉速公式为了说明影响颗粒沉淀的主要因素,现以单体球形颗粒的自由沉淀为例加以说明。
颗粒在重力、浮力的作用下,开始下降(或上浮),由于水的阻力作用下,短暂时间内很快当达到受力平衡,以匀速下沉。
在大多数情况下,Re<1,颗粒下降引起周围水流的扰动,处于层流状态。
颗粒沉淀速度用斯托克斯(Stokes)公式表示。
水中悬浮物的组成比较复杂,颗粒形状多样,且粒径不均匀,密度也有差异,很难用斯笃克斯公式计算颗粒的沉速,而通过试验测定颗粒的沉速比较容易。
因此公式主要用来进行沉淀原理分析和测出颗粒沉速后倒过来进行水中颗粒分析用。
2.沉淀试验沉淀试验用来判定水中颗粒的沉淀性能,并根据所要求的沉降效率确定沉降时间和沉降速度这两个基本的设计参数。
水污染控制工程沉淀的基础理论

1 1 3 2 V d , A d 6 4
得球状颗粒自由沉淀的沉速公式:
4 g ( s L ) d 12 uS [ ] 3 L
式中λ′是雷诺数Re的函数 当
Re
dup
24 Re 1, Re 10 2 Re 500, Re 5 500 Re 10 , 0.44
污水的物理处理
污水的物理处理
污水的物理处理
污水的物理处理
污水的物理处理
3、沉淀池表面负荷与颗粒沉降速度的关系 (1)表面负荷:如果沉淀池沉降区的表面积为A, 处理水量为Q,则有:
H H H B Q u0 q0 t L LB A
上式中的Q/A是沉淀池设计的一个重要参数,称 为表面负荷,以q0表示,其单位是m3/m2· h。
X—城市污水的沉砂量,一般采用30m3/106m3污水 T—排砂时间的间隔,d kz—生活污水流量的总变化系数
5、贮砂斗各部分尺寸计算 设贮砂斗底宽b1=0.5m;斗壁与水平面的倾角为 600;则贮砂斗的上口宽b2为:
2h3 b2 b1 0 tg 60
贮砂斗的容积V1:
1 V1 h3 ( S1 S 2 S1 S 2 3
h′3—贮砂斗高度,m
S1,S2—分别为贮砂斗上口和下口的面积
6、池总高度h
h h1 h2 h3
h1—超高,m
7、核算最小流速vmin
min
Qmin n1 Amin
Qmin—设计最小流量,m3/s n1—最小流量时工作的沉淀池数目 Amin—最小流量时沉砂池中的水流断面面积,m2
假设:(1)颗粒为球形,不可压缩,也无凝聚 性,沉降过程中其大小、形状和质量等均不变; (2)水处于静止状态; (3)颗粒沉降仅受重力和水的阻力作用。 静水中颗粒在重力作用下,在水中加速下沉,直 到作用与颗粒的推力与水的阻力达到平衡时,颗粒开 始以等速下沉。平衡状态是开始沉淀后瞬时达到的。 1、悬浮颗粒在水中受到的推力Fs
沉淀理论 ppt课件

F3
A
L
u2 2
式中:λ—阻力系数,当颗粒周围绕流处于
层流状态时, λ=24/Re;Re为颗粒绕流雷偌
数,与颗粒的直径、沉速、液体的粘度等有
关,
Re udL
A—自由沉淀颗粒在垂直面上的投影面积,
A 1 d 2
4 15
颗粒下沉开始时,沉速为0,逐渐加速,
阻力F3也随之增加,很快三种力达到平衡,颗 粒等速下沉,du/dt=0,代入公式:
为了便于说明沉淀池的工作原理以及分析 水中悬浮颗粒在沉淀池内运动规律, Hazen和Camp提出了理想沉淀池的概念。 理想沉淀池划分为4个区域,即进口区域、 沉淀区域、出口区域及污泥区域。
19
作如下假设
(1) 沉淀区过水断面上各点的水流速度均 相同,水平流速为ν;
(2) 悬浮颗粒在沉淀区等速下沉,下沉速 度为u;
u—颗粒沉速,m/s;
t—沉淀时间,s;
F1—颗粒的重力 F2—颗粒的浮力 F3—颗粒沉淀过程中受到的摩擦阻力。
13
(1)颗粒的重力:
F1
d3
6
S
g
其中:ρS为颗粒密度,kg/m3; d为颗粒直径,m;
g为重力加速度。
(2)颗粒的浮力:
F2
d3
6
L
g
其中:ρL为液体密度,kg/m3;
14
(3)颗粒沉淀过程中受到的摩擦阻力:
6
2、絮凝沉淀
这是一种絮凝性固体颗粒 在稀悬浮液中的沉淀。
虽然悬浮固体浓度也不高 (50-500mg/L),但颗粒在沉 降过程中接触碰撞时能互相聚 集为较大的絮体,因而颗粒粒 径和沉降速度随沉降时间的延 续而增大。
实例:颗粒在初 沉池内的后期 沉降,生化处 理中污泥在二 沉池中间段的 沉淀,及水处 理的混凝沉淀。
沉淀的基础知识

沉淀理论(Gravity Separation Theory )一、分类根据悬浮物质的性质、浓度及絮凝性能,范围,沉淀可分为:1.自由沉淀(Discrete particle settling):悬浮物质浓度不高,在沉淀过程中颗粒之间互不碰撞,呈离散状态,各自独立地完成沉淀过程。
颗粒形状、尺寸、质量不变。
如沉砂池中砂粒沉淀、浓度低的污水在初沉池中的沉淀。
2.絮凝沉淀(干扰沉淀, Flocculent Settling ):悬浮物浓度在50~500mg/l ,颗粒间可能互相碰撞产生絮凝作用,使粒径与质量加大,沉速不断加快。
如初沉池沉淀,活性污泥在二沉池沉淀上部沉淀以及化学混凝沉淀。
3.拥挤沉淀(分层沉淀, Hindered settling, Zone settling ):浓度>500mg/l ,沉淀中相邻颗粒互相妨碍、干扰,沉速大的颗粒无法超越沉速小的颗粒,各自保持相对位置不变,并在聚合力的作用下,颗粒群结合成一个整体向下沉淀,清水与浑水间形成明显的交界面,沉淀显示为界面下沉。
如二沉池下部的沉淀过程及浓缩池开始阶段。
4.压缩沉淀(Compression settling ):浓度大。
颗粒间互相支承,上层颗粒在重力作用下,挤出下层颗粒的间隙水,使污泥得到浓缩。
如活性污泥在二沉池的污泥斗中及浓缩池中的浓缩过程。
活性污泥在二沉池中沉淀实际是依次进行,只是各类沉淀出现时间不同。
二、颗粒沉淀理论(Particle Settling Theory)1.公式根据牛顿第二定律,得出颗粒最终沉速为:d C g u ll s D ρρρ-=34 粒径有关阻力系数,与液体密度颗粒密度----d C D l s Re ρρ在不同流态下阻力系数C D 以及沉速u 的表达公式:2.应用(1)已知d,推求u=?(2)已知u,反推d=?三、各种沉淀类型分析(一)自由沉淀1.低浓度离散性颗粒在水中沉淀,开始时加速下沉,水流阻力不断增加,短暂时间后达到与重力平衡,颗粒开始匀速下沉。
水解酸化+好氧+2沉淀_理论说明

水解酸化+好氧+2沉淀理论说明1. 引言1.1 概述本文探讨了水解酸化+好氧+2沉淀的处理工艺,在污水处理领域中得到广泛应用。
该工艺通过结合水解酸化、好氧降解和二次沉淀等步骤,能够高效地去除废水中的有机物、氮、磷等污染物,并实现废水的净化与回用。
本文将从定义和原理、操作参数与影响因素、以及应用扩展和发展趋势三个方面对该工艺进行详细论述。
1.2 文章结构本文共分为五个主要部分。
引言部分为第一部分,主要对文章的研究内容和结构进行简要介绍。
第二部分将深入讨论水解酸化过程,包括其定义和原理、操作参数与影响因素,以及应用扩展和发展趋势。
第三部分将重点关注好氧处理过程,包括好氧降解机理、工艺流程与条件优化,以及好氧处理效果评估及案例分析。
接着,在第四部分中详细介绍二次沉淀过程,包括背景介绍与目标设定、操作步骤及工艺参数控制要点,以及沉淀效果与后续处理措施研究。
最后,在第五部分中给出结论,总结本文的研究内容和发现,并评估其在实际应用中的意义和推广价值。
此外,本文还会提出未来需要进一步研究和改进之处的建议与展望。
1.3 目的本文旨在系统地介绍水解酸化+好氧+2沉淀处理工艺,并对其进行详细阐述。
通过对水解酸化、好氧降解和二次沉淀等关键环节的探索和分析,本文将为相关领域的研究者提供有价值的参考和指导。
同时,对该工艺在实际应用中的意义和推广价值进行评估,为废水处理行业提供技术支持,并为未来研究和改进提供展望。
2. 水解酸化2.1 定义和原理水解酸化是一种常用的废水处理方法,通过在中性或弱碱性条件下将废水中的有机物质通过水解反应转化为可溶性有机酸,从而实现废水的预处理和降解。
该过程主要利用了微生物和酶类等生物催化剂的作用。
在水解酸化过程中,废水中的有机物质首先被分解为较小的分子,如蛋白质被水解成氨基酸,淀粉被分解成糖类。
这些小分子进一步代谢为有机酸,如乙酸、丁酸等。
整个过程是一个逐步降解有机物质的过程。
2.2 操作参数与影响因素水解酸化过程中涉及到许多操作参数和影响因素。
沉淀与絮凝Ⅱ

沉淀理论
拥挤沉淀 在高颗粒浓度下,颗粒间的斥力会干扰 沉淀过程。并且,也没有空间让流体流过颗 粒周围,从而阻碍颗粒的沉淀。
沉淀池的典型设计
停留时间(h) 表面负荷 (m3/m2· d) 2~4 20~40 0.75~1.5 1.5~2.5 1.5~2.5 2~3 60 30~50 24~32 16~28
R
C 0 Ci C0
100%
沉淀理论
絮凝沉淀实验
纵坐标为取 样口深度,横坐 标为取样时间, 将同一沉淀时间, 不同深度的去除 率画点,然后把 去除率相等的各 点连接成等去除 率曲线。
沉淀理论
絮凝沉淀实验 任给一个tn和hn,可以算出来一个沉降 速度vn,大于等于vn的颗粒都会被去除,小 于vn的颗粒v的去除率为v/vn。对于特定时 间t去除率也为h/hn。
絮凝的概念
ቤተ መጻሕፍቲ ባይዱ
脱稳的胶体或微小悬浮物聚集成大的 絮凝体的过程。 要使两个完全脱稳的胶体颗粒聚集成 大颗粒絮体,需要给胶体创造互相碰撞的 机会。 创造碰撞的动力有两种:一是布朗运 动;二是外力推动作用。
布朗运动(异向絮凝)
胶体颗粒的布朗运动是无规则的,每 一个脱稳的胶体颗粒可能不规则的向各个 方向运动,也可能同时受到来自各个方向 的颗粒的碰撞,两个胶体颗粒向不同的方 向运动而发生碰撞聚集。 布朗运动随颗粒粒径的增大而逐渐减 弱,当颗粒粒径大于0.5μ m时,布朗运动 不再起作用。
搅拌(同向絮凝)
当布朗运动不起作用时,需要外力来 推动流体运动,如在机械搅拌、水力等外 力作用下产生的流体运动推动脱稳的胶体 颗粒,使所有胶体颗粒向同一方向运动。 由于不同胶体颗粒存在速度快慢的差 异,速度快的胶体颗粒将赶上速度慢的胶 体颗粒。 如果两个胶体颗粒在垂直方向的球心 距离小于它们的半径之和,两个胶体颗粒 将会碰撞聚集而发生絮凝。
第二节沉淀的生成和溶解详解

当判断两种溶液混合后能否生成沉淀时, 可按下列步骤进行。
(1) 先计算出混合后与沉淀有关的离子浓度;
(2) 计算出浓度积Qc; (3) 将Qc与Ksp进行比较,判断沉淀能否生成。
例1 将20.0mL 0.0010mol/L的CaCl2溶液与30.0mL 0.010 mol/L 的 KF 溶 液 混 合 后 , 有 无 CaF2 沉 淀 ? 已 知 Ksp(CaF2) =1.5×10-10
则 BaSO4(s) 平衡
Ba2+ + SO42x 0.1+ x
x ·0.10 = 1.08×10-10
≈ 0.1 mol ·l-1
x = 1.08×10-9 mol ·l-1
一般认为:残留在溶液中的被沉淀离子的浓度< 10-5 或10-6时,通常认为该离子已经沉淀完全了。
应用溶度积规则判断沉淀的生 成在实际应用过程中应该注意:
= 1.4×10-8
∵Q>Ksp
∴有CaF2沉淀析出。
例2 将100mL 2.0×10-4mol/L的BaCl2溶液和100mL 1.0×10-3 mol/L的K2CrO4溶液混合,试问混合后 ⑴ 达平衡时溶液中的Ba2+离子浓度是多少? ⑵ 生成BaCrO4沉淀多少克? 已知Ksp(BaCrO4)=1.17×10-10
第二节 沉淀的生成和溶解
一、沉淀的生成 (QC >Ksp)
根据溶度积规则,在一定温度下,难溶 电解质形成沉淀的必要条件是QC >Ksp 。因 此要使某物质以沉淀方式从溶液中析出,必 须设法增大有关离子浓度,使其离子浓度幂
的乘积大于该难溶电解质的溶度积,平衡就
向生成沉淀方向移动。通常采用的方法是加 入适当的沉淀剂。
⑵ BaCrO4的摩尔质量为253g/mol,所以BaCrO4的沉淀量 m=(1.0×10-4-x) ×(200/1000) ×253 ≈ 5.0×10-3g
稀土沉淀理论计算
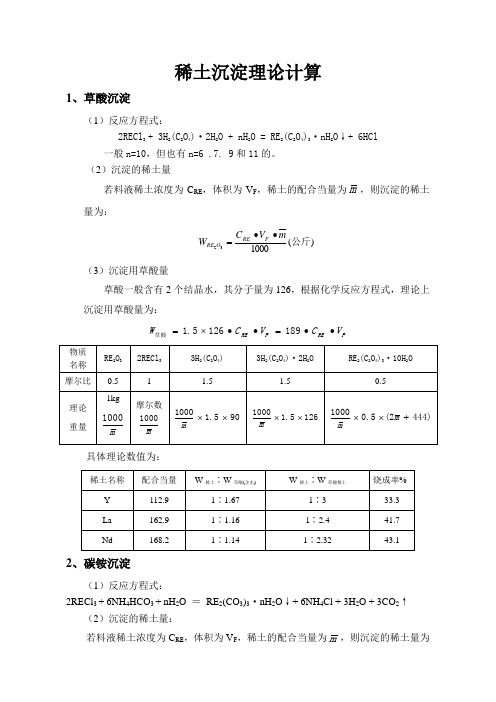
稀土沉淀理论计算1、草酸沉淀(1)反应方程式:2RECl 3 + 3H 2(C 2O 4)·2H 2O + nH 2O = RE 2(C 2O 4)3·nH 2O ↓+ 6HCl 一般n=10,但也有n=6 .7. 9和11的。
(2)沉淀的稀土量若料液稀土浓度为C RE ,体积为V F ,稀土的配合当量为m ,则沉淀的稀土量为:)(100032公斤mV C W F RE O RE ••=(3)沉淀用草酸量草酸一般含有2个结晶水,其分子量为126,根据化学反应方程式,理论上沉淀用草酸量为:F RE F RE V C V C W ••=••⨯=1891265.1草酸具体理论数值为:2、碳铵沉淀(1)反应方程式:2RECl 3 + 6NH 4HCO 3 + nH 2O = RE 2(CO 3)3·nH 2O ↓+ 6NH 4Cl + 3H 2O + 3CO 2↑(2)沉淀的稀土量:若料液稀土浓度为C RE ,体积为V F ,稀土的配合当量为m ,则沉淀的稀土量为)(100032公斤mV C W F RE O RE ••=(3)沉淀用碳铵量:萃取分离出口稀土料液一般呈酸性,用碳铵沉淀时,沉淀用碳铵量为中和[H +]用量和沉淀RE 3+用量之和。
① 中和[H +]用碳铵量: 中和反应方程式:HCl + NH4HCO3 = NH4Cl + CO2↑+ H2O[])公斤(1000][34pmC V W HF HCO NHH •••=++(其中C [H+]为溶液酸度、m 为NH 4HCO 3分子量79、P 为NH 4HCO 3含量0.9294)。
② 沉淀RE 3+用碳铵量:)公斤(793343pC V W REF HCO NH RE••⨯=+(其中C RE 为溶液稀土浓度、m 为稀土的配合当量、79为NH 4HCO 3分子量,P 为NH 4HCO 3含量0.9294)。
具体理论数值为:。
沉淀理论-ppt课件

d
P 1 u0
P0udP
0
而沉淀池能去除的颗粒包括u≥u0以及 u<u0的 两部分,故沉淀池对悬浮物的总去除率为:
(1P0)u10
P0udP
0
24
η
1 0.9
0.8 0.7
0.6 0.5 0.4
0.3 0.2
0.1 0
0 0.67 1.33 2 2.67 4
8
u,cm/min
不同沉淀速度的总去除率
qvu0(L/H )H bu0A
u0 qv /A
qv/A—反映沉淀池效力的参数, 一般称为沉淀池的表面负荷率,
或称沉淀池的过流率,用符号q H
表示:
qqv / A
v
u0
L
27
比较两式可知: u0 qv/A
qqv / A
理想沉淀池中,u0与q在数值上相同,但它们 的物理概念不同:
u0的单位是m/h;q表示单位面积的沉淀池 在单位时间内通过的流量,单位是m3/m2·h。 故只要确定颗粒的最小沉速u0,就可以求得理 想沉淀池的过流率或表面负荷率。
(3) 在沉淀区的进口区域,水流中的悬浮 颗粒均匀分布在整个过水断面上;
(4) 颗粒一经沉到池底,即认为已被去除。
19
当某一颗粒进入沉淀池后
一方面随着水流在水平 方向流动,其水平流速
v等于水流速度;
另一方面,颗粒在重力 作用下沿垂直方向下沉, 其沉速即是颗粒的自由
沉降速度u。
颗粒运动的轨迹为其水平分速v和沉速u的矢量和,在 沉淀过程中,是一组倾斜的直线,其坡度为i=u/v。
30
解:(1)计算各沉淀时间相应的沉速u,
表观去除率E
(2)以Pi为纵坐标,u为横纵标作图得沉淀曲线: P-u曲线
物理处理(2沉淀)

初沉池后期、二沉池前期、给水混凝沉淀
区域沉淀(成层沉淀,拥挤沉淀)
颗粒浓度大(>500mg/L),相互间发生干扰, 分层 。 水与颗粒群之间形成一个清晰的界面, 沉降过 程实际上是该界面的下沉过程。
高浊水、二沉池、污泥浓缩池
压缩沉淀
颗粒间相互挤压,下层颗粒间的水在上层颗粒 的重力下挤出,污泥得到浓缩。
3.2 沉淀的基础理论
思考题 概述 沉淀类型 理想沉淀池原理
思考题
沉淀法在污水处理厂有哪几种用法? 沉淀类型有哪几种?各有什么特点? 实际沉淀池与理想沉淀池存在什么误差?
3.2.1 概述
沉淀法是水处理中最基本的方法之一。它是利用水中 悬浮颗粒的可沉降性能,在重力作用下产生下沉作用, 以达到固液分离的一种过程。 按照废水的性质与所要求的处理程度的不同,沉淀处 理工艺可以是整个水处理过程中的一个工序,亦可以 作为唯一的处理方法。 在典型的污水厂中,有下列四种用法:
C0 Ci 100 % C0
以沉淀时间为横坐标,去除率为纵坐标绘制曲线图(图(a)); 以沉淀速度为横坐标,去除率为纵坐标绘制曲线图(图(b)) 当已知沉淀时间,或已知要去除的颗粒沉速,即可在曲线上查得去除率, 或反之。
C0 Ci 100 % C0
H i ti
第二篇 城市污水处理
3 污水的物理处理(12h)
4 污水的生物处理(16h) 5 污水的生物处理(二)(4h) 6 污水的自然生物处理(2h) 8 污泥处理(2h) 9 污水处理厂设计(2h)
3 污水的物理处理
(2)沉淀理论培训
2.1.3 沉淀类型
种类 悬浮物浓度 固体颗粒 不碰撞, 不具有絮 凝特征
碰撞,有 凝聚特性 互相干扰 污泥沉淀 高
沉淀过程特征
应用
沉砂池初沉 池前期
自由沉淀
低
不改变尺寸、形状 不互相粘合
絮凝沉淀
不高 50~500mg/L
改变尺寸形状
絮凝反应池 二沉池后期
沉速下降、颗粒分层
压缩沉淀
很高
互相接触、 支撑
为了提高除铬效果,应投加过量的碳酸钡,反应 时间应保持25—30min。投加过量的碳酸钡会使 出水中含有一定数量的残钡。在回用前可用石膏 法去除: CaSO4+Ba2+ ⇌ BaSO4↓+Ca2+
2 沉淀理论
2.1 概述 2.1.1 沉淀:水中的可沉固体物质在重力作用下下 沉,从而与水分离的过程。 2.1.2 沉淀功能: ① 用于一级处理去除杂质、颗粒物质 ② 用于二级处理 初次沉淀池,减轻后续处理设施的负荷 二次沉淀池,分离去除生物污泥 ③ 用于灌溉或氧化塘稳定水质去除水中虫卵或 固体颗粒
自由沉淀的沉淀实验,沉淀曲线 1.第一种实验 ① 污水搅拌均匀注入n个沉淀筒(沉淀筒的大小d=80mm, h=1500~2000mm),测量悬浮物浓度C0; ② 经过t1 、t2……tn-1、 tn沉淀时间后,分别从各沉淀筒的一定高度H处 (1200mm)取同样样品,分别测C1 、C2…… Cn-1、Cn; ③ 计算各沉淀时间的沉淀效率和沉淀速度u
H u i ti E C 0 C i 100% Ci
④ 绘制沉淀效率曲线(E~t)
2.第二种实验
① 污水搅拌均匀后注入n个沉淀筒,经过t1 、t2……tn-1、 tn时后取 H段以上的全部水样,测水样中悬浮物浓度C1 、C2…… Cn-1、Cn; ② ut ≥u0=H/t,去除率η1 ut < u0,但取样面附近η2 ∴η=η1+η2 令u0——某一特定沉速 P0——ut ≥u0时,颗粒与悬浮颗粒总量之比,即悬浮物剩余量 C P0 i C0 ③ 对ut < u0的每一种颗粒,去除 各种不同粒经
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
作沉淀速度与沉淀率的曲线:(该曲线抵消了取样高度对结果的影响)
80
去除率(%)
100 80
E (%)
60 40 20 0 0 0.05 0.1 0.15 0.2 0.25 沉淀速度(mm/s) u0
60 40 20 0 0 20 40 60 80 100 120 140 沉淀时间(min)
沉淀速度与沉淀效率
淀需要多点取样,计算方法与前相似)
絮凝沉淀试验:(其具体实验方法见教材 P66页,
计算方法见教材P67页例 3-3。)
(1)每隔一定时间(10min)从各取样口同 时取样。求各自的SS去除率,并作出各取样 口去除率与沉淀时间曲线
去 除 率 %
沉淀时间 0.25 0.5 1.0 1.5
0.25 0.50 0.75 1.00 1.25 1.5 1.75
U0
Ui 则: U 0
考虑颗粒的粒径分布,则沉速<U0的所有颗粒的去除率:
p0
Ui 1 dp U0 U0 0
p0
U dp
i 0
沉淀时间内颗粒总去除率:
沉速 U0 的颗粒去除率:
E=1-P0
p0
沉速 <U0 的所有颗粒的去除率 :
Ui 1 dp U0 U0 0
p0
U dp
i 0
2.0
0 10 20
例如求沉淀时间 30min,深度2m处的 总去除率。
1)先计算 U0=H/t=2/30=0.067m/min,沉速大于等 于U0的颗粒去除率 45%。 2)再计算沉速小于U0颗粒的去除率,作图法。
U1 U 1.81/ 30 0.5 / 30 (60 45) 2 (75 60) (60 45) (75 60) U0 U0 0.067 0.067
15% 30%
45%
60%
75%
m)
1.75
2.0 0 10 20 30 40 50 60 (min)
自由沉淀作业:
作业 1 :水中离散颗粒静止沉淀实验数据如下表。 实验取样点水深为 120cm ,表中 C 代表在沉淀时 间t时由取样口取样中的悬浮物浓度,C0代表起始 的悬浮物浓度。求沉淀速度为 0.6mm/s 时颗粒的 总去除率。
E (1 p0 )
Ut pi U0
3)计算总去除率:45%+
U1 U 1.81/ 30 0.5 / 30 (60 45) 2 (75 60) (60 45) (75 60) U0 U0 0.067 0.067
0
深 度 (
0.25
0.5 0.75 1.0 1.25 1.5
求:当沉速为U=2.5mm/s的总沉淀率。
解:1)作Ci/C0—沉速曲线: 求出P0=0.56,1-P0=0.44
Ci p0 C0 0.7
(沉速 2.5mm/S颗粒比例)
剩 0.6 余 量 0.5 0.4
2 ) 作 图 求 解 沉 速 <U0 (2.5mm/S)颗粒的沉淀率。
0.5 1.0 1.5 2.0 2.5 3.0 3.5mm/s 沉速 Ut
2.00
( 2)找出各深度处同样去除率所经历的时 间(作等去除率曲线)
(2)找出各深度处同样去除率所经历的时间 (作等去除率曲线)
0
深 度 (
0.25 0.5 0.75 1.0 1.25 1.5 1.75 2.0 0 10 20 30 40 50
15% 30%
45%
75%
m)
60%
60 (min)
F2
F1
F2
颗粒沉降过程的受力分析:
F1 重力;
F2 浮力;
F1
F3
d 3
6
g g
F2
d3
6
g y
d
4
2
F3 摩擦阻力:
F3 c
y
u 2
2
F1
颗粒下沉条件:F1>F2, g>y, d—颗粒直径(m), g—m/s2, u—沉速(m/s), c—阻力系数
F1
可用牛顿第二定律及斯托克斯公式描述 in grit chamber & primary setting tank.
80 60 40 20 0 0 0.05 0.1 0.15 0.2 0.25 沉淀速度(mm/s)
再根据实验结果作的 关系曲线,求沉速小于U0的颗 粒的去除率: 1 U p
p0 0
Ci U C0
U0
t
两部分相加,得总去除率:
1-P0 +
1 U0
U
0
p0
t
p
例题:某城市污水,含有的悬浮物质浓度不高, 而且为非凝聚性,进行静止沉淀实验,取得以 下数据,实验用量筒的取样高度为1.2m 。取得 的静态沉淀试验数据如下:
d cu 2 再整理: g ( g y ) y 3 4
沉速u: u 4 g ( g y ) d 1/ 2 3 c y
4 ( g y ) 1/ 2 u g d 3 c y
F2 F3
在层流状态下,阻力系数:
c 24 Re
Re
du y
c
1/ 2
24 24 Re du y
1/ 2
F1
4 du y g y u g ( )d y 3 24
1 ( g y ) 2 gd u 18
两边同时平方:
1 ( g y ) 2 u gd u 18
沉淀时间内颗粒总去除率:
Ui 1 0 (1 p0 ) dp (1 p0 ) U t dp U0 U0 0 0
p0
p
该式中 第1项可由前述实验方法,用沉速—沉淀率曲线求出, 第2项需修改实验,再整理资料,作图求得。
去除率(%)
先求沉速U0颗粒的去除率: E=1-P0=(C0-Ci)/C0
d 3
6
g g
F2
d3
6
g y
u2 F3 c y 4 2
d 2
F2 F3
颗粒下降过程的力平衡分析:颗粒匀速下 沉时,力平衡方程:F1=F2+F3
d 3
6
g g
d 3
6
g y c
d 2
u2 y 4 2
F1
简化:
d d cu 2 g g y g y 3 4 3
由于假定条件,Stokes’
F3
F1
law应用的局限性。
所以,对于实际污水(颗粒非球形) ,颗粒的沉淀性能、 颗粒沉速需进行修正,一般通过实验确定。
3.自由沉淀试验及沉淀曲线
用已知SS浓度C0的污水,灌满5-6个沉淀筒(1.5-2.0m),这 些沉淀筒在同一高度H处有一取样口。每隔一定时间段,依 次从量筒中取一定量(100mL)污水。 绘制沉时—沉淀效率曲线:
(3)求沉淀率: (仍然是大于等于U0与小于U0两部分之和)
先计算UtU0的颗粒去 0
除率,再计算UtU0的
颗粒去除率。
75%
深 度 (
0.25 0.5 0.75 1.0 1.25 1.5 1.75
15% 30%
45% 60%
E (1 p0 )
Ut pi U0
m)
例如求沉淀时间 30min,深度2m处 的总去除率。 30 40 50 60 (min)
依据可沉物质的性质、浓度、凝聚性能,分为:
1) 自由沉淀 ( Discrete settling):
2) 絮凝沉淀(也称干涉沉淀) (Flocculant settling) 3) 成层沉淀(区域沉淀,拥挤沉淀) (Zone settling / Hindered settling)
4) 压缩沉淀 (Compression settling)
3.3 沉淀理论
Settling Theory
* Sedimentation / Settling * Sedimentation tank / clarifier / settling basin or tank
1. 沉淀的类型
Types of sedimentation in wastewater treatment
沉淀时间与沉淀效率
沉速-去除率曲线仍有不足之处
在设计沉淀时间内,大于等于设计 沉速( u0 )的颗粒可全部通过取样 界面(即全部沉降),这部分颗粒 沉淀效率可在Et-Ut曲线上查出。而 对于沉速小于设计沉速 u0 的颗粒, 实际上可部分去除(靠近取样界面 的颗粒可去除),但由于实验时取 样的关系(以局部少量水样代替 H 界面以上全部水样),这部分沉速 小于设计沉速 u0 的颗粒的去除率没 有从实验数据上反映出来。即Et-Ut 曲线并不包括这部分去除率,使得 计算去除率小于实际去除率。
2
1 (g y ) u gd 2 18
The equation is Stokes’ law.
根据Stokes’ law分析颗粒沉降性能:
1 (g y ) u gd 2 18
F2
u g, , y , d2 • g > y --- u >0, particle ; d, udown • g < y --- u<0, particle; d, uup • g = y --- u=0, particle suspending • -- u; • Temp. --- u ;
t1
H
t2
t3
t4
t5
E (%)
100 80 60 40 20 0 0 20 40 60 80 100 沉淀时间(min) 120 140
