原辅料及包材相容性试验
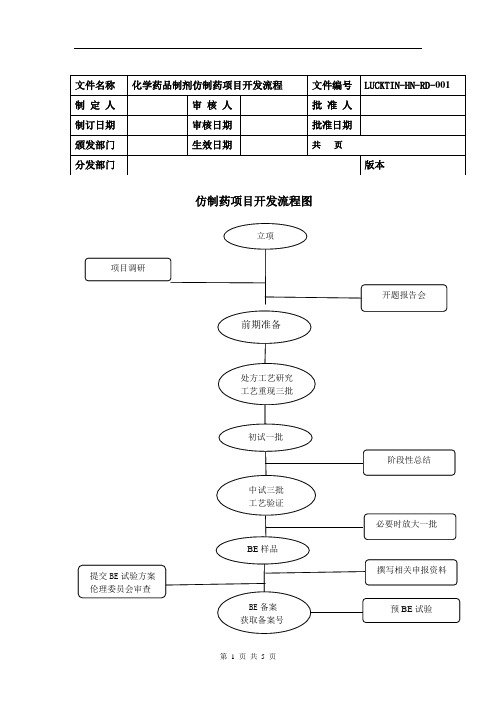
仿制药详细研发流程
3)工艺研究:是否微粉化,制粒是干法、湿法、直接压片、包衣目的等
4)方法
常规方法:重量、水分测定、HPLC等
仪器分析:X-光衍射、扫描电镜
四
处方工艺研究
工艺参数研究
1、处方工艺摸索:
1)辅料相容性试验
2)处方筛选
3)工艺参数研究
2、小试验证三批
1)固体口服制剂可用A01、A02.....
2)液体口服可用B01、B02.........
3)注射剂可用C01、C02...........
4)医疗器械可用D01、D02....等)
1)三批重现性样品
2)验证工艺
3、初试一批
1)样品全检
2)工艺参数验证
4、中试三批
1)三批全检
2)用于稳定性考察
5、注册三批(BE)
五
质量研究1Leabharlann 质量研究方法的确定(初试、中试样品)
2、质量标准的方法学验证
1)质量标准的初步验证(对照品、杂质、原料、参比、小试)
2)系统的方法学验证(初试、中试样品)
1、综述资料
2、药学研究资料
3、药理毒理研究资料
4、BE试验资料
九
向省局提交注册申请
1、省局形式审查
2、省局现场核查(研制现场、生产现场、临床试验现场)
十
资料移交总局
2、总局审评中心审评
2、总局审评过程或有因的核查和抽样检验
十一
完整性审评
1、补充后续稳定性资料
2、完整性通过
十二
批准上市
1、售后
说明:
1、原辅料检验(原料研究溶解性、晶型、粒径、水合物、
药品与药包材相容性研究方法探索和应用举例

收集有关的药包材信息
直接与药品接触的药包材信息(初级包装) 基本信息: 药包材名称(标准名称) 材质/规格/型号/生产商(供应商) 注册证/执行的标准/材料成分表 样品信息: 批号/生产商COA/自检COA 重点关注:外包装/预处理工艺;有关的 次级包装 必要时追踪:管制瓶的玻璃管供应商/塑 料瓶、盖、接口等的粒料供应商/胶塞的 原料胶的供应商;提供证明和有关资料。
1999
2005
国外主要参考资料(二)
学术机构/协会 内容 PDA PDA J Pharm Sci and Tech ;Technical (美国注射剂协会) Reports
PQRI SAFETY THRESHOLDS AND BEST PRACTICES FOR (美国产品质量研究 EXTRACTABLES AND LEACHABLES IN ORALLY 协会) INHALED AND NASAL DRUG PRODUCTS (OINDP) 2006 Parenteral and Ophthalmic Drug Products (PODP) Leachables and Extractables Working Group 2009
分配平衡
吸附
接触界面
药品的安全性评价
药+包装=药品 商品
药(API) 安全性评价 急性毒性 长期毒性 致畸性 致癌性 致突变 生殖毒性 刺激性 溶血性 药包材 安全性评价 材料生物相容性 (药包材依据)
药物制剂 + 合适的包装 = 安全使用
铁桶包装物相容性实验报告结论

铁桶包装物相容性实验报告结论药包材对保证药品的稳定性起着重要作用,因而药用包装材料将直接影响用药的安全性。
直接接触药品的包装材料、容器是药品的一部分,尤其是药物制剂中,一些剂型本身就是依附包装而存在的(如气雾剂等)。
由于药品包装材料、容器组成配方、所选择的原辅料及生产工艺的不同,导致不恰当的材料引起活性成分的迁移,吸附甚至发生化学反应,使药物失效,有的还会产生严重的副作用。
这就要求在为药品选择包装容器(材料)之前,必须检验证实其是否适用于预期用途,必须充分评价其对药物稳定性的影响,评定其在长期的贮存过程中,在不同环境条件下(如温度、湿度、光线等),在运输使用过程中(如与药物接触反应,对药物的吸附等)、容器(材料)对药物的保护效果和本身物理、化学、生物惰性,所以在使用药包材之前需做相容性试验。
药包材与药品相容性试验的原则(一)、药物在选择药包材材料、容器时,应首先考虑其保护功能,然后考虑材料、容器的特点和性能,包括化学、物理学、生物学、形态学等性能。
(二)、药包材应具有良好的化学稳定性、较低的迁移性、阻氧、阻水、抗冲击、无生物意义上的活性、微生物数在控制范围内、与其它包装物有良好的配合性、适合于自动化包装设备等。
(三)、在评价之前药包材与药物应符合有关标准。
(四)、药包材与药物相容性试验应考虑以下几个方面:1、形成包装单元时,各包装物应有良好的配合性。
2、包装单元形成时,能适合特定的包装设备。
3、包装中的药物,能通过药物稳定性试验的所有项目。
4、药包材根据生产工艺要求耐受特殊处理的能力(如钴60消毒等)5、同一包装单元中首次至末次使用保证药物的一致性。
6、对恶劣运输、不同贮存环境的抵抗能力。
(五)、所有试验都应根据具体的包装形式和药物,设计试验方案并按《药品非临床研究质量管理规范》(GLP)进行实验。
(六)、所有样品均为上市包装。
(七)、所有试验均应至少取3个不同的批号。
试验内容-案例示例一:玻璃输液瓶与药物相容性试验(以葡萄糖输液采用玻璃瓶为例)(一)材料的一致性1、应提供原材料及添加剂的来源、牌号、配方,控制其一致性。
药品包装材料与药物相容性试验指导原则完整版

国家药品监督管理局直接接触药品包装材料和容器标准(试行)YBB00142002药品包装材料与药物相容性试验指导原则Yaopinbaozhuangcailiao yu yaowu xiangrongxingshiyan zhidao yuanzeGuidelines of evaluating compatibilitybetween pharmaceutical packaging and pharmaceuticals 药品包装材料与药物相容性试验是指为考察药品包装材料与药物之间是否发生迁移或吸附等现象,进而影响药物质量而进行的一种试验。
由于包装材料众多、包装容器的各异及被包装制剂的不同,为方便、有效地进行本试验,特制定本指导原则。
一、相容性试验测试方法的建立在考察药品包装材料时,应选用三批包装材料制成的容器对拟包装的一批药品进行相容性试验;考察药品时,应选用三批药物用拟上市包装的一批材料或容器包装后进行相容性试验。
当进行药品包装材料与药物的相容性试验时,可参照药物及该包装材料或容器的质量标准,建立测试方法。
必要时,进行方法学的研究。
二、相容性试验的条件1、光照试验采用避光或遮光包装材料或容器包装的药品,应进行强光照射试验。
将供试品置于装有日光灯的光照箱或其它适宜的光照装置内,放置10天,照照射试验。
将供试品置于装有日光灯的光照箱或其它适宜的光照装置内,放置10天,照度条件为:4500lx±500lx,于第5天和第10天取样,按重点考察项目,进行检测。
2、加速试验将供试品置于温度40℃±2℃ 、相对湿度为90%±10%或20%±5%的恒温恒湿箱内,放置6个月,分别于0、1、2、3、6月取出,进行检测。
对温度敏感的药物,可在25℃±2℃、相对湿度为60%±10%条件下,放置6个月后,进行检测。
用以预测包装对药物保护性的有效性,推测药物的有效期。
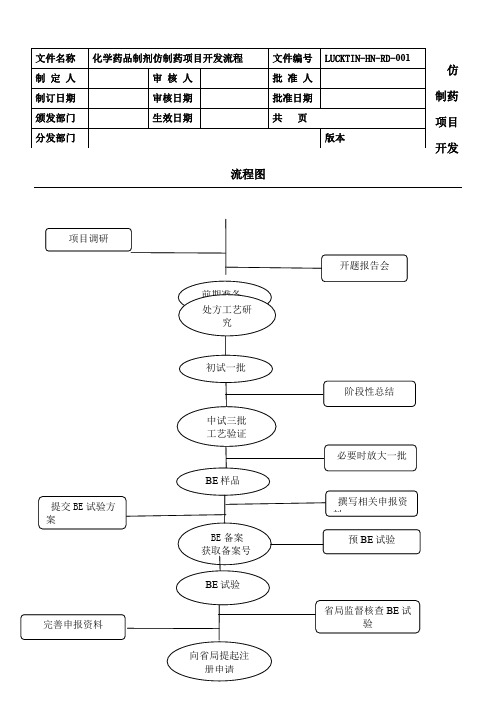
仿制药详细研发流程
文件名称
化学药品制剂仿制药项目开发流程
文件编号
LUCKTIN-HN-RD-001
制 定 人
审 核 人
批 准 人
制订日期
审核日期
批准日期
颁发部门
生效日期
共 页
分发部门
版本
仿制药研发具体流程
项目
内容
备注
一
品种调研
(立项)
1、原研信息(规格、处方组成、工艺、来源等)
2、质量标准(原研、药典、首仿)
1、综述资料
2、药学研究资料
3、药理毒理研究资料
4、BE试验资料
九
向省局提交注册申请
1、省局形式审查
2、省局现场核查(研制现场、生产现场、临床试验现场)
十
资料移交总局
2、总局审评中心审评
2、总局审评过程或有因的核查和抽样检验
十一
完整性审评
1、补充后续稳定性资料
2、完整性通过
十二
批准上市
1、售后
说明:
2)处方组成:辅料种类、规格及资料来源, 不同规格处方或比例是否一致
3)工艺研究:是否微粉化,制粒是干法、湿法、直接压片、包衣目的等
4)方法
常规方法:重量、水分测定、HPLC等
仪器分析:X-光衍射、扫描电镜
四
处方工艺研究
工艺参数研究
1、处方工艺摸索:
1)辅料相容性试验
2)处方筛选
3)工艺参数研究
2、小试验证三批
1、进度计划及预算,参见项目开题报告附件;
2、1-14项,填写主要内容汇总,如有需要,可另附表,附表按编号命名及排序。
3、备注:文件编号XKY-HN-RD-***
包材与药物相容性研究汇总

直接接触药品的包装材料和容器是药品不可分割的一部分,它伴随药品生产、流通及使用的全过程。
由于包装材料、容器的组成、药品所选择的原辅料及生产工艺的不同,药品包装材料和容器中有的组份可能会被所接触的药品溶出、或与药品发生互相作用、或被药品长期浸泡腐蚀脱片而直接影响药品的质量;而且,有些对药品质量及人体的影响具有隐患性(即通过对药品质量及人体的常规检验不能及时发现的问题)。
例如,安瓿、输液瓶(袋),如果不是针对不同药品采用不同的处方和生产工艺进行选择,常常会有药品包装材料和容器中的组份被溶出及玻璃脱片现象,这些影响在一般的常规药检时不能被发现;再例如,天然橡胶塞中溶出的异性蛋白对人体可能是致热源,溶出的吡啶类化合物是致癌、致畸、致突变的肯定因素,而细微的玻璃脱片是堵塞血管形成血栓或肺肉芽肿隐患等等。
从另一个方面讲,由于药品的种类多且有效活性基团复杂,不同药品与直接接触药品的包装材料和容器之间的相互影响也不同,所以,一种包装材料和容器适用于所有的药品,或者一种药品可以采用任何可获得的包装材料和容器都是存在巨大的质量和安全性隐患的。
药品是一种特殊的商品,特别是注射剂产品,其质量和由包装材料和容器引起的安全性隐患要高于口服剂型,所以对注射剂产品的直接接触药品的包装材料和容器的选择,不仅要考虑包装材料和容器是否能满足药品本身应能达到的无菌保证水平的要求,同时更要关注直接接触药品的包装材料和容器与药品之间的相互作用。
1 我国药包材生产企业的现状与管理要求我国药包材生产企业和药包材产品相对落后。
虽然,现有药包材生产企业约1000家,生产药用玻璃、金属、药用明胶制品、橡胶、塑料(容器、片材、膜)及其复合片(膜)等五大类六十多个品种的直接接触药品的包装材料和容器,但是,现有药包材生产企业多为乡镇集体企业,普遍存在规模小,人员素质、装备、技术及管理水平低,产品质量不稳定等问题。
因而,质量不高、不符合标准的药包材产品常见;使用不合格药包材产品或使用未经审批药包材问题尚未解决;所以,优新药包材产品的推广应用缓慢,一些落后、使用不便、甚至影响药品质量的药包材淘汰困难,有的仍然在影响着药品的质量。
注射剂药品与包装材料相容性试验之二

评价方法
塑料材料的重点考察项目:
双向穿透性(溶剂,水分、气体及挥发性药物的渗入与透出等) 溶出性(塑料添加剂的溶出;有害金属元素的释放) 吸附性(塑料对药物的吸附、转移) 化学反应性(与溶剂的作用及加工时分解物对药物的影响) 微粒(塑料容器制备不良产生) 密封性
应关注相容性试验:
聚合物添加剂 单体、起始物质、降解产物 药品接触材料中物质残留量的数据 样品化学组成、物理组成 方法的检测限、精密度、回收率与试验结果.
评价方法
3.建立新的试验方法
例2:注射用粉液双室袋药物稳定性试验 方法的建立
除符合一般的考察原则及方法条件外 注意本包装内液体与固体药物的分别考察条件 双室袋虚焊开通前药物各时间点的全项考察数据 虚焊开通混合后不同时间点相关项目的考察数据 注意虚焊用黏合剂的安全性考察
稳定性试验
定义: 为考察药物在温度、湿度、光线的影响 下随时间变化的规律而进行的试验。
这个试验为药品的生产、包装、贮存、 运输条件及有效期的建立提科学的依据。
稳定性试验
目的: 为保证药物的安全有效,选择适合药品剂 型、处方、生产、包装、贮存、运输条件 与有效期。
稳定性试验
原则:
(基本要求)
对包装在半透性容器中的药物
ICH
( ℃/RH% )
时间周期: 12个月 25±2℃/40±5% 或 30±2℃/35±5% 由申请者决定
说明: 采用前者为长期试验条件时,中间试验条件为 30±2℃/65±5% (时间周期: 6个月)
特别要求试验(相容性)
药包材与药品相容性试验的原则

药包材与药品相容性试验的原则药包材与药品相容性试验的原则一、药包材与药品相容性试验的目的药包材对保证药品的稳定性起着重要作用,因而药用包装材料将直接影响用药的安全性。
直接接触药品的包装材料、容器是药品的一部分,尤其是药物制剂中,一些剂型本身就是依附包装而存在的(如气雾剂等)。
由于药品包装材料、容器组成配方、所选择的原辅料及生产工艺的不同,导致不恰当的材料引起活性成分的迁移,吸附甚至发生化学反应,使药物失效,有的还会产生严重的副作用。
为此,国家SDA发布了《药品包装用材料容器管理办法》(暂行)、《药品包装、标签和说明书管理规定》(暂行)二个局长令,以切实从根本上保证用药的安全性、有效性、均一性。
这就要求在为药品选择包装容器(材料)之前,必须检验证实其是否适用于预期用途,必须充分评价其对药物稳定性的影响,评定其在长期的贮存过程中,在不同环境条件下(如温度、湿度、光线等),在运输使用过程中(如与药物接触反应,对药物的吸附等)、容器(材料)对药物的保护效果和本身物理、化学、生物惰性,所以在使用药包材之前需做相容性试验。
二、药包材与药品相容性试验的原则(一)、药物在选择药包材材料、容器时,应首先考虑其保护功能,然后考虑材料、容器的特点和性能,包括化学、物理学、生物学、形态学等性能。
(二)、药包材应具有良好的化学稳定性、较低的迁移性、阻氧、阻水、抗冲击、无生物意义上的活性、微生物数在控制范围内、与其它包装物有良好的配合性、适合于自动化包装设备等。
(三)、在评价之前药包材与药物应符合有关标准。
(四)、药包材与药物相容性试验应考虑以下几个方面:1、形成包装单元时,各包装物应有良好的配合性。
2、包装单元形成时,能适合特定的包装设备。
3、包装中的药物,能通过药物稳定性试验的所有项目。
4、药包材根据生产工艺要求耐受特殊处理的能力(如钴60消毒等)5、同一包装单元中首次至末次使用保证药物的一致性。
6、对恶劣运输、不同贮存环境的抵抗能力。
药品包装材料与药物相容性试验指导原则

药品包装材料与药物相容性试验指导原则药包材与药物相容性实验药品是一种特殊商品。
药品的质量广受政府、制药企业和患者的亲密关注。
而药品的包装却并不被普通人所关注。
殊不知,药品包装用材料、容器〔简称药包材,下同〕随同药品从消费到销售的全进程,假设包装资料和方式选用不当,能够会招致最动摇的药物处方失效,甚至对人体发生严重的反作用。
据报道,包装在聚氯乙烯输液袋中的安宁注射液,60%的药物活性成分被包装资料所吸附,其疗效遭到严重影响;用薄的聚乙烯软管包装软膏制剂,会使膏体变硬、变色,无法正常运用。
因此,选择适宜的药包材是制药工业一项很重要的任务。
选择适宜的药包材,就要停止药包材与药物的相容性实验--这是一种评价药包材功用优劣的有效方法。
实验目的:选择适宜的药包材直接接触药品的包装资料、容器是药品的一局部,尤其是在药物制剂中,一些剂型自身就是依靠包装而存在的,如气雾剂。
药包材的配方、组成,所选择的原、辅料及消费工艺的不同,都会对药质量量发生影响。
不恰当的包装资料会引发药物活性成分的迁移、吸附甚至使其发作化学反响,招致药物失效,有的还会使药物对人体发生严重的反作用。
因此,国度药品监视管理局专门发布了«药品包装用资料容器管理方法»〔暂行〕和«药品包装、标签和说明书管理规则»〔暂行〕,以规范药品的包装,从而保证人民用药的平安有效。
那么,如何为药品选择适宜的药包材呢?在为药品选择包装容器〔资料〕之前,首先必需检验这种容器〔资料〕能否适用于预期用途:必需充沛评价其对药物动摇性的影响,评定其在临时贮存进程中,在不同的温度、湿度、光照等环境条件下,在运输运用进程中与药物的接触反响、对药物的吸附等状况,以及容器〔资料〕自身的物理、化学、生物惰性和其对药物的维护效果,即停止药包材与药物的相容性实验。
一套完整的药包材与药物相容性实验,应该充沛思索包装资料和包装方式对药物的影响,并制定一个良好的实验方案。
药品包装材料与药物相容性试验指导原则完整版

国家药品监督管理局直接接触药品包装材料和容器标准(试行)YBB00142002药品包装材料与药物相容性试验指导原则Yaopinbaozhuangcailiao yu yaowu xiangrongxingshiyan zhidao yuanzeGuidelines of evaluating compatibilitybetween pharmaceutical packaging and pharmaceuticals 药品包装材料与药物相容性试验是指为考察药品包装材料与药物之间是否发生迁移或吸附等现象,进而影响药物质量而进行的一种试验。
由于包装材料众多、包装容器的各异及被包装制剂的不同,为方便、有效地进行本试验,特制定本指导原则。
一、相容性试验测试方法的建立在考察药品包装材料时,应选用三批包装材料制成的容器对拟包装的一批药品进行相容性试验;考察药品时,应选用三批药物用拟上市包装的一批材料或容器包装后进行相容性试验。
当进行药品包装材料与药物的相容性试验时,可参照药物及该包装材料或容器的质量标准,建立测试方法。
必要时,进行方法学的研究。
二、相容性试验的条件1、光照试验采用避光或遮光包装材料或容器包装的药品,应进行强光照射试验。
将供试品置于装有日光灯的光照箱或其它适宜的光照装置内,放置10天,照照射试验。
将供试品置于装有日光灯的光照箱或其它适宜的光照装置内,放置10天,照度条件为:4500lx±500lx,于第5天和第10天取样,按重点考察项目,进行检测。
2、加速试验将供试品置于温度40℃±2℃ 、相对湿度为90%±10%或20%±5%的恒温恒湿箱内,放置6个月,分别于0、1、2、3、6月取出,进行检测。
对温度敏感的药物,可在25℃±2℃、相对湿度为60%±10%条件下,放置6个月后,进行检测。
用以预测包装对药物保护性的有效性,推测药物的有效期。
相容性实验浅谈

一、药包材与药品相容性试验的目的药包材对保证药品的稳定性起着重要作用,因而药用包装材料将直接影响用药的安全性。
直接接触药品的包装材料、容器是药品的一部分,尤其是药物制剂中,一些剂型本身就是依附包装而存在的(如气雾剂等)。
由于药品包装材料、容器组成配方、所选择的原辅料及生产工艺的不同,导致不恰当的材料引起活性成分的迁移,吸附甚至发生化学反应,使药物失效,有的还会产生严重的副作用。
为此,国家SDA发布了《药品包装用材料容器管理办法》(暂行)、《药品包装、标签和说明书管理规定》(暂行)二个局长令,以切实从根本上保证用药的安全性、有效性、均一性。
这就要求在为药品选择包装容器(材料)之前,必须检验证实其是否适用于预期用途,必须充分评价其对药物稳定性的影响,评定其在长期的贮存过程中,在不同环境条件下(如温度、湿度、光线等),在运输使用过程中(如与药物接触反应,对药物的吸附等)、容器(材料)对药物的保护效果和本身物理、化学、生物惰性,所以在使用药包材之前需做相容性试验。
二、药包材与药品相容性试验的原则(一)、药物在选择药包材材料、容器时,应首先考虑其保护功能,然后考虑材料、容器的特点和性能,包括化学、物理学、生物学、形态学等性能。
(二)、药包材应具有良好的化学稳定性、较低的迁移性、阻氧、阻水、抗冲击、无生物意义上的活性、微生物数在控制范围内、与其它包装物有良好的配合性、适合于自动化包装设备等。
(三)、在评价之前药包材与药物应符合有关标准。
(四)、药包材与药物相容性试验应考虑以下几个方面:1、形成包装单元时,各包装物应有良好的配合性。
2、包装单元形成时,能适合特定的包装设备。
3、包装中的药物,能通过药物稳定性试验的所有项目。
4、药包材根据生产工艺要求耐受特殊处理的能力(如钴60消毒等)5、同一包装单元中首次至末次使用保证药物的一致性。
6、对恶劣运输、不同贮存环境的抵抗能力。
(五)、所有试验都应根据具体的包装形式和药物,设计试验方案并按《药品非临床研究质量管理规范》(GLP)进行实验。
药品包装材料与药物相容性试验指导原则YBB00142002

国家食品药品监督管理局直接接触药品包装材料和容器标准(试行)YBB00142002药品包装材料与药物相容性试验指导原则Yaopinbaozhuangcailiao yu yaowu xiangrongxingshiyan zhidao yuanzeGuidelines of evaluating compatibilityBetween pharmaceutical packageing and pharmaceuticals 药品包装材料与药物相容性试验是指为考察药品包装材料与药物之间是否发生迁移或吸附等现象,进而影响药物质量而进行的一种试验。
由于包装材料众多、包装容器的各异及被包装制剂的不同,为方便、有效地进行本试验,特制定本指导原则。
一、相容性试验测试方法的建立在考察药品包装材料时,应选用三批包装材料制成的容器对拟包装的一批药品进行相容性试验:考察药品时,应选用三批药物用拟上市包装的一批材料或容器包装后进行相容性试验。
当进行药品包装材料与药物的相容性试验时,可参照药物及该包装材料或容器的质量标准,建立测试方法。
必要时,进行方法学的研究。
二、相容性试验的条件1、光照试验采用避光或遮光包装材料或容器包装的药品,应进行强光照射试验。
将供试品置于装有日光灯的光照箱或其它适宜的光照装置内,放置10天,照照射试验。
将供试品置于装有日光灯的光照箱或其它适宜的光照装置内,放置10天,照度条件为:4500lx±5001x,于第5天和第10天取样,按重点考察项目,进行检测。
2、加速试验将供试品置于温度40℃±2℃、相对湿度为90%±10%或20%±5%的恒温恒湿箱内,放置6个月,分别于0、1、2、3、6月取出,进行检测。
对温度敏感的药物,可在25℃±2℃、相对湿度为60%±10%条件下,放置6个月后,进行检测。
用以预测包装对药物保护的有效性,推测药物的有效期。
药品与药包材相容性研究方法探索和应用举例

Testing for the Label
X (2)
X (3)
---
--
参考资料:Parenteral and Ophthalmic Drug Products Leachables and Extractables Working Group 2011
相容性研究试验方案--提取研究
可提取物检测方法学研究:检测限、定量限、线性、精 密度、稳定性;
一 试验依据 二 试验方法 三 案例分析
试验前
调研产品的同时调研包装形式和材料
项目立项
确定风险类型与给药途径剂型和包材接触形式关系
收集选择
初步确定剂型、包装形式、材料、给药方式、 包装组件(初级和次级)、合格包材供应商(两家以 上)、提供样品、或参考已有的包材的提取研究的结果。
预实验确认
YBB标准规定,外观、尺寸、组件间配合、注射剂包装清 洁度、外包装、处理工艺、澄清度、硅油含量、已有胶 塞提取试验参考。基本选定包材供应商。
样品信息:
批号/生产商COA/自检COA
重点关注:外包装/预处理工艺;有关的
次级包装
必要时追踪:管制瓶的玻璃管供应商/塑
料瓶、盖、接口等的粒料供应商/胶塞的 原料胶的供应商;提供证明和有关资料。
药包材相容性研究内容
提取研究 迁移研究 吸附研究 安全性评价
药包材相容性研究内容
提取研究 迁移研究 吸附研究 安全性评价
PODP OINDP PODP
PODP
药包材相容性研究试验基本信息
根据基本信息和参数,确定研究的接触组件: 风险类型:吸入制剂、注射剂、眼用制剂; 接触系统:初级包装组件或影响明显的接触系统; 接触时间:产品生命周期内的末段时间; 接触面积:直接接触面积/单位重量或体积
药品包装材料与药品相容性试验在新药研发中的重要作用

一
药 品 包 装 材料 有 了很 大 的 发 展
,
但我国药包
部分
,
它伴 随 药 品 生 产
、
、
流通
、
贮 存 及 使 用 的全 过 程
、
。
由
材 生 产 企 业 和 药 包材 产 品 还 是 相 对 落 后 平低
,
药 品 包 装整 体 水
。
干 药 品 包 装 材料
工
容 器的组 成配 方
所选 择 原 辅 料 及 生 产
一
性 。规定 I指出药品的包装分内包装与外包装 。并分 别 { 】
( 在评价 之前药包 材与药物 应符合有关标准 。 三)
吸附药
。
献 率都 明 显 低 干 发 达 国 家 水 平
品 中的 活 性 成 分
,
降 低 有效 成 分 含 量 而 影 响 药 品 的 疗 效
。
我 国 现 有 药 包 材 生 产 企 业 中虽 然 有 大 型 企 业
分 多 为 乡镇 集 体 企 业
,
但 大部 技术及
或 波 药 品 长期 浸 泡 腐 蚀 脱 片 而 直 接影 响 药 品 质量
定 “ 药品包装必须适合药品质量的要求 ,方便储存 、运输
和医疗 使用” 。国家 S DA发布 了 《 F 药品包装 用材料容 器
数在控制范 围内、 与其它包装物有 良好的配 合性 、 适 合干
自动 化包装设备等 。
管理 办法》 《 、 药品包装 、标签和说 明书管理 规定》二个
局长 令,以切实从根本上保证用药的安全性 、有效性 、均
、
溶 出的吡 啶 类化 合 物 是 致
丁 基 胶 塞 中有 的 添 加 剂 在
原辅料及包材相容性试验

原辅料及包材相容性试验原辅料及包材相容性试验药包材与药品相容性试验的目的药包材对保证药品的稳定性起着重要作用,因而药用包装材料将直接影响用药的安全性。
直接接触药品的包装材料、容器是药品的一部分,尤其是药物制剂中,一些剂型本身就是依附包装而存在的(如气雾剂等)。
由于药品包装材料、容器组成配方、所选择的原辅料及生产工艺的不同,导致不恰当的材料引起活性成分的迁移,吸附甚至发生化学反应,使药物失效,有的还会产生严重的副作用。
为此,CFDA发布了《药品包装用材料容器管理办法》(暂行)、《药品包装、标签和说明书管理规定》(暂行)二个局长令,以切实从根本上保证用药的安全性、有效性、均一性。
这就要求在为药品选择包装容器(材料)之前,必须检验证实其是否适用于预期用途,必须充分评价其对药物稳定性的影响,评定其在长期的贮存过程中,在不同环境条件下(如温度、湿度、光线等),在运输使用过程中(如与药物接触反应,对药物的吸附等)、容器(材料)对药物的保护效果和本身物理、化学、生物惰性,所以在使用药包材之前需做相容性试验。
药包材与药品相容性试验的原则(一)、药物在选择药包材材料、容器时,应首先考虑其保护功能,然后考虑材料、容器的特点和性能,包括化学、物理学、生物学、形态学等性能。
(二)、药包材应具有良好的化学稳定性、较低的迁移性、阻氧、阻水、抗冲击、无生物意义上的活性、微生物数在控制范围内、与其它包装物有良好的配合性、适合于自动化包装设备等。
(三)、在评价之前药包材与药物应符合有关标准。
(四)、药包材与药物相容性试验应考虑以下几个方面:1、形成包装单元时,各包装物应有良好的配合性。
2、包装单元形成时,能适合特定的包装设备。
3、包装中的药物,能通过药物稳定性试验的所有项目。
4、药包材根据生产工艺要求耐受特殊处理的能力(如钴60消毒等)5、同一包装单元中首次至末次使用保证药物的一致性。
6、对恶劣运输、不同贮存环境的抵抗能力。
(五)、所有试验都应根据具体的包装形式和药物,设计试验方案并按《药品非临床研究质量管理规范》(GLP)进行实验。
包材相容性操作规程

包材相容性操作规程1. 引言本操作规程旨在指导企业在使用包装材料时,确保包材与产品之间的相容性。
正确选择和使用包材可以有效保护产品的质量和安全性,避免因包材与产品发生相互作用而导致产品质量问题。
2. 相容性测试相容性测试是确保包材与产品相互作用正常的重要环节。
在选择包材之前,企业需要进行相应的相容性测试,以确保所选择的包材与产品之间不存在不良反应。
相容性测试的步骤如下:2.1 准备样品从已经确定的产品批次中,随机选取一定数量的样品作为测试样品。
2.2 选择测试方法根据产品的特性和包装材料的种类及属性,选择适当的相容性测试方法。
常用的相容性测试方法包括可溶性测试、迁移测试、化学分析等。
2.3 进行测试按照选定的测试方法,将测试样品与包装材料置于一定的条件下进行测试。
例如,可将样品与包装材料置于高温高湿环境下,观察是否产生色泽变化、褪色、变质等现象。
2.4 分析结果对测试结果进行分析,判断包材与产品之间的相容性情况。
如果发现不良反应或异常情况,应及时采取措施,进行调整或更换包装材料。
3. 包材选择原则在进行相容性测试之前,企业应该根据产品的特点和需求,合理选择适用的包装材料。
下面是一些常用的包材选择原则:3.1 材料的物理特性包材应具有适当的强度、韧性和耐磨性,以确保产品在运输和储存过程中不会受到损坏。
3.2 材料的化学性质包材应具有较好的耐腐蚀性能,以防止包装材料的成分溶解、迁移、变质等现象对产品质量造成不良影响。
3.3 材料的安全性包材应符合国家相关法律法规的要求,不含有对人体健康有害的物质,以确保产品的安全性。
3.4 材料的环保性包材应具有可降解性或可回收性,以减少对环境的污染和资源消耗。
4. 包材使用和储存注意事项4.1 使用注意事项•在使用包材时,应按照规定的使用方法进行使用,不得超过包材的负荷限制。
•注意防止包装材料与产品发生物理、化学上的相互作用,避免对产品质量造成不良影响。
•避免包材受到日晒、潮湿、高温等不良环境的影响。
包材相容性操作规程

包材相容性操作规程《包材相容性操作规程》一、目的包材相容性操作规程的目的是为了保证使用的包材与产品相互兼容,防止因包材原料或成分与产品发生反应而造成产品质量问题,确保生产过程中的安全和稳定。
二、适用范围本操作规程适用于所有涉及包材的生产、使用和储存过程,包括但不限于原料采购、生产加工、包装、运输等环节。
三、操作程序1. 包材选择在选择包材时,应考虑产品的性质、包装方式、存储条件等因素,并严格执行公司标准或客户要求的包材选用标准。
2. 包材检查对所有收到的包材进行检查,确保包材的质量和完整性符合要求。
对于有疑问的包材,应立即停用并通知相关部门进行处理。
3. 包材试验对新引进的包材或有变更的包材进行相容性试验,以确保包材不会对产品造成影响。
试验内容包括包材与产品的接触试验、加工工艺试验等。
4. 包材使用严格按照包材使用规范进行操作,避免包材错用或混用。
对于包材的设备、储存条件等也应符合相关要求。
5. 包材储存包材的储存应符合要求,避免因储存条件不当导致包材性能下降或受到污染。
应定期检查储存条件,并记录相关情况。
6. 包材变更如需变更包材,需按照公司规定的变更程序进行,并重新进行相容性试验,确保产品质量不受影响。
四、相关记录应建立相应的包材相容性试验记录、包材检查记录、包材储存记录等,确保全程可追溯。
五、附则1. 需严格按照本操作规程执行,如有违反应当及时纠正;2. 对于包材相容性问题,应尽快通知相关部门,并采取相应措施加以解决。
以上为《包材相容性操作规程》,如有变更或补充,应经过相关部门审批才能执行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原辅料及包材相容性试验药包材与药品相容性试验的目的药包材对保证药品的稳定性起着重要作用,因而药用包装材料将直接影响用药的安全性。
直接接触药品的包装材料、容器是药品的一部分,尤其是药物制剂中,一些剂型本身就是依附包装而存在的(如气雾剂等)。
由于药品包装材料、容器组成配方、所选择的原辅料及生产工艺的不同,导致不恰当的材料引起活性成分的迁移,吸附甚至发生化学反应,使药物失效,有的还会产生严重的副作用。
为此,CFDA发布了《药品包装用材料容器管理办法》(暂行)、《药品包装、标签和说明书管理规定》(暂行)二个局长令,以切实从根本上保证用药的安全性、有效性、均一性。
这就要求在为药品选择包装容器(材料)之前,必须检验证实其是否适用于预期用途,必须充分评价其对药物稳定性的影响,评定其在长期的贮存过程中,在不同环境条件下(如温度、湿度、光线等),在运输使用过程中(如与药物接触反应,对药物的吸附等)、容器(材料)对药物的保护效果和本身物理、化学、生物惰性,所以在使用药包材之前需做相容性试验。
药包材与药品相容性试验的原则(一)、药物在选择药包材材料、容器时,应首先考虑其保护功能,然后考虑材料、容器的特点和性能,包括化学、物理学、生物学、形态学等性能。
(二)、药包材应具有良好的化学稳定性、较低的迁移性、阻氧、阻水、抗冲击、无生物意义上的活性、微生物数在控制范围内、与其它包装物有良好的配合性、适合于自动化包装设备等。
(三)、在评价之前药包材与药物应符合有关标准。
(四)、药包材与药物相容性试验应考虑以下几个方面:1、形成包装单元时,各包装物应有良好的配合性。
2、包装单元形成时,能适合特定的包装设备。
3、包装中的药物,能通过药物稳定性试验的所有项目。
4、药包材根据生产工艺要求耐受特殊处理的能力(如钴60消毒等)5、同一包装单元中首次至末次使用保证药物的一致性。
6、对恶劣运输、不同贮存环境的抵抗能力。
(五)、所有试验都应根据具体的包装形式和药物,设计试验方案并按《药品非临床研究质量管理规范》(GLP)进行实验。
(六)、所有样品均为上市包装。
(七)、所有试验均应至少取3个不同的批号。
试验内容示例一:玻璃输液瓶与药物相容性试验(以葡萄糖输液采用玻璃瓶为例)(一)、材料的一致性1、应提供原材料及添加剂的来源、牌号、配方,控制其一致性。
2、原材料的质量控制:应确认或证实同一厂家、不同批号的材料的一致性(二)、药用玻璃输液瓶的质量控制:应符合GB2630-90的规定。
(三)、玻璃瓶与胶塞、铝盖的配合性:1、胶塞、铝盖、玻璃输液瓶的质量应分别符合YY0169.1-94、GB5197-96及GB2630-90的规定。
2、胶塞、铝盖的来源:应提供生产厂家、牌号、配方。
3、上机试验:通过上机试验,确定所用参数(为产品推荐使用的参数)。
(四)、装药试验1、选择玻璃输液瓶作为葡萄糖注射剂的包装形式。
2、中华人民共和国药典2015年版二部葡萄糖注射剂要求项目有:性状、鉴别、pH值、5一羟甲基糠醛、重金属、细菌内毒素、无菌、含量测定、其它。
3、试验方法的选择:i.注射剂的装量检查:按药典方法检查。
ii.注射剂包装容器的温度适应性:121℃饱和蒸汽压,30min。
iii.瓶塞与容器的配合性:抽真空至75±5kPa,维持30min,以目力检查亚甲蓝溶液是否渗入玻璃输液瓶内。
iv.玻璃容器的耐老化试验:按IS02230规定方法进行。
v.玻璃容器的脱片试验:按IS0718中方法B的规定进行抗热冲击性试验,将玻璃输液瓶置于不少于80℃的温差条件下时,该瓶不得碎裂或有脱片。
vi.不溶性微粒检查:按药典方法进行。
vii.穿刺落屑试验:按YY0169.1-94规定进行。
viii.迁移:取样品,于40℃横放或倒置10天,在第0、1、3、5、10天取样,进行下列检测:a、重金属的迁移b、酸碱度检查c、硫化物的迁移d、铵盐的迁移e、锌盐的迁移f、5-羟甲基糠醛的检查(9)、生物相容性I.急性毒性试验:取于40℃横放或倒置10天的样品,按GB/T16175的有关规定检测。
II.细菌内毒素试验:取于40℃横放或倒置10天的样品,按GB/T16175的有关规定检测。
III.皮内刺激试验:取于40℃横放或倒置10天的样品,按GB/T16175的有关规定检测。
(10)、稳定性试验:取样品,于40℃、RH75±5%条件下横放或倒置6个月,在第0、1、2、3、6个月末取样进行外观色泽、含量、pH、澄明度、5-羟甲基糠醛检测。
(11)、模拟恶劣运输环境的试验▪光照试验:于4500±5001x横放或倒置10天,检查外观色泽、含量、PH、澄明度、5-羟甲基糠醛。
▪浸水试验:取样分别于水中放置30min中,暴露4h后进行含量测定。
(12)、模拟不良贮存环境的试验:▪条件1:-18℃▪条件2:20℃、RH90%▪条件3:55℃、RH30%取样品于上述条件下分别放置72h后进行外观色泽、含量、pH、澄明度、5-羟甲基糠醛检测。
示例二:药品包装用铝箔与药物相容性试验(以头孢氨苄胶囊采用铝塑泡罩为例)(一)、材料的一致性1、应提供原材料及添加剂的来源、牌号、配方,控制其一致性。
2、铝箔的质量控制:应确认或证实同一厂家、不同批号的材料的一致性。
3、粘合剂的质量控制:确认或检验证实同一厂家、不同批号的材料的一致性,应符合有关标准的规定。
4、保护剂的质量控制:确认或检验证实同一厂家、不同批号的材料的一致性,应符合有关标准的规定。
(二)、药品包装用铝箔的质量控制:应符合GBl2255-90的规定。
(三)、与药用聚氯乙烯(PVC)硬片的配合性:1、所用PVC的质量应符合GB5663-2000的规定2、所用PVC的来源:生产厂、牌号、配方的一致性3、上机试验:通过上机试验,确定所用参数(为产品推荐使用的参数)4、上机试验后的铝塑泡罩应符合ZBC08003-87质量标准。
(四)、装药试验:1、选用铝塑泡罩为头孢氨苄胶囊的包装形式2、中华人民共和国药典2015年版二部头孢氨苄胶囊要求项目有:鉴别、检查(有关物质、水分、溶出度)、含量测定、其它。
3、试验方法(1)、配合性:铝塑泡罩的密封性试验(2)、迁移a、重金属的迁移b、酸度检查c、氯乙烯单体的迁移d、邻苯二甲酸二异辛酯(DEHP)的迁移e、聚氨酯类粘合剂的迁移(二氨基甲苯的测定)(3)、生物相容性试验o急性毒性试验:取于40℃放置10天的样品按GB/T16175的有关规定检测。
o皮内刺激试验:取于40℃放置10天的样品按GB/T16175的有关规定检测。
(4)、稳定性试验:取样品,于40'C、RH75±5%条件下放置6个月,在第0、1、2、3、6个月末取样进行外观、内容物色泽、含量、有关物质、囊壳、溶出度、水份检测。
(5)、模拟恶劣运输环境的试验•光照试验:于4500~500h放置10天,进行外观、内容物色泽关物质、囊壳、溶出度、水份检测。
•浸水试验:取样分别于水中放置30min中,暴露4h后检查水份。
(6)、模拟不良贮存环境的试验:▪条件1:-18℃▪条件2: 20℃、RH90%▪条件3: 55℃、RH30%取样品于上述条件下分别放置72h后进行外观、内容物色泽、含量、有关物质、囊壳、溶出度、水份检测。
示例三药用液体塑料瓶与药物相容性试验(以酞丁安搽剂为例)(一)、材料的一致性1、应提供原材料及添加剂的采源、牌号、配方,控制其一致性。
2、塑料瓶原材料的质量控制:应确认或证实同一厂家、不同批号的材料的一致性。
(二)、药用液体塑料瓶的质量控制:应符合YYXXXX-200X的规定。
(三)、装药试验:1、选用药用液体塑料瓶为酞丁安搽剂的包装形式2、中华人民共和国药典2015年版二部酞丁安搽剂要求项目有:性状、鉴别、检查、含量测定、其它。
(三)、试验方法(1)、配合性(密封性)(2)、迁移a、重金属的迁移b、pH值检查(3)、生物相容性试验▪急性毒性试验:取于40℃放置10天的样品按GB/T16175的有关规定检测。
▪皮内刺激试验:取于40℃放置10天的样品按GB/T16175的有关规定检测。
▪皮肤致敏试验:取于40℃放置10天的样品按GB/T16175的有关规定检测。
(4)、稳定性试验:取样品,于40~C、RH75±5%条件下放置6个月,在第0、1、2、3、6个月末取样进行性状、含量的测定。
(5)、模拟恶劣运输环境的试验1、光照试验:于4500±5001x放置10天,进行性状、含量的测定。
2、浸水试验:取样分别于水中放置30min中,暴露4h后进行含量测定,3、跌落试验:取样品从1.2m处自然跌落至刚性光滑表面,不得破损。
(6)、模拟不良贮存环境的试验:条件:-18℃20℃、RH90%40℃、自由相对湿度取样品于上述条件下分别放置72h后进行性状、含量测定。
原辅料相容性试验如果没有原料药光稳定性问题,原则上原辅料相容性只考察高温高湿即可。
新药肯定是要做的;仿制药如果和原研采用相同的辅料,以前是不要求,但是现在也是要做的。
因为实际中我们发现国内厂家的某些辅料的质量确实不如国外,所以现在仿制药和原研处方一致也是要做原辅料相容性的,目的是考察辅料的质量。
如果处方一致,但是原辅料相容性结果很差,就要考虑辅料的来源或者型号等方面的问题。
具体试验过程是这样的。
按照原则,原辅料相容性就是一对一,API加一个辅料,而不是多个辅料,除了有稳定剂等特殊情况。
做的时候,辅料的量不是处方的用量,而是比处方量高出5-10倍,试验目的就是看高用量的情况下的影响。
也正因如此,原辅料相容性的结果不能和制剂划等号。
原辅料按照一定的比例混合后,然后分装成几份,一般会加上5%的水,注意滴上水不要再混和,而是要密封。
密封之后放样,水会蒸发,自然就均匀的在容器中了。
不要敞口做,敞口之后放样,一加热,水都挥发掉了,试验还有什么意义呢?而且最好一个取样点放一个样,因为打开之后再密封重新放样,里面的水分含量和湿度就变了。
另外,每个取样点的样品量不要太多,也不要太少。
除了观察外观或者测水分外,准确的称量,然后全部溶掉,测定有关和含量。
有时直接放置在加速条件(40℃+75%湿度)的情况下,也可以的。
至于是加5%的水,还是放在75%的湿度条件,具体情况具体分析。
如果样品特别容易吸潮,放到75%湿度条件,可能吸潮特别厉害,都没办法取样。
如果样品不是很容易吸潮,敞口直接放在75%的湿度条件下更便捷。
这个实验遇到的问题千奇百怪,各种各样的都有,比如锯齿状的数据。
主要出现的问题就是混不匀,取样的时候也没考虑到均匀性,所以就造成不同取样时间的数据忽高忽低,说明不了问题。
还有检测指标的问题,一般大家是看外观和有关物质,这是不够的。
