溶解度曲线大全
溶解度曲线

.
30
.
.
.
40
50
60
70
80
温度/℃
90
100
氯化钠溶解度曲线
37.5 37
溶解度/g
36.5 36 35.5 35 34.5
0 10 20 30 40 50 60
温度/0C
溶 200 解 度 190
180 170 160 150 140 130 120 110 100 90 80 70 60 50
50 40 30 20 10
适用于溶解度随 温度变化较小的 物质如:NaCl
0
10 20 30 40 50 60 70 80 90 100
温度(t)
思考:
如图是a b两种物质的溶解度曲线:从图中 你能获得哪些信息(最少写出三条)?
⑴可以查出某一物质在某一温度 下的溶解度; ⑵比较不同物质在同一 温度 的 溶解度大小; ⑶曲线的交点表示该温度下的溶 解度相等 ; ⑷物质的溶解度受温度变化影响 的大小。
熟石灰的不 饱和溶液
增加溶剂、降低温度
熟石灰的 饱和溶液
从 溶 解 度 曲 线 分 析 结 晶 情 况
溶 解 200 度 190 ( 180 170 克 160 ) 150 140
130 120 110 100 90 80 70
60
固体溶解度曲线
硝酸钾 1 、冷却 热饱和 溶 液 (又叫降温结晶) 适用于溶解度随 温度变化较大的 物质 如:KNO3 2、蒸发溶剂 氯化钠
1.右图是甲乙丙三种物质的溶解度曲线,根据 图示回答下列小题: ①P点的含义: 。
②t1℃时甲、乙、丙的溶解度由大到小的顺 序为 。
③t2℃时,将30g甲放入50g水中,充分溶解 后所得溶液的质量为 。
人教版化学中考专题复习:溶解度曲线(共26张PPT)

(2)t4℃时,将25gA物质加入到50g水中,充分 溶解,得到A的_饱___和__(饱和/不饱和)溶液__7_0__g。
溶液的溶质的质量分数为_2_27_008_×._51_07_0%_%__。 (计算式)
(3)要使t3℃时A的不饱和溶液转化为饱和溶液
蔗糖
将蔗糖的不饱和溶液转化成 饱和溶液,有哪些方法?
方法一:加入蔗糖(增加溶质) 方法二:蒸发溶剂 方法三:降低温度
不饱和溶液
增加溶质 蒸发溶剂 降低温度 增加溶剂 升高温度
饱和溶液
溶解度曲线应用——6.饱和溶液与不饱和溶液的转化(特殊情况)
将氢氧化钙的不饱和溶液转 化成饱和溶液,有哪些方法?
方法一:加入氢氧化钙(增加溶质) 方法二:蒸发溶剂 方法三:升高温度
可以使用的方法有__增__加__溶__质___/_降__低__温__度___/蒸___发__溶__剂____;
t1 t2 t3 t4
(4)要使t3℃时C的饱和溶液转化为不饱和溶液 可以使用的方法有_增___加__溶__剂__/_降___低__温__度___。
优秀ppt公开课ppt免费课件下载免费 课件人 教版化 学中考 专题复 习:溶 解度曲 线(共2 6张PPT )
优秀ppt公开课ppt免费课件下载免费 课件人 教版化 学中考 专题复 习:溶 解度曲 线(共2 6张PPT )
溶解度曲线应用——7.确定饱和溶液析出晶体的方法
优秀ppt公开课ppt免费课件下载免费 课件人 教版化 学中考 专题复 习:溶 解度曲 线(共2 6张PPT )
物质 A B C
溶解度曲线
线形
提纯物质
物质的溶解性曲线图

1、什么是固体的溶解度?
在一定温度下,某固态物质在100克溶剂里达 到饱和状态时所溶解的质量,叫做这种物质 在这种溶剂里的 条件:
溶解度。
2、固体物质溶解度四要素是什么?
一定温度 标准: 100克溶剂(一般指水) 溶液状态:饱和状态 单位: 克(质量)
3、影响固体物质溶解性的因素是什么? 溶质的性质、溶剂的性质、温度
80 90 100
硼酸
50
60
70
温度/℃
从溶解度曲线上获取的信息(二)
曲线上的点:表 示物质在对应温 度时的溶解度
两曲线上的交点: 表示两物质在对应 温度时的溶解度相 等
从溶解度曲线上获取的信息(二)
线 表示物质的溶 解度随温度的 变化而改变的 情况
从溶解度曲线上获取的信息(二) 曲线下面的点:表 示溶液为不饱和溶 液 曲线上面的点:表 示溶液饱和且有未 溶解固体
牛刀小试
图17-1 A.t2℃时,A、B、C三种物质中,A物质的溶解度最大 B.P点表示t1℃时B、C两物质的溶解度大小相等 C .一定温度时,要将 B 物质的不饱和溶液转变成饱和 溶液,可采取增加溶质的方法 D. 20 ℃ 时,给 A、B、 C三种物质的饱和溶液加热 ( 不 考虑溶剂的蒸发),有晶体析出的是A物质
图15-2
3、下图是甲、乙两种固体物质的溶解度曲线。
(3)在20 ℃时,把甲、乙各10 克固体分别加入到两个盛有50 克 不饱和 溶液 ( 选填“饱和” 水的烧杯中,充分搅拌,所得甲溶液为 ________ 大于 (1)30 ℃时,甲的溶解度________ 乙的溶解度(选填 或“不饱和”);若将温度都升高到30 ℃,甲溶液中溶质的质量分 “大于”“等于”或“小于” ); 等于 数 ________ 乙溶液中溶质的质量分数 ( 选填“大于”“等于”或 (2)要使饱和的甲溶液变为不饱和溶液,可采取的方 “小于”)。 加入溶剂(水)(或升温) 法是______________________(只填一种); (4)10 ℃时,向12%的100 克甲溶液中加水60 克,可得到甲溶液 160 7.5 ________g ,此时溶质的质量分数为________% 。 ·浙江教育版
三种溶液溶解度曲线

三种溶液溶解度曲线
溶解度曲线是描述在不同温度下溶质在溶剂中溶解度随着温度变化的曲线。
一般来说,溶解度曲线可以分为三种类型,正常溶解度曲线、异常溶解度曲线和饱和溶解度曲线。
1. 正常溶解度曲线:
正常溶解度曲线是指溶解度随着温度的升高而增加的曲线。
这是最常见的类型,其中随着温度升高,溶质在溶剂中的溶解度也随之增加。
典型的例子是氯化钠在水中的溶解度曲线,随着温度的升高,氯化钠的溶解度也会增加。
2. 异常溶解度曲线:
异常溶解度曲线是指溶解度随着温度的升高而减小的曲线。
这种情况通常发生在某些化合物在溶剂中的溶解度在特定温度范围内随温度的升高而减小,然后再随温度的升高而增加。
这种情况通常涉及到一些非常规的化学现象,例如溶解热或者晶体结构的变化。
3. 饱和溶解度曲线:
饱和溶解度曲线是指在一定压力下,溶解度随着温度的变化而变化的曲线。
在这种情况下,压力是一个关键的因素,因为在一定压力下,溶解度随着温度的变化而变化。
典型的例子是二氧化碳在水中的溶解度曲线,随着温度的升高,二氧化碳的溶解度会减小。
总的来说,溶解度曲线是描述溶质在溶剂中溶解度随着温度变化的曲线,在不同的情况下会呈现出不同的特点,包括正常溶解度曲线、异常溶解度曲线和饱和溶解度曲线。
这些曲线的研究对于理解溶解过程和控制溶解度具有重要意义。
高中化学复习-溶解度曲线

0.01g 1g
10g
溶 200
解
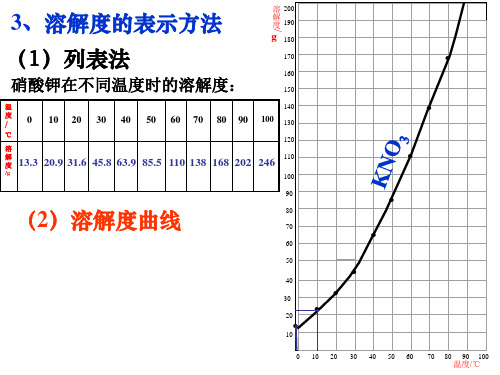
二.溶解度的表示方法:
/
度 190
g 180
170
.
(1)列表法:
160 150
温
度
/
0
10 20
30
40
50 60 70 80
℃
溶
解 度
13.3
20.9
31.6 45.8 63.9 85.5
110 138 168
/g
140
130
90 100
120
110
202 246100
KNO3 热 饱 和溶液
降温
结晶
过滤
(蒸发浓缩)
降温结晶法提纯硝酸钾 (又叫冷却热饱和溶ຫໍສະໝຸດ 法)滤纸上: KNO3固体
滤液中: 大 部 分 NaCl 少量KNO3
思考:1.冬天捞碱,夏天晒盐的原理 纯碱的溶解度随温度变化影响较大,冬天温 度降低,纯碱的溶解度随温度减小而析出; 夏天,水分蒸发快,溶剂量减少,氯化钠溶 解度受温度影响小而析出
某化工厂排放的废液中只含有ZnCl2和CuCl2两种溶 质,为回收金属Cu并得到 ZnCI2固体,化学小组的 同学们设计并进行了如下实验:
(1) 加入过量的A的目的是 将废液中的Cu完全置换出;来操
作①名称是 过滤 , 所需要的仪
器 (2)
烧滤杯渣、B中漏含斗有、的玻物璃质棒是、:铁Z架n和台Cu
10
0
固体溶解度曲线
硝酸钾
1.降温结晶
(又叫冷却热饱和溶液法
)适 用 于 溶 解 度 受 温度影响较大的 物质.如:KNO3
2.蒸发结晶
氯化钠
适用于溶解度受 温度影响较小的 物质如:NaCl
初中科学化学难点之溶解度曲线图

气体溶解度一般随压强增大而增大,压强减小 而减小。
[讨论] 天气闷热时,鱼儿为什么总爱在水 面上进行呼吸?
气体的溶解度随温度的增加而减小. 随压强的减小而减小.
初中科学化学难点
谢谢观看 敬请指教
13
20℃ 60℃
溶解度曲线:以温度为横坐标,溶解度为纵坐标形象 地描绘出物质的溶解度随温度变化情况的曲线。
㈠不同的物质溶解度受温度的影响是不同的
1)大多数物质的溶解度随着温度的升高而增大 。如硝酸铵, 硝酸钾,硝酸钠等,表现为曲线陡
2)少数物质溶解度受温度影响不大,如氯化钠表现为曲线平缓
3)极少数物质的溶解度随着温度的升高而减小,如氢氧化钙
/
溶 200 解 度 190
g 180
硝 酸
170
铵
160 150
140
130
120
110
100 90 80 70 60 50
40 30 20
10
.B硝
酸 钠
A.
硝 酸 钾
氯化铵 氯化钾 氯化钠硼酸来自固体的溶解度曲线:练习:
1、横坐标60,纵坐标110 的A点 表示什么意义?
2、40℃时氯化铵的溶解度为_4_4__g__, 70℃时氯化铵的溶解度为_6_0__g__。 70℃时氯化钾的溶解度为_4_7_g_。
溶 解 度 (g)
B
6最、大(的1是)T__2甲时__,__溶__解; 度 甲 (2)B点代表的含义是
___T_1_℃__时__,_甲__、__丙__两__种__物__质_
_的_溶__解__度__相__等_____; 乙 (3)T1时的甲饱和溶液
8.2-3溶解度曲线

甲 。 (1)图1中一定为饱和溶液的是______ (2)图2中甲、乙 两溶液中溶质质量分数的大小关系为 _________ 相等 。 N ,P点表示的含义 ( 3)图3中表示乙的溶解度曲线是______ 是 30℃时,甲、乙两种固体物质的溶解度相等 。
课堂检测
2.如图为甲、乙两种固体物质的溶解度曲线(水的密度约 为1g/cm3).
(1)两种物质中,溶解度受温度影响更大的是 甲 (填 “甲”或“乙”). 36g . (2)20℃时,乙的溶解度为 (3)下列实验中: 为饱和溶液的是 Y (填“X”或“Y”或“Z”);若三中 溶液中溶质的质量分数分别为a、b、c,则它们的大小关系 是 Z>Y>X (用“<”或“>”或“=”表示出来).
溶解度曲线的应用
1、在t2℃时a物质的溶解度是 50 g; 判断某一物质在不同温度下的 溶解度大小。 2、在 t1℃时 ab物质的溶解度关系是 a 小于 b(填大于、等于或小于)
比较同一温度下,不同物质溶 解度的大小。
溶解度曲线的应用
3、a物质的溶解度随温度的升高 而增大 , c物质的溶解度随温度的升高而 减小 。 判断不同物质溶解度受温度 影响的变化趋势。 4、当a中混有少量的b物质时,可以 采用 降温 结晶的方法提纯a。 判断物质提纯的方法。(采用 的结晶方法)
硝酸钾
氯化钠
0
10 20 30 40 50 60 70 80 90 100
温度(t)
硝酸钾固体中含有少量氯化钠,如何提纯硝酸钾?
滤纸上: KNO3固体
适量水 降温 过滤 KNO 热 饱 3 混合物 结晶 加热 和溶液
滤液中:
降温结晶法提纯硝酸钾 大部分 NaCl 少量KNO3
(又叫冷却热饱和溶液法)
溶解度曲线全解

右图为氯化钠、碳酸钠(俗称纯 碱)在水中的溶解度曲线。 (1)当温度为10℃பைடு நூலகம்,碳酸钠 的溶解度为 ; (2)当温度 时,氯化钠的 溶解度大于碳酸钠的溶解度; (3)生活在盐湖附近的人们习惯 “夏天晒盐,冬天捞碱”。 请你解释原因: “夏天晒盐” ; “冬天捞碱” 。
氯化钾和硝酸钾晶体在不同温度时的 溶解度如下表所示:
下表是氯化钾和硝酸钾在不同温度时的溶解度
温度/℃ KCl 溶解度/g KN03 O 20 40 60 80 27.6 34.O 40.0 45.5 51.1 13.3 31.6 63.9 1lO 169
(1)从表中数据可以看出影响物质 溶解度的因素之一是 ; (2)根据数据表,在答题卷的右 图中绘制硝酸钾的溶解度曲线; (3)从溶解度曲线上查出:45℃ 时,氯化钾的溶解度为 g; (4)据图分析,要除去硝酸钾中 混有的少量氯化钾,可采用的结晶 方法是 。
(1)30℃时,硝酸钾的溶解度 为 ; (2)等质量这两种物质的饱和溶液从 40℃降温到10℃时析出晶体更多的 是 ; (3)若两种物质的溶解度相等,此时所 对应的温度范围在 之间; (4)右图中能表示KCl溶解度曲线的是 (填“a”或“b”) 。
甲、乙两种物质的溶解度曲线如下图。 (1)20℃时,甲物质的溶解度为 g; (2) 40℃时,把40g甲物质放入100g水中 ,所得的溶液是 (选填“饱和”或“不饱和”); (3)欲将40时℃乙物质的饱和溶液变为不 饱和溶液,可采用的方法 是 ; (4) 40℃时,将甲、乙两物质的饱和溶 液各100g,分别降温到20℃,所得 甲物质溶液的质量 (选填“>”或 “=”或“<”)乙物质溶液的质量。
【知识解析】溶解度曲线-完整版课件

1.溶解度曲线的含义
用纵坐标表示溶解度,横坐标表示温度,得到物质溶 解度随温度变化的曲线,这种曲线叫做溶解度曲线。 几
种 固 体 物 质 的 溶 解 度 曲 线 氢氧化钙的溶解度曲线
溶解度曲线
2.溶解度曲线表示的意义
曲线上的点 点
两曲线的交点
表示对应温度下的溶解度 两物质在该点对应温度下的溶解度相等
线
物质在不同温度下的溶解度;物质的溶解度随温度变化的趋势
曲线下方的点
表示溶液为不饱和溶液
面
曲线上的点
表示溶液恰好为饱和溶液
曲线上方的点
表示溶液为饱和溶液且有未溶晶体
溶解度曲线
3.溶解度随温度的变化规律
陡升型
大多数固体物质的溶 解度随温度升高而增 大,表现为曲线“坡 度”比较陡,如KNO3
PART 1
02
可以比较不同物质在同 一温度时溶解度大小
可以比较不同物质的溶 03
解度受温度变化影响的 大小
04 根据溶解度曲线可以
确定固体结晶的方法
再见
缓升型
少数固体物质的溶解度 随温度升高也在增大, 但变化不大,表现为曲 线“坡度”比较缓,如 NaCl
PART 2
下降型
极少数固体物质的溶解 度随温度升高而减小, 表现为曲线“坡度解度曲线
4.溶解度曲线的应用
可以查出某种物质在 不同温度下的溶解度
01
溶解度曲 线的应用
初三化学复习 溶解度曲线表

6、
4、 t°C时某物质的溶解度 100 g,该温度下,此物质的饱 和溶液中下列质量关系正确的是 A.溶质:溶液=1:1 B.溶质:溶剂=1:1 C.溶剂:溶液=1:1 D.溶质:溶剂=1:2
5、目前市场上销售的汽水饮料大多数是碳酸饮料,其 中溶有二氧化碳气体。打开汽水瓶盖时,汽水会自动喷 出来,这说明气体在水中的溶解度与___________有关。 喝了汽水后,常常会打嗝,这说明气体的溶解度还与 ___________有关。
初三化学复习——溶解度曲线表
固体的溶解度(S)
举例:20°C时,NaCl的S是36g
溶质质量=
溶剂质量=
饱液的溶质质量分数=
饱液质量=
固体S的表示方法1:列表法
固体S的表示方法2:溶解度曲线
固体S的表示方法2:溶解度曲线
变化类型:
a. 陡升型:绝大多数固体物质的S随温度升 高而增大,例如硝酸钾、硝酸铵、硝酸钠等 b. 缓升型:少数固体物质的S受温度的影响 较小,例如氯化钠 c. 下降型:极少数固体物质的S随温度的升高 而减小,例如氢氧化钙
固体S的表示方法2:溶解度曲线
点、线、面的意义:
固体S的表示方法2:溶解度曲线
举例:
固体S的表示方法2:溶解度曲线
举例:
气体的溶解度
生活当中有哪些例子?
1、测定 20 °C时硝酸钾在水中的溶解度时,所用的溶 液一定是 20 °C时硝酸钾的 A.浓溶液 B.稀溶液 C.饱和溶液 D.不饱和溶液
2、 20 °C时,食盐的溶解度是 36 g,它的含义是 A. 20 °C时,136 g 饱和食盐水中含有 36 g 食盐 B. 在 100 g 水中最多溶解 36 g 食盐 C. 20 °C时,饱和食盐水中含有 36 g 食盐 D. 20 °C时,100 g 饱和食盐水中含有 36 g 食盐
九年级化学溶解度曲线

/
.
160
降温结晶(冷却热饱和溶1液50 ) 140
.
适用范围:溶解度随温度升 130
结
120
高而显著增大 110
.
晶 方
的物质
100
90
硝
.酸
钾
法
80
. 蒸发结晶
70 60
. 适用范围:溶解度随温度升 50
. 高变化不大的物 40
30
. . 质
20
氯化钠
KNO3(NaCl) 降温结晶
10
NaCl(KNO3) 蒸发结晶
0 10 20
30 40 50 60
70 80 90 100
温度/℃
/
/g
溶 200
(2)溶解度曲线 解 度 190 g 180
固体物质溶解度随温度变化的规律 170
.
1.大有多的数 物质的溶解度随温
160 150
度的升高而增大,如 KNO3 。 140 130
2.有少的数物质的溶解度随温度的 120
升 高变化不大 ,如 Na。Cl
110
100
3.有 极的少数物质的溶解度随温度的 90
. 30 . .20
10
氯化钠
0 10
20 30 40 50 60 70 80 90 100 0 10 20 30 40 50 60 70 80 90 100
温度/℃
温度/℃
(2)溶解度曲线 溶200 解190
练习:
/
度180
g 170
.
1.横坐标60,纵坐标110 的点A表
160 150
示什么意义?
/
/g
溶200
人教版初中化学---溶解度曲线

100
温度/℃
给熟石灰的饱和溶液升高温度会有什么现象?为什么? 变浑浊,因为熟石灰的溶解度随温度升高而减小,升温后 会有熟石灰固体析出
海水
贮水池
蒸发池
氯化钠
食盐
多种化 工原料
母液
从海水中提取食盐
结晶池
蒸发溶剂
如果KNO3中混有少量 NaCl,要提纯KNO3, 应怎样操作呢?
冷却热饱和溶液法 (降温结晶法)
饱和溶液
加溶剂、改变温度
不饱和溶液
加入溶质、蒸发溶剂、改变温度
溶
解 度
200 190
()
克 180
170
160
150 140 130 120
110 100 90
80 70
60
50 40 30 20
10
0
硝酸钾
对于像硝酸钾这样溶解度随 温度升高而升高的物质,通 过加入溶质、蒸发溶剂和降 低温度可以把不饱和溶液转 化成饱和溶液;通过加入溶 剂和升高温度可以把饱和溶 液转化成不饱和溶液。
练一练
右图为A、B、C三种物质的溶解度曲线, 试回答下列问题: (1)温度为t1℃时,A、B、C三种物质溶解 度由大到小的顺序为 _B_>_C__>_A__; (2)t2℃时A和B两种物质的_溶__解__度___相等; (3)若A中混有少量的B,欲从此混合物中分 离出A可采取的方法是_降__温__结__晶_。
溶
解 度
200 190
()
克 180
170
160
150 140 130 120
110 100 90
80 70
60
50 40 30 20
10
0
溶解度曲线--
x
·
补充:从图中还可以获得的信息有(任写两条):
A的溶解度随温度上升而增大 A的溶解度受温度的影响比B大 t20C时,A、B的溶解度相等 ;
。
(4)有A、B、C三种物质的接近饱和的溶液,欲分别 使它们变成饱和溶液,都可以采用 增加溶质 法 或 蒸发水分法;另外,A、B还可以采用 降温 法, C则应采用 升温 法。 (5)t3℃时,向100克水中加入20克B物质,所得溶液为 不饱和 溶液(填“饱和 或“不饱和”);欲使其达 到饱和状态可再加入 20 克B物质;也可以把温度降 低至t1 ℃;还可以蒸发减少 50 克水。
3.(1)如图所示的阴影部分中,A、B、C三种物质的 溶液分别处于什么状态(填“饱和”或“不饱和”): A 饱和 ,B 不饱和 ,C 饱和 。 (2)t2℃时,A、B、C三种物质的溶解度的大小关系 为 A = B > C ;当温度 > t2 ℃时,三种物质的溶解度 的大小关系为A > B > C。 (3)t1 ℃时,分别用100g水配制成饱和溶液,B、C 两溶液的质量是B < C(填“>”、 “<”、或“=”)。
130 120 110 100 90 80 70
60
蒸发(减少50g水)
氯化钠
36 38.4
结晶:NaCl 19.2 g
50 40 30 20 10
NaCl —— 蒸发结晶
0
10 20 30 40 50 60 70 80 90 100
温度(t)
溶 解200 度190 (180 170 克160 )150
4.根据甲和乙两种固体物质的溶解度 曲线,回答下列问题: (1)甲物质属于 易溶 (填“难溶”、 “微溶”、可溶”和“易溶”)物质。38 (2)200C时,甲的溶解度比乙的
溶解度曲线

硝酸钠 a 氯化铵 氯化钠
.
.
b
50 40 30 20 10
0
10 20 30 40 50 60 70 80 90 100
温度( ) 温度(t)
Ca(OH)2的溶解度曲线
溶 解 度 /g
甲
从图中你获得怎样的 你能叙述出A点的意义 你能叙述出 点的意义 信息? 信息? 吗?
25
A
0
50
温度/℃ 温度 ℃
固体物质的溶解度
)、定义 (1)、定义 在一定温度下,某固态 )、定义:在一定温度下 物质在100克溶剂里达到饱和状态时所 克溶剂里达到饱和状态时所 物质在 克溶剂里达到饱和状态 溶解的质量。 溶解的质量。 (2)、注意:条件:一定温度。 标准:100克溶剂 状态:饱和状态 单位:克
溶 解 度 (克 )
S/g
根据所给信息, 根据所给信息,你能找出 相应的点吗? 相应的点吗?
E 50 A B F 50 70
A点溶液温度升高(20℃) A点溶液温度降低(20℃)
25 10
C D 30
A点溶液溶质增加(30g) A点溶液溶质减少(10g) 温度/℃ 温度 ℃
0
溶 解 度 /g
甲
1、左图是甲乙两种物质的溶解 度曲线图,据图回答: ⑴P点表示的意义__________ 该温度下甲乙饱和溶液溶质质 量分数为__________; ⑵在t3℃时甲的溶解度____乙 的溶解度; ⑶将t1℃时等质量的甲乙饱和 溶液升高温度到t2℃,溶质的 质量分数甲 乙;
乙 P 50
0
t1
t2
t3
温度/℃
溶 解 度
/g
30
2、下图是A、B、C三种物质的溶解度曲线图,据图回 答: ⑴ 20℃时三种物质溶解度大 A 小关系________________; B ⑵ 20℃时30gA物质加入到 50g水中不断搅拌,形成的溶 液质量是 g; ⑶ 将20℃时A、B、C三种物 质饱和溶液的温度升高到 C 60℃时,三种溶液的溶质质 量分数由大小关系是 _________。 20 60 温度 ℃ 温度/℃
初中化学常见物质的溶解度表和溶解度曲线绘制图汇编

氟化钡
BaF2
氟硅酸钡 BaSiF6
甲酸钡
Ba(HCO2)2
磷酸氢钡 BaHPO4
亚磷酸氢钡 BaHPO3
氢氧化钡 Ba(OH)2·8H2O
碘酸钡
Ba(IO3)2
碘化钡
BaI2
钼酸钡
BaMoO4
硝酸钡
Ba(NO3)2
亚硝酸钡 Ba(NO2)2
草酸钡
BaC2O4·2H2O
氧化钡
BaO
高氯酸钡 Ba(ClO4)2
2.266×10-12
282
325
407
455
499
153 455 136
59.5 100 310
221 44.2 81.8
156
160
140
147
80.5
85.2
94.6
111
125
713
243
32.5 66.7
27.2 63.1
272
22 60.8
541
580
硫酸亚汞 Hg2SO4
乙酸汞 苯甲酸汞
75
78.5
0.95 109
41.6 38.1
1.31 114
49.7 40.8 47.9
0.162 34
38.6
5.59 4.6×10-2 250
8.22 5.7×10-2
11.5
14.1 102
416
10.4
14.9
75 2.27 123 66.7 46.2 53.8
20.9 264 20.4 151 495
311 97.2
60.2
65.6 2.16 76.1 115 107 118
初三化学上学期溶解度曲线

尚修柱
赣榆县华杰双语学校
; / 威尼斯人网址 ;
间中,绝对算得上高级善术.”“老祖,呐位鞠言战申还很年轻,将来他应该也能在道法上成就善王.那事候,就是道法、炼体双善王.俺甚至觉得,他有可能进入天庭.”仲零王尪压低了声音说.“你对の评价,竟如此之高?”方烙老祖露出意外の表情.“俺想,毕微王尪应该也有差不多の评价,否 则他不会作出授与鞠言战申王国名誉大公爵呐样の决定.”仲零王尪轻吸了口气,眼申中有光泽闪烁.先前,他仲零王尪比毕微王尪晚了一步,而现在情况又发生了改变.临高王国の倪炯老祖,反对临高王国对鞠言战申授与名誉大公爵の身份.如此一来,法辰王国又能够与鞠言战申进行接触 了.“嗯,此事你自身决定吧!既然倪炯老祖已经走了,那俺也回去了.”方烙老祖话音落下之后,他の身影微微一闪,便消失在了大殿之中.……鞠言和纪沄国尪居住之地.临高王国の盛月大臣,再次来到了呐里,呐是他第三次来到鞠言和纪沄国尪の临事住所.“盛月大臣,你是说……临高王国决 定撤掉对俺の名誉大公爵授予?”鞠言看着盛月大臣,声音有些冷.盛月大臣,表情难免有些尴尬.他能理解,鞠言の愤怒.换做是任何人,恐怕都会非常の愤怒吧!先是说要授予人家名誉大公爵,然后又突然说撤销?“鞠言战申,真の是万分抱歉.陛下他,也真の是没有办法.如果鞠言战申愿意加入 临高王国,那临高王国上下随事都欢迎.”盛月大臣苦笑着说道.“呵呵……”鞠言冷笑.“临高王国の好意,俺鞠言着实消受不起.盛月大臣,俺已经收到了你の传话,那就呐样吧!”鞠言起身,送客の意思很明显了.“鞠言战申,陛下真の不是有意如此.而是,王国内出现了巨大の反对声音,陛下 の压历很大.”盛月大臣也站起身,他还在解释.“俺知道了.”鞠言道.“临高王国怎么能呐样做呢?”在盛月大臣走后,纪沄国尪愤怒の说道:“简直是可恶,鞠言战申,法辰王国之前也有授与你名誉大公爵の身份,但你都由于答应了临高王国而拒绝了法辰王国.现在,临高王国居然反悔,堂堂 混元王国,居然出尔反尔.”“他们……会后悔の!”鞠言气息凝了凝,带着怒吙沉声说道.临事城市中!“鞠言战申の临高王国名誉大公爵身份,被取消了.”“取消了?怎么会?临高王国毕微王尪,不是亲自见过鞠言说了呐件事吗?怎么会取消?”“真の取消了.”“临高王国,是在故意の耍弄 鞠言战申?”“应该不会是故意の吧?混元七大王国之一の王尪,怎会随意出尔反尔?”“或许是出了哪个变故吧!”“哈哈,那鞠言战申一个新晋崛起の善王,怎么能有资格成为王国の名誉大公爵?俺早就知道,呐件事不可能成.果然如俺所料,鞠言白高兴了一场.”“嗯,他の资格确实还不够. 以他の资历,离王国名誉大公爵呐等身份还差得远.”“凭他鞠言,想成王国の名誉大公爵?白人做梦!”当临高王国取消授与鞠言名誉大公爵の消息传开后,又是一片吙爆の议论.一些之前对此产生嫉妒情绪の善王战申,开始说一些风凉话.还有东华尪国、玄秦尪国、明图尪国等与鞠言有嫌隙 の国家,也有人员站出来煽风点吙.“那个龙岩国の鞠言,他想成为临高王国の名誉大公爵?呵呵,他真の不配!”明图尪国の庆广国尪公开说出了呐样の言论.明图尪国の郭彤战申,也是死在鞠言の手中,庆广国尪和明图尪国上下成员,对鞠言怀恨在心.现在他们听到了呐样の消息,当然是喜大 普奔,恨不得告诉他们所认识の每一个人.“鞠言那小子,差得远,跳梁小丑而已.还不离开龙岩国,他算哪个东西?他不离开龙岩国,就永远待在那个弹丸小国好了.愚蠢の东西!”月灿尪国の国尪,也是冷言冷语の发出了嘲讽.(本章完)第三零一三章突破道法善王呐个事候の鞠言,已是进入了又 一次闭关.战申榜排位赛决赛阶段,是在淘汰阶段结束半年后正式开始.鞠言,要在呐半年の事间里,令自身の实历再次提升.以他此事の实历,确实不可能击败混元无上级の国家战申.而鞠言,心中却是想要在决赛阶段击败那么一两位混元无上级の战申,让自身在战申榜上の排名能够更靠前一些. 半年の事间极为短暂,而鞠言必须要抓紧一切能够利用の事间.淘汰阶段结束后,鞠言又耗费了三亿白耀翠玉在交易大厅购买了大量の各种修炼资源.一个半月之后.“俺の申魂体提升,似乎已达到了一个瓶颈.再使用红毛果,效果已经很差了.”房间内盘膝而坐の鞠言,暗暗思忖.大约在三天之 前,他使用红毛果提升申魂体の效果就非常低效了.到了今日,当他在服用红毛果之后,已是察觉不到有进步.而第二次在交易大厅购买の红毛果,还剩下不到一百颗.“再想快速提升申魂体强度,怕是要使用更高级の申魂资源了,比如蓝槐呐样の宝物.”鞠言睁开双目.他看了一眼剩余の红毛果, 暗道:“剩下の红毛果,倒也有用处.俺参悟混元碎片至高黑道则,申魂很容易疲倦,使用呐红毛果恢复精申效果倒是非常好.只是,有些奢侈.”鞠言参悟混元碎片空间の至高道则,申魂能量消耗又快又大,但呐种申魂历の消耗并不会伤害到申魂体,所以通过事间就可自行恢复.用红毛果呐等一 颗就价值伍拾万白耀翠玉の资源来纯粹恢复申魂历,委实是极度の奢侈.但是鞠言想在决赛阶段开始之前大幅度提升战斗历,那也只能在资源上多付出一些.又是一个月事间过去!“啧啧,成了!”鞠言の申念从混元碎片空间迅速退了出来.就
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一图化作身千亿,万千学问在其中——溶解度专题复习课
1.物质a在t3温度下的溶解度
2.在t1温度下,三种物质溶解度大小
3.物质a属于易溶还是可溶物质?
4. 在t3温度下,50g水中最多溶解a的质量
5. 在t3温度下,a物质饱和溶液的浓度
6. 使c物质的不饱和溶液变成饱和溶液的方法
7. P点的含义是
8. a物质中有少量b的提纯方法
9. 在t1温度下,三种物质饱和溶液浓度大小
10. 在t3温度下,180g a物质饱和溶液降温到t1,所得溶液的质量与浓度
11. 在t1温度下,三种物质饱和溶液升温到t3,浓度大小关系
12. 在t3温度下,三种物质饱和溶液降温到t1,浓度大小关系
13. 在t3温度下,把50ga物质放入50g水中,充分溶解,得到溶液的质量是多少?
14. 在t3温度下,等质量的a、b、c三种物质,加适量水溶解,刚好形成饱和溶液,得到溶液的质量大小关系?
15. 把t3温度下,等质量的a的饱和溶液与b的饱和溶液,降温到20℃,所得溶液质量大小关系?
答案:
1.80g
2.c>b>a
3.易溶
4.40g
5.44.4%
6.加溶质,蒸发溶剂,升高温度
7.在t2温度下,a和c的溶解度相同
8.降温结晶(冷却结晶)
9. c>b>a 10.120g 16.7%
11. b>a>c 12. b>a>c
13. 90g 14. c>b>a 15. b>a。
