煅制工艺规程
常规中药前处理煅制药材岗位操作规程

常规中药前处理煅制药材岗位操作规程目的:建立煅制工作程序,保证煅制工作规范有序,避免差错,确保药品质量。
范围:适用于前处理车间煅制的生产操作。
职责:车间主任、设备管理部门、设备操作人、设备保养员。
内容:1、生产准备:1.1操作人详细阅读批生产指令。
1.2 检查煅炉状况,应有正常状态标志。
1.3 检查煅炉、容器具清洁,应有清洁状态标志。
2、生产操作:2.1 到待炮制净药材中转间领取药材,核对品名、批号、规格、数量。
2.2 点试煅炉(一开一关),煅炉无阻碍时,再重心开起煅炉使煅炉正常运转。
2.3 打开煅炉的液化汽管道的控制阀,顺次打开点火开关,火点着后,将火候调到猛火。
2.4 煅筒烧热后,打开进药炉门,将100.0㎏煅药投入煅筒(煅药约占煅筒体积2/3)。
投完煅药后关好时药炉门进行翻煅。
2.5 约煅4小时,煅药筒开到倒转,加开煅炉出药炉门,放出适量的药材着,块状蛎内部洁白,易酥脆已煅透,赤石脂内外红透已煅透。
将煅药全部放出,装入不锈钢槽推车里。
药放完后,煅炉开到正转后进行煅制下锅药。
2.6 放出部分药材看时,如没有煅透时,把放出的药材投入锅内继续煅,每隔15分钟放出来看一次煅药,直到煅透为止。
3、生产结束:3.1 给不锈钢槽推车挂上药品状态标志(包括品名、批号、数量、规格),送到晾药间晾凉。
3.2 当日生产完毕清场:3.2.1 清扫地面的外包装和废弃状态标志等废弃物送到场外指定的场所。
3.2.2 用毛刷刷去煅药机外壁的灰尘。
3.2.3 煅药机的外壁用湿抹布抹尽灰尘后,再用干抹布抹干外壁的水。
3.2.4 生产工具送到清洗间清洗。
4、注意事项:4.1 煅药机煅完药后,将火熄灭。
再空转约30分钟后,停止运转。
冷至常温后,用高压水枪将煅筒内的残留药冲洗干净。
冲洗干净后,再用干抹布擦干水。
4.2如遇停电,应立即熄灭炉火。
——————————————。
中药炮制工(高级) 第三章 第一节 煅制(3

谢 谢
知识要求 第三ห้องสมุดไป่ตู้ 中药炮制
第一节 煅制
——闷煅法
三、闷煅法
(一)定义 将药材生品在高温缺氧条件下煅烧成炭的
方法;又称扣锅煅、密闭煅、暗煅。 (二)炮制目的
(1)改变中药性能,产生新的疗效,增强 止血作用,如血余炭,棕榈炭等。
(2)降低毒性,如干漆、蜂房等。
三、闷煅法
(三)炮制工艺 1.将药材生品置于锅中,上扣一小锅,两锅合 处用盐泥封严,扣锅上压一重物,防止锅内气 体膨胀冲开扣锅。 2.扣锅底部贴一白纸条或放几粒大米,武火煅 至白纸条或大米变黄、中药全部炭化为度。 3.或在两锅封闭处留一小孔,用筷子塞住,随 时观察小孔处的烟雾,当烟雾由黄转青,之后 逐渐减少时降低火力,煅至基本无烟时离火, 完全冷却后取出。 4.大生产中具有密闭功能的特制转炉可完成传 统炮制的闷煅过程。
三、闷煅法 (五)适用中药-棕榈
炮制方法: 净棕榈段或棕板块置锅内,上 扣小锅,两锅合处盐泥固封, 上压重物,并贴一片白纸条或 几粒大米,武火煅至白纸或大 米呈深黄色停火,锅凉后取 出。
三、闷煅法 (五)适用中药-棕榈
质量要求: 不规则块状,表面黑褐色至黑 色,有光泽,略有焦香,味苦 涩。 炮制作用: 味苦、涩,性平,归肺、肝、 大肠经;功效为收敛止血。
三、闷煅法 (五)适用中药-莲房
炮制方法: 莲房碎块经煅炭法或炒炭法 (净莲房碎块置锅内,武火 加热炒至表面黑色、内部焦 褐色,喷淋清水熄灭火星, 取出晾干)制备。
三、闷煅法 (五)适用中药-莲房
质量要求: 形如莲房块,表面焦黑色,内 部棕褐色。 炮制作用: 味苦、涩,性温,归肝经;功 效为化瘀止血;制炭后收涩力 增强,用于崩漏、尿血、痔血 等下部出血症。
中药炮制学——煅法

石膏
炮制方法: 煅石膏:取净石膏块,置容器中,武火加热煅 至红透,取出放凉,研碎。
炮制目的: 生:清热泻火、除烦止渴 -- 白虎汤 煅:收湿生肌、敛疮止血 -- 九一散
硼砂
P258
炮制方法:
煅硼砂:取净硼砂适当破碎,置容器中,武 火加热煅(炒)至鼓起小泡成雪白疏松块 状,取出放凉,研碎。
炮制目的: 煅后燥湿收敛固涩。 (喉科用药) -- 冰硼散
一 蒸法
❖ 药物加辅料或不加辅料,装入蒸制容器内 隔水加热至一定程度的方法,称为蒸法。
❖ 不加辅料者为清蒸,加辅料者为合蒸。
❖ 直接利用流通蒸汽蒸煮称为“直接蒸法”。 在密闭条件下隔水蒸者称“间接蒸法”(炖)。
一 蒸法
目的:改变药性,扩大用药范围:地黄 减少副作用:黄精、大黄 保存药效,利于贮存:黄芩、桑螵蛸 便于软化切片:天麻、木瓜
炮制研究
远志
❖ 传统要抽去木心,取根皮入药。
1.化学:远志皮和远志木心的化学成分种类相 同。而皮部皂苷含量是木心的25倍。
2.药理:远志皮的去痰、抗惊厥和溶血作用及 急性毒性均较远志木心为强。
∴ 远志去心的目的不是降低毒副作用,而是去 除药效较弱的部位。
吴茱萸
炮制方法: 1.吴茱萸 2.制吴茱萸:取甘草切片或破碎,加水适量煎
梓醇苷苷元→加热聚合,聚合物:黑色 糖→与氨基酸结合→蛋白黑素(黑色)
何首乌
炮制方法:
1.何首乌:取原药材,除去杂质,洗净,稍浸, 切厚片或块,干燥。筛去碎屑。
2.制首乌:取生首乌或块,用黑豆汁拌匀,润 湿,置非铁质蒸制容器内,密闭,蒸或炖至汁 液被吸尽药物呈棕褐色时,取出,干燥。 何首乌每100kg,用黑豆10kg 。
3.酒五味子:取净五味子,加酒拌匀稍闷,蒸 至酒尽,转黑色,取出晒干。(100:20)
精选煅烧设备工艺及操作规程

通过冷却后常温100~120℃的物料落入S0208,S0209电子胶带输送机计量后(B500,L8500,β=0°,V0.8m/s,Y1175-80-5050/3KW,耐高温皮带)输送给—S0211,S0212斗式提升机(TD350,H33043mm,输送量45~50t/h,物料容量0.75t/m³,斗容5.8L,斗距280,斗速1.36m/s,滚柱逆止器)通过S0210电液三通下料溜管转换二台斗提交替使用。—S0213,S0214转换电液翻板阀下料到S0215,S0216胶带输送机B500,L8500,β0°,V=0.8m/s,Y1175-80-5050/3KW,进入煅后料仓—料仓底部S0217,S0218,S0219,S0220电动插板控制通过伸缩溜槽S0221,S0222,S0223,S0224进入运输车外售
知道了原料在窑内的流动速度就很容易计算出原料通过回转窑的时间,即原料在回转窑内的逗留时间T:
T=L/Vm
式中: T ——物料通过回转窑的时间(分钟)
燃烧器坐落在地面轨道上,可移动。离心风机9-19-9P,风压1597-4551Pa,风量30695-7511m³/h,功率1.5KW,转速1450r/min。干气风等均匀的转联接,可随燃烧器前后移动。燃烧器内配置环风,助燃风,使燃气充分雾化燃烧,环保、节能。关火装置变压器放电打火,安全阀、关火枪、电子阀自动开启点火,火焰检测器检测到火焰后,停止打火。自动化控制较高,安全,操作方便。
(1)煅前仓储运: 铲车将原料送入格网料斗S0101,格网孔Φ200mm,—惯性振动给料机S0102,100t/h,双振幅根据振幅大小调节给料量至双辊齿式破碎机S0103,破碎粒度调整双辊间隙破碎至Φ100mm——胶带输送机S0104,B650,L10800,β11.5°,V′=0.8m/s,5.5KW,——磁力除铁器S0105,除去铁物至斗式提升机S0106,H23.8m,输送管170m³/h,斗速1.41m/s,斗容14.4L。驱动电动机,逆止装置,滚柱逆止器,——电动插板S0107-S0108电液三通插板阀。—S0109可逆式胶带输送机,B650,L10700,β0°,V=0.8M/S,7.5KW,C二台。
煅制工序操作规程

目的:建立煅制工序标准操作规程,统一规范煅制工序的操作,保证中药饮片生产的均一性。
范围:适用于本公司中药饮片车间煅制工序。
职责:煅制岗位操作人员对执行本规程负责,上、下工序操作人员、车间主管及车间QA对执行本规程相关内容负责,车间QA负责监督本规程的执行。
内容:1.生产前准备:1.1. 复核清场清洁情况,确认无上次遗留物。
1.1.1. 确认生产场地无与本批生产相关的文件及杂物。
1.1.2. 检查煅制室门上的状态标示牌是否为“清场清洁合格证”,证上是否有车间QA的签字,是否在有效期内。
1.1.3. 车间QA按《生产场地清场清洁操作规程》复核清场清洁情况。
1.2. 接受生产指令:1.2.1. 接受“批生产指令”、“煅制生产记录”、“中间产品标签”等文件。
1.2.2. 仔细阅读“批生产指令”、“煅制生产记录”,清楚了解生产的产品名称、产地、批号、批量、使用设备及操作规程,工艺参数及要求、注意事项等煅制操作指令。
1.3. 物料准备:1.3.1. 根据指令到上一工序领取待煅制物料。
1.3.2. 阅读中间产品标签上的内容,核对其品名、产地、批号是否与生产指令相符,数量是否与实物相符,是否有车间QA的签名及日期。
1.3.3. 检查待煅制物料是否超过最长加工期限,是否霉变有异味。
1.3.4. 根据生产指令领取周转容器,清点的同时检查是否已清洁干净,有无破损。
1.3.5. 将待煅制物料、周转容器分别运到煅制室,置于指定位置。
1.3.6. 领取煅制物料的同时,把本批的“生产记录”文件夹带到煅制室,置于记录台上。
1.4. 设备检查:1.4.1. 根据《煅药锅操作及维护保养操作规程》检查煅药锅。
1.4.2. 合上电源开关后,打开炒药机或煅药锅的电源开关,检查该设备空车运行情况是否有异常响声,是否运行正常。
1.4.3. 根据生产指令设定煅药锅的煅制温度和煅制时间。
1.5. QA确认并发证:1.5.1. 操作人员认为准备工作就绪后,向车间QA申请检查。
煅牡蛎工艺规程

目录2、生产工艺流程4、质量监控:见“SCGL509301 煅牡蛎生产关键工序质量监控要点”。
5、原辅料、半成品、成品质量标准5.1 牡蛎原料质量标准:见“ZLJS100101 原药材质量标准”。
5.2 煅牡蛎中间产品质量标准:见“ZLJS400101 饮片中间产品质量标准”。
5.3 煅牡蛎成品质量标准:见“ZLJS500101 饮片成品质量标准”。
6、包材质量标准和文字说明6.1 包材质量标准:见“ZLJS300101~ZLJS300601包装材料质量标准”6.2 包装说明文字:品名:煅牡蛎规格:产地:重量:产品批号:生产日期:贮藏:置干燥处生产企业:7、生产区的工艺卫生要求7.1 生产区卫生要求:执行“CSGL001401一般生产区环境卫生管理规程”, 7.2 生产区清洁工作要求:执行“CSSOP000301一般生产区厂房清洁规程”, 7.3 生产区人员卫生要求:执行“SCGL000101一般生产区个人卫生规程”, 7.4 生产区工作服管理要求:执行“SCGL005701一般生产区工作服管理规程”9、技术经济指标核算9.2包装材料物料平衡使用量+残损量+剩余量塑料袋物料平衡= ×100%(99.0-101.0%) 本批领用量使用数+残损数+剩余数标签物料平衡= ×100%(99.0-101.0%) 本批领用数10、技术安全及劳动保护10.1 员工转岗或新工上岗前均要进行安全操作培训,熟悉本岗位的操作要点、质控要点及注意事项。
10.2 严格按工艺规程和岗位标准操作程序操作,切忌擅改工艺和岗位操作方法,工作应严肃认真。
10.3 电机设备严禁用水直接冲洗,清洁时亦不可用湿布擦拭。
在确保一切准备工作就绪后方可开机,以防轧手等事故发生。
10.4 设备定期保养,严格按设备维护保养管理制度操作使用。
10.5 拣选、切药、干燥、筛分等产尘、产湿岗位应有除尘排湿装置。
11、劳动组织和岗位定员11.1 劳动组织11.1.1 由生产制造部下达生产指令,车间依此组织生产。
锻造工艺规程制定

锻造工艺规程制定
(5)冲孔连皮 当模锻件的孔径D>25mm时,应将孔形锻出,
由于模锻不能锻出通孔,则在孔中留出冲孔连皮,
当孔径D为25~80mm时,其厚度取为4~8mm。
锻造工艺规程制定
二. 坯料质量及尺寸计算
1 坯料质量
G坯料=G锻件 + G烧损 + G料头
镦粗时的锻造比:y = H0 / Hm
锻造工艺规程制定
例题:锻造比常用来表示什么?拔长与镦粗时的锻造
比 用 什 么 来 表 示 ? 如 原 始 坯 料 长 150mm , 拔 长 到 450mm,锻造比是多少?
y = F0 / Fm
根据锻造前后体积不变假设
VV y H0 150 450 3
锻造工艺规程制定
例题:指出下图所示模锻件结构不合理之处。 试修改不合理部位(重画图)。
结构不合理之处: (1)模锻斜度与圆角;(2)壁厚差太 大,轮辐部分壁太薄;(3)齿轮的齿锻不出来,必须 用机加工,未考虑锻敷造工艺料规程制;定 (4)未考虑冲孔连皮。
V V 150 H 450
锻造工艺规程制定
三、确定模锻工步——根据锻件形状和尺寸确定
1. 长轴类模锻件 此类锻件在锻
造过程中,锤击方 向垂直于锻件的轴 线。
常用工序: 拔长、滚压、弯曲、 预锻和终锻。
锻造工艺规程制定
对于小型长轴类锻件,为了减少钳口料和提高 生产率,常采用一根棒料同时锻造出几个锻件的方 法,此时应增设切断工步。
(a)工艺性差的结构
(b)工艺性好的结构
锻造工艺规复程制杂定 结构件
例题:指出下图所示自由锻件结构不合理之处。试修
第四节 自由锻工艺规程的制订

锻出头部
拔长
1
拔长及修整台阶
拔长并留出台阶
锻出凹档及拔长端部并修整
计算变形力 确定设备吨位
• 1.理论计算法(P70~73) • 2.经验计算法
• (五)确定锻造温度范围 • 锻造温度范围是指始锻温度和终锻温度之间的温 度范围。 • 锻造温度范围应尽量选宽一些,以减少锻造火次, 提高生产率。加热的始锻温度一般取固相线以下 100~200℃,以保证金属不发生过热与过烧。终锻 温度一般高于金属的再结晶温度50~100℃,以保证 锻后再结晶完全,锻件内部得到细晶粒组织。碳素钢 和低合金结构钢的锻造温度范围,一般以铁碳平衡相 图为基础,且其终锻温度选在高于Ar3点,以避免锻 造时相变引起裂纹。高合金钢因合金元素的影响,始 锻温度下降,终锻温度提高,锻造温度范围变窄。部 分金属材料的锻造温度范围见表 。 • 此外,锻件终锻温度还与变形程度有关,变形程度较 小时,终锻温度可稍低于规定温度。
(一)绘制自由锻件图
以零件图为基础,结合自由锻工艺特点绘制而成的图形,它是工艺规 程的核心内容,是制定锻造工艺过程和锻件检验的依据。锻件图必须准确 而全面反映锻件的特殊内容,如圆角、斜度等,以及对产品的技术要求, 如性能、组织等。 绘制时主要考虑以下几个因素: 1.敷料 对键槽、齿槽、退刀槽以及小孔、盲孔、台阶等难以用自由 锻方法锻出的结构,必须暂时添加一部分金属以简化锻件的形状。 为了简化锻件形状以便于进行自由锻造而增加的这一部分金属,称为敷料, 如图所示。 2.锻件余量 在零件的加工表面上增加供切削加工用的余量, 称之为锻件余量,如图2-11所示。锻件余量的大小与零件的材料、形状、 尺寸、批量大小、生产实际条件等因素有关。零件越大,形状越复杂,则 余量越大。
1006-煅法生产工艺规程

生产工艺规程菏泽健民中药饮片有限公司目的:为饮片煅制法生产提供符合要求的生产工艺,规范饮片煅制操作,严格工艺管理,特制订本规程。
范围:本规程适用于饮片煅制法生产操作。
责任:生产车间、生产部、质量部。
内容:一、产品概述(一)产品名称、性状(二)煅制工艺简介1、定义;将药物直接放于无烟炉火中或适当的耐火容器内煅烧的方法。
将药物煅红后,趁炽热投入规定的液体辅料中淬之,称为煅淬法。
2、煅制目的:药物经过高温短少后,药物质地、药性、功效发生变化,使药品疏松,利于粉碎和使有效成分易于溶出,减少或消除副作用,从而提高疗效或产生新的疗效。
3、适用范围:主要适用于矿物类药材,以及质地坚硬的药物,如贝壳类、化石类等。
此外闷煅法多用于制备某些植物类和动物类药物的炭药。
4、煅制要求:煅制时要掌握药物粒度的大小和煅制温度、煅制时间关系,注意药物受热要均匀,掌握煅至“存性”的质量要求,植物类要特别注意防止灰化。
矿物类及其他类药物均需煅至体松质脆的标准。
5、煅制分类:明煅法、煅淬法、闷煅法。
5.1明煅法:煅制时不隔绝空气的方法。
本法适用于除闷煅以外的一切药物。
5.2煅淬法:将药物按明煅法煅烧至红透后,立即投入规定的液体辅料中骤然冷却的方法。
煅后的操作程序称为淬,所用的液体辅料称为淬液。
常用淬液有醋、酒、药汁等。
5.3闷煅法:药物在缺氧条件下煅烧成炭的方法。
适用于煅制质地疏松、炒炭易炭化及某些药材在制备过程中需要综合制炭的药物。
(三)煅制方法1、明煅法1.1目的:使药物质地酥脆;除去结晶水,如白矾、硼砂等;使药物有效成分易于煎出,如含碳酸钙类矿物药等。
1.2操作方法1.2.1敞煅法:将药物直接放入煅锅内,用武火加热煅制。
多用于含结晶水的易熔矿物类药。
如白矾等。
1.2.2炉膛煅:质地坚硬的矿物药,直接放于炉火中煅至红透,取出放凉。
煅后易碎或煅时爆裂的药物需装入耐火容器或适宜容器内煅透,放凉。
1.2.3平炉煅:将药物置炉膛内,武火加热并用鼓风机促使温度迅速升高和升温均匀。
自由锻造工艺规程的编制及举例
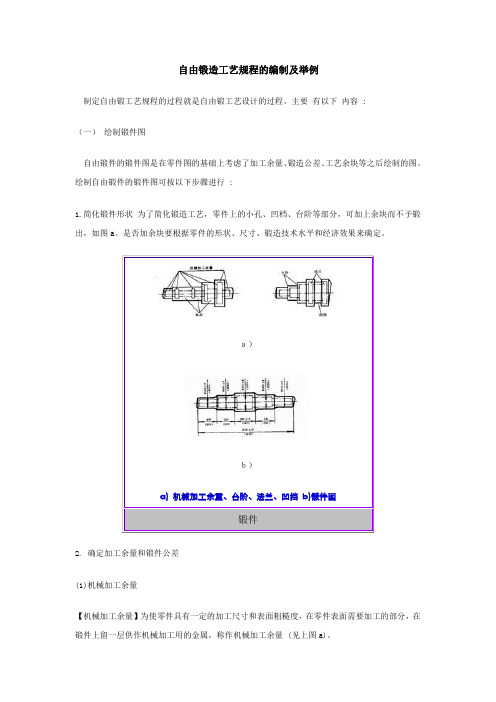
自由锻造工艺规程的编制及举例制定自由锻工艺规程的过程就是自由锻工艺设计的过程。
主要有以下内容 :(一)绘制锻件图自由锻件的锻件图是在零件图的基础上考虑了加工余量、锻造公差、工艺余块等之后绘制的图。
绘制自由锻件的锻件图可按以下步骤进行 :1.简化锻件形状为了简化锻造工艺,零件上的小孔、凹档、台阶等部分,可加上余块而不予锻出,如图a。
是否加余块要根据零件的形状、尺寸、锻造技术水平和经济效果来确定。
a)b)a) 机械加工余量、台阶、法兰、凹挡b)锻件图锻件2. 确定加工余量和锻件公差(1)机械加工余量【机械加工余量】为使零件具有一定的加工尺寸和表面粗糙度,在零件表面需要加工的部分,在锻件上留一层供作机械加工用的金属,称作机械加工余量 (见上图a)。
(2) 余块【余块】为简化锻件外形及锻造过程,在锻件的某些地方和添一些大于机械加工余量的金属,这种加添的金属称作余块 (见上图a)。
(3)锻件公差【锻件公差】锻件实际尺寸与基本尺寸之间所允许的误差。
公差值的大小是根据锻件形状、尺寸并考虑生产的具体情况而定的。
3.绘制锻件图在锻件图上,规定用粗实线绘出锻件的形状。
为了便于了解零件的形状和检查锻件的实际加工余量,在锻件图上还要用双点划线绘出零件的主要形状,如图10-27b。
(二)计算坯料质量与尺寸【坯料质量】坯料质量可按下式计算G 坯料 =G 锻件 +G 烧损 +G 料头式中 G 坯料——坯料质量G 锻件——锻件质量G 烧损——加热时由于坯料表面氧化而烧损的质量。
第一次加热取被加热金属的2~3%,以后每次加热取1.5~2.0%G 料头——在锻造过程中冲掉或切掉的那部分金属的质量。
如冲孔时坯料中部的料芯,修切端部的料头等。
当锻造大型锻件时,如采用钢锭作坯料,还要考虑应切掉的钢锭头部和尾部的质量。
2.坯料尺寸根据坯料质量即可确定坯料尺寸。
在计算坯料尺寸前,先要考虑锻造比。
【锻造比】是指坯料在锻造前后的断面积的比值。
对于拔长工序来说,其锻造比 R d 可按下式计算:R d =A 0 /A 1 或 L 1 /L 0式中 A 0 、 A 1 ——拔长前、后坯料的断面积;L 0 、 L 1 ——拔长前、后坯料的长度。
中药炮制工(高级) 第三章 第一节 煅制(2

二、煅淬法
(五)适用中药-炉甘石(2.制炉甘石)
炮制方法:①黄连汤拌:黄连加水 煎汤2-3次,过滤去渣,合并药汁 浓缩,加入煅炉甘石细粉中,搅匀 吸尽后干燥(每100kg煅炉甘石用 黄 连 12.5kg ) ; ② 三 黄 汤 拌 : 黄 连、黄柏、黄芩煎汤2-3次,过滤 去渣,合并药汁浓缩,加入煅炉甘 石细粉中,搅匀吸尽后干燥(每 100kg煅炉甘石用黄连、黄柏、黄 芩各12.5kg)。
炮制方法: 净炉甘石置耐火容器内武火加 热,煅至红透取出,立即倒入水 中浸淬搅拌,倾取上层混悬液 ( 煅 淬 法 ) ; 残 渣 继 续 煅 淬 3-4 次,至不能混悬为度,合并混悬 液,静置澄清后倾去上层清水干 燥(水飞法)。
二、煅淬法 (五)适用中药-炉甘石(1.煅炉甘石)
质量要求: 白色或灰白色无定形细粉,质 轻松。 炮制作用: 消除了由于颗粒较粗对敏感部 位的刺激,宜于眼科及外敷使 用。
二、煅淬法
(四)注意事项 (1)煅淬要反复进行几次,使液体敷料吸尽, 中药应全部酥脆为度,避免生熟不均。 (2)煅淬次数、所用的淬液种类和用量由各个 中药的性质和临床用药目的要求而定。
二、煅淬法 (五)适用中药-自然铜
炮制方法: 去净自然铜,置耐火容器,用武 火加热,煅至红透立即取出,投 入醋液中淬制,待冷后取出,继 续煅烧醋淬至黑褐色,外表脆 裂,光泽消失,质地酥脆,取 出,摊开放凉,干燥后碾碎。
二、煅淬法 (五)适用中药-自然铜
质量要求: 呈不规则的碎粒,黑褐色或黑 色,无金属光泽。质地酥脆,有 醋气,碾碎后呈无定形黑色粉 末。 炮制作用: 煅淬后增强散瘀止痛作用。
二、煅淬法 (五)适用中药-磁石
炮制方法: 净磁石块经煅淬法煅至红透, 醋淬,碾成粗粉。 质量要求: 呈不规则的颗粒或粉末,表面 黑色,质硬而酥,无磁性,有 醋香气。
煅制技术—明煅技术(中药炮制技术课件)

煅石决明
不规则碎块 (断面呈层状) 灰白色无光泽 或粗粉
气微,味微咸 气微,味微咸
质地 质坚硬 质酥脆
实操举例
生石决明:咸、寒,平肝潜阳, 清肝明目
煅石决明:咸寒之性降低, 平肝潜阳作用缓和,增强了 固涩收敛、明目作用,质地 疏松,利于涂敷散布,利于 有效成分煎出
实操举例
规格
形状
成品性状
颜色
气味
质地
白矾
不规则块状或颗 粒
无色或淡黄白色,有玻璃样光泽
气微,味酸,微甘而极 涩
质硬而脆
枯矾
蜂窝状或海绵状 固体块状或细粉
不透明、白色
味酸、涩
体轻质松, 手捻易碎
实操举例
生品:酸寒,解毒杀虫, 清热消痰,燥湿止痒
煅后酸寒降低,涌吐减 弱,增强了收涩敛疮、 止血化腐。
煅制概念
注意事项: 煅存性 植物类 大小分档 必须研细后才能入药
分类:明煅法、煅淬法、煅炭法
02 明 煅 技 术
明煅技术
净制并适当破碎的矿物药, 置于无烟炉火上或适当的耐火容 器内,不隔绝空气高温煅烧的方 法称为明煅法。
定 义
目的
适用于矿物类药物及质地 坚硬的贝壳类、化石类药物。
适用 范围
1.使药物质地酥脆,利于粉碎,便于煎 出有效成分
实操举例
石膏 (CaSO4·2H2O)
始载于《神农本草经》,其炮制首见于 汉代《金匮玉函经》。《中国药典》(2015 年版)载有生石膏、煅石膏两种炮制品。
实操举例
炮
制
方
法
石膏
煅石膏
取原药材,除去杂质, 打碎或研细
一法或二法煅制,煅 至酥松时取出,放凉 后碾碎
实操举例
锻工工艺操作规程

锻工工艺操作规程遵义钛厂管理体系文件文件名称:遵义盛钛机械设备制造有限公司技术标准发布单位:遵义盛钛机械设备制造有限公司受控状态:分发号:QB/ZT-TC-JS-JX. 05. ZH -2011 文件编号文件拟制人拟制日期文件审核人审核日期文件签发人签发日期文件实施日期序号文件名称编号QB/ZT-TC-JS-JX. 05. ZH. 01 -2011 锻丄工艺操作规程QB/ZT-TC-JS-JX. 05. ZH. 02 -2011 热处理工艺技术操作规程QB/ZT-TC-JS-JX. 05. ZH. 03 -2011 钳工工艺技术操作规程QB/ZT-TC-JS-JX. 05. ZH. 04 -2011 电丄工艺技术操作规程QB/ZT-TC-JS-JX. 05. ZH. 05 -2011 钏丄技术操作规程QB/ZT-TC-JS-JX. 05. ZH. 06 -2011 焊工技术操作规程QB/ZT-TC-JS-JX. 05. ZH. 07 -2011 工程作业钏、焊工技术规程QB/ZT-TC-JS-JX. 05. ZH. 08 -2011 精加工工艺技术操作规程QB/ZT-TC-JS-JX. 05. ZH. 09 -2011 反应器加丄制作工艺QB/ZT-TC-JS-JX. 05. ZH. 10 -2011 10复合板反应器加丄制作工艺1112 13 14 15 16 17锻工工艺操作规程1.工作前认真看懂图纸,根据图纸技术要求选用锻工设备、工具。
2.熟悉所用设备的结构、性能、工作状态要求及安全操作规程。
3.各种材料锻造加热温度标准1)Q235钢锻造温度为780-1050?2)45#钢锻造温度为780-1100?3)不锈钢锻造温度为830-1150?)T8钢锻造温度为800-1150? 4钢材加热时,要加热均匀,内外温度一致。
4.拔长时原料外圆尺寸应大于方形工件尺寸的1. 4倍,钳口要与夹持部吻合。
变形要均匀,给进量要大于压缩量。
第二节 锻造工艺规程的制定

举例:齿轮坯模锻件图
(1)分模面(2)加工余量、公差、敷料 (3)模锻斜度(4)圆角半径(没有注明 圆角半径都取R=2.5mm)
二、坯料重量和尺寸的计算
•G
坯料=G锻件+G烧损+G料头
G锻件→由锻件体积算出 G烧损→与加热次数有关
• 锻件的尺寸:与选用的锻造工序有关 • 应用镦粗工序:H/D<2.5 ,太大易弯 • 应用拔长工序:一般不小于2.5~3,
对轧材取1.3~1.5
三、锻造工序的确定
1、长轴类模锻件 (1)不用制坯工序,直接终锻 —适合于形状简单、截面变化不大的 场合; (2)拔长→预锻→终锻 —适合于坯料横截面大于锻件最大截面 (3)拔长→滚压→预锻→终锻 —适合于坯料横截面小于锻件最大截面
2、盘类锻件(短轴类模锻件)
1、镦粗→终锻 ——适合一般形状简单的锻件 2、镦粗→预锻→终锻 ——适合高轮毂,薄轮辐的锻件 四、锻造工艺中的其它内容 (1)根据合金确定始锻及终锻温度 (2)确定加热规范(加热温度、保温时间) (3)选择锻造设备 (4)辅助工序(校正,切飞边、冲孔连皮)
分形面的选择比较图
模锻斜度
模锻斜度比铸件
大,一般取5~ 15°、模锻圆角半径和冲孔连皮
有利于冲型,减
小应力集中,提 高模具寿命; 外圆角半径 1.5~2mm; 内圆角半径 2~3mm;
模锻无法直接锻
出通孔,冲孔连 皮的厚度由锻件 孔径决定,如 φ20~80mm时, 厚度取4~8mm。
第二节 锻造工艺规程的制定
零件图→锻件图→锻造→锻件→机加工→锻件 一、绘制锻件图 1、敷料、余量及公差 敷料—简化锻件形状 余量—0.4~5mm,与锻件尺寸、加工精度有 关 公差—±0.3~3mm,与锻件大小,模具精度, 设备状态有关
第四节 自由锻工艺规程的制订

2.确定坯料尺寸 根据塑性加工过程中体积不变原则和 采用的基本工序类型(如拔长、镦粗等) 的锻造比、高度与直径之比等计算出坯料 横截面积、直径或边长等尺寸。
V坯=G坯/ρ
典型锻件的锻造比见表
锻件名称 碳素钢轴类 锻件 合金钢轴类 锻件 热轧辊 计算部位 最大截面 锻造比 2.0~2.5 锻件名称 锤 头 计算部位 最大截面 锻造比 ≥2.5
1180
850
0.3~0.8
1150 800~90 0 450~50 0
800 650~70 0 350~38 0
0.3~0.8 — —
(六)填写工艺卡片
半轴的自由锻造工艺卡片见表。 半轴自由锻工艺卡
锻件名称 坯料质量 坯料尺寸 材 火 料 次 半 轴 25kg φ130×240 18CrMnTi 工 序
液压机产生静压力使金属坯料 变形。目前大型水压机可达万吨以上, 能锻造300吨的锻件。由于静压力作 用时间长,容易达到较大的锻透深度, 故液压机锻造可获得整个断面为细晶 粒组织的锻件。液压机是大型锻件的 唯一成形设备,大型先进液压机的生 产常标志着一个国家工业技术水平发 达的程度。另外,液压机工作平稳, 金属变形过程中无振动,噪音小,劳 动条件较好。但液压机设备庞大、造 价高。 • 自由锻设备的选择应根据锻件大 小、质量、形状以及锻造基本工序等 因素,并结合生产实际条件来确定。 例如,用铸锭或大截面毛坯作为大型 锻件的坯料,可能需要多次镦、拔操 作,在锻锤上操作比较困难,并且心 部不易锻透,而在水压机上因其行程 较大,下砧可前后移动,镦粗时可换 用镦粗平台,所以大多数大型锻件都 在水压机上生产。 •
(四)选择锻造设备
根据作用在坯料上力 的性质,自由锻设备分 为锻锤和液压机两大类。
锻件厂自由锻工艺规程的制定

锻件厂自由锻工艺规程的制定一、自由锻工艺规程制订的原则及内容制订自由锻工艺规程的原则:必须结合生产实际条件、设备能力和技术水平等,所编制的工艺先进,能满足产品的全部技术要求;在保证质量的前提下,力求提高生产率、节约金属材料消耗,经济合理。
自由锻工艺规程包括下列内容:根据零件图绘制锻件图;确定坯料的材料、质量和尺寸;制订变形工艺及选取工具;选取锻造设备吨位;确定锻造温度范围,制订坯料加热和锻造后锻件冷却规范;制订锻件热处现工艺规范;提出锻件的技术要求和检验结果;填写工艺规程卡片等。
二、自由锻锻件图的制订与绘制自由锻锻件图是在零件图基础上考虑加工余量、锻件公差、锻造余块、检验试样和工艺夹头等因素而绘制而成的图。
1.机械加工余量一般锻件的尺寸精度和表面质量达不到图纸要求,需要机械加工,在零件表面需要加工的部分,锻件表面留有一层机械加工用的金属,称为机械加工余量。
加工余量的大小与零件的形状尺寸、加工精度、表面要求、锻造加热质量、设备工具精度和操作技术水平有关,对于非加工面,可无需加放加工余量。
2.锻件公差锻造生产中,由于锻造温度、锻造设备及其操作者技术水平的影响。
锻件的实际尺寸达不到公称尺寸,允许有一定的偏差,称为锻件公差。
通常锻造公差为加工余量的1/4~1/3。
3.锻造余块对于锻件上较小的孔、狭窄的凹挡、直径差较小而长度不大的台阶等难锻造的地方,通常都需填满金属,而不锻造出,通过后续机械加工办法加工成形,把锻造时这部分附加的金属称为锻造余块。
显然加放锻造余块,会增加机械加工工时和消耗金属材料,是否加放锻造余块,要根据零件形状、锻造技术水平加工成本等决定。
4.检验试样和工艺夹头对于某些有特殊要求的锻件,须在锻件适当的部位添加供检验锻件内部组织和力学性能的试样余块,以利于检验锻件组织和进行力学性能测试。
为便于热处埋及其机械加工的吊挂和夹持定位,在锻件的适当位置增加部分工艺夹头。
5.绘制锻件图机械加工余量、公差和各种锻造余块确定后可绘制锻件图。
煅牡蛎炮制生产工艺规程
1、目的、范围及责任1.1、目的:建立煅牡蛎饮片生产工艺规程,使其生产操作规范化、标准化,符合本公司生产实际和GMP 的管理要求,保证生产出的产品质量均一、稳定。
1.2、适用范围:本工艺规程适用于牡蛎炮制的全过程,是各部门共同遵循的技术准则。
1.3、责任:生产车间按该工艺规程组织生产和按该规程编制标准操作程序,生产部、质量管理部负责监督该规程的实施。
2、产品概述2.1药品名称品名:牡蛎汉语拼音: Muli2.2药材来源本品为牡蛎科动物长牡蛎Ostrea gigas Thunberg、大连湾牡蛎 Ostrea talienwhanensis Crosse或近江牡蛎Ostrea rivularis Gould的贝壳。
全年均可捕捞,去肉,洗净,晒干。
2.3功能主治:重镇安神,潜阳补阴,软坚散结。
用于惊悸失眠,眩晕耳鸣,瘰疠痰核,癥瘕痞块。
煅牡蛎收敛固涩,制酸止痛。
用于自汗盗汗,遗精滑精,崩漏带下,胃痛吞酸。
2.4性味与归经:咸,微寒。
归肝、胆、肾经。
2.5性状:本品为不规则粗粉,灰白色,质酥脆。
2.6商品名:煅牡蛎2.7 等级/规格:统2.8 包装规格:聚乙烯袋装,250g/500g/袋。
2.9 复验期:暂定12个月。
2.10贮藏:置干燥处。
3、法定制法和依据3.1法定制法:洗净,干燥,;取净药材置于煅药锅内,用武火锻至红透或酥脆,取出,放凉。
3.2依据:《中国药典》2015年版。
3.3批量:35kg3.4所用的原辅料清单和处方量:4、5、生产操作过程 5.1领料车间领料人根据生产指令开具领料单,经车间主任审批签字后,领料人凭领料单去仓库领料,领料时应同发料人一起复核所领物料的品名、批号、数量、质量,然后双方在领料单上签字。
外包装应无破损、受潮、水渍、霉变、鼠咬等现象,如不符合质量要求可拒绝领料,并向有关质量人员反映,待解决后领取。
5.2 净选5.2.1净选准备5.2.1.1仔细阅读批生产指令;5.2.1.2检查净选间清场状态标志;5.2.1.3检查设备状态标志;5.2.1.4检查生产用容器、用具清场状态标志;5.2.1.5领取净选牡蛎并核对品名、规格、数量等是否与生产指令一致;5.2.1.6以上各项检查合格后,将清洁状态标志清除,悬挂生产状态标志;开始净选操作。
中药煅制工艺流程

中药煅制工艺流程中药煅制是中医药学中的一种重要制剂方法,通过高温加热使药材中的水分蒸发、挥发性成分析出或发生化学变化,达到药物成分更易吸收、疗效得以增强的目的。
下面将介绍中药煅制的工艺流程。
首先,要选择合适的煅制器具。
传统的煅制用具有瓦砾煅器或砂锅煅器。
现代中药煅制常用的是煅炉,其由主体炉体、炉盖、温控系统等组成,可以精确控制温度和时间。
其次,需要选择合适的煅制药材。
一般来说,适合煅制的药材有多汁、水分含量较高的草本植物。
同时,药材的质量也要求较好,无霉变、无虫蛀等情况。
接下来,需要对药材进行前处理。
一般来说,将药材放在通风干燥的地方进行晾晒,以减少药材中的水分含量,使其更易煅制。
然后,需要对药材进行初煅。
将预处理后的药材放入煅制器具中,加热至一定温度,使药材中的水分蒸发。
这个过程需要控制好煅制的温度和时间,以免煅制过度,导致药材损失活性成分。
接下来,需要对药材进行再煅。
将经过初煅的药材取出,晾凉后重新放入煅制器具中,继续加热至一定温度。
这个过程可以使药材中的有效成分发生一些化学变化,提高药材的疗效。
最后,需要对药材进行冷却。
将煅制好的药材取出,放在通风的地方进行冷却。
这个过程中,药材的温度会逐渐降低,使其恢复到室温。
总结起来,中药煅制工艺流程包括选择合适的煅制器具和药材,对药材进行前处理,进行初煅和再煅,最后将煅制好的药材进行冷却。
这个过程可以提高药材的疗效,增加药物有效成分的含量。
但是在煅制过程中,也需要注意温度和时间的控制,以避免药材的损失和煅制过度。
对于不同的药材,其煅制的温度和时间也会有所不同,需要根据具体情况进行调整。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中药材炮制规范通则SOP-PM-034-01
包装工序清场操作规程SOP-PM-005-01
包装岗位标准操作规程SOP-PM-032-01
车间设备清洁规程SOP-PM-033-01
煅石膏操作规程SOP-PM-038-01
8.劳动组织与岗位定员
车间组织机构与人员配置图
1称量前应确认计量器具使用正常,有检定合格证并在有效期内。
2原药材经检验,有检验合格报告书。
3称量时必须由二人进行,其中一个负责称料,另一人负责复核。
4称量时应仔细确认所称物料的品名,编号,规格等标志。
5剩余药材应附有标志,注明名称,规格,数量,日期等,包装完好,摆放到指定地点或退库。
4.3.2.净选
物料核算 设备安全 生产操作
工艺规程
标题
中药饮片煅制工艺规程
颁发部门
质量管理部
编号
PP-001-01
页次:10/11
9.设备一览表及主要设备生产能力
9.1.设备一览表
设备名称
规格型号
生产厂家
安装使用地点
煅药炉
DY-700型
兰阳中药机械有限公司
生产车间
碰碎机
BYJ-125型
兰阳中药机械有限公司
生产车间
规程:
1.产品名称及概述
煅石膏
[汉语拼音] Duanshigao;
[贮藏]置干燥处;
[包装]2Kg/袋:内包装为塑料袋,外包装为编织袋;
[有效期]36个月;
[执行标准]《中国药典》2005版。
2.原药材、包装材料规格及质量标准
2.1.原药材质量标准及性状
2.1.1.原药材质量标准
原药材名称
质量标准编号
作规程执行。
(3)碰碎后的药材盛装于洁净容器中,称量,定量包装。每件周转容器均应附有标志,注明药材名称,批号、数量、生产日期、操作者等。
(4)碰碎收率:≥95.0%
经质量检验合格后交下工序。
工艺规程
标题
中药饮片煅制工艺规程
颁发部门
质量管理部
编号
PP-001-01
页次:6/11
4.3.5.包装、检验、入库
包装
≥95%
包装数量/煅制后饮片数量
收率
≥95%
总产量/原药材数量
注:总产量=入库数+QA取留样数+本批零头数-上批零头数
11.2.技术经济指标的计算
(1)收率计算方法:
产出量×100%
投入量
(2)物料平衡分析:
收率应在上述规定范围内,否则应查找生产过程损失情况及设备设施的运行情况等原因。原因不明,即使成品检验合格也不予放行。
煅淬
煅至红透时,立即投入规定的液体辅料中,淬酥。
碰碎收率
≥95%
包装
包装规格
2Kg/袋、
工艺规程
标题
中药饮片煅制工艺规程
颁发部门
质量管理部
编号
PP-001-01
页次:4/11
4.2.工艺验证
按上述工艺技术参数生产三批,各工序中间品,成品质量符合质量标准。
4.3.工艺过程
4.3.1.称量
生产前,确认生产现场的卫生,清场,容器用具,计量器具等及其标志符合要求,并确认无上次遗留物。
热风循环风箱
CT-C-I
兰阳中药机械有限公司
生产车间
9.2.主要设备生产能力
设备名称
规格型号
设备最大生产能力
煅药炉
DY-700型
20Kg
碰碎机
BYJ-125型
3Kg
热风循环风箱
CT-C-I
100Kg
10.物料消耗定额
包装材料消耗定额
包材名称
单位
损耗
内包装塑料袋
个
2%
标签
张
2%
装箱单
个
2%
外包装编织袋或外包装箱
工艺规程
标题:中药饮片煅制工艺规程
生效日期年月日页次:1/11
颁发
部门
质量管理部
分发
部门
生产部、质量管理部。
编号:PP-001-01
口新订、口修订、
原文件号
编制
部门
审核
QA
审 核
批准
目的:建立一个中药饮片煅制工艺规程,确保产品质量和生产的有序、规范进行。
范围:适用于中药饮片的煅制生产过程。
责任者:所有涉及中药饮片煅制生产的有关人员。
②根据药材选用合适的煅制方法,煅制前开启通风除烟装置。
③煅制:煅制时应注意煅透,使酥脆易碎。
明煅 取净药材,砸成小块,置无烟的炉火上或置适宜的容器内,煅至酥脆或红透时,取出,放凉。
含有结晶水的盐类药物,不要求煅红,但须使结晶水蒸发尽,或全部形成蜂窝状的块状固体。
煅淬 将净药材煅至红透时,立即投入规定的液体辅料中,淬酥(如不酥,可反复煅淬至酥),取出,干燥。
5.2.产品质量标准及贮存注意事项
(1)取样、留样:
每批产品应按下述样品数随机取样和留样,取样由QA检查员负责;
(2)产品质量标准
每个产品均有企业内控标准,标准的制定依据为法定标准及企业的生产实际,其标准编号见下表;
产品名称
产品质量标准编号
标准依据
有效期
贮藏
煅石膏
QS-031-01
《中国药典》2005版一部
3年
置干燥处
备注:1、质量标准原件存于QA;
2、留样产品应保存至有效期后一年。
6.技术安全、劳动保护及环境卫生
6.1.技术安全
(1)防火:车间内严禁使用明火,应设有消防栓灭火器,有安全通道。
(2)防暴:所有的耐压容器和设备,每年按规定做耐压检验,并安装安全阀、压力表,定期校验。
(3)碰碎工序要有相应的除尘和防尘措施。
SOP名称编号
生产区个人卫生管理规程SOP-PM-002-01
生产区工艺卫生管理规程SOP-PM-003-01
车间清场管理规程SOP-PM-008-01
7.产品工艺过程中所需的SOP名称及编号(注:原件存放于QA)
SOP名称编号
中药材称量标准操作规程SOP-PM-029-01
净选工序操作规程SOP-PM-016-01
个
2%
工艺规程
标题
中药饮片煅制工艺规程
颁发部门
质量管理部
编号
PP-001-01
页次:11/11
11.物料平衡及技术经济指标的计算
11.1.各工序物料平衡及计算
工序
收率合格范围(%)
计算方法
净选
≥95%
净药材数量/原药材数量
煅制
≥80%
煅制后饮片数量/净选后净药材数量
碰碎
≥95%
碰碎后药材数量/原药材数量
备注
石膏
QS-021-01
原药材质量标准原件存放于QA
工艺规程
标题
中药饮片煅制工艺规程
颁发部门
质量管理部
编号
PP-001-01
页次:2/11
2.1.2.原药材贮藏要求
原药材名称
贮藏要求
使用期限
备注
石膏
常温,置干燥处
36个月
备注:1.“贮藏要求”填常温保存或阴凉保存;
2.常温库温度控制在0-30℃间,阴凉库温度控制在25℃以下。相对湿度控制在75%以内。
手工打印、打印前核对批号印章。打印前试打一张检查批号是否正确,位置是否适中,字迹是否清晰,经QA检查员确认合格即可开始打印。其余同机器打印。
打印结束后应及时统计合格品数、损耗数、剩余数、领用数应等于合格品数+损耗数+剩余数,剩余数及时退回车间中间站。
(2)包装
生产前,确认生产现场的卫生,清场,工用具,计量器具等及其标志符合要求,并确认无上次遗留物。
4.4.注意事项及异常情况处理
4.4.1.在生产过程中严格执行各岗位SOP和有关的操作法。
4.4.2.在所有生产过程中,中药材都不能直接接触地面。
4.4.3.生产操作人员操作时,一定要穿戴好劳动保护用品,以免受伤。
4.4.4.检验结果不符合标准时,不得擅自进行处理,必须配合车间查找原因,按有关的处理程序进行。
生产前,确认生产现场的卫生,清场,设备,容器用具,计量用具等及其标志符合要求,并确认无上次遗留物。
①检查需拣选的药材,并称量记录。
②拣净杂质,打碎,除去夹石、筛去灰屑并根据药材的大小进行分档。
③拣选药材工作台表面应平整,不易产生脱落物。
④拣选后药材盛装于周转容器,称量记录,定量包装,每件周转容器均应附有标志,注明药材名称,批号、数量、生产日期、操作者等。
5.生产工艺和质量控制检查,中间体和成品质量标准
5.1.生产工艺和质量控制检查
工序
质量控制点
质量控制项目
频次
领料
原药材
核对物料品名、数量、检验合格报告书
1次/批
净选
净药材
杂质含量、净选程度
随时/班
煅制
明煅
煅后药材的质量
1次/批
煅淬
加入液体辅料的数量,煅后药材的质量
随时/班
碰碎
破碎程度
随时/班ቤተ መጻሕፍቲ ባይዱ
包装
打印批号(标签、装箱单)
品名、批号、内容、规格、数量、有效期、领用记录、打印记录,生产日期
随时/班
内包装
装量、均匀度、扎口紧密度
随时/班
外包装
品名、批号、数量、装箱单、封口严密
随时/班
贴签
内容、数量、外观(品名、批号、生产日期)、
随时/班
工艺规程
标题
中药饮片煅制工艺规程
颁发部门
