药品研发流程图
详解原料药研发的基本流程和原料药备案流程图

详解原料药研发的基本流程和原料药备案流程图工艺路线的开发阶段1. 工艺路线的选择质量源于设计,不同的工艺路线导致API的杂质谱会有较大的区别。
故在工艺路线开发阶段,需要对路线全面的工艺分析(反应条件是否苛刻,是否用到有毒物料)。
对不同的工艺路线,分析每个反应步骤的反应机理,后处理方案等,对工艺路线的杂质谱有一个大致的判断。
综合分析,确定拟开发的工艺路线。
然后,根据注册申报指导原则要求,确定工艺路线的起始原料,并结合文献设计关键起始原料对API质量影响的控制策略。
2. 工艺路线摸索(打通工艺阶段)1) 反应设计工欲善其事,必先利其器。
在开始工艺摸索之前,我们要比较全面的了解原料,试剂,溶剂,催化剂及各中间体的物理化学性质。
例如, 化合物的溶解度,为选择适宜的反应介质提供了参考。
根据化合物的化学性质,结合反应的机理,我们可以在理论上分析反应过程中的物料平衡,副反应。
对副产物、副反应产物--杂质,做到心中有数,为后处理设计提供思路和依据。
2) 后处理设计后处理的目的, 一般原则就是尽可能的得到纯度较高的主产物。
一个好的后处理方法,能使主产物和副产物、杂质有效的分离。
后处理设计的关键是利用主产物与副产物、杂质之间的物理化学性质差异,分离纯化得到较高纯度的主产物。
中间体的纯度,直接影响API的质量(含量、有关物质、溶残、重金属以及炽灼残渣等)。
3) 在打通工艺阶段,我们还需要完成以下的研究工作:(1)分析部门开发初步的分析方法。
(2)工艺杂质研究除了中间体、降解杂质,工艺杂质往往是杂质研究中的重中之重。
合成部门在此阶段,通过实验,发现主要的工艺杂质,并结合文献,实验数据,分析判断产生主要工艺杂质的关键工艺步骤和关键工艺参数。
判断关键的工艺杂质,经验告诉我们:关注HPLC 上主峰之后的杂质。
HPLC上主峰之前的杂质,通过重结晶的方式,都能比较容易的有效除去;而主峰之后的一些杂质,很难通过重结晶的方式有效的除去。
(完整版)产品研发流程图
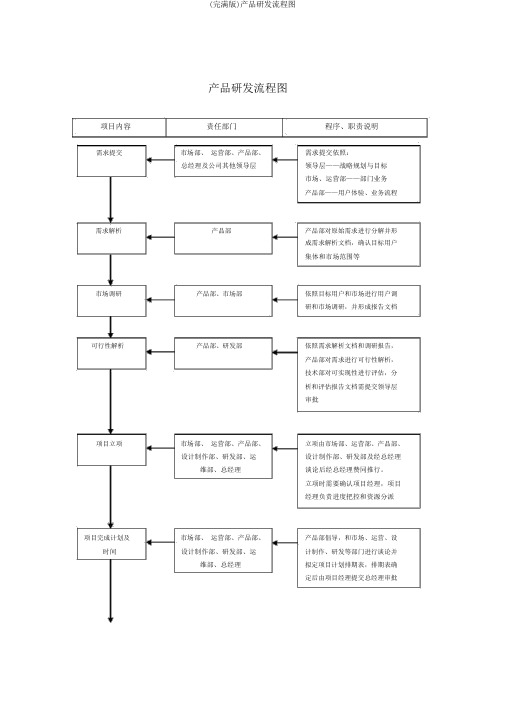
产品研发流程图项目内容责任部门程序、职责说明需求提交市场部、运营部、产品部、总经理及公司其他领导层需求提交依照:领导层——战略规划与目标市场、运营部——部门业务产品部——用户体验、业务流程需求解析产品部产品部对原始需求进行分解并形成需求解析文档,确认目标用户集体和市场范围等市场调研产品部、市场部依照目标用户和市场进行用户调研和市场调研,并形成报告文档可行性解析产品部、研发部依照需求解析文档和调研报告,产品部对需求进行可行性解析,技术部对可实现性进行评估,分析和评估报告文档需提交领导层审批项目立项市场部、运营部、产品部、设计制作部、研发部、运维部、总经理立项由市场部、运营部、产品部、设计制作部、研发部及经总经理谈论后经总经理赞同推行。
立项时需要确认项目经理,项目经理负责进度把控和资源分派项目完成计划及时间市场部、运营部、产品部、设计制作部、研发部、运维部、总经理产品部倡导,和市场、运营、设计制作、研发等部门进行谈论并拟定项目计划排期表,排期表确定后由项目经理提交总经理审批项目经费估量市场部、运营部、产品部、研发部、运维部、总经理各部门提交部门相关项目估量,由项目经理汇总后提交总经理审批产品策划产品部产品部依照需求解析和可行性分析文档,完成产品策划文案提交需求部门和项目经理审察需求文档及产品原型产品部依照经过的产品策划文案,产品部进行需求文档撰写,同时进行产品原型规划。
需求文档和产品原型完成后提交需求部门和项目经理审察UI 设计产品部、设计制作部设计制作部依照从前确认的原型进行 UI 设计,由产品部进行首次确认后,需求部门和项目经理进行二次确认审察交互设计、页面产品部、设计制作部、研设计制作部依照已确认的UI 稿进重构及前端开发发部行重构工作,尔后对重构完成的静态页面进行交互和前端功能开发,工作完成后由项目经理确认产品开发产品部、研发部详尽的研发计划、任务及推行过程由研发部自主安排,产品部进行跟进和功能确认,项目经理协调资源及跟进进度测试产品部、研发部研发部手下测试部门进行黑盒及白盒测试,其中黑盒测试的部分工作可有产品部协调运营部门联合进行。
药品生产典型工艺流程框图汇编

药品生产典型工艺流
程框图
常见药品生产典型工艺流程框图
药品生产对环境的洁净等级要求与药品的品种、剂型和生产特点有关。
常见药品生产的典型工艺流程及环境区域划分如图1-1至图1-9。
图1-1 非无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-2 无菌原料药精制、干燥、包装工艺流程框图及环境区域划分
图1-3 片剂生产工艺流程框图及环境区域划分
图1-4 硬胶囊剂生产工艺流程框图及环境区域划分
图1-5 压制法软胶囊剂生产工艺流程框图及环境区域划分
图1-6 可灭菌小容量注射剂生产工艺流程框图及环境区域划分
图1-7 可灭菌大容量注射剂生产工艺流程框图及环境区域划分
图1-8 注射用无菌分装产品生产工艺流程框图及环境区域划分
图1-9 注射用冷冻干燥制品生产工艺流程框图及环境区域划分。
药品研发流程图
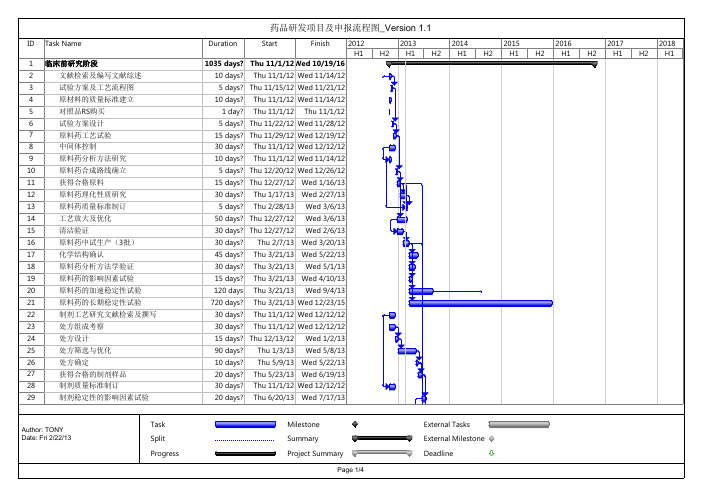
Thu 2/7/13 Wed 3/20/13 Thu 3/21/13 Wed 5/22/13 Thu 3/21/13 Thu 3/21/13 Wed 5/1/13 Wed 9/4/13 Thu 3/21/13 Wed 4/10/13 Thu 3/21/13 Wed 12/23/15 Thu 11/1/12 Wed 12/12/12 Thu 11/1/12 Wed 12/12/12 Wed 1/2/13 Wed 5/8/13 Thu 1/3/13
5 days? Thu 11/22/12 Wed 11/28/12 15 days? Thu 11/29/12 Wed 12/19/12 30 days? 10 days? Thu 11/1/12 Wed 12/12/12 Thu 11/1/12 Wed 11/14/12
5 days? Thu 12/20/12 Wed 12/26/12 15 days? Thu 12/27/12 Wed 1/16/13 30 days? 5 days? Thu 1/17/13 Wed 2/27/13 Thu 2/28/13 Wed 3/6/13 Wed 3/6/13 Wed 2/6/13
5 days? Thu 11/26/15 Wed 12/2/15 10 days? Thu 10/22/15 Wed 11/4/15 100 days? 30 days? 100 days? 333 days? 5 days? 5 days 60 days 120 days 20 days 10 days 20 days 15 days? 3 days? 5 days 10 days 10 days 10 days 10 days 10 days 10 days 10 days 10 days? Thu 12/3/15 Wed 4/20/16 Thu 4/21/16 Thu 1/14/16 Thu 6/2/16 Thu 6/16/16 Wed 6/1/16 Wed 4/6/16 Wed 6/1/16 Wed 6/8/16 Wed 9/7/16
研发项目管理-正大天晴

类别
代号
EQM HRM
档案管理类
计算机技术和软件验证
ARC
CSV
健康、安全和环保
实验方法及工作流程类 样品安全和监管
HSEMET SAM实验记录、原始数据处理和计算 DAT
• 综合管理类 ADM
– SOP的制订、审核、管理 – 实验室安全卫生管理 – 物料采购管理 – 合同管理 – 固定资产管理 – ……..
原料药研究内容
• 工艺开发 • 中试放大 • 工艺验证
• 质量研究及质量控制
工艺开发
– 路线设计
• 查阅文献,确定拟开发原料药的名称和化学结构; • 对文献报道的各种合成路线的优缺点进行分析、比 较,设计或选择合成路线,要求避开专利、成本可 控、操作简易、便于工业化。
– 工艺参数研究
• 以提高收率和纯度、简化操作和便于工业化生产、 稳定工艺为目的。结合TLC或HPLC、GC等监控手段, 对包括反应溶剂、试剂、催化剂、投料比、温度、 压力、时间等进行优化; • 对工艺参数优化结果按步骤列表总结,比较内容包 括选择溶剂、试剂、反应温度、时间、收率、纯度、 残留杂质情况等。
质量研究基本要求
• 及时做好记录:完整、规范; • 仪器:按规定定期校验,电子图谱保存好,定 期备份,做好使用记录; • 对照品:统一管理,并按照规定条件储存;标 准溶液和试液按期标化;做好取用记录; • 方法学验证:要求完整、规范。
正大天晴研发管理制度
管理制度分类
类
综合管理类 动物管理类
别
代号
科 研 管 理 办 公 室
南京研究所
连云港研究所
吸 入 送 药 中 心
氘 代 药 物 中 心
药物研发流程ppt课件

试验方法1:单剂量给药交叉试验设计
筛查 研究日 -7天
入院
-1天
给药 出院
1天
3天
A组服试验药物
B组服对照药物
给药 出院 入院
14天 清洗期
15天 17天 B组服试验药物
A组服对照药物
随访
20天
试验方法2:单剂量给药平行试验设计
筛查 研究日 -7天
入院
-1天
给药
1天
A组服用试验药物 B组服对照药物
出院 随访
8天
11
不予受理通知书 审查结果通知 申请人补充资料
中国仿制药申报生产流程
申请人向省局提出申请 报送资料和生产现场检查申请
省局形式审查
受理通知书
省局审查内容: 研制情况、原始资料现场核查 根据工艺、标准进行生产现场检查 抽验连续生产的3批样品 通知药检所进行样品检验 申报资料初审,提出审查意见 (30日)
耗时
7天
30天
7天 60天 15天 15天
7天 中试后60天
30天 15天 与加速剂长期同步 180天 180天 7天 ——
稳定性试验完成后 30天内
30天
10
仿制药生物等效性研发流程
适用范围: 改变国内已上市销售药品的剂型,但不改变给药途径的口服制剂或其他有关制剂; 已有国家药品标准的制剂; 改变口服药物制剂处方或工艺的补充申请。
创制新药的四要素;靶标的确定;检测模型的确定;先导化合物的发现及先导化合物的优化。
确定靶标
先 导 化 建立模型 合 物 先导化合 研 物的发现 发
先导化合 物的优化
目的
详情
方法
投入
确 定 治 疗 的 疾 病 , 600多种小分子药物靶标;1800 基因组技术
新药研发流程及研发项目管理时间表
finish
10/19/16 11/14/12 11/21/12 11/14/12
11/1/12 11/28/12 12/19/12 12/12/12 11/14/12 12/26/12
1/16/13 2/27/13 3/6/13 3/6/13 2/6/13 3/20/13 5/22/13 5/1/13 4/10/13 9/4/13 12/23/15 12/12/12 12/12/12 1/2/13 5/8/13 5/22/13 6/19/13 12/12/12 7/17/13 12/4/13 7/31/13 1/15/14 1/2/13 2/12/14 7/2/14 10/19/16 1/15/14 3/20/13 7/2/14
20days
28
制剂质量标准制定
30days
29
制剂稳定性的影响因素试验
20days
30
制剂工艺放大及优化
120days
31
制剂车间清洁验证
30days
32
制剂中试生产(3批)
30days
33
照顾护分析方法学验证
45days
34
制剂的影响因素影响
20days
35
制剂的加速稳定性试验
120days
36
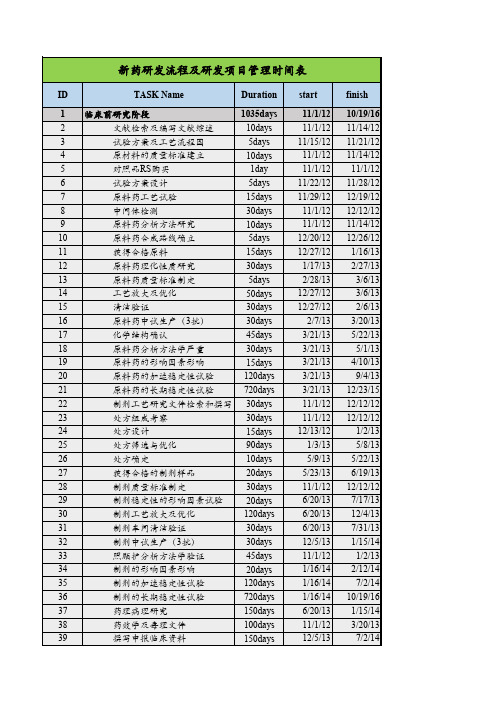
新药研发流程及研发项目管理时间表
ID
TASK Name
Duration
1 临床前研究阶段
1035days
2
文献检索及编写文献综述
10days
3
试验方案及工艺流程图
5days
4
原材料的质量标准建立
10days
5
对照品RS购买
1day
6
化学仿制药研发流程幻灯片

4.3
第三阶段-相关质量标准的初步建立及制剂处方工艺研究
4.4
第四阶段-中试放大研究及质量研究、质量标准的建立、
正式稳定性研究、
4.5
第五阶段-资料整理、项目申报
7
第一阶段-文献调研和合成工艺摸索
基本目标
1. 合成路线选择 2. 实验室合成路线打通
8
第一阶段-文献调研和合成工艺摸索
化学部门任务
2
根据研究工作的基本时间及各室介入的顺序划分阶段 ▪原料(工艺研究、样品制备)→分析(研究分析方法、建 立标准)→制剂(处方工艺研究)→原料及制剂中试→完成 必要时间稳定性试验、申报;
分析部门任务
1
对照品(原料及杂质)纯度标定方法研究及标准拟定 (3.2.S.5);
2
完善原料药质控标准;
3
与原料工艺人员合作,进行杂质谱分析研究(3.2.S.3.2)
包括:
①对合成起始原料及中间体所含主要杂质成分进行定性
研究,考察这类杂质在工艺中的去向和变化;
②原料药工艺杂质推导及溯源;
③原料药降解途径及降解产物研究;
4
为包装贮藏及制剂研究提供参考信息。
11
第二阶段-原料药实验室放大及分析方法开发
分析部门任务
1
初步研究合成起始原料及中间体的质控方法,进行 必要的方法学验证;
2
对原料药主要检测项目如有关物质、含量等进行方 法学研究,初步建立标准;
3
初步考察原料药的理化性质(注意考察使用的原料 晶型和纯度等);
4
10
第二阶段-原料药实验室放大及分析方法开发
化学部门任务
1
原料合成工艺优化及适当放大,制备供分析研究用必要 数量及纯度的样品及杂质;
新产品开发设计流程图

新产品开发流程图
1.对市场进行详细系统的分析,确定研发产品类型、规格参数、性能指标、安全性能等信息
2.新产品研发的可行性评估
2.1 上级领导审批通过后,产品研发小组对相关产品情况进行调查;可行性分析、预测;总结、编写可行性研究报告
2.2 《可行性研究报告》上报上级领导,审批 OK后正式进入产品的研发阶段
3.形成产品设计方案
根据审批通过的产品《可行性研究报告》,产品研发小组编制《产品设计方案》
4.确定最终产品设计方案
4.1 市场部、研发部会同生产部从产品可行性、生产技术性、技术来源方面对产品进行评估、筛选出适合的方案
4.2 根据最终选出的《产品设计方案》确定产品设计投入,并进行综合比较,确定最终的《产品设计方案》,并进行项目立项,制定出《新产品开发进度时间表》
5.产品设计
根据确定的《产品设计方案》产品,开发小组成员进行产品设计、绘制产品设计相关图纸及产品的测试检验标准
6.样品试制、测试
6.1 产品设计图纸经过项目负责人审批通过后,可进入样品试制阶段,准备样品制造所需的材料等
6.2 样品试制完成后,对其进行性能检测,并保存测试报告,对于不合格的样品设计不合理的地方进行修改,并重新进行样品试制
7.投入批量生产
对产品进行鉴定,合格后将产品研发设计的相关资料进行保存并发行,再投入批量生产
新产品开发流程图
制定:审核:批准:
第3页,共3页。
新药研究开发与上市流程图

新药研究开发与上市流程图人们生活水平提高要求更多更好的新药,药物科学的发展为新药开发提供了理论基础和技术,市场经济竞争也促进了新药快速发展。
美国食品与药物管理局(FDA)近十年来每年批准上市的新药都在20种以上。
我国近年来引进新药品种很多,但需要加快创新。
新药开发是一个非常严格而复杂的过程,各药虽然不尽相同,药理研究却是必不可少的关键步骤。
临床有效的药物都具有相应的药理效应,但具有肯定药理效应的药物却不一定都是临床有效的药物。
例如抗高血压药都能降低血压,但降压药并不都是抗高血压药,更不一定是能减少并发症、延长寿命的好药。
因此新药开发研究必需有一个逐步选择与淘汰的过程。
为了确保药物对病人的疗效和安全,新药开发不仅需要可靠的科学实验结果,各国还对新药生产上市的审批与管理制定了法规,对人民健康及工商业经济权益予以法律保障。
新药来源包括天然产物、半合成及全合成化学物质。
过去选药主要方法是依靠实践经验,现在可以根据有效药物的植物分类学找寻近亲品种进行筛选或从有效药物化学结构与药理活性关系推断,定向合成系列产品,然后进行药理筛选。
近年来对于机体内在抗病物质(蛋白成分)利用DNA基因重组技术,即将DNA 的特异基因区段分离并植入能够迅速生长的细菌或酵母细胞,以获得大量所需蛋白药物。
此外,还可对现有药物进行化学结构改造(半合成)或改变剂型,也可获得疗效更好,毒性更小或应用更方便的药物。
医学教育网搜集整理新药研究过程大致可分三步,即临床前研究、临床研究和售后调研。
临床前研究包括用动物进行的系统药理研究及急慢性毒性观察。
对于具有选择性药理效应的药物,在进行临床试验前还需要测定该药物在动物体内的吸收、分布及消除消除过程。
临床前研究是要弄清新药的作用谱及可能发生的毒性反应。
在经过药物管理部门的初步审批后才能进行临床试验。
目的在于保证用药安全。
临床研究首先在10~30例正常成年志愿者观察新药耐受性,找出安全剂量。
再选择有特异指征的病人按随机分组、设立已知有效药物及空白安慰剂双重对照(对急重病人不得采用有损病人健康的空白对照),并尽量采用双盲法(病人及医护人员均不能分辨治疗药品或对照药品)观察,然后进行治疗结果统计分析,客观地判断疗效。
研发流程(EVT-DVT-PVT-MP)

Quality Management System 文件制订/变更申请单O-053F1.目的落实新产品开发设计之作业流程管制,确保其设计结果能符合客户及公司对品质之要求。
2.范围凡本移动通讯事业群新产品之开发设计案均属之。
3.名词解释3.1 PM:产品经理3.2 MRS:Marketing Requirement Spec3.3 PDS(Product Development Schedule):新产品开发进度3.4 BOM(Bill of Material):材料构成表3.4.1 E-BOM:研发阶段初期之零件表。
不能用于正式生产.3.4.2 M-BOM:研发成熟后,将用于产线生产使用之零件表。
3.5 Kick Off Meeting:设计开发案启动会议3.6 FTA(Full Type Approval):产品认证3.7 ES(Evaluation Specification):提案及市场/客户需求分析、研发计划申请阶段3.8 EV(Evaluation Validation):产品概念发展、设计规划及设计雏型阶段3.9 DV(Design Validation):研发样品、工程试作阶段3.10 PV(Production Validation):量试阶段3.11 MP(Mass Production):量产阶段3.12 EVT 1.x:PCBA样品、手工样品、CNC样品试作代号(通信基本功能、外观参考用)3.13 DVT 2.x:新产品设计验证试作代号(正式模具品Soft/Hard T ooling、全功能验证、研发技转确认产线)3.14 PVT 3.x:产品小量量产验证试作代号(确认制程&良率)4.管理重点:4.1 产品概念发展/设计规划阶段(ES):4.1.1 提案客户产品之开发构想,由产品规划人员提出开发案申请。
4.1.2 市场/客户需求分析:(A)市场信息,销售预计(B)成本预估(C)必要时合同审查之结果(D)国际或国家法规4.1.3 可行性分析:视产品需求,可由产品规划人员主导进行市场分析及技术可行性分析(RD),客制化的专案项目的市场可行性分析可由客户承担4.1.4 提出产品规格书及专案计划:PM依据『MRS』与Project Team人员共同研讨各项设计需求,(A) 项目组织结构:(1)每一新产品研发项目需指派PM 负责整个计划之推动。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
120 days? Thu 10/22/15
Thu 6/2/16 Mon 9/11/17 Thu 6/9/16 Wed 6/15/16 Thu 9/8/16 Wed 2/22/17 Thu 2/23/17 Wed 3/22/17 Thu 3/23/17 Wed 4/5/17 4/19 Thu 3/23/17 Wed 4/19/17 Thu 4/20/17 Wed 5/10/17 Thu 5/11/17 Mon 5/15/17 Tue 5/16/17 Mon 5/22/17 Tue 5/23/17 Tue 6/20/17 Mon 6/5/17 Mon 7/3/17 Tue 6/6/17 Mon 6/19/17 Tue 7/4/17 Mon 7/17/17 Tue 7/18/17 Mon 7/31/17 Tue 8/1/17 Mon 8/14/17 Tue 8/15/17 Mon 8/28/17 Tue 8/29/17 Mon 9/11/17
93 days? Thu 4/20/17 Mon 8/28/17
Author: TONY Date: Fri 2/22/13
Task Split Progress
Milestone Summary Project Summary
Page 3/4
External Tasks External Milestone Deadline
药品研发项目及申报流程图_Version 1.1
ID 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 Task Name 临床前研究阶段 文献检索及编写文献综述 试验方案及工艺流程图 原材料的质量标准建立 对照品RS购买 试验方案设计 原料药工艺试验 中间体控制 原料药分析方法研究 原料药合成路线确立 获得合格原料 原料药理化性质研究 原料药质量标准制订 工艺放大及优化 清洁验证 原料药中试生产(3批) 化学结构确认 原料药分析方法学验证 原料药的影响因素试验 原料药的加速稳定性试验 原料药的长期稳定性试验 制剂工艺研究文献检索及撰写 处方组成考察 处方设计 处方筛选与优化 处方确定 获得合格的制剂样品 制剂质量标准制订 制剂稳定性的影响因素试验 Task Split Progress Duration Start Finish 2012 H1 H2 2013 H1 H2 2014 H1 H2 2015 H1 H2 2016 H1 H2 2017 H1 H2 2018 H1
Page: Fri 2/22/13
External Tasks External Milestone Deadline
药品研发项目及申报流程图_Version 1.1
ID 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 Task Name 研究单位申请伦理委员会的批文 临床启动会议准备及获得“登记号” 试验启动、执行试验和监察 试验总结/报告/图谱递交 试生产(3批)并生产工艺验证 撰写申报生产/进口资料 申报生产/进口阶段 递交申报生产/进口资料 省局现场检查(抽样3批) 药检所检验 药审中心技术审评 国家局批准 药品认证中心动态现场检查 获得药品批准文号和新药证书或注册证 GMP认证 GMP认证申请和申报材料准备 提交认证申请和申报材料 省局对申报材料形式审查 认证中心对申报材料进行技术审查 认证中心制定现场检查方案 省局审批方案 认证中心组织实施现场检查 认证中心对现场检查报告初审 省局对认证初审意见进行审批 报国家局发布审查公告 价格备案 Duration Start Finish 2012 H1 H2 2013 H1 H2 2014 H1 H2 2015 H1 H2 2016 H1 H2 2017 H1 H2 2018 H1
15 days? Thu 12/13/12
Thu 5/9/13 Wed 5/22/13 Thu 5/23/13 Wed 6/19/13 Thu 11/1/12 Wed 12/12/12 Thu 6/20/13 Wed 7/17/13 Milestone Summary Project Summary
Thu 2/7/13 Wed 3/20/13 Thu 3/21/13 Wed 5/22/13 Thu 3/21/13 Thu 3/21/13 Wed 5/1/13 Wed 9/4/13 Thu 3/21/13 Wed 4/10/13 Thu 3/21/13 Wed 12/23/15 Thu 11/1/12 Wed 12/12/12 Thu 11/1/12 Wed 12/12/12 Wed 1/2/13 Wed 5/8/13 Thu 1/3/13
50 days? Thu 12/27/12 30 days? Thu 12/27/12 30 days? 45 days? 30 days? 15 days? 120 days 720 days? 30 days? 30 days? 90 days? 10 days? 20 days? 30 days? 20 days?
Page 1/4
Author: TONY Date: Fri 2/22/13
External Tasks External Milestone Deadline
药品研发项目及申报流程图_Version 1.1
ID 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 Task Name 制剂工艺放大及优化 制剂车间清洁验证 制剂中试生产(3批) 制剂分析方法学验证 制剂的影响因素试验 制剂的加速稳定性试验 制剂的长期稳定性试验 药理病理研究 药效学及毒理文件 撰写申报临床资料 申报临床阶段 递交临床申报资料 现场核查并抽样 药检所样品检验并质量标准复核 药审中心技术审评 药品注册司审核 国家局批准 获得药物临床试验批件 对照制剂购买/RLD 一次性进口? 生产临床试验用样品(符合GMP条件) 生产工艺调整及自行验证 临床试验 编写临床预算 撰写研究者手册和药品说明书(草案) 试验基地筛选 具体方案讨论(BE/人体PK/100对/临床 确定其他参试医院和研究者 准备临床试验药品 准备试验用物品、印刷品 Task Split Progress Duration 120 days 30 days? 30 days? 45 days? 20 days? 120 days 720 days? 150 days? 100 days? 150 days? 500 days? 5 days? 5 days 60 days 120 days 40 days 20 days 20 days 5 days? 20 days? 50 days? Start Finish 2012 H1 H2 2013 H1 H2 2014 H1 H2 2015 H1 H2 2016 H1 H2 2017 H1 H2 2018 H1
160 days? Thu 10/22/15
3 days? Thu 10/22/15 Mon 10/26/15 10 days? Thu 10/22/15 Wed 11/4/15 5 days? Thu 10/22/15 Wed 10/28/15 10 days? Thu 11/5/15 Wed 11/18/15 5 days? Thu 11/19/15 Wed 11/25/15 3 days? Thu 11/26/15 Mon 11/30/15 10 days? Thu 11/26/15 Wed 12/9/15 Milestone Summary Project Summary
5 days? Thu 11/26/15 Wed 12/2/15 10 days? Thu 10/22/15 Wed 11/4/15 100 days? 30 days? 100 days? 333 days? 5 days? 5 days 60 days 120 days 20 days 10 days 20 days 15 days? 3 days? 5 days 10 days 10 days 10 days 10 days 10 days 10 days 10 days 10 days? Thu 12/3/15 Wed 4/20/16 Thu 4/21/16 Thu 1/14/16 Thu 6/2/16 Thu 6/16/16 Wed 6/1/16 Wed 4/6/16 Wed 6/1/16 Wed 6/8/16 Wed 9/7/16
5 days? Thu 11/22/12 Wed 11/28/12 15 days? Thu 11/29/12 Wed 12/19/12 30 days? 10 days? Thu 11/1/12 Wed 12/12/12 Thu 11/1/12 Wed 11/14/12
5 days? Thu 12/20/12 Wed 12/26/12 15 days? Thu 12/27/12 Wed 1/16/13 30 days? 5 days? Thu 1/17/13 Wed 2/27/13 Thu 2/28/13 Wed 3/6/13 Wed 3/6/13 Wed 2/6/13
药品研发项目及申报流程图_Version 1.1
21 36 48 原料药的长期稳定性试验 新原料药申报时需要12个月的长期试验数据 制剂的长期稳定性试验 新制剂申报时需要12个月的长期试验数据 对照制剂购买/RLD 一次性进口? Orange Book 自行从国外购买国内未上市的药品,只能用于临床前药学质量对比研究,不能用于人体临床试验 60 临床启动会议准备及获得“登记号” 关于试行药物临床试验信息登记的通知_20121119
Thu 6/20/13 Wed 12/4/13 Thu 6/20/13 Wed 7/31/13 Thu 12/5/13 Wed 1/15/14 Thu 11/1/12 Thu 1/16/14 Wed 1/2/13 Wed 7/2/14 Thu 1/16/14 Wed 2/12/14 Thu 1/16/14 Wed 10/19/16 Thu 6/20/13 Wed 1/15/14 Thu 11/1/12 Wed 3/20/13 Thu 12/5/13 Thu 7/3/14 Thu 7/3/14 Wed 7/2/14 Wed 6/1/16 Wed 7/9/14
