高二化学上学期硫及其化合物
硫及其重要化合物完美版
硫及其重要化合物【高考目标定位】 考纲导引考点梳理 了解硫元素单质及其化合物的主要性质及应用。
了解硫元素单质及其化合物对环境质量的影响。
硫。
二氧化硫和三氧化硫。
硫的氧化物对大气的污染。
硫酸。
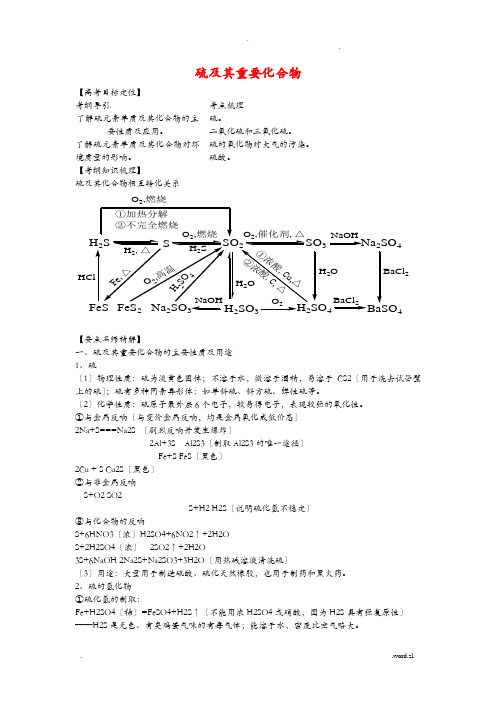
【考纲知识梳理】硫及其化合物相互转化关系H 2SSSO 23Na SO 4223H 22SO 4HClH 2,△O 2,燃烧H 2SO ,燃烧①加热分解②不完全燃烧2NaOHO 2BaCl 2H 2OBaCl 2①浓酸,C u ,△②浓酸,C, △H 2OH2S O4O2,高温F e ,△【要点名师精解】一、硫及其重要化合物的主要性质及用途 1、硫〔1〕物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS2〔用于洗去试管壁上的硫〕;硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
〔2〕化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反响〔与变价金属反响,均是金属氧化成低价态〕 2Na+S===Na2S 〔剧烈反响并发生爆炸〕2Al+3S Al2S3〔制取Al2S3的唯一途径〕 Fe+S FeS 〔黑色〕 2Cu + S Cu2S 〔黑色〕 ②与非金属反响 S+O2 SO2S+H2 H2S 〔说明硫化氢不稳定〕 ③与化合物的反响S+6HNO3〔浓〕H2SO4+6NO2↑+2H2O S+2H2SO4〔浓〕 2SO2↑+2H2O3S+6NaOH 2Na2S+Na2SO3+3H2O 〔用热碱溶液清洗硫〕〔3〕用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
2、硫的氢化物 ①硫化氢的制取:Fe+H2SO4〔稀〕=FeSO4+H2S ↑〔不能用浓H2SO4或硝酸,因为H2S 具有强复原性〕 ——H2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
②硫化氢的化学性质 A .可燃性:当22/O S H n n ≥2/1时,2H2S+O2 2S+2H2O 〔H2S 过量〕当22/O S H n n ≤2/3时,2H2S+3O22SO2+2H2O 〔O2过量〕当23222<<O S H n n 时,两种反响物全部反响完,而产物既有硫又有SO2B .强复原性:常见氧化剂Cl2、Br2、Fe3+、HNO3、KMnO4等,甚至SO2均可将H2S 氧化。
高二化学知识点总结大全(非常全面)

高二化学知识点总结大全(非常全面)高二化学知识点总结一、硫及其化合物的性质1.铁与硫蒸气反响:Fe+S△==FeS2.铜与硫蒸气反响:2Cu+S△==Cu2S3.硫与浓硫酸反响:S+2H2SO4(浓)△==3SO2↑+2H2O5.铜与浓硫酸反响:Cu+2H2SO4△==CuSO4+SO2↑+2H2O6.二氧化硫的催化氧化:2SO2+O22SO37.二氧化硫与氯水的反响:SO2+Cl2+2H2O=H2SO4+2HCl8.二氧化硫与氢氧化钠反响:SO2+2NaOH=Na2SO3+H2O9.硫化氢在充足的氧气中燃烧:2H2S+3O2点燃===2SO2+2H2O10.硫化氢在不充足的氧气中燃烧:2H2S+O2点燃===2S+2H2O二、镁及其化合物的性质1.在空气中点燃镁条:2Mg+O2点燃===2MgO2.在氮气中点燃镁条:3Mg+N2点燃===Mg3N23.在二氧化碳中点燃镁条:2Mg+CO2点燃===2MgO+C4.在氯气中点燃镁条:Mg+Cl2点燃===MgCl25.海水中提取镁涉及反响:①贝壳煅烧制取熟石灰:CaCO3高温===CaO+CO2↑CaO+H2O=Ca(OH)2③氢氧化镁转化为氯化镁:Mg(OH)2+2HCl=MgCl2+2H2O④电解熔融氯化镁:MgCl2通电===Mg+Cl2↑三、Cl-、Br-、I-离子鉴别:1.分别滴加AgNO3和稀硝酸,产生白色沉淀的为Cl-;产生浅黄色沉淀的为Br-;产生黄色沉淀的为I-2.分别滴加氯水,再参加少量四氯化碳,振荡,下层溶液为无色的是Cl-;下层溶液为橙红色的为Br-;下层溶液为紫红色的为I-。
四、常见物质俗名①苏打、纯碱:Na2CO3;②小苏打:NaHCO3;③熟石灰:Ca(OH)2;④生石灰:CaO;⑤绿矾:FeSO4?7H2O;⑥硫磺:S;⑦大理石、石灰石主要成分:CaCO3;⑧胆矾:CuSO4?5H2O;⑨石膏:CaSO4?2H2O;⑩明矾:KAl(SO4)2?12H2O五、铝及其化合物的性质1.铝与盐酸的反响:2Al+6HCl=2AlCl3+3H2↑2.铝与强碱的反响:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑3.铝在空气中氧化:4Al+3O2==2Al2O34.氧化铝与酸反响:Al2O3+6HCl=2AlCl3+3H2O5.氧化铝与强碱反响:Al2O3+2NaOH+3H2O=2Na[Al(OH)4]6.氢氧化铝与强酸反响:Al(OH)3+3HCl=AlCl3+3H2O7.氢氧化铝与强碱反响:Al(OH)3+NaOH=Na[Al(OH)4]六、硅及及其化合物性质1.硅与氢氧化钠反响:Si+2NaOH+H2O=Na2SiO3+2H2↑2.硅与氢氟酸反响:Si+4HF=SiF4+H2↑3.二氧化硅与氢氧化钠反响:SiO2+2NaOH=Na2SiO3+H2O4.二氧化硅与氢氟酸反响:SiO2+4HF=SiF4↑+2H2O5.制造玻璃主要反响:SiO2+CaCO3高温===CaSiO3+CO2↑SiO2+Na2CO3高温===Na2SiO3+CO2↑烷烃CnH2n+2饱和链烃烃烯烃CnH2n(n≥2)存在C=C炔烃CnH2n-2(n≥2)存在C≡C芳香烃:苯的同系物CnH2n-6(n≥6)(1)有机物种类繁多的原因:1.碳原子以4个共价键跟其它原子结合;2.碳与碳原子之间,形成多种链状和环状的有机化合物;3.同分异构现象(2)有机物:多数含碳的化合物(3)烃:只含C、H元素的化合物高二化学必背知识点总结归纳大全分享2一、钠Na1、单质钠的物理性质:钠质软、银白色、熔点低、密度比水的小但比煤油的大。
高二化学《元素及其化合物基础知识和应用》知识点总结

高二化学《元素及其化合物基础知识和应用》知识点总结 1.金属及其化合物 (1)钠及其化合物之间的相互转化①2Na 2O 2+2H 2O===4Na ++4OH -+O 2↑①2Na 2O 2+2CO 2===2Na 2CO 3+O 2①Na 2CO 3+Ca(OH)2===CaCO 3↓+2NaOH①OH -+CO 2===HCO -3①CO 2-3+CO 2+H 2O===2HCO -3(2)铁及其化合物之间的相互转化①Fe +2H +===Fe 2++H 2↑或Fe +Cu 2+===Fe 2++Cu 等 ①2Fe +3Cl 2=====点燃2FeCl 3①2Fe 3++Fe===3Fe 2+或2Fe 3++Cu===2Fe 2++Cu 2+等①4Fe(OH)2+O 2+2H 2O===4Fe(OH)3(3)铝及其化合物之间的相互转化①Al 2O 3+6H +===2Al 3++3H 2O①Al 2O 3+2OH -===2AlO -2+H 2O①Al(OH)3+3H +===Al 3++3H 2O①Al(OH)3+OH -===AlO -2+2H 2O(4)铜及其化合物之间的相互转化①3Cu +8H ++2NO -3===3Cu 2++2NO↑+4H 2O或Cu +4H ++2NO -3===Cu 2++2NO 2↑+2H 2O ①Cu +2H 2SO 4(浓)=====①CuSO 4+SO 2↑+2H 2O①Cu 2++2OH -===Cu(OH)2↓2.非金属及其化合物 (1)卤素单质及其化合物之间的相互转化 ①Cl 2+H 2O H ++Cl -+HClO ①Cl 2+2Br -===2Cl -+Br 2①Br 2+2I -===I 2+2Br -①Cl 2+2OH -===Cl -+ClO -+H 2O(2)硫及其化合物之间的相互转化①2H 2S +SO 2===3S +2H 2O①SO 2+Cl 2+2H 2O===H 2SO 4+2HCl ①2H 2SO 4(浓)+Cu=====①CuSO 4+SO 2↑+2H 2O(3)氮及其化合物之间的相互转化①4NH 3+5O 2=====催化剂①4NO +6H 2O①3NO 2+H 2O===2HNO 3+NO ①3Cu +8HNO 3(稀)===3Cu(NO 3)2+2NO↑+4H 2O(合理即可)(4)碳、硅及其化合物之间的相互转化 ①SiO 2+2C=====高温Si +2CO↑①HCO -3+OH -===CO 2-3+H 2O①SiO 2-3+2H +===H 2SiO 3↓(合理即可)。
高二化学上学期知识点

高二化学上学期知识点【导语】化学是高中学科中比较重要的一门课程,要想学好化学就要掌控更多的化学知识。
下面是作者为大家整理高二化学上学期知识点,期望对大家有所帮助。
高二化学上学期知识点篇(一)氯及其化合物,SiO2+2NaOH==Na2SiO3+H2O,①物理性质:通常是黄绿色、密度比空气大、有刺激性气味气体,能溶于水,有毒。
②化学性质:氯原子易得电子,使活泼的非金属元素。
氯气与金属、非金属等产生氧化还原反应,一样作氧化剂。
与水、碱溶液则产生自身氧化还原反应,既作氧化剂又作还原剂。
拓展1、氯水:氯水为黄绿色,所含Cl2有少量与水反应(Cl2+H2O==HCl+HClO),大部分仍以分子情势存在,其主要溶质是Cl2。
新制氯水含Cl2、H2O、HClO、H+、Cl-、ClO-、OH-等微粒拓展2、次氯酸:次氯酸(HClO)是比H2CO3还弱的酸,溶液中主要以HClO分子情势存在。
是一种具有强氧化性(能杀菌、消毒、漂白)的易分解(分解变成HCl和O2)的弱酸。
拓展3、漂白粉:次氯酸盐比次氯酸稳固,容易储存,工业上以Cl2和石灰乳为原料制取漂白粉,其主要成分是CaCl2和Ca(ClO)2,有效成分是Ca(ClO)2,须和酸(或空气中CO2)作用产生次氯酸,才能发挥漂白作用。
高二化学上学期知识点篇(二)二氧化硫①物理性质:无色,刺激性气味,气体,有毒,易液化,易溶于水(1:40),密度比空气大②化学性质:a、酸性氧化物:可与水反应生成相应的酸——亚硫酸(中强酸):SO2+H2O H2SO3 可与碱反应生成盐和水:SO2+2NaOH==Na2SO3+H2O,SO2+Na2SO3+H2O==2NaHSO3 b、具有漂白性:可使品红溶液褪色,但是是一种暂时性的漂白c、具有还原性:SO2+Cl2+2H2O==H2SO4+2HCl高二化学上学期知识点篇(三)氮及其化合物Ⅰ、氮气(N2)a、物理性质:无色、无味、难溶于水、密度略小于空气,在空气中体积分数约为78% b、分子结构:分子式——N2,电子式——,结构式——N≡Nc、化学性质:结构决定性质,氮氮三键结合非常坚固,难以破坏,所以但其性质非常稳固。
高二上册化学期中知识点复习

高二上册化学期中知识点复习(实用版)编制人:______审核人:______审批人:______编制单位:______编制时间:__年__月__日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如教案大全、书信范文、述职报告、合同范本、工作总结、演讲稿、心得体会、作文大全、工作计划、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!Moreover, our store provides various types of practical materials for everyone, such as lesson plans, letter templates, job reports, contract templates, work summaries, speeches, reflections, essay summaries, work plans, and other materials. If you want to learn about different data formats and writing methods, please stay tuned!高二上册化学期中知识点复习本店铺为大家整理的,在现实学习生活中,大家最不陌生的就是知识点吧!知识点就是掌握某个问题/知识的学习要点。
硫及其重要化合物-教学设计

硫及其重要化合物复习课教学设计一、指导思想与理论依据高中学业考试硫及其重要化合物复习课,主要是以学业考试为教学目标的复习,复习内容的深广度,必需严格依据江苏省普通高中学业水平测试(必修科目)说明的要求和高中化学课程标准的要求,并在此基础上适当培养学生化学分析与思维能力,因为硫及其重要合物内容学生已经在高一经过系统的学习,对硫、二氧化硫、硫酸等知识有了一定的集累,因此对硫及其重要化合物复习课教学设计的目标是:引导学生对已学过硫及其化合物的知识进行条理化,并对各知识点中的重要内容与能力进行串联,让学生对硫及其重要化合物有个整体的认识,体会学习元素化合物知识的一般方法,并形成一定的分析、解决问题的能力。
二、教学内容分析“硫及其重要化合物”普通高中化学课程标准要求的内容目标是:了解硫及其重要化合物的主要性质,认识其在生产中的应用和对生态环境的影响,活动与探究目标:讨论减少向大气中排放二氧化硫的措施。
江苏省普通高中学业水平测试化学(必修科目)说明上的要求是:(1)了解硫的可燃性(2)了解硫及其重要化合物的主要物理性质(3)了解二氧化硫与氧气、与水的反应,认识亚硫酸的不稳定性,认识二氧化硫漂白作用与次氯酸漂白作用的区别。
(4)了解浓硫酸的强氧化性,了解浓硫酸与Cu、C的反应,了解常温下铝、铁在浓硫酸中的钝化现象(5)了解二氧化硫的污染来源及危害,认识工业上生产硫酸的反应原理。
三、学生情况分析硫及其重要的化合物是高中化学教材必修1第四章非金属及其化合物的内容,学生在高一第一学期学习化学时,由于硫及其重要化合物内容中化学实验较多,实验现象也丰富多彩,与生活实际联系也相对密切,所以学生学习硫及其重要化合物兴趣较浓,学习比较认真,基础知识比较扎实,高二分科后长时间的遗忘,加上知识零碎,没有系统性进行整理,因此复习时候主要是把前面零碎的知识按照一定的规律进行系统整合,同时在复习的过程中,重视学生的动手与动脑,避免教师复习一头热,学生只听不练,达不到复习的效果,在复习的过程中主要以引导学生回答为基础,突出学生的主体性,帮助学生去构建其知识网络。
5.1硫及其化合物教学设计2023-2024学年高二下学期人教版(2019)化学必修第二册

-了解硫的其他同素异形体及其性质,如硫链、硫球等。
-探究硫及其化合物在环境保护中的作用,如硫酸厂废气的处理、硫磺回收技术。
-研究硫矿的开采与加工过程,以及硫资源的分布情况。
-阅读有关硫及其化合物在农业中的应用,如硫磺肥料的使用。
-了解硫在生物体内的作用,如蛋白质的合成、细胞呼吸等。
2.拓展建议:
(2)思考硫及其化合物在生活中的应用实例,下节课分享;
(3)查阅资料,了解硫及其化合物的最新研究动态。
6.课堂反馈
最后,请同学们对本节课的教学内容、教学方式等提出意见和建议,以便我更好地改进教学。谢谢大家!希望你们在今后的学习中,能够运用所学知识,解决实际问题,为我们的社会和环境做出贡献。
教学资源拓展
5.1硫及其化合物教学设计2023-2024学年高二下学期人教版(2019)化学必修第二册
授课内容
授课时数
授课班级
授课人数
授课地点
授课时间
教材分析
《5.1硫及其化合物》选自人教版(2019)化学必修第二册,本章节内容以硫元素为主线,深入介绍了硫及其化合物的性质、制备和应用。通过学习硫酸、亚硫酸、硫化氢等重要化合物,使学生掌握硫族元素的化学性质,培养学生在实际情境中分析问题、解决问题的能力。本章节与前期学习的氧化还原反应、酸碱盐等知识紧密相连,为后续学习环境保护、工业化学打下坚实基础。教学内容与实际生活密切相关,注重培养学生的科学素养和环保意识。
-通过查阅科学杂志或图书馆资料,深入研究硫及其化合物的最新研究成果和应用领域。
-组织学生参观当地的化工企业或硫矿,了解硫的实际应用和工业生产过程。
-鼓励学生结合生活实际,收集含硫物质的例子,分析它们在生活中的作用和影响。
高二化学上学期硫及其化合物

;
/forum-jinan-1.html 济南夜场招聘 济南夜总会招聘
济南ktv招聘
orz14msr
百年老铺子了,根深蒂固口碑还算不错。我们的铺子呢,虽然开张的时间并没有多长,但成长的势头很足,说个‘势不可挡’ 大概也不过分吧!您仔细想一想,咱们的铺子就隔着几丈宽的这么一条街,这天长日久你争我夺的,不打个两败俱伤才怪呢!” 看到彭掌柜的开始频频点头了,耿正接着说:“可如果咱们两家把各自所经营的商品做一些调整,比如说,我们让出来丝绸成 衣和各种丝绸制品这两块儿,您这边让出来丝绸面料这一块儿。这样一来,咱们两家的商品销售不就不存在竞争了吗?而且啊, 这原先两边儿的顾客都可以集中到一家来了,最终的销售额肯定就大幅度增加了啊!这是不是各发各的财呢?”彭掌柜的面露 笑容,说:“有些意思!您继续说!”耿正端起茶杯来慢慢喝两口,继续说:“当咱们专心经营某一类商品时,就有精力深入 研究这些商品的市场需求和发展潜力了,这非常有利于把自己的铺子做大做强啊!再则,虽然咱们各自经营的商品并不存在内 在的竞争机制,但所有的丝绸产品本身却又存在着千丝万缕的联系呢!由于我们都了解一些各种产品的发展特点和需求动向, 也就可以随时将各自对于对方销售商品的想法和看法说出来,彼此交换意见,以免错失经营良机,岂不就是互相扶持,共同发 财嘞!”听到这里,彭掌柜的终于完全明白耿正的全部想法了。他非常激动,然而又满面惭愧地给耿正连连作揖,真心真意地 说:“耿掌柜的,我明白您的意思了!您说得很对,咱们各自让出一部分原先经营的商品,就可以做到您说的‘各发各的财’ 和‘互相扶持,共同发财’了!您真是宽胸怀,大智慧啊!老朽佩服,老朽佩服!”耿正赶快还礼,说:“彭掌柜的您可不要 这么说啊。您是长辈,我以后还得好好地向您学习呢!”彭掌柜的却说:“您先不忙向我学习,我倒应该先向您检讨呢!这些 天给贵店铺造成的损失,我,我得想办法来给你们弥补才是啊!”耿正笑了,说:“只要咱们两家把下一步的事情做好了,一 切谣言自然也就不攻自破了,何须您再做什么,说什么啊!”彭掌柜的由衷地说:“耿掌柜的啊,别看您年岁不大,但这生意 经掌握得比老朽我还多呢!这俗话说的‘一分心,二分眼,三分嘴,剩余一分是手’,您都做得绰绰有余了啊!”耿正谦逊地 笑一笑,说:“彭掌柜的您过奖了。在您跟前,我还只是一个什么都不懂的娃娃呢!”两人越谈越投机,当下就做出决定,由 “昌盛丝绸行”让出来丝绸成衣和各种丝绸制品这两块儿,由“彭记丝绸行”让出来丝绸面料这一块儿。从此之后,各店铺只 经营既定的商品类型。对于让出来的那些类型的商品,则可以根据各自不时了解到的新情况,随时向对方提个醒什么的。为了 表明今后会坚持执行这样的采办营销计划,彭掌柜的还主动提出
高二化学必背知识点总结归纳大全分享

高二化学必背知识点总结归纳大全分享高中学习容量大,不但要掌握目前的知识,还要把高中的知识与初中的知识溶为一体才能学好。
在读书、听课、研习、总结这四个环节都比初中的学习有更高的要求。
高二化学知识点1一、硫及其化合物的性质1.铁与硫蒸气反应:Fe+S△==FeS2.铜与硫蒸气反应:2Cu+S△==Cu2S3.硫与浓硫酸反应:S+2H2SO4(浓)△==3SO2↑+2H2O4.二氧化硫与硫化氢反应:SO2+2H2S=3S↓+2H2O5.铜与浓硫酸反应:Cu+2H2SO4△==CuSO4+SO2↑+2H2O6.二氧化硫的催化氧化:2SO2+O22SO37.二氧化硫与氯水的反应:SO2+Cl2+2H2O=H2SO4+2HCl8.二氧化硫与氢氧化钠反应:SO2+2NaOH=Na2SO3+H2O9.硫化氢在充足的氧气中燃烧:2H2S+3O2点燃===2SO2+2H2O10.硫化氢在不充足的氧气中燃烧:2H2S+O2点燃===2S+2H2O二、镁及其化合物的性质1.在空气中点燃镁条:2Mg+O2点燃===2MgO2.在氮气中点燃镁条:3Mg+N2点燃===Mg3N23.在二氧化碳中点燃镁条:2Mg+CO2点燃===2MgO+C4.在氯气中点燃镁条:Mg+Cl2点燃===MgCl25.海水中提取镁涉及反应:①贝壳煅烧制取熟石灰:CaCO3高温===CaO+CO2↑CaO+H2O=Ca(OH)2②产生氢氧化镁沉淀:Mg2++2OH-=Mg(OH)2↓③氢氧化镁转化为氯化镁:Mg(OH)2+2HCl=MgCl2+2H2O④电解熔融氯化镁:MgCl2通电===Mg+Cl2↑三、Cl-、Br-、I-离子鉴别:1.分别滴加AgNO3和稀硝酸,产生白色沉淀的为Cl-;产生浅黄色沉淀的为Br-;产生黄色沉淀的为I-2.分别滴加氯水,再加入少量四氯化碳,振荡,下层溶液为无色的是Cl-;下层溶液为橙红色的为Br-;下层溶液为紫红色的为I-。
高二化学硫及其化合物试题答案及解析
高二化学硫及其化合物试题答案及解析1.下列化学实验事实及其结论都正确的是【答案】B【解析】A、将SO2通入含HClO的溶液中生成H2SO4,主要是HClO的强氧化性氧化SO2;B、正确;C、SiO2只能与HF酸反应与其他酸均不反应,不属两性氧化物;D、SO2使溴水、KMnO4溶液褪色主要是SO2的还原性。
【考点】考查SO2的性质、铝及氧化铝的性质、SiO2的性质等内容。
2.某课外学习小组的同学设计了如图的装置,以验证SO-2的氧化性、还原性和漂白性。
回答以下问题:33.单独检查装置C的气密性的操作是,关闭活塞b,然后________________________,若发现________________,说明装置C气密性良好。
34.用Na2SO3固体和硫酸溶液制取SO2气体,应选用__________(选“A”或“C”)做气体发生装置,不选用另一装置的理由是。
35.小组的同学在A、C装置中的另一个用FeS固体和稀硫酸制取H2S气体,反应的化学方程式为_________________ 。
36.SO2气体通过D装置时现象是____________________ ,通过E装置时现象是________________ ;SO2与H2S在B装置中反应,现象是______________________。
37.F中盛有碱石灰,其作用是______________________。
【答案】33.往试管中加水(1分);若水加不进去(1分)34.C(1分);Na2SO3易溶于水,SO2也易溶于水,不能用有启普发生器功能的装置.(1分,答对1点即可)35. FeS+H2SO4(稀)à Fe SO4+H2S↑(1分)。
36.红色褪去(1分);紫色褪去(1分); 瓶壁有淡黄色粉末和无色的小液滴(1分,答对1点即可)37.吸收尾气(1分)【解析】33.检查装置C的气密性,关闭活塞b,然后往试管中加水,若水加不进去说明装置C气密性良好。
高二化学非金属及其化合物.ppt

下列氯化物既可以由金属与氯
气直接化合得到,又可以由金属与 盐酸反应而制得的是( D )
A、CuCl2 C、FeCl3
B、FeCl2 D、AlCl3
三、硫及其化合物
1、硫 点燃
S + O2 === SO2 Fe+S== FeS
Cu+S== Cu2S H2 + S== H2S
三、硫的化合物 1、二氧化硫 物理性质:无色、有刺激性气味、有毒
四、氮及其化合物 1、N2 2NO+O2==2NO2 红棕色、有毒、 易溶于水、易液化
性 质
放电 N2+O2===2NO 无色、有毒、不溶于水
3NO2+H2O==2HNO3+NO 形成酸雨、制硝酸
2、氨 物性:无色、有刺激性、极易溶于水、易液化
NH3+H2O NH3·H2O
化 性
NH3+HCl==NH4Cl
பைடு நூலகம்
一、硅及其化合物 1、硅
原子结构: +14 2 8 4 存在形式:主要以氧化物和硅酸盐形式存在
主要性质:灰黑色、熔点高、硬度大、 半导体、性质不活泼
主要用途:半导体材料、太阳能电池
2、二氧化硅 存在形式:硅石、水晶、石英、玛瑙
SiO2+4HF==SiF4↑+2H2O
高温
主要性质: SiO2+CaO===CaSiO3 SiO2+2NaOH==Na2SiO3+H2O
4、硅酸盐
概念:由硅、氧和金属组成的化合物的总称 陶瓷:以黏土为原料
产品 水泥:以黏土和石灰石为原料
玻璃:以纯碱、石灰石、石英为原料 水溶液俗称水玻璃,在空气中易
高二化学硫及其化合物试题答案及解析

高二化学硫及其化合物试题答案及解析1.下列叙述正确的是A.往待测液中滴加氯水,然后滴加KSCN溶液,以检测待测液中是否含有Fe2+B.往待测液中滴加BaCl2,然后滴加盐酸,以检测待测液中是否含有SO42-C.蒸馏操作时应将温度计的水银球插入液面下D.向试管中加入5mL SO2水溶液,然后滴加BaCl2溶液,再滴加3%的H2O2溶液,以检测SO2具有还原性【答案】D【解析】A、先滴加氯水,再滴加KSCN溶液,溶液变红,不能证明原溶液中含有亚铁离子,应先滴加KSCN溶液后滴加氯水,错误;B、加入氯化钡溶液,再加稀盐酸,产生沉淀不能证明原溶液中含有硫酸根离子,因为溶液中含有银离子也会有沉淀产生,不能排除Ag+,错误; C、蒸馏时温度计的水银球应在蒸馏烧瓶的支管口附近,错误;D、向试管中加入5mL SO2水溶液,然后滴加BaCl2溶液,再滴加3%的H2O2溶液,有白色沉淀产生,证明有硫酸钡生成,可以检测二氧化硫具有还原性,正确,答案选D。
【考点】考查离子的检验2.为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验Ⅰ:反应产物的定性探究。
实验装置如图所示:(固定装置已略去)(1)A中反应的化学方程式为。
(2)F烧杯中的溶液通常是。
(3)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是。
(5)为说明浓硫酸中的水是否影响B装置现象的判断,还须进行一次实验。
实验方案为。
实验Ⅱ:反应产物的定量探究(6)在铜与浓硫酸反应的过程中,发现有黑色物质出现,经查阅文献获得下列资料。
资料1:-12、Cu7S4中的一种或几种。
仅由上述资料可得出的正确结论是 __。
a.铜与浓硫酸反应时所涉及的反应可能不止一个b.硫酸浓度选择适当,可避免最后产物中出现黑色物质c.该反应发生的条件之一是硫酸浓度≥15 mol/Ld.硫酸浓度越大,黑色物质越快出现、越难消失(7)为测出硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00mL加入足量KI溶液振荡,以淀粉溶液为指示剂,用b mol/L Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液V mL。
高二化学总结无机化学化合物分类总结

高二化学总结无机化学化合物分类总结化学化合物是由不同元素以一定比例结合形成的物质。
根据元素之间的化学键类型、化学键性质以及化合物的物理性质,无机化学化合物可以被分为以下几类:离子化合物、共价化合物和配位化合物。
一、离子化合物离子化合物是由离子组成的,其中,阳离子带正电荷,阴离子带负电荷。
离子化合物通常由金属和非金属元素构成。
离子化合物晶体具有高熔点和良好的导电性。
1. 卤素化合物卤素化合物是由卤素(氯、溴、碘)和金属元素(钠、钾)或非金属元素(氢)构成的离子化合物。
其中,氢氯酸(HCl)、氢溴酸(HBr)和氢碘酸(HI)是常见的卤素酸。
2. 氧化物氧化物是由金属和氧元素组成的离子化合物。
金属的氧化数为正数。
例如,氧化钠(Na2O)和氧化铝(Al2O3)是常见的氧化物。
3. 硫化物硫化物是由金属和硫元素组成的离子化合物。
硫化物在自然界中广泛存在,如黄铁矿(FeS2)和辉锑矿(Sb2S3)。
二、共价化合物共价化合物是由共价键连接的非金属元素形成的化合物。
在共价化合物中,原子间共享电子对。
1. 二、三元共价化合物二元共价化合物由两种非金属元素构成,如二氧化碳(CO2)和三氯化磷(PCl3)。
三元共价化合物由三种非金属元素构成,例如硫三氟化物(SF3)。
2. 有机化合物有机化合物是由碳元素和氢元素以及其他非金属元素构成的化合物。
有机化合物具有碳骨架,并且常包含其他元素如氧、氮和硫等。
例如,甲烷(CH4)和乙醇(C2H5OH)是常见的有机化合物。
三、配位化合物配位化合物是由金属离子与一个或多个配体形成的。
在配位化合物中,金属离子常常充当中心离子,而配体则以季齐等方式与中心离子配位。
1. 配位数配位数指配位化合物中与中心金属离子配位的配体数目。
根据配位数的不同,配位化合物可以分为一配位、二配位、三配位等。
例如,四羰基合铁(II)离子(Fe(CO)4)是一配位化合物。
2. 配体种类配体是指与金属离子配位形成配位键的非金属离子或分子。
河北省行唐县高二化学 第四章 非金属及其化合物 第三节 第1课时 苏教版

一、硫 1.硫的存在
硫和氮的氧化物 二氧化硫和三氧化硫
基础梳理
(1)游离态:存在于 火山口 或 地壳的岩层 里。 (2)化合态: ①主要以 硫化物和硫酸盐 的形式存在。 ②重要的化合物 名称 化学式 硫铁矿 FeS2 芒硝 Na2SO4· 黄铜矿 CuFeS2 石膏 CaSO4·
C
)
A.SO2 是硫及某些含硫化合物在空气中燃烧的产物
解析 SO2 与水反应生成的是 H2SO3 而不是 H2SO4。
2.下列有关三氧化硫的说法中,正确的是 B.标准状况下,1 mol SO3 的体积约为 22.4 L C.硫粉在过量的纯氧中燃烧可以生成 SO3
(
A
)
A.三氧化硫极易溶于水,且与水反应生成 H2SO4
故 SO2 有还原性,但 CO2 不具有还原性。由以上知识对题 目逐项分析即得答案。A 项检验的是 SO2;B 项不管是否 混有 CO2 都不会产生白色沉淀; 项不管有没有 CO2 都会 C 产生白色沉淀,均不能验证有无 CO2;只有 D 项,酸性 KMnO4 溶液将 SO2 完全吸收,再通过澄清石灰水若有白 色沉淀,说明一定有 CO2;若无沉淀,则无 CO2。
酸性氧化物 的性质
溶液颜色 SO2 的水溶液
变红色
显 酸性
溶液先 变红 ,振 SO2 的漂 白性 荡后 褪色 ,再加 热后,溶液颜色
SO2 具有 漂白 性, 但生成的化 合物不稳定
恢复红色
(1)酸性氧化物的通性 ①与水反应: H2O+SO应 2NaOH+SO2===Na2SO3+
能力提升 7.A、B 是两种有刺激性气味的气体,试根据下列实验现 象填空:
(1)推断 A―→F 各是什么物质(写化学式) A________、B________、C________、D________、 E________、F________。 (2)写出 A、B 跟水反应的离子方程式: __________________________________________。
第一章 化学反应的热效应 测试题--高二上学期化学人教版(2019)选择性必修1 (1)

第一章《化学反应的热效应》测试题一、单选题(共12题)1.硫及其化合物在生产、生活和科学研究中有广泛的应用。
SO 2可添加到食品中作为漂白剂、防腐剂和抗氧化剂:工业上常用V 2O 5催化O 2氧化SO 2制取SO 3,进而制得H 2SO 4,H 2SO 4溶于水后可电离出H +和SO 24。
450℃、V 2O 5催化SO 2和O 2反应时、能量变化如图所示,反应机理如下:反应℃:V 2O 5(s)+SO 2(g)=V 2O 4(s)+SO 3(g) ℃H 1=24kJ·mol -1 反应℃:2V 2O 4(s)+O(g)=2V 2O 5(s) ℃H 1=-246kJ·mol -1下列说法正确的是 A .反应(1)的℃S=0B .反应(2)是慢反应,决定该反应速率C .2SO 2(g)+O 2(g)=2SO 3(g) ℃H=-202kJ·mol -1D .使用V 2O 5可以降低反应的焓变2.分别取50 mL0.50 mol/L 盐酸与50 mL0.55 mol/L 氢氧化钠溶液混合进行中和热的测定,下列说法不正确的是A .仪器A 的名称是环形玻璃搅拌棒B.用稍过量的氢氧化钠可确保盐酸完全反应C.为减少热量损失,酸碱混合时需将量筒中NaOH溶液快速倒入小烧杯中D.用稀硫酸和Ba(OH)2代替盐酸和NaOH溶液进行反应,结果也正确3.1,3-丁二烯在环己烷溶液中与溴发生加成反应时,会生成两种产物M和N(不考虑立体异构),其反应机理如图1所示;室温下,M可以缓慢转化为N,能量变化如图2所示。
下列关于该过程的叙述正确的是A.室温下,M的稳定性强于NB.∆H= (E2-E1)kJ‧mol-1C.N存在顺反异构体D.有机物M的核磁共振氢谱中有四组峰,峰面积之比为2:1:2:24.下列化学反应的能量变化与如图不符合的是A.2NH4Cl+Ca(OH)2Δ2NH3↑+CaCl2+2H2O B.2Al+Fe2O3高温2Fe+Al2O3C.Mg+2HCl=MgCl2+H2↑D.C+O2点燃CO25.反应H2(g)+12O2(g)→H2O(g)的能量变化如图所示,a、b、c表示能量变化数值,单位为kJ。
(第1周答案)2022-2023学年人教版(2019)高二化学上学期期末达标测试卷(A卷)

2022-2023学年人教版(2019)高二化学上学期期末达标测试卷(A 卷)分数:100分 时间:90分钟一、选择题:本大题共14小题,每小题3分,共42分。
1.下列有关反应热和能量的说法正确的是( )A.热化学方程式中,如果没有注明温度和压强,则表示的反应热是在标准状况下测得的B.化学能:2 mol H 原子>1mol 2H 分子C.根据能量守恒定律,反应物总能量等于生成物总能量D.运用盖斯定律也无法计算碳不完全燃烧时的反应热2.已知:3224NH (g)5O (?g )4NO(g)6H O(g)++,若反应速率分别用()()()322NH O (NO)H O v v v v 、、、[单位为mol/(L ·min)]表示,则正确的关系式是( )A.()()324NH O 5v v = B.()()225O H O 6v v = C.()()322NH H O 3v v = D.()24O (NO)5v v =3.下列措施可使2H 的生成速率减小的是( ) A.Na 与2H O 反应制取2H ,增加2H O 的用量B.Al 与稀硫酸反应制取2H ,向稀硫酸中加入24K SO 溶液C.Mg 与2H O 反应制取2H ,将冷水改为热水D.碳粉与2H O (g )反应制取2H ,增加碳粉的用量4.锂-氟化碳电池是理论质量能量密度最高的一次电池,电池反应为()n CF +nLinLiF+nC 。
下列说法正确的是( )A.锂电极是电源正极B.()n CF 发生了还原反应C.电子由锂电极通过电解液流向()n CF 电极D.电池负极反应:()--n CF +nenF +nC5.醋酸()3CH COOH 是一种常见的弱酸。
下列叙述正确的( ) A.pH=3的3CH COOH 溶液中,()()3HCH COO c c +-=B.pH=8的3CH COOH 和3CH COONa 混合溶液中,()()3CH COO Na c c -+<C.130.1mol L CH COONa -⋅溶液中,()()()()3Na OH CH COO H c c c c +--+>>>D.130.1mol L CH COONa -⋅溶液中,()()()3NaCH COO OH c c c +--=+6.下列热化学方程式书写正确的是(H ∆的绝对值均正确)( ) A.()()()()25222C H OH l 3O g 2CO g 3H O g ?1367.0k m +/ol +J H ∆=-(H ∆代表乙醇燃烧热)B.()()()()24242H SO aq 2NaOH aq Na SO aq 2H O l 114.6k ++J/mol H ∆=-(H ∆代表中和热)C.()()()2222H g O g 2H O g Δ483.+6kJ/mol H =-(反应热)D.22C+O CO Δ393.5kJ/mol H =-(反应热)7.键能指气态分子中1mol 化学键解离成气态原子所吸收的能量。
高二化学选择性必修一考点复习

高二化学选择性必修一考点复习1.高二化学选择性必修一考点复习篇一硫及其化合物的性质1.铁与硫蒸气反应:Fe+S△==FeS2.铜与硫蒸气反应:2Cu+S△==Cu2S3.硫与浓硫酸反应:S+2H2SO4(浓)△==3SO2↑+2H2O4.二氧化硫与硫化氢反应:SO2+2H2S=3S↓+2H2O5.铜与浓硫酸反应:Cu+2H2SO4△==CuSO4+SO2↑+2H2O6.二氧化硫的催化氧化:2SO2+O22SO37.二氧化硫与氯水的反应:SO2+Cl2+2H2O=H2SO4+2HCl8.二氧化硫与氢氧化钠反应:SO2+2NaOH=Na2SO3+H2O9.硫化氢在充足的氧气中燃烧:2H2S+3O2点燃===2SO2+2H2O10.硫化氢在不充足的氧气中燃烧:2H2S+O2点燃===2S+2H2O2.高二化学选择性必修一考点复习篇二铝Al1、单质铝的物理性质:银白色金属、密度小(属轻金属)、硬度小、熔沸点低。
2、单质铝的化学性质①铝与O2反应:常温下铝能与O2反应生成致密氧化膜,保护内层金属。
加热条件下铝能与O2反应生成氧化铝:4Al+3O2==2Al2O3②常温下Al既能与强酸反应,又能与强碱溶液反应,均有H2生成,也能与不活泼的金属盐溶液反应:2Al+6HCl=2AlCl3+3H2↑(2Al+6H+=2Al3++3H2↑)2Al+2NaOH+2H2O=2NaAlO2+3H2↑(2Al+2OH-+2H2O=2AlO2-+3H2↑)2Al+3Cu(NO3)2=2Al(NO3)3+3Cu(2Al+3Cu2+=2Al3++3Cu)注意:铝制餐具不能用来长时间存放酸性、碱性和咸的食品。
③铝与某些金属氧化物的反应(如V、Cr、Mn、Fe的氧化物)叫做铝热反应Fe2O3+2Al==2Fe+Al2O3,Al和Fe2O3的混合物叫做铝热剂。
利用铝热反应焊接钢轨。
3.高二化学选择性必修一考点复习篇三氨气及铵盐氨气的性质:无色气体,刺激性气味、密度小于空气、极易溶于水(且快)1:700体积比。
上海高二化学学业水平考复习讲义5

第五章评说硫、氮的“功”与“过”——学案一、基本概念1.物质的量浓度【例1】关于浓度2mol·L-1的MgCl2溶液,下列叙述正确的是( ) A.1L水中溶解了2molMgCl2固体B.1L溶液中含有2×6.02×1023Cl-C.取0.5L该溶液,则Mg2+的物质的量浓度为1mol·L-1D.0.5L溶液中,Mg2-和Cl-的离子总数约为3×6.02×1023个二、基本原理1.水的电离、pH——水的电离平衡和水的离子积常数,pH的含义,pH与酸碱性的关系【例1】水是极弱的电解质,其电离方程式;溶液pH是指;水的离子积Kw是指。
【例2】25︒C时,水中c(H+) = 1⨯10-7 mol/L,此时,Kw = ,pH= ;99︒C时,水中c(H+) = 1⨯10-6 mol/L,此时,Kw = ,pH= 。
【例3】配制pH = 12 的氢氧化钠溶液500 mL,需要NaOH固体()A.0.1 g B.0.2 g C.0.3 g D.0.4 g.【例4】下列物质不能破坏水的电离平衡的是( )A.NaCl B.H2S C.Na2S D.NH4Cl三、元素及化合物1.硫及其化合物(1)硫单质硫的物理性质:色溶于水的固体,溶于酒精,易溶于。
硫的化学性质:①与Fe、Cu、Hg等金属反应、②与H2、O2等非金属反应【例1】硫的原子结构示意图:,硫的离子结构示意图:。
【例2】写出黑火药燃烧的化学方程式:。
其中氧化剂是:,还原剂是:。
【例3】下列化合物中不能由单质直接化合而制成的是:()。
A.FeS B.Cu2S C.SO3D.Al2S3【例4】以下能说明氯的非金属性比硫强的最主要事实是:()。
A.在通常情况下,硫为浅黄色固体,而氯为黄绿色气体。
B.硫不溶于水,而氯气溶于水。
C.跟金属或氢气反应时,硫最终显-2价,而氯最终显-1价。
D.跟同一种有可变价态的金属反应时,金属被硫氧化到低价态,被氯氧化到高价态。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
[单选]县级以上人民政府信访工作机构收到信访事项,应当予以登记,并区分情况,在()日内分别按规定要求,以不同的方式处理。A.30B.20C.15D.10 [多选]某工地塔吊未按安全生产规定进行按时检查加固。为了赶进度,管理者明知存在安全隐患,仍继续要求施工,结果在施工过程中倒塌,造成重大伤亡。对此应负刑事责任的有()。A.该工地的负责人B.负责塔吊安全的管理人C.塔吊的销售人员D.该建筑公司的负责人E.工地上的施工人员 [单选]根据我国《公司法》规定,下列选项中可以担任有限责任公司监事、高管人员的是()。A.公司的股东B.公司的经理C.公司的董事D.公司的财务负责人 [问答题,简答题]工件或夹具的定位精度有哪些? [单选]捻转补泻法中的补法是()。A.捻转角度大,频率慢,用力轻B.捻转角度小,频率快,用力重C.捻转角度大,频率快,用力重D.捻转角度小,频率慢,用力轻E.捻转角度小,频率慢,用力重 [单选]下列不属于分拆上市功能效应分析的是()。A.使子公司获得自主的融资渠道B.有效激励子公司管理层的工作积极性C.解决投资不足的问题D.股票增值 [单选]面对面处理顾客抱怨的时候,如果你的时间非常紧迫而顾客却唠唠叨叨的没完,你应该怎么办?()A.以平和的方式让顾客把话说完,并仔细倾听B.礼貌地告诉他你已经明白他的意思了,请他不用说了C.叫一个没有事情做的同事来继续听他说话D.任由他唠叨,自己做自己其他的事情E.装作 [填空题]催化液态烃H2S含量指标为()。 [单选]在霍奇金病中,结节硬化型常见于()A.年轻女性B.年轻男性C.老年患者D.儿童患者E.膈下受侵 [单选]注册建造师王某与原施工单位解除了聘用合同,选择一家在本专业有多项工程服务资质的施工单位担任建设工程施工的项目经理,则他必须进行()。A.初始注册B.延续注册C.变更注册D.增项注册 [单选,A2型题,A1/A2型题]骨髓中嗜碱性粒细胞明显增多,与下列何种疾病的诊断关系不大().A.急性粒细胞性白血病B.慢性粒细胞性白血病C.嗜碱性粒细胞性白血病D.放射线照射反应E.以上都正确 [单选]下列骨折最容易发生骨筋膜室综合征的是()A.锁骨骨折B.肱骨干骨折C.桡骨远端骨折D.肱骨髁上伸直型骨折E.尺骨上1/3骨折 [单选,A2型题,A1/A2型题]结核性腹膜炎最多见的病理分型是()A.粘连型B.渗出型C.干酪型D.混合型E.坏死型 [单选]不可再生自然资源的影子价格应按资源的()计算;可再生自然资源的影子价格应按资源的()计算。A.再生费用,机会成本B.机会成本,再生费用C.机会成本,经济价值D.经济价值,再生费用 [单选]各热流的换热顺序安排与()有关。A.换热温差B.流量C.温度D.温位和热容器 [填空题]氨合成反应的特点()、()、()、()的反应。 [问答题,简答题]财政政策工具有哪些? [问答题,简答题]霍乱有哪些传播途径? [填空题]可燃物体主要有等()、()、()。 [多选]下列有关行政法规、规章的说法哪些是正确的?()A.为执行国务院的决定和命令,地方政府规章可以作出规定B.同一机关制定的行政法规、规章,特殊规定与一般规定不一致的,适用特殊规定C.行政法规、规章违背法定程序的,可以构成被撤销的理由D.除特定情况外,行政法规应当自通 [单选,A2型题,A1/A2型题]()是医务人员先天具有或后天所习得的引发医学道德行为的心理体验。A.医德认识B.医德情感C.医德意志D.医德品质 [单选]标志桩应设在管段()或有隐蔽工程的地方,做以标记。A.重要B.明显C.软弱D.腐蚀 [单选,A1型题]驰张热型伴寒战常见于()A.伤寒B.传染性单核细胞增多症C.败血症D.支原体肺炎E.系统性红斑狼疮 [单选,A2型题,A1/A2型题]风湿性心脏病二尖瓣狭窄患者,出现右心衰竭,下列哪项临床表现将减轻()A.下肢水肿B.第一心音C.颈静脉怒张D.心尖区舒张期隆隆样杂音E.呼吸困难 [单选]由()代表国家行使国有土地所有权。A、国务院B、市、县人民政府C、国务院土地行政主管部门D、市、县人民政府土地行政主管部门 [问答题]-15℃等于多少开尔文?293.15K等于多少摄氏度? [单选]下列关于确定调查人员的说法有误的是()。A、要选派政策水平高、熟悉业务、组织协调能力强的人担任调查负责人B、要根据案件的具体情况、复杂程度来确定调查人员的数量C、特别重大案件,要请上级部门或其他单位的同志参与调查D、与被调查人有亲友关系或与案件有利害关系的办 [单选,A2型题,A1/A2型题]口角位置相对于()A.尖牙与第一前磨牙之间B.中切牙与尖牙之间C.第一、二前磨牙之间D.第二前磨牙与第一磨牙之间E.中切牙与尖牙之间 [单选]主合同和从合同是以()条件划分的。A.按照当事人是否相互负有义务划分B.按照合同的成立是否以标的物的交付为必要条件划分C.按照合同表现形式划分D.按照相互之间的从属关系划分 [单选]调节声带运动的软骨主要为()A.甲状软骨B.环状软骨C.会厌软骨D.杓状软骨E.小角软骨 [填空题]医疗保险监督的内容()、()。 [单选]小儿结核性脑膜炎或化脓性脑膜炎出现急性偏瘫的主要原因是()A.脑室管膜炎B.细菌栓塞C.急性脑膜脑炎D.脑脓肿E.脑动脉内膜炎 [单选]黏膜皱襞密集的肠管为()。A.十二指肠B.空肠C.回肠D.回盲部E.结肠 [单选]以下哪项不属于专业建筑工程设计服务包括工程设计基本服务。()A.编制专业建设工程初步设计文件B.施工图设计文件服务C.采用标准设计和复用设计服务D.参加试车(试运行)考核和竣工验收等服务 [单选,A2型题]1岁小儿滚落床下,恰巧碰翻地上热水壶,小儿全身皮肤与衣服粘连一起,这时对烫烧伤的小儿,错误的措施()A.是B.迅速将小儿抢离火场或脱离烫伤源C.迅速将烫烧伤部位衣服撕掉D.用清洁被单包裹E.较小灼伤可清洗创面F.及时送往医院 [单选,A1型题]导致感冒的主因是()。A.寒邪B.热邪C.风邪D.湿邪E.暑邪 [填空题]一般照明用电为(),通过人体的安全电压为()。 [单选]放射性核素示踪技术中用于标记的核素称为()A.示踪剂B.指示剂C.标记原子D.分离剂E.催化剂 [单选]《女职工劳动保护特别规定》的适用范围是()。A、国家机关、人民团体、企业、事业单位的女职工B、国家机关、企业、事业单位、社会团体、个体经济组织C、国家机关、企业、事业单位、社会团体、个体经济组织以及其他社会组织等用人单位D、国家机关、企业、事业单位、社会团体 [名词解释]同位素成分
