第五章相图(冶金物理化学)PPT课件
第5章 相图

2.可逆与不可逆多晶转变
z 多晶转变相图 4个单相区
晶型II熔融曲线
晶型转变线 晶型I的升华曲线
熔体的蒸气压曲线
3相平衡点: 晶型II的升华曲线 晶型II、熔体和气相
3相平衡点: 晶型I、II和气相
z 多晶转变相图(介稳平衡态)
过热晶型I熔融曲线 过热晶型I的介稳单相区
过冷熔体的介稳单相区
硅钙石:不一致熔 各种高炉矿渣中
水泥熟料生产重要
9%体积效应
C2S:一致熔融化合物 具有复杂的多晶转变 C3S:不一致熔融化合物
2150℃ ~ 1250℃
IV. 三元系统相图
对于三元凝聚态系统, C=3,n=1(T)
相律:F = C-P + n = 4-P
Fmin = 0,Pmax = 4 Pmin = 1,Fmax = 3
z 自由度(F)
在温度、压力、组分浓度等可能影响系统平衡状态的变量中, 可以在一定范围内任意改变而不会引起旧相消失或新相产生的 独立变量数目.
z 组分及独立组分(C)
组分 系统中每个能独立分离出来,并能独立存在的化学纯物质. 独立组分 足以表示系统中各个相的组成所需的组分的最小数目.
C = 组分数-独立的化学反应数-独立的限制条件数
M’熔体的结晶路程
液相点
L M’
1
F=2
L→S F=1
3
L→S F=1
5
固相点
L→S 2
4 L→S
6S
M
⑦ 形成有限固溶体的二元相图
B在A中 形成的 固溶体
SA(B)的 溶解度 曲线
B在A中 的最大 固溶度
A在B中 的最大 固溶度
A在B中 形成的 固溶体
冶金物理化学第5章熔渣-脱氧及选择性氧化

6
4.9 钢液脱氧反应 9
4. 注意
1. 2. 脱氧能力最强的元素,其ωmin不是钢液脱氧的实际要求。 对同一脱氧元素,可能有不同的脱氧产物生成。
例:Al脱氧
7
4.9.4 锰、硅、铝的脱氧反应
一、Mn脱氧
Mn是弱脱氧剂.其脱氧产物不能是纯MnO,而是MnO与FeO的熔体。相当于[Mn] 高时的脱氧产物。
4.9 钢液脱氧反应
吹氧 铁 钢
随C含量的降低,钢液中溶解氧的含量会不断提高, 影响: 影响: 后序的合金化; 在钢液冷却与凝固过程发生氧化反应,造成气孔和夹杂。 氧化冶炼终了必须脱氧。 脱氧的基本方法:结合成氧化物而分离去除。
0
4.9 钢液脱氧反应
1. 沉淀脱氧
1
4.9 钢液脱氧反应
1. 沉淀脱氧
再由FeO的熔化自由能数据:
(1)+(6)-(4)得
11
4.9.4 锰、硅、铝的脱氧反应
二、Si脱氧 1600 ℃时,FeO与SiO2能形成熔体。
图7-104.9.4 锰、硅、铝的脱氧反应
三、Al脱氧
铝是强脱氧剂。炼钢中常用它作终脱氧,并可控制晶粒。由FeO-A1203相图。
13
4.9.4 锰、硅、铝的脱氧反应
当W[Al]>(9x 10-6)%时,产物是A1203。所以,一般情况下铝脱氧反应写为:
1600℃ 时, W[Al]低于(9xI0-6)%,含氧超过0.06%时,脱氧产物是FeO-A1203反应为
1600℃
时,
14
4.9.4 锰、硅、铝的脱氧反应
将(a)、(b)两式取对数:
将以上两式作图,如图所示。
15
4.9.4 锰、硅、铝的脱氧反应
相图分析ppt课件
当碳在铁中的含量超过溶解度时,多余碳以Fe3C 形式存在于铁碳合金,称为渗碳体。
Fe3C硬度高、强度低(b35MPa), 脆性大, 塑 性几乎为零。
Fe3C是一个亚稳相,在一定条件下可发生分解: Fe3C→3Fe+C(石墨), 该反应对铸铁有重要意义。
42
最新编辑ppt
⒉ 碳在铁中的固溶度
形成稳定化合物的合金: 性能-成分曲线出现拐点。
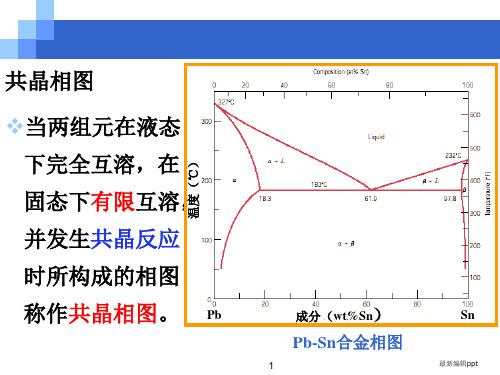
❖共晶合金
两相机械混合物的合金: 性能与合金成分呈直线关
系,是两相性能的算术平
均值。
混= ∙Q + β∙Qβ
HB混=HB ∙Q +HBβ∙Qβ
(Q 、Qβ为两相相对重量)36
最新编辑ppt
相图铸造性能的关系
固溶体合金:
液固相线间距越大、偏
析倾向大, 树枝晶发达, 流动性降低, 补缩能力 下降, 分散缩孔增加.
三条水平线hjbpskfe55一工业纯铁002二钢002214c高温组织为单相亚共析钢002077c共析钢077c过共析钢077214c214二fefec合金的平衡结晶过程56三白口铸铁214669c铸造性能好亚共晶白口铸铁21443c共晶白口铸铁43c过共晶白口铸铁43669c21457工业纯铁的结晶过程12点间转变为34点间56点间7点开始从中析出fe585921460共析相图与共晶相图相似共析相图与共晶相图相似共析线共析线pskpsk线线共析点共析点s点点共析温度共析温度共析共析成分成分共析合共析合金金共析成共析成分合金分合金亚共析合金亚共析合金共共析线上共析点以左的合析线上共析点以左的合金金过共析合金过共析合金共析线共析线上共析点以右的合金上共析点以右的合金
61
铁碳合金相图
最新编辑ppt
铁碳相图课件

亚共晶白口铁相组成物与组织组成物相对量
1148
oC时初晶γ相析出完毕,剩余L发生共晶反应,形成Ld;
继续冷却时,初晶γ相和共晶γ相中均将析出Fe3CII,冷却到
727 oC时剩余初晶γ相转变为P,Ld转变为Ld′;
室温相组成:α+Fe3C; 室温组织组成:P+Ld′+Fe3CII 以3.0%C的亚共晶白口铁为例,1148 oC时:
6.69 0.4 w 100% 94% 6.69 0.0218 wFe3C 1 94% 6%
组织组成物相对量
0.77 0.4 100% 49% 0.77 0.0218 wP 1 49% 51% wF先
21/70 21/66 /63
14/70 14/66 /63
2、共析钢结晶过程
室温组织:P(F+Fe3C)
单相液体的冷却
15/70 15/66 /63
匀晶反应 L 相中析出 γ 相(奥氏体 A )
γ单相固溶体的冷却
γ相发生共析反应生成珠光体P
16/70 16/66 /63
共析转变:由一个固相在恒温下转变为另外
两个固相的转变。组织为F+FeC3两相交替排
亚共析钢组织组成物中Fe3CIII最大含量
含0.0218%C的过共析钢冷却到室温时析出的Fe3CIII 最多。 wFe3CIII 0.0218 0.0008 100% 0.3% 6.69 0.0008
4、过共析钢结晶过程
室温组织P+Fe3CⅡ
单相液体的冷却 L相→ γ相(A)
组成物是什么?如何计
算?
5%C钢在1148 oC时 的组织组成物是什 么?如何计算?
!第五章-课件Fe-C相图4

温度下降, Fe3CⅡ量增加。到4点, 成分沿
ES线变化到S点,余下的 转变为P。
室温组织为:P+ Fe3CⅡ
凝固过程:L→L+γ→γ→γ+Fe3CⅡ →P + Fe3CⅡ
珠光体金相组织
在同一珠光体中,铁素体和渗碳体具有一定的晶体学位向关系
亚共析钢(Wc=0.0218~0.77% )的平衡结晶过程及组织
冷却曲线如图:
室温组织为:α+ P 的白色为α。 过程如下:L→L+δ→ L+δ+γ→L+γ→ γ→α+γ → α+P+γ→α+ P (析出Fe3CⅢ)
需注意:①室温组织为α+ P, 由于α发生在共析转变之前, 称为先共析铁素体。 ②共析转变之前α和γ的相对量 (即共析转变后α和P的相对量) 可通过杠杆法则计算。
N
L+ H B
J
+
+
S
铁素体
转变过程:L→L+δ→δ→δ+γ→γ →α+γ→α→α+ Fe3CⅢ
共析钢(Wc=0.77%)的平衡结晶过程及组织
合金液体在1-2点间转 变为。到S点发生共析 转变:S⇄P+Fe3C, 全 部转变为珠光体。
L→L+γ→γ→P(α+ Fe3C)
共析钢的室温组织
亚共析钢的室温组织
亚共析钢室温下的组织为F+P . 在0.0218~0.77%C 范围内珠光体量随含碳 量增加而增加。
大学材料科学基础 第五章铁碳相图(2)

1.2% C过共析钢室温下平衡组织
计算1.2%C 过共析钢中Fe3CII和Fe3C的含量。
亚共析钢和过共析钢的固态相变区别:亚共析钢中先 共析相是F,过共析钢中先共析相是Fe3C。
The evolution of the microstructure of hypoeutectoid and hypereutectoid steels during cooling. In relationship to the Fe-Fe3C phase diagram.
(2)碳在铁中的固溶体 铁素体:碳在α铁中的间隙固溶体,用α 或F (ferrite) 表示。碳在δ铁中的间隙固溶体 也称高温铁素体,用δ表示。 奥氏体:碳在γ铁中 的间隙固溶体,用γ或A (austenite) 表示。
工业纯铁的显微组织
奥氏体的显微组织
(3)渗碳体(Fe3C,cementite) 渗碳体是铁和碳形成 的化合物,具有复杂的晶 体结构,熔点为1227℃。 渗碳体硬度极高,塑性几 乎等于0,是硬脆相。是 钢中的主要强化相。在一 定条件下,渗碳体可以分 解而形成石墨状的自由碳: Fe3C→3Fe + C(石墨)。这 一过程对于铸铁和具有重 要意义。
三、 铁碳合金相图
铁碳相图的历史很悠久了,早在1897年, 英国皇家矿业学院教授Roberts Austen 就绘制了 世界上第一张铁碳相图,1900年,荷兰阿姆斯特 丹大学的物理化学教授Roozeboom根据相律对其 做了修订,与我们目前使用的铁碳相图已基本相 同。 铁碳合金是现代工业使用最广泛的合金,即 碳钢。生产中使用的钢铁材料90%是碳钢,10% 是合金钢。铁碳相图是研究铁碳合金的重要工具, 对于钢铁材料的研究和使用, 特别是热加工工艺 的制订都有重要的指导意义。
相图在冶金中的应用全解PPT课件

第一讲:绪论
• 组元(指独立组元)
• 组元是构成平衡体系中各相所需要的最少的独立 成分。
• 组元数不一定等于构成该体系的物种数。 • 组元数与物种数的区别和联第12页/共59页
第一讲:绪论
• 组元(指独立组元)
• 体系的组元数为1,单元系 • 组元数为2、二元系 • 其余类推
Temperature (oC)
CaO - MgO
Data from FToxid - FACT oxide database 2010
ASlag-liq
0.236
0.410
2374o
AMonoxide + AMonoxide#2
2825o
0.944
0.2
0.4
0.6
0.8
1
mole MgO/(CaO+MgO)
)
G fus A(TB )
RT
ln
a(l) A(TB
)
T
* f,
A
G
fus A
0
fus
H
A
Tf*,
A
S
fus A
第36页/共59页
第二讲:二元系
• 简单共熔(共晶)型二元系相图计算的原理
• A的熔点 处 T f*, A
•
fus
S
A
设
fus
H
A
T* f ,A
随温度
变化fu不sSA大和, f则usH
A
TB
)
T* f ,A
G fus A(TB )
RT
ln
a(l) A(TB
)
R
T
ln
a
金属材料与热处理第五章-铁-碳-合-金ppt课件

29
图5-21 铁碳合金组织、性能与成分的对应关系
30
五、铁碳相图的应用
铁碳相图从客观上反映了钢铁材料的组织随 化学成分和温度变化的规律, 因此,在工程上为选材 及制定铸造、锻造、焊接、热处理等热加工工 艺提供了重要的理论依据。
1.在选材方面的应用
31
铁碳相图揭示了合金的性能与成分之间的关系,为合理 选择材料提供了依据。 2.在制定热加工工艺方面的应用
AC线和DC线为液相线,铁碳合金在液相线温度以上处于 液态,用符号L表示。
11
表5- 1 Fe-Fe3C相图中的特性点
12
表5-2 Fe-Fe3C相图中的特性线
13
3.相图中各相区分析 Fe-Fe3C相图中各相区的相组分见表5-3。
14
表5-4 铁碳合金的分类
二、铁碳合金的分类 在Fe-Fe3C相图中,按碳的质量分数和室温平衡组织
碳溶于α-Fe中所形成的间隙固溶体称为铁素体,用符号 F表示。
5
6
图5-5 渗碳体的晶体结构示意图
7
二、奥氏体
碳溶于γ-Fe中所形成的间隙固溶体称为奥氏 体,用符号A表示。 三、渗碳体
渗碳体的分子式为Fe3C,它是一种具有复杂 晶体结构的金属化合物,其晶体结构如图5-5所示。
8
第二节 铁 碳 相 图 Fe-Fe3C相图是指在极其缓慢的冷却条件下,
44
5.叙述铁碳合金的平衡组织、性能随碳的质量分数变化的规
律。
6.为什么铸铁适于铸造成形,而钢适于压力加工成形?
45
42
8.铁碳相图有哪几个方面的应用?
练习题 1.现有三种铁碳合金,一种合金的显微组织中珠光体量占80 %,铁素体量占20%;第二种合金的显微组织中全部为珠光体; 第三种合金的显微组织中珠光体量占95%,二次渗碳体量占5 %。问这三种合金各属于哪一类合金?其碳的质量分数各是 多少?
铁碳合金及相图课件
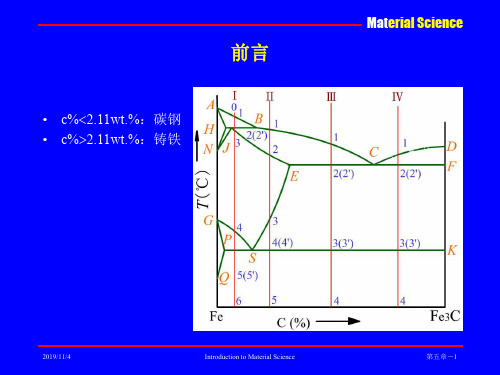
• c%2.11wt.%:碳钢 • c%2.11wt.%:铸铁
Material Science
2019/11/4
Introduction to Material Science
第五章-1
第一节 Fe-Fe3C相图
基本内容:
• Fe-C合金的基本相及组织 Lessons • Fe-Fe3C相图
② -Fe在770℃恒温下发生磁性转变(A2转变); 2. C在Fe中的间隙固溶体
① 铁素体(ferrite)
C在-Fe中的固溶体,bcc晶格,含C量低,C%max=0.0218wt.% (727℃),常用或F表示;
② 奥氏体(austenite)
C在-Fe中的固溶体,fcc晶格,C%max=2.11wt.%(1148℃), 常用或A表示
Material Science
3. 其它线
①A2线(770℃) 的 磁 性 转 变 线 , 770℃ 时 为 铁磁性
②A0线(230℃)
Fe3C 的 磁 性 转 变 线 , 230℃ 时 Fe3C为铁磁性
2019/11/4
Introduction to Material Science
单质的C(100%C),多出现在铸铁组织中,强度、硬度、塑性都 很低 。
2019/11/4
Introduction to Material Science
第五章-4
Material Science
2. Fe-Fe3C相图
本节的主要内容是阐述相图中的几条重要线。
Lessons
1. 三条水平线 ①包晶转变 1495℃,HJB:L0.53+δ 0.090.17 ; ②共晶转变 即 L Ld 1148℃,ECF:L0.43 (2.11 + Fe3C6.69) ③共析转变 即 P, 727℃,PSK(A1线): 0.77 (0.0218 + Fe3C6.69)
第五章相图(冶金物理化学)PPT课件

图中无水平线
Au
l s+l s
960.5℃ Ag
重庆科技学院
冶金与材料工程学院
第五章 相图
(3) 完全互溶型
T
T
l
Nl
s
M
s
A
B
A
B
最低熔点(M),最高熔点(N)——少见。
如 KCl-NaCl系,Ag2S-Cu2S系
重庆科技学院
冶金与材料工程学院
第五章 相图
(4) 固态部分互溶的二元系
① 生成部分互溶的共晶类型
Tf,*A E1 :A物液相线;
T
* f, B
E
2
:B物液相线;
T* f, A
T* f, C
Ⅱ
H
E1
KE1和KE2:C物液相线; 线
HE1D :A、C共晶线; GE2F :B、C共晶线;
Ⅵ A
Ⅰ K
Ⅲ D
Ⅳ
G
E2
C
T* f, B
Ⅴ F
Ⅶ B
重庆科技学院
冶金与材料工程学院
第五章 相图
①稳定化合物二元系
冶金与材料工程学院
第五章 相图
5.3.4 常见的几种二元系相图
◆具有简单共晶体(前已讲) ◆生成化合物 ◆完全互熔的固熔体型 ◆固态部分互溶的固熔体型 ◆液态部分互溶型
重庆科技学院
冶金与材料工程学院
第五章 相图
(1)具有简单共晶体的二元系相图 基本要求:
体系最低熔点(共晶点 f=0);T
共晶线,共晶反应
GEH —— 共晶线:
l(E)
冷 热
(G )
(H)
T* f, A
E
——
大学物理化学经典课件5-6-相图

上一内容 下一内容 回主目录
返回
2013-12-12
形成稳定水合物的相图举例
Question: 与冰共 存的硫酸水合物最 多几种,与硫酸水 溶液共存的水合物 最多有几种?
上一内容
下一内容
回主目录
返回
2013-12-12
理想的完全互溶双液系
(1) p-x图(恒温相图)
* A
pA p xA
* pB pB (1 x A )
p pA pB
* * * pB ( pA p B ) xA
上一内容
下一内容
回主目录
返回
2013-12-12
上一内容 下一内容 回主目录
返回
2013-12-12
形成不稳定化合物的相图举例
上一内容
下一内容
回主目录
返回
2013-12-12
形成不稳定化合物的相图举例
相区分析与简单二元相图 类似,在OIDN范围内是C(s)与 熔液(L)两相共存。 分别从a,b,d三个物系点 冷却熔液,与线相交就有相变, 依次变化次序为: a线: L A(s) L A(s) C(s) L(N) A(s) C(s) b线: L A(s) L A(s) C(s) L(N) C(s) d线: L A(s) L A(s) C(s) L(N) C(s) L
5.3.5.1 稳定化合物(同份熔融化合物、相合熔
点化合物)
稳定化合物,包括稳定的水合物,它们有自己 的熔点,在熔点时液相和固相的组成相同。属于 这类体系的有: CuCl(s) - FeCl3 (s)
第五章:铁碳合金相图PPT课件

0.77-0.02
0.45-0.02
0.02
0.77
0.45
6.69
P=
100% = 57% P = 1 – WF = 57%
0.77-0.02
相组成物: F ; Fe3C
6.69-0.45
F=
100% = 94% Fe3C = 1 - WF = 6%
6.69-0.02
第四节 碳的质量分数对铁碳 合金组织、性能的影响
-
1
第一节 Fe - C相图的基础知识
1.铁与碳可以形成 Fe3C、Fe2C、FeC 等一系列化合物。
2.稳定的化合物可以作为一个独的组 元。
3.Fe – C 二元相图。
-
2
Fe – C 二元相图
温 度
Fe Fe3C Fe2C FeC (6.69%C)
-
C
3
Mg – Si 合金相图
第二节 形成Fe - Fe3C 相图组元 和基本组织的结构与性能
一.组元 * 铁 ( ferrite ) * 渗碳体 ( Cementite )
-
5
二.基本组织
1.铁素体 ( F )
( Ferrite ) 碳溶于
α–Fe中形成 的间隙固溶 体。
-
6
铁素体组织金相图
-
7
2.奥氏体 ( A ) --- Austenite
碳溶于 γ-Fe中形成 的间隙固溶 体。
-
64
3.碳素工具钢
T 12 A
高级优质
Wc = 12%0
碳素工具钢
-
65
4.铸造碳钢
ZG 200 - 400 σb ≥ 400MPa σs≥ 200MPa
材料科学基础课件-第五章相平衡与相图第五节第六节

可用杠杆定 律
共轭连线:两平衡相成分点连接线。
三元系相图
等温截面是由实验测定,合金成分确定,共轭 连接线是唯一的,所以两个相的相对含量也是确定 的。任意两条连接线不相交,也不平行于成分三角 形的边。连接线的方向受组元熔点制约和影响,固 相中熔点高的组元含量一般比液相高。连接线偏向 熔点低的组元(如A)。同一成分合金,在不同温 度下的连接线都通过合金成分点O,随T降低,连接 线逐渐向低熔点组元方向偏转,固相成分点接近合 金成分点,液相成分点远离合金成分点。
相图的热力学解释
处于平衡状态: 另:
相图的热力学解释
平衡时: 则: (1) γ-Fe 与α-Fe:
说明压力增加将降低α与γ的平衡温度。
(2)L与δ-Fe: VVm LVm 0
相图的热力学解释
HHLH0,则 dP 0
提高L与δ相的平衡温度。dT 平衡
,压力增加将
据此 ,增加压力可以扩大摩尔体积小的相在相
液相面
三元系相图
固相面:二相平衡转变终了曲面
二元共晶转变终了曲面
固相面
三元系相图
三元共晶面abc
70
三元系相图
二元共晶区: 由三相构成的三棱柱体 如由L、α、β构成的三棱柱 底面:三元共晶面aEb 侧面:两个二元共晶转变开始
面和一个终了面。 上底:封闭成一条二元共晶线a1e1b1 三条棱:a1a、e1E、b1b分别是α、L、β的成分变
三元系相图
④3个三相平衡区的9条 单变量线:e1E、e2E、 e3E(液相单变量线, 汇于E点),a1a、b1b、 b2b、c2c、c1c、a2a (二元共晶转变) ⑤4个三相平衡区 合金O的结晶过程,室温组织组成物:
α +( α +β)+ ( α +β +γ)+ α Ⅱ + β Ⅱ + γ Ⅱ
【冶金精品文档】相平衡.pptx

上一内容 下一内容 回主目录
2020/10/11
5.3 相律
相律(phase rule)
f F C 2
相律是相平衡体系中揭示相数 ,独立组分数C和
自由度 f 之间关系的规律,可用上式表示。式中2
通常指T,p两个变量。相律最早由Gibbs提出,所以 又称为Gibbs相律。如果除T,p外,还受其它力场影
5.1 引言
相平衡是热力学在化学领域中的重要应用之一。 研究多相体系的平衡在化学、化工的科研和生产中 有重要的意义,例如:溶解、蒸馏、重结晶、萃取、 提纯及金相分析等方面都要用到相平衡的知识。
相图(phase diagram) 表达多相体系的状态如何 随温度、压力、组成等强度性质变化而变化的图形, 称为相图。
O点 是三相点(triple point),气-液-固三相 共存,F 3, f 0 。三 相点的温度和压力皆由
体系自定。
H2O的三相点温度为273.16 K,压力为610.62 Pa。
上一内容 下一内容 回主目录
2020/10/11
水的相图
两相平衡线上的相变过程 在两相平衡线上的任何
一点都可能有三种情况。如 OA线上的P点:
上一内容 下一内容 回主目录
2020/10/11
5.1 引言
自由度(degrees of freedom) 确定平衡体系的状 态所必须的独立强度变量的数目称为自由度,用字 母 f 表示。这些强度变量通常是压力、温度和浓度 等。
如果已指定某个强度变量,除该变量以外的其它强
度变量数称为条件自由度,用 f *表示。
OB 是气-固两相平衡线,即 冰的升华曲线,理论上可延长 至0 K附近。
OC 是液-固两相平衡线,当C点延长至压力大于 2108 Pa 时,相图变得复杂,有不同结构的冰生成。
冶金物理化学--相图

基本概念回顾v自由度:体系的总变量数减去独立方程数的式,为 独立变量数,也即体系的自由度。
----计算方法冶金物理化学—相图体系总变量数为:(m-1)r+2(考虑温度和压力条件下)其中:假设体系有m个组元,存在r个相,则其中m-1个组元应为独立组 元。
则变量数为:(m-1)r独立方程数:(r-1)m 故自由度: f=m+2-r相律:若C表示组元的数量,P表示相的数量,则 相律常写为f=C-P+2。
冶金物理化学(相图)基本概念回顾 几个定义:v组元:组成系统的独立化学组成物。
合金中元素 视为组元,陶瓷中某一化合物视为组元。
v相:在一个多相体系中由界面分开的物质的均匀 部分,它们具有相同的物理、化学性质和晶体结 构。
v自由度:平衡状态下,在不改变相的类型和数目 时,可以独立变化的状态函数的数量。
冶金物理化学(相图)二元相图的类型v十二个基本类型1、具有最低共溶点或称简单共晶; 2、具有稳定化合物或称同分熔点化合物; 3、具有异分熔点化合物; 4、具有固相分解的化合物; 5、固相晶型转变; 6、液相分层; 7、形成连续固溶体; 8、具有最低点或最高点的连续固溶体; 9、具有低共熔点并形成不连续固溶体; 10、具有转熔反应并形成有限固溶体; 11、具有共析反应; 12、具有包析反应。
冶金物理化学(相图)二元相图的几何元素---面、线v 二元相图由曲线、水平线、垂直线和斜线组成,这些 线把整个图面分成若干区域 区域,形成若干交点 交点。
从而形成相 图中的基本几何元素点、线、面。
v二元相图的几何元素---线二元相图的垂直线:是两组分形成化合物的组成线,可以是 稳定化合物也可以是不稳定化合物。
在化合物的熔点温度,液相和固相有相同的组成,此种化合物 即为稳定化合物,又称同分熔点化合物 同分熔点化合物;若化合物没有固定熔点 仅有分解温度,作为分解产物的固相和液相组成都与原固相化合 物不同,此化合物即为不稳定化合物,也称为异分熔点化合物 异分熔点化合物。
金属材料及热处理(第5版)课件第5章 铁碳合金相图和碳钢

第1节 纯铁、铁碳合金的相结构及其性能
一、纯铁的同素异构转变 二、Fe-Fe3C合金的相结构及其性能
1.纯铁的的同素异构转变
•纯铁的冷却曲线上有三种同素异构体,如图5-1 所示。液态纯铁(L)在1538℃时开始结晶出具 有体心立方晶格的δ-Fe;继续缓冷到1394℃时δFe开始转变为具有面心立方晶格的γ-Fe;再冷却 到912℃时又由γ-Fe转变为α-Fe
• 抗拉强度σb =180~280MPa • 屈服点σs=100~170MPa
• 伸长率δ×100 30~50%
• 断面收缩率ψ×100
70~80%
• 冲击韧度ak = 160~200J/cm2
• 硬度
~80HBW
铁素体在770℃以下具有磁性,在
770℃以上则失去铁磁性。
2.奥氏 ( A )
碳溶于γ-Fe中形成的间隙固溶体。
•共晶白口铸铁的室温组织是渗碳体和珠 光体组成的机械混合物 (P+Fe3CⅡ+Fe3C),称为低温莱氏体, 用符号L´d表示。
•(二)亚共晶白口铸铁的组织转变
•参考图5-12,亚共晶白口铸铁(WC> 2.11~<4.3%),液态合金缓冷至1处的亚 共晶白口铸铁组织为(A+Ld)。
•在点1~点2之间缓冷时,奥氏体含碳量沿 ES线而减少,因此,从奥氏体(包括Ld中 的A)中不断以Fe3CⅡ形式析出碳,这个 温度区域的组织是(A+ Fe3CⅡ+Ld)。 •再冷却到点2处,奥氏体含碳量降到共析 点S(WC=0.77%)发生共析转变,所有的 奥氏体都转变为珠光体(P);再冷却到 点2以下直到室温,亚共晶组织不再转变。
PSK(A1)。 • 两个重要转变: • 共晶转变反应式 • 共析转变反应式 • 二个重要温度:共晶转变温度 1148 ℃ 、共析
《相图及其类型》课件

目 录
• 相图概述 • 单组分系统相图 • 二组分系统相图 • 三组分系统相图 • 相图的实验测定方法
相图条件下,描述物质中不同相之间关系的图解。它通过图形和数据 展示物质在不同温度、压力等条件下的相态变化,是研究物质相变规律的重要工 具。
三组分系统相图的分类
简单相图
三个组分之间只发生两两相互作用, 形成两个或三个单相区和一个或两个 双相区。
复杂相图
三个组分之间发生三组分相互作用, 形成多个单相区和多相区,具有更复 杂的相平衡关系。
三组分系统相图的实例分析
实例一
水-盐-烃三组分系统相图在石油工业中的 应用,用于研究油藏中水、盐、烃的相 平衡关系,指导石油开采和分离过程。
VS
实例二
硫酸-水-原料油三组分系统相图在化学工 业中的应用,用于研究硫酸、水和原料油 之间的反应和分离过程,提高生产效率和 产品质量。
相图的实验测定方
05
法
热分析法
差热分析法(DSC)
通过测量物质在加热或冷却过程中温度的变 化,确定物质的状态变化和相变。
热重分析法(TGA)
通过测量物质在加热过程中质量的变化,研 究物质在加热过程中的分解、氧化等反应。
要点一
总结词
描述合金的相图特点
要点二
详细描述
合金的相图是单组分系统相图中的另一种类型,它展示了 合金在不同成分和温度下的相变情况。在相图中,我们可 以看到合金的固溶线、共晶点和包晶点等关键点的位置, 以及在这些点之间发生的相变过程。这些相变过程对于合 金的制备、加工和使用具有重要意义,因为它们决定了合 金在不同条件下的力学、物理和化学性质。
二组分系统相图
03
液态完全互溶的二组分系统相图
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
τ→
A
xB→
B
纯物质:均匀降温→液态凝固(T不变) →均匀降温
合金:均匀降温→有固体析出(降温变缓)→两种固体
同时析出(T不变) →均匀降温
重庆科技学院
冶金与材料工程学院
第五章 相图
具有简单共晶体的二元系相图
T
T* f, A
T* f, B
重庆科技学院
G
E
H
A
B
xB→
冶金与材料工程学院
第五章 相图
TM →T1 M →a1 M→ a1 b1
T1 →T2 a1 →m a1 →a2 b1→ b2
T* f, B
T2 →TE m →n a2 →E b2→ H T < TE n → —— H →, G →
b1(T1) b2(T2) H
B
无论从何处开始, 体系点达到共晶线 液相组成达到E点
冶金与材料工程学院
冶金与材料工程学院
第五章 相图
5.3.4 常见的几种二元系相图
◆具有简单共晶体(前已讲) ◆生成化合物 ◆完全互熔的固熔体型 ◆固态部分互溶的固熔体型 ◆液态部分互溶型
重庆科技学院
冶金与材料工程学院
第五章 相图
(1)具有简单共晶体的二元系相图 基本要求:
体系最低熔点(共晶点 f=0);T
共晶线,共晶反应
5.3.2 简单共晶二元系相图分析
(1)点:
纯物质凝固点——
T
* f, A
和
T
* f, B
,f
= 0;
共晶点——E,三相点, T
f E = 2-3+1=0;
T* f, A
T* f, B
共晶反应:
l(E) 冷却 sA(G) + sB(H)
G
加热
E
H
重庆科技学院
A
B
xB→
冶金与材料工程学院
第五章 相图
冶金与材料工程学院
第五章 相图
5.2 相律
相律:研究相态变化的规律。 相数(Φ ),组元数(K),自由度数(f )之间的变化规律。
①相数:体系中所含相的数目,记为Φ。 相数的计算方法:
自然界中物质有三种存在形态(s,l,g) 气态:一般能无限混合 ——单相 液态:完全互溶 —— 单相
不完全互溶 —— 多相 固态:一般不能互溶 —— 多相
第五章 相图
分析相图:点、线、面(区)的意义
三条二元平衡线将平面图分
为三个区,交于一个点O
线:两相平衡 ,两相平衡线
pC
A
面: AOB(g) ,AOC(L) ,BOC(S)
水
(单相平衡)
p2
点O:p = 610Pa
p1 冰 F
O 水蒸气
T = 273.01K 三相平衡
(三相平衡点)
重庆科技学院
B T1 T2 T
第五章 相图
5.3.3 杠杆规则(计算平衡时各相的量)
以物系点M的冷却过程为例
T
M
T* f, A
T* f, B
G
a1 a2 m
n
E
b1(T1) b2(T2) H
A
xB→
B
重庆科技学院
T2 :
Wl(a2) b2m
WB(s,b2 )
a2m
刚到 TE :
Wl(E) Hn W En B(s,H)
刚完成:共W晶 A(G s,) Hn W Gn B(,sH)
(2) 线:
A物液相线——
T E * f, A
液相线上,f = 2-2+1=1;
; B物液相线—— Tf,*B E
共晶线——GEH线,三相线, f = 2-3+1=0;
T
(3)面:
单相区—— 液相线以上
T* f, A
f = 2-1+1=2;
两相区—— 和Tf,*BGEHHBA Tf*,A EG
l + sA
第五章 相图
第五章 相图
5.1 水的相图 5.2 相律 5.3 二元系相图及应用 5.4 三元系相图及应用
重庆科技学院
冶金与材料工程学院
第五章 相图
5.1 水的相图
相图:用几何的方法表示相平衡关系。 T、P、组成和相数相互关系的几何图形。
相:体系中物理、化学性质完全一致的所有部分的总和。
绘制:(1)实验 测 H2O(L)= H2O(g) 平衡的 T ,p H2O(S)= H2O(g)
G
f = 2-2+1=1;
l
E
sA + sB
T* f, B
l + sB
H
总结相区标注的规律,会标注相区 A
(相邻相区相数差1 )
重庆科技学院
B
xB→
冶金与材料工程学院
第五章 相图
(4)冷却过程分析
温度 体系点 液相点 固相点
T
T* f, A
G A
M
a1 a2 m
n E
xB→
重庆科技学院
TM
M
M ——
固溶体 —— 单相
重庆科技学院
冶金与材料工程学院
第五章 相图
②组元和组元数
组元(组分),也称独立组元 描述体系中各相组成所需最少的、能独立存在的物质
组元(分)数: 体系中组元的个数,简称组元,记为K。 无化学反应体系:组元数 = 物种数(S) 有化学反应(R)体系:组元数 ≠ 物种数 如 H2(g), O2(g), H2O(g) ★ 常温、常压下, K = 3 ★ 2000℃、常压下,2H2(g)+ O2(g) == 2H2O(g)
(L=S1+S2);分析物系点
T* f, A
T* f, B
的结晶过程。
应用:造渣材料、耐火材料 G 选择组成配比
独立反应式数R=1 , K = S-R=3-1=2
Kp
p2 H2O
p p 2 H2 O2
重庆科技学院
冶金与材料工程学院
第五章 相图
③自由度或独立变量
自由度:指体系可变因素(T、P 、C…)的数目,这些
因素在一定程度内变动时新相不产生,旧相不消失。
用符号 f 表示。
自由度数=独立变量数
f=K-φ+2 相律的数学式
冶金熔体,凝聚相 ,P影响小
f=K-φ+1
讨论温度——组成图
5.3.1 绘制二元系相图(热分析法)
方法: 称样 →熔化→ 缓慢冷却过程中记录τ、t℃ →作t℃——τ图 (步冷曲线图) → 绘t℃——组成图
重庆科技学院
冶金与材料工程学院
第五章 相图
T 纯A ① ② ③ ④ ⑤ 纯B
二元系相图
步冷曲线各 段 f=?
式中的2——考虑T、P两个与外界有关的因素 若对凝聚相,忽略P的影响:f=K-φ+1(如冶金炉渣) 若考虑外界T、P、磁场的影响:f=K-φ+3
通式可写成: f=K-φ+n
重庆科技学院
冶金与材料工程学院
第五章 相图
5.3 二元系相图
二元相图:f=K-φ+2 fmax=2-1+2=3 φmax= K-f+2=2-0+2=4
H2O(S)= H2O(L) (2)作p—T图
重庆科技学院
冶金与材料工程学院
第五章 相图
水的相图 p-T图 —— 根据实验数据绘制
OA:L—g平衡 OC:L—S平衡 OB:S—g平衡 O:p =610Pa
T = 273.01K
重庆科技学院
pC
p2 p1 冰
F
A 水O 水蒸气来自B T1 T2 T冶金与材料工程学院
