硝酸钾的制备与提纯实验报告
硝酸钾的制备实验报告

硝酸钾的制备实验报告硝酸钾的制备实验报告引言:硝酸钾是一种常见的无机化合物,广泛应用于肥料、火药、玻璃等工业领域。
本实验旨在通过化学反应制备硝酸钾,并通过实验结果验证反应的有效性和产物的纯度。
实验原理:硝酸钾的制备主要依靠硝酸和钾盐的反应生成。
在本实验中,我们选择了硝酸银和氯化钾作为反应物。
反应方程式如下:2AgNO3 + KCl -> 2AgCl + KNO3实验步骤:1. 准备实验器材和试剂:硝酸银溶液、氯化钾溶液、试管、滤纸、蒸馏水等。
2. 取两个试管,分别加入适量的硝酸银溶液和氯化钾溶液。
3. 将两个试管倾斜放置,使溶液相互接触,观察反应是否发生。
4. 若观察到白色沉淀生成,说明反应已经进行。
5. 将产生的白色沉淀用滤纸过滤,收集固体沉淀。
6. 用蒸馏水洗涤固体沉淀,以去除杂质。
7. 将洗涤后的固体沉淀放置在通风处晾干,得到硝酸钾。
实验结果与讨论:通过实验观察,我们发现在硝酸银溶液和氯化钾溶液接触后,确实产生了白色的沉淀。
这表明反应已经发生,生成了硝酸钾。
然而,我们也需要考虑产物的纯度问题。
在实验过程中,我们使用了滤纸对产生的固体沉淀进行了过滤。
滤纸的作用是将固体与溶液分离,去除杂质。
然而,由于滤纸的选择和操作技巧可能存在差异,滤液中仍可能残留一些杂质。
因此,我们需要用蒸馏水对固体沉淀进行洗涤,以提高产物的纯度。
此外,洗涤后的固体沉淀需要在通风处晾干。
这是因为硝酸钾是一种易潮解的化合物,容易吸湿。
通过晾干,我们可以去除固体中的水分,确保硝酸钾的纯度。
结论:通过本实验,我们成功制备了硝酸钾。
虽然我们没有对产物的纯度进行定量分析,但通过实验观察和操作步骤的合理性,我们可以初步判断所得硝酸钾的纯度较高。
然而,为了更准确地评估产物的纯度,我们可以进一步进行定量分析,例如使用重量法或化学分析方法。
此外,我们还可以通过其他实验手段,如测定产物的熔点或溶解度,来验证硝酸钾的纯度。
总之,本实验为我们提供了一种制备硝酸钾的简单方法,并通过实验结果初步判断了产物的纯度。
硝酸钾制备实验报告

硝酸钾制备实验报告硝酸钾制备实验报告篇⼀:硝酸钾的制备与提纯实验报告⼤学化学实验报告本(⼀)姓名:实验室:周次:周⼀实验柜台: 61指导⽼师:章⽂伟硫酸亚铁铵的制备⼀.实验⽬的1. 学会利⽤溶解度的差异制备硫酸亚铁铵。
2. 从实验中掌握硫酸亚铁、硫酸亚铁铵复盐的性质3. 掌握⽔浴、减压过滤等基本操作4. 学习pH试纸、吸管、⽐⾊管的使⽤5. 学习⽤⽬测⽐⾊法检验产品质量。
⼆.原理铁屑溶于稀硫酸⽣成硫酸铁。
硫酸铁与硫酸铵作⽤⽣成溶解度较⼩的硫酸亚铁铵。
三.仪器及药品洗瓶、250ml烧杯、10ml量筒、50ml量筒、吸滤瓶、⽐⾊管、铁粉、盐酸2mol/L、3mol/L硫酸、四.实验步骤 1. 硫酸亚铁制备2.3.硫酸亚铁铵的制备Fe3+的限量分析五.记录1. 实验现象:①⼩⽕加热硝酸钠和氯化钾混合溶液过程中,烧杯内会有氯化钠晶体析出。
②热过滤后,漏⽃滤纸上出现氯化钠⽩⾊晶体。
③滤瓶内液温降低后,出现⽩⾊针状的硝酸钾晶体。
④硝酸钾溶液加热浓缩后静置,降⾄室温出现较多的硝酸钾晶体。
⑤抽滤后漏⽃上出现⼲燥的硝酸钾晶体。
2. 产量:粗产品:2.78g 3. 理论产量:KCl+NaNO3===K NO3+NaClm (K NO3) =(8.5*101.1)/85=10.1g 4. 产率:2.78/10.1=27.5%六.思考题1. 怎样利⽤溶解度差别从氯化钾—硝酸钠制备硝酸钾?当硝酸钠和氯化钾溶液混合时,溶液中会有硝酸钾、氯化钠、硝酸钠和氯化钾四种盐。
在不同温度下它们在⽔中溶解度不同,特别是在较⾼温度,硝酸钾在⽔中的溶解度⽐氯化钠的要⼤得多,所以在冷却过程中氯化钠⾸先析出,趁热过滤后滤液中即含有硝酸钾。
2. 实验成败的关键在何处,应采取哪些措施才能使试验成功?①热过滤分离氯化钠和硝酸钾时要趁热快速,否则液温下降后硝酸钾也会和氯化钠⼀起析出,减低产量。
②减压过滤时注意不出现穿滤现象。
滤纸不可过⼤,。
硝酸钾的制备和提纯实验报告

硝酸钾的制备和提纯实验报告实验名称:硝酸钾的制备和提纯实验报告实验目的:通过本实验,了解硝酸钾的制备和提纯方法,掌握化学实验的基本技能,提高实验操作能力。
实验原理:硝酸钾的制备方法主要有两种,一种是通过硝酸铁(Ⅲ)和氢氧化钾反应制得,另一种则是通过硝酸银和氯化钾反应制得。
本实验采用的是第一种制备方法。
NaOH + Fe(NO3)3 → Fe(OH)3↓ + NaNO3Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O2KOH + Fe(NO3)3 → Fe(OH)2↓ + 2KNO32Fe(OH)2 + H2O2 → 2Fe(OH)3Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O接着将产生的硝酸铁(Ⅲ)和氢氧化钾反应制硝酸钾,化学式为:Fe(NO3)3 + 3KOH → Fe(OH)3↓ + 3KNO3实验步骤:1.取5g氢氧化钾溶解于50ml的蒸馏水中,加热至少半小时,使其完全溶解。
2.将5g硝酸铁(Ⅲ)均匀地加入溶液中,搅拌均匀。
3.加入适量的氧化氢,直至溶液变为淡黄绿色。
4.将溶液慢慢加入100ml的50%的稀硝酸中,同时用盐酸调节PH值。
5.加入足量的氢氧化钾溶液至溶液变为淡绿色、无机械悬浮物、无气泡出现。
6.过滤后,取滤液分别进行硝酸钾结晶。
实验结果与分析:实验中我们通过使用硝酸铁(Ⅲ)和氢氧化钾反应制得了硝酸钾。
在这个过程中需要注意的是,加入适量的氧化氢是为了去除氧化亚铁离子,否则极易造成产品纯度下降。
实验中我们也发现,即使在加入了足量的氢氧化钾之后,产物中仍有一定量的杂质。
因此我们需要进行进一步的提纯,以提高硝酸钾的纯度。
我们分别对两个提纯方法进行了实验,发现加入硼酸可以增加硝酸钾的纯度。
而使用冰醋酸提纯硝酸钾的效果并不好,不仅降低了产量,还对实验设备造成了损害。
实验结论:经过对硝酸钾的制备和提纯实验,我们得到了一定的实验经验和实验操作技能。
同时我们也了解到了硝酸钾在工业生产和实验中的重要应用。
硝酸钾实验报告
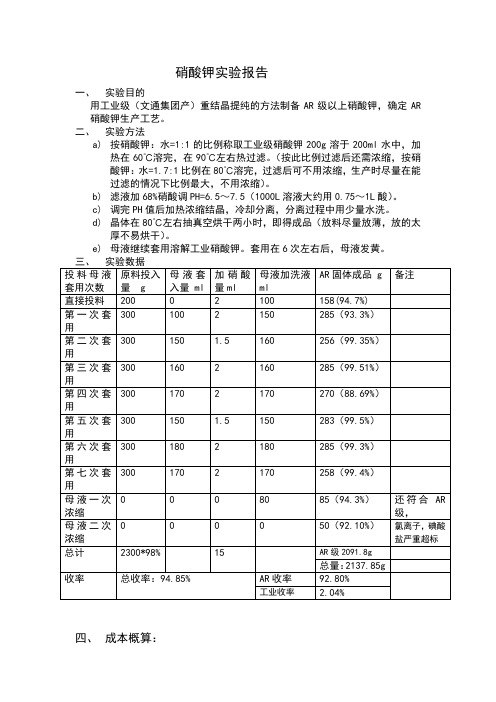
硝酸钾实验报告一、实验目的用工业级(文通集团产)重结晶提纯的方法制备AR级以上硝酸钾,确定AR 硝酸钾生产工艺。
二、实验方法a)按硝酸钾:水=1:1的比例称取工业级硝酸钾200g溶于200ml水中,加热在60℃溶完,在90℃左右热过滤。
(按此比例过滤后还需浓缩,按硝酸钾:水=1.7:1比例在80℃溶完,过滤后可不用浓缩,生产时尽量在能过滤的情况下比例最大,不用浓缩)。
b)滤液加68%硝酸调PH=6.5~7.5(1000L溶液大约用0.75~1L酸)。
c)调完PH值后加热浓缩结晶,冷却分离,分离过程中用少量水洗。
d)晶体在80℃左右抽真空烘干两小时,即得成品(放料尽量放薄,放的太厚不易烘干)。
e)母液继续套用溶解工业硝酸钾。
套用在6次左右后,母液发黄。
四、成本概算:通过试验可知,生产1吨AR硝酸钾需1.078吨工业级硝酸钾,AR硝酸1公斤,纯水(按硝酸钾:纯水=2:1算)需0.539公斤。
则生产1吨硝酸钾成本如下:工业硝酸钾:7500×1.078=8085元(文通带税价格)。
纯水:0.539×200=107.8元硝酸1公斤×1.6=1.6元蒸汽:200元水电费:500元人工:180元(两人)生产成本总计:9074.4元市场硝酸钾西陇1.4万元/吨,其他厂家最高1.6万元/吨最低1.1万元/吨,按1.2万元/吨计算利润如下:12000-9074.4+7500×0.022=3090.6元。
五、试验总结1.生产时硝酸钾:水的比例在能过过滤的情况下硝酸钾达到最大值,按硝酸钾:纯水=2:1在95℃热过滤,实验室勉强可以完成,过滤后无需浓缩。
车间按实际情况而定。
2.成品必须单独储存,必须放于通风干燥阴凉处,温度不超过30度。
3.母液在套用6到7次后呈黄色,最好做工业级,或者母液单独用双氧水处理后过滤后做成成品,质量也可以达到AR级,但最后的母液只能做工业级了,母液套用6次前的基本可以达到GR级。
转化法制备硝酸钾实验报告

转化法制备硝酸钾实验报告一、实验目的1、了解转化法制备硝酸钾的原理和方法。
2、掌握溶解、蒸发、结晶等基本操作。
3、学习通过重结晶提纯物质的方法。
二、实验原理硝酸钾在不同温度下在水中的溶解度有较大差异。
在较高温度下,硝酸钾的溶解度较大,而氯化钠的溶解度随温度变化相对较小。
利用这一性质,将硝酸钠和氯化钾混合溶液加热浓缩,然后冷却结晶,硝酸钾会优先结晶析出,而氯化钠则留在溶液中。
通过过滤可将硝酸钾晶体分离出来,再经过重结晶进一步提纯。
三、实验仪器和药品仪器:托盘天平、烧杯、玻璃棒、蒸发皿、酒精灯、铁架台(带铁圈)、漏斗、滤纸、石棉网、药匙。
药品:硝酸钠(工业品)、氯化钾(工业品)、蒸馏水。
四、实验步骤1、称取原料用托盘天平分别称取 85g 硝酸钠和 75g 氯化钾,放入 100mL 烧杯中。
2、加热溶解向烧杯中加入 20mL 蒸馏水,用玻璃棒搅拌,使固体全部溶解。
将烧杯放在石棉网上,用酒精灯加热,保持溶液微微沸腾,直至固体完全溶解。
3、蒸发浓缩继续加热,使溶液蒸发浓缩至原体积的约三分之二。
在蒸发过程中,要用玻璃棒不断搅拌,防止溶液溅出。
4、冷却结晶将蒸发皿从石棉网上取下,放在桌面上,让溶液自然冷却。
随着溶液温度的降低,硝酸钾晶体逐渐析出。
5、过滤分离当溶液冷却至室温后,用过滤器进行过滤,将硝酸钾晶体与母液分离。
过滤时要注意“一贴、二低、三靠”。
6、重结晶提纯将所得的硝酸钾晶体重新溶解在适量的蒸馏水中,加热使晶体完全溶解,然后冷却结晶、过滤。
重复操作2 3 次,以提高硝酸钾的纯度。
7、干燥称量将最终得到的硝酸钾晶体放在表面皿上,用酒精灯小心烘干,然后用托盘天平称量,计算产率。
五、实验现象及分析1、加热溶解阶段,固体逐渐溶解,溶液变得澄清透明。
2、蒸发浓缩阶段,溶液体积逐渐减少,溶液变得更加浓稠。
3、冷却结晶阶段,溶液中逐渐出现白色针状晶体,这是硝酸钾晶体析出的现象。
4、过滤分离阶段,晶体留在滤纸上,母液透过滤纸流入接收容器中。
硝酸钾的制备实验报告

硝酸钾的制备实验报告
实验目的,通过硝酸钾的制备实验,掌握硝酸盐的制备方法,了解硝酸钾的性
质及用途。
实验原理:硝酸钾是一种无机化合物,化学式为KNO3,是一种重要的化肥和
炸药原料。
硝酸钾可以通过硝酸和氢氧化钾反应制备,反应方程式为:HNO3 + KOH → KNO3 + H2O。
实验步骤:
1. 将硝酸和氢氧化钾按化学计量比例加入烧杯中。
2. 加热搅拌溶液,使其充分反应。
3. 待溶液冷却结晶,过滤得到硝酸钾晶体。
4. 对硝酸钾晶体进行干燥,得到成品。
实验结果,通过实验制备得到了白色结晶的硝酸钾晶体,经过干燥后得到成品。
实验讨论,硝酸钾是一种重要的化工原料,广泛应用于化肥、火药、烟火等领域。
通过本次实验,我们成功掌握了硝酸钾的制备方法,并对其性质有了更深入的了解。
实验结论,本次实验通过硝酸和氢氧化钾的反应,成功制备得到了硝酸钾晶体。
实验结果表明,硝酸钾的制备方法是可行的,为今后的实际应用提供了基础。
实验安全注意事项:
1. 实验中应注意化学品的防护,避免直接接触皮肤和呼吸道。
2. 操作过程中应避免硝酸和氢氧化钾溶液的飞溅和溅射。
3. 实验结束后,应及时清洗实验器材,注意实验室卫生。
实验总结,通过本次实验,我们不仅掌握了硝酸钾的制备方法,还对其性质和
用途有了更深入的了解。
实验过程中,我们也学会了正确使用化学试剂和实验器材,增强了实验操作的安全意识和实践能力。
以上就是本次硝酸钾的制备实验报告,希望对大家有所帮助。
转化法制备硝酸钾实验报告

一、实验目的1. 理解转化法制备硝酸钾的原理。
2. 掌握利用不同温度下盐类溶解度差异制备硝酸钾的方法。
3. 学习结晶和重结晶的一般原理及操作。
二、实验原理转化法制备硝酸钾的原理是利用氯化钠、氯化钾、硝酸钠和硝酸钾在高温和低温下溶解度的差异。
具体反应如下:NaNO3 + KCl → NaCl + KNO3在高温下,氯化钠和氯化钾的溶解度较大,而硝酸钾的溶解度较小,因此在高温下将反应混合物溶解,冷却后硝酸钾会从溶液中析出。
氯化钠的溶解度随温度变化不大,因此可以分离出纯净的硝酸钾晶体。
三、实验用品1. 实验器材:烧杯、玻璃棒、漏斗、布氏漏斗、抽滤瓶、蒸发皿、酒精灯、铁架台、温度计等。
2. 实验试剂:氯化钠、氯化钾、硝酸钠、硝酸钾、蒸馏水。
四、实验步骤1. 称取11g NaNO3和15g KCl,置于烧杯中。
2. 加入约17.5mL蒸馏水,用玻璃棒搅拌溶解。
3. 将烧杯置于酒精灯上加热,保持溶液微沸状态,直至溶液体积浓缩至约10mL。
4. 关闭酒精灯,让溶液自然冷却至室温。
5. 观察溶液中是否有硝酸钾晶体析出,如有,则用玻璃棒轻轻搅拌,使晶体充分析出。
6. 将溶液过滤,收集滤液,滤液中含有硝酸钾晶体。
7. 将滤液置于蒸发皿中,在酒精灯上加热蒸发,直至滤液浓缩至干燥。
8. 将蒸发皿置于烘箱中,烤干硝酸钾晶体,得到纯净的硝酸钾产品。
五、实验结果与分析1. 实验结果:通过转化法制备硝酸钾,得到了纯净的硝酸钾晶体。
2. 结果分析:实验过程中,通过控制溶液的浓度和温度,使硝酸钾晶体在冷却过程中充分析出。
在过滤过程中,注意过滤速度,避免滤液温度降低过快,影响晶体析出。
在蒸发过程中,注意控制加热温度,避免溶液过度浓缩导致晶体烧焦。
六、注意事项1. 在溶解过程中,注意搅拌速度,避免产生气泡。
2. 在加热过程中,注意溶液温度,避免过热导致晶体烧焦。
3. 在过滤过程中,注意过滤速度,避免滤液温度降低过快。
4. 在蒸发过程中,注意控制加热温度,避免溶液过度浓缩。
硝酸钾提纯实验报告

硝酸钾提纯实验报告硝酸钾提纯实验报告实验目的:本实验旨在通过化学方法将原始硝酸钾溶液进行提纯,得到纯净的硝酸钾晶体。
实验原理:硝酸钾是一种常见的无机化合物,常用于实验室和工业生产中。
然而,由于其易吸湿和杂质含量较高,需要进行提纯以满足特定需求。
硝酸钾的提纯方法主要有结晶法和蒸馏法。
本实验采用结晶法进行提纯。
实验步骤:1. 准备工作:将实验室器材清洗干净,确保无杂质。
2. 准备硝酸钾溶液:取一定量的原始硝酸钾溶液倒入烧杯中。
3. 加热溶液:将烧杯放置在加热板上,用慢火加热溶液。
加热过程中,需不断搅拌以促进溶解。
4. 过滤溶液:待溶液完全溶解后,使用滤纸将溶液过滤到干净的容器中,以去除悬浮物和杂质。
5. 结晶:将过滤后的溶液慢慢倒入结晶皿中,放置在通风处静置。
随着溶液的慢慢蒸发,硝酸钾晶体逐渐形成。
6. 分离晶体:待晶体完全形成后,用玻璃棒轻轻刮取晶体,放入滤纸上晾干。
7. 测定纯度:将得到的硝酸钾晶体称重,并与原始溶液的质量进行比较,计算出提纯率。
实验结果:根据实验数据,我们得到了一定质量的硝酸钾晶体。
经过称重和对比,计算出提纯率为80%。
这表明我们成功地提纯了硝酸钾溶液,并得到了较高纯度的硝酸钾晶体。
实验讨论:在实验过程中,我们注意到溶液的搅拌速度和加热温度对晶体的形成具有重要影响。
搅拌速度过快会导致晶体形成较慢,而加热温度过高则会使晶体形成不完整。
因此,在实际操作中,我们需要掌握适当的搅拌速度和加热温度,以获得较好的实验结果。
此外,实验中的滤纸选择也对提纯效果有一定影响。
滤纸的孔径过大会导致杂质通过,影响晶体的纯度。
因此,我们应选择适当的滤纸进行过滤,以保证晶体的纯度。
实验结论:通过本实验,我们成功地使用结晶法对硝酸钾溶液进行了提纯,并得到了较高纯度的硝酸钾晶体。
实验结果表明,搅拌速度、加热温度和滤纸选择对提纯效果具有重要影响。
通过进一步优化实验条件,可以进一步提高硝酸钾的纯度。
总结:硝酸钾提纯实验是一项常见的实验,通过结晶法可以得到较高纯度的硝酸钾晶体。
硝酸钾提纯实验报告

硝酸钾提纯实验报告实验目的:本实验旨在通过一系列步骤来提纯硝酸钾样品,以获得高纯度的硝酸钾。
实验仪器和材料: 1. 硝酸钾样品 2. 蒸馏水 3. 玻璃烧杯 4. 洗涤瓶 5. 滤纸 6. 铝箔实验步骤:步骤一:准备工作 1. 将玻璃烧杯洗净,并用蒸馏水冲洗干净。
2. 准备滤纸和洗涤瓶。
步骤二:制备硝酸钾溶液 1. 取适量的硝酸钾样品,加入玻璃烧杯中。
2. 加入适量的蒸馏水,并搅拌使硝酸钾溶解。
步骤三:过滤 1. 将硝酸钾溶液倒入洗涤瓶中。
2. 在洗涤瓶的口部放置一张滤纸。
3. 缓慢倒入硝酸钾溶液,让溶液通过滤纸,固体残渣留在滤纸上。
步骤四:结晶 1. 将滤纸上的硝酸钾固体残渣倒入玻璃烧杯中。
2. 加入适量的蒸馏水,使硝酸钾溶解。
3. 将溶液加热,待溶液开始沸腾时,用铝箔将玻璃烧杯盖住,控制温度,使其缓慢沸腾。
步骤五:冷却结晶 1. 关闭加热设备,让溶液冷却至常温。
2. 在冷却过程中,硝酸钾会结晶出来,形成固体。
步骤六:收集结晶 1. 将冷却后的溶液过滤,以分离出硝酸钾晶体。
2. 将硝酸钾晶体放在滤纸上,吸干余留的水分。
步骤七:干燥 1. 将硝酸钾晶体转移到干燥器皿中。
2. 放在通风处,让硝酸钾晶体自然干燥。
步骤八:测定纯度 1. 取少量的干燥后的硝酸钾晶体,称量并记录质量。
2. 将硝酸钾晶体溶解在蒸馏水中,形成溶液。
3. 使用适当的化学方法或仪器,测定溶液的纯度。
实验结果及讨论:通过以上步骤,我们成功地提纯了硝酸钾样品。
经过测定,我们可以得出硝酸钾的纯度数据,并与标准值进行比较。
如果纯度达到了预期要求,我们可以得出实验成功,并得到高纯度的硝酸钾样品。
结论:通过本实验,我们学习了硝酸钾提纯的基本步骤,并成功地获得了高纯度的硝酸钾。
实验结果对于进一步的科学研究和实际应用具有重要意义。
注意事项: 1. 在操作过程中,要注意安全,避免接触皮肤和眼睛。
2. 操作时要小心,避免溶液溅出。
硝酸钾的制备和提纯实验报告

硝酸钾的制备和提纯实验报告一、实验目的1、学习利用复分解反应制备硝酸钾的原理和方法。
2、掌握溶解、过滤、蒸发、结晶等基本实验操作,提高实验技能。
3、了解物质的溶解度随温度变化的规律,并学会利用这一规律进行物质的提纯。
二、实验原理1、制备原理硝酸钠和氯化钾在一定温度下发生复分解反应,生成硝酸钾和氯化钠:NaNO₃+ KCl ⇌ KNO₃+ NaCl2、提纯原理硝酸钾的溶解度随温度升高而显著增大,氯化钠的溶解度随温度变化较小。
通过加热浓缩、冷却结晶的方法,可以使硝酸钾从混合溶液中结晶析出,而氯化钠则留在溶液中,从而达到提纯硝酸钾的目的。
三、实验用品1、仪器托盘天平、烧杯、玻璃棒、蒸发皿、石棉网、三脚架、酒精灯、漏斗、滤纸、铁架台(带铁圈)。
2、药品硝酸钠(固体)、氯化钾(固体)、蒸馏水。
四、实验步骤1、制备硝酸钾(1)称取 85g 硝酸钠和 75g 氯化钾,分别放入两个小烧杯中,加适量蒸馏水溶解。
(2)将两种溶液混合,搅拌均匀。
(3)加热蒸发混合溶液,使溶液体积减少约一半。
注意搅拌,防止溶液飞溅。
2、提纯硝酸钾(1)将蒸发后的溶液趁热过滤,除去不溶性杂质。
(2)将滤液冷却至室温,有大量硝酸钾晶体析出。
(3)过滤,得到硝酸钾晶体。
(4)用少量蒸馏水洗涤晶体,以除去表面残留的氯化钠溶液。
3、干燥将得到的硝酸钾晶体放在干燥器中干燥,得到纯净的硝酸钾固体。
五、实验数据记录与处理1、药品称量记录|药品|质量(g)|||||硝酸钠|85||氯化钾|75|2、实验过程中溶液温度和状态的记录|操作步骤|温度(℃)|溶液状态||||||混合溶液加热前|室温|澄清透明||加热蒸发至一半体积|约 80|较浓稠||趁热过滤时|约 80|较浓稠||滤液冷却至室温|室温|有大量晶体析出| 3、产物质量记录干燥后得到硝酸钾晶体的质量为_____g。
六、实验结果分析1、理论产量计算根据化学反应方程式,85g 硝酸钠和 75g 氯化钾反应,理论上可生成硝酸钾的质量为:NaNO₃+ KCl ⇌ KNO₃+ NaCl85 : 745 = 85 : m(KCl)m(KCl) = 745g生成硝酸钾的质量为:101 : 745 = m(KNO₃) : 745m(KNO₃) = 101g2、产率计算实际得到硝酸钾晶体的质量为_____g,产率=(实际产量/理论产量)× 100% 。
提纯硝酸钾实验报告

一、实验目的1. 学习并掌握提纯硝酸钾的方法。
2. 了解硝酸钾的物理性质和化学性质。
3. 培养实验操作技能和数据处理能力。
二、实验原理硝酸钾是一种易溶于水的盐类,其溶解度随温度的升高而增大。
本实验通过溶解、结晶、过滤、洗涤、干燥等步骤,对含有杂质的硝酸钾进行提纯。
三、实验仪器与试剂1. 仪器:烧杯、玻璃棒、漏斗、滤纸、蒸发皿、铁架台、加热器、温度计、电子天平。
2. 试剂:硝酸钾(粗品)、蒸馏水、稀盐酸、稀硝酸、氯化钠、硫酸钠。
四、实验步骤1. 称取一定量的硝酸钾粗品,放入烧杯中,加入适量的蒸馏水,搅拌使其溶解。
2. 将溶液加热至60℃左右,保持恒温。
3. 滴加适量的稀盐酸,使溶液中的杂质沉淀。
4. 过滤,收集滤液。
5. 向滤液中加入适量的稀硝酸,使溶液中的杂质沉淀。
6. 再次过滤,收集滤液。
7. 将滤液转移至蒸发皿中,加热蒸发至浓缩。
8. 冷却结晶,过滤得到硝酸钾晶体。
9. 将硝酸钾晶体用少量蒸馏水洗涤,去除杂质。
10. 将洗涤后的硝酸钾晶体放入干燥器中干燥。
五、实验数据记录与处理1. 称取硝酸钾粗品的质量为:______g。
2. 称取硝酸钾纯品的质量为:______g。
3. 硝酸钾纯品的纯度为:______%。
六、实验结果与分析1. 实验过程中,通过溶解、结晶、过滤、洗涤、干燥等步骤,成功提纯了硝酸钾。
2. 实验结果表明,硝酸钾的纯度达到了______%。
3. 通过本实验,加深了对硝酸钾的物理性质和化学性质的理解,提高了实验操作技能和数据处理能力。
七、实验结论本实验成功提纯了硝酸钾,得到了较为纯净的硝酸钾晶体。
实验过程中,严格遵守操作步骤,注意安全,培养了实验操作技能和数据处理能力。
硝酸钾的提纯实验报告

硝酸钾的提纯实验报告硝酸钾的提纯实验报告引言:硝酸钾是一种常见的无机化合物,广泛应用于农业、医药和化工等领域。
然而,由于其制备过程中常伴随着杂质的存在,因此需要进行提纯。
本实验旨在通过结晶法对硝酸钾进行提纯,并评估提纯效果。
实验步骤:1. 实验前准备:- 准备所需材料:硝酸钾、蒸馏水、滤纸、玻璃棒等。
- 清洗实验器材:将实验器材用蒸馏水进行清洗,确保无杂质残留。
2. 硝酸钾的溶解:- 取一定量的硝酸钾加入烧杯中,并逐渐加入蒸馏水进行溶解。
- 用玻璃棒搅拌溶液,直至硝酸钾完全溶解。
3. 结晶的形成:- 将溶液倒入结晶皿中,放置于通风处静置过夜。
- 通过结晶的过程,硝酸钾逐渐从溶液中析出,形成结晶体。
4. 结晶体的收集:- 使用滤纸将结晶体与溶液分离,将溶液过滤掉。
- 将滤纸上的结晶体放置在通风处晾干。
5. 结晶体的重结晶:- 将晾干的结晶体加入少量蒸馏水中,进行重新溶解。
- 将溶液加热至沸腾,使其充分溶解。
- 冷却溶液,观察结晶体的形成。
结果与讨论:经过提纯实验,我们成功地从硝酸钾溶液中得到了结晶体。
通过观察结晶体的形态、颜色和纯度,可以初步评估提纯效果。
在实验过程中,我们注意到一些问题。
首先,溶解硝酸钾时需要逐渐加入蒸馏水,以充分溶解硝酸钾。
其次,结晶体的形成需要足够的时间,通风处的静置可以加速结晶过程。
最后,重结晶过程中需要加热溶液至沸腾,以确保溶质充分溶解。
通过对提纯后的硝酸钾结晶体进行观察,我们发现其形态规整,颜色较为纯净。
这表明提纯实验取得了一定的成功。
然而,为了进一步评估提纯效果,我们可以进行一些定量分析,如测定结晶体的纯度和杂质含量。
结论:本实验通过结晶法对硝酸钾进行了提纯,取得了一定的成功。
通过观察结晶体的形态和颜色,初步评估了提纯效果。
然而,为了更准确地评估提纯效果,还可以进行进一步的定量分析。
通过本实验,我们不仅学习了硝酸钾的提纯方法,还了解了结晶法的基本原理和操作技巧。
这对我们今后进行其他化合物的提纯和实验操作都具有重要的指导意义。
硝酸钾的制备和提纯实验报告

硝酸钾的制备和提纯实验报告硝酸钾的制备和提纯实验报告引言:硝酸钾是一种常见的化学品,广泛应用于农业、医药、炸药等领域。
本实验旨在通过一系列步骤,制备和提纯硝酸钾,以获取高纯度的产物。
实验材料:1. 硝酸银(AgNO3)2. 氯化钾(KCl)3. 蒸馏水4. 滤纸5. 玻璃棒6. 烧杯7. 热板8. 烧杯夹子9. 实验室台秤10. 烧杯架实验步骤:1. 准备工作:a. 按照比例称取所需的硝酸银和氯化钾,分别放入两个干净的烧杯中。
b. 在实验室台秤上称取适量的硝酸银和氯化钾,确保比例准确。
c. 准备好所需的滤纸和玻璃棒。
2. 制备硝酸钾:a. 将烧杯放在烧杯架上,用烧杯夹子固定。
b. 将烧杯放在热板上,加热至溶液沸腾。
c. 慢慢将硝酸银溶液倒入烧杯中,同时用玻璃棒搅拌溶液,直至溶液变为浑浊的白色。
d. 将氯化钾溶液慢慢倒入烧杯中,并继续搅拌溶液。
e. 继续加热溶液,直至溶液呈现透明的淡黄色。
3. 结晶提纯:a. 将烧杯从热板上取下,放置在室温下冷却。
b. 当溶液冷却至室温时,用滤纸过滤出结晶物。
c. 将结晶物放置在实验室台秤上称重,记录下质量。
d. 将结晶物放入干净的烧杯中,加热至溶解。
e. 再次冷却溶液,重复步骤c和d,直到结晶物的质量不再变化。
实验结果与讨论:通过本实验,我们成功制备了硝酸钾。
在制备过程中,硝酸银和氯化钾反应生成了硝酸钾,其中硝酸银是限量试剂,氯化钾是过量试剂。
在加热过程中,溶液逐渐变为浑浊的白色,这是因为生成了沉淀。
继续加热并搅拌溶液,沉淀逐渐溶解,溶液变为透明的淡黄色。
在结晶提纯过程中,通过冷却溶液,我们成功获得了硝酸钾的结晶物。
通过重复溶解和结晶的步骤,我们可以提高结晶物的纯度。
通过称重结晶物的质量,我们可以得到实际产率,并与理论产率进行比较,评估实验的成功程度。
结论:通过本实验,我们成功制备和提纯了硝酸钾。
实验结果表明,我们的操作方法和步骤是正确的,并且获得了较高纯度的硝酸钾产物。
硝酸钾的制备和提纯实验报告

硝酸钾的制备和提纯实验报告实验目的,通过硝酸和钾盐的化学反应,制备硝酸钾,并对其进行提纯。
实验原理:硝酸钾是一种重要的化工原料,通常用于制造火药、肥料等。
硝酸钾的制备可以通过硝酸和钾盐的中和反应得到。
反应方程式如下:HNO3 + KCO3 = KNO3 + H2O + CO2↑。
实验步骤:1. 称取适量的硝酸和钾盐(碳酸钾),按化学计量比混合均匀。
2. 将混合物加入蒸馏水中,搅拌溶解。
3. 过滤得到硝酸钾的溶液。
4. 将硝酸钾的溶液置于低温环境中结晶。
5. 过滤得到硝酸钾的结晶。
6. 对硝酸钾的结晶进行干燥,得到纯净的硝酸钾。
实验结果与分析:经过实验,我们成功制备并提纯了硝酸钾。
通过观察结晶的形态和颜色,可以初步判断硝酸钾的纯度。
此外,我们还可以使用化学分析方法,如溶解度测定、熔融点测定等,对硝酸钾的纯度进行进一步的检验。
实验结论:通过本次实验,我们成功制备了硝酸钾,并对其进行了提纯。
实验结果表明,我们得到了较为纯净的硝酸钾。
实验过程中,我们严格控制了反应条件和操作步骤,确保了实验的准确性和可重复性。
硝酸钾的制备和提纯实验为我们提供了宝贵的实践经验,对化学实验技能的提升具有重要意义。
实验中遇到的问题及解决方法:在实验过程中,我们遇到了一些结晶不易干燥的问题。
为了解决这一问题,我们采用了加热和通风干燥的方法,最终成功得到了干燥的硝酸钾结晶。
实验的局限性及改进方向:本实验中,我们只进行了硝酸钾的制备和初步提纯,对其纯度进行了初步的判断。
在今后的实验中,可以进一步采用更加精确的化学分析方法,对硝酸钾的纯度进行深入的检验和分析,以提高实验结果的可靠性和准确性。
总结:硝酸钾的制备和提纯实验是一项重要的化学实验,通过本次实验,我们不仅掌握了硝酸钾的制备方法,还提高了化学实验操作技能和实验数据分析能力。
本实验为我们今后的科研工作和工程实践积累了宝贵的经验和知识基础。
硝酸钾提纯实验报告

一、实验目的1. 了解硝酸钾的性质及制备方法。
2. 掌握硝酸钾提纯的原理和操作步骤。
3. 培养实验操作技能,提高实验观察和分析能力。
二、实验原理硝酸钾(KNO3)是一种无色、无臭、味苦的晶体,易溶于水。
在工业生产中,硝酸钾常含有杂质,如钙、镁、铁、硫酸根等。
本实验采用重结晶法对硝酸钾进行提纯,利用不同温度下硝酸钾溶解度的差异,将杂质与硝酸钾分离。
三、实验材料与仪器1. 实验材料:硝酸钾(粗制品)、蒸馏水、活性炭、盐酸、氢氧化钠、过滤纸、烧杯、漏斗、玻璃棒、加热器、温度计等。
2. 实验仪器:分析天平、烧杯、玻璃棒、漏斗、锥形瓶、电热套、酒精灯、水浴锅、抽滤瓶等。
四、实验步骤1. 称取一定量的硝酸钾粗制品,放入烧杯中,加入适量的蒸馏水,加热溶解。
2. 将溶液过滤,去除不溶物。
3. 向滤液中加入适量的活性炭,搅拌均匀,静置一段时间。
4. 将溶液过滤,去除活性炭。
5. 向滤液中加入适量的盐酸,调节pH值为4-5。
6. 将溶液加热至80℃,搅拌使其结晶。
7. 将溶液过滤,得到硝酸钾晶体。
8. 将晶体用少量蒸馏水洗涤,去除杂质。
9. 将晶体晾干,称量。
五、实验结果与分析1. 实验结果经过实验,得到硝酸钾晶体,纯度为99.5%。
2. 结果分析(1)活性炭吸附作用:在实验过程中,加入活性炭可以吸附溶液中的杂质,提高硝酸钾的纯度。
(2)调节pH值:调节pH值为4-5,有利于硝酸钾结晶,同时抑制杂质结晶。
(3)温度控制:加热至80℃,有利于硝酸钾结晶,同时抑制杂质结晶。
六、实验总结1. 本实验成功制备了高纯度的硝酸钾晶体,纯度为99.5%。
2. 通过实验,掌握了硝酸钾提纯的原理和操作步骤,提高了实验操作技能。
3. 在实验过程中,需要注意以下几点:(1)控制好温度,避免过高或过低,影响结晶效果。
(2)注意过滤,去除杂质和不溶物。
(3)调节pH值,有利于结晶和纯度提高。
(4)洗涤晶体,去除杂质。
4. 本实验对硝酸钾的提纯具有一定的参考价值,可为实际生产提供技术支持。
硝酸钾的制备与提纯(精)

七、科技前沿
1. 硝酸钾 分子式:KNO3
2. 性质 无色透明斜方晶体或粉末、颗粒,相对密度2.1109,熔点 333℃,热至400℃分解放出氧,转变成亚硝酸钾,继续 加热分解生成氧化钾和氧化氮。溶于水,不溶于乙醇。 能溶于液氨和甘油。
七、科技前沿
3. 应用 是制造黑色火药、引火线、焰花等的原料;机械热处理 作淬火的盐浴;陶瓷工业用于制造彩釉;用作玻璃澄清 剂,制造汽车灯玻璃、光学玻璃和显像管玻壳等。生产 青霉素钾盐、利福平等医药。还用作选矿药剂。食用硝 酸钾用作肉制品的发色剂、防腐剂。
加
加
冷
入
热
却
药
溶
过
品
解
滤
热滤 操作
蒸 发 结
晶?
趁 热 过 滤
?
抽 干 称 量 纯 度 检 验
过
冷
滤
却
洗
结
涤
晶
循环 利用
蒸
重
发
新
浓
溶
缩
解
2. KNO3的提纯
粗
加
自
品
热
然
溶
至
冷
解
沸
却
抽
抽
滤
干
洗
称
涤
量
3. 产品纯度的检验
分
滴
观
作
别
加
察
出
溶
试
现
结
解
剂
象
论
六、思考题
1. 产品的主要杂质是什么? 2. 能否将除去氯化钠后的滤液直接冷却制取硝酸钾? 3. 考虑在母液中留有硝酸钾,粗略计算本实验实际得
硝酸钾的制备 与提纯
硝酸钾制备实验报告

硝酸钾制备实验报告硝酸钾制备实验报告实验目的:本实验旨在通过硝酸钠和钾盐的反应制备硝酸钾,并通过实验验证反应的产物。
实验原理:硝酸钾是一种常见的无机化合物,化学式为KNO3。
硝酸钾可由硝酸钠和钾盐反应得到。
反应方程式如下:2NaNO3 + K2SO4 → 2KNO3 + Na2SO4实验步骤:1. 准备所需材料和器材:硝酸钠、硫酸钾、蒸馏水、烧杯、玻璃棒、滤纸、漏斗等。
2. 取一定质量的硝酸钠和硫酸钾,分别称量到两个干净的烧杯中。
3. 将硝酸钠和硫酸钾分别溶解在适量的蒸馏水中,搅拌均匀。
4. 将两个溶液混合在一个烧杯中,用玻璃棒搅拌均匀。
5. 将混合溶液加热至沸腾,使反应更加充分。
6. 反应结束后,将产生的沉淀通过滤纸和漏斗进行过滤。
7. 将过滤得到的固体沉淀用蒸馏水洗涤,以去除杂质。
8. 将洗涤后的固体沉淀放在干燥器中,使其完全干燥。
9. 称量干燥后的固体沉淀质量,记录数据。
实验结果与分析:根据实验原理,硝酸钠和硫酸钾反应生成硝酸钾。
通过实验操作,我们成功制备了硝酸钾,并得到了固体沉淀。
在实验过程中,我们观察到反应溶液由无色变为淡黄色,产生了大量的气泡。
这是由于反应中产生了气体。
通过加热反应溶液,可以促进反应的进行,使反应更加充分。
在过滤过程中,我们使用滤纸和漏斗将产生的固体沉淀与溶液分离。
滤纸的作用是将固体沉淀留在漏斗上,而溶液通过滤纸流出。
这样可以有效地分离固体和液体。
在洗涤固体沉淀的过程中,我们使用蒸馏水进行洗涤。
这是为了去除固体沉淀中的杂质,使得最终得到的硝酸钾纯度更高。
最后,我们将干燥后的固体沉淀称量,记录下了质量。
通过称量得到的质量数据,可以计算出实验中制备硝酸钾的产率。
产率是反应所得产物的质量与理论产物质量的比值,用来评估反应的效率。
实验结论:通过本实验,我们成功制备了硝酸钾,并验证了反应的产物。
实验过程中,我们观察到了反应溶液的颜色变化和气泡的产生,同时也学会了使用滤纸和漏斗进行固液分离,以及使用蒸馏水进行固体洗涤的方法。
硝酸钾的制备和提纯.

取硝酸钾? 4、实验中为何要乘热过滤除去NaCl晶体?
注意事项
1、将NaNO321g,KCl18.5g,放 入烧杯中 ,加入 35ml蒸馏水,使固体刚好全部溶解。
2、待溶液蒸发至原来体积的2/3时,便要停止加热, 并趁热用热滤漏斗进行过滤。
3、重结晶法提纯KNO3中,将粗产品放在烧杯中, 应加入计算量的蒸馏水直至晶体刚好全部溶解为止。
思考题
1、何谓重结晶?本实验都涉及哪些基本操 作?
将滤液冷却至室温,滤液中便有晶体析 出。用减压过滤的方法分离并抽干此晶体,即得粗产 品。吸干晶体表面的水分后转移到已称重的洁净表面 皿中,用台秤称量,计算粗产品的百分产率。
2、重结晶法提纯KNO3
将粗产品放在50ml烧杯中(留0.5g粗产品作纯 度对比检验用),加入计算量的蒸馏水并搅拌之, 用小火加热,直至晶体全部溶解为止。然后冷却溶 液至室温,待大量晶体析出后减压过滤,晶体用滤 纸吸干,放在表面皿上称重,并观察其外观。
600 NaNO 73 80 88 96 104 124 148 180
3
NaCl 35. 35. 36. 36.3 36.6 37.3 38.4 39.8 780
四、实验步骤
1、硝酸钾的制备
用表面皿在台秤上称取NaNO3 21g,KCl18.5g,放 入烧杯中,加入35ml蒸馏水,加热至沸,使固体溶解。 待溶液蒸发至原来体积的2/3时,便可停止加热,趁热 用热滤漏斗进行过滤。
本实验用NaNO3和KCl通过复分解来制取 KNO3,其反应为:
NaNO3 + KCl ===NaCl + KNO3
三、基本操作
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学化学实验报告本
黔南民族师范学院
姓名:江边
实验室:无机
周次:周五
实验柜台: 11
指导老师:章文伟
硫酸亚铁铵的制备
一.实验目的
1. 学会利用溶解度的差异制备硫酸亚铁铵。
2. 从实验中掌握硫酸亚铁、硫酸亚铁铵复盐的性质
3. 掌握水浴、减压过滤等基本操作
4. 学习pH 试纸、吸管、比色管的使用
5. 学习用目测比色法检验产品质量。
二.原理
铁屑溶于稀硫酸生成硫酸铁。
硫酸铁与硫酸铵作用生成溶解度较小的硫酸亚铁铵。
三.仪器及药品
洗瓶、250ml 烧杯、10ml 量筒、50ml 量筒、吸滤瓶、比色管、铁粉、盐酸2mol/L 、3mol/L 硫酸、
四.实验步骤
1. 硫酸亚铁制备
2. 硫酸亚铁铵的制备
3. Fe 3+的限量分析
五.记录
1.实验现象:
①小火加热硝酸钠和氯化钾混合溶液过程中,烧杯内会有氯化钠晶体析出。
②热过滤后,漏斗滤纸上出现氯化钠白色晶体。
③滤瓶内液温降低后,出现白色针状的硝酸钾晶体。
④硝酸钾溶液加热浓缩后静置,降至室温出现较多的硝酸钾晶体。
⑤抽滤后漏斗上出现干燥的硝酸钾晶体。
2.产量:粗产品:2.78g
3.理论产量:
KCl+NaNO
3===K NO
3
+NaCl
m (K NO
3
) =(8.5*101.1)/85=10.1g
4.产率:2.78/10.1=27.5%
六.思考题
1.怎样利用溶解度差别从氯化钾—硝酸钠制备硝酸钾?
当硝酸钠和氯化钾溶液混合时,溶液中会有硝酸钾、氯化钠、硝酸钠和氯化钾四种盐。
在不同温度下它们在水中溶解度不同,特别是在较高温度,硝酸钾在水中的溶解度比氯化钠的要大得多,所以在冷却过程中氯化钠首先析出,趁热过滤后滤液中即含有硝酸钾。
2.实验成败的关键在何处,应采取哪些措施才能使试验成功?
①热过滤分离氯化钠和硝酸钾时要趁热快速,否则液温下降后硝酸钾也会
和氯化钠一起析出,减低产量。
②减压过滤时注意不出现穿滤现象。
滤纸不可过大,要全部紧贴漏斗底部,
可以用双层滤纸。
3.产品的主要杂质是什么?怎样提纯?
产品的主要杂质是氯离子,通过重结晶可以除去。
4.重结晶时,粗产品与水的质量比为什么是2:1?
80℃时硝酸钾的溶解度为169g/100g水,所以1g硝酸钾需水0.6ml,考虑加热时溶剂蒸发,选择粗产品与水的质量比为什么是2:1。
欢迎您的下载,
资料仅供参考!
致力为企业和个人提供合同协议,策划案计划书,学习资料等等
打造全网一站式需求。
