白砂糖GB
白砂糖国标

白砂糖国标
白砂糖,是一种普遍的食品添加剂,也是日常生活中经常使用的
调味品。
在中国,白砂糖的国标有严格的规定,其主要的化学成分为
蔗糖,在生产和储存中都有其特定的要求。
下面,我们就来了解一下
白砂糖的国标有哪些方面需要注意。
首先,白砂糖的外观应该是白色晶体,呈现出均匀的颗粒状,无
结晶、无杂质,无异味等特点。
其次,国标要求白砂糖的粘合度应该
控制在适宜范围内,不得过高或过低,以免影响其在烹饪和使用时的
体验和效果。
除此之外,国标还要求白砂糖的糖度应该在规定的范围内。
据统计,标准的白砂糖的糖度应该为99.7%以上,可达到非常纯净的效果。
国标中还规定了白砂糖的水分含量,应该在2.0%以内,这对于其保质
期和使用效果都非常重要。
此外,国标还要求,在白砂糖的生产过程中,应该保证其不含色
素或着色剂、不含铅、不含含氯有机物,以及其他有害物质。
这些因
素不仅对人体健康有影响,也会影响到食品的口感和质量。
综上所述,白砂糖的国标涉及多个方面,包括了其外观、粘合度、糖度、水分含量以及含有害物质等方面。
这些标准的制定,不仅保证
了人们在日常生活中安全食用白砂糖,同时也促进了食品行业的发展
和升级。
我们在选择和使用白砂糖时,不仅需要关注其国标的要求,
还需要了解其确切的减糖效果和适宜使用的量,以确保摄入的糖分不会对健康产生负面影响。
白砂糖GB

白砂糖GB 317—1998本标准是根据GB317.1—91《白砂糖》、GB/T317.2—91《白砂糖试验方法》、QB1213—91《精制白砂糖》及其实施情况以及GB13104—91《白糖卫生标准》的要求进行修订的,在技术要求上非等效采用CODEX STAN 4—1981《白糖》和《国际糖品统一分析方法》(SUGAR ANALYSIS—ICUMSA Methods,1986年英国版),在其他条款上严格按照我国有关标准和法规的要求编写,以适应我国市场经济下糖业发展和国内外贸易发展的需要。
在技术要求中,白砂糖的分级增加了“精制”,目的是为了将精制白砂糖行业标准并入白砂糖国家标准中,以适应我国制糖技术不断发展和精制白砂糖市场不断扩大的需要。
理化要求中多项指标有所提高,卫生要求中的二氧化硫(SO2)指标首次同时作为分级的依据之一。
在卫生要求中还增加了细菌和螨的项目、指标。
在检验规则中规定了新的抽样方法,标签和包装的要求也是根据有关最新标准和法规进行编写的。
在试验方法中,“色值的测定”以缓冲溶液法代替以往的调pH法,增加了螨的检验。
本标准从生效之日起,同时代替GB317.1—91、GB/T317.2—91。
本标准由中国轻工总会提出。
本标准由全国甘蔗糖业标准化中心和全国甜菜糖业标准化中心归口。
本标准由中国轻工总会甘蔗糖业研究所起草。
本标准主要起草人:梁达奉、张玲玲、严容百。
本标准于1984年首次制定,于1991年首次修订。
白砂糖White granulated sugar代替GB317.1-91GB/T317.2—911范围本标准规定了白砂糖的技术要求、试验方法、检验规则和标签、包装、运输、贮存的要求。
本标准适用于以甘蔗、甜菜或糖为原料生产的白砂糖。
2引用标准下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。
本标准出版时,所示版本均为有效。
所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
白砂糖检验标准Y006

6.1感官
将样品倒于干净的白纸上,在自然光线下目测其颜色和状态,直接品尝起滋味。
6.2干燥失重
a法:称取20~30g样品于已烘干至恒重的称量瓶中,置于105℃的烘箱中干燥3h,取出冷却后称重,计算减少的重量。
b法:称取9.5~10.5g样品于已烘干至恒重的称量瓶中,置于130℃的烘箱中干燥18min,取出冷却后称重,计算减少的重量。
5、检验规则
5.1每批白砂糖必须附有生产厂的产品合格证。
5.2抽样规则
以堆为单位,从糖堆的四个侧面及上面共五个面抽样,上面抽中心一个点,每个侧面在其中一条对角线上按如下规定均匀抽取若干点:300t以上(含300t)为三个点;300t以上每增加100t增加一个点,也即300t以下(含300t)的糖堆每堆抽13个点,300t以上的堆抽取的点数按式下面公式计算。
6.3蔗糖分:按GB317-1998中4.2规定的方法检验。
6.4还原糖分:按GB317-1998中4.3规定的方法检验。
6.5色值:按GB317-1998中4.6规定的方法检验。
6.6重金属及其它指标:按GB317-1998规定的方法测定。
6.7微生物:按GB4789规定的方法测定。
7、保质期:在所要求的保存条件下保质期不少于18个月。
优级
一级
蔗糖分,% ≥
99.7
99.6
还原糖分,% ≤
0.05
0.10
干燥失重,% ≤
0.06
0.07
色值,IU ≤
80
170
浊度,≤
7
9
不溶于水杂质,mg/kg
≤30
≤50
4.2.2重金属及其它指标:符合GB317-1998标准要求。
食糖糖类食品安全抽检方法实施细则

食糖糖类食品安全抽检方法实施细则1.1适用范围适用于食糖食品安全抽检监测产品范围包括白砂糖、绵白糖、赤砂糖、冰糖、冰片糖、方糖等产品。
本细则内容包括适用范围、产品种类、企业规模划分、检验依据、抽样、检验要求、判定原则、异议处理复检。
1.2产品种类食糖产品主要有白砂糖、绵白糖、赤砂糖、冰糖、冰片糖、方糖等。
1.3企业规模划分根据食糖产品行业的实际情况,生产企业规模以食糖产品年销售额为标准划分为大、中、小型企业。
见表1。
1.4检验依据下列文件凡是注明日期的,其随后所有的修改单或修订版均不适用于本细则。
凡是不注明日期的,其最新版本适用于本细则。
GB317白砂糖GB1445绵白糖GB2760食品安全国家标准食品添加剂使用标准GB4789.2食品安全国家标准食品微生物学检验菌落总数测定GB4789.3食品安全国家标准食品微生物学检验大肠菌群测定GB4789.4食品安全国家标准食品微生物学检验沙门氏菌检验GB4789.5食品安全国家标准食品微生物学检验志贺氏菌检验GB4789.10食品安全国家标准食品微生物学检验金黄色葡萄球菌检验GB/T4789.11食品卫生微生物学检验溶血性链球菌检验GB4789.15食品安全国家标准食品微生物学检验霉菌和酵母计数GB/T5009.11食品中总碑及无机碑的测定GB5009.12食品安全国家标准食品中铅的测定GB/T5009.15食品中镉的测定GB/T5009.17食品中总汞和有机汞的测定GB/T5009.55食糖卫生标准的分析方法GB5009.33食品安全国家标准食品中亚硝酸盐和硝酸盐的测定GB/T5009.35食品中合成着色剂的测定GB/T5009.141食品中诱惑红的测定GB/T5009.204食品中丙烯酰胺含量的测定方法气相色谱•质谱(GC-MS)法GB13104食糖卫生标准SN/T1547进出口食品中甲醛的测定液相色谱法QB/T1173单晶体冰糖QB/T1174多晶体冰糖QB/T1214方糖QB/T2343.1赤砂糖QB/T2343.2赤砂糖试验方法QB/T2685冰片糖经备案现行有效的企业标准及产品明示质量要求相关的法律法规、部门规章和规定。
白砂糖指标

白砂糖主要品质指标白砂糖主要品质指标按中华人民共和国国家标准——白砂糖((GB 317-1998)),其质量标准分为精制、优级、一级和二级。
另外,白砂糖国家新标准(GB 317-2***,替代GB 317-1998)已经修订完毕,正在国家审批程序之中。
附录2:《白砂糖》国家标准的新、旧指标对照中华人民共和国国家标准GB 317-1998:感官要求(1)晶粒均匀、粒度在下列范围内应不少于80%;——粗粒:0.800~2.50mm;——大粒:0.630~1.60mm;——中粒:0.450~1.25mm;——细粒:0.280~0.800mm。
(2)晶粒或其水溶液味甜无异味。
(3)干燥松散、洁白、有光泽、无明显黑点。
表2 理化要求项目指标精制优级一级二级蔗糖分,% ≥99.8 99.7 99.6 99.5还原糖分,% ≤0.03 0.05 0.10 0.17电导灰分,% ≤0.03 0.05 0.10 0.15干燥失重,% ≤0.06 0.06 0.07 0.12色值,IU ≤30 80 170 260混浊度,度≤ 3 7 9 11不溶于水杂质mg/kg≤20 30 50 802: 卫生要求项目指标精制优级一级二级二氧化硫(以SO2计)mg/kg ≤10 20 40 50砷(以As计),mg/kg ≤0.5 0.5 0.5 0.5铅(以Pb计),mg/kg ≤ 1.0 1.0 1.0 1.0铜(以Cu计),mg/kg ≤ 2.0 2.0 2.0 2.0菌落总数,个/g ≤200 350 350 350大肠菌群,个/100g ≤30 30 30 30致病菌(系指肠道致病菌和致病性球菌)不得检出不得检出不得检出不得检出螨(在250g白砂糖中)不得检出不得检出不得检出不得检出附录1:食糖的品种与质量食糖因原料、加工工艺不同,有普通白砂糖,精制幼(小粒)砂糖、精制绵白糖,普通绵白糖,方糖和块糖,冰糖,红糖等。
精制幼砂糖即精制小粒砂糖,因其纯净度高,蔗糖份含量达到99.8%以上,水份含量极少,各项卫生指标控制严格,晶粒小、均匀、松散,易溶化、易贮藏,不易受潮结块,特别适合于供作家庭常备食用糖和餐桌糖。
白砂糖质量标准
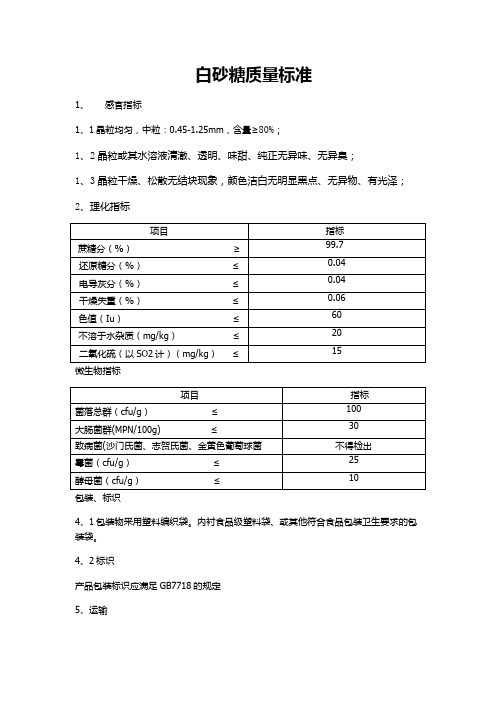
白砂糖质量标准
1、感官指标
1、1晶粒均匀,中粒:0.45-1.25mm,含量≥80%;
1、2晶粒或其水溶液清澈、透明、味甜、纯正无异味、无异臭;
1、3晶粒干燥、松散无结块现象,颜色洁白无明显黑点、无异物、有光泽;
2、理化指标
4、1包装物采用塑料编织袋。
内衬食品级塑料袋、或其他符合食品包装卫生要求的包装袋。
4、2标识
产品包装标识应满足GB7718的规定
5、运输
运输工具应清洁、干燥、无异味、无污染,运输中应防雨、防潮、防爆晒、防污染,严谨与有毒、有气味及其他会影响白砂糖质量的货物混运。
6、贮存
产品应存在清洁、干燥、低温的仓库中,严谨与有毒、有害及其他易对白砂糖造成污染的物品混放。
离墙壁、暖气管、水泥柱1m以外、离地0.1m以上的防潮隔板上,出入仓时应避免骤冷骤热。
7、净含量检验
符合标准标注要求,净含量允许短缺量按国家质量监督局检验检疫总局(2005)第75号令的规定执行。
白糖交割标准及升贴水相关规定
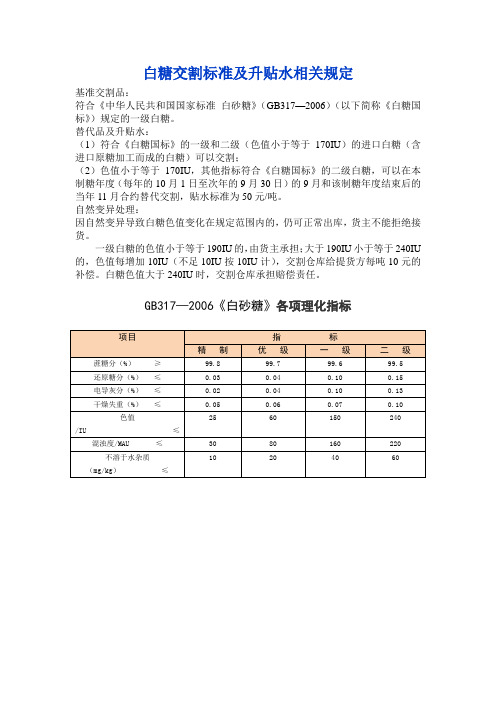
白糖交割标准及升贴水相关规定
基准交割品:
符合《中华人民共和国国家标准白砂糖》(GB317—2006)(以下简称《白糖国标》)规定的一级白糖。
替代品及升贴水:
(1)符合《白糖国标》的一级和二级(色值小于等于170IU)的进口白糖(含进口原糖加工而成的白糖)可以交割;
(2)色值小于等于170IU,其他指标符合《白糖国标》的二级白糖,可以在本制糖年度(每年的10月1日至次年的9月30日)的9月和该制糖年度结束后的当年11月合约替代交割,贴水标准为50元/吨。
自然变异处理:
因自然变异导致白糖色值变化在规定范围内的,仍可正常出库,货主不能拒绝接货。
一级白糖的色值小于等于190IU的,由货主承担;大于190IU小于等于240IU 的,色值每增加10IU(不足10IU按10IU计),交割仓库给提货方每吨10元的补偿。
白糖色值大于240IU时,交割仓库承担赔偿责任。
GB317—2006《白砂糖》各项理化指标
项目指标
精制优级一级二级
蔗糖分(%)≥99.899.799.699.5
还原糖分(%)≤0.030.040.100.15
电导灰分(%)≤0.020.040.100.13
干燥失重(%)≤0.050.060.070.10色值
2560150240
/IU ≤
混浊度/MAU ≤3080160220不溶于水杂质
10204060
(mg/kg)≤。
白砂糖验收标准
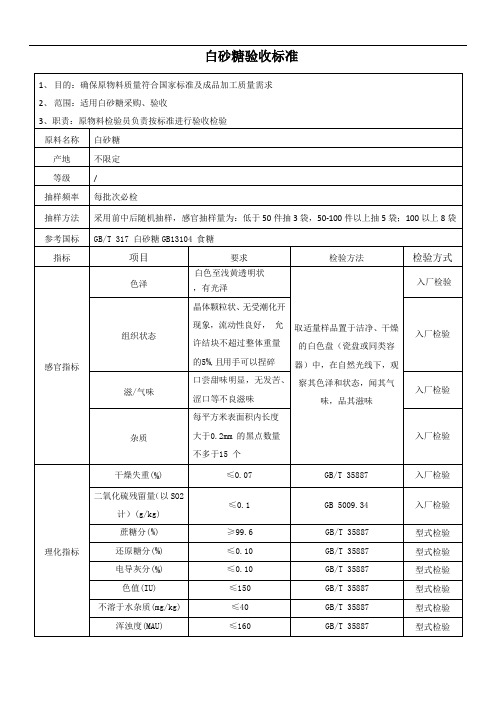
白砂糖验收标准
1、目的:确保原物料质量符合国家标准及成品加工质量需求
2、范围:适用白砂糖采购、验收
3、职责:原物料检验员负责按标准进行验收检验
原料名称白砂糖
产地不限定
等级/
抽样频率每批次必检
抽样方法采用前中后随机抽样,感官抽样量为:低于50件抽3袋,50-100件以上抽5袋;100以上8袋参考国标GB/T 317 白砂糖GB13104 食糖
指标项目要求检验方法检验方式
感官指标
色泽
白色至浅黄透明状
,有光泽
取适量样品置于洁净、干燥
的白色盘(瓷盘或同类容
器)中,在自然光线下,观
察其色泽和状态,闻其气
味,品其滋味
入厂检验组织状态
晶体颗粒状、无受潮化开
现象,流动性良好,允
许结块不超过整体重量
的5,且用手可以捏碎
入厂检验滋/气味
口尝甜味明显,无发苦、
涩口等不良滋味
入厂检验杂质
每平方米表面积内长度
大于0.2mm 的黑点数量
不多于15 个
入厂检验
理化指标
干燥失重() ≤0.07 GB/T 35887 入厂检验二氧化硫残留量(以SO2
计)(g/kg)
≤0.1 GB 5009.34 入厂检验蔗糖分() ≥99.6 GB/T 35887 型式检验还原糖分() ≤0.10 GB/T 35887 型式检验电导灰分() ≤0.10 GB/T 35887 型式检验色值(IU) ≤150 GB/T 35887 型式检验不溶于水杂质(mg/kg) ≤40 GB/T 35887 型式检验浑浊度(MAU) ≤160 GB/T 35887 型式检验。
白砂糖的分级质量与检验二

白砂糖的分级质量与检验二2005-3-11 15:19:12 期货日报四、白砂糖的检验这里所谈的对白砂糖的检验,其对象系指经国家认可的生产工厂,按标准《GB317-1998》所要求的质量进行生产制造,且符合标准《GB7718-2004》预包装食品标签通则要求堆存入库的成品白砂糖,检验是对其内在品质、单包计量工、包装/标识和堆存条件等所进行的一种认可式的检验。
其结果可表明所验货物的即时品质状况,也可对预见使用时限提供参考。
对此所实施的检验可从如下几个方面进行。
1.确定所验货物是否符合取样条件确认货物是否符合取样条件是判定所抽取样品是否具有代表性的前题。
对堆存入库的货物应首先查明货物来源、生产包装日期、包装计量/标签标识等情况是否符合国家标准要求。
其次应查明货物包装是否受到外来物的污染,堆存是否符合要求等。
总之,货物各项外观特征是否一致等是确定能否抽取样品的先决条件。
2.样品的抽取所验货物因加工批号、原料情况(来源、种类、地点、季节等)、加工方法、运输、保藏条件和销售中的各个环节(如有无防蛀、防污染、防蟑螂及防鼠等设备)不同,以及相关人员责任心和卫生知识水平有差异等均可对所验项目指标造成影响。
因此,依相关检验标准的要求所抽取的样品必须有代表性。
白砂糖可以按每个交收批作为一个检验批,也可按每个堆存单位作为一个检验批。
取样时从每个堆存单位的4个侧面及上面共5个面进行抽样,上面可在其中心部位确定一个取样点,每个侧面在其中一条对角线上按如下规定均匀置布若干点。
如300吨以下堆存单位(含300吨)布3个点,300吨以上每增加100吨增加一个点。
取样布点数可按下式求得:n=4(M/100)+1。
取样时必须在无菌操作下进行,每一点用专用抽样器抽取150克,装入洁净无菌的容器内,边取边混合,将每垛各点所取样品置于专用样品容器内混均,作为该垛位的样品。
若每批有多个堆存单位也可将各所取样品混均后作为该批样品。
取样后在容器外立即贴上标签,每件样品必须标记下列内容:品名、来源、数量、地点、取样时间及取样人员等,并立即送交实验室进行各项指标的检测。
白砂糖质量标准
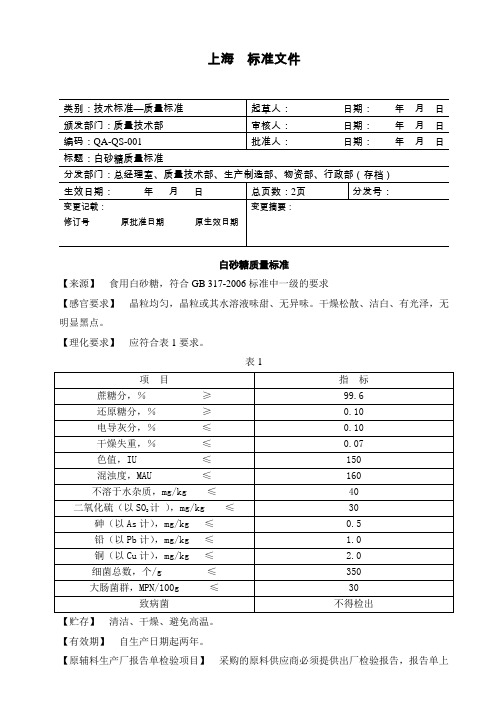
上海标准文件
标题:白砂糖质量标准
白砂糖质量标准
【来源】食用白砂糖,符合GB 317-2006标准中一级的要求
【感官要求】晶粒均匀,晶粒或其水溶液味甜、无异味。
干燥松散、洁白、有光泽,无明显黑点。
【理化要求】应符合表1要求。
表1
【贮存】清洁、干燥、避免高温。
【有效期】自生产日期起两年。
【原辅料生产厂报告单检验项目】采购的原料供应商必须提供出厂检验报告,报告单上
2/2 白砂糖质量标准QA-QS-001 至少包括感官、蔗糖分、还原性糖分、电导灰分、干燥失重、色值、浑浊度、不溶于水杂质及二氧化硫的指标。
【原辅料进厂检验项目】感官、电导灰分、干燥失重、细菌总数、大肠菌群、霉菌、酵母菌、致病菌。
【原辅料进厂验收标准】应符合表2
表2。
白砂糖等级划分标准

白砂糖等级划分标准
白砂糖是日常食品中常见的甜味剂,其等级划分标准主要是按照国家标准GB/T
317-2006《白砂糖》进行的,下面详细介绍一下。
1. 一级白砂糖:其含有白砂糖不低于99.8%,不含任何色素、质量提高剂、防腐剂、香精药用成分等物质,且无异味。
2. 优级白砂糖:其含有白砂糖不低于99.5%,且相比一级白砂糖,在制造过程中允许使用酸性、酶法或其他适当工艺的脱色剂和去杂剂,但总使用量不超过0.1%,且不含任何非食品添加物和异味。
4. 一般白砂糖:其含有白砂糖不低于98.5%,允许少量添加食品添加剂(如焦糖色素),但添加量不得超过0.5%。
综上所述,白砂糖的等级由高到低依次为一级白砂糖、优级白砂糖、合格白砂糖和一
般白砂糖。
在选择和购买白砂糖时,应尽可能选择质量等级高、添加物和杂质含量低的产品,以保证食品的安全和品质。
国家标准化管理委员会关于实施GB317-2006《白砂糖》等2项国家标准有关问题的通知

国家标准化管理委员会关于实施GB317-2006《白砂糖》等2项国家标准有关问题的通知
文章属性
•【制定机关】国家标准化管理委员会
•【公布日期】2006.09.30
•【文号】国标委农轻[2006]71号
•【施行日期】2006.10.01
•【效力等级】部门规范性文件
•【时效性】现行有效
•【主题分类】标准化
正文
国家标准化管理委员会关于实施GB317-2006《白砂糖》等2
项国家标准有关问题的通知
(国标委农轻[2006]71号)
各有关单位:
GB317-2006《白砂糖》、GB15108-2006《原糖》国家标准已于2006年3月31日发布,将于2006年10月1日实施。
现就该2项标准实施工作通知如下:
一、自2006年10月1日起,生产企业应严格执行GB317-2006《白砂糖》、GB15108-2006《原糖》国家标准。
二、2006年10月1日前生产的白砂糖和原糖,在保质期内按GB317-1998《白砂糖》、GB/T 15108-1994《原糖》国家标准执行。
特此通知
二〇〇六年九月三十日。
白砂糖标准 (3)

白砂糖标准1. 简介白砂糖是一种常见的食用糖,主要由蔗糖组成。
在食品工业中,白砂糖被广泛应用于食品加工、烘焙、制作软糖和饼干等食品制造过程中,也用于调味和糕点制作。
本文档将介绍白砂糖标准,包括其外观、化学成分、检测方法和质量要求等内容。
2. 外观白砂糖应呈无色或微黄色结晶体,有一定的光泽。
在干燥条件下,应该是无臭的。
外观应该均匀细腻,无明显杂质的存在。
3. 化学成分白砂糖的主要成分是蔗糖(C12H22O11)。
蔗糖是由葡萄糖和果糖结合而成的二糖。
除了蔗糖外,白砂糖中还含有少量的水分和微量的灰分。
水分和灰分的含量对糖的质量有一定的影响,需要符合相应的标准。
4. 检测方法4.1 外观检测外观检测主要是通过目测来判断白砂糖的外观是否符合标准。
应将白砂糖取一定量,放在透明的容器中观察。
外观应呈均匀细腻的结晶体,无明显杂质的存在。
颜色应该接近无色或微黄色,有一定的光泽。
4.2 化学成分检测化学成分检测主要是通过化学分析方法来测定蔗糖、水分和灰分的含量。
4.2.1 蔗糖含量检测蔗糖含量可以通过重量法或色谱法进行检测。
重量法是通过称量一定重量的白砂糖,溶解于适量的水中,并加入适量的酶解剂,然后经过加热和过滤等处理,最后用称量法测定产物的重量来计算蔗糖的含量。
色谱法则是利用色谱仪测定样品中蔗糖的峰面积或峰高来计算蔗糖的含量。
4.2.2 水分含量检测水分含量检测可以采用称重法或干燥法。
称重法是将一定重量的样品在约定的条件下加热,直至其质量不再变化,记录下称量前后的质量差值,再通过计算来确定水分含量。
干燥法则是将样品放置在一定的温度下,在一定时间内进行干燥,然后再称量样品的质量差值来计算水分的含量。
4.2.3 灰分含量检测灰分含量检测可以采用干燥法或燃烧法。
干燥法是将一定重量的白砂糖样品加热至一定温度下,烘干一段时间,再称量样品的质量差值来计算灰分含量。
燃烧法是将样品放入燃烧炉中进行加热燃烧,然后称量样品的质量差值来计算灰分含量。
白砂糖执行标准

白砂糖执行标准
白砂糖是我们日常生活中常见的食品原料,也是烹饪和烘焙中常用的甜味剂。
为了确保生产的白砂糖符合卫生安全、质量稳定的要求,制定了白砂糖的执行标准。
本文将对白砂糖执行标准进行详细介绍,包括其主要内容和相关要求。
一、外观要求。
白砂糖应呈白色,无杂质、异物和霉斑。
颗粒大小均匀,不应有结块和结晶。
二、理化指标。
1. 水分含量,白砂糖水分含量不得高于0.06%。
2. 灰分含量,白砂糖灰分含量不得高于0.04%。
3. PH值,白砂糖PH值应在5.5-7.0之间。
4. 可溶性固体含量,白砂糖可溶性固体含量不得低于99.5%。
5. 色度,白砂糖色度不得高于45ICUMSA。
三、化学指标。
白砂糖中不得含有对人体有害的化学物质,如重金属、农药残留等。
四、微生物指标。
白砂糖中不得含有大肠菌群、霉菌、酵母菌等微生物。
五、贮存要求。
白砂糖应贮存在通风、干燥、清洁的环境中,远离有害气体和异味。
六、包装标识。
白砂糖包装上应标注生产日期、保质期、生产厂家、产品批号等信息,并符合国家相关标准的要求。
七、质量控制。
生产企业应建立健全的质量控制体系,加强原料采购、生产工艺、包装运输等各个环节的质量管理,确保产品质量稳定可靠。
以上即是白砂糖执行标准的主要内容和相关要求。
生产企业应严格按照执行标准的要求进行生产,确保产品质量安全、稳定,为消费者提供优质的白砂糖产品。
同时,监管部门也应加强对白砂糖产品的监督检查,确保市场上的白砂糖产品符合标准要求,保障公众健康。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
白砂糖GB 317—1998本标准是根据GB317.1—91《白砂糖》、GB/T317.2—91《白砂糖试验方法》、QB1213—91《精制白砂糖》及其实施情况以及GB13104—91《白糖卫生标准》的要求进行修订的,在技术要求上非等效采用CODEX STAN 4—1981《白糖》和《国际糖品统一分析方法》(SUGAR ANALYSIS—ICUMSA Methods,1986年英国版),在其他条款上严格按照我国有关标准和法规的要求编写,以适应我国市场经济下糖业发展和国内外贸易发展的需要。
在技术要求中,白砂糖的分级增加了“精制”,目的是为了将精制白砂糖行业标准并入白砂糖国家标准中,以适应我国制糖技术不断发展和精制白砂糖市场不断扩大的需要。
理化要求中多项指标有所提高,卫生要求中的二氧化硫(SO2)指标首次同时作为分级的依据之一。
在卫生要求中还增加了细菌和螨的项目、指标。
在检验规则中规定了新的抽样方法,标签和包装的要求也是根据有关最新标准和法规进行编写的。
在试验方法中,“色值的测定”以缓冲溶液法代替以往的调pH法,增加了螨的检验。
本标准从生效之日起,同时代替GB317.1—91、GB/T317.2—91。
本标准由中国轻工总会提出。
本标准由全国甘蔗糖业标准化中心和全国甜菜糖业标准化中心归口。
本标准由中国轻工总会甘蔗糖业研究所起草。
本标准主要起草人:梁达奉、张玲玲、严容百。
本标准于1984年首次制定,于1991年首次修订。
白砂糖White granulated sugar代替GB317.1-91GB/T317.2—911范围本标准规定了白砂糖的技术要求、试验方法、检验规则和标签、包装、运输、贮存的要求。
本标准适用于以甘蔗、甜菜或糖为原料生产的白砂糖。
2引用标准下列标准所包含的条文,通过在本标准中引用而构成为本标准的条文。
本标准出版时,所示版本均为有效。
所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。
GB4789.1~4789.31—94食品卫生检验方法微生物学部分GB/T5009.55—1996食糖卫生标准的分析方法GB7718—94食品标签通用标准GB13104—91白糖卫生标准3技术要求白砂糖按技术要求的规定分为精制、优级、一级和二级共四个级别。
3.1感官要求3.1.1晶粒均匀,粒度在下列范围内应不少于80%:——粗粒:0.800~2.50mm;——大粒:0.630~1.60mm;——中粒:0.450~1.25mm;——细粒:0.280~0.800mm。
3.1.2晶粒或其水溶液味甜、无异味。
3.1.3干燥松散、洁白、有光泽,无明显黑点。
3.2理化要求白砂糖的各项理化指标见表1。
3.3卫生要求白砂糖的各项卫生指标见表2。
4试验方法卫生要求中的二氧化硫、砷、铅、铜按GB/T5009.55规定的方法进行测定,菌落总数、大肠菌群、致病菌按GB4789.1~4789.31规定的方法进行测定,其余各项目按本章相应方法进行测定。
4.1粒度的测定4.1.1方法提要用一套试验筛将糖样品在一定的条件下进行筛选,将各个筛中截留的糖颗粒称量,求得留在筛网上糖颗粒的百分数对筛孔的关系。
4.1.2仪器、设备4.1.2.1试验筛:筛孔0.280~2.50mm一套,直径200mm。
4.1.2.2震筛机:其振动频率,以防止磨损糖晶体为准。
4.1.2.3天平:精确度为±0.1g。
4.1.3步骤4.1.3.1取样样品按四分法进行二次分离,使二次分出的样品能满足筛分检验之用。
4.1.3.2筛分称取白砂糖样品100g,准确至0.1g。
将经过选择并称量的筛子,按筛孔尺寸由小到大自下而上叠装好,然后,将样品放入最上层的筛中,用盖盖好,将套筛装于震筛机上,并开动时钟或计时表,振动10min,待震动完全停止后,将筛取下,称出每一个筛子及截留糖样质量,准确到0.1g。
4.1.3.3计算及结果表示计算出粒度上下限相对应孔径的两层筛之间所截留的糖样质量百分数,结果以孔径上下限及其质量百分数表示,计算结果取整数。
4.2蔗糖分的测定4.2.1术语国际糖度标尺international sugar scale规定量纯蔗糖溶液[在标准大气压状态下,在空气中用黄铜砝码称取26.0000g纯蔗糖(在真空中为26.0160g),在20.00℃时溶成体积为100.000mL],用λ=546.2271nm波长的光(真空198Hg的绿色偏振光),在温度为20.00℃时,用200.00mm观测管,所测得的光学旋光度,规定为糖度标尺的100度点。
100度点被指定为100°Z(国际糖度),并且标尺在0°Z(纯水时)和100°Z之间进行线性分度。
与100°Z相当的旋光值为:实际旋光测定,也允许在波长540~633nm的范围内,以固定100度点。
在黄色钠光波长下,100°Z 相当的旋光值为:在氦/氖(He/Ne)激光波长下,100°Z相当的旋光值为:4.2.2方法提要在规定条件下采用以国际糖度标尺刻制读数为100°Z的检糖计,测定规定量糖样品的水溶液的旋光度。
4.2.3仪器、设备4.2.3.1检糖计检糖计应是根据国际糖度标尺,按糖度(°Z)刻度的,测量范围能够从-30~+120°Z,或者这个范围的一部分,自动检糖计准确度应为0.05°Z,目测检糖计应精确至0.1°Z,并用标准石英片加以校准,可选三种形式:——装有可调整分析器即检偏器的检糖计(圆盘式旋光计),采用单色光源(波长在540~590nm 之间),通常采用绿色的汞光或黄色的钠光;——石英楔检糖计;a)配有单色光源的(波长在540~590nm之间);b)配有白炽灯作为光源的,而用适当的滤色器分离出有效波长为587nm的光。
——装有法拉第线圈作为补偿器的检糖计,采用单色光源(波长在540~590nm之间)。
注:旧糖度°S刻度的检糖计仍然可以使用,但读数°S须乘上一个系数0.99971转换为°Z。
4.2.3.2容量瓶容积:1O0.OO±0.05mL,应分别用20.0±0.1℃的水称量加以校正。
容量瓶的容量在100.00±0.01mL范围内,不必更正便可使用;超出此范围,应采用与100.00mL相应的校正数加以更正,才可使用。
4.2.3.3旋光观测管长度:200.00±0.02mm,须由法定的计量机构出具合格证明,或者用具有该项证明的观测管来进行比较检验。
4.2.3.4分析天平精确度±0.001g。
4.2.4试剂蒸馏水:旋光测定用的蒸馏水应不含旋光物质。
4.2.5检糖计的校准检糖计的读数要用经法定的计量机构鉴定或曾与鉴定标准进行检定的标准石英片校准,检糖计不能用蔗糖溶液校准。
4.2.5.1石英片旋光度的温度校正使用检糖计(没有石英楔补偿器的)读取石英片读数时的温度应测定,并记录到0.2℃,如果这个温度与20℃相差大于±0.5℃,则采用式(4)进行标准石英片旋光度的温度校正。
式中:t——读取石英片读数时石英片的温度,℃;a1——t℃时,标准石英片的旋光值,°Z;a20——20℃时,标准石英片的旋光值,°Z。
4.2.5.2不同波长下石英片的换算系数石英片的糖度读数在不同波长下以绿色汞光(波长546nm)为基准,可按表3进行换算。
4.2.6溶液的配制称取一规定量糖样品(26.000±0.002g)于干洁的小烧杯中,加蒸馏水40~50mL,使其完全溶解。
移入100mL的容量瓶中,用少量蒸馏水分3~5次冲洗烧杯及玻璃棒,每次倒入洗水后,摇匀瓶内溶液,直至加蒸馏水至容量瓶量标线附近。
至少放置10min使达到室温,然后加蒸馏水至容量瓶标线下约1mm处,确保容量瓶颈部已洗净。
有气泡时,可用乙醚或乙醇消除。
用长嘴的滴管加水至标线,用干净的滤纸吸干容量瓶颈的内壁,将塞子塞紧,充分摇匀。
如发现混浊,用滤纸过滤,漏斗上须加表面玻璃,将最初10mL滤液弃去,收集以后的滤液50~60mL。
4.2.7旋光度的测定用待测的溶液将旋光观测管至少冲洗2次,然后将溶液装满观测管,注意不使观测管内夹带空气泡。
将旋光观测管置于检糖计中,目测的检糖计测定5次,读数至0.05°Z;如用自动检糖计,在测定前,应有足够的时间使仪器达到稳定。
测定旋光读数后,立即测定观测管内溶液的温度,并记录至0.1℃。
4.2.8计算及结果表示测定旋光度的温度应尽可能接近20℃,一般应在15~25℃的范围。
如果旋光度不是在20.0±0.2℃时测定的,则应校正到20℃。
白砂糖样品的蔗糖分按式(5)、(6)计算,以百分数表示,计算结果取到一位小数。
采用石英楔补偿器的检糖计:没有石英楔补偿器的检糖计:式中:P1——观测旋光度读数,°Z;t——观测P t时糖液温度,℃。
4.2.9允许误差两次测定值之差不得超过其平均值的0.05%。
4.3还原糖分的测定4.3.1方法提要本法是基于碱性铜盐溶液中金属盐类的还原作用,用碘滴定法定量奥氏试剂与糖液作用生成的氧化亚铜,从而确定样品中的还原糖分。
本法各项试验条件(包括试液量、奥氏试剂量、煮沸时间、碘液耗用量及碘的反应时间等)都应严格按标准规定。
4.3.2仪器、设备4.3.2.1锥形烧瓶:容量300mL。
4.3.2.2滴定管:50mL,刻度刻至0.1mL。
4.3.3试剂4.3.3.1奥氏试剂:分别称取硫酸铜(CuSO4·5H2O)5.0g,酒石酸钾钠300g及无水碳酸钠(Na2CO3)10.0g,磷酸氢二钠(Na2HPO4·12H2O)50g(或无水盐19.8g),溶于900mL蒸馏水中,如有必要可将其微微加热。
待完全溶解后,放入沸水浴中,加热杀菌2h,然后冷却至室温,稀释至1000mL,加入少量活性炭或硅藻土过滤,贮于棕色试剂瓶中。
4.3.3.2硫代硫酸钠贮备溶液:取硫代硫酸钠(Na2S2O3·5H2O)20g及无水碳酸钠0.1g(或1m0l/L氢氧化钠溶液1mL),用经煮沸灭菌蒸馏水溶解,稀释至500mL,保存于棕色试剂瓶中,放置8~14天后过滤备用。
4.3.3.30.032mol/L硫代硫酸钠溶液,需用时配制如下:吸取硫代硫酸钠贮备溶液100mL,移入容量瓶中并用经煮沸灭菌的蒸馏水稀释至500mL,该试剂用重铬酸钾标准溶液标定,并校正其浓度。
4.3.3.40.01615mol/L碘液:称取10g左右的碘化钾(无碘),先溶解于数毫升的水中,另称取纯碘2.050g,溶于碘化钾溶液,将溶液全部移入500mL容量瓶中并加水至标线,贮存于具有玻璃塞密封的棕色瓶内。
