1306氢原子能级及能级跃迁.ppt
高考物理氢光谱和能级(PPT)4-1

全球均一性热带、亚热带气候逐渐变成在中、高纬度地区四季分明的多样化气候,蕨类植物因适应性的欠缺进一步衰落,裸子植物也因适应性的局限而开始 走上了下坡路。这时,被子植物在遗传、发育的许多过程中以及茎叶等结构上的进步性,尤其是它们在花这个繁殖器官上所表现出的巨大进步性发挥了作用; 股票入门 炒股入门知识学习 股市入门基本知识 /stock 股票 入门 股票入门基础知识txt 炒股入门知识书籍下载 股票的基础知识入门 ;使它们能 够通过本身的遗传变异去适应那些变得严酷的环境条件反而发展得更快,分化出更多类型,到现代已经有了多个目、多个科。正是被子植物的花开花落,才 把四季分明的新生代地球装点得分外美丽。 植物 植物(张) 据估计,现存大约有个植物物种,被分类为种子植物、苔藓植物、蕨类植物和藻类植物。直至年, 其中的个物种已被确认,有种开花植物、种苔藓植物、种蕨类植物和种绿藻。 非正式的类群 门 物种数量(现存的大概数量) 藻类植物 绿藻门 , 轮藻门 , - , 苔藓植物 地钱门 , - , 角苔门 - 苔藓植物门 , 蕨类植物 石松门 , 蕨类植物门 , 种子植物 裸子植物门 被子植物门 组成器官编辑 植物共有六大器官:根、茎、 叶、花、果实、种子。茎是植物体中轴部分。直立或匍匐于水中,茎上生有分枝,分枝顶端具有分生细胞,进行顶端生长。茎一般分化成短的节和长的节间 两部分。茎具有输导营养物质和水分以及支持叶、花和果实在一定空间分布成形的作用。有的茎还具有光合作用、贮藏营养物质和繁殖的功能。 植物 植物 (张) 叶是维管植物营养器官之一。功能为进行光合作用合成有机物,并有蒸腾作用提供根系从外界吸收水和矿质营养的动力。花是具有繁殖功能的变态短枝。 果实主要是作为传播种子的媒介。种子具有繁殖和传播的作用,种子还有种种适于传播或抵抗不良条件的结构,为植物的种族延续创造了良好的条件。 根 根 是植物的营养器官,通常位于地表下面,负责吸收土壤里面的水分 及溶解其中的离子,并且具有支持、贮存合成有机物质的作用。(气生根和固着根除外) 根由薄壁组织、维管组织、保护组织、机械组织和分生组织细胞组成。 根可分为四个区,最顶端的是帽状结构——根冠,以上是分生区和伸长区,再上则是 带根毛的根毛区。 根冠位于根顶端分生组织的外面。外层细胞壁的高度粘液化可以减少根在往下生长过程中与土壤接触的摩擦力,起到保护作用。同时细胞 中的造粉体还可保证根的向地生长,即保证其向地性(Gravitropism)。 分生区是位于根冠内方的顶端分生组织。分生区细胞能不断分裂,一方面小部分用 来形成根冠细胞,而大部分则向后
4-4 第2课时玻尔理论对氢光谱的解释 氢原子能级跃迁( 课件高中物理人教版(2019)选择性必修三

巴 耳 末 系
氢原子能级跃迁与光谱图
玻尔理论与巴耳末公式
请同学们用这几个公式推出巴耳末公式
结果与实验值符合的很好
玻尔理论与巴耳末公式
Hδ
Hγ
Hβ
Hα
n=2n=1 n=3 n=4
n=5
n=6
玻尔理论与巴耳末公式
Hδ
Hγ
巴尔末系氢吸收光谱
n=2 n=1 n=3 n=4 n=5
n=6
Hβ Hα
玻尔理论解释气体导电发光
光子的发射和吸收
注意一群原子和一个原子
氢原子核外只有一个电子,这个电子在某个时刻只能处在某一个可能 的轨道上,在某段时间内,由某一轨道跃迁到另一个轨道时,可能的 情况只有一种,但是如果容器中盛有大量的氢原子,这些原子的核外 电子跃迁时就会有各种情况出现
注意直接跃迁与间接跃迁
原子从一种能量状态跃迁到另一种能量状态时,有时可能是直接跃迁 ,有时可能是间接跃迁。两种情况的辐射(或吸收)光子的频率不同 ,但都满足频率条件
电子从低能级(如基态)向高能 级(如第一激发态)跃迁时,需 要吸收能量
若给它10.1eV的能量,电子能否 发生跃迁?
不能
若给它13.6的能量,电子将会如 何运动?大于13.6eV的能量呢?
光子的发射和吸收
原子发光现象:原子从较高的激发态向较低的激发态或基态跃迁的过程,是
辐射能量的过程,这个能量以光子的形式辐射出去,这就是原子发光现象。
问题与练习 如图,用玻尔理论解释,当巴耳末公式n=5时计算出的氢原子 光谱的谱线,是哪两个能级之间的跃迁造成的?
根据巴耳末公式,n=5时计算出的氢原 子光谱的谱线是量子数为5的能级跃迁 到量子数为2的能级形成的
问题与练习 请用玻尔理论解释:为什么原子的发射光谱都是一些分立的亮线?
13-06氢原子能级及能级跃迁
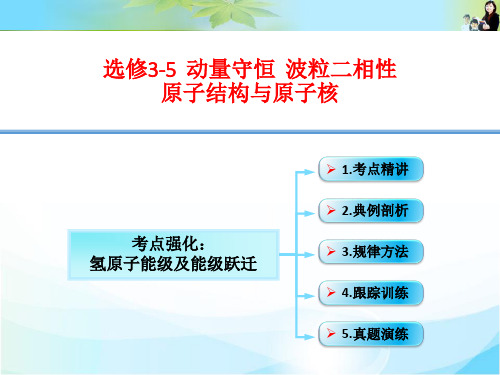
相邻横线间 的距离
带箭头的竖线
返回目录
结束放映
数字媒体资源库
2.定态间的跃迁——满足能级差. n小→n大吸收能量 hν=En大-En小. n大→n小放出能量 hν=En大-En小.
吸收一 定频率 的光子
释放 一定 频率 光子
3.电离 电离态与电离能 (1)电离态:n=∞,E=0 基态→电离态:E吸=0-(-13.6 eV)=13.6 eV电离能. n=2→电离态:E吸=0-E2=3.4 eV (2)如吸收能量足够大,克服电离能后,获得自由的电子还携带 动能.
第12页
返回目录
结束放映
数字媒体资源库
【典例2】 [2013· 江苏单科,12C(2)]根据
玻尔原子结构理论,氦离子(He+)的能级图
如图所示.电子处在n=3轨道上比处在n= 近 选填“近” 5轨道上离氦核的距离_____( 或“远”).当大量He+处在n=4的激发态 6 条. 时,由于跃迁所发射的谱线有_____
1 1 1 =R22-n2 ,(n=3,4,5,…), λ
R是里德伯常量,R=1.10×107 m-1,n为量子数.
第4页
返回目录
结束放映
数字媒体资源库
2.玻尔理论 (1)定态:原子只能处于一系列________ 不连续 的能量状态中,在这些 能量状态中原子是______ 稳定 的,电子虽然绕核运动,但并不向外 辐射能量. (2)跃迁:原子从一种定态跃迁到另一种定态时,它辐射或吸收 一定频率的光子,光子的能量由这两个定态的能量差决定,即 Em-En h是普朗克常量,h=6.63×10-34 J· hν=________.( s) (3)轨道:原子的不同能量状态跟电子在不同的圆周轨道绕核运 动相对应.原子的定态是_________ 不连续 的, 不连续 的. 因此电子的可能轨道也是________
高考物理氢光谱和能级(PPT)4-4

一、玻尔的原子理论——三条假设 二、氢原子能级及氢光谱
三. 几个重要的关系式 四. 玻尔理论的局限性 五、氢原子中的电子云
055. 08年佛山市教学质量检测(二)2 gk006. 2008年高考物理广东卷 6 gk009. 2008年高考理综山东卷38(1) 054. 08年北京市海淀区一模试卷13 035. 广东茂名市2007年第二次模考 4 064. 08年福建省十大名校高考模拟试题 5 039. 08年深圳市第一次调研考试2 066. 珠海市2008年高考模拟考试 2 018. 湖南省师大附中07—08学年第一次月考 4 052. 2008年北京东城区第一次模拟试题17 057. 广东省汕头市2008年模拟考试6 065. 08年南京一中第三次模拟13(3) gk015. 2008年高考理综四川延考区卷 20 067. 广州市重点中学07~08学年度第三次质检 2
【疤拉】?ɑ同“疤瘌”。 【疤拉眼儿】?ɑ同“疤瘌眼儿”。 【疤瘌】?ɑ名疤。也作疤拉。 【疤瘌眼儿】?ɑ〈口〉名①眼皮上有疤的眼睛。②眼皮上有疤的 人。‖也作疤拉眼儿。 【捌】数“八”的大写。参看页〖数字〗。 【笆】用竹片或树的枝条编成的片为半球形。 【笆篱】〈方〉名篱笆。 【笆篱子】?〈方〉名监狱。 【笆篓】名用树条或竹篾等编成的器物,多用来背东西。 【粑】〈方〉名饼类 食物:糍~|糖~|糯米~。 【粑粑】〈方〉名饼类食物:玉米~。 【鲃】(?)名鱼,体侧扁或略呈圆筒形,生活在淡水中,种类很多。 【拔】①动把固 定或隐藏在其他物体里的东西往外拉;抽出:~草|~剑|~刺|~了一颗牙◇~了祸根。②动吸出(度气等):~度|~火|~罐子。③挑选(多指人
才):选~。④动向高提:~嗓子。⑤超出;高出:海~|出类~萃。⑥动夺取;攻克(据点、城池等):连~敌军三个据点。⑦〈方〉动把东西放在凉水 里使变凉:把西瓜放在冰水里~一~。⑧()名姓。 【拔除】动拔掉;除去:~杂草|~敌军据点。 【拔刀相助】形容见义勇为,打抱不平。 【拔地而起】 形容山峰、建筑物等陡然矗立在地面上。 【拔份】(~儿)〈方〉动抬高身份;出风头:他学武术是为了增进健康,不是为了~。 【拔高】∥动①提高:~ 嗓子唱。②有意抬高某些人物或作品等的地位:这部作品对主人公过分~,反而失去了真实性。 【拔罐子】?一种治疗方法,在小罐内点火燃烧片刻,把罐 口扣在皮肤上,造成局部充血,以调理气血。常用于治疗感冒、头痛、哮喘、腰背疼痛等。有的地区说拔火罐儿()。 【拔河】∥动一种体育运动,人数相 等的两队队员,分别握住长绳两端,向相反方向用力拉绳,把绳上系着标志的一点拉过规定界线为胜。 【拔火罐儿】〈方〉拔罐子。 【拔火罐儿】名一种上
氢原子光谱课件

氢原子光谱课件引言氢原子光谱是量子力学和原子物理学领域的基础内容,对于理解原子结构、光谱现象以及化学键的形成具有重要意义。
本课件旨在介绍氢原子光谱的基本原理、实验观测和理论解释,帮助读者深入理解氢原子的能级结构和光谱特性。
一、氢原子的基本结构1.1电子轨道和量子数氢原子由一个质子和一个电子组成,电子围绕质子旋转。
根据量子力学的原理,电子在氢原子中只能存在于特定的轨道上,这些轨道被称为能级。
每个能级由主量子数n来描述,n的取值为正整数。
1.2能级和能级跃迁氢原子的能级可以用公式E_n=-13.6eV/n^2来表示,其中E_n 是第n能级的能量,单位为电子伏特(eV)。
当电子从一个能级跃迁到另一个能级时,会吸收或发射一定频率的光子,这个频率与能级之间的能量差有关。
二、氢原子光谱的实验观测2.1光谱仪和光谱图氢原子光谱可以通过光谱仪进行观测。
光谱仪将入射光分解成不同频率的光谱线,并将这些光谱线投射到感光材料上,形成光谱图。
通过观察光谱图,可以得知氢原子的能级结构和光谱特性。
2.2巴尔末公式实验观测到的氢原子光谱线可以通过巴尔末公式来描述,公式为1/λ=R_H(1/n1^21/n2^2),其中λ是光谱线的波长,R_H是里德伯常数,n1和n2是两个能级的主量子数。
巴尔末公式可以准确地预测氢原子光谱线的位置。
三、氢原子光谱的理论解释3.1玻尔模型1913年,尼尔斯·玻尔提出了氢原子的量子理论模型,即玻尔模型。
该模型假设电子在氢原子中只能存在于特定的轨道上,每个轨道对应一个能级。
当电子从一个能级跃迁到另一个能级时,会吸收或发射一定频率的光子。
3.2量子力学解释1925年,海森堡、薛定谔和狄拉克等人发展了量子力学理论,为氢原子光谱提供了更为精确的解释。
量子力学认为,电子在氢原子中的状态可以用波函数来描述,波函数的平方表示电子在空间中的概率分布。
通过解薛定谔方程,可以得到氢原子的能级和波函数。
四、结论氢原子光谱是量子力学和原子物理学的基础内容,对于理解原子结构、光谱现象以及化学键的形成具有重要意义。
原子的能级分布和跃迁PPT课件
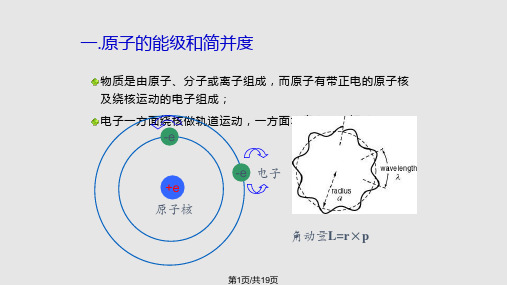
1s2 2s2 2 p6 3s
1s2 2s2 2 p6
这10原子称原子实。原子实以外 的电子称为价电子,可以被激发
n≥3的激发态的钠原子电子组态为
(1s2 2s2 2 p6 3p) (1s2 2s2 2 p6 3d) (1s2 2s2 2 p6 4s) 等等
第11页/共19页
4.原子态的标记
由于原子中电子的轨道角动量与自旋角动量之间的相互作 用,原子的同一电子组态可以形成不同的原子组态。(以两个 电子为例来说明)
对同一个 n ,角动量有n个不同的值但能量相同,代表
轨道的形状和轨道角动量,这也同电子的能量有关.对于l=0, 1,2,3等的电子顺次,依次用字母s、p、d、f 来表示,通常
称 s电子、p电子
3.
磁量子数
ml
( 0,±1, ± 2,……. , ± l )
Lz ml
代表轨道在空间的可能取向,即轨道角动量在某一特殊
一个原子内不可能有两个或两个以上的电子具有完全相同 的状态
或说 一个原子内不可能有四个量子数完全相同的电子 或说 不可能有两个或两个以上的电子处于同一个量子态 电子填充各壳层的次序是:
1s,2s,2p,3s,3p,4s,3d,4p,5s,4d,5p,6s…
第9页/共19页
2.能量最低原理 “电子优先占据最低能态”
则对应于电子的一种状态
每个状态用量子数 n , l , ml ms
来描述
1
第2页/共19页
能级: 粒子的内部能量值
高能级: 能量较高的能级 低能级: 能量较低的能级
基能级: 能量最低的能级
(相应的状态称基态) 激发能级: 能量高于基能
级的其它所有能级(相应 状态称激发态)
高考物理氢光谱和能级(PPT)4-2

迪什非常喜欢化学实验,有一次实验中,他不小心把一个铁片掉进了盐酸中,他正在为自己的粗心而懊恼时,却发现盐酸溶液中有气泡产生,这个情景一下 子吸引了他。他又做了几次实验,把一定量的锌和铁投到充足的盐酸和稀硫酸中(每次用的硫酸和盐酸的质量是不同的),发现所产生的气体量是固定不变 的。这说明这种新的气体的产生与所; 幼小衔接班加盟 幼小衔接班加盟 ; 用酸的种类没有关系,与酸的浓度也没有关系。 卡文迪什用排 水法收集了新气体,他发现这种气体不能帮助蜡烛的燃烧,也不能帮助动 氢气 氢气 物的呼吸,如果把它和空气混合在一起,一遇火星就会爆炸。卡文迪什 经过多次实验终于发现了这种新气体与普通空气混合后发生爆炸的极限。他在论文中写道:如果这种可燃性气体的含量在 .%以下或%以上,点火时虽然会燃 烧,但不会发出震耳的爆炸声。 随后不久他测出了这种气体的比重,接着又发现这种气体燃烧后的产物是水,无疑这种气体就是氢气了。卡文迪什的研究已
13-06-考点强化:氢原子能级及能级跃迁详解

第6页
返回目录
结束放映
【例 1】
[2015· 海南单科, 17(1)]氢原子基态的能量为 E1 =
- 13.6 eV。大量氢原子处于某一激发态。由这些氢原子可能发 出的所有的光子中,频率最大的光子能量为-0.96E1,频率最小 0.31
的光子的能量为
可具有 10
eV(保留两位有效数字),这些光子
种不同的频率。
解析 原子A从激发态E2 跃迁到E1,只辐射一种 频率的光子,A错.原子 B从激发态E3跃迁到基态 E1可能辐射三种频率的 光子,B对.由原子能级 跃迁理论可知,原子A可 能吸收原子B由E3跃迁到 E2时放出的光子并跃迁 到E3,但不能跃迁到E4, C错.A原子发出的光子 能量ΔE=E2-E1大于E4 -E3,故原子B不可能跃 迁到能级E4,D错. 解析显隐 答案 B
吸收一 定频率 的光子
释放 一定 频率 光子
3.电离 电离态与电离能 (1)电离态:n=∞,E=0 基态→电离态:E吸=0-(-13.6 eV)=13.6 eV电离能. n=2→电离态:E吸=0-E2=3.4 eV (2)如吸收能量足够大,克服电离能后,获得自由的电子还携带 动能.
2017版高三一轮物理教学实用课件
2017版高三一轮物理教学实用课件
第11页
返回目录
结束放映
规律方法
对原子跃迁条件的理解
(1)原子从低能级向高能级跃迁,吸收一定能量的光子.只有当一个光子的能 量满足 hν=E 末-E 初时, 才能被某一个原子吸收, 使原子从低能级 E 初向高 能级 E 末跃迁,而当光子能量 hν 大于或小于 E 末-E 初时都不能被原子吸收.
2017版高三一轮物理教学实用课件
第16页
返回目录
【物理】高考一轮专项复习名师精讲第五十一讲——氢原子能级

高三物理
第五十讲
氢原子能级、核物理
隔壁老王
1、阿尔法粒子散射实验
2、氢原子能级
核物理
1、天然放射现象:放射性元素自发的发出射线的现象
核物理
核物理
1、如图所示,A、B为平行金属板,两板相距为d,分别与电源两极相连,两板的中央各有一小孔M和N.今有一带电质点自A板上方相距为d的P点由静止自由下落(P、M、N在同一竖直线上),空气阻力忽略不计,到达N孔时速度恰好为零,然后沿原路返同.若保持两极板间的电压不变,则()
(A)把A板向上平移一小段距离,质点自P点自由下落后仍能返回
(B)把A板向下平移一小段距离,质点自P点自由下落后将穿过N孔继续下落
(C)把B板向上平移一小段距离,质点自P点自由下落后仍能返回
(D)把B板向下平移一小段距离,质点自P点自由下落后将穿过N孔继续下落
猿辅导物理老师王羽@微博
高中物理复习@贴吧
297073024@QQ
416926882。
课件2:4.4 第2课时 玻尔理论对氢光谱的解释 氢原子能级跃迁

的动能可部分地被原子吸收,所以只要入射粒子的能量大于两能级的能量差值
(E=En-Ek),就可使原子发生能级跃迁。
点睛:处于激发态的原子是不稳定的,它会自发地向较低能级跃迁,经过一次或
几次跃迁到达基态。
例4 玻尔首先提出能级跃迁,如图所示为氢原子的能级图,现有大量处于n=3能级
有可能向上跃迁到激发态,处于激发态的原子是不稳定的,会自发地向能量
较低的能级跃迁,放出光子,最终回到基态。
3. 解释氢原子光谱的不连续性
原子从较高能级向低能级跃迁时放出光子的能量等于前后两能级差,由
于原子的能级是分立的,所以放出的光子的能量也是分立的,因此原子的发
射光谱只有一些分立的亮线。
4. 解释不同原子具有不同的特征谱线
第四章
原子结构和波粒二象性
4 第2课时 玻尔理论对氢光谱的解释 氢原子能级跃迁
知识梳理
氢
原
子
n 量子数
∞
5
4
3
2
能
能级 E/eV
0
-0.54
-0.85
布喇开系
-1.51 激发态
帕邢系
巴耳末系
量子数
-3.4
n=3
n=2
级
图
莱曼系
1
电子
n=1
-
+
原子核
-13.6 基态
一、玻尔理论对氢光谱的解释
1. 解释巴耳末系公式
的氢原子向低能级跃迁,下列说法正确的是(
)
A.这些氢原子总共可辐射出6种不同频率的光子
B.氢原子由n=3能级跃迁到n=1能级产生的光波长最长
物理氢原子能级跃迁

物理氢原子能级跃迁
物理氢原子能级跃迁是指氢原子中电子从一个能级到另一个能级的过程。
当电子从高能级向低能级跃迁时,会释放出能量,这被称为辐射跃迁。
相反地,当电子从低能级向高能级跃迁时,需要吸收能量,这被称为吸收跃迁。
在氢原子中,电子的能级由主量子数n来确定。
当电子从一个能级n1跃迁到另一个能级n2时,它会释放或吸收一个光子,光子的能量等于两个能级之间的能量差。
这个过程可以用爱因斯坦的方程E=hν来描述,其中E是光子的能量,h是普朗克常数,ν是光子的频率。
氢原子的能级跃迁PPT课件 人教版

五、氢原子中的电子云 对于宏观质点,只要知道它在某一时刻的位置和速 度以及受力情况,就可以应用牛顿定律确定该质点 运动的轨道,算出它在以后任意时刻的位置和速度。 对电子等微观粒子,牛顿定律已不再适用,因此不 能用确定的坐标描述它们在原子中的位置。玻尔理 论中说的“电子轨道”实际上也是没有意义的。更 加彻底的量子理论认为,我们只能知道电子在原子 核附近各点出现的概率的大小。在不同的能量状态 下,电子在各个位置出现的概率是不同的。如果用 疏密不同的点子表示电子在各个位置出现的概率, 画出图来,就像一片云雾一样,可以形象地称之为 电子云。
( B )
∞
B.2
D.4
4 3 2
n
E(eV)
0 -0.85 -1.51
A.1
C.3
-3.40
1
-13.60
2007年理综全国卷Ⅰ 19 19. 用大量具有一定能量的电子轰击大量处于基态的 氢原子,观测到了一定数目的光谱线。调高电子的 能量再次进行规测,发现光谱线的数目比原来增加 了5条。用△n表示两次观测中最高激发态的量子数 n E(eV) 之差,E表示调高后电子的能量。 n -0.28 根据氢原子的能级图可以判断,
07年苏锡常镇四市二模8 2007年高考广东卷2 2007年重庆卷14 2007年物理海南卷19(1) 2007年理综全国卷Ⅱ18
一、玻尔的原子理论——三条假设 (1)“定态假设”:原子只能处于一系列不连续的能 量状态中,在这些状态中,电子虽做变速运动,但并不向外 辐射电磁波,这样的相对稳定的状态称为定态。 ( 2)“跃迁假设”:电子绕核转动处于定态时不辐射 电磁波,但电子在两个不同定态间发生跃迁时,却要辐 射(吸收)电磁波(光子),其频率由两个定态的能量 差值决定 。 hv=E2-E1 跃迁假设对发光(吸光) 从微观(原子等级)上给出了解释 (3)“轨道量子化假设”:由于能量状态的不连续, 因此电子绕核转动的轨道半径也不能任意取值,必须满 nh 足 mvr ( n 1 , 2 , 3 ) 2 轨道量子化假设把量子观念引入原子理论,这是玻尔的 原子理论之所以成功的根本原因。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
数字媒体资源库
解析 量子数小的轨道半径小,因此n=3的轨道比n=5的轨道
离核近;能级跃迁发射的谱线条数为C2n=C24=6条.
答案 近 6
解析显隐
第13页
返回目录
结束放映
数字媒体资源库
【典例3】 (2012·江苏,12C)如图所示是某原子的能级图,a、b、 c为原子跃迁所பைடு நூலகம்出的三种波长的光.在下列该原子光谱的各选 项中,谱线从左向右的波长依次增大,则正确的是( ). b光的能量最 小,波长最长
3.电离 电离态与电离能
吸收一 定频率 的光子
释放 一定 频率 光子
(1)电离态:n=∞,E=0
基态→电离态:E吸=0-(-13.6 eV)=13.6 eV电离能. n=2→电离态:E吸=0-E2=3.4 eV (2)如吸收能量足够大,克服电离能后,获得自由的电子还携带
动能.
第9页
返回目录
结束放映
数字媒体资源库
第6页
数字媒体资源库
返回目录
结束放映
原子物理知识结构
状元微博
数字媒体资源库
第7页
返回目录
结束放映
数字媒体资源库
氢原子能级及能级跃迁
1.能级图中相关量意义的说明
相关量
意义
能级图中的横线
表示氢原子可能的能量状 态——定态
横线左端的数字 “1,2,3…”
表示量子数
横线右端的数字“ -13.6,-3.4…”
所示,一群处在n=3能级的氢原子
向低能级跃迁时,能够从金属钾的
表面打出光电子的光波共有( ).
A.一种
B.两种
C.三种
D.四种
解析 要从金属钾的表面打审出题光视电角子,入射光的能量应大于钾的
逸能逸1逸2出级出..当因 因出功向功氢EE功,,32原1--2EE一因.能子2112==群此级e从11V20处选、高..时12在21eB能,Ve能.V级>即n>级=2向能2.向23.低22够2e能1能Ve从V能级,级金,级的能跃属能跃氢打迁钾打迁原出释表出时子光放面光发向电的打电出低子能出子的能;量光;光级大电子跃于子能迁金. 量时属大,钾于只的钾有的3
a光的能量最 大,波长最短
审题导析 1.两个能级间的能量差值越 大,辐射光的频率就越大, 其波长就越短 . 2.E3-E1>E2-E1>E3-E2
第3页
返回目录
结束放映
数字媒体资源库
二、氢原子光谱及能级 1.光谱 (1)光谱 用光栅或棱镜可以把光按波长展开, 获得光的__波__长___ (频率)和强度分布 的记录,即光谱. (2)光谱分类 有些光谱是多条_亮__线__,称为线状谱. 有些光谱是连在一块的_光__带__,称为 连续谱.
(3)氢原子光谱的实验规律 巴耳末线系是氢原子光谱在可见光区的谱线,其波长公式
答案因EB3-E2= 1.89eV < 2.22eV,不能打出光电子;
解析显隐
第12页
返回目录
结束放映
【典例2】 [2013·江苏单科,12C(2)]根据 玻尔原子结构理论,氦离子(He+)的能级图 如图所示.电子处在n=3轨道上比处在n= 5轨道上离氦核的距离__近___(选填“近” 或“远”).当大量He+处在n=4的激发态 时,由于跃迁所发射的谱线有__6___条.
表示氢原子的能量
相邻横线间 的距离
表示相邻的能量差,量子数 越大相邻的能量差越小,距
离越小
表示原子由较高能级向较
带箭头的竖线 低能级跃迁,原子跃迁的条
件为hγ=Em-En
第8页
返回目录
结束放映
数字媒体资源库
2.定态间的跃迁——满足能级差.
n小→n大吸收能量 hν=En大-En小. n大→n小放出能量 hν=En大-En小.
1λ=R212-n12 ,(n=3,4,5,…),
R是里德伯常量,R=1.10×107 m-1,n为量子数.
第4页
返回目录
结束放映
数字媒体资源库
2.玻尔理论 (1)定态:原子只能处于一系列_不__连__续___的能量状态中,在这些 能量状态中原子是__稳__定__的,电子虽然绕核运动,但并不向外 辐射能量. (2)跃迁:原子从一种定态跃迁到另一种定态时,它辐射或吸收 一定频率的光子,光子的能量由这两个定态的能量差决定,即 hν=__E_m_-__E_n_.(h是普朗克常量,h=6.63×10-34 J·s) (3)轨道:原子的不同能量状态跟电子在不同的圆周轨道绕核运 动相对应.原子的定态是__不__连__续___的, 因此电子的可能轨道也是__不__连__续__的.
入射光子和入射电子的区别: 若是在光子的激发下引起原子跃迁,则要求光子的能量必须 等于原子的某两个能级差; 若是在电子的碰撞下引起的跃迁,则要求电子的能量必须大 于或等于原子的某两个能级差.
第10页
返回目录
结束放映
数字媒体资源库
➢2. 典例剖析
第11页
返回目录
结束放映
数字媒体资源库
【典例1】已知金属钾的逸出功为2.22 eV,氢原子的能级如图
第5页
返回目录
结束放映
3.氢原子的能级、能级公式 (1)氢原子的能级 能级图如图所示 (2)氢原子的能级和轨道半径 ①氢原子的能级公式: En=E1/n2 (n=1,2,3,…), 其中E1为__基__态__能__量___,其数 值为E1=-13.6 eV. ②氢原子的半径公式: rn=n2r1 (n=1,2,3,…),其 中r1为___基__态__半__径____,又称 玻尔半径,其数值为 r1= 0.53×10-10 m.
选修3-5 动量守恒 波粒二相性 原子结构与原子核
考点强化: 氢原子能级及能级跃迁
➢ 1.考点精讲 ➢ 2.典例剖析 ➢ 3.规律方法 ➢ 4.跟踪训练 ➢ 5.真题演练
数字媒体资源库
➢1.考点精讲
第2页
返回目录
结束放映
数字媒体资源库
一、原子的核式结构 1.电子的发现:英国物理学家__汤__姆__孙___发现了电子. 2.α粒子散射实验:1909~1911年,英国物理学家__卢__瑟__福__和他的助 手进行了用α粒子轰击金箔的实验,实验发现绝大多数α粒子穿过金箔 后基本上仍沿__原__来__方向前进,但有少数α粒子发生了大角度偏转, 偏转的角度甚至大于90°,也就是说它们几乎被“撞”了回来. 3.原子的核式结构模型:在原子中心有一个很小的核,原子全部的 _正__电__荷___和几乎全部__质__量___都集中在核里,带负电的电子在核外空间 绕核旋转.
