化学反应速率化学动力学简史与诺贝尔化学奖1850威廉
诺贝尔化学奖得主及获奖理由盘点

诺贝尔化学奖得主及获奖理由盘点文件管理序列号:[K8UY-K9IO69-O6M243-OL889-F88688]得主及获奖理由盘点诺贝尔化学奖是以瑞典着名化学家、硝化甘油炸药发明人阿尔弗雷德·贝恩哈德·诺贝尔(1833-1896)的部分遗产作为基金创立的5项奖金之一。
诺贝尔化学奖由瑞典皇家科学院从1901年开始负责颁发,总共被颁发了107次。
期间只有1916、1917、1919、1924、1933、1940、1941和1942八年没有颁发。
诺贝尔奖奖项空缺,除了受到两次世界大战影响之外,还受到了诺贝尔奖组委会“宁缺毋滥”的评奖理念的影响。
到目前为止,诺贝尔化学奖共有172位获奖者。
其中英国生物化学家弗雷德里克·桑格(FrederickSanger)在1958年和1980年两次获得诺贝尔奖,因此历史上获得诺贝尔奖的总共只有171人。
诺贝尔化学奖获奖者的平均年龄是58岁。
其中有32人获奖年龄介于50岁和54岁之间,几乎占到了总获奖人数的20%。
历届诺贝尔化学奖得主及其获奖原因1901年--1910年1901年:雅克布斯范特霍夫(荷)发现了化学动力学法则和溶液渗透压。
1902年:赫尔曼费歇尔(德)合成了糖类和嘌呤衍生物。
1903年:阿累尼乌斯(瑞典)提出了电离理论,促进了化学的发展。
1904年:威廉拉姆齐爵士(英)发现了空气中的稀有气体元素,并确定他们在周期表里的位置。
1905年:阿道夫拜耳(德)对有机染料以及氢化芳香族化合物的研究促进了有机化学与化学工业的发展。
1906年:穆瓦桑(法)研究并分离了氟元素,并且使用了后来以他名字命名的电炉。
1907年:爱德华毕希纳(德)对酶及无细胞发酵等生化反应的研究。
1908年:欧内斯特卢瑟福爵士(新西兰)对元素的蜕变以及放射化学的研究。
1909年:威廉奥斯特瓦尔德(德)对催化作用,化学平衡以及化学反应速率的研究。
1910年—1919年1910年:奥托瓦拉赫(德)在脂环类化合物领域的开创性工作促进了有机化学和化学工业的发展的研究。
1909年诺贝尔化学奖

【1909年诺贝尔化学奖】
物理化学之父
湖北省石首市文峰中学刘涛 434400
1909年诺贝尔化学奖授予德国物理化学家威廉•奥斯特瓦尔德,以表彰他在催化剂的作用、化学平衡、化学反应速率方面研究的突出贡献。
奥斯特瓦尔德主要从事化学反应动力学研究。
1888年提出了稀释定律,并通过大量实验数据进行了验证,还将质量作用定律应用于电解质的电离,引入了离解常数和溶度积概念,这些定律和概念对物理化学的学科发展有着重要作用。
1891年又使用电离理论成功解释了酸碱指示剂的原理。
1900年左右对溶液粘度性质的测量时,发明了奥斯特瓦尔德黏度计,至今仍然被广泛使用。
1901年发表了现代催化剂概念,将化学热力学原理引入结晶学和催化现象的研究中,对大量现象给予了解释,并成功完成了催化剂的工业应用。
1902年提出奥斯特瓦尔德过程,成功地使氨在铂上氧化转变成一氧化氮,研制成用氨制硝酸并获得专利,具有重大的工业价值,为现代硝酸工业化发展奠定了基础。
他一直坚持结合物理手段与化学分析来进行科学研究,创办了世界第一种物理化学期刊,努力将物理化学从有机化学和分析化学中独立出来,使得物理化学得以成为一门独立的科学和其他化学的理论基础,从此以后,物理化学这一分支学科开始形成和发展,由于一生对物理化学学科的建立作出了重要贡献,认为他是古典物理化学的创立者之一,后人常尊称奥斯特瓦尔德为“物理化学之父”。
化学动力学简史与诺贝尔化学奖精编

化学动力学简史与诺贝尔化学奖精编Document number:WTT-LKK-GBB-08921-EIGG-22986一、化学动力学简史与诺贝尔化学奖1850威廉米(Ludwig Ferdinand Wilhelmy, 1812-1864, 德国物理学家) 研究在酸性条件下蔗糖分解(水解为D-(+)-果糖和D-(-)-果糖)的反应速率,发现反应速率正比于蔗糖和酸的浓度。
1864古德博格(Cato Maximillian Guldberg, 1836-1902, 挪威数学家,理论化学家) 和瓦格(Peter Waage, 1833-1900,挪威化学家) 给出“质量作用定律”的公式。
按照这个公式,反应“推动力”正比于反应物浓度的乘积:K=[R]r[S]s/([A]a [B]b)其中,a, b, r, s分别为化学反应A+B = R+S的整比系数。
因此,前向反应速率正比于[A]a [B]b,而后向反应速率整比于[R]r [S]s。
1865Harcourt 和 Esson (英) 分析了 H2O2和 HI、KMnO4和(COOH)2的反应。
他们写出了相应的微分方程,通过积分得到浓度-时间关系。
他们也提出了反应速率与温度的关系式k = A T C1884范特霍夫(Jacobus Henricus van’t Hoff,1852-1911, 荷兰物理化学家。
提出碳原子价键的空间结构学说;提出稀溶液理论。
)的《化学动力学研究》(“Studies of Chemical Dynamics”,“études de dynamique chimique”)出版。
在这本书中,van’tHoff 推广和继续发展了Wilhelmy, Harcourt 和Esson 的工作。
特别是,他引入了微分解析方法。
他也分析了平衡常数以及正向、反向反应速度与温度的依赖关系。
(平衡常数与温度的关系现在称为van’t Hoff 方程)。
化学反应速率化学动力学简史与诺贝尔化学奖1850威廉

首页→第七章化学反应速率一、化学动力学简史与诺贝尔化学奖1850威廉米(Ludwig Ferdinand Wilhelmy, 1812-1864, 德国物理学家) 研究在酸性条件下蔗糖分解(水解为D-(+)-果糖和D-(-)-果糖)的反应速率,发现反应速率正比于蔗糖和酸的浓度。
1864古德博格(Cato Maximillian Guldberg, 1836-1902, 挪威数学家,理论化学家) 和瓦格(Peter Waage, 1833-1900,挪威化学家) 给出“质量作用定律”的公式。
按照这个公式,反应“推动力”正比于反应物浓度的乘积:K=[R]r [S]s/([A]a [B]b)其中,a, b, r, s分别为化学反应A+B = R+S的整比系数。
因此,前向反应速率正比于[A]a[B]b,而后向反应速率整比于[R]r [S]s。
1865Harcourt 和Esson (英) 分析了H2O2和HI、KMnO4和(COOH)2的反应。
他们写出了相应的微分方程,通过积分得到浓度-时间关系。
他们也提出了反应速率与温度的关系式k = A T C1884范特霍夫(Jacobus Henricus van’t Hoff, 1852-1911, 荷兰物理化学家。
提出碳原子价键的空间结构学说;提出稀溶液理论。
)的《化学动力学研究》(“Studies of Chemical Dynamics”,“Études de dynamique chimique”)出版。
在这本书中,van’t Hoff 推广和继续发展了Wilhelmy, Harcourt 和Esson 的工作。
特别是,他引入了微分解析方法。
他也分析了平衡常数以及正向、反向反应速度与温度的依赖关系。
(平衡常数与温度的关系现在称为van’t Hoff 方程)。
van’t Hoff由于对化学动力学和溶液渗透压的首创性研究而荣获了1901年的首届诺贝尔化学奖1887奥斯特瓦尔德(Wilhelm Ostwald, 1853-1932, 生于拉脱维亚的德国化学家,唯能论者。
化学反应动力学的发展和应用

化学反应动力学的发展和应用化学反应动力学是研究化学反应机理和速率的学科,是化学的基础。
随着科技的不断发展,化学反应动力学也不断发展,并应用于各个领域。
本文将探讨化学反应动力学的发展和应用。
一、化学反应动力学的发展化学反应动力学理论的起源可以追溯到19世纪下半叶。
瑞士化学家H. Wurtz在1850年提出了某些反应需要时间才能完成的想法,这标志着化学反应动力学的诞生。
此后,许多化学家在这个领域做出了巨大贡献,如瑞典化学家Arrhenius在1889年提出了Arrhenius方程,用于描述温度对反应速率的影响。
紧接着,荷兰物理学家Vant Hoff在1897年引入了化学动力学的热力学理论,这使得化学反应动力学有了更加深入的研究。
20世纪初期,英国化学家Brönsted和德国化学家Lowry提出了酸碱理论,这奠定了化学反应动力学的基础。
此外,地球化学家Urey还建立了正电子电离器质谱法,该方法能够揭示化学反应的分子机制。
这些成果促进了化学反应动力学的发展。
20世纪中期,芝加哥大学化学家Pauling提出了量子力学的概念,从而深化了化学反应动力学的理论。
随后,美国化学家Marcus提出了热电子迁移理论,用于解释电子传递反应。
此外,化学家们还研究了各种反应动力学模型,如扩散反应模型、催化反应模型等。
二、化学反应动力学的应用1、工业生产化学反应动力学在工业生产中有着广泛的应用。
例如,在合成水合肼的过程中,需要控制反应速率,使得反应能够充分完成并且副产物产生率尽可能小。
此时,化学反应动力学可以提供工业界所需的反应条件,如温度、压力、反应物物质浓度等。
此外,石油工业中的各种化学反应也需要掌握动力学性质。
当我们需要提高石油转化率或者降低催化剂的消耗时,就需要深入了解化学反应动力学。
2、环保和食品工业化学反应动力学在环保和食品工业中也有所应用。
例如,在水处理中,了解化学反应动力学可以帮助我们控制水质,加速水中污染物的分解和降解。
历年诺贝尔化学奖汇总.

从事分子内原子化合价的研究
致力于原子量的研究,精确地测 定 了许多元素的原子量
1915 R. 威尔斯泰特(德国人) 1916---1917年 未颁奖 1918 F. 哈伯(德国人) 1919年 未颁奖
从事植物色素(叶绿素国人) 从事电化学和热动力学方面的研究
1926 T. 斯韦德贝里(瑞典人) 从事胶体化学中分散系统的研究
1927 H.O. 维兰德(德国人)
研究确定了胆酸及多种同类物质的化学 结构
1928 A. 温道斯(德国人)
研究出一族甾醇及其与维生素的关系
1929 A. 哈登(英国人) 冯·奥伊勒 - 歇尔平(瑞典人) 阐明了糖发酵过程和酶的作用
1930 1931
西蒙诺夫【苏联】(N.N.Semyonov) 对动力学理论和链反应的研究
1957 塔德【英国】(A.R.Todd)
对核苷酸和核苷酸辅酶等的研究
1958 桑格【英国】(F.Sanger)
确定了胰岛素的分子结构
1959 海洛夫斯基【捷克斯洛伐克】 (H.Heyrovsk)
发明并改进极谱分析法
1960 W.F. 利时(美国人)
1932 1933 1934 1935
1936 1937
1938 1939
H. 非舍尔(德国人)
从事血红素和叶绿素的性质及结构方面的研究
C. 博施(德国人) F.贝吉乌斯 (德国人)
发明和开发了高压化学方法
I. 兰米尔 (美国人)
创立了表面化学
未颁奖
H.C. 尤里(美国人)
发现重氢
J.F.J. 居里 I.J. 居里(法国人)
1950 O.P.H. 狄尔斯、K.阿尔德(德国人) 发现狄尔斯 - 阿尔德反应及其应 用
历届诺贝尔化学奖得主(1901-2014)

历届诺贝尔化学奖得主 (1901-2014)年份获奖者 国籍 获奖原因 1901年 雅各布斯·亨里克斯·范托夫荷兰 “发现了化学动力学法则和溶液渗透压” 1902年 赫尔曼·费歇尔 德国“在糖类和嘌呤合成中的工作” 1903年 斯凡特·奥古斯特·阿伦尼乌斯瑞典 “提出了电离理论” 1904年 威廉·拉姆齐爵士英国 “发现了空气中的惰性气体元素并确定了它们在元素周期表里的位置” 1905年 阿道夫·冯·拜尔德国 “对有机染料以及氢化芳香族化合物的研究促进了有机化学与化学工业的发展” 1906年 亨利·莫瓦桑法国 “研究并分离了氟元素,并且使用了后来以他名字命名的电炉” 1907年 爱德华·比希纳德国 “生物化学研究中的工作和发现无细胞发酵” 1908年 欧内斯特·卢瑟福英国 “对元素的蜕变以及放射化学的研究” 1909年 威廉·奥斯特瓦尔德德国 “对催化作用的研究工作和对化学平衡以及化学反应速率的基本原理的研究” 1910年 奥托·瓦拉赫德国 “在脂环族化合物领域的开创性工作促进了有机化学和化学工业的发展的研究” 1911年 玛丽·居里波兰 “发现了镭和钋元素,提纯镭并研究了这种引人注目的元素的性质及其化合物” 1912年 维克多·格林尼亚 法国 “发明了格氏试剂” 保罗·萨巴捷法国 “发明了在细金属粉存在下的有机化合物的加氢法” 1913年 阿尔弗雷德·维尔纳瑞士 “对分子内原子连接的研究,特别是在无机化学研究领域” 1914年 西奥多·威廉·理查兹美国 “精确测定了大量化学元素的原子量” 1915年 里夏德·维尔施泰特德国 “对植物色素的研究,特别是对叶绿素的研究” 1916年 未颁奖1917年 未颁奖1918年 弗里茨·哈伯德国 “对从单质合成氨的研究” 1919年 未颁奖1920年 瓦尔特·能斯特德国 “对热化学的研究” 1921年 弗雷德里克·索迪英国 “对人们了解放射性物质的化学性质上的贡献,以及对同位素的起源和性质的研究” 1922年 弗朗西斯·阿斯顿英国 “使用质谱仪发现了大量非放射性元素的同位素,并且阐明了整数法则” 1923年 弗里茨·普雷格尔奥地利 “创立了有机化合物的微量分析法” 1924年 未颁奖1925年 里夏德·阿道夫·席格蒙迪 德国“阐明了胶体溶液的异相性质,并创立了相关的分析法” 1926年 特奥多尔·斯韦德贝里 瑞典 “对分散系统的研究”1927年 海因里希·奥托·威兰 德国 “对胆汁酸及相关物质的结构的研究”1928年 阿道夫·温道斯 德国 “对甾类的结构以及它们和维他命之间的关系的研究”1929年 阿瑟·哈登 英国 “对糖类的发酵以及发酵酶的研究” 汉斯·冯·奥伊勒-切尔平 德国1930年 汉斯·费歇尔 德国 “对血红素和叶绿素的组成的研究,特别是对血红素的合成的研究”1931年 卡尔·博施 德国 “发明与发展化学高压技术” 弗里德里希·贝吉乌斯 德国1932年 欧文·兰米尔 美国 “对表面化学的研究与发现”1933年 未颁奖1934年 哈罗德·克莱顿·尤里 美国 “发现了重氢”1935年 弗雷德里克·约里奥-居里 法国 “合成了新的放射性元素” 伊伦·约里奥-居里 法国1936年 彼得·德拜 荷兰 “通过对偶极矩以及气体中的X 射线和电子的衍射的研究来了解分子结构”1937年 沃尔特·霍沃思 英国 “对碳水化合物和维生素C 的研究”保罗·卡勒 瑞士 “对类胡萝卜素、黄素、维生素A 和维生素B2的研究”1938年 里夏德·库恩 德国 “对类胡萝卜素和维生素的研究”1939年 阿道夫·布特南特 德国 “对性激素的研究” 拉沃斯拉夫·鲁日奇卡 瑞士 “对聚亚甲基和高级萜烯的研究”1940年 未颁奖1941年 未颁奖1942年 未颁奖1943年 乔治·德海韦西 匈牙利 “在化学过程研究中使用同位素作为示踪物” 1944年 奥托·哈恩 德国 “发现重核的裂变”1945年 阿尔图里·伊尔马里·维尔塔宁 芬兰 “对农业和营养化学的研究发明,特别是提出了饲料储藏方法”1946年 詹姆斯·B·萨姆纳 美国 “发现了酶可以结晶”约翰·霍华德·诺思罗普 美国 “制备了高纯度的酶和病毒蛋白质” 温德尔·梅雷迪思·斯坦利 美国1947年 罗伯特·鲁宾逊爵士 英国 “对具有重要生物学意义的植物产物,特别是生物碱的研究”1948年 阿尔内·蒂塞利乌斯 瑞典 “对电泳现象和吸附分析的研究,特别是对于血清蛋白的复杂性质的研究”1949年 威廉·吉奥克 美国 “在化学热力学领域的贡献,特别是对超低温状态下的物质的研究”1950年 奥托·迪尔斯 西德 “发现并发展了双烯合成法” 库尔特·阿尔德 西德1951年 埃德温·麦克米伦 美国 “发现了超铀元素” 格伦·西奥多·西博格 美国1952年 阿彻·约翰·波特·马丁 英国 “发明了分配色谱法” 理查德·劳伦斯·米林顿·辛英国格1953年 赫尔曼·施陶丁格 西德 “在高分子化学领域的研究发现”1954年 莱纳斯·鲍林 美国 “对化学键的性质的研究以及在对复杂物质的结构的阐述上的应用”1955年 文森特·迪维尼奥 美国 “对具有生物化学重要性的含硫化合物的研究,特别是首次合成了多肽激素”1956年 西里尔·欣谢尔伍德爵士 英国 “对化学反应机理的研究” 尼古拉·谢苗诺夫 苏联1957年 亚历山大·R·托德男爵 英国 “在核苷酸和核苷酸辅酶研究方面的工作”1958年 弗雷德里克·桑格 英国 “对蛋白质结构组成的研究,特别是对胰岛素的研究”1959年 雅罗斯拉夫·海罗夫斯基 捷克 “发现并发展了极谱分析法”1960年 威拉得·利比 美国 “发展了使用碳14同位素进行年代测定的方法,被广泛使用于考古学、地质学、地球物理学以及其他学科”1961年 梅尔文·卡尔文 美国 “对植物吸收二氧化碳的研究”1962年 马克斯·佩鲁茨 英国 “对球形蛋白质结构的研究” 约翰·肯德鲁 英国1963年 卡尔·齐格勒 西德 “在高聚物的化学性质和技术领域中的研究发现” 居里奥·纳塔 意大利1964年 多萝西·克劳福特·霍奇金 英国 “利用X 射线技术解析了一些重要生化物质的结构” 1965年 罗伯特·伯恩斯·伍德沃德 美国 “在有机合成方面的杰出成就”1966年 罗伯特·S·马利肯 美国 “利用分子轨道法对化学键以及分子的电子结构所进行的基础研究”1967年 曼弗雷德·艾根 西德“利用很短的能量脉冲对反应平衡进行扰动的方法,对高速化学反应的研究”罗纳德·乔治·雷伊福特·诺里什 英国 乔治·波特 英国1968年 拉斯·昂萨格 美国 “发现了以他的名字命名的倒易关系,为不可逆过程的热力学奠定了基础”1969年 德里克·巴顿 英国 “发展了构象的概念及其在化学中的应用” 奥德·哈塞尔 挪威1970年 卢伊斯·弗德里科·莱洛伊尔 阿根廷 “发现了糖核苷酸及其在碳水化合物的生物合成中所起的作用”1971年 格哈德·赫茨贝格 加拿大 “对分子的电子构造与几何形状,特别是自由基的研究”1972年 克里斯蒂安·B·安芬森 美国 “对核糖核酸酶的研究,特别是对其氨基酸序列与生物活性构象之间的联系的研究” 斯坦福·摩尔 美国 “对核糖核酸酶分子的活性中心的催化活性与其化学结构之间的关系的研究”威廉·霍华德·斯坦 美国 1973年 恩斯特·奥托·菲舍尔 西德 “对金属有机化合物,又被称为夹心化合物,的化学性质的开创性研究”杰弗里·威尔金森 英国 1974年 保罗·弗洛里 美国 “高分子物理化学的理论与实验两个方面的基础研究”1975年 约翰·康福思 英国 “酶催化反应的立体化学的研究” 弗拉迪米尔·普雷洛格瑞士 “有机分子和反应的立体化学的研究” 1976年 威廉·利普斯科姆 美国 “对硼烷结构的研究,解释了化学成键问题”1977年 伊利亚·普里高津 比利时 “对非平衡态热力学的贡献,特别是提出了耗散结构的理论”1978年 彼得·米切尔 英国 “利用化学渗透理论公式,为了解生物能量传递作出贡献”1979年 赫伯特·布朗 美国 “分别将含硼和含磷化合物发展为有机合成中的重要试剂”格奥尔格·维蒂希 西德 1980年 保罗·伯格 美国 “对核酸的生物化学研究,特别是对重组DNA 的研究” 沃特·吉尔伯特 美国 “对核酸中DNA 碱基序列的确定方法” 弗雷德里克·桑格 英国1981年 福井谦一 日本 “通过他们各自独立发展的理论来解释化学反应的发生”罗德·霍夫曼 美国 1982年 阿龙·克卢格 英国 “发展了晶体电子显微术,并且研究了具有重要生物学意义的核酸-蛋白质复合物的结构”1983年 亨利·陶布 美国 “对特别是金属配合物中电子转移反应机理的研究”1984年 罗伯特·布鲁斯·梅里菲尔德美国 “开发了固相化学合成法” 1985年 赫伯特·豪普特曼 美国 “在发展测定晶体结构的直接法上的杰出成就” 杰尔姆·卡尔 美国1986年 达德利·赫施巴赫 美国“对研究化学基元反应的动力学过程的贡献” 李远哲 中国台湾约翰·查尔斯·波拉尼 加拿大1987年 唐纳德·克拉姆 美国 “发展和使用了可以进行高选择性结构特异性相互作用的分子” 让-马里·莱恩 法国 查尔斯·佩德森 美国1988年 约翰·戴森霍费尔 西德“对光合反应中心的三维结构的测定”罗伯特·胡贝尔 西德 哈特穆特·米歇尔 西德1989年 悉尼·奥尔特曼 加拿大 “发现了RNA 的催化性质” 托马斯·切赫 美国1990年 艾里亚斯·詹姆斯·科里 美国 “发展了有机合成的理论和方法学”1991年 理查德·恩斯特 瑞士 “对开发高分辨率核磁共振(NMR )谱学方法的贡献” 1992年 鲁道夫·马库斯 美国 “对化学体系中电子转移反应理论的贡献”1993年 凯利·穆利斯 美国 “发展了以DNA 为基础的化学研究方法,开发了聚合酶链锁反应(PCR )”迈克尔·史密斯 加拿大 “发展了以DNA 为基础的化学研究方法,对建立寡聚核苷酸为基础的定点突变及其对蛋白质研究的发展的基础贡献”1994年 乔治·安德鲁·欧拉 美国 “对碳正离子化学研究的贡献”1995年 保罗·克鲁岑 荷兰 “对大气化学的研究,特别是有关臭氧分解的研究”马里奥·莫利纳美国 弗兰克·舍伍德·罗兰美国 1996年 罗伯特·柯尔美国 “发现富勒烯” 哈罗德·克罗托爵士英国 理查德·斯莫利美国 1997年 保罗·博耶美国 “阐明了三磷酸腺苷(ATP )合成中的酶催化机理” 约翰·沃克英国 延斯·克里斯蒂安·斯科丹麦 1998年 沃尔特·科恩 美国 “创立了密度泛函理论” 约翰·波普英国 发展了量子化学中的计算方法 1999年 亚米德·齐威尔埃及 “用飞秒光谱学对化学反应过渡态的研究” 2000年 艾伦·黑格美国 “发现和发展了导电聚合物” 艾伦·麦克德尔米德美国 白川英树日本 2001年 威廉·斯坦迪什·诺尔斯美国 “对手性催化氢化反应的研究”野依良治日本 巴里·夏普莱斯美国 “对手性催化氧化反应的研究” 2002年约翰·贝内特·芬恩美国 “发展了对生物大分子进行鉴定和结构分析的方法,建立了软解析电离法对生物大分子进行质谱分析” 田中耕一日本 库尔特·维特里希 瑞士 “发展了对生物大分子进行鉴定和结构分析的方法,建立了利用核磁共振谱学来解析溶液中生物大分子三维结构的方法”2003年 彼得·阿格雷 美国 “对细胞膜中的离子通道的研究,发现了水通道” 罗德里克·麦金农 美国 “对细胞膜中的离子通道的研究,对离子通道结构和机理的研究”2004年 阿龙·切哈诺沃 以色列“发现了泛素介导的蛋白质降解”阿夫拉姆·赫什科 以色列 欧文·罗斯 美国2005年 伊夫·肖万 法国“发展了有机合成中的复分解法”罗伯特·格拉布 美国 理查德·施罗克 美国2006年 罗杰·科恩伯格 美国 “对真核转录的分子基础的研究” 2007年 格哈德·埃特尔 德国 “对固体表面化学进程的研究”2008年 下村脩 美国“发现和改造了绿色荧光蛋白(GFP )”马丁·查尔菲 美国 钱永健 美国2009年 文卡特拉曼·拉马克里希南 英国 “对核糖体结构和功能方面的研究” 托马斯·施泰茨 美国阿达·约纳特 以色列2010年 理查德·赫克 美国“对有机合成中钯催化偶联反应的研究”根岸英一 日本 铃木章 日本2011年 丹·谢赫特曼 以色列 “准晶体的发现”2012年罗伯特·莱夫科维茨[2]美国“对G蛋白偶联受体的研究”2013年马丁·卡普拉斯美国[3]给复杂化学体系设计了多尺度模型[4]迈克尔·莱维特亚利耶·瓦谢尔2014年埃里克·白兹格(EricBetzig)美国“在超分辨率荧光显微技术领域取得的成就”威廉姆·艾斯科·莫尔纳尔(William E. Moerner)美国斯特凡·W·赫尔(Stefan W.Hell)德国。
历年诺贝尔化学奖获得者1901-2005
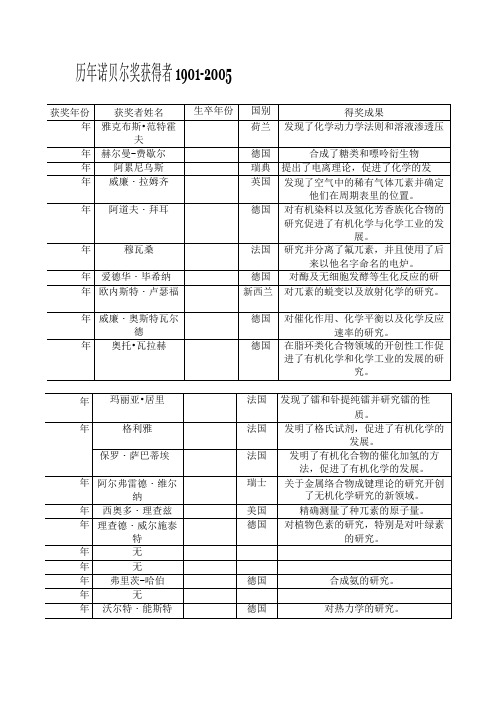
玛丽亚•居里
法国
发现了镭和钋提纯镭并研究镭的性
质。
年
格利雅
法国
发明了格氏试剂,促进了有机化学的发展。
保罗・萨巴蒂埃
法国
发明了有机化合物的催化加氢的方法,促进了有机化学的发展。
年
阿尔弗雷德・维尔纳
瑞士
关于金属络合物成键理论的研究开创了无机化学研究的新领域。
年
西奥多・理查兹
美国
精确测量了种兀素的原子量。
年
理查德・威尔施泰特
德国
对植物色素的研究,特别是对叶绿素的研究。
年
无
年
无
年
弗里茨-哈伯
德国
合成氨的研究。
年
无
年
沃尔特・能斯特
德国
对热力学的研究。
年
弗雷德里克・索迪
英国
对放射性物质以及同位素的研究。
年
弗朗西斯・阿斯顿
英国
使用质谱仪发现了非放射性兀素的同位素并且阐明了整数法则。
年
弗里茨•普雷格尔
奥地利
创立了有机化合物微量分析法。
保罗・博耶
美国
阐明了三磷酸腺苷合成酶的机理。
约翰•沃克尔1
英国
年
沃特•科恩
美籍奥地利
密度泛函理论的研究
约翰•波普
英国
量子化学计算方法的研究
年
艾哈迈德・兹韦勒
美籍埃及
用飞秒激光光谱对化学反应中间过程的研究
年
艾伦-黑格
美国
对导电聚合物的研究
艾伦•马克迪尔米德
美国
白川英树
日本
年
威廉・诺尔斯
美国
手性催化还原反应
梅尔温・卡尔文
诺贝尔化学奖

2021/5/18
7
另外他还提出了两个至今常用的概念: 一、奥斯特瓦尔德规则 二、奥斯瓦尔德熟化(Ostwald Ripening )
奥斯特瓦尔德熟化的基本表示
2021/5/18
8
催化现象的研究
除了电离理论、溶液的依数性和结晶学以外,奥斯特瓦尔德 还是催化现象研究的开创者。
1902年提出了著名的奥斯特瓦尔德过程,即氨气通过催化剂 (例如铂)作用被氧化生成一氧化氮,一氧化氮在空气中氧化为 二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,生成的一氧 化氮可以重新利用。这一过程实际上在1838 年就已经被人申请了 专利,但是当时还无法获得大量的氨气作为原料,所以只有学术 上的意义。奥斯特瓦尔德遇到了类似的困难,直到1908年左右他 获知了德国化学家弗里茨·哈伯等人的合成氨工艺,才将这一制取 硝酸的方法工业化,这一方法使得肥料和炸药的产量大量的增加 ,正如奥斯特瓦尔德自己所说的“工业的关键在于催化剂的使用” ,但这一方法也被德国用于生产第一次世界大战中所需的炸药。 后来这一过程后来经过奥斯特瓦尔德的学生马克斯·博登斯坦( Max Bodenstein)等人的的改进,一直广泛应用。
2021/5/18
9
能量学
1887年奥斯特瓦尔德初任莱比锡大学教 授时候的演讲的题目是“能量与其转变”,当 时他的结论是物理化学对能量的研究可以 补充其他化学对物质的研究,但1891年左 右他开始形成了他的“能量学”(energetics )概念,认为能量是唯一真实的实在,物 质并不是能量的负载者,而只是能量的表 现形式。1895年他在德国吕贝克自然科学 家会议上发表了“克服科学的唯物论”的讲演 ,这是他公开反对原子论的宣言,当即遭 到主张原子论的路德维希·玻耳兹曼的激烈 反对。自此奥斯特瓦尔德和恩斯特·马赫成 为对原子假设持怀疑态度的代表,和玻耳 兹曼、马克斯·普朗克等人产生了长期的论 战。中国大陆因为受到意识形态的影响, 按照列宁的观点把他的能量学称为”唯能论” ,并将这一论战描述成唯心与唯物的斗争。
诺贝尔化学奖得主(1901-2020)

诺贝尔化学奖得主 (1901-2020)年份获奖者 国籍 获奖原因 1901年 雅各布斯·亨里克斯·范托夫荷兰 “发现了化学动力学法则和溶液渗透压” 1902年 赫尔曼·费歇尔 德国“在糖类和嘌呤合成中的工作” 1903年 斯凡特·奥古斯特·阿伦尼乌斯瑞典 “提出了电离理论” 1904年 威廉·拉姆齐爵士英国 “发现了空气中的惰性气体元素并确定了它们在元素周期表里的位置” 1905年 阿道夫·冯·拜尔德国 “对有机染料以及氢化芳香族化合物的研究促进了有机化学与化学工业的发展” 1906年 亨利·莫瓦桑法国 “研究并分离了氟元素,并且使用了后来以他名字命名的电炉” 1907年 爱德华·比希纳德国 “生物化学研究中的工作和发现无细胞发酵” 1908年 欧内斯特·卢瑟福英国 “对元素的蜕变以及放射化学的研究” 1909年 威廉·奥斯特瓦尔德德国 “对催化作用的研究工作和对化学平衡以及化学反应速率的基本原理的研究” 1910年 奥托·瓦拉赫德国 “在脂环族化合物领域的开创性工作促进了有机化学和化学工业的发展的研究” 1911年 玛丽·居里波兰 “发现了镭和钋元素,提纯镭并研究了这种引人注目的元素的性质及其化合物” 1912年 维克多·格林尼亚 法国 “发明了格氏试剂” 保罗·萨巴捷法国 “发明了在细金属粉存在下的有机化合物的加氢法” 1913年 阿尔弗雷德·维尔纳瑞士 “对分子内原子连接的研究,特别是在无机化学研究领域” 1914年 西奥多·威廉·理查兹美国 “精确测定了大量化学元素的原子量” 1915年 里夏德·维尔施泰特德国 “对植物色素的研究,特别是对叶绿素的研究” 1916年 未颁奖1917年 未颁奖1918年 弗里茨·哈伯德国 “对从单质合成氨的研究” 1919年 未颁奖1920年 瓦尔特·能斯特德国 “对热化学的研究” 1921年 弗雷德里克·索迪英国 “对人们了解放射性物质的化学性质上的贡献,以及对同位素的起源和性质的研究” 1922年 弗朗西斯·阿斯顿英国 “使用质谱仪发现了大量非放射性元素的同位素,并且阐明了整数法则” 1923年 弗里茨·普雷格尔奥地利 “创立了有机化合物的微量分析法” 1924年 未颁奖1925年 里夏德·阿道夫·席格蒙迪 德国“阐明了胶体溶液的异相性质,并创立了相关的分析法” 1926年 特奥多尔·斯韦德贝里瑞典 “对分散系统的研究”1927年 海因里希·奥托·威兰 德国 “对胆汁酸及相关物质的结构的研究”1928年 阿道夫·温道斯 德国 “对甾类的结构以及它们和维他命之间的关系的研究”1929年 阿瑟·哈登 英国 “对糖类的发酵以及发酵酶的研究” 汉斯·冯·奥伊勒-切尔平 德国1930年 汉斯·费歇尔 德国 “对血红素和叶绿素的组成的研究,特别是对血红素的合成的研究”1931年 卡尔·博施 德国 “发明与发展化学高压技术” 弗里德里希·贝吉乌斯 德国1932年 欧文·兰米尔 美国 “对表面化学的研究与发现”1933年 未颁奖1934年 哈罗德·克莱顿·尤里 美国 “发现了重氢”1935年 弗雷德里克·约里奥-居里 法国 “合成了新的放射性元素” 伊伦·约里奥-居里 法国1936年 彼得·德拜 荷兰 “通过对偶极矩以及气体中的X 射线和电子的衍射的研究来了解分子结构”1937年 沃尔特·霍沃思 英国 “对碳水化合物和维生素C 的研究”保罗·卡勒 瑞士 “对类胡萝卜素、黄素、维生素A 和维生素B2的研究”1938年 里夏德·库恩 德国 “对类胡萝卜素和维生素的研究”1939年 阿道夫·布特南特 德国 “对性激素的研究” 拉沃斯拉夫·鲁日奇卡 瑞士 “对聚亚甲基和高级萜烯的研究”1940年 未颁奖1941年 未颁奖1942年 未颁奖1943年 乔治·德海韦西 匈牙利 “在化学过程研究中使用同位素作为示踪物” 1944年 奥托·哈恩 德国 “发现重核的裂变”1945年 阿尔图里·伊尔马里·维尔塔宁 芬兰 “对农业和营养化学的研究发明,特别是提出了饲料储藏方法”1946年 詹姆斯·B·萨姆纳 美国 “发现了酶可以结晶”约翰·霍华德·诺思罗普 美国 “制备了高纯度的酶和病毒蛋白质” 温德尔·梅雷迪思·斯坦利 美国1947年 罗伯特·鲁宾逊爵士 英国 “对具有重要生物学意义的植物产物,特别是生物碱的研究”1948年 阿尔内·蒂塞利乌斯 瑞典 “对电泳现象和吸附分析的研究,特别是对于血清蛋白的复杂性质的研究”1949年 威廉·吉奥克 美国 “在化学热力学领域的贡献,特别是对超低温状态下的物质的研究”1950年 奥托·迪尔斯 西德 “发现并发展了双烯合成法” 库尔特·阿尔德 西德1951年 埃德温·麦克米伦 美国 “发现了超铀元素” 格伦·西奥多·西博格 美国1952年 阿彻·约翰·波特·马丁 英国 “发明了分配色谱法”理查德·劳伦斯·米林顿·辛格英国 1953年 赫尔曼·施陶丁格 西德 “在高分子化学领域的研究发现”1954年 莱纳斯·鲍林 美国 “对化学键的性质的研究以及在对复杂物质的结构的阐述上的应用”1955年 文森特·迪维尼奥 美国 “对具有生物化学重要性的含硫化合物的研究,特别是首次合成了多肽激素”1956年 西里尔·欣谢尔伍德爵士 英国 “对化学反应机理的研究” 尼古拉·谢苗诺夫 苏联1957年 亚历山大·R·托德男爵 英国 “在核苷酸和核苷酸辅酶研究方面的工作”1958年 弗雷德里克·桑格 英国 “对蛋白质结构组成的研究,特别是对胰岛素的研究”1959年 雅罗斯拉夫·海罗夫斯基 捷克 “发现并发展了极谱分析法”1960年 威拉得·利比 美国 “发展了使用碳14同位素进行年代测定的方法,被广泛使用于考古学、地质学、地球物理学以及其他学科”1961年 梅尔文·卡尔文 美国 “对植物吸收二氧化碳的研究”1962年 马克斯·佩鲁茨 英国 “对球形蛋白质结构的研究” 约翰·肯德鲁 英国1963年 卡尔·齐格勒 西德 “在高聚物的化学性质和技术领域中的研究发现” 居里奥·纳塔 意大利1964年 多萝西·克劳福特·霍奇金 英国 “利用X 射线技术解析了一些重要生化物质的结构” 1965年 罗伯特·伯恩斯·伍德沃德 美国 “在有机合成方面的杰出成就”1966年 罗伯特·S·马利肯 美国 “利用分子轨道法对化学键以及分子的电子结构所进行的基础研究”1967年 曼弗雷德·艾根 西德“利用很短的能量脉冲对反应平衡进行扰动的方法,对高速化学反应的研究”罗纳德·乔治·雷伊福特·诺里什 英国 乔治·波特 英国1968年 拉斯·昂萨格 美国 “发现了以他的名字命名的倒易关系,为不可逆过程的热力学奠定了基础”1969年 德里克·巴顿 英国 “发展了构象的概念及其在化学中的应用” 奥德·哈塞尔 挪威1970年 卢伊斯·弗德里科·莱洛伊尔 阿根廷 “发现了糖核苷酸及其在碳水化合物的生物合成中所起的作用”1971年 格哈德·赫茨贝格 加拿大 “对分子的电子构造与几何形状,特别是自由基的研究”1972年 克里斯蒂安·B·安芬森 美国 “对核糖核酸酶的研究,特别是对其氨基酸序列与生物活性构象之间的联系的研究” 斯坦福·摩尔 美国 “对核糖核酸酶分子的活性中心的催化活性与其化学结构之间的关系的研究”威廉·霍华德·斯坦 美国 1973年 恩斯特·奥托·菲舍尔 西德 “对金属有机化合物,又被称为夹心化合物,的化学性质的开创性研究”杰弗里·威尔金森 英国 1974年 保罗·弗洛里 美国 “高分子物理化学的理论与实验两个方面的基础研究”1975年 约翰·康福思 英国 “酶催化反应的立体化学的研究” 弗拉迪米尔·普雷洛格 瑞士 “有机分子和反应的立体化学的研究”1976年 威廉·利普斯科姆 美国 “对硼烷结构的研究,解释了化学成键问题”1977年 伊利亚·普里高津 比利时 “对非平衡态热力学的贡献,特别是提出了耗散结构的理论”1978年 彼得·米切尔 英国 “利用化学渗透理论公式,为了解生物能量传递作出贡献”1979年 赫伯特·布朗 美国 “分别将含硼和含磷化合物发展为有机合成中的重要试剂”格奥尔格·维蒂希 西德 1980年 保罗·伯格 美国 “对核酸的生物化学研究,特别是对重组DNA 的研究” 沃特·吉尔伯特 美国 “对核酸中DNA 碱基序列的确定方法” 弗雷德里克·桑格 英国1981年 福井谦一 日本 “通过他们各自独立发展的理论来解释化学反应的发生”罗德·霍夫曼 美国 1982年 阿龙·克卢格 英国 “发展了晶体电子显微术,并且研究了具有重要生物学意义的核酸-蛋白质复合物的结构”1983年 亨利·陶布 美国 “对特别是金属配合物中电子转移反应机理的研究”1984年 罗伯特·布鲁斯·梅里菲尔德美国 “开发了固相化学合成法” 1985年 赫伯特·豪普特曼 美国 “在发展测定晶体结构的直接法上的杰出成就” 杰尔姆·卡尔 美国1986年 达德利·赫施巴赫 美国“对研究化学基元反应的动力学过程的贡献” 李远哲 中国台湾约翰·查尔斯·波拉尼 加拿大1987年 唐纳德·克拉姆 美国 “发展和使用了可以进行高选择性结构特异性相互作用的分子” 让-马里·莱恩 法国 查尔斯·佩德森 美国1988年 约翰·戴森霍费尔 西德“对光合反应中心的三维结构的测定”罗伯特·胡贝尔 西德 哈特穆特·米歇尔 西德1989年 悉尼·奥尔特曼 加拿大 “发现了RNA 的催化性质” 托马斯·切赫 美国1990年 艾里亚斯·詹姆斯·科里 美国 “发展了有机合成的理论和方法学”1991年 理查德·恩斯特 瑞士 “对开发高分辨率核磁共振(NMR )谱学方法的贡献” 1992年 鲁道夫·马库斯 美国 “对化学体系中电子转移反应理论的贡献”1993年 凯利·穆利斯 美国 “发展了以DNA 为基础的化学研究方法,开发了聚合酶链锁反应(PCR )”迈克尔·史密斯 加拿大 “发展了以DNA 为基础的化学研究方法,对建立寡聚核苷酸为基础的定点突变及其对蛋白质研究的发展的基础贡献”1994年 乔治·安德鲁·欧拉 美国 “对碳正离子化学研究的贡献”1995年 保罗·克鲁岑荷兰 “对大气化学的研究,特别是有关臭氧分解的研究” 马里奥·莫利纳美国 弗兰克·舍伍德·罗兰美国 1996年 罗伯特·柯尔美国 “发现富勒烯” 哈罗德·克罗托爵士英国 理查德·斯莫利美国 1997年 保罗·博耶美国 “阐明了三磷酸腺苷(ATP )合成中的酶催化机理” 约翰·沃克英国 延斯·克里斯蒂安·斯科丹麦 1998年 沃尔特·科恩 美国 “创立了密度泛函理论” 约翰·波普英国 发展了量子化学中的计算方法 1999年 亚米德·齐威尔埃及 “用飞秒光谱学对化学反应过渡态的研究” 2000年 艾伦·黑格美国 “发现和发展了导电聚合物” 艾伦·麦克德尔米德美国 白川英树日本 2001年 威廉·斯坦迪什·诺尔斯美国 “对手性催化氢化反应的研究”野依良治日本 巴里·夏普莱斯美国 “对手性催化氧化反应的研究” 2002年约翰·贝内特·芬恩美国 “发展了对生物大分子进行鉴定和结构分析的方法,建立了软解析电离法对生物大分子进行质谱分析” 田中耕一日本 库尔特·维特里希 瑞士 “发展了对生物大分子进行鉴定和结构分析的方法,建立了利用核磁共振谱学来解析溶液中生物大分子三维结构的方法”2003年 彼得·阿格雷 美国 “对细胞膜中的离子通道的研究,发现了水通道” 罗德里克·麦金农 美国 “对细胞膜中的离子通道的研究,对离子通道结构和机理的研究”2004年 阿龙·切哈诺沃 以色列“发现了泛素介导的蛋白质降解”阿夫拉姆·赫什科 以色列 欧文·罗斯 美国2005年 伊夫·肖万 法国“发展了有机合成中的复分解法”罗伯特·格拉布 美国 理查德·施罗克 美国2006年 罗杰·科恩伯格 美国 “对真核转录的分子基础的研究”2007年 格哈德·埃特尔 德国 “对固体表面化学进程的研究”2008年 下村脩 美国“发现和改造了绿色荧光蛋白(GFP )”马丁·查尔菲 美国 钱永健 美国2009年 文卡特拉曼·拉马克里希南 英国 “对核糖体结构和功能方面的研究” 托马斯·施泰茨 美国阿达·约纳特 以色列2010年 理查德·赫克 美国“对有机合成中钯催化偶联反应的研究”根岸英一 日本 铃木章 日本2011年丹·谢赫特曼以色列“准晶体的发现”2012年罗伯特·莱夫科维茨[2]美国“对G蛋白偶联受体的研究”2013年马丁·卡普拉斯美国[3]给复杂化学体系设计了多尺度模型[4]迈克尔·莱维特亚利耶·瓦谢尔2014年埃里克·白兹格(EricBetzig)美国“在超分辨率荧光显微技术领域取得的成就”威廉姆·艾斯科·莫尔纳尔(William E. Moerner)美国斯特凡·W·赫尔(Stefan W.Hell)德国2015年托马斯·林达尔瑞典“在DNA修复的细胞机制方面的研究”保罗·莫德里奇美国阿齐兹·桑贾尔土耳其2016年让·皮埃尔·索瓦法国“分子机器的设计和合成”詹姆斯·弗雷泽·司徒塔特美国伯纳德·费灵格荷兰2015年诺贝尔化学奖授予托马斯·林达尔、保罗·莫德里奇以及阿齐兹·桑贾尔,他们描述并解释了细胞修复DNA的机制以及对遗传信息的保护措施。
化学动力学

分解析方法。他也分析了平衡常数以及正向、反向反应速度与温度 的依赖关系。
1887年 奥斯特瓦尔德(Wilhelm Ostwald,1853-1932,生于拉脱维亚的德国化
学家,唯能论者。发现电解质解离的稀化定律。长期反对原子论,但 终于公开认输)在他的著作《Lehrbuch der allgemeinen Chemie》的引 入“反反应 反应速率方程 简单级数反应速率方程 反应级数的确定n, c
生成速率与消耗速率
rconsumption= −slope rformation= slope
Time, t
0 RR PP
R
P
rR
dcR dt
,r
dcR
R dt
rP
dc P dt
,r
dcP
Pdt
r rR rPR P牛牛文档分享反应速率的表示方法
• 浓度变化率 • 压力变化率 • 反应进度变 化率
• 电流密度
化学反应速率的趣味历史与研究

化学反应速率的趣味历史与研究化学反应速率是化学反应进行的快慢程度的定量描述。
它在化学领域具有重要的意义,不仅关乎着化学反应的动力学过程,也与我们日常生活息息相关。
本文将带您回顾化学反应速率的历史发展,并介绍一些相关的研究成果。
一、历史回顾1. 早期发现对于化学反应速率的研究可以追溯到古希腊时期。
一位叫作亚拉基逻斯的化学学家,他通过对金属与酸反应的实验,发现了反应速率与反应物浓度之间的关系。
虽然当时的观察和理解还不够准确,但这一早期的发现为后来的研究奠定了基础。
2. 反应速率定律的建立19世纪,化学反应速率的研究逐渐成为化学学家们的关注点。
瑞典化学家格纳特在1824年提出了反应速率与反应物浓度的幂函数关系,即将反应速率公式化。
而法国化学家贝尔纳在1864年通过对酶的研究,发现了一种被称为“酶致动力学”的现象,进一步完善了反应速率定律。
3. 利用化学钟研究反应速率20世纪初,英国化学家布伦特和日本化学家托贝使用化学钟的概念研究了反应速率。
他们利用某些反应在一定条件下呈现周期性变化的特性,设计了一种称为化学钟的装置,通过对钟摆周期的变化进行观察,得到了更准确的反应速率数据,为理解复杂反应提供了新的途径。
二、研究成果1. 反应速率与温度温度是影响反应速率的重要因素之一。
随着温度的升高,化学反应速率也会增加。
研究表明,温度每升高10摄氏度,反应速率大约增加一到两倍。
这是因为温度升高会使反应物的分子动能增加,进而推动了反应速率的增加。
2. 反应速率与反应物浓度反应物浓度也是决定反应速率的重要因素之一。
一般来说,反应物浓度越高,反应速率越快。
这是因为反应物浓度的增加会增加反应物分子之间的碰撞频率,从而增加反应的机会。
3. 反应速率与催化剂催化剂是一种可以提高反应速率的物质。
催化剂不直接参与反应,但可以降低反应物之间的活化能,从而加速反应进程。
许多工业过程和生物反应都利用了催化剂的作用,提高了反应速率和产率。
4. 反应速率与表面积固体反应的速率通常与表面积有关。
历年诺贝尔化学奖得主及其成果

历年诺贝尔化学奖得主及其成果
以下是历年诺贝尔化学奖得主及其成果的部分介绍:
1901 年:雅各布斯·范特霍夫(Jacobus Henricus van't Hoff)因发现了化学动力学和热力学的原理以及渗透压定律而获得诺贝尔化学奖。
1902 年:赫尔曼·费歇尔(Hermann Emil Fischer)因对糖和嘌呤的合成做出的贡献而获得诺贝尔化学奖。
1905 年:阿道夫·冯·拜尔(Adolf von Baeyer)因对有机染料和芳香族化合物的研究而获得诺贝尔化学奖。
1907 年:爱德华·比希纳(Eduard Buchner)因发现了无细胞发酵的原理而获得诺贝尔化学奖。
1908 年:欧内斯特·卢瑟福(Ernest Rutherford)因对放射性物质和原子结构的研究而获得诺贝尔化学奖。
1909 年:威廉·奥斯特瓦尔德(Wilhelm Ostwald)因对催化作用、化学平衡和反应速率的研究而获得诺贝尔化学奖。
1910 年:奥托·瓦拉赫(Otto Wallach)因对脂环族化合物的研究而获得诺贝尔化学奖。
1911 年:玛丽·居里(Marie Curie)因发现了镭和钋元素,并对放射性物质的研究做出了巨大贡献而获得诺贝尔化学奖。
以上只是历年诺贝尔化学奖得主的一小部分,他们的研究成果在化学领域产生了深远的影响,并为现代化学的发展奠定了基础。
奥斯特瓦尔德

• 一是他创立了“唯能论”,反对唯物 论。他认为“能量”是万物的本源。 他的这种“唯能量”的观点,受到许 多著名化学家的激烈批评,使他无法 继续在大学里任教, • 二是第一次世界大战期间,德国由于 军火生产逐渐不齐,德军一再挫败。 德国皇家一再问计于奥斯特瓦尔德, 他迫不得已,提出用极易获得的氨来 大量制造硝酸,藉以维持庞大的军火 生产,使德军在战争末期又苟延残喘 了一年多,铸成了他一生中的又一大 错。
退休之后
• 奥斯特瓦尔德退休的比较早,于1906 年从莱比锡大学退休之时年仅五十二岁。 退休之后,他虽然担任过哈佛大学客座 教授,也从事过颜色理论的研究,但是, 大部分时间是在风景优美的莱比锡附近 的格罗斯伯登小村中过着隐居生活,并 撰写自传。1932年4月4日,奥斯特瓦尔 德因病逝世,享年78岁。
11级1班 杨骐毓
弗里德里希·威廉·奥斯特 瓦尔德,德国物理化学家。 1853年生于俄国拉脱维亚里 加,1872年入爱沙尼亚多尔 帕特大学学习,1878年获化 学博士学位,并提出了奥斯 特瓦尔德过程。1909年因其 在催化剂的作用、化学平衡、 化学反应速率方面的研究的 突出贡献,被授予诺贝尔化 学奖。著有《自然哲学概 论》 、《电化学:历史与 理论》等,1932年4月4日于 莱比锡逝世。
年轻简要经历
• 1853年 9月2日,奥斯特瓦尔德出生于俄国 的拉脱维亚的里加。他自幼好学,对化学有特 殊的兴趣和爱好。他常从药房里买回各种化学 药品,做各式各样的玩具,有时做能喷三色火 焰的烟火筒,有时做小巧玲珑的爆竹。1875 年他毕业于多尔帕特大学,1878年获得哲学 博士学位。1882年成为里加工业学院教授。 自此,他开始了化学动力学的研究生涯。
主要的贡献
化学反应动力学理论

化学反应动力学理论的发展史可以追溯至19世纪末期,那时化学家开始倾向于研究化学反应发生的速度和机理,而不仅仅是反应产物的特性。
最初的研究主要集中在化学反应中物质的转化速率上,而后转向研究反应机理和速率的本质。
随着时间的推移,的发展变得越来越重要,它不仅成为化学这门学科中的一个关键领域,也在其他相关领域中扮演着重要角色,例如工程和材料科学等领域。
一、反应速率与化学动力学在17世纪和18世纪,科学家开始使用药品和溶液进行实验。
通过观察固体和气体的反应,他们发现反应速率会受到温度、浓度和物体的表面积等因素的影响。
1850年代,研究人员开始使用实验室瓶处理反应,这使得他们更容易控制反应和收集实验数据。
化学反应是指单个或多个分子组成新分子的过程,在反应中会释放或吸收能量。
当反应速率减缓时,需要进行一个化学动力学方面的分析,以便确定为什么反应速率会减缓。
因此,化学动力学可以描述反应如何开始、如何发展,以及反应发生的速率和过程。
二、热力学和动力学热力学和动力学在研究化学反应方面发挥了不同的作用。
热力学主要关注反应中能量的转移,例如热量和熵。
它可以用来计算反应是否会进行,以及反应的平衡态。
另一方面,动力学描述的是反应的时间尺度和反应机制方面的问题。
热力学和动力学可以从不同的角度来诠释化学反应过程。
三、反应速率与反应生成物对于化学反应,通常会有一个反应方程式,它可以告诉我们反应生成物的类型和数量。
但是,反应方程式通常不能告诉我们反应发生的速率以及生成物如何生成的细节。
因此,化学动力学理论可以帮助我们更好地理解反应机制,尤其是细节问题。
例如,它可以区分化学反应的表观速率,这是指表面上的反应速率和细胞内反应速率之间的差异。
四、反应速率过程的数学与统计为了更好地了解化学反应过程,化学家开发了数学模型和统计学理论,这些理论可以用来预测反应生成物的数量。
数学模型可以用来计算反应速率的数学形式,如果我们知道反应物的初始浓度和反应温度。
诺贝尔化学奖

诺贝尔化学奖诺贝尔奖(Nobel prizewinners in chemistry)是以瑞典著名化学家、硝化甘油炸药发明人阿尔弗雷德·贝恩哈德·诺贝尔(1833-1896)的部分遗产作为基金创立的5项奖金之一。
诺贝尔奖包括金质奖章、证书和奖金支票。
历届诺贝尔化学奖获奖者名单1901范特霍夫(Jacobus Hendricus Van‘Hoff) 荷兰人(1852–1911) 研究化学动力学和溶液渗透压的有关定律一八八五年,范特霍夫又发表了使他获得诺贝尔化学奖的另一项研究成果《气体体系或稀溶液中的化学平衡》。
此外,他对史塔斯佛特盐矿所发现的盐类三氯化钾和氯化镁的水化物进行了研究,利用该盐矿形成的沉积物来探索海洋沉积物的起源。
1902埃米尔·费歇尔(Emil Fischer) 德国人 (1852–1919) 研究糖和嘌呤衍生物的合成埃米尔·费歇尔,德国化学家,是一九零二年诺贝尔化学奖金获得者。
他的研究为有机化学广泛应用于现代工业奠定了基础,后曾被人们誉为”实验室砷明。
”1903阿伦尼乌斯(Svante August Arrhenius) 瑞典人 (1859–1927) 提出电离学说在生物化学领域,阿伦尼乌斯也进行了创造性的研究工作。
他发表了《免疫化学》、《生物化学定量定律》等著作,并运用物理化学规律阐述了毒素和抗毒素的反应。
阿伦尼乌斯是当时公认的科学巨匠,为发展科学事业建立了不可磨灭的功勋,因而也获得了许多荣誉。
他被英国皇家学会接受为海外会员,同时还获得了皇家学会的大卫奖章和化学学会的法拉第奖章。
1904威廉·拉姆赛(William Ramsay) 英国人(1852–1916) 发现了稀有气体他就是著名的英国化学家—成廉·拉姆赛爵士。
他与物理学家瑞利等合作,发现了六种惰性气体:氦、氖、氙、氩、氪。
由于他发现了这些气态惰性元素,并确定了它们在元素周期表中的位置,他荣获了一九零四年的诺贝尔化学奖。
诺贝尔化学奖获得者

1901年-2013年诺贝尔化学奖简介1901 雅各布斯.亨里克斯.范托夫荷兰发现了化学动力学法则和溶液渗透压1902 赫尔曼.费谢尔德国在糖类和嘌呤合成中的工作1903 司凡特.奥古斯特.阿伦尼乌斯瑞典提出了电力理论1904 威廉.拉姆齐爵士英国发现了空气中的惰性气体元素并确定了它们在元素周期表中的位置1905 阿道夫.冯.拜耳德国对有机染料以及氢化芳香族化合物的研究促进了有机化学与化学工业发展1906 亨利.莫瓦桑法国研究并分离了氟元素并使用了后来以他名字命名的电炉1907 爱德华.比西纳德国生物化学研究中的工作和发现无细胞发酵1908 欧内斯特.卢瑟福英国新西兰对元素的蜕变以及放射化学的研究1909 威廉.奥斯特瓦尔德德国对催化作用的研究和对化学平衡以及化学反应速率的基本原理的研究1910 奥托.瓦拉赫德国在酯环族化合物领域的开创性工作促进了有机化学和化学工业的发展1911 玛丽.居里波兰发现了镭和钋,提纯镭并研究其性质1912 维克多.格林尼亚法国发明了格式试剂保罗.萨巴捷法国发明细金属粉存在下的有机化合物的加氢法1913 阿尔弗雷德.维尔纳瑞士对分子内原子连接的研究,特别是在无机化学领域1914 奥西多.威廉.理查兹美国精确测定了大量化学元素的原子量1915 李夏德.威尔士泰特德国对植物色素的研究,特别是叶绿素的研究1916 1917 空1918 弗里茨.哈勃德国对从单质合成氨的研究1919 空1920 瓦尔特.能斯特德国对热化学的研究1921 弗雷德里克.索迪英国对人们了解放射性物质的化学性质的贡献以及对同位素的起源和性质的研究1922 弗朗西斯.阿斯顿英国使用质谱仪发现了大量非放射性元素的同位素并阐明了整数法则1923 弗里茨.普雷格尔奥地利创立了有机化学的微量分析法19241925 李夏德.阿道夫.席格蒙蒂德国匈牙利阐明了胶体溶液的异象性质并创立相关分析法1926 特奥多尔.司伟德贝里瑞典对分散系统的研究 1927 海因里希.奥托.威兰德国对胆汁酸以及相关物质结构的研究1928 阿道夫.温道思德国对甾类结构以及他们和维他命的关系的研究1929 阿瑟.哈登英国对糖类的发酵以及发酵酶的研究汉斯.冯.奥伊勒切尔平德国1930 汉斯.费谢尔德国对血红素和叶绿素的组成的研究特别是对血红素的合成的研究1931 卡尔.博施德国贝吉乌斯德国发明与发展化学高压技术弗里德里希.1932 欧文.兰米尔美国队表面化学的研究发现19331934 哈德罗.克莱顿.尤里美国发现了重氢1935 弗雷德里克.约里奥.居里法国伊伦.约里奥.居里合成了新的放射性元素1936 彼得.德拜荷兰通过对偶极矩以及气体中的X射线和电子的衍射的研究来了解分子结构1937 沃尔特.霍沃斯英国对碳水化合物和VC的研究保罗.卡勒瑞士1938 李夏德.库恩德国对类胡萝卜素的维生素的研究1939 阿道夫.布特南特德国对性激素的研究拉沃斯拉夫.鲁日奇卡瑞士对聚亚甲基和高级萜烯的研究1940 1941 1942 空1943 乔治.德海维希匈牙利在化学过程研究中使用同位素作为示踪物1944 奥托.哈恩德国发现重核的裂变1945 阿尔土里.伊尔马里.维尔塔宁芬兰对农业和营养化学的研究发明,特别提出饲料储藏法1946 詹姆斯.B.萨姆纳美国发现了酶可以结晶约翰.霍华德.诺斯罗普美国制备了高纯度的酶和病毒蛋白质温德尔.每类迪恩.斯坦利美国1947 罗伯特.鲁滨孙爵士英国对具有重要生物学意义的植物产物特别是生物碱的研究1948 埃尔内.迪赛利乌斯瑞典对电泳现象和吸附分析的研究,特别是对于血清蛋白的复杂性质的研究1949 威廉.吉奥克美国在热化学领域的贡献,特别是对超低温状态下物质的研究1950 奥托.蒂尔斯西德发现并发展了双桸合成法库尔特.阿尔德西德1951 埃德温.麦克米伦美国发现了超釉元素格伦.奥西多.西伯格美国1952 阿彻.约翰.波特.马丁英国发明了分配色谱法理查德.劳伦斯.米林顿.辛格英国1953 赫尔曼.施陶丁格西德在高分子化学领域的研究发现1954 莱纳斯.鲍林美国对化学键的性质的研究以及在对复杂物质的结构的阐述上的应用1955 文森特.迪维尼奥美国对生物化学重要性的含硫化合物的研究,特别是首次合成多肽激素1956 西里尔.欣谢尔伍德爵士英国对化学反应机理的研究尼古拉.谢苗诺夫苏联1957 亚历山大.R.托德男爵英国在核苷酸和核苷酸辅酶研究方面的工作1958 弗雷德里克.桑格英国对蛋白质结构组成的研究特别是对胰岛素的研究1959 亚罗斯拉夫.海洛夫斯基捷克斯洛伐克发现并发展了极谱分析法1960 威拉得·利比美国发展了使用碳14同位素进行年代测定的方法,被广泛使用于考古学、地质学、地球物理学以及其他学科1961 梅尔文·卡尔文美国对植物吸收二氧化碳的研究1962 马克斯·佩鲁茨英国对球形蛋白质结构的研究1963 卡尔.齐格勒西德在高聚物的化学性质和技术领域中的研究发现居里奥·纳塔意大利1964 多萝西·克劳福特·霍奇金英国利用X射线技术解析了一些重要生化物质的结构1965 罗伯特·伯恩斯·伍德沃德美国有机合成方面的成绩 1966 罗伯特·S·马利肯美国利用分子轨道法对化学键以及分子的电子结构所进行的基础研究1967 曼弗雷德·艾根西德利用很短的能量脉冲对反应平衡进行扰动的方法,对高速化学反应的研究罗纳德·乔治·雷伊福特·诺里什英国乔治.波特英国1968 拉斯·昂萨格美国发现了以他的名字命名的倒易关系,为不可逆过程的热力学奠定了基础1969 德里克·巴顿英国发展了构象的概念及其在化学中的应用奥德·哈塞尔挪威1970 卢伊斯·弗德里科·莱洛伊尔阿根廷发现了糖核苷酸及其在碳水化合物的生物合成中所起的作用1971 格哈德·赫茨贝格加拿大对分子的电子构造与几何形状,特别是自由基的研究1972 克里斯蒂安·B·安芬森美国对核糖核酸酶的研究,特别是对其氨基酸序列与生物活性构象之间的联系的研究斯坦福·摩尔美国对核糖核酸酶分子的活性中心的催化活性与其化学结构之间的关系的研究威廉·霍华德·斯坦美国1973 恩斯特·奥托·菲舍尔西德对金属有机化合物,又被称为夹心化合物,的化学性质的开创性研究杰弗里·威尔金森英国对金属有机化合物,又被称为夹心化合物,的化学性质的开创性研究1974 保罗·弗洛里美国高分子物理化学的理论与实验两个方面的基础研究1975 约翰·康福思澳大利亚英国酶催化反应的立体化学的研究弗拉迪米尔·普雷洛格瑞士有机分子和反应的立体化学的研究1976 威廉·利普斯科姆美国对硼烷结构的研究,解释了化学成键问题1977 伊利亚·普里高津比利时对非平衡态热力学的贡献,特别是提出了耗散结构的理论1978 彼得·米切尔英国利用化学渗透理论公式,为了解生物能量传递作出贡献1979 赫伯特·布朗美国分别将含硼和含磷化合物发展为有机合成中的重要试剂格奥尔格维蒂希西德1980 保罗.伯格美国对核酸的生物化学研究,特别是对重组DNA的研究沃特·吉尔伯特美国对核酸中DNA碱基序列的确定方法弗雷德里克·桑格英国1981 福井谦一日本通过他们各自独立发展的理论来解释化学反应的发生罗德·霍夫曼美国1982 阿龙·克卢格英国发展了晶体电子显微术,并且研究了具有重要生物学意义的核酸-蛋白质复合物的结构”1983 亨利·陶布美国对特别是金属配合物中电子转移应机理的研究1984 罗伯特·布鲁斯·梅里菲尔德美国开发了固相化学合成法1985 赫伯特·豪普特曼美国在发展测定晶体结构杰尔姆·卡尔美国的直接法上的杰出成就1986 达德利·赫施巴赫美国对研究化学基元反应的动力学过程的贡献李远哲中国约翰·查尔斯·波拉尼加拿大匈牙利1987 唐纳德·克拉姆美国发展和使用了可以进行高选择性结构特异性相互作用的分子让-马里·莱恩法国查尔斯·佩德森美国1988 查尔斯·佩德森美国对光合反应中心的三维结构的测定约翰·戴森霍费尔西德罗伯特·胡贝尔西德哈特穆特·米歇尔西德1989 悉尼·奥尔特曼加拿大美国发现了RNA的催化性质托马斯·切赫美国1990 艾里亚斯·詹姆斯·科里美国发展了有机合成的理论和方法学1991 理查德·恩斯特瑞士对开发高分辨率核磁共振谱学方法的贡献1992 鲁道夫·马库斯美国对化学体系中电子转移反应理论的贡献1993 凯利·穆利斯美国发展了以DNA为基础的化学研究方法,开发了聚合酶链锁反应(PCR)迈克尔·史密斯加拿大发展了以DNA为基础的化学研究方法,对建立寡聚核苷酸为基础的定点突变及其对蛋白质研究的发展的基础贡献1994 乔治·安德鲁·欧拉美国匈牙利对碳正离子化学研究的贡献1995 马里奥·莫利纳美国对大气化学的研究,特别是有关臭氧分解的研究弗兰克·舍伍德·罗兰美国1996 罗伯特·柯尔美国发现富勒烯哈罗德·克罗托爵士英国理查德·斯莫利美国1997 保罗·博耶美国阐明了三磷酸腺苷(ATP)合成中的酶催化机理约翰·沃克英国延斯·克里斯蒂安·斯科丹麦1998 沃尔特·科恩美国创立了密度泛函理论约翰.波普英国1999 亚米德·齐威尔埃及美国用飞秒光谱学对化学反应过渡态的研究2000 艾伦·黑格美国发现和发展了导电聚合物艾伦·麦克德尔米德美国新西兰白川英树日本2001 威廉·斯坦迪什·诺尔斯美国对手性催化氢化反应的研究野依良治日本巴里·夏普莱斯美国2002 约翰·贝内特·芬恩美国发展了对生物大分子进行鉴定和结构分析的方法,建立了软解析电离法对生物大分子进行质谱分田中耕一日本库尔特·维特里希瑞士发展了对生物大分子进行鉴定和结构分析的方法,建立了利用核磁共正谱学来解析溶液中生物大分子三维结构的方法”2003 彼得·阿格雷美国对细胞膜中的离子通道的研究,发现了水通道罗德里克·麦金农美国对细胞膜中的离子通道的研究,对离子通道结构和机理的研究2004 阿龙·切哈诺沃以色列发现了泛素介导的蛋白质降解阿龙·切哈诺沃以色列欧文·罗斯美国2005 伊夫·肖万法国发展了有机合成中的复分解法罗伯特·格拉布美国理查德·施罗克美国2006 罗杰·科恩伯格美国对真核转录的分子基础的研究2007 格哈德·埃特尔德国对固体表面化学进程的研究2008 下村脩美国发现和改造了绿色荧光蛋白(GFP)”马丁·查尔菲美国钱永健美国文卡特拉曼·拉马克里希南英国2009 文卡特拉曼·拉马克里希南英国对核糖体结构和功能方面的研究”托马斯·施泰茨美国阿达·约纳特以色列2010 理查德·赫克美国对有机合成中钯催化偶联反应的研究”根岸英一美国铃木章日本2011 丹·谢赫特曼以色列准晶体的发现2012 罗伯特·莱夫科维茨美国对G蛋白偶联受体的研究”2013年诺贝尔化学奖:犹太裔美国理论化学家马丁-卡普拉斯、美国生物物理学家迈克尔-莱维特及南加州大学化学家亚利耶-瓦谢尔因给复杂化学体系涉及了多尺度模型而获得。
化学反应动力学—化学反应速率

N2O5分解反应的lg(N2O5)t图
N2O5分解反应的 反应速率方程改写为:
lg[(A)/(A)0] = kt / 2.303
当 (A) = (A)0/2时,此刻的反应时间t = t1/2,也就是反应进行一半 所需的时间,称为半衰期(t1/2)。显然,
我们现在学习的反应速率应当是瞬时反应速率,即是某一点上浓度 与时间的比值,也就是经过这一点的切线的斜率。如下图:
R P d[ R ] rR dt d[ P] rp dt
●
从平均速率到瞬时速率:
v=-
v = lim
t 0
(H2O2) t (H2O2) t dt d(H2O2)
般要由实验确定,不能直接按化学方程式的计量系数写出。
(3) 反应级数及各级反应的特点 速率方程式里浓度的方次叫作反应的级数。要正确写出速率方程式 表示浓度与反应速率的关系,必须由实验测定速率常数和反应级数。 化学反应按反应级数可以分为一级、二级、三级以及零级反应等。 各级反应都有特定的浓度-时间关系。确定反应级数是研究反应速 率的首要问题。 CO(g) + NO2(g) CO2(g) + NO(g)
S2O82 + 3I 2SO42 + I3 2HI H2 + I2
对于二级反应,
B P
= k (B)2
d (B) v=- dt 积分可得,
1 1 = + kt (B) (B)0
反应物浓度倒数与时间t呈线性关系是二级反应的特征。
HI(g) 的分解反应速率
t/h (HI) /moldm3 (HI)1 /(moldm3)1
H 2 Cl2 2HCl
它不是通过氢分子和氯分子在一次化学碰撞中来实现的,事实上 ,是通过一系列反应来完成的:
化学动力学的发展与百年诺贝尔化学奖

第20卷 第1期今日化学2005年2月化学史 化学动力学的发展与百年诺贝尔化学奖姚兰英 彭蜀晋(四川师范大学化学学院 成都610066) 摘要 探讨了化学动力学三大发展阶段(宏观反应动力学阶段、元反应动力学阶段和微观反应动力学阶段)中诺贝尔化学奖的13次颁发对其发展的影响。
化学动力学是物理化学发展的四大支柱中的前沿研究领域之一[1],近百年来发展很迅速。
回顾百年来诺贝尔化学奖的颁奖历程,其中有13次颁发给了22位直接对化学动力学发展做出巨大贡献的科学工作者,可见化学动力学在现代化学发展中的重要地位。
这13次诺贝尔化学奖的颁发反映出百年来化学动力学历经的三大发展阶段:宏观反应动力学阶段、元反应动力学阶段和微观反应动力学阶段[2]。
这三大阶段也体现了化学动力学研究领域和研究方法及技术手段的变化发展历程。
1 宏观反应动力学阶段 化学动力学作为一门独立的学科,它的发展历史始于质量作用定律的建立[3]。
宏观反应动力学阶段是研究发展的初始阶段,大体上是从19世纪后半叶到20世纪初,主要特点是改变宏观条件,如温度、压力、浓度等来研究对总反应速率的影响,其间有3次诺贝尔化学奖颁给了与此相关的化学家。
这一阶段的主要标志是质量作用定律的确立和阿伦尼乌斯公式的提出。
1850年,W ilhel m y通过研究蔗糖的水解反应得出了一级反应的速率方程。
1867年,Guld2 berg和W aage在总结了大量实验的基础上提出了质量作用定律。
19世纪80年代,van’t Hoff 及A rrhenius在对质量作用定律所进行的研究中,进一步提出了有效碰撞、活化分子及活化能的概念。
但后来证明,质量作用定律只是描述基元反应动力学行为的定理,在总包反应层次上并不正确。
van’t Hoff对化学反应中反应物浓度与反应速率之间的关系进行了明确的阐述,并提出了化学反应具有可逆性的概念。
他还从热力学角度提出了化学反应中大量分子与温度之间的近似规律。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
首页→第七章化学反应速率
一、化学动力学简史与诺贝尔化学奖
1850威廉米(Ludwig Ferdinand Wilhelmy, 1812-1864, 德国物理学家) 研究在酸性条件下蔗糖分解(水解为D-(+)-果糖和D-(-)-果糖)的反应速率,发现反应速率正比于蔗糖和酸的浓度。
1864
古德博格(Cato Maximillian Guldberg, 1836-1902, 挪威数学家,理论化学家) 和瓦格(Peter Waage, 1833-1900,挪威化学家) 给出“质量作用定律”的公式。
按照这个公式,反应“推动力”正比于反应物浓度的乘积:K=[R]r [S]s/([A]a [B]b)
其中,a, b, r, s分别为化学反应A+B = R+S的整比系数。
因此,前向反应速率正比于[A]a[B]b,而后向反应速率整比于[R]r [S]s。
1865
Harcourt 和Esson (英) 分析了H2O2和HI、KMnO4和(COOH)2的反应。
他们写出了相应的微分方程,通过积分得到浓度-时间关系。
他们也提出了反应速率与温度的关系式k = A T C
1884
范特霍夫(Jacobus Henricus van’t Hoff, 1852-1911, 荷兰物理化学家。
提出碳原子价键的空间结构学说;提出稀溶液理论。
)的《化学动力学研究》(“Studies of Chemical Dynamics”,“Études de dynamique chimique”)出版。
在这本书中,van’t Hoff 推广和继续发展了Wilhelmy, Harcourt 和Esson 的工作。
特别是,他引入了微分解析方法。
他也分析了平衡常数以及正向、反向反应速度与温度的依赖关系。
(平衡常数与温度的关系现在称为van’t Hoff 方程)。
van’t Hoff由于对化学动力学和溶液渗透压
的首创性研究而荣获了1901年的首届诺贝尔化学
奖
1887
奥斯特瓦尔德(Wilhelm Ostwald, 1853-1932, 生于拉脱维亚的德国化学家,唯能论者。
发现电解质解离的稀化定律。
长期反对原子论,但终于公开认输。
)在他的著作《Lehrbuch der allgemeinen Chemie》的引入“反应级数”和“半衰期”的概念。
1909年,Ostwald因研究催化和化学平衡、反应速率的基本原理而荣获诺贝尔化学奖,并被人们誉为“物理化学之父”。
1889
阿伦尼乌斯(Svante August Arrhenius, 1859-1927, 瑞典化学家,物理学家。
建立电解质电离的理论。
) 进一步分析了反应速率对温度的依赖关系,k=A exp(-B/T),并提出一个“能垒”解释;这个方程后来被称为Arrhenius 方程。
1903年,Arrhenius因提出电离学说获得了第3届诺贝尔化学奖。
在20世纪,化学动力学理论有了显著的发展(从“第一原理”确定速率常数和反应级数)。
但是,目前还不能预测实际化学过程的动力学参数。
1913Chapman (英) 创立、Bodenstein (德) 发展了链反应中的稳态近似理论。
按照这个理论,中间产物的速率变化可以忽略不计。
1917
Trautz (德) 和Lewis (英) 分别独立发现反应速率取决于分子碰撞频率。
现在,被称为化学反应动力学的“碰撞理论”。
1920s
朗格缪尔(Irving Langmuir, 1881-1957, 美国化学家。
提出气体在固体表面上的吸附理论。
) 研究了表面反应动力学,得到被后人命名为“Langmuir 等温线”的基本理论。
后来,Hinshelwood(英)进一步发展了这个理论,成为多相催化反应的“Langmuir-Hinshelwood机理”。
1934
赖斯(Rice,美国) 和赫兹菲尔德(Herzfeld, 美国) 证明:与自由基有关的链式反应(用稳态近似求得浓度)是引起有机化合物热分解反应(例如,乙烷和乙醛)反应级数变化的主要原因。
1935
艾林(Eyring, 美国) 发展了一个统计处理方法,称为“绝对反应速率理论”或“过渡态理论”。
按照这个理论,化学反应有两个步骤:
(a) 反应物平衡转化为“活化复合物”
(b)上述复合物的分解(有限速率步骤)。
1950s
Eigen创建了化学弛豫方法。
该方法极大地提高了测量化学反应时间的分辨率,可以对反应时间仅为10-8s的快速反应进行研究,成为液相快速反应动力学研究的有效方法。
Norrish和Porter则发展了闪光光解法,使寿命短至μs量级的激发态中间物种也能被发现。
现在弛豫法和闪光光解法已成为测定快速反应的有效手段,为反应机理的研究提供了有效的研究方法。
Eigen、Norrish和Porter也因通过极短能量脉冲导致平衡移动来研究快速的
化学反应而获得了1967年度的诺贝尔化学奖。
1960s
Herschbach和李远哲等人实现了在单次碰撞下研究单个分子间发生的反应机理的设想,使化学家有可能在电子、原子、分子和量子层次上研究化学反应所出现的各种动态,以探究化学反应和化学相互作用的微观机理和作用机制,揭示化学反应的基本规律(分子反应动力学的核心所在)。
Polanyi则开创了红外化学发光的研究。
1986年,Herschbach、李远哲和Polanyi因对化学基元过程动力学的贡献¨而分享了诺贝尔化学奖。
这也标志着国际学术界对此领域的重视以及对1955~1986年期间取得成就的肯定,是分子反应动力学发展的又一重要里程碑。
1970s
基于快速激光脉冲的飞秒光谱技术发展十分
迅速,时间标度达到了飞秒数量级。
随之发展起来
的飞秒化学(Femtochemistry)有着极其重要的理论
意义和研究价值。
Zewail从20世纪80年代开始,
利用超短激光创立了飞秒化学,从而使人们对过渡
态的研究有了可靠的手段。
Zewail也因用飞秒化学
研究化学反应的过渡态而获得了1999年度的诺贝
尔化学奖。
二、化学动力学与治疗药物监测
药物是治疗疾病的主要手段之一,药物进入生物体内通过调整失调的内源性活性物质或生理生化过程,杀灭抑制病原体达到治疗疾病的目的。
显然,治疗药物在作用部位的浓度或质量不足或过多便会起不到治疗作用或产生新的不良作用,甚至引起药源性疾病乃至危及生命。
因此20世纪60年代治疗药物监测(therapeutic drug monitoring.TDM)作为一门新兴的学科得以诞生和发展。
TDM的主要任务是通过灵敏可靠的检测方法,获得病人血液或其它生物材料中药物的浓度,获取有关药动学参数,利用动力学的相关理论,指导临床合理用药方案的制定和调整,并对药物中毒进行诊断和治疗,从而使药物治疗具有有效性和安
全性。
目前TDM在欧美发达国家已成为临床化学实验室的主要常规工作之一。
药物代谢动力学研究为TDM提供了基础,以药物代谢的消除动力学模型为例予以说明。
消除动力学(elimination kinetics)研究体内药物浓度变化速率的规律,可用下列微分方程表示:
dc/dt =-kc n
式中c为药物浓度,t为时间,k为消除速率常数,n代表消除动力学级数。
当n=1时即为一级消除动力学,n=0时则为零级消除动力学。
药物消除动力学模型即指这两种。
1、一级消除动力学
一级消除动力学(first order elimination kinetics)的表达式为:
dc/dt =- kc
积分得c t=c0 e-kt
由上指数方程可知,一级消除动力学的最主要特点是药物浓度按恒定的比值减少,即恒比消除。
2、零级消除动力学
零级消除动力学(zero order elimination kinetics)时,由于n=0,因此其微分表达式为:
dc/dt =- k
积分得c t=c0- kt
由此可知,零级消除动力学的最基本特点为药物浓度按恒量减少,即恒量消除。
必须指出,药物并不是固定按一级或零级动力学消除。
任何药物当其在体内量较少,未达到机体最大消除能力时(主要是未超出催化生物转化的酶的饱和限时),都将按一级动力学方式消除;而当其量超过机体最大消除能力时,将只能按最大消除能力这一恒量进行消除,变为零级消除动力学方式,即出现消除动力学模型转换。
苯妥英钠、阿司匹林、氨茶碱等常用药,在治疗血药浓度范围内就存在这种消除动力学模型转移,在TDM工作中尤应注意。
从药物代谢的消除动力学模型研究可以看到:化学动力学为TDM的开展提供了必备的基础理论,为临床合理用药提供了保障。
