碳谱2
核磁共振碳谱各基团出峰位置

核磁共振碳谱各基团出峰位置
核磁共振碳谱(13C NMR)是一种常用的化学分析技术,用于确定有机化合物中碳原子的化学环境。
不同基团的碳原子在核磁共振碳谱中会出现在不同的化学位移(ppm,即百万分之一)上,这是由于它们所处的化学环境不同,受到周围电子云的屏蔽效应不同,从而影响了它们对核磁共振信号的响应。
以下是一些常见基团在核磁共振碳谱中的出峰位置:
1. 甲基(CH3-):通常在0-30 ppm范围内出现。
2. 亚甲基(CH2-):通常在10-40 ppm范围内出现,但具体化学位移会受到相邻基团的影响。
3. 次甲基(CH-):通常在30-60 ppm范围内出现,同样也会受到相邻基团的影响。
4. 季碳(C-):由于没有氢原子与之相连,季碳的化学位移范围较广,通常在40-100 ppm之间,但也可能出现在更高或更低的化学位移上。
5. 羰基碳(C=O):通常在160-220 ppm范围内出现。
6. 芳香碳:通常在100-160 ppm范围内出现,但具体化学位移会受到芳香环上取代基的影响。
需要注意的是,以上仅是一些常见基团的大致出峰位置,实际上还会受到许多其他因素的影响,如溶剂、温度、pH值等。
因此,在进行核磁共振碳谱分析时,需要综合考虑各种因素,结合化合物的结构和已知数据进行解析。
最后提醒一点,核磁共振碳谱的解析需要一定的专业知识和经验,建议在进行相关实验或数据分析时寻求专业人士的帮助。
第三章 碳谱
COH
3.2.3影响13C化学位移的因素
Spring 2013
3. 空间效应
化学位移对分子的几何形状非常敏感,相隔几个键的碳,如果它
们空间非常靠近,则互相发生强烈的影响,这种短程的非成键的 相互作用叫空间效应。
Grant提出了一个空间效应的简单公式,由空间效应引起的位移增
量St不仅决定于质子和质子间的距离HH,而且取决于HH轴和 被干扰的C-H键之间的夹角:
sp CCH
O CH2 127 ~ 134 41 第三章 碳谱
在中间 14 CH3
CH2 61
50 ~ 80 ppm
114 36 138 36 126-142
C
171
O
3.2.3影响13C化学位移的因素 2)取代基的电负性
Spring 2013
有电负性取代基、杂原子以及烷基连接的碳,都能使其 C信号向低场 位移,位移的大小随取代基电负性的增大而增加,称诱导效应 Chemical shifts (ppm) of XCH2CH2CH3 1H 13C -CH2 -CH2 -CH3 -CH2 -CH2 -CH3 Et 1.3 1.3 0.9 34 22 14 COOH 2.3 1.7 1.0 36 18 14 SH 2.5 1.6 1.0 27 27 13 NH2 2.6 1.5 0.9 44 27 11 Ph 2.6 1.6 0.9 39 25 15 Br 3.4 1.9 1.0 36 26 13 Cl 3.5 1.8 1.0 47 26 12 OH 3.6 1.6 0.9 64 26 10 NO2 4.4 2.1 1.0 77 21 11
St = C· HH(HH)· F Cos
FHH表示质子之间的排斥力, 是HH的函数; C为常数,St的符号
核磁二维碳谱

核磁二维碳谱
核磁二维碳谱(NMR 2D Carbon Spectrum)是一种核磁共振(Nuclear Magnetic Resonance, NMR)技术,在化学分析中用
于研究和识别分子结构。
与传统的一维核磁谱相比,二维碳谱提供了更丰富的化学信息和分辨率,能够提供更准确和详细的分析结果。
在核磁二维碳谱中,研究者通常先利用一维质子谱(1H NMR)对样品进行初步的分析,确定样品的组成和结构。
然后,利用碳谱探针对样品进行进一步的分析。
核磁二维碳谱使用两个核磁共振射频脉冲,一个作用在碳核上,另一个作用在质子核上。
通过改变两个脉冲之间的时间间隔和脉冲的频率,可以收集大量的数据点,构建二维谱图。
核磁二维碳谱可以提供关于样品中各个碳原子的化学位移(chemical shift)和耦合常数(coupling constant)的信息。
通
过分析谱图中的峰形和位置,可以确定各个碳原子之间的关系和结构。
核磁二维碳谱在有机化学和药物研究中广泛应用,可以用于确认化合物的结构、研究反应机理、鉴定杂质和副产物等。
它是一种非破坏性的分析方法,可以对样品进行无损分析,而且具有高度的准确性和灵敏度。
碳谱

核磁共振碳谱 (13
影响化学位移的因素
1.杂化状态
13C化学位移受C杂化的影响很大,13C化学 位移大小顺序与δH基本平行。
碳的类型 d (ppm)
碳的类型 d (ppm)
TMS
0
=C 100-150
RCH3 RCH2R R3CH sp3 R4C
C-I
8-35 15-50 20-60 30-40 0-40
4.立体效应
主要是指g-邻位交叉效应,即:在环己烷或其类似物中, 间隔两根键的碳,可因相近取代基的空间排斥作用,而使其 上电子云密度增加,从而向高场移动,也称为g-效应。取代 基的构象除了影响a-碳外,对隔三个键的g-碳有明显的影响。 处于直立键的取代基团同g碳空间处于邻位交叉的关系,起屏 蔽作用,向高场移动约5ppm。
5. 分子内部作用
分子内部氢键形成,使羰基碳电荷降低,dc 值增 大。
6 其他因素
溶剂的极性 溶液的浓度 溶液的pH值 温度
去偶技术
质子宽带去偶
简化了谱图,失去了许多有用的结构信息,无法识别伯仲叔季不同 类型的碳原子
偏共振去偶
保留了与碳核直接相连的质子偶合信息
质子选择性去偶 门控去偶 反转门去偶
取代苯环中,供电子基团取代,能使其邻对位碳 的电子云密度增加,对应碳的化学位移减少;而吸电 子基团取代,则使其邻对位碳的电子云密度降低,对 应碳的化学位移增加;取代对其间位碳的电子云密度 影响不大,故间位碳的化学位移变化较小。例:
如有空间障碍,共轭受阻,则去屏蔽dc增大,受阻 角度越大,去屏蔽效应越强,如:
碳谱的解析
核磁共振碳谱 (13C NMR)
化学位移范围:0 ~ 220 ppm,氢谱0 ~16ppm 提供各种类型碳(伯、仲、叔、季碳)的信息。 不能用积分曲线获取碳的数目信息 邻近有吸电子基团,信号移向低场(左移)
第四章核磁共振碳谱习题2

第四章核磁共振碳谱一、判断题[1]自由衰减信号(FID)是频率域信号。
()[2]碳谱的化学位移范围范围较宽(0-200),所以碳谱的灵敏度高于氢谱。
()[3]在宽带去耦碳谱中,不同类型的碳核产生的裂分峰数目不同。
()[4]氢质子在二甲基亚砜中的化学位移比在氯仿中要小。
()[5]在13C NMR谱中,由于13C-13C相连的概率很低,所以通常不考虑13C核只见到耦合。
()[6]含19F的化合物,可观测到19F对13C核的耦合裂分,且谱带裂分数符合n+1规律。
()[7]但在固相核磁共振波谱中,分子运动受到限制,由于磁各向异性作用将是谱线带变宽,分辨率大大下降。
()[8]在碳谱中,13C-1H会发生耦合作用,但是13C-1H的耦合常数远比1H-1H之间的耦合常数小.()[9]在135°DEPT试验中,CH、CH2和CH3均出正峰,季碳原子不出现谱峰。
()[10]在APT实验中,CH和CH3均出正峰,CH2出负峰,季碳原子不出现谱峰。
()二、选择题(单项选择)[1] 下列原子核没有自旋角动量的是哪一种?()。
A. 14N7B. 12C6C. 31P15D. 13C6[2] 在13C NMR波谱中在化学位移125-140产生两个信号的化合物是()。
A. 1,2,3,-三氯苯;B. 1,2,4,-三氯苯;C. 1,3,5,-三氯苯[3] 在13C NMR波谱中在化学位移125-140产生六个信号的化合物是()。
A. 1,2,3,-三氯苯;B. 1,2,4,-三氯苯;C. 1,3,5,-三氯苯[4] 在13C NMR波谱中在化学位移125-140产生三个信号的化合物是()。
A. 对二氯苯;B. 邻二氯苯;C. 间二氯苯。
[5] 在13C NMR中在化学位移0-60产生3个信号;在1H NMR中在化学位移0-5产生3个信号(最低场信号为多重峰)的化合物是()。
A. 1,1-二氯丙烷;B. 1,2二氯丙烷;C. 2,2-二氯丙烷;D. 1,3二氯丙烷。
碳谱

(t)-CH(d)季碳和羰基碳(s),可区分。
4、无畸变极化转移技术(DEPT)
用多脉冲器与射频脉冲450,900,1350相位
移控制技术,令质子去偶通道和13C观测通 道相互配合,适时接通与关闭,同时控制去 偶通道脉冲的质子不同翻转角θ使伯、仲、 叔、季碳表现出不同的峰强与相位,从 而区分它们。如θ=900时,CH为最强正相 峰,而CH3、CH2 为0。 Θ=1350时, CH 、CH3呈现正相峰,CH2呈现负相峰, 而季碳信号不出现。
键能
n→π※ ∠ π→π※ ∠n→σ※∠σ→σ※ 低场 高场
羰基化合物 烯类芳香化合物 饱和碳
>170
100-150
0-80
191.5
196.5
O O
O H
O
CH3
例2、化合物分子式为C7H10O3,其碳谱V
如下,请推断其结构.
H2C
CH3 C
O C O CH2 CH O CH2
例3、某化合物分子量为132,其碳谱 和氢谱如下,求其结构式。
分子式为C9H8O,可能结构式为
化合物的结构式
本章结束
诱导效应
24.3
26.6
27.4 68.8
O
OMe
128.5 159.8 113.5 128.5 120.5 136.2 124.2 149.8
N
共轭效应
O
205
O
192.4
CH3 H3C O 195.7 O 199.0
CH3 O 205.5
杂化方式
SP3杂化(单键):0-80(烷 碳0-50) SP2杂化(双键、芳环):100-150(羰基碳150-220) SP杂化(叁键):70-100(炔碳50-90)
碳谱

• 影响δ值的因素
①取代基电负性对C-1δ值的影响很有规律性
②取代烷基的分枝越多,使C-1δ值增加越多
③重原子效应:可产生高场位移,碘的取代会 对C-1的共振产生很大的高场位移,溴的取代 也使C-1原子有高场位移
(5)羰基化合物
各类羰基化合物在13C NMR谱的最低场共振。 从低场到高场的次序是:
1. 碳谱的特点
• δ:13CNMR: 0~250 (1HNMR:0~10) • 可获得季碳、C=O、C=C、C=N和C=C等不
与氢相连碳的信息(吸收峰) • 可区别碳原子级数(伯、仲、叔、季),信息
比氢谱丰富 • 灵敏度低 • 邻近质子的偶合作用使谱峰变得非常复杂,必
须采用标识技术(去偶技术),13C 谱若不去偶 就不能解析。 • 13C谱化学位移的决定因素是顺磁屏蔽( 1H谱 化学位移的决定因素是抗磁屏蔽)
4.3 核磁共振碳谱
13C Nucleus Magnetic Resonance
% OF BASE PEAK
主120讲:何慧教授
100
90
80
70
65
60
92
50
40
30
165
M
137
93
20
10
0
0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 150 160 170
3
4.2
0
-8.1
算
0
值
138.5 113.6 159.9 117.7 129.4 120.0
137.4 111.4 158.5 118.5 128.4 118.5
• 苯的δ值为128.5ppm
tms碳谱

碳谱分析,主要研究的是13C核自旋磁矩,由于碳核自旋I=1/2,且自旋磁量子数mI=±1/2,因此,碳核可以发生双共振。
在一定条件下,可以用高能电子、中子、质子等作照射源,激发出核磁共振信号。
碳谱通常用来研究有机化合物的结构,尤其是那些不能用氢谱来研究的化合物。
碳谱的优点在于它能够提供更多的结构信息,如化学位移、偶合常数和峰面积比等。
这些信息可以帮助我们确定碳原子的连接顺序、取代基的数目和类型等。
然而,碳谱也存在一些局限性。
例如,碳谱的分辨率较低,因为碳原子在有机分子中的含量较少,且它们的化学位移范围较窄。
此外,碳谱的灵敏度也较低,因为碳原子的磁旋比小,且它们的共振频率较低。
以上内容仅供参考,如需更准确全面的信息,建议查阅相关的文献或咨询专业人士。
碳谱

CH3 C CH2 C CH3 53.5 25.3 29.9 CH3 H
CH3 CH CH2 18.7
CH3 CH2 CH3 15.7
3.炔烃
炔碳的化学位移值介于烷烃碳和烯碳之间, 取值范围约是65—90ppm
CH C CH2CH2CH2CH3
1 2 3 4 5 6
4.芳烃: 100~160ppm 苯环碳的化学位移值为128.5,取代基可使直接 相连的苯环碳高场或低场位移约±35ppm,对其 他位置的影响相对较小。
a.在呋喃、吡咯中,α-C的δ值比β-C的大, 即α-位是去屏蔽的,而在噻吩环中,α-C的 δ值比β-C的小,α-位是屏蔽的,β-位是 去屏蔽的。 b.杂环中的叔胺氮是吸电子的,对环有去屏蔽 作用,所以六元含氮杂环的碳与苯环相比, 多在较低场区,并且α-位与γ-位是去屏蔽 的,β-位受到一定的屏蔽。
3J 4J
OH
3.质子选择性去偶
质子选择性去偶是指定质子去偶,该法
可使待认定的13C核唯一地发生去偶,得
以与其他13C核区别。
4.无畸变极化转移技术(DEPT)
采用二种特殊的脉冲系列分别作用于高 灵敏度的1H核和低灵敏度的13C核,将灵 敏度高的1H核磁化转移到13C核上,从而 大大提高13C核的观测灵敏度。
二、13C的信号裂分
13C 和 1H 均为磁性核,在一定键数范围内可通
过相互自旋偶合干扰。
13 13
C在氢谱中引起的偶合影响干扰极小。 C-13C间的同核偶合可以不予考虑。
由1H引起的异核偶合影响却表现得极为突出。
13
C-NMR 中, 13C 信号因 1H 核偶合产生的裂 分数仍遵守n+1规律: 例:q(CH3)、t(CH2)、d(CH)、S(C) 偶合常数值很大。1JCH≈120~150Hz,且 同时存在2J、3J范围内的远程偶合,使信 号进一步裂分,形成更为复杂的图谱。
有机化学——碳谱

所以在早期的核磁共振研究中,一般只研究1H NMR,直到上个世纪 70 年代脉冲 傅立叶变换核磁共振谱仪问世,13C NMR才迅速发展起来,测试技术和方法也在 不断的改进和增加,从碳谱中可以获得极为丰富的信息。
0= B0
射频场H1
I
1 2
0
B0 2
I 1 2
B0
B0 14092(高斯)
z
M = 宏观磁化强度矢量 B0 = 磁场强度
x
M
y
2.脉冲傅里叶变换技术
一个时间域函数f(t)也可以用频率域F(ω)表示,二者 包含完全相同信息,只是描述形式不同而以,它们之间的 变换关系 f(t)↔F(ω)称为傅里叶变换。
若射频(H1)以脉冲射频方式照射样品(脉冲宽度τ=10~ 50μs,周期T=1~5s)时,由该调制脉冲磁场的频谱可见 ,它相当于在ω1附近采用n台强度基本相等,频率相差 2π/T的射频发动机(包括使所有核同时共振的频率)同时 照射样品。
碳信号的个数以及每个碳信号的化学位移值是 整个碳谱给我们最有价值的信息。 化学位移值与什么因素有关呢?不同的结构片 段特征的化学位移值是多少呢?
羰基碳200
酯基碳170 苯环碳110-140
苯环连氧碳155
缩酮(醛)110 连氧碳60-80 甲氧基55 甲基碳10-20
感
一般情况下,对于宽带去偶的常规谱,几乎化合物的每 个不同种类的碳均能分离开
碳杂化轨道 诱导效应 空间效应
内因
超共轭效应
重原子效应 测定条件:溶解样品的溶剂、溶液的浓度、测定时的温 度等
外因
碳杂化轨道
sp3 CH3 < CH2 < CH < 季C sp2 -CH=CH2 在较高场 0 ~ 50 ppm
碳谱

2.15(1H, m)
-1.96(1H, brs) 1.98(1H, brs) 2.54(1H, m) -2.66(1H, d, J=14.0Hz) 3.65(1H, dd , J=14.0, 2.9Hz) -5.39(1H, brs) 2.18(1H, m) 0.89(3H, d, J=6.8Hz) 0.97(3H, d , J=7.0Hz) 3.92(1H, brd, J=12.0Hz) 3.95(1H, brd, J=12.0Hz)
2
碳谱(13C-NMR):必记基础数据
常见一些基团的化学位移值: 脂肪C: <50 连杂原子C: C-O,C-N 40-100 C-OCH3 : 50-60
糖上连氧C: 60-90
糖端基C : 90-110 炔C: 60-90 芳香碳,烯碳: 120-140 连氧芳碳,烯碳:140-170;其邻位芳碳,烯碳:90-120
O
OH
7 8 9 10 11
1α-hydroxy-10β, 14- epoxy curcumol
12 13 14 15
Note: 1. 400 MHz for 1H-NMR, 100MHz for 13C-NMR. 2. Using CD3OD as a solvent, TMS is the internal standard, the chemical shifts (δ) are expressed in ppm and the coupling constant J in Hz.
C=O: 160-220
3
必记基础数据
C=O: 160-220
酮: 195-220
醛: 185-205
醌: 180-190
羧酸: 160-180
c谱中双二重峰与四重峰的区别

c谱中双二重峰与四重峰的区别在核磁共振(NMR)光谱中,二重峰(doublet)和四重峰(quartet)是两种常见的偶合常数。
它们分别表示两个或四个核自旋之间的相互作用。
在C谱(碳谱)中,双二重峰和四重峰的区别主要体现在它们的化学位移、耦合常数和积分面积等方面。
1. 化学位移化学位移是指核磁共振信号在磁场中的偏移程度,通常用ppm(百万分之一)表示。
在C谱中,双二重峰和四重峰的化学位移主要取决于核自旋所处的环境。
一般来说,双二重峰的化学位移较小,而四重峰的化学位移较大。
这是因为四重峰中的两个相邻的核自旋之间的相互作用较强,导致它们在同一环境中的化学位移差异较大。
2. 耦合常数耦合常数是指两个或多个核自旋之间的相互作用强度,通常用赫兹(Hz)表示。
在C谱中,双二重峰和四重峰的耦合常数主要取决于核自旋之间的相互作用距离和方向。
一般来说,双二重峰的耦合常数较小,而四重峰的耦合常数较大。
这是因为四重峰中的两个相邻的核自旋之间的相互作用较强,导致它们的耦合常数较大。
3. 积分面积积分面积是指核磁共振信号在图谱上的面积大小,通常用高斯(Gaussian)表示。
在C谱中,双二重峰和四重峰的积分面积主要取决于核自旋的数量和相互作用强度。
一般来说,双二重峰的积分面积较小,而四重峰的积分面积较大。
这是因为四重峰中的两个相邻的核自旋之间的相互作用较强,导致它们的积分面积较大。
4. 分辨率分辨率是指核磁共振光谱中不同信号的分离程度,通常用单位赫兹(Hz)表示。
在C谱中,双二重峰和四重峰的分辨率主要取决于核自旋之间的相互作用距离和方向。
一般来说,双二重峰的分辨率较高,而四重峰的分辨率较低。
这是因为四重峰中的两个相邻的核自旋之间的相互作用较强,导致它们的分辨率较低。
5. 信噪比信噪比是指核磁共振光谱中信号与噪声的比例,通常用对数表示。
在C谱中,双二重峰和四重峰的信噪比主要取决于核自旋的数量和相互作用强度。
一般来说,双二重峰的信噪比较高,而四重峰的信噪比较低。
第三章第六节 波普学核磁共振碳谱 2

选择某特定的质子作为去耦对象,用去耦频率照射该特 定的质子,使被照射的质子对13C的耦合去掉,13C成为单峰, 以确定信号归属。(略)
3、门控去耦p134
4、反转门去耦p135
三、 13C NMR化学位移及影响因素
(一)影响C的因素 1、碳原子的杂化轨道 一般规律:sp3杂化的碳共振吸收在=0-100范围 内,sp2杂化的碳在=100-210范围内,
C(K)=123.3+∑Aki(Ri)+∑ A’ki(R’i) + ∑ S(修正
值)
-C—C-C-C=C-C-C-C-
k k
’ ’ ’
式中Aki(Ri)表示在碳链中第i位置引入取代基Ri对烯碳 k的化学位移的增值。 R’i为双键另一边的取代基位置。 各种取代基Aki和A’ki参数及修正值S见表4.11
宽带去耦的缺点是只能帮助确定化合物中碳的种数, 但不能像1HNMR图谱一样用峰的强度衡量各种碳的个 数。图中四个峰各代表一种碳。
除了宽带去耦还有四种去耦方法: 1、不完全去耦(偏共振去耦) 在进行H去耦时,将去耦频率放在偏离H共振中心频率 几百到几千赫兹处,这样在谱中出现几十赫兹以下的J C-H, 而长距离耦合则消失了,从而避免谱峰交叉现象,便于识 谱。利用不完全去耦技术可以在保留NOE使信号增强的同 时,仍然看到CH3四重峰,CH2三重峰,CH二重峰,不与H 直接键合的季碳等单峰。 2、选择去耦
-210范围内。
1、烷烃13C化学位移
计算经验式:
i=-2.6+9.1n+9.4n-2.5n 分别为i碳原子、和 位所连接碳原子的个数。
例 CH3-CH2-CH2-CH2-CH3
1 2 3 4 5 式中, i为i碳原子的化学位移, n、n和n
碳谱碳同位素峰

碳谱碳同位素峰
碳谱(Carbon Spectrum)通常是指通过核磁共振技术来测定有机化合物中碳原子的化学环境。
在这个过程中,碳同位素(尤其是^13C)起到了关键作用,因为它们的核自旋不为零,可以在核磁共振仪器中产生信号。
碳同位素峰在碳谱中表现为不同的化学位移,这些位移反映了碳原子所处的化学环境。
例如,与碳原子相连的氢原子数量、相邻碳原子的取代基、以及与碳原子形成双键或三键的其他原子等因素都会影响碳同位素峰的化学位移。
在解读碳谱时,需要注意以下几点:
1.化学位移:不同化学环境的碳原子在碳谱中的化学位移不
同。
一般来说,化学位移越大,表示该碳原子的电子云密度越低,即该碳原子所处的环境越趋于缺电子状态。
2.峰形:碳谱中的峰形可以反映碳原子的数量和它们之间的
连接方式。
例如,单个峰通常表示一个独立的碳原子,而多重峰可能表示存在多个相邻的碳原子。
3.峰强度:峰强度与碳原子的数量成正比。
在定量分析中,
可以通过比较不同峰的强度来确定化合物中各种碳原子的比例。
总之,碳谱是一种非常有用的分析工具,可以帮助化学家了解有机化合物的结构和性质。
而碳同位素峰则是碳谱中的关键信息,通过解读这些峰的化学位移、峰形和峰强度,可以推断出有机化合物中碳原子的化学环境和连接方式。
怎么解析碳谱

怎么解析碳谱碳谱是一种分析物质结构的方法,利用了同位素碳13和碳12的不同比例来推断化合物的结构。
碳谱在有机化学领域中非常重要,可以帮助研究人员识别和确定有机分子的结构。
本文将介绍碳谱的解析方法和基本原理,以及一些常见的谱线和它们所代表的结构。
1. 碳原子和碳谱的基本原理碳谱是基于核磁共振(NMR)技术的,利用同位素碳13和碳12的不同比例来识别和确定分子中的碳原子的环境和连接方式。
在自然界中,碳原子最常见的同位素是碳12,而稀有同位素碳13的含量仅约为1%。
因此,利用碳谱来分析组成碳12和碳13的化合物,可以通过谱峰的强度和位置来区分不同的结构和类型。
2. 通过解析谱峰来推断结构碳谱可以通过观察不同化合物的峰形和谱线特征来推断结构。
其中,主要有四种谱线:甲基(methyl)、甲烷(methylene)、亚甲(methine)和芳香(aromatic)。
- 甲基峰一般在20-30 ppm的化学位移范围内,是因为甲基中没有其他质子或惰性原子与碳原子相连。
它的峰形类似于单个尖锐的峰。
- 甲烷峰在30-40 ppm,因为甲烷中有一个氢原子与碳原子相连,它的峰形类似于一对上下对称的峰。
- 亚甲峰在40-60 ppm,其中一个碳原子与两个氢原子相连,它的峰形类似于单个峰。
- 芳香峰在120-200 ppm间,通常是分离的,呈现单条或多条肩峰的峰形。
3. 确定化学位移来推断结构化学位移是指在不同环境下的碳原子的吸收频率。
通过测量不同环境下的碳原子的化学位移,可以推断分子中不同碳原子的环境和连接方式。
例如,苯环中的碳原子各不相同,对应的峰形也会不同。
最外层的邻位(ortho)碳原子和对位(para)碳原子的化学位移大约在130-140 ppm之间。
而邻位和对位之间的甲基碳原子的化学位移通常在20-30 ppm之间。
4. 结语总之,碳谱是物质结构分析的重要工具。
通过测量不同的化合物的谱线和化学位移,可以定量分析和推断原子的环境和结构。
碳谱二级耦合常数范围

碳谱二级耦合常数范围
碳谱二级耦合常数是指在核磁共振(NMR)碳谱中观察到的两个
不同碳原子之间的耦合常数。
这个数值通常以赫兹(Hz)为单位。
耦合常数的范围可以根据不同的化合物和实验条件而变化,但一般
来说,对于^13C-NMR谱,二级耦合常数的范围大约在0到250赫兹
之间。
这个范围是根据实验观察得出的,不同的化合物、溶剂、温
度等因素都会对耦合常数产生影响。
需要注意的是,二级耦合常数的具体数值受到多种因素的影响,包括化学环境、分子构型、溶剂效应等。
在实际的NMR实验中,可
以通过调整实验条件和对比标准化合物的谱图来确定具体化合物的
二级耦合常数范围。
此外,现代NMR仪器的高灵敏度和先进的数据
处理技术也使得对二级耦合常数的测定更加精确和可靠。
总的来说,二级耦合常数在碳谱中是一个重要的参数,其范围
可以根据具体的化合物和实验条件而变化,需要通过实验测定来获
得准确的数值。
对于化学研究和结构分析来说,理解和确定二级耦
合常数的范围对于解释NMR谱图和推断化合物结构具有重要意义。
双二重峰 碳谱xps

双二重峰碳谱(Double Doublet Carbon Spectroscopy,简称DD-C)是一种用于分析材料表面化学成分的表征技术。
它通过测量样品在电子束照射下产生的二次电子和俄歇电子的能量分布,从而获得材料的化学信息。
DD-C具有高灵敏度、高分辨率和非破坏性等优点,因此在材料科学、纳米技术和生物医学等领域得到了广泛应用。
X射线光电子能谱(X-ray Photoelectron Spectroscopy,简称XPS)是一种用于研究材料表面元素组成和化学状态的表征技术。
它通过测量材料表面在受到X射线激发后发射出的光电子的能量和强度,从而获得材料的化学信息。
XPS具有高灵敏度、高分辨率和快速扫描等优点,因此在材料科学、半导体工业和环境科学等领域得到了广泛应用。
将DD-C与XPS相结合,可以更全面地了解材料表面的化学成分和结构特征。
例如,DD-C可以提供关于碳原子的价态和结合方式的信息,而XPS可以提供关于其他元素(如O、N、S等)的化学状态的信息。
此外,DD-C还可以用于定量分析,通过比较不同样品的双二重峰信号强度,可以计算出各元素的相对含量。
总之,双二重峰碳谱和X射线光电子能谱是两种互补的表面分析技术,它们在材料科学、纳米技术和生物医学等领域具有广泛的应用前景。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
由IR图谱中的1690和1575cm-1以及1200cm-1附近的宽峰可知,分子 中应含有α,β不饱和酯官能团。图中发现没有S-H的振动吸收,说明S 原子应与C或O原子相连。
NMR谱中各种H的比值为5:1:1:2:3。δ6、7附近的两组双峰 构成AB系统,这是两个烯碳上的H,证实了IR谱α,β不饱和酯的论断。δ= 7.3的5个H应是苯环氢,说明是单取代苯。δ= 3.7的3个H,应是CH3O-。 MS图谱中存在(M-31)和(M-59)峰也支持甲酯基-CO-OCH3推断。
MS
从MS图谱可知,分子离子质量为208,从M+2峰的强度可知分子内含有 1个S原子。M+1峰的强度扣除S的贡献(0.8%)之后,可计算得该化合物 含有11个C。由M+2峰减去C和S的贡献计算得O原子的数目为2,进而求得 H原子数目为12。所以分子式为C11H12O2S。UN = 6,可能有苯环。(M-91) 以及m/z = 91的离子峰存在说明分子中可能含有苄基。
13C和DEPT-NMR显示有10个碳原子,其中包括1个
甲基碳原子,2个亚甲基和2个次甲基,但是这些与MS 所给出的分子量不符合,提示可能是对称结构。结合 MS,可以得出有一个甲基,二个亚甲基,四个次甲基。 在13C-NMR中,高场的δC 22.5表示这是甲基,由其 化学位移可知,这个碳原子与羰基相连。由δC 35.7, δC 42.4的两个亚甲基可以知道,一个与苯环相连,另 一个与氨基相连。δC 116.2和δC 130.7是苯环上的碳。 δC 116.2可知这是苯环上连接有烷基碳原子。δC 130.7 为连接有羟基的碳原子。根据质谱给出的分子量和13CNMR、1H-NMR给出的信息,可以判断苯环为对位取代。
13C-NMR(100MHz,氘代吡啶)δ(ppm):
171.5(s), 165.5(s), 60.9(d), 51.2(d), 32.2(d), 20.9(q), 19.1(q), 17.1(q).
O NH O NH
例6:C6H10O2 的 δ(ppm) 14.3 谱线多重性 q
13C
NMR 的数据
振动类型
归属
芳氢伸缩振动 苯环骨架振动 C6H5苯环CH面外弯曲 CH伸缩振动 C=C伸缩振动 -C=CH2 C=C面外弯曲 C-O伸缩振动 -O-
图3. C9H10O的核磁共振氢谱图
氢分布:a:b:c:d:e:f=2:1:1:1:3:2
1.δ4.4双重峰,与一个H偶合, 且δ高于一般 亚甲基说明 与O相连,可能是O-CH2-CH 2.δ5.2,5.3,5.9为三个稀氢, 可能是ABC偶合系统,可能 含有CH2=CH3.δ7.0多重峰,为O和苯环相 连的单取代苯峰形,是A2B3 高级偶合系统。
1H
由13C NMR图谱信息可知分子中存在甲基、亚甲基、烯碳、苯环碳、 羰基碳。 δ值(ppm):166.9 羰基碳,148.8 和羰基相连的烯碳,137.2 和亚甲 基相连的苯基碳,129.0、128.8、127.5 苯基碳,113.2 烯碳,51.2 甲基 碳,39.4 亚甲基碳。
综上所述可以得出该化合物的几个片段:
化合物可能的结构为:
CH2=CH-OCOCH2(CH2)6CH2COO-CH=CH2
例3
O
不饱和度U=5 可能含有苯环
例4. 由质谱测得未知化合物的分子式为C9H10O。 试通过该未知物的质谱图(图1),红外吸收光 谱(图2),核磁共振氢谱(图3),核磁共振碳 谱(图4),进行综合解析,以确定其化学结构。 已知:由紫外可见光谱可知,未知物溶液的最大 吸收波长为267.5nm。
6.5. 13C NMR谱的解析
13C
NMR谱解析的一般程序:
(1)由分子式计算不饱和度。 (2)分析13C NMR的质子宽带去偶谱,识别重氢剂峰,排除其干扰。 (3)由各峰的δ值分析sp3、sp2、sp杂化的碳各有几种,此判断应与不 饱和度相符。若苯环碳或烯碳低场位移较大,说明该碳与电负性大的氧或 氮原子相连。由C=O的δ值判断为醛、酮类羰基还是酸、酯、酰类羰基。 (4)由偏共振谱分析与每种化学环境不同的碳直接相连的氢原子的数目, 识别伯、仲、叔、季碳,结合δ值,推导出可能的基团及与其相连的可能 基团。若与碳直接相连的氢原子数目之和与分子中氢数目相吻合,则化合 物不含-OH、-COOH、-NH2、-NH-等,因这些基团的氢是不与碳 直接相连的活泼氢。若推断的氢原子数目之和小于分子中的氢原子,则可 能有上述基团存在。 在sp2杂化碳的共振吸收峰区,由苯环碳吸收峰的数目和季碳数目, 判断苯环的取代情况。
55.6 q
132.7 137.9
谱线多重性
d
s
d
s
s
不饱和度为4。有两个甲氧基、取代苯环、端烯存在
OCH 3
OCH 3
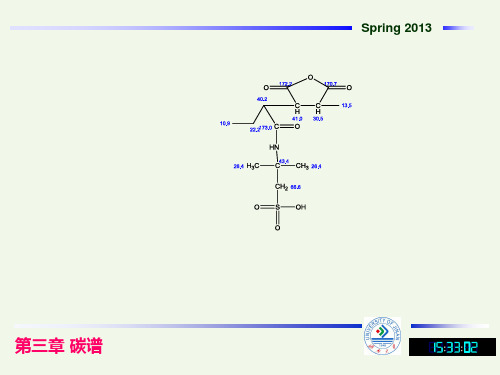
例8. N-(p-Hydroxyphenethyl)acetamid是从放线菌内分离得到的一个化
合物。此化合物为白色结晶,该化合物在显色时可与H2SO4烘烤过后碘化 铋钾显色呈现桔黄色,提示其可能为一个酰胺类的化合物。根据1H-NMR 和13C-NMR以及MS可知化合物分子式为C10H13NO2。
+
-CH =CH2+ m/z 27C 4 H3 +
C 5 H5 +
m/z 51
m/z 65
例5: 从云南某著名中草药中分离得到一无色针状结晶,与茚三酮反应 呈阴性,但将该化合物水解后呈阳性;其红外光谱在3300、1650cm-1 处有明显吸收;其质谱显示分子离子峰为m/z 170;其核磁共振波谱数 据如下,试推断其化学结构。 1H-NMR(400MHz,氘代吡啶)δ(ppm): 9.25(1H,br.s), 8.98(1H,br.s), 4.35(1H, m), 4.13(1H, m), 2.67(1H, m), 1.66(3H, d, J=4.0Hz), 1.14(3H, d, J=8.0Hz), 1.07(3H, d, J=8.0Hz);
例1:化合物的分子式为C10H13NO2,其质子宽带去偶谱(a) 及偏共振谱(b)如下图所示,试推导其结构。
解:C10H13N,UN = 10 + 1 + 1/2 – 13/2 = 5,可能有苯 基, 40.9 ppm为溶剂峰,有三种sp3杂化的碳,五种 sp2杂化的碳,谱峰数小于碳数目,存在对称因素。 (对位取代)已知的氢原子数为12,有1个氢没连在碳 原子上,(可能为NH),分子中可能有下列基团: OCH2CH3, NH, CH3, C=O, -Ph-O sp3C : 14.7 CH3-C;23.8 CH3-C; 63.3 CH2-O
17.4 60.0 123.2 144.2 166.4 q t d d s
有六个数据,表明有六种 C,与分子式中 C 的数目相 同,说明 C 没有对称性。
CH3-CH2-O-CO-CH=CH-CH3
例7:C11H14O2 的 δ(ppm) 谱线多重性 δ(ppm) 39.9 t 120.7
13C
NMR 的数据 55.7 q 111.9 d 147.9 112.5 115.5 d 149.4 t
位置
δH
C δ
OH
1
2 3 4 5
——
7.02, d, J=9.2 6.71, d, J=8.5
131.2
130.7 116.2 156.9
6.71, d, J=8.5 7.02, d, J=9.2 3.33, t, J=7.5 2.69, t, J=7.5 —— 1.89, s, Me
sp2C: 114.5: 2CH;121.0 2CH, 132.7 C;154.8
C-O; 168.2 C=O
化合物可能的结构为:
CH3NHCO (a) OCH2CH3 CH3CONH (b) OCH2CH3
己知:sp3C 23.8 CH3-C, 计算值:在前一结构中,取代参数为37, -2.5 + 37 = 34.5 后一结构中取代参数为22 -2.5 + 22 = 19.5 因此(b)为可能的结构。
为苯环B带的 特征吸收
图1. C9H10O的质谱图
强度最高为 CH2=CH-CH2+
C6H5-OH麦氏 重排离子峰
分子离 子峰M+
结论:
化合物应含 C6H5-O基 丙稀基
77,65,51,39均为苯环的特征离子
图2. C9H10O 的红外吸 收光谱图
吸收峰cm-1
3030 1600,1490 760,690 3060 1650 990,920 1240,1030
a峰:-CH2-
稀丙基苯醚 C6H5- O-CH2 -CH =CH2
由质谱验证:
C6H5- O-CH2 -CH =CH2 -CH2 -CH =CH2+ m/z 41 C 6 H5 + m/z 77
C6H5- O-CH2 -CH =CH2+(M+ m/z 134) C6H5-OH + m/z 94 C7H7 m/z + 91 C 3 H3 m/z 39
该化合物的不饱和度UN=6 从IR分析:1750 cm-1(s)为υC=O的吸收峰。 1630 cm-1(s)为υC=C的吸收峰。 1600 cm-1(s);1580 cm-1(s);1510 cm-1(s)为苯 环骨架振动。820 cm-1(s)为苯环上两个相邻氢的面外弯曲 振动,可表明为对位取代。
2个一价基团和1个二价基团只有一种拼接方式,结合1H NMR图谱AB系 统的偶合常数约为10Hz可知碳碳双键上的H是顺式,得出未知化合物的 分子式:
例10. 化合物C14H18O4的MS,IR,1HNMR,13CNMR谱的数据如 下,请推导其化学结构。 IR:2960 cm-1(s);2780 cm-1(s);1750 cm-1(s);1630 cm1(s);1600 cm-1(s);1580 cm-1(s);1510 cm-1(s);1450 cm-1(s)(m); 1380 cm-1(s)(w) 820 cm-1(s);1100~1300 cm1(s)(宽,强)。
