高中化学 专题第一单元第3课时 元素周期表及其应用学案 苏教版必修2
苏教版高中化学必修二课件1.1.3元素周期表及其应用

【变式备选】下列各表为元素周期表的一部分(表中数字为原 子序数),其中正确的是( )
【解析】选D。由元素周期表可知:A项中2、3、4不能在同一 横行(周期),且3、11、19为第ⅠA族应在元素周期表的最左边, A错误;B项中2、10、18为0族应在元素周期表的最右边,B错 误;C项中6、12、24不应在同一纵行(族),C错误;D项完全符合 元素周期表,D正确。
内容
同周期元素(左→右,0 同主族元素(上→
族元素除外)
下)
金属性与 非金属性
金属性逐渐减弱 非金属性逐渐增强
金属性逐渐增强 非金属性逐渐减弱
单质的还原性 与氧化性
还原性逐渐减弱 氧化性逐渐增强
还原性逐渐增强 氧化性逐渐减弱
非金属元素的 气态氢化物
生成由难到易 稳定性由弱到强
生成由易到难 稳定性由强到弱
类型一元素周期表的结构 【典例】下列关于元素周期表的说法中,正确的是( ) A.元素周期表是按照元素的相对原子质量大小排布而成的 B.元素周期表共有7个周期16个族 C.过渡元素都是金属元素,第ⅠA族都是金属元素 D.最外层电子数相同的元素都在同一族
【解题指南】解答该题要注意以下3点: (1)元素周期表的编排依据是原子序数。 (2)7个横行7个周期,18个纵行16个族。 (3)第ⅠA族包括氢和碱金属。
ⅦA族
含的元素种数
能容纳的元素种数)
2.性质与位置的互推: (1)根据元素的性质可以推知元素在周期表中的位置: 若同周期元素A、B、C的金属性逐渐增强,则A、B、C在同周期 中按照C、B、A的顺序从左到右排列。 (2)根据元素在周期表中的位置关系可以推断元素的性质:若 同主族元素A、B、C在同一主族中从上往下排列,则可推知A、 B、C的单质的氧化性依次减弱或还原性依次增强。
苏教版高中化学必修二课件第3课时元素周期表及其应用

灿若寒星整理制作
第3课时 元素周期表及其应用
如图是1869年门捷列夫发表的第 一张元素周期表。 【思考】 (1)门捷列夫开始是按照什么原 则来排列元素的? (2)现在的元素周期表编排的依 据是什么? (3)哪种依据更科学呢?
1.能描述元素周期表的结构。了解元素周期表的 意义与应用。 2.知道同主族、同周期元素原子核外电子排布、 元素化学性质的递变规律。(重点) 3.了解元素周期表中金属元素、非金属元素的分 布。了解主族元素在元素周期表中的位置、原子 结构、元素性质三者之间的关系。(重点)
第3周期,VIA族。
2.某元素位于第2周期,ⅦA族,它是_氟__元素。
元素得、失电子能力与元素在周期表中位置的关系
族 周期
IA IIA ⅢA IVA VA
VIA ⅦA
1
得电子能力逐渐增强
2
失 电
B
得
金属和非
电
3子
Al Si
金属分界线
子
能 4力
Ge As
能 力
5 6
逐 渐 两性,半导体 增 强
Sb Te Po
发现的
主族
I A
族的结构
零族
0
1 1 II
A
23 4
副族
Ⅷ族
2 III IV V VI VII
K2
AA A AA
ห้องสมุดไป่ตู้
5
6
7
8
9
10
L K
8 2
3 11
12
III IV BB
V B
VI B
VII
B
VIII
I B
II B
13 14 15 16 17 18
高中化学苏教版必修2课件:专题1第一单元第三课时 元素周期表及其应用
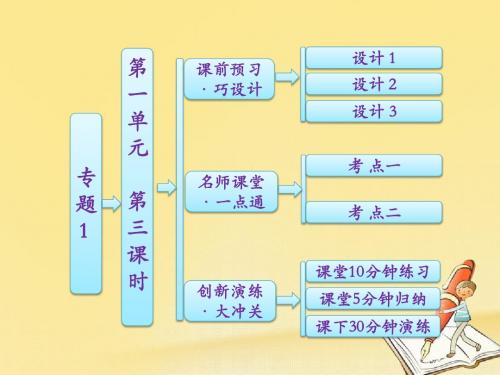
增多 电子层数 ―→ 增大 原子半径
―→
增强 失电子能力 增强 元素金属性 ―→ 得电子能力 减弱 非金属性 减弱
―→
3.金属元素和非金属元素的分区
(1)分界线:
(2)元素性质:
①金属性最强的元素为 Cs (除放射性元素);
②非金属性最强的元素为 F ; ③分界线附近的元素既表现出一定的 金属性 ,又表现 出一定的 非金属性 。
答案:(1) √ (2) × (3) × (4) ×
4.完成下列填空:
(1)同主族相邻两元素的原子序数之差可能为
________________________________________________ ________________________; (2)x为第ⅡA族元素原子序数,则同周期第ⅢA族元素 原子序数可能为____________________________。
②在 过渡 元素中寻找各种优良的催化剂及耐高温、耐腐蚀的合 金材料。
1.连连看。
①ⅠA族(氢除外)
②ⅦA族 ③0族 ④过渡元素
a.卤族元素
b.稀有气体元素 c.副族和第Ⅷ族 d.碱金属元素
分析:要熟悉第ⅠA族、ⅦA族、0族的俗称及过渡元素
的内容。
答案:①—d ②—a ③—b ④ —c
2.填空。
(6)铁元素在周期表中的位置:______________。
分析:在元素周期表中元素种类最多的族是第ⅢB族(含有 镧系元素和锕系元素),元素种类最多的周期是第6周期(32 种);7个主族中,只有第ⅡA族全为金属元素,第ⅦA族全 为非金属元素,且第ⅦA族单质中F2、Cl2为气体,Br2为液
体,I2为固体;(6)铁元素在周期表中位于第4周期第Ⅷ族。
江苏省江阴市成化高级中学高中化学 元素周期表及其应用教案 苏教版必修2

第一单元原子核外电子排布与元素周期律第三课时:元素周期表及其应用【三维目标】知识与技能目标:使学生了解元素周期表的结构以及周期、族等概念;使学生理解同周期、同主族元素性质的递变规律,并能运用原子结构理论解释这些递变规律;使学生了解原子结构、元素性质及该元素在周期表中的位置三者间的关系,初步学会运用周期表;使学生了解元素周期律和周期表的意义,认识事物变化由量变引起质变的规律,过程与方法目标:通过自学有关周期表的结构的知识,培养学生分析问题、解决问题的能力。
具有把元素周期表的位置与元素组成微粒的结构初步联系起来并在一定条件下相互转化的运用能力。
情感态度与价值观目标:通过对元素性质的递变规律与元素组成微粒结构的联系。
从而认识事物变化过程中量变引起质变的规律性,接受辨证唯物主义观点的教育。
【教学重点】周期表结构、元素性质、元素在周期表中的位置与原子结构的关系。
【教学难点】元素的性质、元素在周期表中的位置和原子结构的关系。
【复习】元素周期律;【引入】把已知的元素按元素周期律排成一个表格,这就是元素周期表。
【展示】元素周期表。
(元素周期表有不同的形式,我们这里介绍的是其中一种常见的形式;它的编排原则是:根据元素周期律,按原子序数递增的顺序从左到右从上到下的排列,把电子层数目相同的排成一个横行;再把最外层电子数相同的排成一个纵行。
这样就得到我们目前的这个表格,这个表就叫元素周期表。
)【过渡】下面我们就来认识元素周期表的结构。
请大家数一数元素周期表有多少个横行?(有7个横行)【讲评】我们把每一个横行称作一个周期,所以元素周期表共有7个周期,从上到下,依次为第一周期、第二周期、……。
把不同的元素排在同一个横行即同一个周期的依据是什么?请大家以第2周期和第3周期的元素为例进行思考。
分析每一周期元素在结构上有何共同点?(电子层数相同且等于周期序数)【板书】一元素周期表的结构1周期:周期序数=电子层数①除第1周期只包括氢和氦,第7周期尚未填满外,每一周期的元素都是从最外层电子数为1的碱金属开始,逐步过渡到最外层电子数为7的卤素,最后以最外层电子数为8的稀有气体结束。
高一化学 专题1第一单元第3课时 元素周期表及其应用 苏教版必修2

3.第3周期元素X的气态氢化物化学式是H2X, 下列叙述不正确的是( ) A.该元素的原子最外电子层上只有两个电子 B.该元素最高价氧化物的化学式为XO3 C.该元素是非金属元素 D.该元素最高价氧化物对应水化物的化学式是
H2XO4 答案:A
课堂互动讲练
要点一 由原子序数确定元素位置的方法
1.比大小定周期 比较该元素的原子序数与0族元素的原子序数大小, 找出与其相邻近的0族元素,那么该元素就和原子 序数大的0族元素处于同一周期。 2.求差值定族数 (1)若某元素原子序数比相应的0族元素多1或2,则 该元素应处在0族元素所在周期的下一个周期的ⅠA 族或ⅡA族。
二、同主族和同周期元素性质的递变
1.同周期元素性质的递变
同周期元素(除稀有气体元素外)中,随着核电荷数增 多,原子半径逐渐_减__小__,原子核对最外层电子的吸 引力逐渐_增__强___,原子失电子能力逐渐__减__弱_,得电 子能力逐渐_增__强___,所以元素的金属性逐渐_减__弱__, 非金属性逐渐_增__强___。
2.同主族元素性质的递变 同主族元素中随着核电荷数增多,原子半径逐渐__增_ _大_,原子核对最外层电子的吸引能力逐__减__弱_,原子 失电子能力逐渐_增__强__,得电子能力逐渐_减__弱___。所 以元素的金属性逐渐增__强___,非金属性逐渐_减__弱__。
3.金属元素和非金属元素的分区 (1)分界线
三、元素周期表的应用
1.位、构、性之间的关系 (1)元素的_原__子__结__构___决定了元素在周期表中的位
置。 (2)元素在周期表中的位置反映了元素的原__子__结__构__ 和元素的_性__质____特点。
2.应用 (1)根据元素在周期表中的位置,推测元素的_原__子_ _结__构___,预测其主要_性__质______。 (2)研究合成新物质 ①在金属和非金属的分界线附近寻找半__导__体____材 料(如_S__i、__G__e、___S_e___等); ②在_过__渡____元素中寻找各种优良的催化剂及耐高 温、耐腐蚀的合金材料。
2024-2025年高中化学专题1第1单元第3课时元素周期表及其应用教案苏教版必修2
4.教学手段:
-小组讨论,让学生合作探索元素周期表的规律。
-实验操作,通过实际操作来加深对元素周期表的理解。
-问题解答,鼓励学生提出问题并尝试解答,以巩固知识点。
教学实施过程
1.课前自主探索
教师活动:
-发布预习任务:提供元素周期表的PPT、视频和文档等资源,明确预习目标和要求。
1.学生已经学习了原子结构和元素的基本概念,对原子的组成和性质有一定的了解。
2.学生已经学习了化学反应的基本原理,对化学反应中元素的转化有一定的认识。
3.学生已经学习了物质的分类和性质,对不同类型的物质有一定的了解。
核心素养目标
本节课的核心素养目标包括:
1.提高学生的科学探究能力,通过观察、实验、分析等方法,让学生能够自主探究元素周期表的构成和规律。
-提供拓展资源:提供与元素周期表相关的拓展资源,如书籍、网站、视频等,供学生进一步学习。
-反馈作业情况:及时批改作业,给予学生反馈和指导。
学生活动:
-完成作业:学生认真完成老师布置的课后作业,巩固学习效果。
-拓展学习:学生利用老师提供的拓展资源,进行进一步的学习和思考。
-反思总结:学生对自己的学习过程和成果进行反思和总结,提出改进建议。
2.课中强化技能
教师活动:
-导入新课:通过讲解门捷列夫发现元素周期表的故事,激发学生对元素周期表的兴趣。
-讲解知识点:详细讲解元素周期表的构成、周期律及其应用,结合实例帮助学生理解。
-组织课堂活动:设计小组讨论、实验等活动,让学生在实践中掌握元素周期表的应用。
-解答疑问:针对学生在学习中产生的疑问,进行及时解答和指导。
-提交预习成果:学生将预习成果(如笔记、思维导图、问题等)提交至平台或老师处。
苏教版高一化学必修二专题一第一单元第三课时元素周期表 教案设计

《元素周期表》教学设计一、教学内容分析《元素周期表》是高中化学必修2专题一第一单元内容。
元素周期表是学习化学的基本工具,是高考的高频考点之一,是化学学科的基石。
元素周期表是学生学习了碱金属和卤素两族元素后,对元素周期律有了初步的理性认识的基础上,对元素周期律的一种表现形式的学习。
让学生了解元素周期律,认识元素周期表,体会元素在周期表中的位置、元素的原子结构、元素的性质(即元素周期表是学生学习了碱金属和卤素两族元素后,对元素周期律有了初步位、构、性)的关系,初步学会在元素周期律和元素周期表的指导下探究化学知识的学习方法;对化学1和初中学过的元素化合物知识进行整合;同时体会元素周期律、元素周期表在元素化合物学习中的重要指导作用。
二、教学对象分析学生在初三对1-20号元素的原子结构和元素周期表都有初步了解,但在学习中较多是用机械记忆的方法,对知识的理解不够深刻,易遗忘,解决实际问题的能力较低。
这节课内容又比较枯燥,如何激发学生的学习兴趣,如何引导学生从方法的高度来重新审视这一内容应成为教学设计的关键。
三、教学目标及教学重难点(一)知识与技能使学生初步掌握元素周期表的结构,以及周期、族等概念。
(二)过程与方法通过学生亲自动手编排元素周期表培养学生的抽象思维能力和逻辑思维能力;(三)情感、态度与价值观组织开展对问题的探究、讨论和发现规律,进一步培养主动探索、自主学习的习惯(四)教学重点掌握元素周期表的结构、周期,族的概念(五)教学难点理解元素周期表同一周期或族相邻两种元素原子序数之差四、教学方法、过程及整合点(一)用元素周期表作为教学的主题背景,使课堂教学“学不离表,表不离学”,从而突出重点。
(二)将周期表中潜在的规律转化为问题,设疑诱思,步步深入,从而突破学习难点。
五、教学过程六、板书设计一、元素周期表的结构短周期(1-3)2、8、8 周期(7个)长周期(4-6)18、18、32不完全周期(7) 26主族(A)7个副族(B)7个族(16个,18列)VIII族(8、9、10三列)1个0族:1个二、元素结构与位置周期数=电子层数最外层电子数=主族序数七、教学反思为圆满完成教学任务,教师要做好宏观调控,课前指导学生自主学习,熟悉前20号元素的名称、元素符号及原子结构示意简图。
苏教版高中化学必修2全套教案

化学必修2教案蔡本松专题一:微观结构与物质的多样性第一单元:原子核外电子排布与元素周期律第一课时一、教学目标课标内容:了解原子核外电子的排布会考考纲:1.了解核外电子的排布(B)2.能画出1~18号元素的原子结构示意图(B)教学目标:(一)知识与技能原子核外电子排布规律(二)过程与方法掌握原子核外电子排布规律,通过1-20号元素的原子和离子结构示意图的学习,扩展到主族元素的电子排布规律的认识,初步体会归纳与演绎的学习方法。
(三)情感与价值观通过原子核外电子排布规律,了解物质运动的复杂性和特殊性二、教学重、难点和突破方法教学重点:了解原子的结构,能画出1~18号元素的原子结构示意图教学难点:核外电子排布规律三、教学过程:1.创设情境,引入新课下表是构成原子的各微粒的一些参数,请根据表中所提供的信息回答问题:问题解决:1.原子是由、和三部分构成的。
2.在原子中,质量集中在上,其大小是由和之和决定的。
3.在原子中:==4.原子不显电性的原因:交流与讨论:原子核带正电荷,核外电子带负电荷,正负电荷相互吸引,那为什么电子不会落入原子核内呢?2.进行新课讲解:原子核外电子并不是静止的,而是绕原子核做高速圆周运动,它们之间的引力提供了圆周运动的向心力,有摆脱原子核对电子的吸引的倾向,所以,在不受外界影响的条件下,电子既不能被原子吸入核内,也不能离开核自由运动。
过渡:那么,多电子原子的核外电子是如何绕原子核作高速运动的呢?一、原子核外电子的排布1.核外电子运动特征科学探究:根据所给的一些数据,请你总结电子运动的特征①核外电子的质量:9.10×10-31kg②炮弹的速度2km/s,人造卫星7.8 km/s,宇宙飞船11 km/s;氢核外电子2.2×108m/s③乒乓球半径:4×10-2m;原子半径:n×10-10m结论:电子运动的特征是:电子质量,运动速度,运动空间范围。
过渡:在初中我们已经学过原子核外电子的排布规律,知道含有多个电子的原子里,电子分别在能量不同的区域内作高速运动。
苏教版化学必修2讲义:专题1 第1单元 第3课时 元素周期表及其应用

第3课时元素周期表及其应用
1.能描述元素周期表的结构。
2.知道同主族、同周期元素原子核外电子排布、元素化学性质的递变规律。
(重点)
3.了解元素周期表中金属元素、非金属元素的分布。
4.了解主族元素在元素周期表中的位置、原子结构、元素性质三者之间的关系。
(重点)
5.了解元素周期表的意义与应用。
[基础·初探]
1.编排原则
(1)横行:电子层数相同,每一个横行称为一个周期。
(2)纵行:最外层电子数相同,每个纵行称为一个族(第8、9、10纵行除外)。
2.结构
(1)周期(即横行)
(2)族(18个纵行,16个族)
[探究·升华]
[思考探究]
1.元素周期表中为什么把C、N、O、F、Ne等元素编排在同一周期?元素周期表中共有多少周期?1~6周期中各含有多少种元素?
【提示】C、N、O、F、Ne等元素原子的电子层数相同,故编排在同一周期。
元素周期表中共有7个周期;1~6周期中所含元素种数分别为2,8,8,18,18,32。
2.最外层电子数为2的元素一定在第ⅡA族吗?
【提示】不一定。
如He最外层电子数为2,但为0族元素。
3.对主族元素,如何根据原子结构示意图确定主族元素在周期表中的位置?
【提示】在原子结构示意图中,原子所具有的电子层数,即该元素的周
期序数,最外层电子数即该元素的主族序数。
苏教版高中化学必修二课件:专题1 第一单元 原子核外电子排布与元素周期表——元素周期表及其应用(2)

2.下列关于元素周期表中第三周期元素性质从左到右变 化趋势的叙述错误的是( B ) A.最高正价依次升高 B.原子半径逐渐增大
C.气态氢化物稳定性逐渐增强
D.最高价氧化物对应的化合物碱性减弱, 酸性增强
3. 短周期元素中,
Na a. 与水反应最剧烈的金属是_____
b.与水反应最剧烈的非金属是_____ F
“位置”、“结构”、 “性质”
原子序数=质子数=核电荷数 周期序数=电子层数 主族序数=最外层电子数
位置
结构
推测
性质
左到右, 半径↓, 金属性↓, 非金属性↑;
上到下, 半径↑, 金属性↑, 非金属性↓;
内容 原子半径 电子层数 最外层电子 失电子能力 得电子能力
同周期(从左到右) 大→小 相同 1→8 减小 增大 减弱 增强 +1→+7, -4 →-7 碱性减弱 酸性增强 形成:难→易 稳定性:弱→强
1. 最外层电子数 2.化合价变化 3.原子半径增大
失电子
4. 金属性
还原性
得电子
推测
判断
1).最高价氧化物对应水化物碱性变强; 2).单质与水(或酸)反应, 置换H2变易; 3).活泼金属置换较其不活泼金属。
1).最高价氧化物对应水化物酸性减弱; 非金属性 2).与H2化合变难及氢化物稳定性减弱; 判断 3).活泼非金属置换较其不活泼非金属。 氧化性 推测
失电子
4. 金属性
还原性 得电子
推测
判断
1).最高价氧化物对应水化物碱性减弱; 2).单质与水(或酸)反应, 置换H2变难; 3).活泼金属置换较其不活泼金属。
1).最高价氧化物对应水化物酸性增强; 非金属性 2).与H2化合变易及氢化物稳定性增强; 判断 3).活泼非金属置换较其不活泼非金属。 氧化性 推测
高中化学苏教版必修2课件:1.1.3元素周期表及其应用

2.判断正误(正确的打“√”,错误的打“×”)。 (1)现行元素周期表中的元素是按相对原子质量由小到大排列 的。( × ) (2)元素周期表揭示了化学元素间的内在联系。( √ ) (3)元素周期表中有七个周期。( √ ) (4)周期序数与该周期元素的电子层数相等。( √ ) (5)元素周期表共 18 个纵行,18 个族。( × )
2 新知识· 预习探索 设计一 想一想 目标定位 1.能描述元素周期表的结构。 2.知道同主族、同周期元素原子核外电子排布,元素化学性 质的递变规律。 3.了解元素周期表中金属元素、非金属元素的分布。 4.了解主族元素在元素周期表中的位置、原子结构、元素性 质三者之间的关系。 5.了解元素周期表的意义与应用。
5. 某同学有关卤素的笔记中有如下记录, 这些记录都正确吗? (1)卤素只以化合态形式存在于自然界中。( √ ) (2)随核电荷数增加,单质熔、沸点降低。( × ) (3)随核电荷数增加,单质氧化性增强。( × ) (4)随核电荷数增加,气态氢化物稳定性逐渐增强。( × ) (5)从上到下原子半径逐渐减小。( × ) (6)从上到下非金属性逐渐减弱。( √ )
非金属元 素的气态 氢化物 最高价氧 化物的水 化物
生成难易 稳定性 碱性 酸性
难→易 增强 减弱 增强
易→难 减弱 增强 减弱
注:O、F 无正价,更没有最高正价。
设计三 做一做 思维辨析 1.元素周期表中每格有如下信息,它们分别指的是什么?
【答案】 ①元素符号 ②原子序数 子质量
③元素名称 ④相对原
3.将下列元素或原子序数与其所对应的位置连接起来。 (1)C A.第 2 周期第ⅥA 族 (2)O B.第 3 周期第ⅦA 族 (3)13 C.第 2 周期第ⅣA 族 (4)17 D.第 3 周期第ⅢA 族
高中化学 专题1 第1单元 第3课时 元素周期表及其应用学案 苏教版必修2

亲爱的同学:这份试卷将再次记录你的自信、沉着、智慧和收获,我们一直投给你信任的目光……学习资料专题第3课时元素周期表及其应用学习目标:1.知道元素周期表的结构。
2.会比较同周期、同主族元素的金属性和非金属性的变化规律,知道元素周期表金属元素区和非金属元素区的划分。
3.体会元素周期表在学习元素化合物知识与科学研究中的重要作用。
[自主预习·探新知]一、元素周期表的结构1.编排原则(1)横行:电子层数相同,每一个横行称为一个周期。
(2)纵行:最外层电子数相同,每个纵行称为一个族(第8、9、10纵行除外)。
2.结构(1)周期(即横行)(18个纵行,16个族二、主族元素性质的递变规律1.元素金属性与非金属性递变规律(1)同周期(从左到右)元素性质的递变规律(2)同主族(自上而下)元素性质的递变规律2.金属元素与非金属元素的分区(1)分界线的划分请填写出图中序号所表示的内容:①增强②增强③增强④增强⑤Al ⑥Si ⑦金属⑧非金属(2)分界线附近元素的性质:既能表现出一定的金属性,又能表现出一定的非金属性。
三、元素周期表的应用1.帮助我们更好地学习和研究化学元素的原子结构决定了元素在周期表中的位置,而元素在周期表中的位置反映了元素的原子结构和元素的性质特点,我们可以根据元素在周期表中的位置,推测元素的原子结构,预测其主要性质。
2.借助元素周期表研究合成有特定性质的新物质(1)在金属和非金属的分界线附近寻找半导体材料,如锗、硒、硅等。
(2)在过渡元素(副族和Ⅷ族元素)中寻找各种优良的催化剂和耐高温、耐腐蚀的合金材料。
3.推进化学科学的发展元素周期表不仅对元素进行了分类,也揭示了一系列的科学观念,如结构决定性质、量变引起质变、复杂现象中蕴涵着简洁的规律等。
[基础自测]1.判断正误(正确的打“√”,错误的打“×”)(1)元素周期表中共有18个纵行,16个族。
( )(2)最外层有2个电子的元素一定是第ⅡA族元素。
苏教版高中化学必修二课件1.1.3元素周期表及其应用 (3)

Mg(OH)2↓
H2S+Cl2 S↓+2Cl-+2H+ 或 2Br-+Cl2 Br2+2Cl-
结论
非金属性: Cl>S 或 Cl>Br
16
首页
J 基础知识 ICHU ZHISHI
Z S 重点难点 HONGDIAN NANDIAN
随堂练习
UITANG LIANXI
探究一
探究二
探究三
●名师精讲●
元素周期表中元素金属性、非金属性呈规律性递变的原因: 1.同周期元素金属性、非金属性的递变: 同周期元素(稀有气体元素除外)的原子,核外电子层数相同,随着核电 荷数的递增,最外层电子数逐渐增加,原子半径逐渐减小,元素的原子得到电 子的能力逐渐增强,失去电子的能力逐渐减弱。因此,金属性逐渐减弱,非金 属性逐渐增强。 2.同主族元素金属性、非金属性的递变: 同一主族元素原子的最外层电子数相同,随着核电荷数的增大,电子层 数逐渐增加,原子半径逐渐增大,原子失去电子的能力逐渐增强,获得电子的 能力逐渐减弱。因此,元素的金属性逐渐增强,非金属性逐渐减弱。
首页
J 基础知识 ICHU ZHISHI
Z 重点难点 HONGDIAN NANDIAN
S 随堂练习 UITANG LIANXI
4
一二
首页
J 基础知识 ICHU ZHISHI
Z 重点难点 HONGDIAN NANDIAN
S 随堂练习 UITANG LIANXI
主族(A)(由长周期、短周期共同构成)
族(纵)
答案:B
13
首页
J 基础知识 ICHU ZHISHI
Z S 重点难点 HONGDIAN NANDIAN
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第3课时元素周期表及其应用1.了解元素周期表的结构,认识同周期同主族元素性质的递变规律。
2.了解金属、非金属元素在周期表中的位置及其性质的递变规律。
3.理解元素性质、原子结构及元素在周期表中的位置三者之间的关系并掌握其应用。
元素周期表的结构[学生用书P7]1.编排依据:元素周期律。
2.排列原则(1)横行:电子层数相同,每个横行称为周期。
(2)纵行:最外层电子数相同,每个纵行称为族。
3.组成结构(1)周期周期序数 1 2 3 4 5 6 7元素种类 2 8 8 18 18 32 26(未填满) 分类短周期长周期,其中第7周期又称不完全周期族主族0族副族Ⅷ族构成周期由长周期元素和短周期元素共同构成仅由长周期元素构成所含纵行1,2,13~17 18 3~7,11,12 8,9,10族序数ⅠA,ⅡA,ⅢA~ⅦAⅢB~ⅦB,ⅠB,ⅡBⅧ1.判断正误(1)最外层电子数是2的元素,都是ⅡA族元素。
( )(2)氧元素为第ⅥA族元素,故其最高正价为+6价。
( )(3)周期序数=原子的电子层数,主族序数=原子的最外层电子数。
( )(4)若第7周期填满,会包含32种元素。
( )(5)Fe元素位于周期表的ⅧB族。
( )(6)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素。
( ) 答案:(1)×(2)×(3)√(4)√(5)×(6)×2.下列说法正确的是( )A.我们常用的元素周期表中元素排序的依据是元素的相对原子质量B.元素周期表中同一横行元素原子的电子层数相同C.元素周期表有16个纵行D.元素周期表已发展成一个稳定的形式,它不可能再有新的变化了答案:B3.甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是( )A.x+2 B.x+4C.x+8 D.x+18解析:选B。
据元素周期表中各周期元素的种类及各主族中元素相对位置可知,相邻周期的同主族元素之间原子序数之差有如下几种情况:2(如H和Li之间),8(如Li和Na之间),18(如K和Rb之间),32(如Cs和Fr之间)。
显然,A、C、D都是可能的,只有B项x+4是不可能的。
1.元素周期表的结构:七主七副七周期,0族Ⅷ族镧锕系。
2.元素在周期表中位置的推断(1)原子结构示意图法(2)稀有气体原子序数(2、10、18、36、54、86)定位法①比大小定周期比较该元素的原子序数与0族元素的原子序数大小,找出与其相邻近的0族元素,那么该元素就和序数大的0族元素处于同一周期。
②求差值定族数a.若原子序数比相应的0族元素多1或2,则该元素应处在该0族元素所在周期的下一个周期的ⅠA族或ⅡA 族。
b.若原子序数比相应的0族元素少5~1时,则应处在同周期的ⅢA~ⅦA族。
c.若原子序数与相应的0族元素相差其他数,则由相应差找出相应的族。
(3)实例①53号元素由于36<53<54,则53号元素位于第5周期,54-53=1,所以53号元素位于54号元素左侧第一格,即ⅦA族,故53号元素位于第5周期ⅦA族。
②88号元素由于86<88<118,则88号元素位于第7周期,88-86=2,所以88号元素位于第7周期的第二格,即ⅡA族,故88号元素位于第7周期ⅡA族。
记住0族元素的原子序数(He~Rn:2,10,18,36,54,86)是确定元素在周期表中位置的关键。
俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成功合成4个第115号元素的原子。
这4个原子生成数微秒后衰变成第113号元素。
下列有关叙述正确的是( )A.115号元素在第6周期B.113号元素在第7周期ⅢA族C.115号和113号元素都是非金属元素D.镅元素和115号元素不在同一周期[解析] 95号元素镅、115号元素、113号元素,原子序数都大于86而小于118,所以都在第7周期;115号比118号原子序数少3,应在第ⅤA族,113号元素在第ⅢA族;113号元素和115号元素都是金属元素。
[答案] B我国的纳米基础研究能力已跻身于世界前列,曾制得一种合成纳米材料,其化学式为RN。
已知该化合物中的R n+核外有28个电子,则R元素位于元素周期表的( ) A.第3周期第ⅤA族B.第4周期第ⅢA族C.第5周期第ⅢA族D.第4周期第ⅤA族解析:选B。
据化学式RN知N元素为-3价,则RN中R元素的化合价为+3价,所以R 的原子序数为28+3=31;与31最邻近的稀有气体元素原子序数为36(氪,第4周期),所以36-31=5,因此R元素也在第4周期,8-5=3,则R在第ⅢA族。
已知原子结构推断元素在周期表中的位置1.M2+有2个电子层,则M在元素周期表中的位置是( )A.第2周期0族B.第2周期Ⅷ族C.第2周期ⅡA族D.第3周期ⅡA族解析:选D。
M2+有2个电子层,则M原子结构示意图为。
由周期序数=原子核外电子层数,主族序数=原子最外层电子数,得M元素位于第3周期ⅡA族。
2.元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。
若发现第120号元素,在“元素大厦”中它的“房间”是( )A.第7周期0族B.第6周期第ⅠA族C.第8周期第ⅡA族D.第7周期第ⅦA族解析:选C。
第6周期稀有气体元素的原子序数为86;第7周期排满时有32种元素,则第7周期的稀有气体元素的原子序数为118,故120号元素在下一周期的第ⅡA族,C正确。
3.甲、乙两元素原子的L层电子数都是其他层电子总数的2倍。
下列推断正确的是( ) A.甲与乙处于同一周期B.甲与乙处于同一主族C.甲与乙的单质在通常情况下为固体D.甲与乙的原子序数之和为奇数解析:选C。
L层最多可以容纳8个电子,符合题给条件的元素一定位于短周期,若为2个电子层,则为2、4结构,若为3个电子层,则为2、8、2结构,故可知甲、乙两元素分别为碳元素、镁元素,所以A、B、D均不正确。
已知元素的位置推断元素4.如图是元素周期表的一部分,下列说法中正确的是( )A.元素①位于第3周期ⅤA族B.元素①、②、③原子最外层电子数之和为24C.元素④的原子序数比元素②的大8D.元素的最高正化合价:③=⑤解析:选C。
最右一纵列是稀有气体元素,所以判断元素①、②、③分别为第2周期元素N、O、F,元素④、⑤分别为第3周期元素S、Cl。
5. X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的常见最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。
下列说法正确的是( )A.原子最外层电子数:X>Y>ZB.单质摩尔质量:X>Y>ZC.离子半径:X2->Y+>Z-D.原子序数:X>Y>Z解析:选D。
短周期元素X、Z形成的常见最低价离子为X2-、Z-,Y+和Z-具有相同的电子层结构,则X、Y、Z三种元素分别处于第ⅥA、ⅠA、ⅦA族。
又知X和Y处于同一周期,Y+和Z-具有相同的电子层结构,从而推知X、Y、Z分别为S、Na和F。
A.原子最外层电子数:F>S>Na。
B.Na的摩尔质量为23 g·mol-1,S的摩尔质量为32 g·mol-1,F2的摩尔质量为38 g·mol-1,故单质摩尔质量:F2>S>Na。
C.具有相同电子层结构的离子,元素的原子序数越大,离子半径越小,Na+、F-具有相同的电子层结构,则离子半径:F->Na+,S2-多一个电子层,所以S2-半径最大。
D.三种元素的原子序数关系为S>Na>F。
6. X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示。
已知X、Y、Z三种元素的质子数之和为40,请回答:XY Z(1)写出X、Y、ZX________,Y________,Z________。
(2)写出Y在周期表中的位置:______________。
解析:(1)假设X的原子序数是a,则与X同一主族的下一周期元素的原子序数是a+8,Y的原子序数是a+9,Z的原子序数是a+10。
X、Y、Z三种元素的质子数之和为40,则a +a+9+a+10=40,a=7,所以X是N元素,Y是S元素,Z是Cl元素。
(2)S元素原子的核外电子排布是2、8、6,即元素原子核外有3个电子层,最外层有6个电子,因此在周期表中的位置是第3周期第ⅥA族。
答案:(1)N S Cl (2)第3周期第ⅥA族同周期和同主族元素性质的递变1.同周期元素性质的递变同周期元素(除稀有气体元素外)中,随着核电荷数增多,原子半径逐渐减小,原子核对最外层电子的吸引力逐渐增强,原子失电子能力逐渐减弱,得电子能力逐渐增强,所以元素的金属性逐渐减弱,非金属性逐渐增强。
2.同主族元素性质的递变同主族元素中随着核电荷数增多,原子半径逐渐增大,原子核对最外层电子的吸引能力逐渐减弱,原子失电子能力逐渐增强,得电子能力逐渐减弱。
所以元素的金属性逐渐增强,非金属性逐渐减弱。
3.金属元素和非金属元素的分区(1)分界线(2)性质的递变①金属性最强的元素处于周期表的左下角,它是铯(Cs)元素(放射性元素除外)。
②非金属性最强的元素处于周期表的右上角,它是氟(F)元素。
③临近虚线两侧的元素既表现出一定的金属性,又表现出一定的非金属性。
1.判断正误(1)同一周期元素的原子,随核电荷数的递增,原子半径逐渐减小,最高正化合价从+1~+7,最低负化合价从-7~-1。
( )(2)同主族元素从上到下,随电子层数的递增,金属性逐渐增强,非金属性逐渐减弱。
( )(3)一般情况下,原子半径越大,金属性越强,原子半径越小,非金属性越强。
( )答案:(1)×(2)√(3)√2.下列说法正确的是( )A.Li是最活泼金属元素,F是最活泼非金属元素B.Mg(OH)2碱性比Ca(OH)2强C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16个纵行D.X2+的核外电子数目为10,则X在第3周期ⅡA族解析:选D。
Cs为最活泼金属元素,A错;Mg的金属性弱于Ca,碱性:Mg(OH)2<Ca(OH)2,B错;Ⅷ族含3个纵行,C错。
3.元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。
下列推测不正确的是( )A.同周期元素中X的金属性最强B.原子半径X>Y,离子半径X+>Z2-C.同族元素中Z的氢化物稳定性最高D.同周期元素中Y的最高价含氧酸的酸性最强解析:选B。
分析题给条件可推知:X是钠(Na)、Y是氯(Cl)、Z是氧(O)。
原子半径X>Y,但X+(Na+)与Z2-(O2-)电子层结构相同,故离子半径为X+<Z2-。
同周期、同主族元素性质的变化规律比较项目同周期(从左到右) 同主族(从上到下)最外层电子数由1逐渐增到7(第1周期由1到2)相同主要化合价最高正价+1→+7,负价-4→-1(O、F除外)最高正价相同(O、F除外)原子半径逐渐减小(稀有气体除外)逐渐增大得失电子能力得电子能力增强,失电子能力减弱得电子能力减弱,失电子能力增强单质的氧化性、还原性还原性减弱,氧化性增强氧化性减弱,还原性增强最高价氧化物对应水化物的酸碱性碱性减弱,酸性增强酸性减弱,碱性增强非金属氢化物的生成难易和稳定性生成由难到易,稳定性由弱到强生成由易到难,稳定性由强到弱(1)短周期中金属元素的最外层电子数≤3。
