总皂苷的测定方法
保健食品中总皂苷的测定

附件:一、保健食品中大蒜素的测定1 范围本方法适用于以大蒜及其制品为原料的保健食品中大蒜素(三硫二丙烯,C6H10S3)的含量测定。
本方法最低检出浓度为0.0430mg/mL;取100mg试样,提取定容5.0mL时,试样中大蒜素最低检出质量浓度为0.20g/100g。
本方法最佳线性范围: 0.320mg/mL~3.00 mg/mL。
2 原理:根据大蒜素为挥发性油成分,经有机溶剂提取,用气相色谱仪分析,采用外标法定量。
3 试剂除特殊说明,所用试剂均为分析纯。
3.1 无水乙醇3.2 正己烷3.3标准溶液:称取0.1000g标准品,置于10mL容量瓶中,用正己烷定容至刻度,该溶液中含大蒜素浓度为10.0mg/mL。
此溶液可在冰箱中保存七天。
取该溶液1.0mL,置于10mL容量瓶中,用正己烷定容至刻度,此溶液含大蒜素浓度为1.0mg/mL。
4 仪器4.1气相色谱仪:附氢火焰(FID)检测器4.2数据处理机或积分仪4.3分析天平:万分之一4.4超声清洗机4.5离心机:3000r/min5分析方法5.1试样提取5.1.1固体试样:称取试样适量(相当于含大蒜素5mg,精确至0.001g),加无水乙醇适量,密塞,超声70min,取出冷却,加正己烷定容(调节大蒜素含量约为1mg/mL),振摇,静置分层后,取上层溶液进样。
5.1.2液体试样吸取试样适量(相当于含大蒜素5mg,精确至0.001g),置于分液漏斗中,加5mL 正己烷振摇提取1min ,静置(或离心)分层后,取上层溶液进样。
5.2 气相色谱参考条件5.2.1 色谱柱:HP-5(30m×0.25mm)5.2.2 柱箱温度:100℃(3min )min)10(℃200℃150℃/min 20℃/min 10−−−→−−−−→−5.2.3 进样口温度:220℃ 5.2.4 检测器温度:250℃ 5.2.5 载气:氮气(1mL/min )5.2.6 氢气:40mL/min ;空气:400mL/min 5.2.7 进样量:1μL5.3 定性分析:在参考操作条件下,以对照品与试样比较保留时间定性。
分光光度法测定夏枯草中总皂苷的含量(精)

分光光度法测定夏枯草中总皂苷的含量【摘要】[目的]测定夏枯草药材中总皂苷的含量。
[方法]甲醇超声提取夏枯草样品溶液,5%香草醛-冰醋酸显色,分光光度法测定样品中总皂苷含量。
[结果]总皂苷在26.95~94.31μg范围内与吸光度呈良好的线性关系,回收率在97.0%~100.5%之间;三批夏枯草样品中总皂苷的含量在2.02%~2.56%之间。
[结论]分光光度法测定夏枯草中总皂苷的含量,方法准确可靠、操作简便。
【关键词】夏枯草; 总皂苷; 分光光度法; 含量测定Abstract:[Objective] To measure the content of total saponins in selfheal herb.[Method] Extract selfheal resolution with carbinol ultrasound,5% vanilla aldehyde—icy vinegar acid coloring,measure content of total saponins in sample with spectrophotometry.[Result]In 26.95~94.31μg,the total saponin has good linear relationship with absorbency,the recycle rate is 97.0%~100.5%; 3 batches of selfheal samples have saponins 2.02%~2.56%.[Conclusion]Spectrophotometry measuring saponins in selfheal is correct,reliable and easy of operation.Key words:selfheal; total saponins; spectrophotometry; content measure夏枯草为唇形科植物夏枯草(Brunellae cum fructu L.)的干燥果穗,具有清火、明目、散结、消肿之功效,用于目赤肿痛,头痛眩晕,瘰疬,乳痈肿痛,高血压,急性黄疸型传染性肝炎等病症[1]。
中国药典 2020版中人参总皂苷含量测定方法

【导言】我国药典是国家药典的统称,是指对我国境内生产、流通和使用的药品质量标准的权威性规定,是保障药品质量和使用合理、安全的基本依据。
其中,人参总皂苷含量是人参药材质量的重要评价指标,其测定方法对于保证人参药材的质量具有重要意义。
本文将对我国药典2020版中人参总皂苷含量测定方法进行详细介绍。
【正文】1. 依据依据我国药典是国家药典,是依法规定的药品标准,它规定了符合标准的药品质量要求、规范药品生产、流通和使用。
人参作为一种重要的中药材,在我国药典中有着详细的质量标准,其含有的总皂苷含量是一个至关重要的指标。
2. 人参总皂苷含量的意义总皂苷是人参中的重要有效成分之一,它具有调节免疫功能、提高机体抗氧化能力、增强心肌供血量、预防心绞痛、心肌梗死等保护心脏的作用。
测定人参总皂苷含量不仅有利于评价人参的药用价值,还能为人参的质量控制提供依据。
3. 我国药典2020版中人参总皂苷测定方法我国药典2020版中,人参总皂苷的测定方法主要包括提取、净化、分离和定量测定这几个步骤。
具体操作步骤如下:3.1 溶剂选择:首先选择合适的溶剂,如乙醇、丙酮等,将人参样品粉碎成粉末状,然后用溶剂进行提取,得到提取液。
3.2 净化分离:将提取液进行净化分离,去除杂质,得到待测液。
3.3 定量测定:采用分光光度计或者高效液相色谱仪等仪器,进行人参总皂苷的定量测定,计算出含量结果。
4. 测定方法的操作要点在操作过程中,需严格控制提取温度、时间和溶剂的体积比例,避免提取效果不佳。
净化过程中也需保证分离效果,避免杂质对测定结果的影响。
测定过程中应根据仪器的要求进行参数设置,确保测定结果的准确性。
为了保证人参总皂苷含量的测定结果的可靠性和稳定性,建议重复测定并取平均值。
5. 结论我国药典2020版中的人参总皂苷测定方法,是一种全面、准确的测定方法,可以有效地评价人参药材的质量,并为制定人参制剂的合理使用提供依据。
基于该方法,人们可以对人参药材的质量进行科学评价,保证人参产品的质量和疗效。
三七总皂苷提取的实验原理

三七总皂苷提取的实验原理三七总皂苷是从中药材三七中提取的一种活性成分,具有多种药理活性,包括抗炎、抗氧化、抗肿瘤、抗凝血、心血管保护等作用。
下面将详细介绍三七总皂苷的提取原理。
三七总皂苷主要成分是三萜皂苷类化合物,包括三七皂苷R1、R2、Rb1、Rb2、Rd、Re等,其中以三七皂苷R1、三七皂苷Rb1和三七皂苷Rd的含量较高。
提取三七总皂苷的方法主要有超声波提取法、超临界流体萃取法、醇沉法等。
以下以醇沉法为例,说明三七总皂苷的提取原理。
首先,将醇沉法提取三七总皂苷的步骤分为以下几个关键步骤。
1. 材料预处理:将新鲜的三七材料进行清洗和磨碎,以增大总皂苷的释放面积。
2. 溶剂选择:选择高极性的溶剂,如乙醇、甲醇等,用于提取三七总皂苷。
溶剂的选择要考虑溶剂对三七总皂苷的溶解能力,以及提取效率和成本因素。
3. 提取条件:选择适宜的提取温度和时间。
温度过高可能导致三七总皂苷的降解,而温度过低可能会降低提取效率。
根据实验条件的不同,选择合适的提取时间。
4. 离心分离:在提取完成后,使用离心机将提取液和残渣分离。
离心分离可以有效去除悬浮固体颗粒和大分子物质,得到较为纯净的提取液。
5. 浓缩和精制:提取液中的三七总皂苷含量还相对较低,因此需要进行浓缩和精制以获得较高纯度的三七总皂苷。
浓缩可以通过蒸发溶剂或低温浓缩等方法进行。
精制一般采用色谱等技术,以去除提取液中的杂质。
通过以上步骤,可以获得较高纯度的三七总皂苷。
然而,提取总皂苷的效果不仅与提取方法有关,还与原料的品质、配方和处理工艺等因素有关。
为了获得更好的提取效果,有时还需要对提取过程进行优化。
总之,三七总皂苷的提取是通过选择适宜的溶剂、提取温度和时间等条件,将三七材料中的活性成分转移到溶剂中,经过离心分离、浓缩和精制等步骤,最终得到纯度较高的三七总皂苷。
该提取方法具有简单、有效、成本低廉等优点,在中药研究和应用中有着广泛的应用前景。
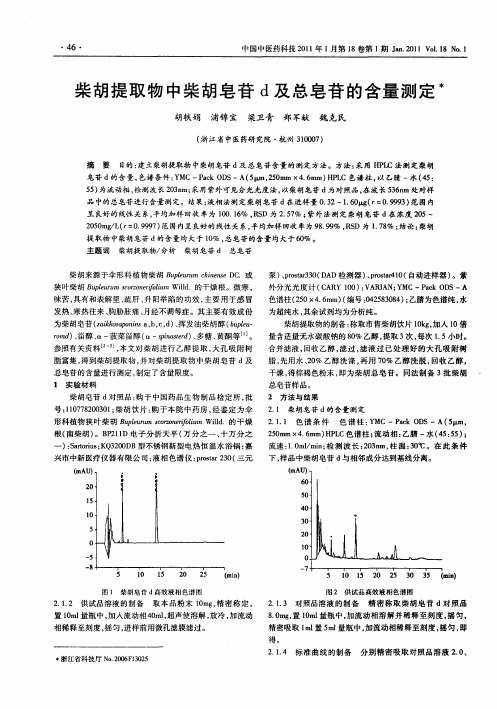
柴胡提取物中柴胡皂苷d及总皂苷的含量测定
泵 ) pot 30 D D检测器 ) potr1 ( 、rs r3 ( A a 、rs 40 自动进样器 ) a 。紫
外 分 光 光 度 计 ( A Y 10 : A I N; MC—P c D C R 0 ) V R A Y akO S—A
味苦 , 具有和表解里 、 疏肝 、 阳举陷 的功效 , 升 主要用 于感 冒
一
2 11 色 谱 条 件 色 谱 柱 : MC—P c D .. Y ak O S—A( w 5 m, 2 0 m× . m H L 5m 46 m) P C色谱柱 ; 流动相 : 乙腈 一水 (5 5 ) 4 :5 ; 流速 :. m/ i ; 测 波长 :0 n 柱 温 :0 。在 此 条 件 10 lm n 检 2 3 m, 3℃ 下 , 品中柴胡皂苷 d 样 与相邻成分达到基线分离 。
取本 品粉末 1 m , 0 g 精密 称定 ,
2 13 对照品溶液 的制备 ..
精 密称 取柴 胡皂苷 d对照 品
置 1m 量 瓶 中 , 0l 加入 流动 相 4 m , 声 使 溶 解 , 冷 , 0 l超 放 加流 动
80 g 置 1m 量瓶 中, 流动相溶 解并稀释 至刻度 , 匀 , .m , 0 l 加 摇
主 题 词 柴胡 提 取 物/ 析 分 柴 胡皂 苷 d 总 皂 苷
柴胡来源 于伞形科植 物柴胡 B p uu h es D .或 ul rm ci ne C e n
狭 叶 柴胡 B perm so oeil m Wid ul u r nroi H .的 干燥 根 。微 寒 , u cz f u
总 皂 苷 的 含 量进 行 测 定 , 制定 了含 量 限 度 。
1 实 验 材 料
保健食品中总皂甙的测定方法

精选文档保健食品中总皂甙的测定方法(引自《保健食品检验与评价技术规范》 2003 年版:二十三、保健食品中总皂甙的测定)1 试剂1.1 Amberlite-XAD-2 大孔树脂, Sigma 化学公司、 U.S.A. 。
1.2 正丁醇分析纯。
1.3 乙醇分析纯。
1.4 中性氧化铝层析用, 100-200 目。
1.5 人参皂甙 Re 购自中国药品生物制品检定所1.6 香草醛溶液称取 5g 香草醛,加冰乙酸溶解并定容至 100mL1.7 高氯酸分析纯。
1.8 冰乙酸分析纯。
1.9 人参皂甙 Re 标准溶液:精确称取人参皂甙 Re 标准品 0.020g ,用甲醇溶解并定容至10.0mL ,即每毫升含人参皂甙 Re 2.0 mg 。
2 仪器2.1 比色计2.2 层析柱3.实验步骤3.1 试样处理3.1.1 固体试样:称取 1.000 g 左右的试样(根据试样含人参量定),置于 100 mL 容量瓶中,加少量水,超声 30 min ,再用水定容至 100 mL ,摇匀,放置,吸取上清液 1.0 mL 进行柱层析。
精选文档3.1.2 液体试样:含乙醇的补酒类保健食品,吸取 1.0 mL 试样放水浴挥干,用水浴溶解残渣,用此液进行柱层析。
非乙醇类的液体试样:吸取 1.0 mL 试样(假如浓度高、或颜色深,需稀释一定体积后再取1.0mL )进行柱层析。
3.2 柱层析:用 10 mL 注射器作层析管,内装 3cm Amberlite-XAD-2 大孔树脂,上加 1 cm 中性氧化铝。
先用 25 mL 70 % 乙醇洗柱,弃去洗脱液,再用 25 mL 水洗柱,弃去洗脱液,精确加入1.0 mL 已处理好的试样溶液(见 3.1 ),25 mL 水洗柱,弃去洗脱液,用 25 mL70 % 乙醇洗脱人参皂甙,收集洗脱液于蒸发皿中,置于60 C水浴挥干。
以此作显示用。
3.3 显色:在上述已挥干的蒸发皿中准确加入 0.2 mL 5% 香草醛冰乙酸溶液,转动蒸发皿,使残渣都溶解,再加 0.8 mL高氯酸,混匀后移入 5 mL带塞刻度离心管中,60 C水浴上加热 10 min ,取出,冰浴冰却后,准确加入冰乙酸 5.0mL ,摇匀后,以 1cm 比色池于 560 nm 波长处与标准管一起进行比色测定。
总皂苷的测定方法

A1 总皂苷的测定方法方法来源:《保健食品检验与评价技术规范》(2003版)保健食品中总皂苷的测定方法(分光光度法)A1.1 试剂Amberlite-XAD-2大孔树脂,Sigma化学公司U.S.A正丁醇分析纯乙醇分析纯中性氧化铝层析用,100-200目人参皂苷Re 购自中国药品生物制品检定所香草醛溶液称取5g香草醛,加冰乙酸溶解并定容至100ml。
高氯酸分析纯冰乙酸分析纯人参皂苷Re标准溶液:精确称取人参皂苷Re标准品0.020g,用甲醇溶解并定容至10.0ml,即每毫升含人参皂苷Re2.0mg。
A1.2 仪器比色计、层析柱A1.3 试验步骤A1.3.1 试样处理A1.3.1.1 固体试样:称取1.000g左右的试样(根据试样含人参量定),置于100ml 容量瓶中,加少量水,超声30min,再用水定容至100ml,摇匀,放置,吸取上清液1.0ml进行柱层析。
A1.3.1.2 柱层析:用10mL注射器作层析管,内装3cm Amberlite-XAD-2大孔树脂,上加1cm中性氧化铝。
先用25ml70%乙醇洗柱,弃去洗脱液,再用25ml水洗柱,弃去洗脱液,精确加入1.0ml已处理好的试样溶液(见3.1),用25ml水洗柱,弃去洗脱液,用25m170%乙醇洗脱人参皂苷,收集洗脱液于蒸发皿中,置于60℃水浴挥干。
以此作显色用。
A1.3.1.3 显色:在上述已挥干的蒸发皿中准确加入0.2ml5%香草醛冰乙酸溶液,转动蒸发皿,使残渣都溶解,再加0.8ml高氯酸,混匀后移入5ml比色管中,塞紧盖子于60℃水浴上加热10min,取出,冰浴冷却后,准确加入冰乙酸5.0ml,摇匀后,以1cm 比色池于560nm 波长处与标准管一起进行比色测定。
A1.3.1.4 标准管:吸取人参皂苷Re 标准溶液(2.0mg/ml )100μl 放蒸发皿中,放在水浴挥干(低于60℃),或热风吹干(勿使过热),以下操作从“3.2柱层析……”起,与试样相同。
比色法测定甘草中总皂苷的含量

比色法测定甘草中总皂苷的含量【摘要】目的建立甘草中甘草总皂苷含量的测定方法。
方法用香草醛 高氯酸试剂,在589 nm处有最大吸收,并对比色条件进行了优化。
结果该法精密度高,1 h内稳定,平均加样回收率为99.03%。
结论此法简便、准确、稳定性、重复性好,可用于甘草总皂苷的测定。
【关键词】甘草;总皂苷;香草醛 高氯酸Determination of Total Saponins in Glycyrrhiza by ColorimetryAbstract:ObjectiveTo establish the method of determination of total saponins in Glycyrrhiza. MethodsUse Vanillin HClO4 as the chromogenic reagent and detect the maximum absorption at the wavelength of 589 nm. Choose the best chromogenic preparation to determine the contents of the samples. Results The precision of the method is high. The color of the treated samples was stable within 1h. The average value of the recovery was 99.03%.ConclusionThe method is simple, accurate, highly sensitive and reproducible. It may be used for the quantitative determination of total saponins in Glycyrrhiza.Key words:Glycyrrhiza; Total saponins; Vanillin- HClO4甘草为豆科(Leguminosae)甘草属(Glycyrrhiza)植物,为我国重要的传统中草药。
总皂苷的检测方法

1性质 皂甙 (a o i s 又称皂 素, spn n) 是广泛存在 于植物界 的一类特殊 的甙类 , 的 它 水溶液振摇 后可生产 持久 的肥皂样 的泡沫 , 因而得名 。 根据 皂甙水解 后生 成 皂甙元 的结构, 可分 为三 萜皂甙 ( r t r e o d l a o i s 与甾体 皂甙 t i e p n i a s p n n ) ( t r i a s p n n ) 大类 组 成皂甙 的糖 常见 的有 葡 萄糖 、半乳糖 、 s eo d l a o i s 两
强 烈的 促丝 裂剂和 趋 化剂 】 。
出挥 干石 油醚后 , 用 2 O l 7%的乙醇水 溶液浸 提 4 , 转蒸发 回收 乙醇 再 0W 的 0 h旋 相, 水相 k 一 大孔 吸附树 脂柱 (0 m 8 O m 树脂床层 高1 0 m 吸附过夜 , AB 8 3m* Om , 5r ) a 经 多 次水洗 去除糖等 杂质后 , 用乙醇 水溶液洗 脱大豆 皂苷, 回收溶 剂后用 水定容
6m X2 0Il )锍 速 为 1Ol/m n检 测波长 为 17m 柱 温为室 温, m 5 I: pm I5 I I .m i: 9n:
采用 二元梯度洗 脱, 流动相 为 乙腈 一水 。 三七 总皂甙液相 色谱 定量方法 具有较 强 的针对性和 准确性 。三七 总皂甙在 p 值> , 温条件 下, H 4低 比较稳 定, 而在 强 酸高温 下受影 响较大, p 值为 3 总皂甙含 量 降低 约3 . %, 10 ℃下, 在 H 时, 25 在 0 总皂 甙含量降低 约 1 . %。三七 总皂甙在 弱酸弱碱 , 温条 件下, 25 低 比较 稳定 ,
E S - P C 定大豆 皂苷 含量测 定步骤 L D HL 测 称取 大豆胚 芽粉 ( 水分 含量 为8 8 % 2 g 用石 油醚 (0 6  ̄ 脱脂3 , .6 )0 , 3— 0 C) h 取
人参总皂苷

人参总皂苷Renshen ZongzaoganTOTAL GINSENOSIDE GINSENG ROOT本品为五加科植物人参Panax ginseng C.A.Mey.的干燥根及根茎经加工制成的总皂苷。
【制法】取人参,切成厚片,加水煎煮二次,第一次2小时,第二次1.5小时,煎液滤过,合并滤液,通过D101型大孔吸附树脂柱,水洗脱至无色,再用60,乙醇洗脱,收集60,乙醇洗脱液,滤液浓缩至相对密度为1.06,1.08(80?)的清膏,干燥,粉碎,即得。
【性状】本品为黄白色或淡黄色的粉末;微臭,味苦;具吸湿性。
本品在甲醇或乙醇中易溶,在水中溶解,在乙醚或石油醚中几乎不溶。
【鉴别】(1)取本品0.1g,置试管中,加水2ml,用力振摇,产生持久性泡沫。
(2)取本品0.1g,加甲醇10ml使溶解,作为供试品溶液;另取人参对照药材1g,加水100ml煎煮2小时,滤过,滤液通过D101型大孔吸附树脂柱(内径为1cm,柱高为15cm),用水洗至无色,弃去水液,再用60,乙醇20ml洗脱,收集洗脱液,蒸干,残渣加甲醇10ml使溶解,作为对照药材溶液。
再取人参皂苷Rb对照品、人参皂苷Rg对照品与人参皂苷Re11对照品,加甲醇溶解制成每1ml各含2mg的混合溶液,作为对照品溶液。
照薄层色谱法(附录VI B)试验,吸取上述三种溶液各2μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15:40:22:10)10?以下放置的下层溶液为展开剂,展开,取出,晾干,喷以10,硫酸乙醇溶液,在105?加热至斑点显色清晰,分别置日光和紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置,日光下显相同颜色的斑点,紫外光下显相同颜色的荧光斑点。
【检查】粒度依法检查(附录? B第二法),能通过120目筛的粉末不少于95,。
干燥失重取本品,在105?干燥至恒重,减失重量不得过5.0,(附录?G)。
紫外可见分光光度计测人参总皂苷

人参总皂苷Renshen ZongzaoganTOTAL GINSENOSIDE GINSENG ROOT本品为五加科植物人参JPanaa: ginseng C. A. Mey. 的干燥根及根茎经加工制成的总皂苷。
【制法】取人参,切成厚片,加水煎煮二次,第一次2 小时,第二次1. 5 小时,煎液滤过,合并滤液,通过D 1 0 1型大孔吸附树脂柱,水洗脱至无色,再用6 0 %乙醇洗脱,收集60% 乙醇洗脱液,滤液浓缩至相对密度为1.06?1.08(80°C)的清膏,干燥,粉碎,即得。
【性状】本品为黄白色或淡黄色的粉末;微臭,昧苦;具吸湿性。
本品在甲醇或乙醇中易溶,在水中溶解,在乙米或石油米中几乎不溶。
【鉴别】(1)取本品O.lg,置试管中,加水2ml,用力振摇,产生持久性泡沫。
(2)取本品O.lg,加甲醇10ml使’溶解,作为供试品溶液;另取人参对照药材lg,加水100ml煎煮2 小时,滤过,滤液通过D101型大孔吸附树脂柱(内径为1cm,柱高为15cm) ,用水洗至无色,弃去水液,再用6 0 %乙醇20ml洗脱,收集洗脱液,蒸干,残淹加甲醇10ml使溶解,作为对照药材溶液。
再取人参皂苷R b i对照品、人参皂苷R gl对照品与人参皂苷R e对照品,加甲醇溶解制成每lml各含2 m g 的混合溶液,作为对照品溶液。
照薄层色谱法(通则0502)试验',吸取上述三种溶液各2M1,分别点于同一硅胶G 薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15 : 40 : 22 : 10) 1 0 1以下放置的下层溶液为展开剂,展开,取出,晾干,喷以1 0 %硫酸乙醇溶液,在105°C加热至斑点显色清晰,分别置日光和紫外光灯(365mn)下检视。
供试品色谱中,在与对照药材色谱和对照品色谱相应的位置,日光下显相同颜色的斑点,紫外光下显相同颜色的荧光斑点。
【检査】粒度依法检查(通则0982第二法),能通过1 2 0目筛的粉末不少于95% 。
比色法测定总皂苷含量

比色法测定总皂苷含量比色法测定总皂苷含量1、仪器紫外分光光度计、电热恒温水浴锅、电子分析天平、旋转蒸发器、大孔树脂柱(内径0.8 cm,长20 cm)。
试剂无水甲醇、无水乙醇、正丁醇、冰醋酸、高氯酸和香草醛等均为分析纯;大孔树脂 DM-301、对照品、洋金花药品。
2、方法2.1 对照品溶液的制备取对照品 10 mg,加甲醇溶解定容至 10 ml,制成 1 mg/ml对照品溶液。
2.2供试品溶液的制备取药材粉末(过4号筛)约0.2 g,准确称定,置于150 ml具塞锥形瓶中。
精密加入50 ml 甲醇后,准确称重。
浸泡60 min,超声提取30 min,再次称重,补加甲醇至超声前重量。
过滤,精密移取续滤液25 ml于蒸发皿中,水浴蒸发至干,用5 ml水溶解残留物,所得溶液缓缓通过已处理好的大孔吸附树脂柱(径高比1:5),以水50 ml洗脱,弃去水液,之后再以50 ml 95%乙醇洗脱,收集乙醇洗脱液,蒸干。
用20 ml水分次将残留物溶解转移至60 ml分液漏斗中,用水饱和的正丁醇萃取(4×20 ml),合并正丁醇层,减压蒸干。
残留物用70%甲醇溶解转移至10 ml量瓶中,定容,摇匀,即得。
2.3测定波长的选择精密移取1.5 ml的对照品及l ml供试品溶液,于70℃水浴蒸发至干,加入5%香草醛一冰醋酸(临用新配)0.2ml,高氯酸0.8 ml,于60℃水浴显色15 min后流水冷却 lO min。
加冰醋酸5 ml,摇匀。
立即在紫外分光光度计于400~800 nm波长下扫描,同时空白溶液作参比。
对照品及供试品的最大吸收波长均在475 nm,故选取475 nm 为检测波长。
2.4线性关系考察精密量取对照品溶液0.60,1.50,2.40,3.30,4.20 ml,置具塞试管中,于70℃水浴蒸发至干,加入5%香草醛-冰醋酸(临用新配)O.2 ml,高氯酸0.8 ml,于60℃水浴显色15min后流水冷却10 min。
皂苷含量测定方法

皂苷含量测定方法
1. 高效液相色谱法,这就像在成分的世界里开启了一扇清晰的窗户!比如我们检测人参中的皂苷含量,通过高效液相色谱,就能把那些隐藏的皂苷清晰地找出来。
2. 比色法呀,这可是个神奇的手段!就像你能在一群颜色中精准挑出你想要的那一个。
比如检测植物提取物里的皂苷,能快速知道有多少呢!
3. 薄层色谱法呢,可以想象成是在一张大地图上寻找宝藏的标记!比如说检测某种药材里含有的皂苷,一下子就能确定它们的位置啦。
4. 分光光度法,哇哦,这简直是一把探索皂苷含量的利剑!好比在黑暗中找到闪闪发光的宝物。
像对一些含有皂苷的样品进行检测时,它就能大显身手啦。
5. 重量法,哎呀呀,这个方法就像称一称宝贝有多重一样!就拿确定某种中药里皂苷的含量来说,用重量法不就能知道个大概嘛!
6. 酶联免疫吸附测定法,哈哈,这可是如同侦探寻找线索一样厉害的方法哟!比如说去检测一些生物样本中的皂苷含量,它可在行啦。
7. 气相色谱法呢,它就像是在气流中捕捉那些关键信息!例如检测一些经过特殊处理的样品中的皂苷,靠它就能搞定呀。
8. 近红外光谱法呀,这就像拥有了一双超级眼睛,能迅速看穿皂苷的秘密呢!在快速分析某些复杂样品中的皂苷含量时,可好用了。
9. 质谱法啊,那可是如同超级显微镜一样的存在!想想对那些微量的皂苷进行检测时,它可不就是大功臣嘛!
我的观点结论:这些皂苷含量测定方法都各有其独特之处和适用场景,我们可以根据实际情况灵活选择,以获得最准确的结果。
总皂苷的测定方法

总皂苷的测定方法(分光光度法)本方法适用于功能性食品中总皂苷的测定。
本方法人参皂苷Re的最低检出量为2μg/mL。
一、方法提要样品中总皂苷经提取、PT—大孔吸附树脂柱预分离后,在酸性条件下,香草醛与人参皂苷生成有色化合物,以人参皂苷Re为对照品,于560nm处比色测定。
二、仪器1.722分光光度计。
2.PT—大孔吸附树脂柱(河北省津杨滤材厂)。
3.超声波振荡器。
三、试剂1.甲醇(分析纯)。
2.乙醇(分析纯)。
3.人参皂苷Re标准品(中国药品生物制品检定所)。
4.5%香草醛溶液:称取5g香草醛,加冰乙酸溶解并定容至l00mL。
5.高氯酸(分析纯)。
6.冰乙酸(分析纯)。
7.人参皂苷Re标准溶液:精确称取人参皂苷Re标准品20.0mg,用甲醇溶解并定容至10mL,即每1mL含人参皂苷Re2.0mg。
8.重蒸水。
四、测定步骤1.样品处理:(1)固体样品称取1.0g左右样品于100mL烧杯中,加入20~40mL 85%乙醇,超声波振荡30min,再定容至50mL,摇匀,放置,吸取上清液1.0mL挥干后以水溶解残渣,进行柱分离。
(2)液体样品含乙醇的酒类样品:准确吸取1.0mL样品放于蒸发皿中,蒸干,用水溶解残渣,用此液进行柱层析;非乙醇类液体样品:准确吸取1.0mL样品(如浓度高或颜色深,需稀释一定体积后再取1.0mL)直接进行柱分离。
2.柱层析以PT—大孔吸附树脂柱进行层析分离,准确吸取上述已处理好的样品溶液1.0mL上柱,用15mL水洗柱,以洗去糖分等水溶性杂质,弃去洗脱液,再用20mL85%乙醇洗脱总皂苷,收集洗脱液于蒸发皿中,于水浴上蒸干,以此作显色用。
3显色在上述已挥干的蒸发皿中准确加入0.2mL 5%香草醛冰乙酸溶液,转动蒸发皿,使残渣溶解,再加0.8mL高氯酸,混匀后移入l0mL比色管中,塞紧盖子于60℃以下水浴上加温15min取出,冷却后准确加入冰乙酸5.0mL,摇匀后以1.0cm 比色皿、于560nm处与人参皂苷Re标准管同时比色。
总皂苷的含量测定方法

总皂苷的含量测定方法宝子!今天咱们来唠唠总皂苷含量的测定方法呀。
一种常见的方法就是比色法哦。
这就像是给总皂苷找个颜色伙伴来“衡量”它呢。
通常会利用一些显色剂,让总皂苷发生显色反应。
比如说,有一些试剂和总皂苷反应后会产生特定的颜色,然后通过仪器去检测这个颜色的深浅程度。
就好比我们看东西的颜色深浅来判断它的多少一样。
在这个过程中呢,要特别注意各种反应条件,像温度呀、反应时间呀,这些小细节就像做菜时的火候和时间,掌握不好就可能影响最后的结果哦。
还有重量法呢。
这个方法听起来就很实在,就像称东西一样。
把含有总皂苷的样品经过一系列处理,让总皂苷从混合物里分离出来,然后称一称它的重量。
不过这个方法可有点小麻烦,因为要把总皂苷分离得很干净不容易,就像从沙子里挑出金子一样,得很细心才行。
高效液相色谱法(HPLC)那可是个很厉害的方法哦。
它就像一个超级精密的侦探,可以把总皂苷从复杂的样品里精准地找出来并且测定含量。
它的原理有点复杂啦,简单说就是利用不同物质在流动相和固定相之间的分配系数不同,把总皂苷和其他成分分开,然后通过检测信号来确定总皂苷的含量。
这种方法虽然很精准,但是仪器比较贵,操作也需要一定的技术水平,就像开高级跑车,得有点本事才行呢。
薄层色谱法也能用来测定总皂苷含量。
它就像是把总皂苷和其他小伙伴们放在一个特殊的跑道(薄层板)上赛跑,然后根据它们跑的位置和颜色等特征来判断总皂苷的情况。
这个方法比较直观,但是准确性可能相对前面几种方法会差一点,不过它操作起来比较简单,就像玩一个简单的小游戏一样。
宝子,这些就是总皂苷含量测定的一些常见方法啦,各有各的优缺点,就看具体的需求和条件来选择合适的方法喽。
。
白英中总皂苷的含量测定

白英中总皂苷的含量测定作者:甄会贤,齐烨,陈扬,孙立新【摘要】目的建立白英中总皂苷的含量测定方法。
方法选用薯蓣皂苷元为对照品,采用分光光度法,高氯酸显色,在410 nm处测定吸光度,计算白英中总皂苷含量。
结果薯蓣皂苷元的质量浓度在8.91~29.70μg/ml范围内与吸光度值呈良好线性关系(r=0.999 2),方法的平均回收率为95.9%(n=9),RSD为1.5%;不同来源的白英药材中总皂苷含量有较大差异。
结论该方法操作简便、准确、灵敏、重现性好,可用于白英药材的质量控制。
【关键词】白英总皂苷薯蓣皂苷元分光光度法Abstract:ObjectiveTo study the assay method of total saponins in Solanum lyratum Thunb. .MethodsSelecting diosgenin as control article,colorating with perchloric acid,determining absorbability in the point of 410nm by adopting spectrophotometric method,then calculating total saponins in Solanum lyratum Thunb..ResultsThe calibration curve was linear over the range of 8.91~29.70 μg/ml with the correlation of 0.9992. The average recoveries of diosgenin was 95.9%(RSD=1.5%,n= 9). The samples from different areas containedvarious amounts. ConclusionThe method is simple, accurate, sensitive and reproducible. It can be applied to the quality control of Solanum lyratum L.Key words:Solanum lyratum Thunb.; Total saponins;Diosgenin; Spectrophotometric method白英为茄科植物Solanum lyratum Thunb.的干燥全草,性微寒,味苦。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
总皂苷的测定方法(分光光度法)
本方法适用于功能性食品中总皂苷的测定。
本方法人参皂苷Re的最低检出量为2μg/mL。
一、方法提要
样品中总皂苷经提取、PT—大孔吸附树脂柱预分离后,在酸性条件下,香草醛与人参皂苷生成有色化合物,以人参皂苷Re为对照品,于560nm处比色测定。
二、仪器
1.722分光光度计。
2.PT—大孔吸附树脂柱(河北省津杨滤材厂)。
3.超声波振荡器。
三、试剂
1.甲醇(分析纯)。
2.乙醇(分析纯)。
3.人参皂苷Re标准品(中国药品生物制品检定所)。
4.5%香草醛溶液:称取5g香草醛,加冰乙酸溶解并定容至l00mL。
5.高氯酸(分析纯)。
6.冰乙酸(分析纯)。
7.人参皂苷Re标准溶液:精确称取人参皂苷Re标准品20.0mg,用甲醇溶解并定容至10mL,即每1mL含人参皂苷Re2.0mg。
8.重蒸水。
四、测定步骤
1.样品处理:
(1)固体样品
称取1.0g左右样品于100mL烧杯中,加入20~40mL 85%乙醇,超声波振荡30min,再定容至50mL,摇匀,放置,吸取上清液1.0mL挥干后以水溶解残渣,进行柱分离。
(2)液体样品
含乙醇的酒类样品:准确吸取1.0mL样品放于蒸发皿中,蒸干,用水溶解残渣,用此液进行柱层析;非乙醇类液体样品:准确吸取1.0mL样品(如浓度高或颜色深,需稀释一定体积后再取1.0mL)直接进行柱分离。
2.柱层析
以PT—大孔吸附树脂柱进行层析分离,准确吸取上述已处理好的样品溶液1.0mL上柱,用15mL水洗柱,以洗去糖分等水溶性杂质,弃去洗脱液,再用20mL85%乙醇洗脱总皂苷,收集洗脱液于蒸发皿中,于水浴上蒸干,以此作显色用。
3显色
在上述已挥干的蒸发皿中准确加入0.2mL 5%香草醛冰乙酸溶液,转动蒸发皿,使残渣溶解,再加0.8mL高氯酸,混匀后移入l0mL比色管中,塞紧盖子于60℃以下水浴上加温15min取出,冷却后准确加入冰乙酸5.0mL,摇匀后以1.0cm 比色皿、于560nm处与人参皂苷Re标准管同时比色。
4标准曲线的绘制:
吸取人参皂苷Re标准溶液(2.0mg/mL)0、20、40、60、80、100μL(相当于人参皂苷Re0、40、80、120、160、200μg),于10mL比色管中,用氮气吹干,同4.(3)显色步骤测定吸光度。
并绘制标准曲线。
人参总皂苷浓度为20~200μg/mL之间与吸光度值呈线性关系,相关系数(r)0.999。
五、结果计算
式中X——样品中总皂苷(以人参皂苷Re计)(g/kg或g/L);
m——试样质量或试液体积(g或mL);
V1——样品提取液总体积(mL);
V2——样品提取液测定用体积(mL);
m1——从标准曲线查得待测液中人参皂苷Re量(μg)。
六、注释
1.人参系五加科植物是人参Panax ginseng C A Meyer的根,含有多种人参皂苷(ginsenoside),多数为达玛烷型皂苷,如人参皂苷Ra l、Ra2、Rb l、Rb2、Rb3、Re、Rd等;少数为齐墩果酸型(C型)皂苷,如人参皂苷Re。
由于苷元不同,达玛烷型皂苷又分为:20S—原人参二醇类皂苷(A型)和20S—原人参三醇类皂苷(B型)。
其中,A型和B型皂苷酸水解后,分别得到人参二醇(Panaxadial)和人参三醇(panaxatriol)。
除人参外,五加科的西洋参、三七、刺人参、刺五加和葫芦科的绞股蓝中亦含有与人参皂苷类似的化合物。
当保健食品原料配方中含有上述多种原料时,即以本法“总皂苷(以人参皂苷Re计)”报告检测结果。
2.对于人参、西洋参、绞股蓝纯品或以其为主要原料加工的保健食品,按《中华人民共和国药典》2000年版一部第99页,以薄层色谱法进行鉴定试验,将受试品色谱与对照药材色谱及对照品色谱进行比较确定其主要原料后,人参、西洋参制品仍以人参皂苷Re为对照品进行检测,而绞股蓝制品以绞股蓝总皂苷(中国药品生物制品检定所)为对照品进行检测,分别以“人参总皂苷”、“西洋参总皂苷”、“绞股蓝总皂苷”报告检测结果。
3.回收率:90%~105%。
