超敏心肌肌钙蛋白T(hs-cTnT)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求puenguangde
血清高敏肌钙蛋白T(hs-TNT)测定

血清高敏肌钙蛋白T(hs-TNT)测定
一、检测原理
用电化学发光技术的双抗体夹心法进行测定,检测原理:第一次孵育:50ul样品,生物素化的单克隆hs-TNT特异性抗体以及钌复合物标记的单克隆hs-TNT抗体一起孵育,形成抗原抗体夹心复合物。
第二次孵育:添加包被链酶亲和素的磁珠微粒进行孵育,复合体与磁珠通过生物素和链酶素作用结合。
将反应液吸入测量池中,通过电磁作用将磁珠吸附在电极表面,未与磁珠结合的物质通过Procell被去除,给电极加一定的电压,使复合物化学法光,并通过电倍增器测量发光强度,仪器自动通过校准曲线计算得到hs-TNT浓度。
二、参考区间
血清、血浆:>0.014ug/L
三、临床意义
1、肌钙蛋白仅存在于心肌细胞中是心肌特异性最高的心肌酶。
2、肌钙蛋白是心肌损伤坏死的标记物,对急性心肌梗死的
诊断具有重要的价值。
3、肌钙蛋白升高的主要病因包括:急性心肌梗死,严重的不稳定性心绞痛,肺梗死严重的心力衰竭,化疗药物的副作用,胸外按压、电复律、结缔组织病等
4、肌钙蛋白一般在发病后3-4小时后开始升高,10-24小时可以达到峰值,在7-10天内恢复正常
5、临床检验常用的指标是肌钙蛋白I和肌钙蛋白T。
超敏肌钙蛋白T

ACS诊断过程中肌钙蛋白的使用
2007年ESC指南推荐--诊断流程
就诊 询问病史 心电图 生化检测 危险分层
胸闷,胸痛 怀疑ACS(急性冠脉综合症)
持续ST段抬高 ST/T段异常 Troponins 阳性 心电图正常
Troponins 阴性X2
高危
ST段抬高心梗 (STEMI) 非ST段抬高心梗
低危
507位超过20分钟胸痛患者
cTnT-hs的早期诊断灵敏度优于其他肌钙蛋白
APACE 研究
灵敏度
(95% CI)
特异性
(95% CII)
阴性预测值
(NPV)
阳性预测值 value (PPV)
70
(50-86)
Abbott cTnI Architect 99th percentile (0.028
µg/L)
肌红蛋白/CKMB 敏感性↑特异性↓ 肌钙蛋白 敏感性↓ 特异性↑
高敏肌钙蛋白T
敏感性↑特异性↑
为何要使用高敏肌钙蛋白
• 高敏肌钙蛋白带来检验的进步
– 更高的敏感性 – 更佳的准确度
• 高敏肌钙蛋白带来临床的获益
– 提前诊断心梗时间 – 发现更多心梗患者
制作工艺不断进步,肌钙蛋白检测水平不断提高
高敏肌钙蛋白T的临床应用
(High-Sensitivity Cardiac Troponin T Assay)
Acute Chest Pain-->AMI
• • • •
Delay in adequate therapy Morbidity("time is muscle") Cost Patient:Anxiety...
70
(50-.86)
肌钙蛋白T(cTnT)测定试剂盒(化学发光免疫分析法)产品技术要求taige
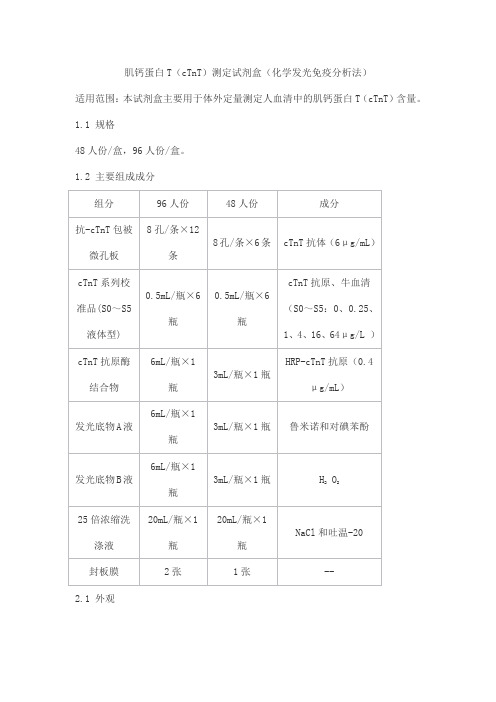
肌钙蛋白T(cTnT)测定试剂盒(化学发光免疫分析法)
适用范围:本试剂盒主要用于体外定量测定人血清中的肌钙蛋白T(cTnT)含量。
1.1 规格
48人份/盒,96人份/盒。
1.2 主要组成成分
2.1 外观
液体组分澄清,无沉淀或絮状物;其它组分无包装破损,标签外观完整、无脱落、标签标识清晰。
2.2 装量
装量不少于标示值。
2.3 准确性
回收率应在90.0%~110%范围内。
2.4 剂量-反应曲线线性相关系数
在[0.25,64]μg/L范围内,用log-logit数学模式拟合,剂量-反应曲线相关系数(r)的绝对值应不小于0.9900。
2.5 精密度
2.5.1 重复性(C.V%)应不高于15.0%;
2.5.2 批间差(C.V%)应不高于20.0%。
2.6 最低检出量
应不高于0.250μg/L。
2.7 质控血清测定值
应在允许的范围之内。
2.8 特异性
cTnT与肌红蛋白、cTnI、肌酸激酶同工酶的交叉反应如下:
2.9 稳定性
2.9.1 37℃放置3天,测定结果应符合上述2.1~2.7项要求。
2.9.2 成品试剂盒2~8℃存放6个月后,测定结果应符合上述2.1~2.7项要求。
2.10 校准品溯源性
按照GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》要求,该校准品溯源至本公司内部工作校准品,通过与湖南隆润达生物技术有限公司的cTnT试剂盒比对赋值。
高敏肌钙蛋白I测定试剂盒(化学发光免疫分析法)产品技术要求万孚

2性能指标
2.1外观
外观应符合如下要求:
a)磁珠包被物R1摇匀后应为棕褐色悬浊液;静止久后,棕褐色磁珠沉降于底部,上清液应为无色液体;酶标记物R2应为无色液体,无沉淀或絮状物;样本处理液R3应为无色液体;校准品应为外观均匀,成形完整,呈乳白色的冻干品,复溶后较清亮,无浑浊及沉淀;
b)试剂盒各组分应齐全、完整,液体无渗漏;
c)中文包装标签清晰,无磨损。
2.2准确度
将具有溯源性的两个正确度控制品进行检测,检测结果与标定浓度的相对偏差在±10% 范围内。
2.3空白限
空白限不大于0.006ng/mL;
2.4线性
试剂盒在0.01ng/mL~50 ng/mL 区间内,其相关系数(r)的绝对值不低于0.9900。
2.5重复性
变异系数CV≤8%。
2.6批间差
变异系数CV≤10%.
2.7分析特异性
测定浓度均为1000ng/mL 的心肌肌钙蛋白C、心肌肌钙蛋白T、骨骼肌肌钙蛋白I,交叉反应率应≤0.1%。
2.8校准品
2.8.1校准品准确度
测定校准品,C1,C2 测定结果的相对偏差在±10%范围内,C0 测定结果的绝对偏差的绝对值不高于0.006ng/mL。
2.8.2校准品瓶内均一性
校准品C1,C2 瓶内均一性≤8%,C0 的SD≤0.006ng/mL。
2.8.3校准品瓶间均一性
校准品C1,C2 瓶间均一性≤5%,C0 的SD≤0.006ng/mL。
高敏心肌肌钙蛋白I(hs—cTnI)测定试剂盒(化学发光免疫分析法)产品技术要求深圳市锦瑞生物
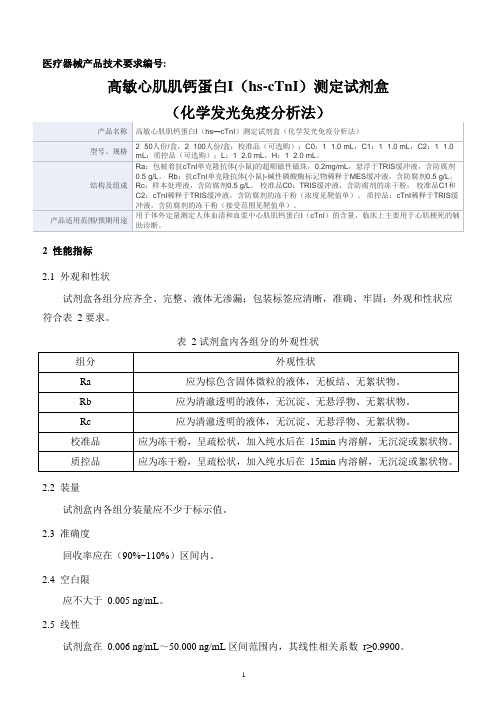
医疗器械产品技术要求编号:高敏心肌肌钙蛋白I(hs-cTnI)测定试剂盒(化学发光免疫分析法)2性能指标2.1外观和性状试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;外观和性状应符合表 2 要求。
表 2 试剂盒内各组分的外观性状2.2装量试剂盒内各组分装量应不少于标示值。
2.3准确度回收率应在(90%~110%)区间内。
2.4空白限应不大于0.005 ng/mL。
2.5线性试剂盒在0.006 ng/mL~50.000 ng/mL 区间范围内,其线性相关系数r≥0.9900。
2.6重复性用急性心肌梗死临界值±50%水平的样本,重复检测10 次,其变异系数(CV)应不大于6%。
2.7批间差用3 个批号试剂盒检测同一份样本,则3 个批号试剂盒之间的批间变异系数(CV)应不大于10%。
2.8特异性2.8.1心肌肌钙蛋白C(cTnC)测定浓度为1000 ng/mL 的心肌肌钙蛋白C,交叉反应率应小于0.1%。
2.8.2心肌肌钙蛋白T(cTnT)测定浓度为1000 ng/mL 的心肌肌钙蛋白T,交叉反应率应小于0.1%。
2.8.3骨骼肌肌钙蛋白I(sTnI)测定浓度为1000 ng/mL 的骨骼肌肌钙蛋白I,交叉反应率应小于0.1%。
2.9质控品测定值用试剂盒配套的校准品校准测量系统后,以试剂盒配套的质控品作为样本进行检测,其测定结果应在标示范围内。
2.10质控品均一性瓶间变异系数(CV)应不大于10%。
2.11校准品测量准确度用工作校准品校准测量系统后,以试剂盒配套的校准品作为样本进行检测,C1、C2 测定结果与标示值的相对偏差应在±10%范围内;C0 测定结果的绝对偏差应不大于0.005ng/mL。
2.12校准品均一性C1,C2 瓶间变异系数(CV)应不大于10%;C0 瓶间标准差(SD)应不大于0.005ng/mL。
磁敏免疫法与化学发光法检测心肌肌钙蛋白I方法与性能比较

磁敏免疫法与化学发光法检测心肌肌钙蛋白I方法与性能比较侯立安,夏良裕,嵇 巍,徐二木,刘 茜,刘 荔(中国医学科学院北京协和医院检验科,北京100730)摘要:目的 评价磁敏免疫法检测cTnI的分析性能以及与化学发光法检测结果的可比性。
方法 选择cTnI水平在参考区间上限附近、低、中和高水平的4类样本,用理邦m16磁敏免疫分析仪进行连续测定,评价检测系统参考范围处精密度、不同批号测试卡精密度和不同仪器的精密度。
检测20例表观健康人进行参考区间验证。
收集西门子DimensionEXL分析系统检测cTnI后患者剩余肝素锂抗凝血浆102例,用理邦m16进行检测,比较两个检测系统结果的相关性和一致性。
结果 参考范围上限精密度CV在5.7%~8.0%之间。
不同批号测试卡在三个水平cTnI检测中不精密度CV在3.4%~9.7%之间,低水平不精密度高于其他两个水平。
测试卡在高、中、低三个水平的总不精密度分别为9.3%、4.1%和4.8%。
两台不同仪器的低、中、高三水平的平均不精密度为8.6%、3.9%和4.6%。
磁敏免疫分析法与化学发光法结果的相关系数r为0.9959。
磁敏免疫分析临床诊断的阳性和阴性符合率均为100%。
结论 磁敏免疫法检测cTnI的分析精密度符合要求,临床诊断性能与本实验室当前在用的化学发光法一致。
关键词:磁敏免疫分析; 心肌肌钙蛋白I;化学发光法; 床旁快速检测中图分类号:R446.1 文献标识码:AAComparisonoftheMethodsandPropertiesofMagnetic SensitiveImmunoassayandChemiluminescenceintheDetectionofCardiacTroponinIHOULi′an,XIALiangyu,JIWei,XUErmu,LIUQian,LIULi(DepartmentofClinicalLaboratory,PekingUnionMedicalCollegeHospital,ChineseAcademyofMdeicalSciences&PekingUnionMedicalCollege,Beijing100730,China)Abstract:ObjectiveToevaluatetheperformanceofmagneticsensitiveimmunoassaystodetectcTnI,andtoanalyzetherelevanceandconsistencyoftheresultsbetweenmagneticsensitiveimmunoassaysandchemiluminescenceassays.MethodsFourclassesofcTnIsampleswereselected,withconcentrationsincluding:neartheupperlimitofthereferenceinterval,low,mediateandhighlevels.Thesamplesweremeasuredcontinuouslybym16magneticsensitiveimmunoanalyzertoevaluatetheprecisionatthereferencerangeofthetestsystem,theprecisionofdifferentbatchnumbertestcardsandtheprecisionofdifferentinstruments.Theserumof20healthyindividualswasselectedtoverifythereferencerangeofmagneticsensitiveimmunoassay.Theremaininglithiumheparinanticoagulantplasmaof102patientsafterthedetectionofcTnIbySiemensDimensionEXLanalysissystemwerecollected.Thesamplesweredetectedbym16magneticsensitiveimmunoanalyzer.Wethencomparedthecorrelationandconsistencyoftheresultsofthetwodetectionsystems.ResultsTheCVoftheupperlimitofthereferencerangewasbetween5.7%and8.0%.Theinter runCVofthetestcardinthreelevelswasbetween3.4%and9.7%,andthelowlevelofimprecisionwashigherthantheothertwolevels.ThetotalCVofthetestcardwere9.3%,4.1%and4.8%atthethreelevelsofhigh,mediumandDOI:10.11748/bjmy.issn.1006-1703.2020.10.024收稿日期:2020 06 28;修回日期:2020 09 15基金项目:国家高技术研究发展计划(863计划)子课题(编号:2011AA02A111)作者简介:夏良裕,副主任技师。
超敏肌钙蛋白I测定试剂盒产品技术要求新产业

超敏肌钙蛋白I测定试剂盒产品技术要求新产业1.试剂盒成分:试剂盒应包含超敏肌钙蛋白I检测试剂、质控品、稀释缓冲液等试剂。
2.检测原理:该试剂盒基于化学发光免疫分析法,测定血液中的超敏肌钙蛋白I浓度。
该方法利用特异性抗体与超敏肌钙蛋白I结合,产生荧光信号,通过测定荧光信号的强度来确定样品中超敏肌钙蛋白I的浓度。
3. 灵敏度:试剂盒应具有高灵敏度,能够在低浓度范围内准确测定超敏肌钙蛋白I的浓度。
通常,灵敏度应在1 ng/mL以下。
4.精密度:试剂盒应具有良好的精密度,能够在同一实验条件下反复测定,结果应具有较低的变异性。
精密度可通过重复测定一组质控品来评估。
5.线性范围:试剂盒应具有宽线性范围,能够测定不同浓度范围内的超敏肌钙蛋白I。
一般来说,线性范围应当覆盖从低浓度到高浓度的所有可能浓度。
6.特异性:试剂盒应具有良好的特异性,能够与超敏肌钙蛋白I结合,而不与其他相关蛋白结合。
特异性可以通过与其他蛋白进行交叉反应的实验来评估。
7.储存条件:试剂盒的储存条件应符合通常的实验室要求,通常需要在2-8°C下储存,避免冻结。
8.使用方便性:试剂盒应具有使用方便、操作简单的特点,能够被广泛的临床实验室使用。
试剂盒应提供详细的操作指南,并且包含所有必要的试剂和耗材。
9.技术支持:试剂盒的生产商应提供有效的技术支持,包括现场指导、问题解答和技术培训等。
同时,试剂盒应附带一份完整的说明书,包含使用步骤、注意事项和结果解释等内容。
超敏肌钙蛋白I测定试剂盒的技术要求是确保其在临床实验室中准确、可靠地测定血液中超敏肌钙蛋白I浓度的关键。
通过满足这些技术要求,可以提高心肌梗死的早期诊断和预后评估的准确性,为临床医生提供更好的诊断和治疗决策依据。
肌钙蛋白T测定试剂盒产品技术要求万孚

肌钙蛋白T测定试剂盒产品技术要求万孚1.产品简介:肌钙蛋白T测定试剂盒是一种高灵敏度、高特异性的试剂盒,用于检测肌钙蛋白T水平。
该试剂盒通过化学发光免疫分析法,利用特异性的抗体与肌钙蛋白T结合,生成免疫复合物,进而产生化学发光信号,通过光度计测量信号强度,从而确定样本中肌钙蛋白T的浓度。
2.抗体:该试剂盒中所使用的抗体应为高亲和力、高特异性的肌钙蛋白T抗体。
抗体应经过充分的验证,并能与肌钙蛋白T特异性结合,不与其他相关物质发生非特异性反应。
3.校准品:试剂盒应包含不同浓度的校准品,用于构建标准曲线。
校准品应经过准确测定其肌钙蛋白T浓度,并保证稳定性。
4.灵敏度:试剂盒应具有足够的灵敏度,能够检测出低至0.01 ng/mL的肌钙蛋白T浓度。
5.线性范围:试剂盒应具有宽广的线性范围,能够涵盖生理范围内的肌钙蛋白T浓度变化。
6.重复性:试剂盒应具有良好的重复性,同一样本的重复测定结果应具有较小的变异性。
7.特异性:试剂盒应具有良好的特异性,不受其他相关物质的干扰。
8.稳定性:试剂盒的试剂和材料应具有良好的稳定性,能够保持在规定的储存条件下长期保存。
9.操作简便性:试剂盒的操作步骤应简单明了,能够被普通实验室人员快速掌握并使用。
10.结果解读:试剂盒的结果应能够准确、直接地反映样本中肌钙蛋白T的浓度,并能够被普通实验室人员快速解读。
以上是对肌钙蛋白T测定试剂盒产品技术要求的详细描述,通过满足这些要求,可以确保该产品可以准确、可靠地测定肌钙蛋白T水平,从而在临床诊断和研究中发挥重要作用。
联合cTnT、hs-CRP、NT-ProBNP测定对心力衰竭的诊断及预后判断的意义

联合cTnT、hs-CRP、NT-ProBNP测定对心力衰竭的诊断及预后判断的意义刘路平;谢晓林;林玎【摘要】目的探讨心肌肌钙蛋白T(cTnT)、高敏C反应蛋白(hs-CRP)和B型钠尿肽前体(NT-ProBNP)联合检测对心力衰竭诊断和预后判断的价值.方法测定115例明确诊断为CHF的不同病因、不同心功能分级的患者入院时、出院时血清cTnT、hs-CRP和血浆NT-ProBNP水平,进行治疗前后对比观察,并与30名健康对照组比较,随访观察患者心脏事件再发生的情况.结果血清cTnT、hs-CRP和血浆NT-ProBNP水平在CHF患者不同心功能分级组和对照组之间差异均有统计学意义,且心功能越差,其浓度越高(均P<0.01);三者在CHF患者治疗前后比较,差异均有统计学意义(均P<0.01);三者联合检测在CHF患者早期敏感性为78.3%,明显优于单项检测(均P<0.01);出院后发生心脏事件组血清cTnT、hs-CRP和血浆NT-ProBNP 出院时浓度明显高于未发生心脏事件组(均P<0.01).结论血清cTnT、hs-CRP和血浆NT-ProBNP在CHF患者中明显升高,三者联合检测对CHF临床诊断和预后判断有应用意义.【期刊名称】《心脑血管病防治》【年(卷),期】2011(011)001【总页数】3页(P40-42)【关键词】肌钙蛋白T;高敏C反应蛋白;B型钠尿肽前体;心力衰竭;预后判断【作者】刘路平;谢晓林;林玎【作者单位】杭州市第三人民医院,浙江,杭州,310009;杭州市第三人民医院,浙江,杭州,310009;杭州市第三人民医院,浙江,杭州,310009【正文语种】中文【中图分类】R541.6;R446充血性心力衰竭(congestive heart failure CHF)是心血管疾病最常见的死亡原因,因心衰呈进行性发展,临床处于稳定状态的心衰患者,心肌损伤依旧存在。
肌钙蛋白T(cTnT)是反映心肌损伤的高度敏感、高度特异的标志物;B型钠尿肽(BNP)、B型钠尿肽前体(NT-ProBNP)在心室壁张力增加、心室伸张时分泌增加,因为半衰期长,作为早期心功能损害的标志物,NT-ProBNP更加敏感;高敏C反应蛋白(hs-CRP)为肝脏合成的敏感急性炎症时相蛋白,在心肌损伤发生早期即出现增高,并与心肌损害呈正相关。
心肌肌钙蛋白I测定试剂盒(荧光免疫层析法)产品技术要求zhongjianantai

心肌肌钙蛋白I测定试剂盒(荧光免疫层析法)
适用范围:本试剂盒用于体外定量检测人血清、血浆或全血样本中心肌肌钙蛋白I(cTnI)的含量。
1.1包装规格:20人份/盒,40人份/盒。
1.2主要组成:
表1 试剂盒产品组成表
2.1 物理检查
2.1.1 外观
外观平整,材料附着牢固,内容齐全,试剂无杂质,外包装完整无破损,标签清晰可辨。
2.1.2 膜条宽度
膜条宽度应满足4.0mm±0.2mm。
2.1.3 液体移行速度
液体移行速度应不低于10mm/min。
2.1.4 样本稀释液
样本稀释液的净含量应不少于标示值,且其pH值为7.0±0.2。
2.2准确度
试剂盒的回收率在85%~115%之间。
2.3线性
在[0.2,50]ng/mL范围内,线性相关系数(r)应不低于0.990。
2.4 重复性
分别测定高、低两个浓度的样本,变异系数(CV)应不高于10.0%。
2.5 批间差
用三个不同批号试剂盒分别测定高、低两个浓度的样本,三个批号试剂盒之间的批间变异系数应不高于15.0%。
2.6 空白限
试剂盒空白限应不大于0.1ng/mL。
2.7校准信息溯源性
校准信息所用工作校准品根据GB/T 21415-2008 《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的规定,溯源至工作校准品,工作校准品通过已上市产品进行赋值。
2.8 稳定性
试剂盒在规定的条件下保存至有效期末,取到效期后两个月内的试剂盒,检测2.2、2.3、2.4、2.6项,结果应符合要求。
超敏肌钙蛋白T(HS-TNT)、肌酸激酶同工酶(CK-MB)、肌红蛋白(Mb)浓度监测在诊断急性心肌梗死(AMI)中的作用

心血管病防治知识2015年第7期作者简介:李从凤,1971年生,女,汉族,大理弥渡人,本科学历,副主任检验技师,主要从事临床生化和微生物检验方面的工作。
筝论著/冠心病筝超敏肌钙蛋白T(HS-TNT)、肌酸激酶同工酶(CK-MB)、肌红蛋白(Mb)浓度监测在诊断急性心肌梗死(AMI)中的作用李从凤(云南省大理州弥渡县人民医院,云南大理675600)【摘要】目的探析在急性心肌梗死(AMI)患者中,超敏肌钙蛋白T(HS-TNT)、肌酸激酶同工酶(CK-MB)、肌红蛋白(Mb)浓度监测在临床诊断中的作用和临床意义。
方法选择我院2014年1月至2014年12月收治的46例AMI 患者作为观察组,另选同期的44例体检正常者作为对照组,采用电化学发光分析法测定患者血清中的HS-TNT 、CK-MB 、Mb 值。
结果观察组中HS-TNT 阳性性率为67.4%,CK-MB 阳性性率为46.7%,Mb 阳性性率为32.6%,对照组患者检查结果中均未见HS-TNT 、CK-MB 、Mb ;HS-TNT 和CK-MB 在胸痛后12-24h 出现峰值,Mb 的峰值在3~8h 内最先出现;入院72h 后,Mb 和CK-MB 值均已降至正常范围,HS-TNT 值仍明显高于正常范围。
结论超敏肌钙蛋白T 和肌酸激酶同工酶(CK-MB)监测对急性心肌梗死早期诊断具有较高的特异性和灵敏度,是判断心肌梗死的重要指标。
【关键词】超敏肌钙蛋白;肌酸激酶同工酶;肌红蛋白;急性心肌梗死Monitoring of high-sensitivity troponin T,creatine kinase-MB,and myoglobin in diagnosis ofacute myocardial infarctionLI Cong-feng(Midu County People's Hospital,Dali 675600,China)【Abstract 】Objective To investigate the role and significance of monitoring of high-sensitivity troponin T (HS-TNT),creatine kinase-MB (CK-MB),and myoglobin (Mb)in the clinical diagnosis of acute myocardial infarction (AMI).Method sA total of 46AMI patients who were admitted to Midu County People's Hospital from January 2014toDecember 2014were selected as observation group,and 44healthy people were selected as control group.The levels of HS-TNT,CK-MB,and Mb of the two groups were determined using electrochemiluminescent analysis.Results Thepositive rates of HS-TNT,CK-MB,and Mb in the observation group were 67.4%,46.7%,and 32.6%,respectively,while no HS-TNT,CK-MB and Mb were detected in the control group;the HS-TNT and CK-MB reached peak values at 12to 24h after chest pain,and Mb reached peak value firstly at 3to 8h;72h after admission to the hospital,Mb and CK-MB both decreased to normal levels,but the HS-TNT was still above normal range.Conclusion The monitoring of HS-TNT and CK-MB have high specificity and sensitivity in the diagnosis of AMI,and can be considered as an importantindicator for evaluating myocardial infarction.【Key words 】High-sensitivity troponin T;Creatine kinase-MB;Myoglobin;Acute myocardial infarction长期以来,临床上主要通过检测某些血清酶的变化对急性心肌梗死进行诊断[1]。
心肌标志物6项质控品产品技术要求北京康彻思坦

心肌标志物6项质控品适用范围:本品适用于使用厦门万泰凯瑞生物技术有限公司的心肌肌钙蛋白T 测定试剂盒(化学发光微粒子免疫检测法)、N端脑钠肽前体测定试剂盒(化学发光微粒子免疫检测法)、超敏C反应蛋白测定试剂盒(化学发光微粒子免疫检测法)、心肌肌钙蛋白I测定试剂盒(化学发光微粒子免疫检测法)、肌红蛋白测定试剂盒(化学发光微粒子免疫检测法)和肌酸激酶同工酶测定试剂盒(化学发光微粒子免疫检测法)进行临床检测时的实验室内部质量控制。
1.1 包装规格水平1(复溶体积):1×2mL,10×2mL,30×2mL;水平2(复溶体积):1×2mL,10×2mL,30×2mL;水平3(复溶体积):1×2mL,10×2mL,30×2mL;全水平(复溶体积):水平1 1×2mL,水平2 1×2mL,水平3 1×2mL。
1.2 主要组成成分注:不同批次质控品不能混用;每批次质控品的质控范围见试剂盒内靶值单。
2.1外观试剂(盒)各组分应齐全、完整;标签应清晰,包装无破损。
冻干品应为疏松体,复溶后液体应澄清。
2.2质控品赋值有效性检测结果应在质控范围内。
2.3 均匀性2.3.1瓶间差瓶间变异系数应不高于15%。
2.3.2瓶内均匀性瓶内变异系数应不高于10%。
2.4稳定性2.4.1复溶稳定性原包装质控品在开瓶完全复溶后,置于2℃~8℃条件下保存,放置24小时后进行检测,结果应符合2.2项的规定。
2.4.2 效期稳定性原包装质控品在2℃~8℃的条件下储存,有效期为36个月。
取效期末产品进行检测,结果应符合2.1、2.2、2.3.2项的规定。
肌钙蛋白 I(cTnI)测定试剂盒(胶乳免疫比浊法)说明书

肌钙蛋白I (cTnI)测定试剂盒(胶乳免疫比浊法)说明书【产品名称】肌钙蛋白I(cTnI)测定试剂盒(胶乳免疫比浊法)【包装规格】a)试剂1:1×15mL 试剂2:1×5mL b)试剂1:2×45mL 试剂2:2×15mL c)试剂1:4×60mL 试剂2:4×20mL d)试剂1:2×60mL 试剂2:2×20mL 【预期用途】用于体外定量测定人血清中肌钙蛋白I 的含量。
肌细胞受损时,肌钙蛋白I (cTnI )立即释放入血,在胸痛发生4-6h 后,血中cTnI 水平超过正常上限,12-24h 达高峰,可持续6~10天之久。
由于cTnI 可检出微小心肌损伤,是公认的快速诊断急性心肌梗死和急性冠脉综合症(ACS )[1]。
测定肌钙蛋白I 常用于心肌细胞受损、急性心肌梗死、急性冠脉综合症的辅助诊断。
【检验原理】样本与胶乳试剂在缓冲液中混合后,其中的肌钙蛋白Ⅰ与胶乳颗粒表面的抗体结合,使相邻的胶乳颗粒彼此交联,发生凝集反应产生浊度变化,该浊度变化与样本中的肌钙蛋白的量成正相关。
【主要组成成分】试剂1主要组分磷酸盐缓冲液30mmol/L聚乙二醇(PEG )0.5%表面活性剂及稳定剂适量试剂2主要组分磷酸盐缓冲液30mmol/L抗人肌钙蛋白(cTnI )抗体乳胶颗粒适量表面活性剂及稳定剂适量注:不同批号试剂盒中各组分未经试验不可互换。
【储存条件及有效期】1.试剂原包装在2~8℃储存,有效期为12个月,生产日期、有效期见标签。
2.开口后的试剂在仪器仓中(2~8℃)可稳定30天。
【适用仪器】艾威德AS-420/AS-660/AS-1200;日立HITACHI 7020型/7060型/7180型/7600型/LABOSPECT 008AS 型;贝克曼AU400/AU480/AU640/AU680/AU2700/AU5400/AU5800/AU5811/AU5821;佳能TBA-FX8/TBA-120FR /TBA-2000FR ;罗氏cobas 8000c 702/cobas 8000c 701/cobas 8000c 502;西门子SIEMENS ADVIA 1800/ADVIA 2400;雅培ABBOTT ARCHITECT c8000/ARCHITECT c16000/ARCHITECT ci8200;西森美康SYSMEX BM6010/C ;科华KHB 卓越310/卓越330/卓越400/卓越450/ZY-1200/ZY-1280;迪瑞CS-240/CS-T300/CS-300B/CS-380/CS-400A/CS-400B/CS-600A/CS-600B/CS-800A/CS-800B/CS-1200/CS-1200ISE/CS-1300B/CS-1400;迈瑞MINDRAY BS-220/BS-330/BS-350E/BS-380/BS-390/BS-400/BS-430/BS-600/BS-800/BS-2000M ;颐兰贝ES-200/ES-380/ES-480;赛诺迈德SUNMATIK-9050型;雷杜Chemray 420;英诺华D280;特康TC6010L ;锦瑞GS400;普康6066。
心肌肌钙蛋白I(cTnI)测定试剂盒(化学发光法)产品技术要求tongxin

心肌肌钙蛋白I(cTnI)测定试剂盒(化学发光法)适用范围:本试剂盒用于体外定量测定人血清或血浆中心肌肌钙蛋白I(cTnI)的含量。
分说明1.1 包装规格96人份/盒1.2 主要组成成分表1 主要组成成分备注:校准品溯源至美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)颁布的有证标准参考物质(SRM 2921),校准品(A~F)目标浓度为0、0.5、1.4、4.0、18.0、45.0ng/ml。
2.1 外观组分齐全、完整,液体无渗漏,微孔板包装袋无破损、漏气现象;包装标签应清晰,易识别。
2.2 装量液体装量应不少于标示值。
2.3 准确度在剂量反应曲线检测范围内,用已知浓度的纯品(源自Hytest公司)做回收试验,其回收率应在85~115%范围内。
2.4 线性在线性范围[0.25,45]ng/ml内,剂量反应曲线相关系数(r)的绝对值应不低于0.9900。
2.5 空白限应不大于0.25ng/ml。
2.6 重复性同一次试验中分别重复检测浓度值为1.35±0.33ng/ml、18.83±3.78ng/ml样本10次,其变异系数(CV)应不大于10.0%。
2.7 批间差用3个批号的试剂盒检测浓度值为1.35±0.33ng/ml、18.83±3.78ng/ml样本,3个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.8 分析特异性测定浓度为1000ng/ml 心肌肌钙蛋白C(Cardiac Troponin C,cTnC),交叉反应率小于0.05%。
测定浓度为1000ng/ml 心肌肌钙蛋白T(Cardiac Troponin T,cTnT),交叉反应率小于0.05%。
测定浓度为1000ng/ml 骨骼肌肌钙蛋白I(Skeletal Troponin I,sTnI),交叉反应率小于0.05%。
化学发光高敏肌钙蛋白的优势

化学发光高敏肌钙蛋白的优势化学发光高敏肌钙蛋白(hs-cTn)检测具有多个优势,尤其适用于急性冠状动脉综合征(ACS)的快速诊断和风险分层。
以下是化学发光hs-cTn检测的几个关键优势:1. 提高灵敏度和特异性:hs-cTn检测能够检测到远低于传统肌钙蛋白检测限的水平,这意味着即使在心肌损伤非常轻微的情况下也能被检测到。
同时,由于其高特异性,它可以减少假阳性结果的出现。
2. 早期诊断:由于hs-cTn的高灵敏度,它允许医生在症状出现后的早期阶段检测到心肌损伤,有助于尽早识别和治疗ACS。
3. 风险评估:hs-cTn水平不仅可以用于诊断ACS,还可以用来评估患者的风险,高水平的hs-cTn通常与较高的心血管事件风险相关联。
4. 动态监测:在患者入院后,通过监测hs-cTn水平的变化,医生可以评估病情的进展和治疗效果,以及判断患者是否有再次发生心脏事件的风险。
5. 操作简便快捷:化学发光技术通常配备有自动化的分析仪器,这些仪器能够快速准确地处理样本,并在短时间内(通常是几分钟内)提供结果,从而加快了诊疗流程。
6. 稳定性和重复性好:化学发光技术产生的结果具有很高的稳定性和重复性,这对于确保患者接受一致和可靠的医疗服务至关重要。
7. 广泛的临床应用:hs-cTn检测不仅限于心脏疾病的诊断,还可以用于其他条件下心肌损伤的评估,如心脏手术后、重症监护病人或慢性肾脏病患者的监测。
8. 指导治疗决策:hs-cTn检测结果可以帮助医生做出是否进行侵入性干预(比如冠状动脉造影和介入治疗)的决策,从而为患者提供更加个性化的治疗方案。
总的来说,化学发光hs-cTn检测因其高度的敏感性和特异性,以及快速、准确和方便的特点,已经成为临床上评估心脏损伤不可或缺的工具之一。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
超敏心肌肌钙蛋白T(hs-cTnT)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血浆中心肌肌钙蛋白T(cTnT)的含量。
1.1包装规格
50人份、100人份
1.2 主要组成成分
质控品质控范围批特异,详见标签。
2.1 外观
2.1.1 试剂盒各组分应齐全、完整,液体无渗漏;
2.1.2 中文包装标签应清晰,无磨损。
2.2 空白限
空白限浓度应不高于0.005ng/mL。
2.3 线性
在[0.005,10]ng/mL区间内,线性相关系数(r)应不低于0.99,且线性区间[0.005,2.0]ng/mL内,绝对偏差应不超过±0.3ng/mL;线性区间
(2.0,10]ng/mL内,相对偏差应不超过±15%。
2.4 重复性
分别用高、低浓度的样本各重复检测10次,其变异系数(CV)应不大于10%。
2.5 准确度
用Human Cardiac Troponin Complex(NIST SRM2921)国际标准品作为样本进行检测,其测量结果的相对偏差应在±20%区间内。
2.6 分析特异性
测定浓度均为1000ng/mL的心肌肌钙蛋白C、心肌肌钙蛋白I、骨骼肌肌钙蛋白I,测定结果应不高于0.005ng/mL。
2.7 溯源性
根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》及有关规定提供校准品的来源、赋值过程及测量不确定度等内容。
校准品溯源至美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)的Human Cardiac Troponin Complex(SRM2921)。
2.8 质控品赋值有效性
本试剂盒质控品的测定结果应在质控范围内。
2.9 批间差
用3个批号的产品分别检测同一份样本,3批产品间的相对极差(R)应不大于15%。
2.10 稳定性
试剂盒在(2~8)℃储存条件下的有效期为12个月,试剂盒在规定的条件下保存,取到效期后的试剂盒进行检测,检验结果应符合2.1、2.2、2.3、2.4、2.5、2.6的规定。
