以天然气为原料合成氨实用工艺
天然气制合成氨简介

精选ppt
7
2.1 概述
天 然 气 综 合 利 用 技 术
精选ppt
8
2.2 天然气制合成氨的技术概况
天 然 气 综 合 利 用 技 术
精选ppt
9
2.2 天然气制合成氨的技术概况
天
然 气
2.2.1天然气精脱硫
综 硫化物脱除至0.5×10-6,甚至0.1×10-6。
合 利
2.2.1.1中温氧化锌精脱硫
热效率≈100%
废热锅炉 高压蒸汽过热器
精选ppt
50
2.3 天然气制合成氨生产技术应用及进展
天
然 气
中变炉
440℃
综 合
降温
原料空气预热器 锅炉给水预热器
利 用
低变炉 233℃
2.91MPa
CO 0.5%
技 术
脱除CO2 甲烷化 CO+CO2 < 10×10-6
脱除氨、残余CO2和水分 深冷净化装置
技 术
降低能耗,单程转化率高
优点 催化剂寿命长
合成氨可在较温和条件下操作
降低成本可,节能
提高合成系统的生产能力
精选ppt
42
2.3 天然气制合成氨生产技术应用及进展
天 然 气 综 合 利 用 技 术
精选ppt
43
2.3 天然气制合成氨生产技术应用及进展
天
然
气 ③ KRES合成气生产新工艺
综
合
采用换热式转化炉代替原有一段加
天
然 气
2.2.5.2 Braun深冷净化
综 合合成气
利
分子筛脱水
深冷净化
用
技
术
压缩
精选ppt
合成氨工艺简介

合成氨工艺简介工艺危险特点:1 高温、高压使可燃气体爆炸极限扩宽,气体物料一旦过氧(亦称透氧),极易在设备和管道内发生爆炸。
2 高温、高压气体物料从设备管线泄露时会迅速膨胀与空气混合形成爆炸性混合物,遇到明火或因郜流速物料与裂(喷)口处摩擦产生静电火花引起着火和空间爆炸。
3 气体压缩机等转动设备在高温下运行会使润滑油挥发裂解,在附近管道内造成积炭,可导致积炭燃烧和爆炸。
4 高温、高压可加速设备金属材料发生蠕变、改变金相组织,还会加剧氢气、氮气对钢材的氢蚀和渗氮,加剧设备的疲劳腐蚀,使其机械强度减弱,引发物理爆炸。
5 液氨大规模事故性泄露会形成低温云团引起大范围人群中毒,遇明火还会发生空间爆炸。
合成氨指由氮和氢在高温高压和催化剂存在下直接合成氨,为一种基本无机化工流程。
现代化学工业中,氨是化肥工业和基本有机化工的主要原料。
工艺流程1 原料气制备(制备H2、CO、N2的粗原料气)1-1煤气化煤气化是用气化剂对煤或焦炭等固体燃料进行热加工,使其转变为可燃性气体的过程,简称造气。
气化剂主要是水蒸气、空气(或氧气)及它们的混合气体。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;空气煤气:以空气为气化剂制取的煤气,主要成分为N2和CO2。
合成氨生产中也称之为吹风气。
水煤气:以水蒸气为气化剂制得的煤气,主要成分H2和CO。
混合煤气:以空气和适量水蒸气为气化剂。
半水煤气:以适量空气和水蒸气做气化剂,所得气体组成符合([H2]+[CO])/[N2]=3.1~3.2的混合煤气,即合成氨的原料气。
1-1-1 以空气为气化剂-空气煤气,其主要成分为空气和二氧化碳C + O2 = CO2C + 1/2O2 = COC + CO2 = 2COCO + 1/2O2 = 2CO21-1-2 以水蒸气为气化剂-水煤气,其主要成分为氢气和一氧化碳。
C + H2O = CO + H2C + 2H2O = CO2 + 2H2CO + H2O = CO2 + H2C + 2H2 = CH41-1-3 间歇式生产半水煤气1-1-3-1固定床煤气发生炉右图为间歇式固定床煤气发生炉燃料层分区示意图。
天然气合成氨工艺流程

天然气合成氨工艺流程
天然气合成氨是一种重要的工业化学反应,它是将天然气中的
氮气和氢气通过一系列催化反应转化成氨的过程。
氨是化肥生产的
重要原料,因此天然气合成氨工艺流程对于化肥行业具有重要意义。
下面将介绍天然气合成氨工艺流程的主要步骤。
首先,天然气经过脱硫处理,去除其中的硫化氢和二硫化碳等
杂质。
然后,经过蒸馏和压缩,将天然气中的甲烷和一氧化碳气体
分离出来,以便后续的反应使用。
接下来,将天然气中的氮气和氢
气按照一定的比例混合,送入氨合成反应器中。
在氨合成反应器中,混合气体经过一系列的催化反应,最终转
化成氨。
这个反应过程是一个放热反应,需要控制温度和压力,以
提高反应速率和产率。
同时,反应器中的催化剂也需要定期更换和
再生,以保持反应的高效进行。
经过氨合成反应器,产生的氨气体会通过冷凝和压缩,将其中
的水和未反应的气体分离出来,得到纯净的液态氨。
液态氨是化肥
生产的重要原料,可以直接用于合成尿素等化肥产品。
除此之外,天然气合成氨工艺流程中还包括废气处理和废水处
理等环节。
废气中的二氧化碳和一氧化碳等有害气体需要经过吸收
和催化氧化处理,以减少对环境的影响。
废水则需要经过中和、沉
淀和过滤等步骤,达到排放标准后才能排放。
总的来说,天然气合成氨工艺流程是一个复杂的化学工程过程,涉及到多个环节和技术。
通过合理的工艺设计和操作控制,可以提
高氨的产率和质量,降低能耗和环境污染。
因此,对于化肥生产企
业来说,掌握和优化天然气合成氨工艺流程是非常重要的。
合成氨工艺及反应原理简介

合成氨工艺及反应原理简介合成氨工艺采用烃类蒸汽转化法。
天然气经加压至4.05MPa,经预热升温在脱硫工序脱硫后,与水蒸汽混合,进入一段转化炉进行转化制H2,随后进入二段转化炉,在此引入空气,转化气在炉内燃烧放出热量,供进一步转化,同时获得N2。
工艺气经余热回收后,进入变换系统,将CO变为CO2,随后经脱碳、甲烷化反应除去CO和CO2,分离出的CO2送往尿素工艺。
工艺气进入分子筛系统除去少量水份,为合成氨提供纯净的氢氮混合气。
氢氮混合气经压缩至14MPa,送入合成塔进行合成氨的循环反应,少量惰性气体经过普里森系统分离进行回收利用。
产品氨送往尿素工艺和氨罐保存。
合成氨工艺的5个过程:1、天然气脱硫:R-SH+H2=RH+H2S H2S+ZnO=H2O(汽)+ZnS2、转化CH4+H20(汽)=CO+3H2 CH4+2H2O(汽)=CO2+4H2 (H2+ 1/2 O2=H2O)3、变换:CO+H2O(汽)=CO2+H24、脱碳:1)K2CO3+CO2+H2O⇔2KHCO32KHCO3⇔K2CO3+CO2+H2O2)甲烷化:CO+3H2=CH4+H2O CO2+4H2=CH4+2H2O5、N2+3H2=2NH31 脱硫系统工艺流程及原理1.1流程天然气进入界区后分为两路:一路作原料气,另一路作燃料气。
原料天然气进入原料气压缩机吸入罐116-F,除去携带的液体,经过原料气压缩机102-J被压缩到4.05MPa(G),经过原料气预热盘管预热到399℃,接着原料气与来自合成气压缩机103-J一段的富氢气混合。
经过Co-Mo加氢器101-D把有机硫转换成H2S,将3 ml/m3的有机硫转化为无机硫,原料气中总硫为30~90ml/m3左右,经氧化锌脱硫槽脱硫至总硫小于0.5mg/m3。
随后进入氧化锌脱硫槽,天然气中的硫化物被ZnO所吸附,制得合格原料气。
ZnO脱硫槽共二个,可以串联或并联操作,一般串联操作。
阀门及管线的配置可以使任何一个脱硫槽停止使用而另一个继续运转。
合成氨的生产工艺流程

合成氨的生产工艺流程合成氨是一种重要的化工原料,广泛应用于农药、肥料、塑料等行业。
合成氨的制备是一项复杂的过程,涉及到多个化学反应和工艺步骤。
本文将介绍合成氨的生产工艺流程,并逐步解析其中的关键步骤和反应。
1. 原料准备1.1 天然气处理在合成氨的生产中,最常用的原料是天然气。
天然气中主要含有甲烷,须进行处理以消除其中的杂质。
天然气处理的关键步骤包括脱除硫化物、脱除中烃和脱除水蒸气等。
其中,脱除硫化物通常采用吸收剂法,通过与氢气反应将硫化氢转化为硫,从而降低硫化物的含量。
1.2 空气压缩合成氨的制备过程中需要大量的氢气和氮气。
氮气可通过空气经过压缩和分离获得。
这一步骤主要是将空气压缩至一定压力,然后通过分离装置将其中的氧气和氩气分离出来,得到纯净的氮气。
1.3 氢气制备氢气是合成氨的重要原料,可通过水蒸气重整和空气分离等方法制备。
水蒸气重整是指将甲烷与水蒸气反应产生氢气和一氧化碳的过程。
空气分离则是利用空气中氧气和氮气的不同沸点进行分离,得到纯净的氢气。
2. 氨合成2.1 催化剂制备氨的合成反应需要使用特定的催化剂,最常用的催化剂是铁-铝催化剂。
铁-铝催化剂制备方法主要包括混合沉积法和干法混合沉积法等。
混合沉积法是将铁盐和铝盐混合溶解后沉积得到催化剂,干法混合沉积法则是将铁盐和铝盐直接混合后进行焙烧得到。
2.2 反应器设计合成氨的反应器可采用固定床反应器或流化床反应器。
固定床反应器是将催化剂填充在反应器中,通过氢气和氮气的通入进行反应。
流化床反应器则是将催化剂悬浮在气流中,通过流化床底部的分配装置和氢气、氮气的通入进行反应。
2.3 反应条件合成氨的合成反应需要在一定的温度、压力和催化剂的存在下进行。
通常情况下,合成氨反应的温度约为350-450°C,压力约为200-300atm。
此外,还需要在反应器中加入适量的惰性气体(如氦气)以稀释氢气和氮气,以减少反应的热量和危险性。
2.4 反应过程合成氨的合成反应是一个多步骤的复杂过程。
氨的合成工艺

• 3.催化剂的中毒
催化剂的催化能力一般称为催化活性。有人认为: 由于催化剂在反应前后的化学性质和质量不变, 一旦制成一批催化剂之后,便可以永远使用下去。 实际上许多催化剂在使用过程中,其活性从小到 大,逐渐达到正常水平,这就是催化剂的成熟期。 接着,催化剂活性在一段时间里保持稳定,然后 再下降,一直到衰老而不能再使用。活性保持稳 定的时间即为催化剂的寿命,其长短因催化剂的 制备方法和使用条件而异。
• 国际上有关的研究成果认为,温和条件下 的固些过渡金属的有机 络合物去络合N2,使它的化学键削弱;② 还原过程。它是用化学还原剂或其他还原 方法输送电子给被络合的N2,来拆开N2中 的N—N键;③加氢过程。它是提供H+来和 负价的N结合,生成NH3。
• 催化剂在稳定活性期间,往往因接触少量的杂质而使活性 明显下降甚至被破坏,这种现象称为催化剂的中毒。一般 认为是由于催化剂表面的活性中心被杂质占据而引起中毒。 中毒分为暂时性中毒和永久性中毒两种。例如,对于合成 氨反应中的铁催化剂,O2、CO、CO2和水蒸气等都能使 催化剂中毒。但利用纯净的氢、氮混合气体通过中毒的催 化剂时,催化剂的活性又能恢复,因此这种中毒是暂时性 中毒。相反,含P、S、As的化合物则可使铁催化剂永久 性中毒。催化剂中毒后,往往完全失去活性,这时即使再 用纯净的氢、氮混合气体处理,活性也很难恢复。催化剂 中毒会严重影响生产的正常进行。工业上为了防止催化剂 中毒,要把反应物原料加以净化,以除去毒物,这样就要 增加设备,提高成本。因此,研制具有较强抗毒能力的新 型催化剂,是一个重要的课题。
• 一般采用溶液吸收法脱除CO2。根据吸收剂性能
的不同,可分为两大类。一类是物理吸收法,如 低温甲醇洗法(Rectisol),聚乙二醇二甲醚法 (Selexol),碳酸丙烯酯法。一类是化学吸收法, 如热钾碱法,低热耗本菲尔法,活化MDEA法, MEA法等。 4 ③ 气体精制过程
合成氨的工艺流程

工艺流程 1.合成氨的工艺流程(1)原料气制备将煤和天然气等原料制成含氢和氮的粗原料气。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;渣油可采用非催化部分氧化的方法获得合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
(2)净化对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
①一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2OH→2+CO2 =-41.2kJ/mol 0298HΔ由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO 含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
②脱硫脱碳过程各种原料制取的粗原料气,都含有一些硫和碳的氧化物,为了防止合成氨生产过程催化剂的中毒,必须在氨合成工序前加以脱除,以天然气为原料的蒸汽转化法,第一道工序是脱硫,用以保护转化催化剂,以重油和煤为原料的部分氧化法,根据一氧化碳变换是否采用耐硫的催化剂而确定脱硫的位置。
工业脱硫方法种类很多,通常是采用物理或化学吸收的方法,常用的有低温甲醇洗法(Rectisol)、聚乙二醇二甲醚法(Selexol)等。
粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量最多。
CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。
因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。
根据吸收剂性能的不同,可分为两大类。
一类是物理吸收法,如低温甲醇洗法(Rectisol),聚乙二醇二甲醚法(Selexol),碳酸丙烯酯法。
以天然气为原料的合成氨工艺

以天然气为原料的合成氨工艺天然气,这个大自然的馈赠,不仅可以供暖供燃料,还可以变身为合成氨的原料!是不是听起来就很神奇!合成氨工艺,就是利用天然气中的氮气和氢气,通过一系列反应,合成出氨气。
下面就让我来为你揭开这个神秘的面纱吧!1. 天然气中的氮气和氢气是合成氨的最佳小伙伴。
氮气大概占据天然气的四分之三,而氢气则是剩下的一部分。
所以,这两个小伙伴一旦相遇,就能发生化学反应啦!而这个反应可不是一蹴而就的,是需要一个叫做催化剂的帮手来加快速度的。
就好像是一对行动派的情侣,催化剂就像是搭档一样,相互配合,促进反应进行。
1.1 催化剂,就像一把魔法杖一样,能够让反应变得更加神速。
它既不是消耗品,也不是反应物,而是一个神秘的存在,可以让氮气和氢气之间的化学键得到打破,从而合成出氨气。
在这个过程中,催化剂扮演着至关重要的角色,就好比是情侣之间的红线,让两个人的关系更加紧密。
1.2 当氮气和氢气经过催化剂的帮助,发生了神奇的变化,合成氨气就产生了。
这个过程就像是一场化学魔法表演,让人不禁惊叹大自然的神奇!合成氨气被广泛应用于农业领域,作为化肥的原料,可以帮助作物生长,增加产量。
简直就是大自然送给农民们的一份珍贵礼物。
2. 合成氨的工艺过程看似简单,但其中却蕴含着无限的奥秘。
从天然气中提取氮气和氢气,再经过催化剂的引导,最终合成出氨气,这一切都需要精密的控制和操作。
就好比是做一道菜,需要掌握火候和调味。
2.1 每一个生产合成氨的工厂,都如同一个巨大的烹饪工坊,工人们在其中如同厨师一般,精心烹饪着每一滴氨气的制作过程。
他们需要时刻监控反应的温度、压力和流速,确保反应能够顺利进行。
就好像是烹饪中的火候把握,一不小心就会让菜肴功亏一篑。
2.2 而合成氨工艺中最神奇的地方在于,它能够将天然气中的氮气和氢气充分利用,将看似废弃的资源转化为妙不可言的氨气。
这种工艺不仅可以减少资源的浪费,还可以为农业生产提供更多的支持。
简直就是把“废”变“宝”,让人感慨大自然的鬼斧神工!3. 合成氨工艺,就像是大自然的一场魔术表演,让人目瞪口呆。
合成氨工艺

合成氨工艺————————————————————————————————作者:————————————————————————————————日期:合成氨工艺流程(1)原料气制备将煤和天然气等原料制成含氢和氮的粗原料气。
对于固体原料煤和焦炭,通常采用气化的方法制取合成气;渣油可采用非催化部分氧化的方法获得合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
(2)净化对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
①一氧化碳变换过程在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。
合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。
变换反应如下:CO+H2OH→2+CO2 =-41.2kJ/mol 0298HΔ由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。
第一步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。
因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
②脱硫脱碳过程各种原料制取的粗原料气,都含有一些硫和碳的氧化物,为了防止合成氨生产过程催化剂的中毒,必须在氨合成工序前加以脱除,以天然气为原料的蒸汽转化法,第一道工序是脱硫,用以保护转化催化剂,以重油和煤为原料的部分氧化法,根据一氧化碳变换是否采用耐硫的催化剂而确定脱硫的位置。
工业脱硫方法种类很多,通常是采用物理或化学吸收的方法,常用的有低温甲醇洗法(Rectisol)、聚乙二醇二甲醚法(Selexol)等。
粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量最多。
CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。
因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。
天然气制合成氨工艺技术

天然气制合成氨工艺技术天然气制合成氨是一种重要的工业化学过程,它将天然气中的氨合成为氨气。
这一过程主要应用于肥料生产、合成纤维、涂料和医药等领域。
天然气制合成氨工艺技术主要包括气体净化、氨合成和气体分离三个步骤。
首先是气体净化。
天然气中含有一定的杂质,如二氧化碳、硫化物、水蒸气等,这些杂质会影响氨合成反应的效果。
因此,需要对天然气进行脱碳、脱硫和脱水处理。
脱碳通过吸收剂吸收二氧化碳,脱硫则使用吸收剂吸收硫化物,而脱水则通过冷凝和吸附等方法去除水蒸气。
接下来是氨合成反应。
氨合成反应是将水蒸气和氢气与合成气体(由天然气和空气混合得到)在催化剂的作用下反应生成氨气。
这个反应的催化剂通常是铁、钴或镍,也可以是一些复合催化剂。
合成气体在一定的温度和压力下通过催化剂之间的反应床进行氨合成反应。
反应过程中需要控制温度、压力和气体流量等参数,以提高反应效果和氨合成率。
最后是气体分离。
产生的气体混合物中除了含有合成氨和未反应的氧气、氮气和水蒸气外,还包含一些不利于以氨气为产品的成分,如甲烷、二氧化碳、氮气等。
因此,需要对气体进行分离和纯化,以使得最终得到的产品达到所需的纯度要求。
常用的气体分离方法有吸附分离、膜分离和冷却分离等。
分离后的氨气可以进一步被压缩、液化或制成氮酸铵等形式,以便于储存和运输。
天然气制合成氨工艺技术的发展和应用有助于提高氨制品的产量和质量,同时降低了能源消耗和环境污染。
目前,一些新型的催化剂和工艺技术正在被研究和应用,以进一步优化氨合成反应的效果并提高生产效率。
总之,天然气制合成氨工艺技术是一项重要的化学工程技术,它能够使得天然气资源得到充分利用,并满足人们对氨气的需求。
随着科技的进步,相信天然气制合成氨工艺技术将会继续发展壮大,为人们的生活和工业生产带来更多的便利和效益。
合成氨介绍

合成氨指由氮和氢在高温高压和催化剂存在下直接合成的氨。
世界上的氨除少量从焦炉气中回收副产外,绝大部分是合成的氨。
合成氨主要用作化肥、冷冻剂和化工原料。
生产方法生产合成氨的主要原料有天然气、石脑油、重质油和煤(或焦炭)等。
①天然气制氨。
天然气先经脱硫,然后通过二次转化,再分别经过一氧化碳变换、二氧化碳脱除等工序,得到的氮氢混合气,其中尚含有一氧化碳和二氧化碳约0.1%~0.3%(体积),经甲烷化作用除去后,制得氢氮摩尔比为3的纯净气,经压缩机压缩而进入氨合成回路,制得产品氨。
以石脑油为原料的合成氨生产流程与此流程相似。
②重质油制氨。
重质油包括各种深度加工所得的渣油,可用部分氧化法制得合成氨原料气,生产过程比天然气蒸气转化法简单,但需要有空气分离装置。
空气分离装置制得的氧用于重质油气化,氮作为氨合成原料外,液态氮还用作脱除一氧化碳、甲烷及氩的洗涤剂。
③煤(焦炭)制氨。
随着石油化工和天然气化工的发展,以煤(焦炭)为原料制取氨的方式在世界上已很少采用。
用途氨主要用于制造氮肥和复合肥料,氨作为工业原料和氨化饲料,用量约占世界产量的12%。
硝酸、各种含氮的无机盐及有机中间体、磺胺药、聚氨酯、聚酰胺纤维和丁腈橡胶等都需直接以氨为原料。
液氨常用作制冷剂。
贮运商品氨中有一部分是以液态由制造厂运往外地。
此外,为保证制造厂内合成氨和氨加工车间之间的供需平衡,防止因短期事故而停产,需设置液氨库。
液氨库根据容量大小不同,有不冷冻、半冷冻和全冷冻三种类型。
液氨的运输方式有海运、驳船运、管道运、槽车运、卡车运合成氨是以碳氨为主要原料, 我司可承包的合成氨生成成套项目, 规模有4×104 吨/年, 6×104 吨/年, 10×104 吨/年, 30×104 吨/年, 其产品质量符合中国国家标准.合成氨的主要工艺过程有哪些?各过程的作用是什么?第一步是原料气的制备。
采用合成法生产氨,首先必须制备含氢和氮的原料气。
以天然气为原料合成氨工艺模板

以天然气为原料合成氨工艺模板1目录1 引言....................................................................................错误!未定义书签。
1.1 氨的性质 ..................................................................错误!未定义书签。
1.2 氨的用途 ..................................................................错误!未定义书签。
1.3 合成氨的发展历史 ..................................................错误!未定义书签。
1.3.1 氨气的发现 .....................................................错误!未定义书签。
1.3.2 合成氨的发现及其发展 .................................错误!未定义书签。
1.3.3 国外合成氨工业发展 .....................................错误!未定义书签。
1.3.4 国内合成氨工业发展 .....................................错误!未定义书签。
1.3.5 国内合成氨工业的发展趋势 .........................错误!未定义书签。
1.4 合成氨工段设计主要参数计算的主要内容..........错误!未定义书签。
2 工艺计算............................................................................错误!未定义书签。
2.1 生产流程简述 ..........................................................错误!未定义书签。
国内典型合成氨装置工艺介绍
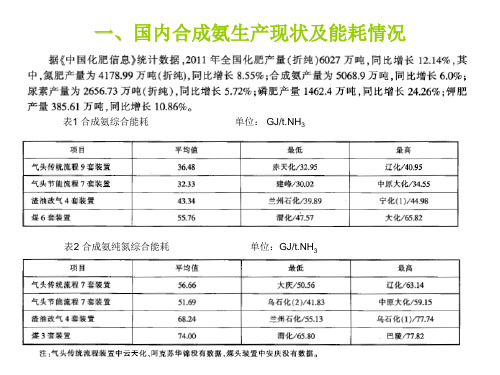
103-J改转子;并联101-JA; 净化使用ACT-1活化剂,更换规整填料;
司,成达
合成回路改塔后分氨、增加小合成塔1105-D工程公司 Nhomakorabea10
五大机组电子调 五大机组电子调速器改造,采用ITCC系统进行控制 速器改造
康吉森公 司
投用时 间
1984.4 1986.2
1990.8 1988.9
1993.9 1997.7 2002.7 2005.1 2008.8
每排42根转化管的底部都同一根集气管相连,后者靠近 一段炉的底部,每根集气管的中部有一上升管,这九根上升 管又把气体引到炉顶上一根装有水夹套的输气管线,再由此 把气体送至二段转化炉103-D的入口。一段炉的热量是由 200个顶部烧嘴供应的。部分转化后的混合气含有12.91%的 甲烷。
二段转化炉103-D所需工艺空气由蒸汽透平压缩机101-J (提供约65%的空气量)和电动压缩机101-JA(约35%)提 供。定量中压蒸汽与工艺空气混合,经过一段炉对流段空气/ 蒸汽混合气预热盘管被加热到599℃,经过二段炉的喷嘴与 来自一段炉的工艺气在燃烧室进行混合燃烧(空气中的氧与 一段转化气中的氢燃烧),接着在内衬耐火材料的圆筒式反 应炉内通过镍触媒进一步转化残余甲烷。二段转化炉出口气 含有0.38%的甲烷,温度约为1000℃,进入第一废热锅炉 101-CA/CB、第二废热锅炉102-C,被来自101-F的锅炉水 继续冷却,冷却后的转化气温度降低到371℃。
合成氨工艺的5个过程:
1、油田气脱硫:
R-SH+H2=RH+H2S H2S+ZnO=H2O(汽)+ZnS 2、转化:
CH4+H20(汽)=CO+3H2 CH4+2H2O(汽)=CO2+4H2 3、变换:
氨的合成工艺

钌系催化剂和深冷净化技术等,是新型的 合成氨节能工艺。
• 4.我国合成氨工业的发展情况 解放前我国只有两家规模不大的合成氨厂,解放 后合成氨工业有了迅速发展。1949年全国氮肥产 量仅0.6万吨,而1982年达到1021.9万吨,成为 世界上产量最高的国家之一。 近几年来,我国引进了一批年产30万吨氮肥的大 型化肥厂设备。我国自行设计和建造的上海吴泾 化工厂也是年产30万吨氮肥的大型化肥厂。这些 化肥厂以天然气、石油、炼油气等为原料,生产 中能量损耗低、产量高,技术和设备都很先进。
• 5.化学模拟生物固氮的研究 目前,化学模拟生物固氮的重要研究课题之一, 是固氮酶活性中心结构的研究。固氮酶由铁蛋白 和钼铁蛋白这两种含过渡金属的蛋白质组合而成。 铁蛋白主要起着电子传递输送的作用,而含二个 钼原子和二三十个铁和硫原子的钼铁蛋白是络合 N2或其他反应物(底物)分子,并进行反应的活 性中心所在之处。关于活性中心的结构有多种看 法,目前尚无定论。从各种底物结合物活化和还 原加氢试验来看,含双钼核的活性中心较为合理。 我国有两个研究组于1973—1974年间,不约而同 地提出了含钼铁的三核、四核活性中心模型,能 较好地解释固氮酶的一系列性能,但其结构细节 还有待根据新的实验结果精确化。
氨的合成工艺
• 氨是重要的无机化工产品之一,在国民经济中占 有重要地位。除液氨可直接作为肥料外,农业上 使用的氮肥,例如尿素、硝酸铵、磷酸铵、氯化 铵以及各种含氮复合肥,都是以氨为原料的。合 成氨是大宗化工产品之一,世界每年合成氨产量 已达到1亿吨以上,其中约有80%的氨用来生产化 学肥料,20%作为其它化工产品的原料。 德国化学家哈伯1909年提出了工业氨合成方法, 即“循环法”,这是目前工业普遍采用的直接合 成法。反应过程中为解决氢气和氮气合成转化率 低的问题,将氨产品从合成反应后的气体中分离 出来,未反应气和新鲜氢氮气混合重新参与合成 反应。合成氨反应式如下: N2+3H2≈2NH3
以天然气合成氨-催化导论作业

以天然气为原料合成氨摘要:合成氨工业诞生于本世纪初,其规模不断向大型化方向发展。
生产合成氨的主要原料有天然气、石脑油、重质油和煤(或焦炭)等。
以天然气为原料,天然气的主要成分为甲烷,约占90%以上,在铁猛脱硫剂和氧化锌脱硫剂的作用下,将天然气中的无机硫和有机硫脱除到0.5ppm以下,配入一定量的水蒸气和空气分别在一段转化触煤和一定温度下将甲烷转化为氢气,制取氨合成所需的氢气和氮气。
合成氨反应式如下:N2+3H2=2NH3关键字:合成氨工艺流程天然气原料气1. 概念氨是一种无色气体,有强烈的刺激气味。
极易溶于水,常温常压下1体积水可溶解700倍体积氨。
氨对地球上的生物相当重要,它是所有食物和肥料的重要成分。
氨也是所有药物直接或间接的组成。
氨有很广泛的用途,同时它还具有腐蚀性等危险性质。
由于氨有广泛的用途,氨是世界上产量最多的无机化合物之一,多于八成的氨被用于制作化肥。
由于氨可以提供孤对电子,所以它也是一种路易斯碱。
20世纪初,工业上开发了氰化法和合成氨法生产氨,前者因能耗远大于后者而被淘汰。
目前,世界上的氨,除从焦炉气中回收一些外,绝大部分是在高压,高温和催化剂存在下由氮气和氢气合成制得。
氮气主要来源于空气;氢气主要来源于含氢和一氧化碳的合成气。
由氮气和氢气组成的混合气即为合成氨原料气。
从燃料化工来的原料气含有硫化合物和碳的氧化物,它们对于合成氨的催化剂是有毒物质,在氨合成前要经过净化处理。
德国化学家哈伯1909年提出了工业氨合成方法,即“循环法”,这是目前工业普遍采用的直接合成法。
反应过程中为解决氢气和氮气合成转化率低的问题,将氨产品从合成反应后的气体中分离出来,未反应气和新鲜氢氮气混合重新参与合成反应。
合成氨反应式如下:N2+3H2=2NH3合成氨的原料可分为固体原料,液体原料和气体原料。
经过不断地发展,合成氨技术趋于成熟,形成了以有特色的工艺流程。
其工艺流程大都分为三步:即原料气制备过程,净化过程以及氨合成过程。
以天然气为原料合成氨工艺.

The production of liquid ammonia, liquid ammonia production capacity of 100000 tons per year, and Compared with the traditional process this process have the characteristics of energy-saving and low consumption. To design a heat exchanger between the waste heat boilers and water coolers, recycling the residual heat in the waste heat boiler gas through the heat exchanger and at the same time as the feed gas preheating. The other also further reduces the synthesis gas for subsequent condensation temperature,favorable for the subsequent condensation and indirect savings in the consumption of heat and cold.
设计参数
年产10万吨合成氨的合成工段工艺设计(以天然气为原料)
产量:10万吨/年,液氨
合成塔入口惰性气体含量:15%
合成塔进口氨浓度:2.5%
合成塔出口氨浓度:13.2%
合成塔操作压力:30MPa
天然气合成氨工艺流程

天然气合成氨工艺流程氨是一种重要的化工原料,广泛用于制造化肥、合成纤维和其他化工产品。
天然气合成氨是一种重要的工艺流程,通过利用天然气中的氮气和氢气来合成氨气。
下面将介绍天然气合成氨的工艺流程。
1. 天然气净化。
天然气中含有少量的硫化氢、二氧化碳和水蒸气等杂质,需要进行净化处理。
首先,天然气通过除硫装置,将硫化氢去除,然后通过脱水装置,去除水蒸气。
最后,通过脱碳装置,去除二氧化碳。
经过净化处理后的天然气成分符合合成氨的要求。
2. 空气分离。
空气中含有大量的氮气,通过空气分离装置,可以将氮气和氧气分离。
通常采用的是低温分馏法,将空气冷却至液态,然后通过分馏将氮气和氧气分离。
得到纯净的氮气用于后续的合成氨反应。
3. 合成氨反应。
合成氨反应是将氮气和氢气在催化剂的作用下进行反应,生成氨气。
通常采用的是哈贝-波希反应,反应条件是在高压(100-250atm)和高温(400-500℃)下进行。
催化剂通常采用铁或钼化合物。
反应过程中,氮气和氢气按一定的摩尔比混合,通过催化剂的作用生成氨气。
4. 氨气提纯。
合成氨反应生成的氨气中还含有少量的氮气、氢气和甲烷等杂质,需要进行提纯处理。
首先经过冷凝器,将氨气冷却成液态,然后通过分馏将杂质分离出去,得到纯净的氨气。
5. 氨气压缩。
提纯后的氨气需要进行压缩,以便于储存和运输。
通过氨气压缩机,将氨气压缩至一定的压力,通常为10-20MPa。
6. 氨气储存和运输。
压缩后的氨气可以储存在氨气储罐中,也可以通过管道或罐车进行运输。
在储存和运输过程中需要注意防止氨气泄漏和避免与氧化剂接触,以防止火灾和爆炸事故的发生。
综上所述,天然气合成氨工艺流程包括天然气净化、空气分离、合成氨反应、氨气提纯、氨气压缩和氨气储存和运输等步骤。
通过这些步骤,可以高效地将天然气转化为合成氨,为化肥和化工产品的生产提供重要的原料。
年产30万吨合成氨工艺设计

毕业设计题目名称:年产30万吨合成氨转变工序设计系别:化学工程系专业:应用化学班级: 06101学生:韩民瑞学号: 5533110119 指导教师(职称):王锐薛慧峰(教授)摘要氨是重要的基础化工产品之一,在国民经济中占有重要地位。
合成氨生产经过多年的发展,现已发展成为一种成熟的化工生产工艺。
本设计是以天然气为原料年产三十万吨合成氨转变工序的设计。
近年来合成氨工业发展很快,大型化、低能耗、清洁生产均是合成氨设备发展的主流,技术改进主要方向是开发性能更好的催化剂、降低氨合成压力、开发新的原料气净化方法、降低燃料消耗、回收和合理利用低位热能等方面上。
设计采用的工艺流程简介:天然气经过脱硫压缩进入一段转化炉,把CH4和烃类转化成H2,再经过二段炉进一步转化后换热进入高变炉,在催化剂作用下大部分CO和水蒸气反应获H2和CO2,再经过低变炉使CO降到合格水平,去甲烷化工序。
本设计综述部分主要阐述了国内外合成氨工业的现状及发展趋势以及工艺流程、参数的确定和选择,论述了建厂的选址;介绍了氨变换工序的各种流程并确定本设计高-低变串联的流程。
工艺计算部分主要包括转化段和变换段的物料衡算、热量衡算、平衡温距及空速计算。
设备计算部分主要是高变炉催化剂用量的具体计算,并根据设计任务做了转化和变换工序带控制点的工艺流程图。
本设计的优点在于选择较为良好的厂址和原料路线,确定良好的工艺条件、合理的催化剂和能源综合利用。
另外,就是尽量减少设备投资费用。
关键字:合成氨;天然气;转化;变换;目录摘要 (I)目录 (II)1 综述........................................................................................................................................ - 1 -1.1 氨的性质、用途及重要性.......................................................................................... - 1 -1.1.1 氨的性质.......................................................................................................... - 1 -1.1.2 氨的用途及在国民生产中的作用.................................................................. - 1 -1.2 合成氨生产技术的发展.............................................................................................. - 2 -1.2.1世界合成氨技术的发展................................................................................... - 2 -1.2.2中国合成氨工业的发展概况........................................................................... - 5 -1.3合成氨转变工序的工艺原理...................................................................................... - 6 -1.3.1 合成氨的典型工艺流程介绍.......................................................................... - 6 -1.3.2 合成氨转化工序的工艺原理.......................................................................... - 8 -1.3.3合成氨变换工序的工艺原理........................................................................... - 8 -1.4 设计方案的确定......................................................................................................... - 9 -1.4.1 原料的选择...................................................................................................... - 9 -1.4.2 工艺流程的选择............................................................................................ - 10 -1.4.3 工艺参数的确定............................................................................................ - 10 -1.4.4 工厂的选址.................................................................................................... - 11 -2 设计工艺计算...................................................................................................................... - 13 -2.1 转化段物料衡算........................................................................................................ - 13 -2.1.1 一段转化炉的物料衡算................................................................................ - 14 -2.1.2 二段转化炉的物料衡算................................................................................ - 17 -2.2 转化段热量衡算........................................................................................................ - 20 -2.2.1 一段炉辐射段热量衡算................................................................................ - 20 -2.2.2 二段炉的热量衡算........................................................................................ - 27 -2.2.3 换热器101-C、102-C的热量衡算.............................................................. - 28 -2.3 变换段的衡算........................................................................................................... - 30 -2.3.1 高温变换炉的衡算........................................................................................ - 30 -2.3.2 低温变换炉的衡算........................................................................................ - 32 -2.4 换热器103-C及换热器104-C的热负荷计算........................................................ - 35 -2.4.1 换热器103-C热负荷.................................................................................... - 35 -2.4.2 换热器104-C热负荷.................................................................................... - 35 -2.5 设备工艺计算........................................................................................................... - 36 -参考文献.................................................................................................................................. - 40 -致谢.......................................................................................................................................... - 41 -附录.......................................................................................................................................... - 41 -1 综述1.1 氨的性质、用途及重要性1.1.1 氨的性质氨分子式为NH,在标准状态下是无色气体,比空气轻,具有特殊的刺激性臭味。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
目录1 引言 (1)1.1 氨的性质 (1)1.2 氨的用途 (2)1.3 合成氨的发展历史 (2)1.3.1 氨气的发现 (2)1.3.2 合成氨的发现及其发展 (2)1.3.3 国外合成氨工业发展 (3)1.3.4 国合成氨工业发展 (3)1.3.5 国合成氨工业的发展趋势 (4)1.4 合成氨工段设计主要参数计算的主要容 (5)2 工艺计算 (6)2.1 生产流程简述 (6)2.2 原始条件 (6)2.3 物料衡算 (7)2.3.1 合成塔物料衡算 (8)2.3.2 氨分离器气液平衡计算 (9)2.3.3 冷交换器气、液平衡计算 (11)2.3.4 液氨贮槽气、液平衡计算 (11)2.3.5 液氨贮槽物料计算 (13)2.3.6 合成系统物料计算 (14)2.3.7 进出合成塔物料计算 (15)2.3.8 进出水冷器物料计算 (16)2.3.9 进出氨分离器物料计算 (16)2.3.10 冷交换器物料计算 (17)2.3.11 氨冷器物料计算: (18)2.3.12 冷交换器物料衡算 (20)2.3.13 液氨贮槽物料计算 (21)2.3.14 物料计算结果汇总 (21)2.4 热量核算 (22)2.4.1 交换器热量核算 (22)2.4.2 氨冷器热量核算 (25)2.4.3 循环机热量核算 (27)2.4.4 合成塔热量核算 (28)2.4.5 废热锅炉热量核算 (31)2.4.6 热交换器热量核算 (32)2.4.7 水冷器热量核算 (33)2.4.8 氨分离器热量核算 (34)3 氨合成过程中的绿色化学化工 (35)3.1 绿色化学化工的基本概念 (35)3.2 合成氨工段的原子经济性 (35)3.3 合成氨工段的热能综合利用 (35)3.4 合成氨工段的“三废”处理 (36)4 设备选型 (37)4.1 合成塔催化剂层设计 (37)4.2 换热器: (42)4.3 废热锅炉设备工艺计算 (43)4.3.1 计算条件 (43)4.3.2 官给热系数α计算 (43)计算 (45)4.3.3 管给热系数αi4.3.4 总传热系数K 计算 (46)计算 (46)4.3.5 平均传热温差Δtm4.3.6 传热面积 (46)4.4 水冷器设备工艺计算: (47)4.4.1 计算条件 (47)4.4.2 管给热系数的计算 (47)4.4.3 管外给热系数 (48)4.4.4 传热温差 (49)4.4.5 传热总系数K (49)4.4.6 传热面积 (49)4.5 冷交换器设备工艺计算 (49)4.5.1 计算条件 (49)4.5.2 管给热系数的计算 (50)4.5.3 管外给热系数 (52)4.5.4 总传热系数 (55)4.5.5 传热面积核算 (55)4.5.6 主要设备选型汇总表 (55)5 合成氨合成车间的安全生产 (57)5.1 合成氨车间的职业危害 (57)5.2 安全措施 (58)5.3 合成氨工序重大事故危险与防 (59)5.3.1 蒸汽锅炉的重大事故危险与防 (59)5.3.2 容器爆炸 (60)5.3.3 灼烫 (60)5.3.4 起重伤害 (60)参考文献 (62)致谢 (63)设计参数年产10万吨合成氨的合成工段工艺设计(以天然气为原料)产量:10万吨/年,液氨合成塔入口惰性气体含量:15%合成塔进口氨浓度:2.5%合成塔出口氨浓度:13.2%合成塔操作压力:30MPa新鲜补充气:N2 24%;H2 75%;CH4 0.3%;Ar 0.7%精炼气温度:35℃水冷器出口气体温度:35℃循环机进出口压差:1.47Mpa年工作日:300d产品质量规格:氨含量(wt%)>=99%以天然气为原料年产10万吨合成氨厂合成工段的工艺设计设计说明书任务来源:本次设计按照化工系下达的设计任务书进行编制的,并且参照双联化工厂合成氨工段的现场生产而设计而成。
设计标准:按照国家相关化工安全生产标准和化工仪器设备设计标准设计设计原则:本设计的原则是以绿色化工为准则,低耗能、低成本、无污染的原则。
设计的主要容及特点:本工段生产液氨,生产能力为10万吨液氨/年,与传统的流程相比较具有节能低耗的特点。
在废热锅炉和水冷器之间设计一个热交换器,通过热交换器回收了废热锅炉出来的气体中剩余的热量并同时为原料气进行了预热,另外也进一步降低了合成气的温度,为对后续的冷凝工作有利,间接的节约了消耗的热量和冷量。
现将具体的设计容介绍如下:(1)循环机位置本工段循环机设置在氨分离系统后,合成塔之前,从而充分利用循环机压缩功,提高进合成塔温度,减少冷量消耗,降低氨冷器负荷,同时提高进塔压力,提高合成率,而进循环机的氨冷量较低,避免了塔后循环机流程容易带液氨而导致循环机泄漏。
(2)反应热回收的方式及利用热量的回收主要集中在合成塔处,这里涉及到废热锅炉的热量回收利用和合成塔塔外换热器如何科学设置的问题,废热锅炉的配置实际上是如何提高反应热的回收率和获得高品位热的问题,本次设计选择的是塔后换热器及后置锅炉的工艺路线,设置塔后换热器使废热锅炉出口气体与合成塔二进气体换热,充分提高合成塔二进温度,相应提高了合成塔二出温度,进废热锅炉的气体温度为365度,副产1.372兆帕的中压蒸汽,充分提高回收热量品位。
(3)采用“二进二出”合成流程全部冷气经合成塔的外围环隙后进入热交换器,可使合成塔塔体各点温度分布均匀,出口气体保持较低温度,确保合成塔长期安全稳定运行,与循环机来的冷气直接进入热交换器相比,使热交换器出口温度增大。
进入水冷的气体温度降低意味着合成余热回收率高和水冷器的负荷低。
(4)水冷器和氨冷器的设置水冷后直接进行分离液氨然后再进行冷交,水冷有利于降低后续氨冷的负荷,边冷却边分离液氨,即提高了液氨的分离效果,又避免了气液两相流的存在,通过设置氨冷器的冷凝充分解决了低压下,水冷后很少有氨冷凝下来的矛盾,达到了进一步冷却,保证合成塔入口氨含量的要求。
(5)新鲜气及放空点位置设置新鲜气的补充设置在冷交换气的二次入口,以便减少系统阻力,并通过氨冷器进一步洗脱微量二氧化碳和一氧化碳及氨基甲酸等杂质,有利于保护触媒、防止管道和设备堵塞。
放空点设置在冷交换器和氨分离器之间,氨分后有效气体浓度较低,惰性气体含量较高,有利于降低新鲜气单耗。
(6)冷交换器设备的使用分离器为外向型旋流板,上部换热器为列管换热器和下部氨分离器,将热气体在进入氨冷器前用冷气体进行冷却换热,以回收冷气体的冷冻量,使入氨冷器的热气体预冷却,从而节省冷冻量,同时分离经氨冷后含氨混和气中的液氨,化工公司发表与《小氮肥》杂志上的有关资料表明,该设备节能降耗显著。
(7)三废治理及环境保护①放空气弛放气送膜提氢回收系统,先用氨洗涤塔回收几乎全部氨,制成浓氨水,再回收大部分氨送入高压机压缩后制氨既可以避免氨气进入大气,与放空气作燃料相比又更合理经济。
②其他废水废渣集中处理达到国家排放标准后排放。
(8)生产制度:每年操作日300天,三班连续操作。
(9)结论本设计主要是对于合成氨的工艺流程的设计;其中包括合成氨各主要工段设备的物料衡算和热量核算包括:合成塔的物料衡算和热量衡算、氨冷器的物料衡算及热量核算、冷交换器的物料衡算和热量核算等;合成氨各主要设备的工艺计算和选型;合成氨车间的安全因素及防措施;工艺流程、车间中设备布置图以及氨合成塔、废热锅炉、水冷器三个主要设备的CAD图纸。
关键词:合成氨;物料衡算;热量核算;工艺设计Using natural gas as raw material with annual output of 100000 tons of synthetic ammonia plant of the section in process designDesign specificationThe source of the taskThis design is according to the chemical industry department issued the design task book prepared, and referring to Shijiazhuang joint chemical factory ammonia section on-site production and designed.Design standards:In accordance with the relevant national safety production standard and chemical equipment designDesign principles:The principle of design is based on the green chemical industry as a criterion, low energy consumption, low cost, no pollution principle.Design of the main contents and characteristics:The production of liquid ammonia, liquid ammonia production capacity of 100000 tons per year, and Compared with the traditional process this process have the characteristics of energy-saving and low consumption. To design a heat exchanger between the waste heat boilers and water coolers, recycling the residual heat in the waste heat boiler gas through the heat exchanger and at the same time as the feed gas preheating. The other also further reduces the synthesis gas for subsequent condensation temperature,favorable for the subsequent condensation and indirect savings in the consumption of heat and cold.The specific design and content are as follows:(1) circulation machine locationThis section cycle machine is arranged in the behind of the ammonia separation system, and before the synthetic tower, thus make full use of recycling machine compression work, raise the gas temperature of synthetic tower, reduce the cold consumption, reduce the ammonia cooler load, meanwhile increasing the inlet pressure of tower, improve the rate of synthesis and into the circulation machine ammonia cooling capacity is relatively low, avoiding the tower posterior circulation machine process with liquid ammonia and lead to circulating machine easy to leak.(2)The ways of reaction heat recovery and utilizationHeat recovery focuses on the synthetic tower, it involves in waste heat boiler heat recovery utilization and how scientific setting problem of heat exchanger of synthetic tower outside, waste heat boiler configuration is actually how to improve reaction heat recovery rateand obtain high grade heat problem. This design is the choice of the process route is that the heat exchanger in behind of the tower and post boiler. Set behind the tower heat exchanger made of waste heat boiler outlet gas and synthesis tower two into the gas heat exchanger,fully improve the synthetic tower two inlet gas temperature, increase the synthesis tower two outlet gas temperature.The temperature of the gas that is into the waste heat boiler is 365 degrees, and produce 1.372MPa steam pressure,so it improve recovery of heat grade.(3)The use of the "The two gas inlet two outlet " synthesis processAll air-conditioning into the heat exchanger after the peripheral annulus of the synthetic tower, the synthetic tower body at each point of a uniform temperature distribution, and export gas to maintain a lower temperature to ensure that the synthesis tower directly into the long-term safe and stable operation. Compared with the circulation machine to cold gas directly into the heat exchanger, the heat exchanger outlet temperature increase. Enter the water temperature of the gas to reduce means that there have a high of synthesis waste heat recovery rate and low load of water cooler.(4) Water cooler and ammonia cooler settingsAfter water-cooled ,the gas directly the separation of liquid ammonia then cold exchang, water-cooling is helpful to reduce the subsequent ammonia cooling load, Edge cooling and separation of liquid ammonia not only improve the liquid ammonia separation, but also to avoid the presence of gas-liquid two-phase flow. Through the setting of ammonia tanks condensation fully solved under low pressure after the water cooling few ammonia condensing the contradiction down, to further cooling, ensure that the content of ammonia synthesis tower entrance requirements.(5) The fresh gas and vent position settingThe supplementary of fresh gas set in the cold exchanger`s two entrance, so as to reduce the resistance of the system, and through the ammonia cooler further elution trace impurities such as carbon dioxide , carbon monoxide and amino acid and so on, beneficial to the protection of catalysts, and prevent piping and equipment jam. The setting of vent point located between the cold exchanger and ammonia separator. After the concentration of the gas effective ammonia points lower, inert gas content is higher, which helps reduce fresh gas consumption.(6) The use of cold heat exchanger equipmentSeparator for extroversion swirl plate, heat exchanger tube heat exchanger for upper and lower ammonia separator, hot gas into ammonia cooler for cold air cooling and heat exchange, to recover the freezing cold gas refrigeration, make the hot gas that into theammonia cooler cooling, which can save frozen volume, meanwhile separated the liquid ammonia after ammonia cooling ammonia containing gas mixture. Anhui chemical industry company in Huainan and Small Nitrogenous Fertilizer published on the magazine of relevant data show that the equipment is saving energy and reducing consumption is significant.(7) Waste management and environmental protection①Empty gas and purge gas film feeding hydrogen extraction recovery system, using ammonia washing tower recovery almost all ammonia, make concentrated ammonia, and recycling most ammonia then into high pressure machine compressed ammonia can avoid the ammonia gas into the atmosphere, and the discharge gas as fuel and more reasonable than ecommic.②The other wastewater reatment to focus on waste residue after national emission standard emissions.(8) Te production systemAnnual operating on the 300 days and three consecutive operations.(9) ConclusionThis design is mainly to the synthetic ammonia processing flow design; it includes synthetic ammonia process flow design, the material balance and heat calculation of synthesis tower, ammonia cooler calculation and cold exchanger, the process calculation and equipment selection of the major equipments of ammonia synthesis, and ammonia synthesis plant safety factors and preventive measure. According to the results, five CAD drawings on process, workshop equipment layout and ammonia synthesis tower, waste heat boiler, water cooler are attached in the article.Key words: Ammonia synthesis; material balance; thermal calculation; process design1引言氮是植物营养的重要成分之一,大多数的植物不能直接吸收存在于空气中的游离氮,只有当氮与其他元素化合以后,才能被植物吸收利用。
