植株全钾的测定火焰光度法DB37T1626-2010
植株氮磷钾测定

植物体内全氮、磷、钾的测定一、实验原理作物体中的氮、磷、钾通过硫酸和H2O2消化,使有机氮化物转化成铵态氮,各种形态磷化物转化成磷酸,N、P、K均转变成可测的离子态(氮转化为NH4+,磷转化为H3PO4,钾为K+)。
然后采用相应的方法分别测定。
磷的测定原理(钒钼黄比色法):在酸性条件下,溶液中的磷酸根与偏钒酸盐和钼酸盐作用形成黄色的钒钼酸盐。
黄色深浅与溶液中磷浓度呈正比。
此法要求酸度0.04—1.6N(以0.5—1.0N最好);测磷浓度范围0—20mg/kg,比色波长460—490nm,磷浓度低时选用较短的波长,反之可选较长的波长。
钾的测定原理(火焰光度法):含钾溶液雾化后与可燃气体(如:汽化的汽油等)混合燃烧,其中的钾离子(基态)接受能量后,外层电子发生能级跃迁,呈激发态,由激发态变成基态过程中发射出特定波长的光线(称特征谱线)。
单色器或滤光片将其分离出来,由光电池或光电管将特征谱线具有的光能转变为电流。
用检流计测出光电流的强度。
光电流大小与溶液中钾的浓度呈正比,通过与标准溶液光电流强度的比较求出待测液中钾的浓度。
二、仪器与试剂仪器:分析天平(0.0001)、凯氏定氮仪、分光光度计、火焰光度计、消煮管、容量瓶(50ml)移液管(5、10、20ml)消煮及定氮试剂:1.浓硫酸2.30%H2O 23. 10mol/L NaOH:称400.0gNaOH溶解于1L蒸馏水中4. 显色剂:称0.099g溴甲酚绿和0.066g甲基红,溶于95%乙醇且定容至100ml5. 2%硼酸:称样品20.0gH3BO2溶于1L蒸馏水中6. 硼酸指示剂:取显色剂20 ml与1L2%硼酸溶液混合均匀7.0.02N H2SO4 (0.01 mol/L)标准溶液:量取浓H2SO42.83ml定容至5 L8. 0.01N H2SO4 :将0.02N H2SO4稀释1倍(7.8合并: 1.413ml定容到5L)测P、K试剂:1.钒钼酸试剂:25.0克钼酸铵〔(NH4)2Mo7O2• 4H2O〕溶于400ml水中,另取1.25克偏钒酸铵(NH4VO3)溶于300ml沸水中,冷却后加入250ml浓HNO3,冷却后,将钼酸铵溶液慢慢地混入偏钒酸铵溶液中,边混边搅拌,用水稀释至1升。
植物全氮磷钾的测定1

植物全氮磷钾的测定1植物氮、磷、钾全量分析植物中氮、磷、钾测定包括待测液制备和氮、磷、钾定量2大步骤。
1植物全氮、磷、钾含量测定—待测液制备(H2SO4+H2O2消煮法)1.1适用范围:本方法不包括硝态氮的植物全氮测定,适合于含硝态氮低的植物样品的测定。
1.2方法提要植物中的氮、磷大多数以有机态存在,钾以离子态存在。
样品经浓H2SO4和氧化剂H2O2消煮,有机物被氧化分解,有机氮和磷转化成铵盐和磷酸盐,钾也全部释出。
消煮液经定容后,可用于氮、磷、钾等元素的定量。
采用H2O2为加速消煮的氧化剂,不仅操作手续简单快速,对氮、磷、钾的定量没有于扰,而且具有能满足一般生产和科研工作所要求的准确度。
但要注意遵照操作规程的要求操作,防止有机氮被氧化成N2气或氮的氧化物而损失。
1.3试剂1.3.1硫酸(化学钝,比重1.84);+1.3.2 30%H2O2 (分析纯)。
1.4主要仪器设备1.4.1消煮炉1.5 操作步骤称取植物样品(0.5mm)0.3 g ~0.5g(称准至0.0002g)装入100mL开氏瓶或消煮管的底部,加浓H2SO4 5mL,摇匀,放置过夜。
第二天在电炉或消煮炉上先小火加热,待H2SO4发白烟后再升高温度,当溶液呈均匀的棕黑色时取下。
稍冷后加10滴H2O2,再加热至微沸,消煮约7~10min,稍冷后重复加H2O2,再消煮。
如此重复数次,每次添加的H2O2应逐次减少,消煮至溶液呈无色或清亮后,再加热约10min,除去剩余的H2O2。
取下冷却。
用水将消煮液无损地转移入100mL容量瓶中,冷却至室温后定容(V1)。
用无磷钾的干滤纸过滤,或放置澄清后吸取清液测定氮、磷、钾。
每批消煮的同时,进行空白试验,以校正试剂和方法的误差。
1.6注意事项1.6.1所用的H2O2应不含氮和磷。
H2O2在保存中可能自动分解,加热和光照能促使其分解,故应保存于阴凉处。
在H2O2中加入少量H2SO4酸化,可防止H2O2分解。
植物全氮磷钾的测定1

植物全氮磷钾的测定1植物氮、磷、钾全量分析植物中氮、磷、钾测定包括待测液制备和氮、磷、钾定量2大步骤。
1植物全氮、磷、钾含量测定—待测液制备(H2SO4+H2O2消煮法)1.1适用范围:本方法不包括硝态氮的植物全氮测定,适合于含硝态氮低的植物样品的测定。
1.2方法提要植物中的氮、磷大多数以有机态存在,钾以离子态存在。
样品经浓H2SO4和氧化剂H2O2消煮,有机物被氧化分解,有机氮和磷转化成铵盐和磷酸盐,钾也全部释出。
消煮液经定容后,可用于氮、磷、钾等元素的定量。
采用H2O2为加速消煮的氧化剂,不仅操作手续简单快速,对氮、磷、钾的定量没有于扰,而且具有能满足一般生产和科研工作所要求的准确度。
但要注意遵照操作规程的要求操作,防止有机氮被氧化成N2气或氮的氧化物而损失。
1.3试剂1.3.1硫酸(化学钝,比重1.84);+1.3.2 30%H2O2 (分析纯)。
1.4主要仪器设备1.4.1消煮炉1.5 操作步骤称取植物样品(0.5mm)0.3 g ~0.5g(称准至0.0002g)装入100mL开氏瓶或消煮管的底部,加浓H2SO4 5mL,摇匀,放置过夜。
第二天在电炉或消煮炉上先小火加热,待H2SO4发白烟后再升高温度,当溶液呈均匀的棕黑色时取下。
稍冷后加10滴H2O2,再加热至微沸,消煮约7~10min,稍冷后重复加H2O2,再消煮。
如此重复数次,每次添加的H2O2应逐次减少,消煮至溶液呈无色或清亮后,再加热约10min,除去剩余的H2O2。
取下冷却。
用水将消煮液无损地转移入100mL容量瓶中,冷却至室温后定容(V1)。
用无磷钾的干滤纸过滤,或放置澄清后吸取清液测定氮、磷、钾。
每批消煮的同时,进行空白试验,以校正试剂和方法的误差。
1.6注意事项1.6.1所用的H2O2应不含氮和磷。
H2O2在保存中可能自动分解,加热和光照能促使其分解,故应保存于阴凉处。
在H2O2中加入少量H2SO4酸化,可防止H2O2分解。
微波消解-火焰光度法测定植物中全钾
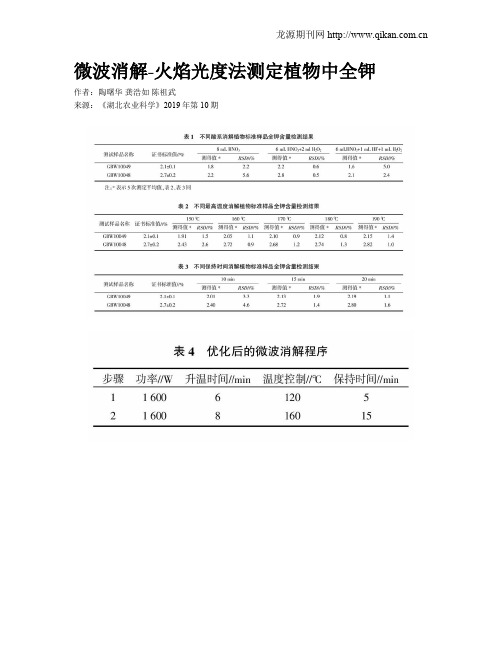
微波消解-火焰光度法测定植物中全钾作者:陶曙华龚浩如陈祖武来源:《湖北农业科学》2019年第10期摘要:通过优化微波消解用酸种类、最高温度及保持时间等条件,建立微波消解-火焰光度计测定植物中全钾的新方法。
结果表明,采用6 mL HNO3+2 mL H2O2酸系,微波消解最高温度160 ℃,保持时间15 min的优化消解方法,测定的检出限0.002 mg/g;测定两种植物标准物质的全钾含量均在其证书标准值范围内;测定水稻植株样品的全钾含量加标回收率97.5%~103.0%,相对标准偏差0.63%~2.27%。
该方法适用于植物不同部位全钾的测定,操作简便安全,结果准确可靠。
关键词:微波消解;火焰光度法;植物;全钾中图分类号:S132; ; ; ; ;文献标识码:A文章编号:0439-8114(2019)10-0142-04Abstract: A new method for the determination of total potassium in plants by microwave digestion-flame photometry was established by optimizing the conditions of digested acid,maximum digestion temperature and retention time of microwave digestion. The results showed that the optimal digestion condition was as follows:6 mL HNO3+2 mL H2O2 acid system, maximum digestion temperature 160 ℃ and retention time 15 min, and the detection limit was 0.002 mg/g. The results of the total potassium content of two plant reference materials determined by the optimal digestion procedure showed that the data was within the range of the certificate standard values. The recovery rates of total potassium contents of rice plant samples tested by the optimal digestion procedure were 97.5%~103.0% and the relative standard deviation was 0.63%~2.27%. The results suggested that this method is suitable for the determination of total potassium in different parts of plants, and the operation is simple and safe, and the result is accurate and reliable.Key words: microwave digestion; flame photometry; plant; total potassium鉀是植物生长必需的大量营养元素之一,在植物中以阳离子K+的形式存在,它在调节植物细胞渗透势方面起重要作用,也能激活许多参与呼吸作用和光合作用的酶[1],对作物的生长发育有不可替代的作用,因此在农业科学研究和农业生产中经常需要测定植物中钾元素含量。
微波消解-火焰光度法测定植物中全钾

微波消解-火焰光度法测定植物中全钾陶曙华;龚浩如;陈祖武;陈英姿;苗雪雪;王洁敏【摘要】通过优化微波消解用酸种类、最高温度及保持时间等条件,建立微波消解-火焰光度计测定植物中全钾的新方法.结果表明,采用6 mL HNO3+2 mL H2O2酸系,微波消解最高温度160℃,保持时间15 min的优化消解方法,测定的检出限0.002 mg/g;测定两种植物标准物质的全钾含量均在其证书标准值范围内;测定水稻植株样品的全钾含量加标回收率97.5%~103.0%,相对标准偏差0.63%~2.27%.该方法适用于植物不同部位全钾的测定,操作简便安全,结果准确可靠.【期刊名称】《湖北农业科学》【年(卷),期】2019(058)010【总页数】4页(P142-145)【关键词】微波消解;火焰光度法;植物;全钾【作者】陶曙华;龚浩如;陈祖武;陈英姿;苗雪雪;王洁敏【作者单位】湖南省水稻研究所,长沙 410125;农业部长江中下游遗传育种重点实验室,长沙 410125;湖南省水稻研究所,长沙 410125;农业部长江中下游遗传育种重点实验室,长沙 410125;湖南省水稻研究所,长沙 410125;农业部长江中下游遗传育种重点实验室,长沙 410125;湖南省水稻研究所,长沙 410125;农业部长江中下游遗传育种重点实验室,长沙 410125;湖南省水稻研究所,长沙 410125;农业部长江中下游遗传育种重点实验室,长沙 410125;湖南省水稻研究所,长沙 410125;农业部长江中下游遗传育种重点实验室,长沙 410125【正文语种】中文【中图分类】S132钾是植物生长必需的大量营养元素之一,在植物中以阳离子K+的形式存在,它在调节植物细胞渗透势方面起重要作用,也能激活许多参与呼吸作用和光合作用的酶[1],对作物的生长发育有不可替代的作用,因此在农业科学研究和农业生产中经常需要测定植物中钾元素含量。
植物中钾的测定一般采用火焰原子吸收光谱法[2],还可以采用 ICP-OES[3,4]、ICPMS[5,6]等,在多元素测定时采用ICP 等仪器准确快速,但这些仪器都比较昂贵,资金不雄厚的实验室难以购置。
植株全钾测定方法

植株全钾的测定1范围本标准规定了植株全磷测定的硫酸-过氧化氢消煮、火焰光度法测定。
本标准适用于禾本科植株全钾含量的测定。
2引用标准GB/T 603-2002 化学试剂试验方法中所用制剂及制品的制备GB/T6682-2008 分析实验室用水规格和试验方法NY/T 298-1995 有机肥料全磷的测定3测定原理植株样品经硝酸、高氯酸消煮后,消化液中的钾用火焰分光光度计测定。
火焰分光光度法是利用火焰做激发源,使钾原子激发。
根据激发出能量的大小测定钾素的含量。
4试剂所有试剂除注明者外,均为分析纯。
分析用水应符合GB/T 6682分析实验室用水规格和试验方法三级水的规格。
4.1硫酸(GB/T 625)。
4.2 30%过氧化氢(GB 6684)。
4.3钾标准溶液:称取1.907g经110℃条件下干燥2h的氯化钾(GB 646),溶于水,于1L 容量瓶中定容,即为1000mg/L钾标准y液,将其存于塑料瓶中。
5仪器与设备通常实验室用仪器设备和5.1消煮管:50mL或100mL。
5.2消煮炉或可调电炉:1000W。
5.3弯颈小漏斗:¢2cm。
5.4火焰光度计。
5.5分析天平:感量为0.1mg。
5.6移液管:5,10mL。
5.7容量瓶:50,100,1000mL。
6试样的制备取风干的实验室待测样品充分混匀后,按四分法缩减至100g,粉碎,籽粒全部通过0. 25mm(秸秆通过0.5mm)孔径筛,装入样品瓶备用。
7分析步骤7.1试样溶液制备称取试样0.5g,精确至0.001g,置于50ml消煮管(5.1)中(勿将样品粘附在瓶颈上)。
先滴入少些水湿润样品,然后加8mL硫酸(4.1),轻轻摇匀并放置过夜。
在管口放一弯颈小漏斗(5.3),在消煮炉上先250℃消煮(温度稳定后计时,时间约30min),待H2SO4分解冒出大量白烟后再升高温度至400℃,当溶液呈均匀的棕黑色时取下。
(时间约3h),稍冷后加10滴H2O2(注1),摇匀,再加热至微沸(注2),消煮约5min,取下稍冷后,重复加H2O2 5-10滴,再消煮。
植物全氮、全磷、全钾含量的测定

实验报告课程名称:土壤学实验指导老师:倪吾钟成绩:__________________ 实验名称:植物全氮、全磷、全钾含量的测定 同组学生XX :余慧珍一、实验目的和要求二、实验内容和原理 三、实验材料与试剂四、实验器材与仪器五、操作方法和实验步骤六、实验数据记录和处理 七、实验结果与分析八、讨论、心得一、 实验目的和要求1. 掌握植物样品消煮液制备方法;2. 掌握植物全氮、磷、钾的测定与结果分析。
二、 实验内容和原理1. 植物样品消煮——H 2SO 4-H 2O 2消煮法在浓H 2SO 4溶液中,植物样品经过脱水、碳化、氧化等作用后,易分解的有机物则分解。
再加入H 2O 2 ,H 2O 2在热浓H 2SO 4溶液中会分解出新生态氧,具有强烈的氧化作用,可继续分解没被H 2SO 4破坏的有机物,使有机态氮全部转化为无机铵盐。
同时,样品中的有机磷也转化为无机磷酸盐,植株中K 以离子态存在。
故可用同一消煮液分别测定N 、P 、K 。
2. 植株全氮的测定——靛酚蓝比色法经消煮待测液中氮主要以铵态氮存在,被测物浸提剂中的NH 4+,在强碱性介质中与次氯酸盐和苯酚反应,生成水溶性染料靛酚蓝,其深浅与溶液中的NH 4+-N 含量呈正比,线性X 围为0.05-0.5mg/l 之间。
3. 植株全磷的测定——钒钼黄比色法经消煮待测液中磷主要以磷酸盐存在,在酸性条件下,正磷酸能与偏钒酸和钼酸发生反应,形成黄色的三元杂多酸—钒钼磷酸[1]。
溶液黄色稳定,黄色的深浅与磷的含量成正相关。
4.植株全钾的测定——火焰光度计法消煮待测液中难容硅酸盐分解,从而使矿物态钾转化为可溶性钾。
待测液中钾主要以钾离子形式存在,用酸溶解稀释后即可用火焰光度计测定。
三、实验器材与仪器样品:三叶草,取于东七教学楼南侧,研磨过18目筛备用;试剂:浓硫酸、300g/l H2O2、6mol/l NaOH溶液、0.2%二硝基酚指示剂、酚溶液、次氯酸钠溶液、铵标准溶液(准确称量0.3142g经105℃干燥2h的氯化铵(NH4Cl),用少量水溶解,移100mL 容量瓶中,用吸收液稀释至刻度。
植株全氮的测定凯氏定氮法DB37T1627-2010

ICS65.020.20B 05 DB37 山东省地方标准DB 37/ T 1627—2010前言本标准按照GB/T 1.1-2009给出的规则起草。
本标准由山东省农业厅提出。
本标准由山东省农业标准化技术委员会归口。
本标准起草单位:山东省土壤肥料测试中心。
本标准主要起草人:泉维洁、赵建忠、侯小芳、蒋斌、卢桂菊、王健。
植株全氮的测定 凯氏定氮法1 范围本标准规定了植株全氮的测定方法。
本标准适用于小麦、玉米、水稻的籽粒与秸秆全氮含量测定。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 601 化学试剂 标准滴定溶液的制备GB/T603 化学试剂 试验方法中所用制剂及制品的制备GB/T 6682 分析实验室用水规格和试验方法DB37/T xxx 植株实验室样品制备3 方法原理样品用浓硫酸加过氧化氢消化,将有机氮转化为铵盐,在碱性条件下蒸馏,经硼酸吸收溶液吸收,用硫酸标准溶液滴定,测定植株全氮含量。
4 试剂和溶液所有试剂除注明者外,均为分析纯。
分析用水应符合GB/T 6682中至少三级水的规格要求。
试验中所需标准滴定溶液、制剂及制品,在没有注明其它要求时均按GB/T 601、GB/T603之规定制备。
4.1 硫酸:ρ(H2SO4)=1.84g/mL。
4.2 过氧化氢:φ(H2O2)≥30%。
4.3 氢氧化钠溶液:c(NaOH)=10mol/L。
4.4 氢氧化钠溶液:c(NaOH)=0.1mol/L;4.5 硼酸吸收溶液:20g硼酸溶于950mL约60℃的水中,冷却至室温后,每升硼酸溶液中加入甲基红–溴甲酚绿混合指示剂(4.7)20mL,并用氢氧化钠溶液(4.4)调节至微红色(pH约4.5),定容至1L。
4.6 硫酸标准滴定溶液:c(1/2H2SO4)=0.02mol/L。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ICS65.020.20
B 05 DB37 山东省地方标准
DB 37/ T 1626—2010
前言
本标准按照GB/T 1.1-2009给出的规则起草。
本标准由山东省农业厅提出。
本标准由山东省农业标准化技术委员会归口。
本标准起草单位:山东省土壤肥料测试中心。
本标准主要起草人:泉维洁、赵建忠、李建伟、王淑玲、侯小芳、许小芳、马红翠。
植株全钾的测定 火焰光度法
1 范围
本标准规定了植株全钾的测定方法。
本标准适用于小麦、玉米、水稻的籽粒与秸秆全钾含量测定。
2 规范性引用文件
下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 601 化学试剂 标准滴定溶液的制备
GB/T603 化学试剂试验方法中所用制剂及制品的制备
GB/T 6682 分析实验室用水规格和试验方法
DB37/T xxx 植株实验室样品制备
DB37/T xxx 植株全氮的测定 凯氏定氮法
3 方法原理
火焰光度法是利用火焰作激发源,使钾原子激发。
根据激发出能量的大小测定钾元素的含量。
植株样品经硫酸加过氧化氢消煮后,用火焰光度计测定消化液中的全钾含量。
4 试剂和溶液
所有试剂除注明者外,均为分析纯。
分析用水应符合GB/T 6682中至少三级水的规格要求。
试验中所需标准溶液、制剂及制品,在没有注明其它要求时均按GB/T 601、GB/T603之规定制备。
4.1 硫酸:ρ(H2SO4)=1.84g/mL;
4.2 过氧化氢:φ(H2O2)≥30%;
4.3 钾标准溶液:1000mg/L
称取1.907g在110℃条件下干燥2h的氯化钾(优级纯),溶于水,于1L容量瓶中定容,即为100 mg/L 钾标准液,将其存于塑料瓶中。
4.4 钾标准溶液:100 mg/L
吸取100mL钾标准溶液(4.3),于1L容量瓶中定容,即为100mg/L的钾标准溶液。
5 仪器
5.1 火焰光度计。
5.2 消煮炉:温度可达400℃,在200℃~400℃温度范围内,温差不大于±3℃。
5.3 弯颈小漏斗:直径2cm。
5.4 移液管:10mL。
5.5 容量瓶:50mL。
5.6 容量瓶:100mL。
5.7
容量瓶:1000mL。
6 分析步骤
警告——使用本标准的工作人员应有正规实验室工作的实践经验。
本标准未指出所有可能的安全问题。
使用者有责任采取适当的安全和健康措施,并保证符合国家有关法规规定的条件。
6.1 试样溶液制备
按照DB37/T xxx《植株全氮的测定 凯氏定氮法》6.1条款执行。
6.2 标准曲线绘制
用移液管(5.5)分别吸取钾标准溶液(4.4)0.00mL,1.00mL,2.50mL,5.00mL,10.00mL,15.00mL,分别置入50mL (5.6)容量瓶中,定容,即得钾含量分别为0.00mg/L,2.00mg/L,5.00mg/L,10.00mg/L,20.00mg/L,30.00mg/L 的标准溶液。
以浓度最高的标准溶液标定火焰光度计检流计的满度(一般只定到90),以空白溶液调节仪器零点,然后从稀到浓依次进行测定,记录检流计读数,以火焰光度计读数为纵坐标,钾浓度为横坐标绘制标准曲线。
6.3 测定
吸取按DB37/T xxx《植株全氮的测定 凯氏定氮法》6.1操作得到的消煮液10.00mL放入50mL容量瓶中,定容,与标准溶液系列同条件在火焰光度计上测定,读取检流计读数,每测5个样品必须用钾标准溶液重新校正仪器。
6.4 空白试验
除不加试样外,试剂用量和操作与测定试样时相同。
7 分析结果的表述
全钾(K)含量ω以克每千克(g/kg)表示,按(1)式计算:
3
0()10V D m
ρρω−−×=⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅⋅ (1)
式中:
ρ——从标准曲线中求得的测读液中钾的浓度,单位为毫克每升(mg/L); ρ0——从标准曲线求得的空白试样中钾的浓度,单位为毫克每升(mg/L); V ——检测液体积,单位为毫升(mL);
D ——分取倍数(定容体积与分取体积之比),本标准中为10; 10-3——将mL单位换算为L的换算因数; m ——测定时称样量,单位为克(g)。
所得结果应保留到小数点后三位。
8 允许差
平行测定结果的相对相差应符合表1的要求。
表1 实验室内测定结果允许相对相差
全钾含量(g/kg) 平行测定允许相对相差(%)
W≤10 ≤10
w>10 ≤5 不同实验室间测定结果允许相对相差应符合表2要求。
表2 不同实验室间测定结果允许相对相差
全钾含量(g/kg) 测定允许相对相差(%)
w≤10 ≤35
w>10 ≤15
_________________________________。
