肺炎支原体抗体检测试剂盒(胶体金法)
肺炎支原体抗体IgG金标检测试剂盒批生产记录

肺炎支原体抗体IgG金标检测试剂盒批生产记录生产批号:制造总量:人份产品总量人份盒投产日期:年月日记录总页数:页负责人(签字):1报告编号:名称:肺炎支原体抗体IgG金标检测试剂盒批号:有效期至:亚批号/数:1/1 生产日期:规格:25人份/盒报告日期:结论:合格 依据:肺炎支原体抗体IgG 金标检测试剂盒注册标准 附注:报告人:审核人: 负责人:No.名称:肺炎支原体抗体IgG金标检测试剂盒批号:抽样数:规格:试验日期:检定依据:结果判定:试验人:核对人:名称:肺炎支原体抗体IgG金标检测试剂盒试验日期:批号:检定依据:肺炎支原体抗体IgG金标检测试剂盒产品注册标准检定标准:1 阴性质控品符合率试剂盒测试阴性质控血清10份,假阳性判断结果不多于1份,符合率应≥90%。
2 阳性质控品符合率试剂盒测试阳性质控血清10份,假阴性判断结果不多于1份,符合率应≥90%。
3阴性质控品重复性使用试剂检测阴性质控血清10次,同一份质控血清的阴性判定结果应基本一致,假阳性判定结果分别不多于1份,检测阴性重复率≥90%。
4阳性质控品重复性使用试剂盒检测阳性质控血清10次,同一份质控血清的阳性判定结果应基本一致,假阴性判定结果分别不多于1份,检测阳性重复率≥90%。
5精密度每批试剂盒随机抽取10个检测卡样品,用阳性质控血清进行检测,要求各检测卡的显色应均一,且假阴性判断结果不多于1份,符合率≥90%。
6 批间差每批试剂随机抽取10个检测卡,用阳性质控血清进行检测,三个批号产品间检测结果应应基本一致,批间差<5%1 阴性质控品符合率向检测卡加样孔中用移液器加入10ul阴性质控品和100uL稀释液,静置15分钟观察结果。
结果:2 阳性质控品符合率向检测卡加样孔中用移液器加入10ul阳性质控品和100uL稀释液,静置15分钟观察结果。
结果:3 阴性质控品重复性向检测卡加样孔中用移液器加入10ul阴性质控品和100uL稀释液,静置15分钟观察结果。
肺炎衣原体MOMP抗体IgG检测试剂盒胶体金法作业指导书
肺炎衣原体MOMP抗体IgG检测试剂盒胶体金法作业指导书1 目的建立肺炎衣原体MOMP抗体IgG检测试剂盒(胶体金法)作业指导书,确保生产过程处于受控状态。
2 范围适用于肺炎衣原体MOMP抗体IgG检测试剂盒(胶体金法)相关工序的操作者。
3 职责3.1 操作人员应严格执行本作业指导书。
3.2 生产主管负责监督检查。
3.3 质检部质检员负责抽查执行情况。
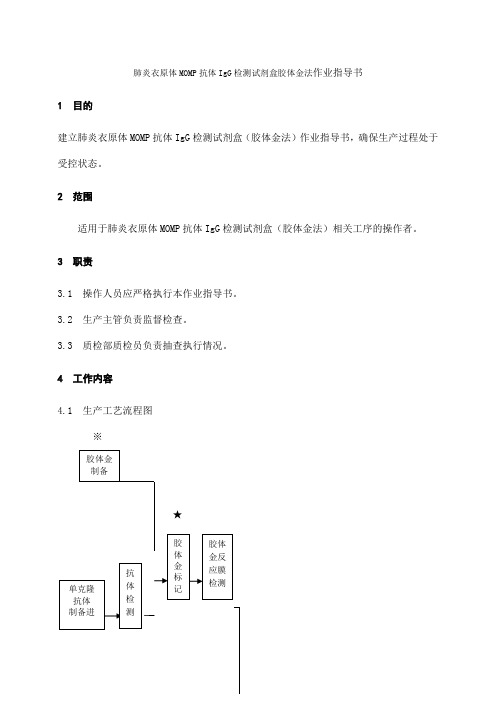
4 工作内容4.1 生产工艺流程图※★注:※ 关键过程 ★ 特殊过程4.2 作业内容4.2.1 胶体金制备(柠檬酸三钠还原法)氯金酸(HAuCl4)水溶液放入三角瓶内加热至沸腾→加热柠檬酸三钠溶液→混匀,搅拌煮沸10至15分钟→待胶体金溶液颜色由蓝→紫→红,冷却即可。
4.2.2 金标抗体(反应膜)制备以0.1M碳酸钾溶液调胶体金溶液pH8.0-9.0→加入抗人IgG单抗,15分钟后加入聚乙二醇→离心,调532nm测OD值5~10,方阵滴定法选定标记工作浓度→用无纺布浸湿胶体金溶液,干燥、平整,检测。
4.2.3 金标抗体反应膜质检将制备好的金标抗体反应膜按5‰比例抽检,与标准反应膜匹配组装成品,同时与标准成品作如下对照检测:a) 符合率:样品稀释液、阴性质控血清无假阳性,阳性质控血清均呈阳性;b) 反应强度:+/+++(阳性反应线/阴性反应线);c) 反应时间:30s~5min。
确认合格后才能转入下一工序。
4.2.4 NC反应膜制备亲和性高分子硝酸纤维素膜→活化处理12小时→用水洗5次,每次20分钟→室温干燥后→取纯化Cpn重组MOPP抗原和兔鼠IgG抗体溶于10%CS中,浓度均为2mg/ml,用Cpn重组MOPP抗原在NC膜上包被肺炎衣原体抗体阳性检测线→用兔抗鼠IgG抗体在NC膜上包被对照线→干燥后,用BS液封闭,H2O 清洗后,室温干燥,备用。
4.2.5 NC反应膜质检4.2.5.1 常规图形模式检测:将制备好的反应膜按5‰比例抽检,与标准金标抗体反映膜匹配组装成品,同时与标准成品对照检测;观察阳性、阴性包被线及本底,要求图形规则程度均匀,无遗漏或重复包被。
肺炎支原体IgM说明书

肺炎支原体抗体( IgM )检测试剂盒(胶体金法)说明书【产品名称】肺炎支原体抗体(IgM )检测试剂盒(胶体金法)【包装规格】40 人份 /盒或 20 人份 / 盒(详细规格见试剂盒包装标签)【预期用途】定性检测人血清中的肺炎支原体IgM 抗体,可用于支原体肺炎的协助诊疗。
【查验原理】本品应用间接法的胶体金标志免疫斑点渗滤原理,质控线采纳双抗夹心的胶体金标志免疫斑点渗滤原理。
该试剂盒里的斑点反响板上的微孔滤膜固相有肺炎支原体P1 蛋白抗原斑点,当待检测的血清中含有肺炎支原体IgM 抗体时,与微孔滤膜上的肺炎支原体P1 蛋白抗原抗原形成复合物,胶体金标志的羊抗人IgM 抗体与上述抗原抗体复合物联合,形成肉眼可见的红色斑点,即为阳性结果,不然为阴性结果。
微孔滤膜上的质控线含有羊抗人IgM 抗体,当待测血清加入后,人血清中的IgM 抗体与质控线上羊抗人IgM 抗体形成复合物,胶体金标志的羊抗人IgM 抗体再与上述复合物联合,形成肉眼可见的红色质控线。
【主要构成成份】1.斑点反响板: 40 块(或 20 块),每块斑点反响板主要由含固相肺炎支原体P1 蛋白抗原斑点的硝酸纤维膜和吸水纸构成。
2.试剂 A: 1 瓶,约 10ml (或 5 ml),无色澄清溶液,主要成份为PH7.4PBS 缓冲液、吐温-20、硫柳汞( 0.1%)。
3.试剂 B: 1 瓶,约 8ml(或 4ml),深红色澄清溶液,主要成份为胶体金标志的羊抗人IgM 抗体、牛血清白蛋白、硫柳汞(0.1%)。
【储藏条件及有效期】试剂盒一般采纳冷链运输,并采纳最迅速的运输方式,缩短运输时间;冬季运输应注意防备制品冻结。
试剂盒储藏条件为2℃~8℃,有效期为8 个月。
【样本要求】1.本试剂盒产品仅合用于对血清样本的检测,其余样本(如,胸腹水、脑脊液、尿液等)未经过产品预期用途的有关研究,不合用于本产品的检测。
2. 样本收集:采纳静脉血于干净离心管中,不加任何抗凝剂、保护剂,置于37℃水浴 20~ 30 分钟(或置室温 1 小时以上),待纤维蛋白原充足凝结后离心(4000 转/ 分, 5~ 10 分钟)分别血清。
肺炎支原体IgGIgM抗体检测试剂盒总体规模

肺炎支原体IgGIgM抗体检测试剂盒总体规模1 统计范围1.1 肺炎支原体IgG/IgM抗体检测试剂盒介绍1.2 肺炎支原体IgG/IgM抗体检测试剂盒分类1.2.1 全球市场不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒规模对比:2017 VS 2021 VS 20281.2.2 胶体金法1.2.3 酶联免疫法1.3 全球肺炎支原体IgG/IgM抗体检测试剂盒主要下游市场分析1.3.1 全球肺炎支原体IgG/IgM抗体检测试剂盒主要下游市场规模对比:2017 VS 2021 VS 20281.3.2 医院1.3.3 药店1.3.4 诊所1.3.5 其他1.4 全球市场肺炎支原体IgG/IgM抗体检测试剂盒总体规模及预测1.4.1 全球市场肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测:2017 VS 2021 VS 20281.4.2 全球市场肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)1.4.3 全球市场肺炎支原体IgG/IgM抗体检测试剂盒价格趋势1.5 全球市场肺炎支原体IgG/IgM抗体检测试剂盒产能分析1.5.1 全球市场肺炎支原体IgG/IgM抗体检测试剂盒总产能(2017-2028)1.5.2 全球市场主要地区肺炎支原体IgG/IgM抗体检测试剂盒产能分析1.6 肺炎支原体IgG/IgM抗体检测试剂盒市场发展趋势、驱动因素和阻碍因素分析1.6.1 肺炎支原体IgG/IgM抗体检测试剂盒市场驱动因素1.6.2 肺炎支原体IgG/IgM抗体检测试剂盒市场阻碍因素1.6.3 肺炎支原体IgG/IgM抗体检测试剂盒市场发展趋势2 主要厂商简介2.1 Remel (Thermo Scientific)2.1.1 Remel (Thermo Scientific)基本情况2.1.2 Remel (Thermo Scientific)主要业务2.1.3 Remel (Thermo Scientific)肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.1.4 Remel (Thermo Scientific)肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.2 InTec Products2.2.1 InTec Products基本情况2.2.2 InTec Products主要业务2.2.3 InTec Products肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.2.4 InTec Products肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.3 Labcorp2.3.1 Labcorp基本情况2.3.2 Labcorp主要业务2.3.3 Labcorp肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.3.4 Labcorp肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.4 Meridian Bioscience2.4.1 Meridian Bioscience基本情况2.4.2 Meridian Bioscience主要业务2.4.3 Meridian Bioscience肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.4.4 Meridian Bioscience肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.5 Savyon Diagnostics2.5.1 Savyon Diagnostics基本情况2.5.2 Savyon Diagnostics主要业务2.5.3 Savyon Diagnostics肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.5.4 Savyon Diagnostics肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.6 SERION Diagnostics2.6.1 SERION Diagnostics基本情况2.6.2 SERION Diagnostics主要业务2.6.3 SERION Diagnostics肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.6.4 SERION Diagnostics肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.7 ZEUS Scientific2.7.1 ZEUS Scientific基本情况2.7.2 ZEUS Scientific主要业务2.7.3 ZEUS Scientific肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.7.4 ZEUS Scientific肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.8 BioMérieux2.8.1 BioMérieux基本情况2.8.2 BioMérieux主要业务2.8.3 BioMérieux肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.8.4 BioMérieux肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.9 北京英诺特生物技术2.9.1 北京英诺特生物技术基本情况2.9.2 北京英诺特生物技术主要业务2.9.3 北京英诺特生物技术肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.9.4 北京英诺特生物技术肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.10 正元盛邦(天津)生物科技2.10.1 正元盛邦(天津)生物科技基本情况2.10.2 正元盛邦(天津)生物科技主要业务2.10.3 正元盛邦(天津)生物科技肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.10.4 正元盛邦(天津)生物科技肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.11 北京贝尔生物工程2.11.1 北京贝尔生物工程基本情况2.11.2 北京贝尔生物工程主要业务2.11.3 北京贝尔生物工程肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.11.4 北京贝尔生物工程肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)2.12 北京金沃夫生物工程2.12.1 北京金沃夫生物工程基本情况2.12.2 北京金沃夫生物工程主要业务2.12.3 北京金沃夫生物工程肺炎支原体IgG/IgM抗体检测试剂盒产品介绍2.12.4 北京金沃夫生物工程肺炎支原体IgG/IgM抗体检测试剂盒销量、价格、收入、毛利率及市场份额(2019、2020、2021和2022)3 全球市场肺炎支原体IgG/IgM抗体检测试剂盒主要厂商竞争态势3.1 全球市场主要厂商肺炎支原体IgG/IgM抗体检测试剂盒销量(2019、2020、2021和2022)3.2 全球市场主要厂商肺炎支原体IgG/IgM抗体检测试剂盒收入(2019、2020、2021和2022)3.3 全球肺炎支原体IgG/IgM抗体检测试剂盒主要厂商市场地位3.4 全球肺炎支原体IgG/IgM抗体检测试剂盒市场集中度分析3.5 全球市场肺炎支原体IgG/IgM抗体检测试剂盒主要厂商总部及产地分布3.6 全球主要厂商肺炎支原体IgG/IgM抗体检测试剂盒产能3.7 肺炎支原体IgG/IgM抗体检测试剂盒新进入者及扩产计划3.8 肺炎支原体IgG/IgM抗体检测试剂盒行业扩产、并购情况4 全球主要地区规模分析4.1 全球主要地区肺炎支原体IgG/IgM抗体检测试剂盒市场规模4.1.1 全球主要地区肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)4.1.2 全球主要地区肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)4.2 北美市场肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)4.3 欧洲市场肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)4.4 亚太市场肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)4.5 南美市场肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)4.6 中东及非洲市场肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)5 全球市场不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒市场规模5.1 全球不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)5.2 全球不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)5.3 全球不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒价格(2017-2028)6 全球市场不同应用肺炎支原体IgG/IgM抗体检测试剂盒市场规模6.1 全球不同应用肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)6.2 全球不同应用肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)6.3 全球不同应用肺炎支原体IgG/IgM抗体检测试剂盒价格(2017-2028)7 北美7.1 北美不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)7.2 北美不同应用肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)7.3 北美主要国家肺炎支原体IgG/IgM抗体检测试剂盒市场规模7.3.1 北美主要国家肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)7.3.2 北美主要国家肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)7.3.3 美国肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)7.3.4 加拿大肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)7.3.5 墨西哥肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)8 欧洲8.1 欧洲不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)8.2 欧洲不同应用肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)8.3 欧洲主要国家肺炎支原体IgG/IgM抗体检测试剂盒市场规模8.3.1 欧洲主要国家肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)8.3.2 欧洲主要国家肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)8.3.3 德国肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)8.3.4 法国肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)8.3.5 英国肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)8.3.6 俄罗斯肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)8.3.7 意大利肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)9 亚太9.1 亚太不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)9.2 亚太不同应用肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)9.3 亚太主要国家肺炎支原体IgG/IgM抗体检测试剂盒市场规模9.3.1 亚太主要地区肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)9.3.2 亚太主要地区肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)9.3.3 中国肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)9.3.4 日本肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)9.3.5 韩国肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)9.3.6 印度肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)9.3.7 东南亚肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)9.3.8 澳大利亚肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)10 南美10.1 南美不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)10.2 南美不同应用肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)10.3 南美主要国家肺炎支原体IgG/IgM抗体检测试剂盒市场规模10.3.1 南美主要国家肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)10.3.2 南美主要国家肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)10.3.3 巴西肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)10.3.4 阿根廷肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)11 中东及非洲11.1 中东及非洲不同产品类型肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)11.2 中东及非洲不同应用肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)11.3 中东及非洲主要国家肺炎支原体IgG/IgM抗体检测试剂盒市场规模11.3.1 中东及非洲主要国家肺炎支原体IgG/IgM抗体检测试剂盒销量(2017-2028)11.3.2 中东及非洲主要国家肺炎支原体IgG/IgM抗体检测试剂盒收入(2017-2028)11.3.3 土耳其肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)11.3.4 沙特肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)11.3.5 阿联酋肺炎支原体IgG/IgM抗体检测试剂盒市场规模及预测(2017-2028)12 肺炎支原体IgG/IgM抗体检测试剂盒销售渠道分析12.1 肺炎支原体IgG/IgM抗体检测试剂盒销售渠道12.1.1 直销12.1.2 经销12.2 肺炎支原体IgG/IgM抗体检测试剂盒典型经销商12.3 肺炎支原体IgG/IgM抗体检测试剂盒典型客户13 研究结论14 附录14.1 研究方法14.2 研究过程及数据来源14.3 免责声明。
免疫胶体金法与间接免疫荧光法在肺炎支原体感染检测中的应用

免疫胶体金法与间接免疫荧光法在肺炎支原体感染检测中的应用摘要:探究免疫胶体金法与间接免疫荧光法在肺炎支原体感染检测中的应用效果。
方法:选取2021年1月~2023年1月于我院进行治疗的呼吸道肺炎支原体感染的患者共134例作为本次实验的研究对象。
比较免疫胶体金法以及间接免疫荧光法检测在肺炎支原体感染检测中的感染阳性率和临床符合率。
结果:使用两种方法进行检测,免疫胶体金法检测出的肺炎支原体感染阳性例数为62例,间接免疫荧光法检测肺炎支原体感染的阳性例数为99例。
比较两组肺炎支原体感染检测方法的检测阳性率,两组检测方法的检测阳性率差异有统计学意义,P<0.05。
比较两组肺炎支原体感染检测方法的临床符合率,免疫胶体金法检测肺炎支原体感染的阳性例数为62例,符合例数为54例,阴性例数为72例,符合例数为19例,免疫胶体金法在肺炎支原体感染检测中的符合率为54.5%。
间接免疫荧光法检测肺炎支原体感染的阳性例数为99例,符合例数为90例,阴性例数为35例,符合例数为18例,间接免疫荧光法检测肺炎支原体感染的临床符合率为80.6%。
结论:间接免疫荧光法对肺炎支原体感染的检测阳性率以及临床符合率高于免疫胶体金法。
两种检测方法对肺炎支原体感染的诊断均有一定的临床价值。
关键词:免疫胶体金法;间接免疫荧光法;肺炎支原体感染;检测应用肺炎支原体是人类支原体肺炎的病原体[1],通常会导致患者发生间质性肺炎,有时并发支气管肺炎。
潜伏期10~20天,临床症状较轻,以头痛,发热,咳嗽等呼吸道症状为主[2]。
一年四季均可发生,临床发病率以青少年最高。
由于肺炎支原体感染的临床症状并不典型,无法与其他肺炎相区别,因此诊断多依靠实验室检测为主。
现阶段检测肺炎支原体感染的方法包括培养法、间接免疫荧光法、胶体金法[3]等。
本实验探究免疫胶体金法与间接免疫荧光法在肺炎支原体感染检测中的应用效果,现报道如下。
一、资料与方法1.1一般资料选取2021年1月~2023年1月与我院进行治疗并确诊为肺炎支原体感染的患者共134例作为实验对象,其中有男性67例,女性67例,最大年龄14岁,最小年龄0.1岁,有普通肺炎33例,大叶性肺炎12例,支气管肺炎89例。
肺炎支原体抗体IgG金标检测试剂盒作业指导书
肺炎支原体抗体IgG金标检测试剂盒作业指导书4.2.6.1 反应体组装程序:a) 在S6塑料基板上贴双面胶带S5(29,48mm)二条;b) 在S5上贴反应膜S1(20mm),S1上下缘距S6上下缘各29mm;c) 在S6上贴吸水纸S3(30mm),吸水纸下缘与S1上缘交接1mm,上缘与S5的上边缘对齐;d) 在S5下端贴无纺布S2-1,其上缘压住S1下缘1mm;e) 在S2-1上平放金标抗体反应膜S4(10mm)上缘对齐;f) 在S4上平放无纺布S2-2(30mm)上下缘分别S4、S6对齐;g) 将组装成型的反应体系用电脑可调式切割机切成4.2mm测试条,装入干燥器,待包装。
4.2.6.2 成品包装:每支成品先装聚苯乙烯塑料外壳,再用镀铝膜包装加干燥剂,附说明书,打批号入库,每批留样100人份,以备复检.4.2.7 参比品制备4.2.7.1 肺支Ig-G阳性血清质控品取临床确诊肺衣病人(临床症状明显、肺炎衣原体培养阳性)血清15份,间接ELISA测定肺炎衣原体IgM抗体阳性,0D492≥0.3,混合血清加防腐剂,分装-70℃保存。
4.2.7.2 肺支Ig-G阴性血清质控品取健康人血清(体查健康,培养法和间接ELISA测定肺炎支原体IgG抗体均阴性,0D492<0.10)15份,混合血清加防腐剂,分装-70℃保存。
4.3 成品检测产品技术要求应符合《肺炎支原体抗体IgG金标检测试剂盒》产品注册标要求。
4.3.1 外观4.3.1.1 要求a)检测条:表面应平整、无划伤、开裂、变形及污渍;检测卡各组分附着牢固、内容齐全;b) 检测卡:外壳应平整,上下盖应均匀合拢,无明显间隙;反应芯试条在外壳内应附着牢固;4.3.1.2 检验在自然光线下,用手感和目力观察方法进行检验。
4.3.2 符合率4.3.2.1 阴性符合率4.3.2.1.1要求试剂卡测试肺炎支原体IgG抗体阴性质控血清10份,假阳性判断结果不多于1份,符合率应≥90%。
肺炎支原体IgM和优生四项TORCH

1.弓形体IgG主要用于弓形体即往感染的诊断,弓形体IgM主要用于 弓形体急性感染的诊断。弓形虫感染弓形虫感染是一种人畜共患疾病 猫与其他动物是传染源。后天感染轻型者常无症状,但血清中可查到 抗体;重型者可引起各种症状如高热、肌肉或关节疼痛、淋巴结肿大 等;通过胎盘宫内感染者可引起死胎早产,出生后可表现一系列中枢 神经系统症状以及眼、内脏的先天损害。妊娠期妇女感染弓形体会引 起流产、早产、胎儿宫内死亡、婴儿脑积水、神经发育障碍等。小动 物身上多携带弓形体。提醒家里养宠物的孕妇注意。
TORCH检测包括IgM与IgG两种抗体,前者表示新近1~2月的感染,后者 表示既往感染,表示具有一定的免疫力,尤其是风疹病毒 IgG阳性, 认为有终身的免疫力。孕前TORCH的检测就是要了解妇女对这几种病 毒的免疫状况,是否需接种风疹疫苗或是否对其他病毒具有一定的免 疫力,从而指导孕前妇女怀孕的时间及注意事项,达到优生的目的。
【检测原理】 胶体金法。以纯化的肺炎支原体(MP)特异性抗原和单克隆抗体,结合金标免疫渗滤 试验(GIFA)原理,以间接法测定血清中的肺炎支原体lgM抗体(MP-lgM)。
【操作方法】
1、取出试剂盒,室温平衡20-30min;
2、滴加洗涤液1滴于反应孔内,待液体将膜完全湿润;
3、加待测血清3-4滴(约150ul)于反应孔内,待液体充分吸收;
3 .巨细胞病毒 IGG 主要用于诊断巨细胞病毒即往感染,巨细胞病毒 IgM主要用于诊断巨细胞病毒急性感染。巨细胞病毒lgM抗体阳性提示 病人近期有巨细胞病毒感染但应结合临床情况进行具体分析。成人感 染后巨细胞病毒可引起肝炎、肺炎。孕妇感染后会造成胎儿受损,最 终导致胎儿宫内死亡。新生儿感染会造成黄疸、血小板减少性紫癜、 溶血性贫血、脑损伤。
胶体金法检测肺炎支原体IgM抗体的临床应用

胶体金法检测肺炎支原体IgM抗体的临床应用作者:刘强韩晓红来源:《延边医学》2015年第01期摘要:目的:胶体金法检测肺炎支原体IgM抗体,用肺炎支原体抗原固相硝酸纤维素膜,应用渗滤式间接法原理,检测血清中肺炎支原体抗体。
主要用于对肺炎支原体IgM抗体的检测,其结果是肺炎支原体早期感染的辅助诊断。
关键词:肺炎支原体 ; 胶体金法 ; 临床应用肺炎支原体(Mycoplasma neumonia ,MP)是引起非典型性肺炎最常见的病原体。
主要侵犯呼吸系统。
肺炎支原体粘附于粘膜上皮细胞的受体上,吸收宿主细胞的养料生长繁殖,同时释放有毒代谢产物使细胞受损,主要通过呼吸道传播。
青少年易感,冬秋季较多见,引起间质性肺炎和急性支气管炎。
严重者可同时引起脑炎、肾炎、心肌炎等多种肺外并发症。
肺炎支原体(MP)的发病率可占到所有肺炎病例的20%~30%,在流行高峰时,其发病率可达到肺炎总发病率的70%~80%。
临床症状如头痛、发热、乏力、不适、咽喉疼痛、咳嗽、胸痛、肌痛等,儿童和老年人的症状较为严重,其起病、发展和康复的速度往往都较缓慢。
1 对象与材料1.1 ;研究对象本组临床患者396例:其中:男性:194例,年龄4~75岁;女性:202 例,年龄 3~73岁。
1.2 ;方法与试剂;肺炎支原体IgM抗体检测试剂盒(胶体金法)由福建三明博峰生物科技有限公司生产。
1.3 ;标本采集与处理采用静脉血3ml将全血放入试管里(内无任何抗凝剂),采集的静脉血置室温30分钟或放置37℃水浴箱孵育15-20分钟后,低速离心3000rpm,5~10分钟,分离血清。
当明显溶血、黄疸(胆红素浓度)40.1μmol/L)、高脂血(甘油三酯浓度)7.0mmol/L)时,血清不能使用。
1.4 标本保存:若分离后的血清不能及时检测的,应将标本保存在2-8℃冰箱内,若保存时间超过7天,则需要将标本保存在-20℃以下,并避免反复冻融,以免抗体效价降低。
三种方法检测肺炎支原体抗体的一致性分析

三种方法检测肺炎支原体抗体的一致性分析肺炎支原体是肺炎的主要病原体之一,其抗体检测有助于肺炎的诊断与治疗。
本文将介绍三种方法检测肺炎支原体抗体的一致性分析,以期对肺炎的诊断与治疗提供帮助。
胶体金法是一种利用金纳米微粒为标记的快速免疫层析试验,其原理是将标记有肺炎支原体抗体的胶体金微粒与样品中的肺炎支原体抗体结合,形成一条可视化的红色条带。
该方法检测肺炎支原体抗体的一致性分析需要进行质量控制。
首先,需采用标准阳性和阴性样品进行控制,保证胶体金试剂盒处于正常状态。
其次,应在相同条件下使用相同批次的试剂盒进行检测,以避免不同批次试剂盒的差异性。
研究发现,胶体金法检测肺炎支原体抗体的一致性较好,其结果可与其他方法检测结果相吻合。
酶联免疫吸附法(ELISA)是一种常见的免疫学方法,利用酶标记的二抗或抗原与待测样品中的抗体结合,形成酶标记复合物,再加入底物后,根据反应体系颜色变化的程度判断样品中抗体的含量。
该方法检测肺炎支原体抗体的一致性分析同样需要进行质量控制。
ELISA检测中,标准阳性和阴性样品是非常重要的控制。
此外,需要保持检测条件和试剂的一致性,同时要定期进行比对试验,保证试验结果的准确性。
研究表明,ELISA法检测肺炎支原体抗体的一致性较好,可用于临床实验和作为监控慢性肺炎的方法。
荧光免疫分析法(FIA)是一种高灵敏度、高效率的免疫学技术,可以用于检测肺炎支原体抗体。
该方法利用荧光标记的抗体与肺炎支原体抗体结合,随后进行荧光信号检测,从而获得抗体的含量。
FIA检测肺炎支原体抗体的一致性分析需要进行定量分析和质量控制。
在FIA检测中,质量控制、标准品、正、负对照样品的添加和分析的标准化十分重要。
厂家提供的质量对照品可以用于确保试剂盒质量,并作为分析的基准点。
总结:目前,肺炎支原体抗体检测已成为肺炎的辅助诊断方法。
在实际应用中,选择合适的检测方法,根据标准化操作流程,严格进行质控,对于保证肺炎支原体抗体检测的一致性分析有着重要的意义。
肺炎支原体抗体IgM金标检测试剂盒产品简介

肺炎支原体抗体IgM金标检测试剂盒产品简介肺炎支原体抗体IgM金标检测试剂盒按2005版《医疗器械分类目录》,属临床医学检验辅助设备(6840)。
管理类别为Ⅱ类。
产品简介如下:3.1结构组成3.1.1产品结构3.1.2检测卡:由检测条和聚苯乙烯塑料外壳制成。
3.1.3检测条:由已包被了检测线和对照线的硝酸纤维素膜、化学偶合物膜、样品吸收膜,胶纸等部分经层压而成,再分切成固定宽度的条状。
3.2主要原材料3.2.1重组肺支特异蛋白抗原:为三种基因重组表达肺支特异蛋白抗原用于包被硝酸纤维素膜检测线。
3.2.2抗人免疫球蛋白M单克隆抗体:纯化的抗人免疫球蛋白M单克隆抗体,用于胶体金的标记。
3.2.3抗鼠免疫球蛋白M抗体:纯化的兔抗鼠免疫球蛋白M抗体,用于包被硝酸纤维素膜控制线。
3.2.4金标检测条:由S1—S7部分构成:S1选用亲和性高分子纤维素膜,经预先处理后制备成反应膜用来显示整体系统的反应结果;S2、S3选用可使液体爬行速度较快,吸附力较强的粗纤维吸水纸或无纺布,其作用在于被粘贴在反应体的不同部位吸收待检样品标本;S4同样选取吸附力较强的无纺布,作为金标记抗体的固相吸附材料;S5为不同规格的双面胶,用于固定各种反应膜和吸水材料于S7上;S6塑料基板,作为测试条反应体的支撑物;S7单面胶带,用于固定金标反应膜和吸水材料于S6上;3.3基本参数3.3.1 试剂盒的基本参数应符合表1的规定。
表2:基本参数3.3.2外观3.3.2.1检测卡表面应平整、无划伤、开裂、变形及污渍;检测条各组分附着牢固、内容齐全;3.3.2.2检测卡壳应平整,上下盖应均匀合拢,无明显间隙;检测条在外壳内应附着牢固。
3.3.3符合率:3.3.3.1阴性符合率:试剂卡测试肺支IgM抗体阴性质控血清10份,假阳性判断结果不多于1份,符合率应≥90%。
3.3.3.2阳性符合率:试剂条测试肺支IgM阳性质控血清10份,假阳性判断结果不多于1份,符合率应≥90%。
肺炎支原体检测试剂盒胶体金法

肺炎支原体检测试剂盒胶体金法背景与引言肺炎支原体是一种常见的致病菌,它是导致上呼吸道感染和肺炎的一种主要病原体。
近年来,肺炎支原体感染的发病率逐渐增加,因此早期快速的检测非常重要。
为了满足临床上对肺炎支原体的检测需求,研发出了肺炎支原体检测试剂盒胶体金法。
本文将详细介绍肺炎支原体检测试剂盒胶体金法的原理、操作步骤和优势。
原理肺炎支原体检测试剂盒胶体金法采用了胶体金免疫层析技术。
该技术利用了胶体金颗粒在溶液中的颜色变化特性,通过金标记的抗原与肺炎支原体的特异性抗体结合形成颗粒免疫复合物,从而实现对肺炎支原体的检测。
操作步骤1.样品处理:取适量标本(一般为呼吸道分泌物或咽拭子),按照说明书的要求进行预处理,如离心、加入提取液等。
2.载板处理:将处理后的样品滴加到测试载板上,一般每个孔滴加样品的量为5-10μL。
3.滴加试剂:将胶体金标记的抗原滴加到载板上,与样品中的肺炎支原体结合形成颗粒免疫复合物。
4.反应时间:根据产品说明书的要求,将载板放置在恒温箱或特定的反应时间,一般为10-20分钟。
5.结果读取:观察载板上颗粒免疫复合物的颜色变化,一般采用裸眼观察或光度计测量吸光度来判断结果。
优势1.快速检测:肺炎支原体检测试剂盒胶体金法可以在短时间内完成检测,通常只需要20分钟左右,大大缩短了检测周期。
2.简单易用:操作步骤简单,只需要少量的样品和试剂,无需复杂的实验仪器和设备,使得检测更加便捷。
3.灵敏度高:胶体金免疫层析技术具有较高的灵敏度,可以检测到低浓度的肺炎支原体,提高了检测的准确性和可靠性。
4.成本低廉:与其他检测方法相比,采用胶体金法进行肺炎支原体检测的成本较低,可以降低医疗机构的检测费用。
5.广泛应用:肺炎支原体检测试剂盒胶体金法适用于不同场景的肺炎支原体检测,可以在临床、疫情监测等多个领域得到广泛应用。
结论肺炎支原体检测试剂盒胶体金法作为一种快速、简单、灵敏度高且成本低廉的检测方法,对于肺炎支原体感染的早期诊断和疫情监测具有重要意义。
肺炎支原体IgM抗体检测SOP

肺炎支原体IgM抗体检测SOP一、检验目的规范实验室人员操作,以保证实验结果的准确性。
二、预期用途该产品用于定性检测血清、血浆或全血中的肺炎支原体IgM抗体。
是引起社区获得性呼吸道感染的主要病原体之一,可以导致支气管炎和非典型性肺炎。
主要引起人非典型肺炎、气管炎及支气管炎,多经口和呼吸道等途径传播,多发于儿童和青年人。
MP感染已占小儿呼吸道疾病30%以上,且有增加趋势。
人体感染肺炎支原体后,能产生特异性IgM和IgG抗体。
IgM 抗体出现早,一般在感染后1周出现,3~4周达高峰,以后逐渐降低。
再次感染或重复感染后,常在1-2周内出现较高水平的IgG抗体。
MP肺炎与一般呼吸道感染和肺炎的临床症状没有明显区别,MP感染早期诊断有利于MP肺炎的治疗。
血青学诊断法是临床常用的主要诊断方法之一,灵敏度和特异性适中,常用的主要有酶联免疫吸附试验和凝集试验。
三、检验原理本产品以胶体金作为指示标记,用胶体金标记抗人IgM单抗,以基因工程技术表达肺炎支原体P1蛋白抗原标被硝酸纤维素膜,应用“间接法”免疫层析技术原理,检测的肺炎支原体感染病人血清、血浆或全血中的肺炎支原体抗体IgM,在检测过程中,若样本中存在肺炎支原体抗体gM, 则肺炎支原体抗体1gM与样本吸附垫中的胶体金一抗人IgM单抗结合物形成复合物,复合物沿硝酸纤维素膜移动到检测区,与检测线上包被的肺炎支原体P1蛋白抗原结合,多余的未被结合的结合物继续移动到质控区,与质控线上包被的羊抗鼠IgG 抗体结合,反应膜上出现1条红色的检测线和1条红色的质控线;若样本中不存在肺炎支原体抗体IgM,则胶体金一抗人IgM单抗结合物直接沿硝酸纤维素膜移动到质控区,与质控线上包被的羊抗鼠IgG抗体结合,仅形成一条红色的质控线。
四、主要组成成份1、试剂盒组分包括肺炎支原体1gM抗体检测卡,样品稀释液。
1.1、检测卡主要组分:包括金标垫和硝酸纤维素检测膜,金标垫内包被有胶体金标记的抗人IgM单克隆抗体;硝酸纤维素检测膜的检测线上包被有基因工程技术表达的肺炎支原体P1蛋白抗原,质控线上包被有羊抗鼠IgG抗体。
肺炎支原体抗体金标检测试剂盒作业指导(精品)

肺炎支原体抗体IgM 金标检测试剂盒作业指导书1目的建立肺炎支原体抗体IgM 金标检测试剂盒作业指导书,确保生产过程处于受控状态。
2范围适用于肺炎支原体抗体IgM 金标检测试剂盒相关工序的操作者。
3职责3.1操作人员应严格执行本作业指导书。
3.2生产主管负责监督检查。
3.3质检部质检员负责抽查执行情况。
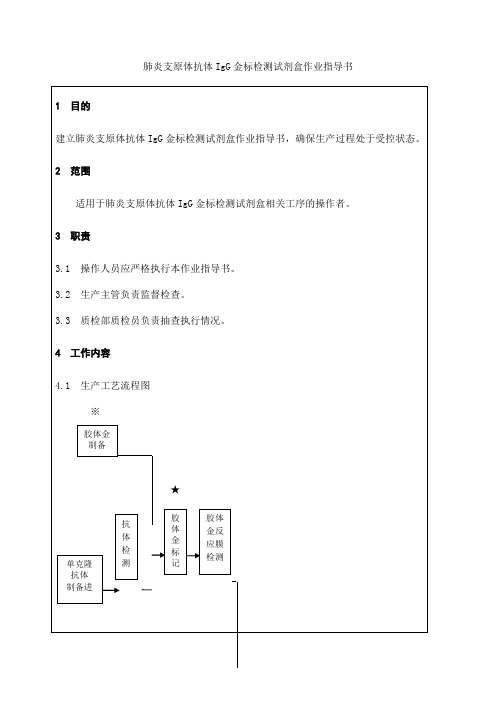
4工作内容4.1生产工艺流程图※胶体金制备★胶体抗胶体金反单克隆体金应膜抗体检标检测制备进测记★肺炎支原体重组抗原的表达※NC膜处理兔抗鼠IgG 抗体制备抗原检测NC膜检测★NC膜包被抗体检测质装产贴切量卡品分NC 检检板条包反测测应膜检测入库注:※关键过程★特殊过程4.2作业内容4.2.1胶体金制备(柠檬酸三钠还原法)氯金酸(HAuCl4)水溶液放入三角瓶内加热至沸腾→加热柠檬酸三钠溶液→混匀,搅拌煮沸10至15分钟→待胶体金溶液颜色由蓝→紫→红,冷却即可。
4.2.2金标抗体(反应膜)制备以0.1M 碳酸钾溶液调胶体金溶液 pH8.0-9.0→加入抗人 IgM 单抗, 15 分钟后加入聚乙二醇→离心,调532nm测OD值5~10,方阵滴定法选定标记工作浓度→用无纺布浸湿胶体金溶液,干燥、平整,检测。
4.2.3金标抗体反应膜质检将制备好的金标抗体反应膜按5‰比例抽检,与标准反应膜匹配组装成品,同时与标准成品作如下对照检测:a)符合率:样品稀释液、阴性质控血清无假阳性,阳性质控血清均呈阳性;b)反应强度:+/+++(阳性反应线/阴性反应线);c)反应时间:30s~5min。
确认合格后才能转入下一工序。
4.2.4NC 反应膜制备亲和性高分子硝酸纤维素膜→活化处理12 小时→用水洗 5 次,每次 20 分钟→室温干燥后→取纯化Cpn重组MOPP抗原和兔鼠IgG抗体溶于10%CS中,浓度均为2mg/ml,用Cpn重组肺炎支原体抗原在NC 膜上包被肺炎支原体抗体阳性检测线→用兔抗鼠IgG 抗体在NC膜上包被对照线→干燥后,用BS 液封闭, H2O 清洗后,室温干燥,备用。
肺炎支原体抗体胶体金法快速检测试剂研制和初步实验室考核

图l免疫层析试纸结构示意图a为正面圈,b为纵截面图。
l劂试带2.对照带3样品垫4.金标垫5.塑料底衬6.硝酸纤维素膜7.双面腔层8.吸水垫2.6试纸检测效果观察取Mp免疫兔血清用生理盐水按l:10、1:20、i:40稀释,正常兔血清按1:20稀释作为待检样品,用上述制备的Mp肺炎免疫胶体金法快速诊断试纸进行检测,具体步骤如下;吸取待检样品150[:i滴加在样品垫上,样品开始层析上行,2min后观察结果,15min观察终止。
结果判定;于质控区(C)和检测区(T)出现2条红色沉淀线,为Mp抗体检测阳性,即有Mp感染;仅于质控区(c)出现I条红色沉淀线,为Mp抗体检测阴性,即无Mp感染;如试验中没有沉淀线出现,说明试验无效(见图2)。
图2免疫胶体合法试纸检测结果判定结果1.Mp灭活菌体抗原的检定图3为荧光显微镜下观察到的Mp灭活的完整菌体形态。
可见其直径大小约为0.3Eha,是呈亮绿色、边界清晰的圆形颗粒。
图3荧光显微镜下的Mp灭活菌体抗原2.胶体金颗粒的检定经电镜观察胶体金颗粒,里圆形或椭圆形,大小均匀一致;随机测量100个金颗粒,平均直径约为20rim,符合试验设计要求(见图4)。
图4电镜舭祭胶体金颗粒3.胶体金标记SPA的最低稳定浓度和最佳剂量根据颜色反应,胶体金标记SPA的最低稳定浓度为第6管,即每ml胶体金溶液需要SPA5=g(见图5),最佳标记量为在此基础上再加20%SPA,即每m】胶体金溶液需要SPA6弯。
图5胶体金标记SPA的最低稳定浓度实验结果4.胶体金标记SPA的最佳pH值胶体金与蛋白质结合一般在蛋白质等电点(PI)略偏硷的条件下比较牢固,经过试验选择SPA标记的最佳pH6.0,结果证明标记效果良好。
5.胶体金标记SPA探针的浓度检定以保存液作对照,用分光光度计测定试验中胶体金标记SPA探针在520rim处的A值为3.51,在适宜的A值(2.5.10)范围内,说明试验中胶体金标记SPA探针的浓度符合设计要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
B19病毒抗体检测试剂盒(胶体金法)
说明书
【产品名称】B19病毒抗体检测试剂盒(胶体金法)
【包装规格】24人份/盒 48人份/盒
【预期用途】用于检测试验血清中的B19病毒抗体(IgM/IgG)
【检验原理】用B19病毒抗原固相硝酸纤维素膜,应用渗滤式间接法原理,检测血清中B19病毒抗体。
【主要组成成份】
1、反应板 24份或48份
2、试剂Ⅰ 1瓶 0.02mol/L PH 7.4 PBS
3、试剂Ⅱ 1瓶胶体金标记物
【储存条件及有效期】产品应储存在2℃~8℃条件中,不能冷冻;有效期24个月。
【样本要求】
1、血清样品不能溶血,应为新鲜血清或2℃~8℃条件保存不超过一周。
2、高脂血症血清不能使用。
【检验方法】
1、滴入二滴试剂Ⅰ于反应板中央孔中,待完全渗入;
2、滴入100µl血清于反应板孔中,待完全渗入;
3、滴加三滴试剂Ⅱ于反应板孔中,待完全渗入;
4、渗入三滴试剂Ⅰ于反应板孔中,待完全渗入。
【结果解释】
阳性:反应板孔中C端出现红色圆斑,T端出现红色圆斑,为B19病毒抗体阳性;
阴性:反应板孔中C端出现红色圆斑,T端不出现红色圆斑,为B19病毒抗体阴性。
失效:反应板孔中C端不出现红色圆斑,或C端、T端均不出现红色圆斑,为试剂盒失效。
【检验方法的局限性】
1、本试剂试验仅用于检测B19病毒抗体而非直接检测B19病毒抗原,因而阳性结果并不能确诊是B19病毒感
染。
对患者状况的诊断应结合患者临床体征与症状和试验结果的综合分析。
2、抗体含量低的血清样品,不能被检测出来是可能的。
部份B19病毒感染的患者,不产生抗体或产生少量
的抗体。
此时,可能显示阴性结果。
3、试验结果可疑时,应用PCR法确诊。
【产品性能指标】
1、批内精密度:阳性符合率和阴性符合率均应≥95%,反应斑点颜色深浅程度应接近。
2、批间精密度:阳性符合率和阴性符合率均应≥95%。
【注意事项】
1、本产品尚未获得产品注册证号,仅供研究,不用临床诊断。
2、试验一旦开始操作,应按操作步骤连续进行,直至结束。
3、试剂盒从冰箱取出时,应使试剂恢复至室温。
