第十章 杂环化合物(1)
合集下载
10-杂环和脂类化合物

CH3(CH2)14COOH 十八碳酸 硬脂酸
十六碳酸
俗名 简写符号 软脂酸(棕榈酸) 16:0
16 10 9
18:0
1 7 8 16
CH3(CH2)5CH=CH(CH2)7COOH
1
俗名:
Δ编码体系命名: 简写符号:
棕榈油酸
Δ 9—十六碳烯酸 16:1Δ9
ω编码体系命名: ω 7—十六碳烯酸 简写符号: 16:1ω 7
(90%)
(2) 加成: H2 / Ni 125 ℃, 100atm
O 呋喃
O 四氢呋喃
S 噻吩
H2 / Pd-C, CH3OH, H2SO4, 3 atm
S 四氢噻吩
H2 / Ni 高温高压 吡咯
四氢吡咯
第三节
六元杂环化合物
六元杂环化合物包括环中有1个杂原子的六元 杂环(如吡啶等);环中有多个杂原子的六元杂环 (如嘧啶等);以及稠杂环(如喹啉、嘌呤等)。
N
杂环
苯稠杂环:
稠杂环
杂稠杂环:
二、命名 命名原则:译音+“口”旁
4
5
3(b)
4 5 1
3 2
4
3
4
5
O
呋喃 furan
3
1
2(a)
5
1
2
N3 S
1 2
S
噻吩 thiophene 吡咯 pirrole
3 1 2
五 元 杂 环
噻唑 thiazole
4
4 5
2
1
5
4 5
N3
O
1 2
咪唑 Imidazole
一、吡啶(C5H5N) 吡啶存在于煤焦油、骨焦油中,其衍生物广泛 存在于自然界。工业上主要从煤焦油的轻油部分提 取吡啶。 吡啶是具有特殊臭味的无色液体,bp115.5℃, 可与水、乙醇、乙醚等混溶。
有机化学杂环化合物

呋喃、噻吩和吡咯的原子轨道示意图:
. .. O .. .. S .. . . . . . . .
.
..
O
..
.
..
S
..
.
..
N H
.
..
N H
芳香性大小: 苯>噻吩>吡咯>呋喃
呋喃、噻吩和吡咯的结构
N ..
吡啶中氮原子采取不等性sp2杂化:
p N sp 2 p 结果是: sp 2 N
p轨道与环平面垂 直,相互重叠形 成六个原子在内 的闭合共轭体系
17 杂环化合物
(Heterocyclic Compounds)
基本内容和重点要求
杂环化合物的分类和命名;
杂环化合物的结构和芳香性;
杂环化合物的化学性质;
生物碱
重点要求掌握芳香性;五元、六元杂环化合物 的化学性质,杂环化合物的亲电取代反应的活性及 规律;酸碱性规律。
17 杂环化合物
17.1 杂环化合物的分类和命名
N O SO3 O SO3H
N N H
H2SO4 S 30℃
SO3 N H SO3H
S
SO3H
吡啶与硝基苯相似,亲电取代比苯困难, 并且主要发生在β位上,反应条件要求较高。
¡¡ + Br2
300 C Ò É Ô Ï
¡
Br N
N N N
å ú Á ¤ b-ä ´ ß à
+ H2SO4 + » Ë ì á
. . .
. .
.
N
..
未共用电子对占据 sp2杂化轨道,与 环共平面,不能参 与环系的共轭
吡啶的结构
有机化学-胺与杂环化合物
第十章:含氮有机化合物
前 言
胺和杂环化合物是两类极其重要的有机含氮化合物:
A:蛋白质的基础物质——氨基酸
B:治疗和控制精神病患者情绪的药物——胺的衍生物
C:储存和传递遗传信息、控制蛋白质合成功能的核酸
D:抗菌消炎的磺胺药物
第十四章:胺和杂环化合物
一、胺的分类和结构
第一节: 胺 类
第一节: 胺 类
四、胺的化学性质
碱性与成盐
B:成 盐:
由于胺具有碱性,不管是否易溶于水,均能定量 地与无机酸反应形成盐。
+ HCI
R — NH3CI
+
R — NH2
:
-
NaOH
R — NH2
:
利用胺的碱性与成盐的性质,可以分离、纯化胺与非碱性化合物的混合物。
NH3
..
H
H
H
112.9°
CH3NH2
..
H
CH3
H
N原子采用sp3不等性杂化成键
NH3 结 构
CH3—NH2 结 构
二、胺的命名
(1)烃基较简单,以胺为母体,烃基作为取代基
二乙胺
N,N-二甲基苯胺
对苯二胺
(2)复杂的胺以烃为母体,氨基作为取代基
2,4-二甲基-2-氨基-3-甲氨基戊烷
四、胺的化学性质
碱性与成盐
A:碱 性:
季铵碱 > 脂肪胺 > NH3 > 芳香胺
H
H
N
H
H
:
R — NH2
+ H2O
R — NH3
+
+ OH—
:
p -π共轭体系的形成,使胺基上的N的电子云向苯环离域化,电子云的密度降低,接受H + 的能力下降 .碱性降低。
杂环化合物

N
N
Br2 300 oC
Br N
β-溴吡啶 溴吡啶 β-吡啶磺酸 吡啶磺酸
H2SO4, SO3 230 oC, 24 h
KNO3 + H2SO4 Fe, 300 oC
SO3H N
NO2 β-硝基吡啶 硝基吡啶 N
N
亲电取代反应为什么主要发生在β 位上? 亲电取代反应为什么主要发生在β-位上?
如果取代在 a 位
4 5
CH3
1-甲基吡唑 甲基吡唑
S
1
CH3 6
CH3 4 5 N3 N 2
1
4-甲基咪唑 甲基咪唑
5-甲基噻唑 甲基噻唑
4-甲基嘧啶 甲基嘧啶
3. 具有特定名称的稠杂环的编号一般和稠环芳烃相同, 具有特定名称的稠杂环的编号一般和稠环芳烃相同 但少数有例外(比如 嘌呤) 但少数有例外 比如 嘌呤
5 6 7 8 4 8 3 2 7 6 5 9 1 2 3 4
N H H
反 发 无 应 生
浓 H2SO4 / HgSO4 N 220oC Br2 / 浮 石 300oC N N
SO3H
Br
环上有给电子基时反应相对较易进行
4 芳环上的亲核取代反应
亲核取代比苯容易,主要发生在 位上 位上。 亲核取代比苯容易,主要发生在α位上。 比苯容易
PhLi N O2 or PhNO2, 化 (氧 ) N Ph
(3)周边编号的方法 (3)周边编号的方法 为表明取代基的位置,还需要对稠杂环的周边给与编号, 为表明取代基的位置,还需要对稠杂环的周边给与编号, 编号原则是基本环用英文字母编号,附加环要用数字编号。 编号原则是基本环用英文字母编号,附加环要用数字编号。
然后对稠杂环进行整体编号,共用碳原子不参与编号, 然后对稠杂环进行整体编号,共用碳原子不参与编号, 共用杂原子参与编号。 共用杂原子参与编号。
杂环化合物
C H3 HO C HC H2 2
4 5
N3 S
1 2
O 4 - 硝基噁唑
4 - 甲基 - 5 - ( 2' -羟乙基 ) 噻唑
C. 稠杂环有特定的母体和固定的编号
嘌呤 (purine)
D.如果接有 —SO3H、—COOH、—NH2、 —CHO等基团时,杂环为取代基。
COOH CHO N
3-吡 啶甲 酸
等电子体系
N
未参与共轭
N
吡啶电子结构与吡咯不同:
N H
N
2.物理性质
氮原子的电负性较大,使吡啶有较大极性,其偶极距数值较大.
=2.20D
=1.17D
吡啶能与水以任意比例混溶,又能溶解大多数极 性或非极性有机化合物,甚至许多无机盐类,是一个 良好的溶剂。
3.化学性质
γ
δ δ δ δ δ
β α
O
HO CHO O
NaOH
O C O
KCN
CH O
CHO O
O
CH2OH
+
COOH O
HOOCCH2CH2 N H
CH2COOH CH2NH2
卟吩胆色素原:通过生物体内特定酶的作用可转变成 卟啉、叶绿素和维生素B12等重要生物活性物质.
CH2COOH N H
3-吲哚乙酸(植物生长促进剂)
OH N C2H5 N H H3COOC H3CO H N C2H5 N R HO OCOCH3 COOCH3
O
2-呋 喃甲 醛
二、五元杂环化合物
1. 结构与芳香性
(1)呋喃、吡咯和噻吩的结构
C C N C H
C C C O C
杂原子均以sp2 杂化(未杂化 的P上有2个电 子参加成环)
第10章 其他类有机化合物简介

1 2
3 4
碳水化合物的结构和分类 单糖
低聚糖 多糖
有机化学
一、碳水化合物的结构和分类
1. 碳水化合物的结构
从化学结构上看,碳水化合物是多羟基醛、多羟基酮, 或者是能水解成多羟基醛或多羟基酮的化合物,即分子中含 有下列结构:
2. 碳水化合物的分类
碳水化合物一般根据它能否水解,以及水解后的产物可
分为三大类。 ①单糖 ②低聚糖
葡萄糖是醛糖,分子中含醛基,所以有醛基的化学性质,
易发生氧化反应和还原反应等。
有机化学
二、单糖
(3)葡萄糖的制法和用途 2. 果糖 (1)果糖的来源和结构
(2)果糖的性质和用途 果糖可用作食物、营养剂和防腐剂。它在人体内极 易转变为葡萄糖,在食品工业中也可作调味剂。
有机化学
三、低聚糖
1. 蔗糖
蔗糖是自然界中分布最广的二糖,它广泛存在于植 物的茎、叶、根、种子和果实内,其中以甘蔗和甜菜含 量最多,故称为蔗糖或甜菜糖。 2. 麦芽糖
纤维素是自然界中分布最广、含量最丰富的有机高分子
多糖类化合物。它们是构成植物细胞壁的主要成分,也是构 成植物基干的基础。
有机化学
第三节 高分子化合物
1 2
3 4
概述 高分子化合物的结构和特性
高分子化合物的合成 合成高分子材料
有机化学
一、概述
1. 高分子化合物的含义 高分子化合物实际上是由许多链节结构相同而聚合度不同
有机化学
四、合成高分子材料
高分子合成材料主要指塑料、合成纤维、合成橡胶三大合
成材料及涂料、黏合剂、离子交换树脂等。这些新型的合成材
料,一般具有密度小、强度高、弹性好,可塑性、绝缘性和耐 腐性好等特点,是一般天然材料所没有的,所以在工业、农业 、航空、医疗卫生以及人民日常生活等方面都有广泛的应用。 1. 塑料 以合成的或天然的高分子化合物为基本成分,在加工过程 中可塑制成型,而产品最后能保持形状不变的材料。多数塑料
3 4
碳水化合物的结构和分类 单糖
低聚糖 多糖
有机化学
一、碳水化合物的结构和分类
1. 碳水化合物的结构
从化学结构上看,碳水化合物是多羟基醛、多羟基酮, 或者是能水解成多羟基醛或多羟基酮的化合物,即分子中含 有下列结构:
2. 碳水化合物的分类
碳水化合物一般根据它能否水解,以及水解后的产物可
分为三大类。 ①单糖 ②低聚糖
葡萄糖是醛糖,分子中含醛基,所以有醛基的化学性质,
易发生氧化反应和还原反应等。
有机化学
二、单糖
(3)葡萄糖的制法和用途 2. 果糖 (1)果糖的来源和结构
(2)果糖的性质和用途 果糖可用作食物、营养剂和防腐剂。它在人体内极 易转变为葡萄糖,在食品工业中也可作调味剂。
有机化学
三、低聚糖
1. 蔗糖
蔗糖是自然界中分布最广的二糖,它广泛存在于植 物的茎、叶、根、种子和果实内,其中以甘蔗和甜菜含 量最多,故称为蔗糖或甜菜糖。 2. 麦芽糖
纤维素是自然界中分布最广、含量最丰富的有机高分子
多糖类化合物。它们是构成植物细胞壁的主要成分,也是构 成植物基干的基础。
有机化学
第三节 高分子化合物
1 2
3 4
概述 高分子化合物的结构和特性
高分子化合物的合成 合成高分子材料
有机化学
一、概述
1. 高分子化合物的含义 高分子化合物实际上是由许多链节结构相同而聚合度不同
有机化学
四、合成高分子材料
高分子合成材料主要指塑料、合成纤维、合成橡胶三大合
成材料及涂料、黏合剂、离子交换树脂等。这些新型的合成材
料,一般具有密度小、强度高、弹性好,可塑性、绝缘性和耐 腐性好等特点,是一般天然材料所没有的,所以在工业、农业 、航空、医疗卫生以及人民日常生活等方面都有广泛的应用。 1. 塑料 以合成的或天然的高分子化合物为基本成分,在加工过程 中可塑制成型,而产品最后能保持形状不变的材料。多数塑料
电子教案与课件:有机化学B幻灯片 第十章杂环化合物

• 1. 萃取 • 将滤纸做成与提取器大小相适应的套袋。称取10g茶
叶,略加粉碎,装入纸袋中,上下端封好,装入脂肪 提取器中(装置如图10-1),圆底烧瓶中加入60ml氯 仿,几粒沸石,用水浴加热,连续提取8~10次(提 取时,溶剂蒸汽从导气管上升到冷凝管中,被冷凝成 液体后,滴入提取器中,萃取出茶叶中的可溶物,此 时溶液呈深草青色,当液面上升到与虹吸管一样高时 ,提取液就从虹吸管流入烧瓶中,这为一次虹吸)。 茶叶每次都能被纯粹的溶剂所萃取,使茶叶中的可溶 物质富集于烧瓶中。待提取器中的溶剂基本上呈无色 或微呈青绿色时(一般8~10次),可以停止提取, 但必须待提取器中的提取液刚刚虹吸下去后,方可停 止加热。
• 含结晶水的咖啡因系无色针状结晶,味苦,能溶于水 、乙醇、氯仿等。在100℃时即失去结晶水,并开始升 华,120℃时升华相当显著,至178℃时升华很快。无 水咖啡因的熔点为234.5℃。
H
N
N
N
N
嘌呤
O H3C N
CH3 N
O
N
N
CH3 咖啡因
升华
• 升华是纯化固体有机物的方法之一。
• 某些物质在固态时有相当高的蒸气压,当加热 时不经进液态而直接气化,蒸气遇次则凝结成 固体,这个过程叫做升华。
• 2. 茶叶袋的上下端也要包严,防止茶叶沫漏出,堵 塞虹吸管
• 3. 升华一步,一定要小火加热,慢慢升温,最好是 酒精灯的火焰尖刚好接触石棉网,徐徐加热10-15分 钟。如果火焰太大,加热太快,滤纸和咖啡因都会炭 化变黑;如果火焰太小,升温太慢,会浪费时间,在 部分咖啡因还没有升华,影响收率
【实验步骤】
• 伍德沃德1917年4月10日生于美国马萨诸塞州的波士顿 。从小喜读书,善思考,学习成绩优异。1933年夏,只 有16岁的伍德沃德就以优异的成绩,考入美国的著名大 学麻省理工学院。在全班学生中,他是年龄最小的一个 ,素有“神童”之称,学校为了培养他,为他一人单独 安排了许多课程。他聪颖过人,只用了3年时间就学完 了大学的全部课程,并以出色的成绩获得了学士学位。 伍德沃德获学士学位后,直接攻取博士学位,只用了一 年的时间,学完了博士生的所有课程,通过论文答辩获 博士学位。
叶,略加粉碎,装入纸袋中,上下端封好,装入脂肪 提取器中(装置如图10-1),圆底烧瓶中加入60ml氯 仿,几粒沸石,用水浴加热,连续提取8~10次(提 取时,溶剂蒸汽从导气管上升到冷凝管中,被冷凝成 液体后,滴入提取器中,萃取出茶叶中的可溶物,此 时溶液呈深草青色,当液面上升到与虹吸管一样高时 ,提取液就从虹吸管流入烧瓶中,这为一次虹吸)。 茶叶每次都能被纯粹的溶剂所萃取,使茶叶中的可溶 物质富集于烧瓶中。待提取器中的溶剂基本上呈无色 或微呈青绿色时(一般8~10次),可以停止提取, 但必须待提取器中的提取液刚刚虹吸下去后,方可停 止加热。
• 含结晶水的咖啡因系无色针状结晶,味苦,能溶于水 、乙醇、氯仿等。在100℃时即失去结晶水,并开始升 华,120℃时升华相当显著,至178℃时升华很快。无 水咖啡因的熔点为234.5℃。
H
N
N
N
N
嘌呤
O H3C N
CH3 N
O
N
N
CH3 咖啡因
升华
• 升华是纯化固体有机物的方法之一。
• 某些物质在固态时有相当高的蒸气压,当加热 时不经进液态而直接气化,蒸气遇次则凝结成 固体,这个过程叫做升华。
• 2. 茶叶袋的上下端也要包严,防止茶叶沫漏出,堵 塞虹吸管
• 3. 升华一步,一定要小火加热,慢慢升温,最好是 酒精灯的火焰尖刚好接触石棉网,徐徐加热10-15分 钟。如果火焰太大,加热太快,滤纸和咖啡因都会炭 化变黑;如果火焰太小,升温太慢,会浪费时间,在 部分咖啡因还没有升华,影响收率
【实验步骤】
• 伍德沃德1917年4月10日生于美国马萨诸塞州的波士顿 。从小喜读书,善思考,学习成绩优异。1933年夏,只 有16岁的伍德沃德就以优异的成绩,考入美国的著名大 学麻省理工学院。在全班学生中,他是年龄最小的一个 ,素有“神童”之称,学校为了培养他,为他一人单独 安排了许多课程。他聪颖过人,只用了3年时间就学完 了大学的全部课程,并以出色的成绩获得了学士学位。 伍德沃德获学士学位后,直接攻取博士学位,只用了一 年的时间,学完了博士生的所有课程,通过论文答辩获 博士学位。
【有机化学】杂环化合物

呋喃、噻吩的酰化反应在-C上发生,而吡咯的酰化反 应(不用催化剂)既能在 -C上发生,又能在N上发生。
(6) 呋喃、噻吩、吡咯的傅氏烷基化反应
总体看,在合成上无实用价值。
+ CH2O + HCl S
ZnCl2 0℃
CH2O + HCl ZnCl2, 25oC
ClH2C S
CH2Cl S CH2Cl
2.环的稳定性顺序 (根据离域能的大小) 苯〉噻吩〉吡咯〉呋喃 150 122 90 68
遇氧化剂或酸不稳定
3 吡咯的反应
NBS
N H
HNO 3, ( CH3C O )2O N H
N , SO3 N H
DMF, PO Cl3 N H
Br N H
NO 2 N H
SO 3H N H
C HO N H
+C 6H5N2+C l-
5
1
N H
2α
吡咯(pyrrole)
4
5
3
6 7
2 N H1
苯并吡咯
吲哚 (indole)
四 六元杂环化合物的命名
六元杂环
γ 4
5
3β
6 N 2α 1
吡啶(pyridine)
4
5
3
6
N2
N
1
哒嗪(pyridazine)
γ 4
5
3β
6 O 2α 1
O
4
5
3
6O 2 1
4
5
3
6
2
OO
1
吡喃(pyran) γ-吡喃酮
HNO 2
RO
Zn - HOAc
RO
EtOOC
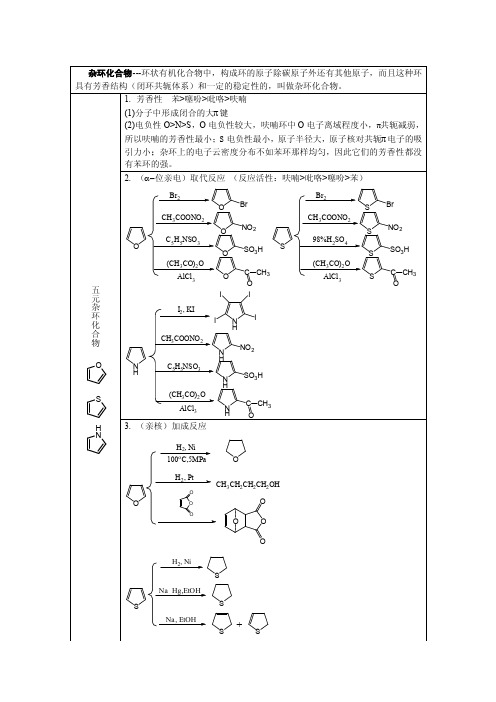
杂环化合物总结
NO2
N
SO3H Br
Br2 H2SO4
+
N
N
Br
KNH2 NH3a, EtOH
N
H
S
S
Na, EtOH
+
S
S
Zn, HAc
N
H2, Ni
H
4. 吡咯的酸碱性
+
N
N
H2, Ni 200oC
N
H
H
H
RMgX
CH3I
N
RH
N
MgXI
N
H
MgX
CH3
KOH,
(1)CO2
(2)H2O
N COOH
N
CO2
K
H O
N H
C OK H3O
N COOH H
C6H5COCl
N O C C6H5
5. 鉴别 呋喃蒸汽遇到被盐酸浸湿过的松木片时,即呈现绿色
噻吩在浓硫酸的存在下,与靛红一同加热显示蓝色
吡咯的蒸汽或其醇溶液,能使进过浓盐酸的松木片变成红色
1. 碱性 (CH3)3N>吡啶>苯胺>吡咯
CH3
+ CH3I
N
280 290oC
+
NI CH3
N CH3 HI
N HI
2. 对氧化作用稳定,氧化侧链
CH2CH3 O
COOH
六
N
N
元 杂
3. 亲电取代,在位,不发生酰基化,烷基化反应
环
Br
化
Br2
合 物
N
N SO3H
H2SO4
N
N
NO2
H2SO4 HNO3 N
杂环化合物和生物碱-有机化学

溶解1份吡咯、呋喃及噻吩,分别需要17、 35、700份的水。 当五元杂环上连有羟基时,溶解度增大。
如: O
H3C O OH
S
S
OH
(1:35)
(1:20)
(1:700)
(1:16)
3. 杂环化合物的化学性质 (1)、亲电取代反 应
N H O S
HNO3
I2 NaOH
吡咯、呋喃、噻吩 α位取代
I
第四节 稠杂环化合物
稠杂环化合物是指苯环与杂环稠合或杂环与杂环稠合在一起的化 合物。常见的有喹啉、吲哚和嘌呤。
泳衣品牌
3 2 d ★ c
N
a b
N
1
N
★ b 2 a 3
N1
S
N
吡啶并[2,3-d]嘧啶
咪唑并[2,1-b] 噻唑
第二节
五元杂环化合物
五元杂环化合物包括含有1个杂原子的五元杂 环和含2个杂原子的五元杂环。 一、含1个杂原子的五元杂环化合物 1.结构
4 5 1N 3 2
4 5 3 2 4 5 3 2
OH
2.亲电取代反应
Cl2, AlCl 3 100 ℃ Br2, 浮石催化 300 ℃ 气相
Cl
3 氯吡啶
N
Br
3 溴吡啶
N
NO2
N
浓 H2SO4 HgSO4 催化, ℃ 220 混酸 300 ℃
3 硝基吡啶
N
SO3H
吡啶 3 磺酸
N
3.氧化还原反应
(1)氧化反应
COOH N β 吡啶甲酸(烟酸) HNO 3 N COOH N α 吡啶甲酸
由于吡啶环的N上在环外有一孤对电子,故吡啶环上的电荷分布不均。
第十章杂环化合物

O
O O
O
H
H
H
H
O OH2
O HO
H O
O
OO
催化加氢:
H2, Ni
O
O THF
四氢呋喃(THF),bp 67℃ ,性质与乙醚相似, 是重要的化学溶剂。
2、糠醛
糠醛的化学性质与苯甲醛相似。可以发生交叉 羟醛缩合反应、Cannizzaro反应、Perkin反应。
dil.NaOH
O
CHO CH3CHO
mp26℃,bp 243℃。难溶于水,易溶于有机溶剂。
N
喹啉
N
异喹啉
来源: 煤焦油和骨油。
制备: Skraup合成法
CH2OH CHOH CH2OH
H2SO4 2H2O
CHO CH C6H5NH2
CH2
C6H5NO2
N
H2SO4
H2O
N H
H C O CH2
CH2 NH
H HO C
CH CH2 NH
五元杂环化合物亲电取代活性顺序: 吡咯>呋喃>噻吩>苯
三、六元杂环化合物的性质
六元杂环化合物发生亲电取代反应主要在β-位。 可以从反应中间体的稳定性给予说明。
α位
E
N
β位
H NE
H E
N
H N
E
H NE
H 不稳定共H振结 构式
E
E
N
N
1、吡啶
吡啶有特殊臭味的无
色液体,bp 115℃,可与
N
水、乙醇、乙醚等混溶。
N
PCl3
NO2 N
HNO3
N
H2SO4
O
NO2
N O
O O
O
H
H
H
H
O OH2
O HO
H O
O
OO
催化加氢:
H2, Ni
O
O THF
四氢呋喃(THF),bp 67℃ ,性质与乙醚相似, 是重要的化学溶剂。
2、糠醛
糠醛的化学性质与苯甲醛相似。可以发生交叉 羟醛缩合反应、Cannizzaro反应、Perkin反应。
dil.NaOH
O
CHO CH3CHO
mp26℃,bp 243℃。难溶于水,易溶于有机溶剂。
N
喹啉
N
异喹啉
来源: 煤焦油和骨油。
制备: Skraup合成法
CH2OH CHOH CH2OH
H2SO4 2H2O
CHO CH C6H5NH2
CH2
C6H5NO2
N
H2SO4
H2O
N H
H C O CH2
CH2 NH
H HO C
CH CH2 NH
五元杂环化合物亲电取代活性顺序: 吡咯>呋喃>噻吩>苯
三、六元杂环化合物的性质
六元杂环化合物发生亲电取代反应主要在β-位。 可以从反应中间体的稳定性给予说明。
α位
E
N
β位
H NE
H E
N
H N
E
H NE
H 不稳定共H振结 构式
E
E
N
N
1、吡啶
吡啶有特殊臭味的无
色液体,bp 115℃,可与
N
水、乙醇、乙醚等混溶。
N
PCl3
NO2 N
HNO3
N
H2SO4
O
NO2
N O
含氮有机化合物和杂环

NO2
Fe / HCl 或Sn / HCl
NH2
12
2. 腈和酰胺的还原
RCN
H2 / Pt LiAlH4
RCH2NH2
O H3C C NH 2
H2/Ni
CH3CH2NH2
13
3. Hofmann降解反应
O R C NH2
Br2 / NaOH or Cl2 / NaOH
RNH2 + NaBr + Na2CO3
O
CH3CCl
NO 2
NHCOCH 3
HNO3 / H2SO4
NHCOCH 3
H2O / OH-
NH 2
NO 2
NO 2
21
4. 与亚硝酸反应
拓展
亚硝酸钠
亚硝酸钠是一种有毒的氧化剂,大量进入血液
后,将血红蛋白中的二价铁氧化为三价铁,形成高 铁血红蛋白血症,失去携氧能力,造成机体组织细 胞缺氧症状,严重影响中枢神经系统,可引起呼吸 困难、循环衰竭。在腌咸肉或加工熟食卤味时,有 时为了使肉色鲜红而加入亚硝酸盐,如加入过量, 同样会引起中毒。另外,食用富含亚硝酸盐的食物 还与一些肿瘤发生有关。据调查发现,食管癌高发 区居民食腌菜者较普遍,食管癌的发病率与食腌菜 量相关,在这些腌制的咸菜中含有大量的亚硝酸盐。
第十章 含氮有机化合物
1
胺
含
氮 重氮化合物、偶氮化合物
有
机 酰胺
化
合 物
含氮杂环
生物碱
2
第一节 胺 一. 胺的分类和命名
1.分类
3
名称 伯胺 仲胺 叔胺 季铵盐 季铵碱
分子式
RNH2 R2NH R3N R4N+XR4N+OH-
杂环化合物

噻吩
噻唑
N
N H
吡咯
N
N H
咪唑
N H
N
吡唑
六元杂环
N
吡啶
N
嘧啶
O
吡喃(无芳香性)
苯并杂环
N N
N H
N N H
吲哚
N
喹啉
N
异喹啉
杂环并杂环
嘌呤
记 忆 口 诀:
氮五吡咯六吡啶;
间氮咪唑和嘧啶; 吲哚喹啉左并苯; 嘧咪相稠是嘌呤。
指出下列杂环化合物中,各含有哪些 杂环母核?
NH N N N H CH2 N
属于富电子结构 结构决定性质,五元杂化富电子结 构会决定它们与苯环哪些性质上的 不同呢?
三.化学性质—3.亲电取代反应 重点
亲电取代活性与环上电子云密度有关—— 电子云密度越大,带正电的亲电试剂的进 攻越容易。 *1 亲电取代反应的活性顺序为:
N H
>
O
>
S
>
吸电子诱导:O(3.5) > N(3.0) > S(2.6) 给电子共轭:N > O > S 综合:N贡献电子最多,O其次,S最少
*2 杂原子和取代基的定位效应
A 杂原子的定位效应:邻位
取代反应主要发生在α-C 上
B 取代基的定位效应:以噻吩为例:
(1) α- 位上有取代基
X = o、 p - 定位基
3 5
Y = m - 定位基 (主) (次)
5 4
(次 ) X
(主 )
S
S
Y
(2) β- 位上有取代基
X = o、 p - 定位基 X (次)
黄连素(小檗碱)是喹啉类生物碱,存在于黄连、黄柏和三颗针等植物
第十章 胺及杂环化合物
胺 amines
胺可以看作氨 (NH3) 的烃基衍生物,是生物界 最丰富的一类化合物
Viagra ®
(普鲁卡因)
胺对有机化学家来说同样是重要的一类化合物
10.1.1 胺的分类和命名
胺的分类
氨 (NH3,ammonia) 的一个或多个氢被烃基取 代所得到的化合物称为胺 (amine)
(氨)
(吗啡)
(阿托品)
大多数生物碱都是 氨基酸的代谢产物
大多数生物碱都具有显著的生物活性
(抗痉挛药)
Atroperum
(颠茄)
(罂粟)
Cinchona ledgeriana
(金鸡纳树)
(抗疟疾药)
Lycoris radiata
(石蒜)
(抗重症肌无力药)
脂肪胺 叔胺 > 仲胺 > 伯胺 > NH3 > 苯胺 酰胺
溶剂化效应
溶剂与溶解于其中的分子 或离子之间的相互作用称 为溶剂化效应
氢键
R
+
N
H H H
:OH2 :OH2 :OH2
--- 共轭酸 (铵正离子) 的稳定性
伯胺 > 仲胺 > 叔胺
空间效应
氮原子上连接的烃基对氮原子上孤对电子的屏蔽作用 烃基的数目越多或体积增大,胺的碱性降低
碱性
氮原子上的孤对电子 没有参与大 p 键的形 成,有一定的自由度
吡啶的碱性弱于氨/胺 (sp3),这是因为sp2杂化 轨道上s成分较多,距核较近,因而该氮原子 孤对电子受核束缚较强 吡啶碱性强于苯胺
吡啶的反应
• 亲电取代反应
活性比苯低,较难反应
取代基多进入b位 (3位)
• 还原反应 (比苯易还原)
NH2
CH3CH2NH2
大学有机化学课件-杂环化合物

(糠醛)
β —CHO
γ 4 5 6
3β 2α
COOH
1 吡啶—3—甲酸 (尼古丁酸 —吡啶甲酸 或烟酸)
N
CH3
4 5
3 N
Br
2
4 5
N S1
2
3
N1 H
5—甲基咪唑
4—溴噻唑
9
稠杂环化合物(P232)
5 6 7 8 N 1 4 3 2
6 7 8 1 5 4 3
N2
喹啉 (quinoline)
糠醛是不具α—氢的芳醛,能进行类似于苯甲 醛的反应。
NaOH
__
O
CH2OH
+
O
__
COONa
O
2
O
__
CHO
康尼查罗反应
OH KCN 乙醇
__
CH___ C___
O
O
安息香缩合反应
O CH3COONa CHO + (CH3CO)2O 150C CH=CHCOOH O
30
普尔金反应
O
CH3COONa CHO + (CH3CO)2O 150C
4β 5α
O 1
β 3 α2
4β 5α
β 3
4β 5α
β 3 α2
呋喃(furan)
1 α2 N H
吡咯(pyrrole)
S 1 噻吩(thiophene)
唑的命名 含有两个或两个以上杂原子的五元杂环,若至少有 一个杂原子是氮时,则该杂环化合物称为唑。
4 5 N H1 3 N2
5 4 N3 2
4 5
N H
>
O
>
S
>
>
12
β —CHO
γ 4 5 6
3β 2α
COOH
1 吡啶—3—甲酸 (尼古丁酸 —吡啶甲酸 或烟酸)
N
CH3
4 5
3 N
Br
2
4 5
N S1
2
3
N1 H
5—甲基咪唑
4—溴噻唑
9
稠杂环化合物(P232)
5 6 7 8 N 1 4 3 2
6 7 8 1 5 4 3
N2
喹啉 (quinoline)
糠醛是不具α—氢的芳醛,能进行类似于苯甲 醛的反应。
NaOH
__
O
CH2OH
+
O
__
COONa
O
2
O
__
CHO
康尼查罗反应
OH KCN 乙醇
__
CH___ C___
O
O
安息香缩合反应
O CH3COONa CHO + (CH3CO)2O 150C CH=CHCOOH O
30
普尔金反应
O
CH3COONa CHO + (CH3CO)2O 150C
4β 5α
O 1
β 3 α2
4β 5α
β 3
4β 5α
β 3 α2
呋喃(furan)
1 α2 N H
吡咯(pyrrole)
S 1 噻吩(thiophene)
唑的命名 含有两个或两个以上杂原子的五元杂环,若至少有 一个杂原子是氮时,则该杂环化合物称为唑。
4 5 N H1 3 N2
5 4 N3 2
4 5
N H
>
O
>
S
>
>
12
有机化学复习-杂环化合物

N + SO3 CH2Cl2
N SO3
(2)吡啶的亲核性 吡啶的烷基化
N + CH3I
+ N CH3
I
N甲基吡啶盐 • N-甲基吡啶盐的重排
NaOH 300 C I 重排
o
+ N CH3
N H CH3
I CH3
N CH3 NaOH
CH3
I N H N
2) 亲电取代反应
取代位置和反应活性
PhN2 X N H
N H
N N Ph
环上已有取代基对亲电取代取向的影响
Electron Donating Group
E
A EDG
+ p
E
A
EDG
HNO3//Ac Ac2O O HNO 3 2 CH S S CH3 3 (AcONO2)) (AcONO 2 O O2N N
2
S S 70%
NO2
S 85%
NO S2
85%
+ + O N NO2 2
S O2 N
NO S 2
E
A
EWG
15% 15%
EWG
EWG
E
+ m
COOH COOH
Br2 Br 2 CHCOOH COOH CH 33 Br Br SS
COOH COOH
A
E
A
SS
2)五员芳杂环的其它反应
(i)还原成饱和杂环化合物(催化氢化)
5 4 4 3 3 65 7 6 8 7
4
2
6 7
3
5N 6
77
O21 N1
N SO3
(2)吡啶的亲核性 吡啶的烷基化
N + CH3I
+ N CH3
I
N甲基吡啶盐 • N-甲基吡啶盐的重排
NaOH 300 C I 重排
o
+ N CH3
N H CH3
I CH3
N CH3 NaOH
CH3
I N H N
2) 亲电取代反应
取代位置和反应活性
PhN2 X N H
N H
N N Ph
环上已有取代基对亲电取代取向的影响
Electron Donating Group
E
A EDG
+ p
E
A
EDG
HNO3//Ac Ac2O O HNO 3 2 CH S S CH3 3 (AcONO2)) (AcONO 2 O O2N N
2
S S 70%
NO2
S 85%
NO S2
85%
+ + O N NO2 2
S O2 N
NO S 2
E
A
EWG
15% 15%
EWG
EWG
E
+ m
COOH COOH
Br2 Br 2 CHCOOH COOH CH 33 Br Br SS
COOH COOH
A
E
A
SS
2)五员芳杂环的其它反应
(i)还原成饱和杂环化合物(催化氢化)
5 4 4 3 3 65 7 6 8 7
4
2
6 7
3
5N 6
77
O21 N1
1 杂环化合物的结构

• 2.1 Hantzsch-Widman 命名法 • 杂原子的种类 • 杂原子的种类用表1中列出的词头来表示。 在命名时,表中列出的杂原子词头次序应 遵从后者优先的原则。
杂原子
词头 (prefix)
杂原子
词头 (prefix)
O
S Se Te N P
噁,氧杂 (oxa)
噻,硫杂 (thia) 硒杂 (selena) 碲杂 (tellura) 吖,氮杂 (aza) 磷杂 (phospha)
• 在某些情况下,可将杂环作为一个取代基
3-(4-吡啶基)丁酸
3-(4-pyridyl) butyric acid
• 3.三员杂环
3.1 氧杂环丙烷
环氧乙烷的结构:
键的分子轨道模型
反应 异构化成羰基化合物
• 亲核开环反应
• 酸催化水解生成 1,2-二醇
• 还原成醇
• 脱氧成烯
合成 (1)-卤代醇环化脱卤化氢
(2) 烯烃的环氧化
\
烯烃与过氧酸反应生成环氧化物。在 Prileschajew 反 应中,常用的是过氧苯甲酸,间氯过氧苯甲酸或单过氧 邻苯二甲酸。在弱酸性条件下,反应是按协同方式进行 的. 过氧酸具有很强的分子内氢键,协同反应是立体选择性 的,(Z)-式烯烃生成 cis-环氧化物,(E)-式烯烃生成 trans-环氧化物。
苯并[b]呋喃 (benzo [b] furan)
呋喃
(furan)
• 若双环和多环体系需要看作整体来编号时,不需 考虑各组分独立的编号,其编号方法是: • 将环系按下列规则放在直角坐标系上:1)使尽可 能多的环放在横坐标上;2)使环中最大的编号在 纵坐标的最上边。 • 体系按顺时针方向,从离纵坐标尽可能远的,非 参加稠合的原子开始编号;即:右边最上方的原 子,或最右边环中最上边的原子。
杂环化合物

五元杂环 单杂环 六元杂环 杂环化合物 苯环及一个杂环 N 稠杂环 两个杂环 N N H N N N O S
二、命名
杂环化合物的命名常用音译法,按外文名词音译 成带“口”字旁的同音汉字。
N H (pyrrole) 吡咯 N N (pyrimidine) 嘧啶
O (furan) 呋喃
S (thiophene) 噻吩
N H
干乙醚N MgX源自N COR RI N RN H N H
COR
R
N H
+ KOH 固体
热 N K
+ H2O
N H
+ RMgX
N MgX
+ RH
RCOCl N H
KOH(固体) 热
N K
N COR RI N R
N H N H
COR
R
RCOCl
RMgX
N H
干乙醚
N MgX
N COR RI N R
CH3COONO 2 E Ac2O E NO2
(2)、磺化反应
Py / SO 3 E SO3H E + H5C5NH Cl
+ -
SO3 H5C5NH
-
+
HCl
E
(3)、卤化反应
Br2 I2/HgO E Br2 Br Br E E I Br (E=NH) Br (E=O,S) E Br (E=O,S)
N H N H
COR
R
CH3MgI _ CH4
CH3I N MgI RCOCl N K N COR CHO N CH3
K
N H
CHCl 3/KOH N H
+
N2Ar N H
二、命名
杂环化合物的命名常用音译法,按外文名词音译 成带“口”字旁的同音汉字。
N H (pyrrole) 吡咯 N N (pyrimidine) 嘧啶
O (furan) 呋喃
S (thiophene) 噻吩
N H
干乙醚N MgX源自N COR RI N RN H N H
COR
R
N H
+ KOH 固体
热 N K
+ H2O
N H
+ RMgX
N MgX
+ RH
RCOCl N H
KOH(固体) 热
N K
N COR RI N R
N H N H
COR
R
RCOCl
RMgX
N H
干乙醚
N MgX
N COR RI N R
CH3COONO 2 E Ac2O E NO2
(2)、磺化反应
Py / SO 3 E SO3H E + H5C5NH Cl
+ -
SO3 H5C5NH
-
+
HCl
E
(3)、卤化反应
Br2 I2/HgO E Br2 Br Br E E I Br (E=NH) Br (E=O,S) E Br (E=O,S)
N H N H
COR
R
CH3MgI _ CH4
CH3I N MgI RCOCl N K N COR CHO N CH3
K
N H
CHCl 3/KOH N H
+
N2Ar N H
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大连民族学院
②其它亲电取代反应:
Friedel-Crafts 反应
无反应发生
浓 H2SO4 / HgSO4
SO3H
N
220oC
N
Br2 / 浮石
Br
300oC
N
③环上有给电子基时反应易于发生:
Jutao LIU
有机化学
大连民族学院
(3) 亲核取代反应 取代主要发生在α位。
PhLi N
O2 or PhNO2, (氧化)
子结合或给出电子,显弱碱性。利用它的碱性,可从混
合物中分离吡啶类化合物,在化学反应中还可用作催化
剂和除酸剂。 4. 化学反应 (1) 氮原子上的反应
+ HCl N
N HCl NH3 N
N
+ SO3 CH2Cl2 室温
N SO3 (90%)
吡啶三氧化硫络合物
是常用的缓和磺化剂
此反应常用于 在反应中吸收 生成的气态酸
Jutao LIU
有机化学
大连民族学院
4
5
N3
6
2
N
1
嘧啶(pyrimidine)
4 5N3
6
2
N
1
吡嗪(pyrazine)
5 6
7 8
4 3
2 N 1
喹啉 (quinoline)
5 6
4 3
7 8
N2 1
异喹啉 (isoquinoline)
67
1N 5 N
8
2
N4 3
N H
9
嘌呤(purine)
大连民族学院
第十章 杂环化合物
Chapter 10. Heterocyclic compounds
Jutao LIU
O
S
有机化学
N H
第三十一次课
大连民族学院
主要内容
第一节 杂环化合物的分类和命名 第二节 六元杂环 第三节 五元杂环
Jutao LIU
有机化学
大连民族学院
第一节 杂环化合物的分类和命名
Jutao LIU
有机化学
大连民族学院
①钝化和 β-亲电取代:
发烟 HNO3 / 发烟 H2SO4
无反应发生
N
发烟 HNO3 / 发烟 H2SO4
起吸电子基作用
300oC / 24h
NO2 N
取代在 位
N(CH3)3
发烟 HNO3 / 发烟 H2SO4
Jutao LIU
有机化学
NO2 N(CH3)3
Jutao LIU
有机化学
大连民族学院
2. 物理性质 氮原子的电负性较大,使吡啶有较大极性,其偶极
距数值较大。
N
=2.20D 吡啶能与水以任意比例混溶,又能溶解大多数极 性或非极性有机化合物,甚至许多无机盐类,是一个良 好的溶剂。
Jutao LIU
有机化学
大连民族学院
3. 碱性
吡啶N是sp2杂化,孤电子对不参与共轭,可以与质
五元杂环
呋喃
O
N
噁唑
O
噻吩
S
N
噻唑
S
N 吡咯
H N
咪唑
N H
N 吡唑
N H
六元杂环
吡啶
N
N 嘧啶
吡喃(无芳香性)
N
O
苯并杂环 杂环并杂环
吲哚
N H
N
N
N
N H
嘌呤
喹啉
N
N 异喹啉
Jutao LIU
有机化学
大连民族学院
二、命名
命名原则: 杂环的命名常用音译法,即按外文名音译成带“口” 字旁的同音汉字。 当环上有取代基时,取代基的位次从杂原子算起依次用 1,2,3,… (或α,β,γ…)编号。 如杂环上含不止一个杂原子时,则按O、S、N顺序依次 编号。编号时杂原子的位次数字之和应最小。
吡咯 结构:吡咯N是sp2杂化,孤电子对参与共轭。 反应:碱性较弱,环易发生亲电取代反应,环上相当
有一个邻对位定位基。
Jutao LIU
有机化学
大连民族学院
呋喃、噻吩、吡咯在结构上具有共同点,即构成环 的五个原子都为sp2杂化,故成环的五个原子处于同一平 面,杂原子上的孤对电子参与共轭形成共轭体系,其π电 子数符合休克尔规则(π 电子数 = 4n+2),所以,它们 都具有芳香性。 2. 物理性质
一、分类
1. 脂杂环 没有芳香特征的杂环化合物称为脂杂环。
三元杂环
O (环氧乙烷)
H
N (氮杂环丙烷)
四元杂环 五元杂环 七元杂环
Jutao LIU
O
(β-丙内酯)
O
O
O
(β-丙内酰胺)
NH
O (顺丁烯二酸酐)
O
(氧杂 )
(1H-氮杂 )
O
N H
有机化学
大连民族学院
2. 芳杂环 具有芳香特征的杂环化合物称为芳杂环。
能溶于有机溶剂,水中溶解度都小于吡啶;溶解度 顺序为:吡咯﹥呋喃﹥噻吩 ;吡咯不但几乎不显碱性, 反而具有弱酸性。
NO H
NO H
NO H
尿嘧啶(U)
胞嘧啶(C)
胸腺嘧啶(T)
Jutao LIU
有机化学
大连民族学院
四、含氧六元杂环
O
吡喃环系
吡喃
O
O
吡喃酮
Jutao LIU
有机化学
大连民族学院
第三节 五元杂环
一、呋喃、噻吩、吡咯
1. 电子结构及芳香性
吡
咯
的
结
N
构
H
N
共轭效应是给电子的。 诱导效应是吸电子的。
孤电子对在p轨道六元杂环
含有两个氮原子的六元杂环体系称作二嗪类,因氮
原子在环中的相对位置不同,二嗪类有三种异构体:哒
嗪、嘧啶、吡嗪。
4
5
3
4
5
N3
4 5N3
6
N2
N
1
哒嗪(pyridazine)
6
2
N
1
嘧啶(pyrimidine)
6
2
N
1
吡嗪(pyrazine)
O NH
NH2 N
O
H3C
NH
Jutao LIU
有机化学
杂环母环实例:
4
3β
5
2α
O
1
呋喃(furan)
4
5
3
6
2
7
N H
1
苯并吡咯
吲哚 (indole)
4
3β
5 S 2α 1
噻吩(thiophene)
γ 4
5
3β
6 N 2α 1
吡啶(pyridine)
大连民族学院
4
3β
5
1
N H
2α
吡咯(pyrrole)
4
5
3
6
N2
N
1
哒嗪(pyridazine)
Jutao LIU
有机化学
大连民族学院
第二节 六元杂环
一、吡啶
1. 电子结构
孤电子对 在sp2杂化 轨道上。
共轭效应和诱导效应都是吸电子的。
结构:吡啶N是sp2杂化,孤电子对不参与共轭。 反应:碱性较强。环不易发生亲电取代反应但易发生亲核
取代反应。发生亲电取代反应时,环上N具有间位 定位基作用。发生亲核取代反应时,环上N具有邻 对位定位基作用。
NaNH2
N
NH3 或 PhNMe2
N
N Ph
+ H2 NH2
Jutao LIU
有机化学
(4) 氧化和还原反应 ①侧链氧化
大连民族学院
Jutao LIU
有机化学
②N氧化 吡啶的类似反应:
大连民族学院
二、喹啉和异喹啉
5 6
4 3
7 8
2
N
1
喹啉
5 6
4 3
7 8
N
2 1
异喹啉
Jutao LIU
有机化学
Jutao LIU
有机化学
大连民族学院
RI N
R
300 ℃
N
NR+ N
RI
I
I
R
OH
NR
OH
N
制取烷基吡啶的一种方法
(2) 亲电取代反应
吡啶环上氮原子为吸电子基,故吡啶环属于缺电子
的芳杂环,和硝基苯相似。其亲电取代反应很不活泼,反
应条件要求很高,不起傅-克烷基化和酰基化反应。亲电 取代 反应主要在β-位上。
