扩散系数计算
扩散系数计算

扩散系数计算WTD standardization office【WTD 5AB- WTDK 08- WTD 2C】扩散系数费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、 气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5210/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即AB BA D D D ==。
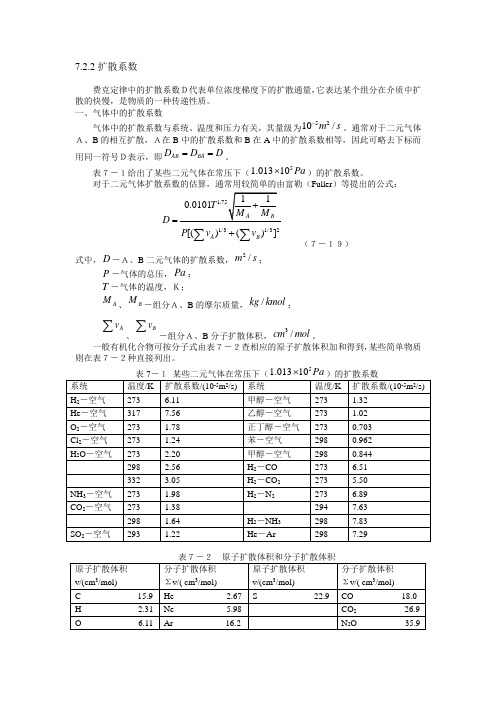
表7-1给出了某些二元气体在常压下(51.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1/31/32[()()]A B D P v v =+∑∑ (7-19)式中,D -A、B 二元气体的扩散系数,2/m s ;P -气体的总压,Pa ;T -气体的温度,K;A M 、B M -组分A、B 的摩尔质量,/kg kmol ;Av∑、Bv∑-组分A、B 分子扩散体积,3/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
51.01310Pa ⨯式7-19的相对误差一般小于10%。
二、 液体中的扩散系数由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得多,其量级为9210/m s -。
表7-3给出了某些溶质在液体溶剂中的扩散系数。
式估算:150.6()7.410T B AB A M TD V -φ=⨯μ 2/m s (7-21)式中,AB D -溶质A在溶剂B中的扩散系数(也称无限稀释扩散系数),2/m s ;T -溶液的温度,K; μ-溶剂B的粘度,.Pa s ;B M -溶剂B的摩尔质量,/kg kmol ;φ-溶剂的缔合参数,具体值为:水;甲醇;乙醇;苯、乙醚等不缔合的溶剂为;A V -溶质A 在正常沸点下的分子体积,3/cm mol ,由正常沸点下的液体密度来计算。
扩散系数计算
7.2.2扩散系数费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5210/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即AB BA D D D ==。
表7-1给出了某些二元气体在常压下(51.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1/31/32[()()]A B D P v v =+∑∑ (7-19)式中,D -A、B 二元气体的扩散系数,2/m s ;P -气体的总压,Pa ; T -气体的温度,K;A M 、B M -组分A、B 的摩尔质量,/kg kmol ;Av∑、Bv∑-组分A、B 分子扩散体积,3/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
51.01310Pa ⨯式7-19的相对误差一般小于10%。
二、液体中的扩散系数由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得多,其量级为9210/m s -。
表7-3给出了某些溶质在液体溶剂中的扩散系数。
对于很稀的非电解质溶液(溶质A+溶剂B),其扩散系数常用Wilke-Chang 公式估算:150.6()7.410T B AB A M TD V -φ=⨯μ 2/m s (7-21)式中,AB D -溶质A在溶剂B中的扩散系数(也称无限稀释扩散系数),2/m s ;T -溶液的温度,K;μ-溶剂B的粘度,.Pa s ;B M -溶剂B的摩尔质量,/kg kmol ;φ-溶剂的缔合参数,具体值为:水2.6;甲醇1.9;乙醇1.5;苯、乙醚等不缔合的溶剂为1.0;A V -溶质A 在正常沸点下的分子体积,3/cm mol ,由正常沸点下的液体密度来计算。
扩散系数计算

它表达某个组分在介质中扩 0.0101T 1.75(7—19)722扩散系数费克定律中的扩散系数D 代表单位浓度梯度下的扩散通量, 散的快慢,是物质的一种传递性质。
一、气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为10 m 2/s 。
通常对于二元气体A 、B 的相互扩散,A 在 B 中的扩散系数和 B 在A 中的扩散系数相等,因此可略去下标而用同一符号D 表示,即 D AB = D BA =D。
表7 — 1给出了某些二元气体在常压下(1.013 105Pa )的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:p[c V A )1/3 e V B )1/3]22式中,D —A 、B 二元气体的扩散系数,m /s ;P —气体的总压,Pa ;T —气体的温度,K ;MA 、MB —组分A 、B 的摩尔质量,kg/kmol ;7 V A 7 V B3、—组分A 、B 分子扩散体积,cm 3/mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
表7-1某些二元气体在常压下(5)的扩散系数系统温度/K 扩散系数/(10-5m 2/s)系统温度/K-5 2扩散系数/(10 m/s)H 2—空气 273 6.11 甲醇一空气 273 1.32 He —空气 317 7.56 乙醇一空气 273 1.0202—空气 273 1.78 正丁醇-空气 273 0.703 Cl 2 —空气 273 1.24 苯-空气 298 0.962 H 2O —空气273 2.20 甲醇一空气298 0.844 298 2.56 H 2— CO 273 6.513323.05 H 2— CO 2 273 5.50 NH 3 —空气 273 1.98H 2— N 2 273 6.89 CO 2 —空气273 1.38294 7.632981.64 H 2— NH 3 298 7.83 SO 2 —空气 2931.22He — Ar2987.297-2 原子扩散体积3v/(cm /mol) 分子扩散体积 3工 V /( cm /mol)原子扩散体积3v/(cm /mol)分子扩散体积3工 V /( cm /mol)C15.9 He 2.67 S22.9CO 18.0,其扩散系数常用 Wilke-Cha ng 公式估算:2 /m/S(7 — 21)AB= 7.4 10‘5(M B )T T 」V A 0.6式7 — 19的相对误差一般小于1 0%。
扩散系数的公式

扩散系数的公式扩散系数(Diffusion coefficient)是描述物质扩散能力的物理量。
一、菲克定律与扩散系数。
1. 菲克第一定律。
- 表达式为J = -D(dc)/(dx),这里J是扩散通量(单位时间内通过单位面积的物质的量),D就是扩散系数,(dc)/(dx)是浓度梯度(沿x方向的浓度变化率)。
- 由该定律可以推导出扩散系数D=(-J)/(frac{dc){dx}}(在已知扩散通量J和浓度梯度(dc)/(dx)的情况下)。
2. 菲克第二定律。
- 表达式为(∂ c)/(∂ t)=Dfrac{∂^2c}{∂ x^2}(在一维扩散情况下),其中c是浓度,t是时间,x是空间坐标。
- 在一些特定的初始条件和边界条件下,通过求解菲克第二定律的方程,可以得到扩散过程中浓度随时间和空间的分布,进而可以确定扩散系数D的值。
例如在简单的扩散问题中,假设扩散物质初始时局限于某一区域,随着时间的推移,根据浓度分布的变化情况来计算D。
- 如果已知浓度c随时间t和空间x的函数关系c(x,t),可以通过对(∂ c)/(∂ t)和frac{∂^2c}{∂ x^2}求导,然后根据菲克第二定律计算D=(frac{∂ c)/(∂ t)}{frac{∂^2c}{∂ x^2}}。
二、爱因斯坦 - 斯托克斯方程(适用于稀溶液中的球形粒子扩散)1. 公式为D = (kT)/(6πeta r),其中k是玻尔兹曼常量(k = 1.38×10^-23J/K),T 是绝对温度,eta是溶剂的粘度,r是球形粒子的半径。
2. 这个公式的推导基于分子运动论和流体力学原理。
它表明扩散系数与温度成正比,与溶剂粘度和粒子半径成反比。
例如,在研究胶体溶液中球形胶粒的扩散时,可以通过测量温度T、溶剂粘度eta以及已知胶粒半径r,利用该公式计算扩散系数D。
科特雷尔方程计算扩散系数

科特雷尔方程计算扩散系数
我们要找出使用科特雷尔方程如何计算扩散系数。
首先,我们需要了解科特雷尔方程是什么以及它与扩散系数的关系。
科特雷尔方程是一个描述物质扩散过程的方程,其形式如下:
dc/dt = D × (dc/dx)
其中:
dc/dt 是物质浓度的变化率,
D 是扩散系数,
dc/dx 是物质浓度随空间位置的变化率。
这个方程告诉我们,物质浓度的变化率与扩散系数和浓度随空间位置的变化率成正比。
为了求出扩散系数D,我们通常需要解这个方程,并从中提取D的值。
计算结果为:扩散系数D = cm^2/s。
所以,使用科特雷尔方程计算得到的扩散系数是 cm^2/s。
活性染料扩散系数计算公式

活性染料扩散系数计算公式活性染料是一种广泛应用于纺织品、皮革、纸张等领域的染料,它具有良好的亲和力和扩散性能,能够在材料表面均匀分布并与材料发生化学反应,从而实现着色的效果。
活性染料的扩散系数是评价染料扩散性能的重要参数,它能够反映染料在材料中的扩散速率和扩散程度,对于染料的选择和应用具有重要的指导意义。
本文将介绍活性染料扩散系数的计算公式及其相关知识。
一、活性染料扩散系数的定义。
活性染料在材料中的扩散过程可以用Fick定律来描述,Fick定律表明了扩散通量与浓度梯度之间的关系。
在一维情况下,Fick定律可以表示为:\[ J = -D \frac{dC}{dx} \]其中,J为扩散通量,单位为mol/(m^2·s);D为扩散系数,单位为m^2/s;C 为染料浓度,单位为mol/m^3;x为扩散方向,单位为m。
根据Fick定律,活性染料在材料中的扩散过程可以通过扩散系数D来描述。
二、活性染料扩散系数的计算公式。
活性染料扩散系数的计算通常采用扩散实验的方法,通过实验数据来确定扩散系数的数值。
一般情况下,可以采用扩散系数的计算公式来进行计算,常用的计算公式有以下几种:1. Fick第一定律。
Fick第一定律是描述非稳态扩散过程的定律,它可以表示为:\[ D = \frac{1}{2} \frac{dC}{dt} \frac{l^2}{C_0} \]其中,D为扩散系数,单位为m^2/s;dC/dt为浓度变化率,单位为mol/(m^3·s);l为材料厚度,单位为m;C0为染料初始浓度,单位为mol/m^3。
Fick第一定律的计算公式可以通过测量不同时间下染料浓度的变化来确定扩散系数的数值。
2. Fick第二定律。
Fick第二定律是描述稳态扩散过程的定律,它可以表示为:\[ D = \frac{Ql}{At} \]其中,D为扩散系数,单位为m^2/s;Q为扩散通量,单位为mol/s;l为材料厚度,单位为m;A为扩散截面积,单位为m^2;t为扩散时间,单位为s。
二维核磁扩散系数计算公式

二维核磁扩散系数计算公式
二维核磁扩散系数的计算公式如下:
D = (πΔδ)^2 / (4γ^2G^2δ^2(Δ - δ/3))
其中,
D 为核磁扩散系数(单位:m^2/s);
Δ为梯度脉冲的总持续时间(单位:s);
δ为梯度脉冲的单个脉冲宽度(单位:s);
γ为核的旋磁比(单位:rad/(T·s));
G 为梯度强度(单位:T/m)。
这个公式描述了二维核磁共振(NMR)中自旋扩散的现象,其中梯度脉冲用于引入空间坐标信息。
通过测量核磁共振信号的强度随时间变化的方式,可以计算出样品中分子的扩散系数。
这个公式是基于经典的自旋扩散理论推导得到的,适用于二维核磁扩散实验的数据处理和解析。
扩散系数计算(仅限借鉴)
7.2.2扩散系数费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5210/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即AB BA D D D ==。
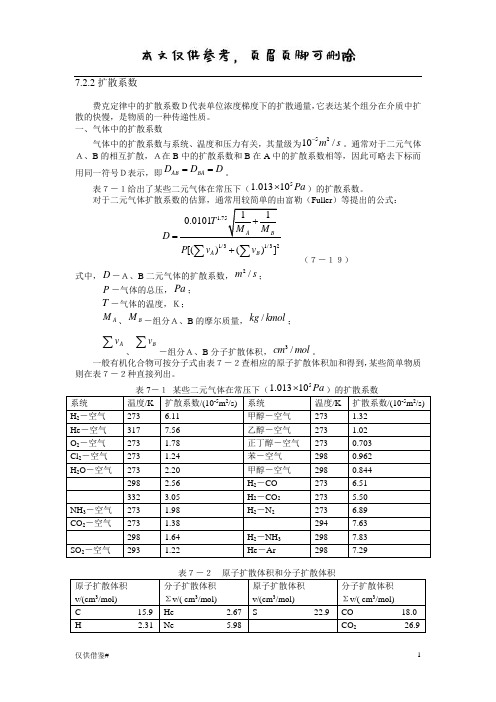
表7-1给出了某些二元气体在常压下(51.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1.751/31/32110.0101[()()]A BA B T M M D P v v +=+∑∑ (7-19)式中,D -A、B 二元气体的扩散系数,2/m s ;P -气体的总压,Pa ; T -气体的温度,K;A M 、B M -组分A、B 的摩尔质量,/kg kmol ;Av∑、Bv∑-组分A、B 分子扩散体积,3/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
51.01310Pa ⨯系统 温度/K 扩散系数/(10-5m 2/s) 系统 温度/K 扩散系数/(10-5m 2/s)H 2-空气 273 6.11 甲醇-空气 273 1.32 He -空气 317 7.56 乙醇-空气 273 1.02 O 2-空气 273 1.78 正丁醇-空气 273 0.703 Cl 2-空气 273 1.24 苯-空气 298 0.962 H 2O -空气 273 2.20 甲醇-空气 298 0.844 298 2.56 H 2-CO 273 6.51332 3.05 H 2-CO 2 273 5.50 NH 3-空气 273 1.98 H 2-N 2 273 6.89 CO 2-空气 273 1.38 294 7.63298 1.64 H 2-NH 3 298 7.83 SO 2-空气2931.22He -Ar2987.29原子扩散体积v/(cm 3/mol)分子扩散体积 Σv/( cm 3/mol) 原子扩散体积 v/(cm 3/mol) 分子扩散体积 Σv/( cm 3/mol)C 15.9 He 2.67 S 22.9 CO 18.0 H 2.31 Ne 5.98CO 2 26.9O 6.11 Ar 16.2 N 2O 35.9 N 4.54 Kr 24.5 NH 3 20.7 芳香族环 -18.3 Xe 32.7H 2O 13.1 杂环 -18.3 H 2 6.12 SF 6 71.3 F 14.7 D 2 6.84 Cl 2 38.4 CL 21.0 N 2 18.5Br 2 69.0 Br 21.9O 2 16.3SO 2 41.8I 29.8 空气 19.7式7-19的相对误差一般小于10%。
气体的扩散与扩散系数

气体的扩散与扩散系数气体扩散是指气体在自然界中由高浓度向低浓度逐渐向外扩散的过程。
扩散现象在自然界中广泛存在,它在我们的日常生活中起着重要的作用。
气体扩散的速率与扩散系数有着密切的关系。
本文将探讨气体扩散的原理以及如何计算扩散系数。
一、气体扩散原理气体扩散是由于气体分子热运动引起的。
气体分子之间存在着无规则的热运动,而热运动会使分子自发地向低浓度区域移动,以使系统达到热平衡。
这种无规则的运动导致了气体分子在垂直于浓度梯度方向上的自由扩散。
二、气体扩散速率的影响因素气体扩散速率与以下几个因素密切相关:1. 浓度差:浓度差是决定扩散速率的重要因素之一。
浓度差越大,扩散速率越快。
2. 温度:温度的提高使气体分子的平均动能增加,从而增加了气体分子的扩散速率。
3. 分子量:分子量较小的气体分子,其平均速度较大,扩散速率也较快。
4. 分子间相互作用力:分子间的相互作用力会影响气体的扩散速率。
相互作用力越大,扩散速率越慢。
三、扩散系数的定义与计算扩散系数是描述气体扩散速率的物理量,定义为单位时间内通过单位面积的气体量。
扩散系数可以用下面的公式来计算:D = (1/3)*√(2*π*R*T/M)其中,D表示扩散系数,R表示气体常数,T表示绝对温度,M表示气体分子的摩尔质量。
四、扩散系数的应用扩散系数在实际应用中有着广泛的应用。
例如在工业上,我们可以利用气体扩散原理来分离和提取所需的气体成分。
此外,在环境科学领域,扩散系数可以用来预测大气中的污染物传播情况。
五、气体扩散中的重要现象——菲克定律在气体扩散的研究中,菲克定律是一个非常重要的定律。
它描述了气体在扩散过程中的浓度变化与时间和距离的关系。
根据菲克定律,气体扩散的速率正比于浓度梯度的负值。
公式可以表示为:J = -D * (∂C/∂x)其中,J为单位面积的气体流量(即单位时间内通过单位面积的气体量),D为扩散系数,C为气体浓度,x为扩散距离。
六、气体扩散实验为了验证气体扩散现象,可以进行一系列实验。
gitt计算扩散系数实例

gitt计算扩散系数实例
Git是一种版本控制系统,计算扩散系数是指在版本控制系统中每个提交的修改所带来的影响范围大小。
在Git中,扩散系数可以用以下公式计算:
扩散系数 = 每个提交所影响的代码行数 / 总代码行数
例如,假设在一个Git仓库中,共有1000行代码,某个提交修改了50行代码,而该提交的前一个提交影响了100行代码,则该提交的扩散系数为:
扩散系数 = 50 / 1000 = 0.05
现在假设该提交被其他开发者拉取并使用,其影响范围将取决于该Git仓库被使用的范围及其他开发者对该提交的采纳程度。
扩散系数计算
7.2.2扩散系数费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5210/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即AB BA D D D ==。
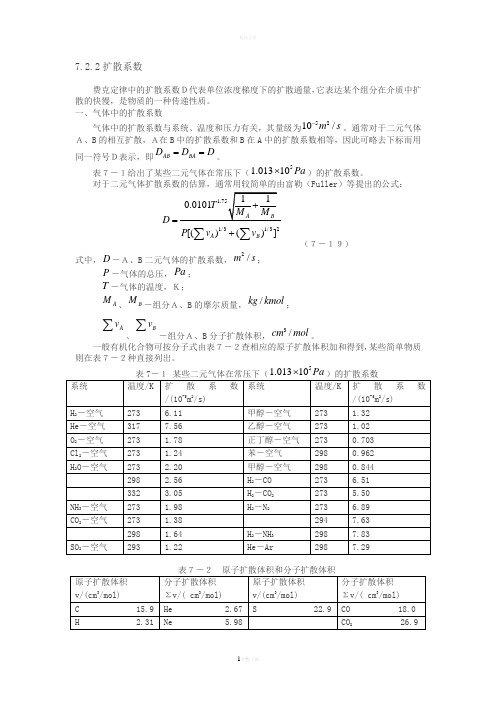
表7-1给出了某些二元气体在常压下(51.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1/31/32[()()]A B D P v v =+∑∑ (7-19)式中,D -A、B 二元气体的扩散系数,2/m s ;P -气体的总压,Pa ; T -气体的温度,K;A M 、B M -组分A、B 的摩尔质量,/kg kmol ;Av∑、Bv∑-组分A、B 分子扩散体积,3/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
51.01310Pa ⨯式7-19的相对误差一般小于10%。
二、液体中的扩散系数由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得多,其量级为9210/m s -。
表7-3给出了某些溶质在液体溶剂中的扩散系数。
对于很稀的非电解质溶液(溶质A+溶剂B),其扩散系数常用Wilke-Chang 公式估算:150.6()7.410T B AB A M TD V -φ=⨯μ 2/m s (7-21)式中,AB D -溶质A在溶剂B中的扩散系数(也称无限稀释扩散系数),2/m s ;T -溶液的温度,K;μ-溶剂B的粘度,.Pa s ;B M -溶剂B的摩尔质量,/kg kmol ;φ-溶剂的缔合参数,具体值为:水2.6;甲醇1.9;乙醇1.5;苯、乙醚等不缔合的溶剂为1.0;A V -溶质A 在正常沸点下的分子体积,3/cm mol ,由正常沸点下的液体密度来计算。
化工传质与分离 第一章(03)传质过程基础

湍流 流体
层流
内层
cAs
缓冲 层
cA f (r)
湍流
中心
cAf
流体与管壁间的浓度分布
一、对流传质的类型与机理
在与壁 面垂直 的方向 上分为 三层
层流 内层
缓冲 层
湍流 主体
传质机理 分子传质
浓度分布 为一陡峭直线
传质机理
分子传质 涡流传质
浓度分布 为一渐缓曲线
传质机理 涡流传质为主
浓度分布 为一平坦曲线
一、停滞膜模型(双膜模型)
(2)组分A通过停滞组分B扩散 组分A通过气膜、液膜的扩散通量方程分别为
DP
NA
AB
RTz G pBM
( p Ab p Ai )
NA
D
AB
zL
Cav c
BM
(c Ai
cAb )
一、滞膜模型(双膜模型)
设对流传质速率方程分别为
N A kG ( p Ab p Ai )
2.对流传质系数的确定 (1)等分子反方向扩散 组分A通过气膜、液膜的扩散通量方程分别为
D
NA
AB
zL
(c Ai
c Ab )
一、停滞膜模型(双膜模型)
设对流传质速率方程分别为
N A kG ( p Ab p Ai )
N
A
k
L
(c
Ai
c
Ab
)
比较得
k
G
D
AB
RTz G
k
L
D
AB
zL
气膜对流 传质系数 液膜对流 传质系数
(
A
B
)
组分A、B
的碰撞直径
kT
分子动力学计算扩散系数

分子动力学计算扩散系数分子动力学的基本原理是根据牛顿力学和哈密顿原理,将体系中的粒子看作是一个个球形硬球,通过计算粒子之间的相互作用力和粒子在各个方向上的运动速度,来模拟体系的宏观性质。
在分子动力学模拟中,通过给定初始位置和初始速度,根据牛顿第二定律模拟粒子的运动轨迹,并统计一定时间内粒子的位置和速度,从而计算出扩散系数。
在分子动力学计算扩散系数时,需要进行以下几个步骤:1.定义模拟系统:确定模拟体系的几何构型、粒子间相互作用势函数和边界条件。
2.初始状态设置:确定粒子的初始位置和速度,可以根据一定的分布函数来生成初始状态的粒子。
3.模拟粒子的运动:通过求解牛顿第二定律的微分方程,模拟粒子在力场中的运动轨迹。
4.统计平均值:对一定时间或者步数内粒子的位置和速度进行统计,得到平均值,以消除其随机性。
5.计算扩散系数:根据粒子的平均位移和时间间隔,可以计算出粒子的扩散系数。
在计算扩散系数时,需要考虑多个因素,如粒子的质量、温度、粒子间相互作用势函数等;同时,也需要进行系统性的误差分析,以验证计算结果的可靠性。
分子动力学方法可以用于计算各种类型的物质的扩散系数,例如气体、液体和固体。
此外,分子动力学方法也可以应用于模拟扩散过程的分子机制和动力学行为,从而揭示扩散过程的微观机理。
通过分子动力学的模拟与实验结合,可以深入研究扩散现象,并为相关研究提供更多的理论依据和实验数据。
总之,分子动力学计算扩散系数是一种重要的方法,它可以通过模拟粒子的运动轨迹来计算物质的扩散系数。
通过这种方法,可以更好地理解和研究扩散现象,并为相关应用提供理论依据和数据支持。
同时,在应用分子动力学计算扩散系数时,也需要考虑多个因素并进行系统误差分析,以保证计算结果的准确性和可靠性。
分子动力学计算扩散系数

分子动力学(Molecular Dynamics,简称MD)是一种计算方法,用于模拟和研究原子或分子在一定时间尺度内的运动和相互作用。
扩散系数是描述物质扩散速率的物理量,表示单位时间内物质从高浓度区域向低浓度区域的传输速率。
在分子动力学计算中,可以通过模拟大量分子的运动来计算扩散系数。
具体步骤如下:
1. 定义模拟系统:确定要研究的分子种类和数量,以及模拟系统的边界条件和温度等参数。
2. 初始化模拟系统:为每个分子分配初始位置和速度,并计算分子之间的相互作用力。
3. 模拟时间演化:使用数值积分方法,如Verlet算法或Leapfrog算法,模拟分子在一定时间间隔内的运动。
在每个时间步长内,更新分子的位置和速度。
4. 计算扩散系数:通过跟踪分子的运动轨迹,可以计算出分子在模拟系统中的平均位移和平均方位移。
根据爱因斯坦关系,扩散系数与平均方位移之间存在线性关系。
5. 统计分析:对多个模拟时间步长内的数据进行统计分析,计算出平均扩散系数和误差。
需要注意的是,分子动力学计算扩散系数的精确性和可靠性取决于模拟系统的大小、时间步长的选择以及模拟时间的长度等因素。
此外,还需要考虑分子之间的相互作用力模型的选择和参数的准确性。
因此,在进行分子动力学计算时,需要进行一系列的验证和优化,以确保结果的可靠性和准确性。
水分扩散系数计算

水分扩散系数计算水分扩散系数是指水分在物质中扩散的速度,是衡量物质内部水分传递能力的重要指标。
在工业生产和科学研究中,水分扩散系数的计算是非常重要的。
本文将从理论和实践两个方面,介绍水分扩散系数的计算方法。
一、理论计算理论计算是通过数学模型和物理原理,推导出水分扩散系数的计算公式。
其中,最常用的是菲克定律。
菲克定律是描述物质扩散的基本定律,它的公式为:J=-D(dC/dx)其中,J表示物质的扩散通量,D表示扩散系数,C表示物质浓度,x表示距离。
根据菲克定律,可以推导出水分扩散系数的计算公式:D=(J*L)/(A*ΔC)其中,J表示水分的扩散通量,L表示样品的厚度,A表示样品的面积,ΔC表示水分浓度的变化量。
这个公式可以用来计算各种物质的水分扩散系数,但是需要注意的是,不同物质的扩散系数是不同的,需要根据实际情况进行调整。
二、实践计算实践计算是通过实验测量,得出水分扩散系数的数值。
实验方法有很多种,其中最常用的是重量法和湿度法。
重量法是将样品放在恒温恒湿的环境中,测量样品的重量变化,从而计算出水分扩散系数。
具体步骤如下:1. 将样品切成一定大小的块状,称重并记录重量。
2. 将样品放在恒温恒湿的环境中,等待一定时间。
3. 取出样品,再次称重并记录重量。
4. 根据样品的重量变化,计算出水分扩散系数。
湿度法是将样品放在恒湿度的环境中,测量样品表面的湿度变化,从而计算出水分扩散系数。
具体步骤如下:1. 将样品放在恒湿度的环境中,等待一定时间。
2. 用湿度计测量样品表面的湿度,记录下来。
3. 等待一定时间后,再次用湿度计测量样品表面的湿度,记录下来。
4. 根据样品表面湿度的变化,计算出水分扩散系数。
总结水分扩散系数的计算是非常重要的,它可以帮助我们了解物质内部水分传递的能力。
理论计算和实践计算都是有效的方法,但是需要根据实际情况进行选择。
在实际应用中,我们需要根据不同物质的特性,选择合适的计算方法,以得到准确的结果。
扩散系数计算

扩 散 系 数费克定律中的扩散系数D 代表单位浓度梯度下的扩散通量, 散的快慢,是物质的一种传递性质。
一、气体中的扩散系数A 、B 的相互扩散,A 在 B 中的扩散系数和 B 在A 中的扩散系数相等,因此可略去下标而 用同一符号D 表示,即 D AB D BA D 。
5表7 — 1给出了某些二元气体在常压下(1.013 10 Pa )的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1/31/3 2P[( V A ) ( V B )](7—19)2 式中,D —A 、B 二元气体的扩散系数, m /s ;P —气体的总压,Pa ; T —气体的温度,K ; M A 、MB —组分A 、 B 的摩尔质量,kg/kmol ;V AV B3、—组分A 、B 分子扩散体积,cm /mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到, 某些简单物质则在表7-2种直接列出。
5表7-1某些二元气体在常压下(1.013 10 Pa )的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5 210 m /s 。
通常对于二元气体它表达某个组分在介质中扩式7 —19的相对误差一般小于1 0%。
、液体中的扩散系数由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得9 2多,其量级为10 m /s。
表7 —3给出了某些溶质在液体溶剂中的扩散系数。
表7 — 3 溶质在液体溶剂中A E),其扩散系数常用Wilke-Cha ng公式估算:式中,D AB—溶质A在溶剂E中的扩散系数(也称无限稀释扩散系数),m2/s ;T —溶液的温度,K;-溶剂E的粘度,Pa.s ;M B—溶剂E的摩尔质量,kg/ kmol ;—溶剂的缔合参数,具体值为:水 2.6 ;甲醇1.9 ;乙醇1.5 ;苯、乙醚等不缔合的溶剂为1.0;VA—溶质A在正常沸点下的分子体积,cm3/mol,由正常沸点下的液体密度来计D AB 7.4 10 15(M B)TV A0.6 2 /m /S (7 — 21)算。
扩散系数计算

扩散系数费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、 气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5210/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即AB BA D D D ==。
表7-1给出了某些二元气体在常压下(51.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1/31/32[()()]A B D P v v =+∑∑ (7-19)式中,D -A、B 二元气体的扩散系数,2/m s ;P -气体的总压,Pa ; T -气体的温度,K;A M 、B M -组分A、B 的摩尔质量,/kg kmol ;Av∑、Bv∑-组分A、B 分子扩散体积,3/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
51.01310Pa ⨯式7-19的相对误差一般小于10%。
二、 液体中的扩散系数由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得多,其量级为9210/m s -。
表7-3给出了某些溶质在液体溶剂中的扩散系数。
估算:150.6()7.410T B AB A M TD V -φ=⨯μ 2/m s (7-21)式中,AB D -溶质A在溶剂B中的扩散系数(也称无限稀释扩散系数),2/m s ;T -溶液的温度,K; μ-溶剂B的粘度,.Pa s ;B M -溶剂B的摩尔质量,/kg kmol ;φ-溶剂的缔合参数,具体值为:水2.6;甲醇1.9;乙醇1.5;苯、乙醚等不缔合的溶剂为1.0;A V -溶质A 在正常沸点下的分子体积,3/cm mol ,由正常沸点下的液体密度来计算。
扩散系数计算

扩散系数费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、气体中的扩散系数气体中的扩散系数与系统、温度和压力有关,其量级为5210/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即AB BA D D D ==。
表7-1给出了某些二元气体在常压下(51.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:1/31/32[()()]A B D P v v =+∑∑ (7-19)式中,D -A、B 二元气体的扩散系数,2/m s ;P -气体的总压,Pa ; T -气体的温度,K;A M 、B M -组分A、B 的摩尔质量,/kg kmol ;Av∑、Bv∑-组分A、B 分子扩散体积,3/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
表7-1 某些二元气体在常压下(51.01310Pa ⨯)的扩散系数表7-2 原子扩散体积和分子扩散体积式7-19的相对误差一般小于10%。
二、液体中的扩散系数由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得多,其量级为9210/m s 。
表7-3给出了某些溶质在液体溶剂中的扩散系数。
表7-3 溶质在液体溶剂中的扩散系数(溶质浓度很低)对于很稀的非电解质溶液(溶质A+溶剂B),其扩散系数常用Wilke-Chang 公式估算:150.6()7.410T B AB A M TD V -φ=⨯μ 2/m s (7-21)式中,AB D -溶质A在溶剂B中的扩散系数(也称无限稀释扩散系数),2/m s ;T -溶液的温度,K; μ-溶剂B的粘度,.Pa s ;B M -溶剂B的摩尔质量,/kg kmol ;φ-溶剂的缔合参数,具体值为:水;甲醇;乙醇;苯、乙醚等不缔合的溶剂为;A V -溶质A 在正常沸点下的分子体积,3/cm mol ,由正常沸点下的液体密度来计算。
扩散系数计算范文

扩散系数计算范文扩散系数是描述物质在扩散过程中向其他区域传递的趋势的物理量。
它可以用来衡量溶质在溶剂中扩散的速度以及扩散行为。
在物质扩散的研究中,计算扩散系数是非常重要的。
扩散现象是一种分子间能量传递的过程,它可以发生在气体、液体和固体之间。
在气体中,分子间的相互作用较弱,因此扩散速度很快。
在液体中,分子之间的相互作用相对较强,扩散速度较慢。
在固体中,分子之间的相互作用非常强,扩散速度最慢。
扩散过程通常被描述为物质从高浓度区域向低浓度区域传递的过程。
在扩散过程中,物质的浓度将逐渐均匀分布,直到达到平衡状态。
扩散系数可以用来描述这个过程的速度。
扩散系数的计算可以根据不同的扩散模型来进行。
最常用的扩散模型是弗里克定律(Fick's law)。
根据弗里克定律,扩散通量(即单位面积单位时间内通过的物质量)与扩散系数、浓度梯度和跨越面积之间有关系。
扩散通量的公式可以表示为:J = -D(dC/dx),其中J表示扩散通量,D表示扩散系数,(dC/dx)表示浓度梯度。
根据弗里克定律,扩散通量是负的,因为扩散是从高浓度向低浓度传递的过程。
浓度梯度越大,扩散通量越大。
扩散系数是一个比例常数,它表示单位浓度梯度的扩散通量。
通过对扩散实验数据的分析,可以利用弗里克定律计算扩散系数。
实验数据通常包括浓度的变化与时间或位置的关系。
通过绘制浓度与时间或位置的曲线,并利用曲线的斜率可以得到浓度梯度的大小。
将浓度梯度代入弗里克定律的公式中,就可以计算出扩散系数。
除了实验方法,还可以通过理论计算来估计扩散系数。
根据物质的性质和系统的参数,可以使用不同的数学模型来计算扩散系数。
常用的模型包括布朗运动模型和爱因斯坦关系。
这些模型根据分子的性质和系统的特点来描述扩散过程。
总之,扩散系数是描述物质在扩散过程中向其他区域传递的趋势的物理量。
它可以通过实验和理论计算来确定。
实验方法主要基于弗里克定律,通过分析扩散实验数据来计算扩散系数。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
7.2.2扩散系数
费克定律中的扩散系数D代表单位浓度梯度下的扩散通量,它表达某个组分在介质中扩散的快慢,是物质的一种传递性质。
一、 气体中的扩散系数
气体中的扩散系数与系统、温度和压力有关,其量级为5
2
10/m s -。
通常对于二元气体A、B 的相互扩散,A在B 中的扩散系数和B 在A 中的扩散系数相等,因此可略去下标而用同一符号D表示,即
AB BA D D D ==。
表7-1给出了某些二元气体在常压下(5
1.01310Pa ⨯)的扩散系数。
对于二元气体扩散系数的估算,通常用较简单的由富勒(Fuller )等提出的公式:
1/31/32
[()()]A B D P v v =
+∑∑ (7-19)
式中,D -A、B 二元气体的扩散系数,2
/m s ;
P -气体的总压,Pa ; T -气体的温度,K;
A M 、
B M -组分A、B 的摩尔质量,/kg kmol ;
A
v
∑、B
v
∑-组分A、B 分子扩散体积,3
/cm mol 。
一般有机化合物可按分子式由表7-2查相应的原子扩散体积加和得到,某些简单物质则在表7-2种直接列出。
5
式7-19的相对误差一般小于10%。
二、 液体中的扩散系数
由于液体中的分子要比气体中的分子密集得多,因此也体的扩散系数要比气体的小得多,其量级为
9210/m s -。
表7-3给出了某些溶质在液体溶剂中的扩散系数。
15
0.6()7.410
T B AB A M T
D V -φ=⨯μ 2/m s (7-21)
式中,AB D -溶质A在溶剂B中的扩散系数(也称无限稀释扩散系数),2
/m s ;
T -溶液的温度,K;
μ-溶剂B的粘度,.Pa s ;
B M -溶剂B的摩尔质量,/kg kmol ;
φ-溶剂的缔合参数,具体值为:水2.6;甲醇1.9;乙醇1.5;苯、乙醚等不缔合的溶剂为1.0;
A V -溶质A 在正常沸点下的分子体积,3/cm mol ,由正常沸点下的液体密度来计算。
若缺乏此密度
数据,则可采用Tyn-Calus 方法估算: 1.048
0.285c V V =,其中c V 为物质的临界体积(属于基本物性),单位
为3
/cm mol ,见表7-4。
从(7-21)可见,溶质A在溶剂B中的扩散系数AB D 与溶质B在溶质A中的扩散系数BA D 不相等,这一点与气体扩散系数的特性明显不同,需引起注意。
对给定的系统,可由温度1T 下的扩散系数1D 推算2T 下的2D (要求1T 和2T 相差不大),如下:
21
211(
)
T D D T 2μ=μ (7-22)
三、 生物物质的扩散系数
表7-5给出了一些生物溶质在水溶液中的扩散系数。
5003
/cm mol 时,可用式(7-21);否则,宜用式(7-23)(Polson 方法),
151/39.4010()AB
A T D M -⨯=
μ2/m s (7-23)
其中,μ-镕基的粘度,.Pa s ;
A M -生物溶质的摩尔质量。
四、 四、固体中的扩散系数
表7-6给出了某些物质在固体中的扩散系数。
对于气体在固体中的扩散,一般是用渗透率M P (permeability )来代替扩散系数D ,两者间的关系为
M AB P D S = (7-24)
其中,S为气体溶质A在固相中的溶解度,/A A S c p =,单位为3m 溶质(标准状态)/(3
m 固体.atm )。
* S ** P M 的单位:m 3溶质(标准状态)/(s ?m 2?atm/m )。
