海水提溴和海带提碘学习教材PPT课件
溴和碘的提取ppt课件

海洋
矿石
提纯
选择原料
海洋
氯碱工业
预处理 转化
海水 日照 粗盐 提纯 精盐
通电
2NaCl + 2H2O 2NaOH + H2↑ + Cl2↑
提纯
NaOH的精制
选择原料 预处理
阅读以下信息,我们应当如何选择提取溴、碘的原料呢?
溴、碘的化学性质活泼,在自然界中主要以Br –、 I –的形式存在
海洋
陆地
成本
选择选料 预处理 转化 提纯
工业生产中,选择氧化剂需要考虑哪些因素呢?
Br -
苦卤
I-
滤液
Cl2 + 2Br Cl2 + 2I -
不同氧化剂氧化生成1吨Br2的成本
Br2 氧化剂
Cl2
I2
KMnO4
成本/元 399.4 40487.5
Br2 + 2Cl I2 + 2Cl -
KClO3 30%H2O2
碘单质
② H2SO4
过滤 固体碘及饱和碘水
该提取过程利用了碘单质的什么特性呢?
碘难溶于水
① 3I2+6OH - 5I-+IO3- +3H2O
溶解度为0.029g/100g水 ② 5I-+IO3-+6H+ 3I2↓ + 3H2O
选择原料 预处理
提取溴、碘的方法 离子交换法
转化
提纯
膜分离法
离子交换法、膜分离法…
化工生产小贴士:提取过程中需考虑能耗、成本。
选择原料 预处理
含溴的苦卤 热空气吹出 含溴的空气 冷凝 粗溴 粗碘 提纯 碘单质
实验室中蒸馏含I2的有机溶液的现象
微项目海带提碘与海水提溴课件-【新教材】2020-2021学年高一化学鲁科版(2019)必修第二册

物质分离提纯的基本思路
物质分离和提纯是化学实验、化工生产的一项重要任务。 (1)物质分离和提纯的基本原则 ①“不增”:不引入新的杂质。 ②“不减”:不减少被提纯物质。 ③“易分离”:被提纯物质与杂质易分离。 ④“易复原”:被提纯物质易复原。
(2)物质分离和提纯的要求 ①“过量”:为除尽杂质,除杂试剂要过量。 ②“后除前”:后加入的试剂要把前面过量的试剂除尽。 (3)物质分离和提纯的基本方法 ①物理方法:过滤法、萃取分液法、蒸发结晶法、蒸馏法、升华法等。 ②化学方法:沉淀法、洗气法、酸碱法、氧化还原法、电解法、离子 交换法等。
(4)物质分离提纯的基本思路,如图所示:
一、海带提碘
1.从海带中提取碘的原理及实验流程
(1)原理:选取氧化剂将I-氧化为碘单质; ①选取氯水,离子方程式:_2_I_-_+__C_l_2_=_=_=_I2_+__2_C_l_-_。 ②若选取溴水,离子方程式:_2_I_-_+__B_r_2_=_=_=_I_2+__2_B__r-__。 ③若选取H2O2溶液,离子方程式:_2_I_-_+__H_2_O__2+__2_H__+_=_=_=_I_2_+__2_H_2_O_。 然后溶液中的碘单质用苯或CCl4萃取,分液提取。
二、海水提溴 1.从苦卤中提取溴单质
(1)写出①中反应的离子方程式_2_B_r_-_+__C__l2_=_=_=_B_r_2_+__2_C_l_-_。 (2)③中常用的吸收剂是_二__氧__化__硫__水__溶__液__,反应的化学方程式是__S_O_2_+__ _B_r_2_+__2_H_2_O_=_=_=_2_H__B_r_+__H_2_S_O_4__。 (3)写出④中反应的化学方程式_2_H__B_r_+__C_l2_=_=_=_2_H__C_l_+__B_r_2 _。
第1章微项目海带提碘与海水提溴第一课时课件【新版】鲁科版高一化学必修第二册(机构用)

P22 3卓 3. 为了从海带浸取液中提取碘,某同学设计了如图实验方案。下列说法 正确的是( C )
A. ①中反应的离子方程式:2I- + H2O2 = I2 + 2OHB. ②中分液时含I2的CCl4溶液从分液漏斗上口倒出 C. ③操作使用的是反萃取法,得到的上层溶液中含有ID. 操作Z的名称是蒸发
氯、钠、镁、硫、钙、钾、碳、锶、溴、硼、氟 (1)氧化反应:①所有的有机物的燃烧均为氧化反应。②烯烃、炔烃和苯的同
③加热煮沸时间也不能过长,防止Cu(OH)2受热分解成黑色的CuO。 3)Ksp(CaF2)=5.29×10-9,除铁后所得100 mL溶液中c(Ca2+)=0.01 mol·L-1,加 (2)NH3分子中H—N—H键角为106.7°,在Ag 中,H—N—H键角近似 源负极相连,为阴极室,开始电解时,阴极上水得电子生成氢气同时生成OH-,生成 =0,则N原子的价层电子对数为3,N原子采取sp2杂化,则其空间构型 (6)标准状况下,2.24 L SO3中含有0.3NA个氧原子( ) C.混合气体密度不变
H2SO4溶液
5I- + IO3- + 6H+ = 3I2 + 3H2O
含I2的悬浊液
过滤
固态I2单质
练习题组一
P22:1、3
P22 1 1. 【2019春·朝阳区期末】实验室从海带中提取碘的部分流程如图: 下列说法不正确的是( A )
A. 完成步骤①需要装置Ⅲ B. 完成步骤③需要装置Ⅱ C. 完成步骤⑤需要装置Ⅰ D. 完成步骤②和④需要装置Ⅳ
第1章 原子结构 元素周期律
微项目
海带提碘与海水提溴
1、海带提碘 2、海水提溴
目录
目录
3.3.2从海水中提取溴、从海带中提取碘(教学课件)——高一上学期化学苏教版(2019)必修第一册

解析:Cl2将I-氧化生成I2,I2被CCl4萃取,所以上层接近无色,下层为紫红色。
3.下列物质与其用途相符的是( )
①Cl2——作消毒剂; ③AgI——人工降雨;
②AgBr——制胶卷、感光纸; ④加碘食盐——预防甲状腺肿大;
⑤淀粉——检验I2的存在; ⑥NaClO——漂白纺织物。
A.②③④⑤⑥
(1)步骤①②的实验目的是_将__海__带__中__的__I-__溶_解__到__水__中_。
(2)步骤③中实验操作的名称是___过__滤___。
(3)步骤④中可供选用的试剂有Cl2、Br2和H2O2(含稀硫酸),你认为 最合适的试剂是_H__2O__2(_含__稀__硫__酸__)。
(4)步骤⑤中提取碘时使用的主要玻璃仪器是_分__液__漏__斗_。
2.已知溴易挥发,碘易升华,向含有NaBr和KI的混合溶液中通入
过量氯气充分反应后将溶液蒸干,并灼烧所得物质,最后剩余的固体
是( )
A.NaCl和KI C.KCl和NaBr
B.NaCl、KCl和I2 D.KCl和NaCl
答案:D
3.溴又称为海洋元素,主要用于制取溴化物,并作为普通分析试 剂和有机合成试剂用于医药、农药、染料、香料、摄影材料、灭火剂、 选矿、冶金、鞣革、净水等方面。从海水中可以提取溴,主要反应之 一为2KBr+Cl2===2KCl+Br2,下列说法中正确的是( )
关键能力 1.Cl2、Br2、I2在水及有机溶剂中的颜色
水
CCl4
汽油
Cl2 黄绿色 黄绿色
黄绿色
Br2 黄→橙 橙→橙红 橙→橙红
I2 深黄→褐 紫→深紫 浅紫红→紫红
2.卤素离子的检验方法 (1)AgNO3溶液——沉淀法
化学微项目海带提碘与海水提溴体验元素性质递变规律的实际应用课件ppt

将溴氧化剂加入海水中,发生氧化反应,将 溴离子氧化成溴单质。
萃取分离
蒸馏回收
将生成的溴单质用有机溶剂(如四氯化碳) 萃取出来,分离出溴单质。
将含有溴单质的有机溶剂进行蒸馏,回收有 机溶剂并得到纯度较高的溴单质。
实验数据分析
数据分析方法
01
通过实验数据,分析比较不同条件下氧化剂的用量、反应温度
等因素对溴提取率的影响。
使用玻璃仪器时需小心操作,避免破损和划伤 。
在通风橱内进行实验,避免吸入有毒有害气体 。
海水提溴实验安全注意事项
实验过程中需远离火源和高温 物体,以免发生危险。
使用溴水和氯气等有毒有害试 剂时需特别小心,避免接触皮
肤和吸入气体。
在通风橱内进行实验,避免吸 入有毒有害气体。
实验室安全一般原则
遵守实验室安全规章制度,不私自使用试剂和仪器设 备。
指导新元素发现
元素周期表为新元素的发现提供了理论指导,科学家可以根 据空白格位可能对应的新元素原子量和化学性质进行探索。
原子结构示意图的应用
理解原子结构
原子结构示意图是描述原子内部结构的重要工具,通过观察示意图可以直观 理解电子排布、原子核等概念。
解释化学现象
原子结构示意图可以解释许多化学现象,如化学键的形成、元素的化学性质 等,有助于理解物质的结构与性质之间的关系。
据分析。
02
数据可靠性判断
对于实验数据要进行可靠性判断,如通过对比不同批次、不同时间的
数据进行对比分析,以确定数据的可靠性。
03
数据处理方法的选择
根据数据特点选择合适的处理方法,如计算平均值、中位数、众数等
,以便更好地反映数据的特征。
对实验教学的改进意见
从海水中提取溴和碘 ppt课件

2020/12/2
7
• 我们需要的是游离态的单质溴,而海水中的 溴是以什么形态存在的呢?我们怎么将这种 形态的溴转变为单质溴呢?
加入氧化剂,如:Cl2 + 2Br- → 2Cl- + Br2
• 海水呈碱性,在通氯气前应对海水做怎样的 处理?
用硫酸酸化
• 如果直接通氯气会怎样呢?
202氯0/12气/2 会有损耗,原料利用率下降。
馏原料,耗时耗能,成本高。 ②“空气吹出、SO2吸收、
20氯20/1化2/2”的过程实际上是一个Br2的浓缩过程。
9
1、海水提溴
提取粗盐
海水
①硫酸酸化
苦卤
②氯气氧化
含Br2 ③热空气或 的海水 水蒸气吹出
含Br2 的空气
⑥热空
Br2蒸气 气吹出
Br2与水 的混合物
④SO2吸收
吸收液
⑤氯气氧化
写出步骤④的化学方程式。 Br2+ SO2 + 2H2O → 2HBr+H2SO4
2020/12/2
21
三、海带提碘
溴
碘
浓度(mg/L)
67
0.06
海带中质量分数 (mg/kg)
3000— 7000
沸点(℃)
58.7 8
184.4
2020/12/2
22
①
海 带 灰
浸 渍
悬 浊 液
②
残渣
含I-
③ 含I2
④
含I2 有机
⑤碘 晶
溶液
溶液
溶液
体
①海 ②带 过 滤
③ 氧化
④
晒干灼烧
⑤ (减压)蒸馏
• 通过对比实 验可知I2在 有机溶剂中 的溶解度远 大于在水中 的溶解度
从海水中提取溴和碘PPT课件

提 溴
Extracting bromine
海 水 提 溴
Extracting bromine
from sea water
Br-的浓度(g /L)
海水
卤水(晒盐之后)
0.067
2.5--3
步骤: 浓缩(concentration ) 氧化(oxidation ) 提取(extraction ) 原理:Cl2+2Br-- Br2 + 2Cl--
(固态物质不经过转变成液态而直接变成气态的现象)
碘的蒸气呈紫色
卤素单质物理性质的变化规律
单质
颜色 状态
F2
浅黄绿色 气 态 增 升
Cl2
黄绿色 气 态
Br2
深红棕色 液 态 大 高
I2
紫黑色 固态
密度
熔沸点
溴的溶解性实验
Br2
水
汽油或苯
溴水 (橙色)
溴的汽油溶液 (橙红色)
Br2
水
CCl4
溴水 (橙色) 溴的四氯化碳溶液 (橙红色)
含碘元素 的溶液
氧化剂
含碘单质 的溶液
CCl4
海带
灼烧
海带灰
溶解、过滤
残渣
碘的有机溶液
1、快乐总和宽厚的人相伴,财富总与诚信的人相伴,聪明总与高尚的人相伴,魅力总与幽默的人相伴,健康总与阔达的人相伴。 2、人生就有许多这样的奇迹,看似比登天还难的事,有时轻而易举就可以做到,其中的差别就在于非凡的信念。 3、影响我们人生的绝不仅仅是环境,其实是心态在控制个人的行动和思想。同时,心态也决定了一个人的视野和成就,甚至一生。 4、无论你觉得自己多么了不起,也永远有人比更强;无论你觉得自己多么不幸,永远有人比你更不幸。 5、也许有些路好走是条捷径,也许有些路可以让你风光无限,也许有些路安稳又有后路,可是那些路的主角,都不是我。至少我会觉得,那些路不是自己想要的。 6、在别人肆意说你的时候,问问自己,到底怕不怕,输不输的起。不必害怕,不要后退,不须犹豫,难过的时候就一个人去看看这世界。多问问自己,你是不是已经为了梦想而竭尽全力了? 7、人往往有时候为了争夺名利,有时驱车去争,有时驱马去夺,想方设法,不遗余力。压力挑战,这一切消极的东西都是我进取成功的催化剂。 8、真想干总会有办法,不想干总会有理由;面对困难,智者想尽千方百计,愚者说尽千言万语;老实人不一定可靠,但可靠的必定是老实人;时间,抓起来是黄金,抓不起来是流水。 9、成功的道路上,肯定会有失败;对于失败,我们要正确地看待和对待,不怕失败者,则必成功;怕失败者,则一无是处,会更失败。1、快乐总和宽厚的人相伴,财富总与诚信的人相伴,聪明总与高尚的人相伴,魅力总与幽默的人相伴,健康总与阔达的人相伴。 2、人生就有许多这样的奇迹,看似比登天还难的事,有时轻而易举就可以做到,其中的差别就在于非凡的信念。 3、影响我们人生的绝不仅仅是环境,其实是心态在控制个人的行动和思想。同时,心态也决定了一个人的视野和成就,甚至一生。 4、无论你觉得自己多么了不起,也永远有人比更强;无论你觉得自己多么不幸,永远有人比你更不幸。 5、也许有些路好走是条捷径,也许有些路可以让你风光无限,也许有些路安稳又有后路,可是那些路的主角,都不是我。至少我会觉得,那些路不是自己想要的。 6、在别人肆意说你的时候,问问自己,到底怕不怕,输不输的起。不必害怕,不要后退,不须犹豫,难过的时候就一个人去看看这世界。多问问自己,你是不是已经为了梦想而竭尽全力了? 7、人往往有时候为了争夺名利,有时驱车去争,有时驱马去夺,想方设法,不遗余力。压力挑战,这一切消极的东西都是我进取成功的催化剂。 8、真想干总会有办法,不想干总会有理由;面对困难,智者想尽千方百计,愚者说尽千言万语;老实人不一定可靠,但可靠的必定是老实人;时间,抓起来是黄金,抓不起来是流水。14、成长是一场和自己的比赛,不要担心别人会做得比你好,你只需要每天都做得比前一天好就可以了。 15、最终你相信什么就能成为什么。因为世界上最可怕的二个词,一个叫执着,一个叫认真,认真的人改变自己,执着的人改变命运。只要在路上,就没有到不了的地方。 16、你若坚持,定会发光,时间是所向披靡的武器,它能集腋成裘,也能聚沙成塔,将人生的不可能都变成可能。 17、人生,就要活得漂亮,走得铿锵。自己不奋斗,终归是摆设。无论你是谁,宁可做拼搏的失败者 9、成功的道路上,肯定会有失败;对于失败,我们要正确地看待和对待,不怕失败者,则必成功;怕失败者,则一无是处,会更5、别着急要结果,先问自己够不够格,付出要配得上结果,工夫到位了,结果自然就出来了。 6、你没那么多观众,别那么累。做一个简单的人,踏实而务实。不沉溺幻想,更不庸人自扰。 7、别人对你好,你要争气,图日后有能力有所报答,别人对你不好,你更要争气望有朝一日,能够扬眉吐气。 8、奋斗的路上,时间总是过得很快,目前的困难和麻烦是很多,但是只要不忘初心,脚踏实地一步一步的朝着目标前进,最后的结局交给时间来定夺。 9、运气是努力的附属品。没有经过实力的原始积累,给你运气你也抓不住。上天给予每个人的都一样,但每个人的准备却不一样。不要羡慕那些总能撞大运的人,你必须很努力,才能遇上好运气。 10、你的假装努力,欺骗的只有你自己,永远不要用战术上的勤奋,来掩饰战略上的懒惰。 11、时间只是过客,自己才是主人,人生的路无需苛求,只要你迈步,路就在你的脚下延伸,只要你扬帆,便会有八面来风,启程了,人的生命才真正开始。 12、不管做什么都不要急于回报,因为播种和收获不在同一个季节,中间隔着的一段时间,我们叫它为坚持。失败。11、学会学习的人,是非常幸福的人。——米南德 12、你们要学习思考,然后再来写作。——布瓦罗 13、在寻求真理的长河中,唯有学习,不断地学习,勤奋地学习,有创造性地学习,才能越重山跨峻岭。——华罗庚 14、许多年轻人在学习音乐时学会了爱。——莱杰 15、学习是劳动,是充满思想的劳动。——乌申斯基 16、我们一定要给自己提出这样的任务:第一,学习,第二是学习,第三还是学习。——列宁 17、学习的敌人是自己的满足,要认真学习一点东西,必须从不自满开始。对自己,“学而不厌”,对人家,“诲人不倦”,我们应取这种态度。——毛泽东 18、只要愿意学习,就一定能够学会。——列宁 19、如果学生在学校里学习的结果是使自己什么也不会创造,那他的一生永远是模仿和抄袭。——列夫· 托尔斯泰 20、对所学知识内容的兴趣可能成为学习动机。——赞科夫 21、游手好闲地学习,并不比学习游手好闲好。——约翰· 贝勒斯 22、读史使人明智,读诗使人灵秀,数学使人周密,自然哲学使人精邃,伦理学使人庄重,逻辑学使人善辩。——培根 23、我们在我们的劳动过程中学习思考,劳动的结果,我们认识了世界的奥妙,于是我们就真正来改变生活了。——高尔基 24、我们要振作精神,下苦功学习。下苦功,三个字,一个叫下,一个叫苦,一个叫功,一定要振作精神,下苦功。——毛泽东 25、我学习了一生,现在我还在学习,而将来,只要我还有精力,我还要学习下去。——别林斯基、学习外语并不难,学习外语就像交朋友一样,朋友是越交越熟的,天天见面,朋友之间就亲密无间了。——高士其 2、对世界上的一切学问与知识的掌握也并非难事,只要持之以恒地学习,努力掌握规律,达到熟悉的境地,就能融会贯通,运用自如了。——高士其 3、学和行本来是有联系着的,学了必须要想,想通了就要行,要在行的当中才能看出自己是否真正学到了手。否则读书虽多,只是成为一座死书库。——谢觉哉、你的假装努力,欺骗的只有你自己,永远不要用战术上的勤奋,来掩饰战略上的懒惰。 11、时间只是过客,自己才是主人,人生的路无需苛求,只要你迈步,路就在你的脚下延伸,只要你扬帆,便会有八面来风,启程了,人的生命才真正开始。 12、不管做什么都不要急于回报,因为播种和收获不在同一个季节,中间隔着的一段时间,我们叫它为坚持。 13、你想过普通的生活,就会遇到普通的挫折。你想过最好的生活,就一定会遇上最强的伤害。这个世界很公平,想要最好,就一定会给你最痛。
微项目 海带提碘与海水提溴 课件 高一化学鲁科版(2019)必修第二册
海带 【思考】4.在你设计的实验方案中,实现物质分离、提纯路是什么?
灼烧
海带灰 浸取
海带灰 悬浊液
过滤
含I-溶液
氧化 Cl2
富
直接法
集
分 离
提
纯
间接法
物理
性
质
物质性质的
差
递变规律
异
化学
含I2溶液 萃取 CCl4 含I2的CCl4溶液
所属物质类别的一般性质 氧化性或还原性 其他
活动项目2 海水提溴
(4)物质分离、提纯的基本原则有哪些? ①“不增”——不能引入新的杂质; ②“不减”——不能减少被提纯物质; ③“易分”——杂质或反应后的杂质易与被提纯物质分离; ④“易复原”——被提纯的物质要容易复原。
知识拓展 Ⅰ.分离和提纯的一般方法 ①物理方法:过滤、蒸发结晶、蒸馏或分馏、萃取、分液、升华等。 ②化学方法:沉淀法、洗气法、转化法等。 Ⅱ.注意事项 ①为除尽杂质,除杂试剂需过量。 ②加入试剂的原则:后面的试剂要把前面过量的试剂除尽。 ③沉淀完全的判断方法是在上层清液中(或取少量上层清液置于小试管中) 滴加沉淀剂,如果不再产生沉淀,说明沉淀已经完全。
6.目前海水提溴的最主要方法之一是空气吹出法,其部分流程图如下:
以下推断不合理的是( C ) A.热空气能吹出溴是利用溴易挥发的性质 B.SO2吸收溴的反应方程式:SO2+2H2O+Br2═H2SO4+2HBr C.因为氧化性Fe3+<Br2,所以氧化过程可选用FeCl3溶液 D.没有采用直接蒸馏含Br2的海水得到单质溴主要是为了节能
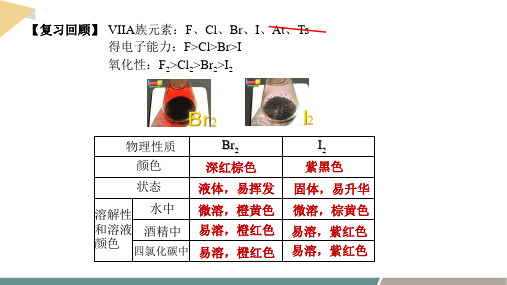
【复习回顾】 VIIA族元素:F、Cl、Br、I、At、Ts 得电子能力:F>Cl>Br>I 氧化性:F2>Cl2>Br2>I2
新教材 鲁教版高中化学必修二 微项目海带提碘与海水提溴 课件(共22张PPT)

第1章 原子结构 元素周期律微项目 海带提碘与海水提溴——体验元素性质递变规律的实际应用【项目学习目标】1.通过海带提碘活动和海水提溴工艺流程的设计,建立真实复杂系统中物质分离、富集、提取的基本思路。
2.通过海带提碘活动和海水提溴工艺流程的设计,体会元素周期律、元素周期表在分析、解决实际问题中的价值。
【重难点】萃取和分液的基本操作1.Br 2、I 2的物理性质色、态密度溶解性特性溴_______色液体均比水的___水中:微溶;有机溶剂中:____碘_____色固体深红棕紫黑大易溶易挥发3易升华2.卤族元素化学性质的递变规律(F→I)(1)相似性。
卤素原子最外层电子数都为 ,都能形成气态氢化物(通式为 ),最高价氧化物对应的水化物化学式为 (F除外),单质具有 性(2)递变性①单质氧化性逐渐F 2 Cl 2 Br 2 I 2。
②卤素离子还原性逐渐③气态氢化物稳定性逐渐 ④单质与氢气反应的能力逐渐7HX HXO 4氧化减弱减弱减弱增强阅读课本P30页,思考下列问题:1.海带紫菜中的碘以什么形式存在?2.海带灼烧的目的是什么?3.如何证明海带灰溶液中含有I- ?提取碘时要用适当的氧化剂将其氧化成I2,可用什么氧化剂?选择的依据是什么?灼烧海带可以分解除去其中的有机化合物以碘化物形式存在①AgNO3溶液和稀HNO3②氯水和淀粉溶液③氯水和CCl4溶液氯水、溴水、H2O2都可以将I- 氧化2.实验方案:(1)在一支试管中加入1~2mLKI溶液,滴加少量新制氯水,再滴加少量CCl4,振荡,静置【活动探究1】将I-转化为I21.实验药品KI溶液、氯水、溴水、CCl4现象及结论:液体分层,上层为无色溶液,下层为紫红色液体。
反应的化学方程式为Cl2+2KI==2KCl+I2(2)在一支试管中加入1~2 mL KI溶液,滴加少量新制溴水,再滴加少量CCl 4,振荡,静置现象及结论:液体分层,上层为无色溶液,下层为紫红色液体。
【高中化学】从海水中提取溴和碘PPT课件

Br2
水
CCl4
溴水 (橙色) 溴的四氯化碳溶液 (橙红色)
碘的溶解性实验
上层:
碘的汽油溶液 (紫红色)
I2
水
汽油或苯
碘水 (棕色)
I2
水
CCl4
碘水 (棕色) 下层:碘的四氯
化碳溶液(深紫色)
溴和碘在不同溶剂中所生成溶液(由稀至浓) 的颜色变化
水
汽油(苯) 四氯化碳
橙至红棕色 橙至红棕色
溴
黄至橙色
含碘元素 的溶液
氧化剂
含碘单质 的溶液
CCl4
海带
灼烧
海带灰
溶解、过滤
残渣
碘的有机溶液
1、不要做刺猬,能不与人结仇就不与人结仇,谁也不跟谁一辈子,有些事情没必要记在心上。 2、相遇总是猝不及防,而离别多是蓄谋已久,总有一些人会慢慢淡出你的生活,你要学会接受而不是怀念。 3、其实每个人都很清楚自己想要什么,但并不是谁都有勇气表达出来。渐渐才知道,心口如一,是一种何等的强大! 4、有些路看起来很近,可是走下去却很远的,缺少耐心的人永远走不到头。人生,一半是现实,一半是梦想。 5、你心里最崇拜谁,不必变成那个人,而是用那个人的精神和方法,去变成你自己。 6、过去的事情就让它过去,一定要放下。学会狠心,学会独立,学会微笑,学会丢弃不值得的感情。 7、成功不是让周围的人都羡慕你,称赞你,而是让周围的人都需要你,离不开你。 8、生活本来很不易,不必事事渴求别人的理解和认同,静静的过自己的生活。心若不动,风又奈何。你若不伤,岁月无恙。 9、命运要你成长的时候,总会安排一些让你不顺心的人或事刺激你。 10、你迷茫的原因往往只有一个,那就是在本该拼命去努力的年纪,想得太多,做得太少。 11、有一些人的出现,就是来给我们开眼的。所以,你一定要禁得起假话,受得住敷衍,忍得住欺骗,忘得了承诺,放得下一切。 12、不要像个落难者,告诉别人你的不幸。逢人只说三分话,不可全抛一片心。 13、人生的路,靠的是自己一步步去走,真正能保护你的,是你自己的选择。而真正能伤害你的,也是一样,自己的选择。 14、不要那么敏感,也不要那么心软,太敏感和太心软的人,肯定过得不快乐,别人随便的一句话,你都要胡思乱想一整天。 15、不要轻易去依赖一个人,它会成为你的习惯,当分别来临,你失去的不是某个人,而是你精神的支柱;无论何时何地,都要学会独立行走 ,它会让你走得更坦然些。 16、在不违背原则的情况下,对别人要宽容,能帮就帮,千万不要把人逼绝了,给人留条后路,懂得从内心欣赏别人,虽然这很多时候很难 。 17、做不了决定的时候,让时间帮你决定。如果还是无法决定,做了再说。宁愿犯错,不留遗憾! 18、不要太高估自己在集体中的力量,因为当你选择离开时,就会发现即使没有你,太阳照常升起。 19、时间不仅让你看透别人,也让你认清自己。很多时候,就是在跌跌拌拌中,我们学会了生活。 20、与其等着别人来爱你,不如自己努力爱自己,对自己好点,因为一辈子不长,对身边的人好点,因为下辈子不一定能够遇见。
《海水提溴和碘》课件

溴和碘的来源
01
溴和碘在地壳中的含量较低,主要存在于海水中。海水中溴和碘的含量分别为 0.065mg/L和0.006mg/L。
02
除了海水,溴和碘还可以从地下卤水、矿物、火山喷发等自然来源中获得。
溴和碘的应用
优点
可实现大规模生产,且吸 收剂可循环使用。
缺点
需要消耗大量的空气和吸 收剂,且吹出率较低。
溶剂萃取法提溴
原理
利用溴在有机溶剂和水中的溶解 度差异,将溴从海水中萃取出来
。
优点
溴的萃取率高,可实现连续生产。
缺点
需要使用大量的有机溶剂,且溶剂 的回收和再生过程较为复杂。
离子交换法提溴
原理
利用溴离子与离子交换树脂之间 的交换反应,将溴离子从海水中
溴和碘在工业、医疗、食品、农业等 领域都有广泛的应用。例如,溴可用 于制造溴化物、染料、农药等,碘可 用于制造碘化物、药物、染料等。
在医疗方面,溴和碘都有消毒杀菌的 作用,可用于医疗器械、手术室、游 泳池等场所的消毒。此外,碘还可用 于治疗甲状腺疾病。
02
海水提溴技术
Chapter
吸附法提溴
01
等新兴领域。
THANKS
感谢观看
海水提溴和碘的前景展望
随着全球人口的增长和经济的发展,对 溴和碘的需求量将不断增加。因此,海
水提溴和碘的前景十分广阔。
在未来,海水提溴和碘的技术将不断进 步和完善,提取效率和产品质量将得到 进一步提升。同时,随着环保要求的提 高,提取过程将更加注重环保和可持续
发展。
此外,随着海洋经济的快速发展,海水 提溴和碘的应用领域也将不断拓展。除 了传统的医药、农药、染料、石油化工 等领域外,还将应用于新能源、新材料
沪科版化学高一上《从海水中提取溴和碘》ppt课件2

卤素单质物理性质的变化规律
单质 颜色
F2 Cl2 Br2
浅黄绿色 黄绿色 深红棕色
I2
紫黑色
状态
气态 气态
液态
固态
密度 增
大
熔沸点 升
高ቤተ መጻሕፍቲ ባይዱ
二、卤素单质的化学性质
1.氯、溴、碘的活泼性
试 现有化学试剂:氯水 溴水 碘水 四氯化碳
一
NaCl(aq) NaBr(aq) KI(aq)
试 设计实验方案:证明卤素单质的活泼性。
萃取的条件:(1)溶质在两种溶剂中的溶解度不 同,相差越大越好。
(2)两种溶剂互不相溶。
分液——把两种互不相溶(分层)的液体进行分 离的操作。
*分液操作时,下层液体从分液漏斗下端流出, 上层液体从分液漏斗上口倒出。
类型
混合物各组分性质
分离方法
实例
一种可溶,另一种不溶
溶解、过滤、 蒸发结晶
粗盐的提纯
五、从海水中提取的元素——溴和碘
1.从海水中提取溴
原理:将Br-氧化为Br2 三个步骤:浓缩、氧化、提取
简单流程:海水 晒盐提取NaCl后 苦卤 提取KCl后 浓苦卤 通Cl2氧化
Br-:0.067g/L
Br-:2.5-3g/L
Br-:6g/L
Br2 鼓入热空气或水蒸气,冷凝 粗Br2 精制 高纯度Br2
* 碘的水溶液——碘水:棕黄色 * 碘和碘水应密闭保存在棕色试剂瓶中 * 碘的特性:①遇淀粉变蓝;②易升华。 想一想:如何将混入砂子中的(或与NaCl固体混
合的)碘提取出来?
试一试:能否根据氯、溴、碘的物理性质推测氟 的物理性质?
4.氟(F2)的物理性质 状态: 气体 颜色: 很淡的黄绿色 气味: 刺激性 毒性: 剧毒 溶解性:与水剧烈反应
鲁科版高中化学必修第二册精品课件 第1章 海带提碘与海水提溴——体验元素性质递变规律的实际应用

可以用CCl4萃取溴水中的溴,C正确;Cl2能与Br-发生反应:
2Br-+Cl2===Br2+2Cl-,CCl4密度比水大,Br2溶于CCl4,所以下层显橙红色,D
正确。
1 2 3 4 5
4.(2023湖北高一统考期末)工业上常用的一种海水提溴技术“吹出法”,利用
反应,所以苯可以作萃取剂从碘的水溶液中提取碘。
(4)请设计一个简单实验,检验提取碘后的水溶液中是否还含有单质碘。
提示 淀粉溶液遇碘变蓝色,所以可以用淀粉溶液检验是否含有碘。其检验
方法是向溶液中滴加淀粉溶液,如果溶液变蓝色,则证明含有碘,否则不含
碘。
深化拓展
1.海带提碘
实验步骤
(1)将海带冲洗干净,用剪刀将
过滤。过滤时需要的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)步骤⑥的目的是从含碘苯溶液中分离出单质碘并回收苯,该步骤的实验
操作名称是什么?
提示 分离互溶且沸点不同的液体可采用蒸馏方法。碘易溶于苯,但碘和苯
的熔、沸点不同,所以可以采用蒸馏的方法分离。
(3)步骤⑤中,为什么选择用苯从碘的水溶液中提取碘?
提示 苯和水不互溶,碘在苯中的溶解度大于在水中的溶解度,且碘与苯不
1 2 3 4 5
3.下列说法不正确的是( B )
A.图Ⅰ振荡后静置,上层溶液颜色变浅或消失
B.图Ⅱ所示装置为用酒精提取溴水中的溴
C.可用CCl4提取溴水中的Br2
D.检验Br-时,在溶液中先加入氯水再加入CCl4,振荡、静置,观察下层溶液
是否显橙色
1 2 3 4 5
解析 Br2能与NaOH反应:Br2+2NaOH===NaBr+NaBrO+H2O,上层溶液颜色
高中化学必修二精品课件:微项目 海带提碘与海水提溴——体验元素性质递变规律的实际应用

(3)操作方法
分液漏斗
四氯化碳
活塞
玻璃塞
水
四氯化碳
紫
烧杯壁 上口
(4)注意事项 ①振荡时,要不时的旋开活塞放气,以防止 分液漏斗 内压强过大引起危险。 ②分液时,要将漏斗下端管口紧贴烧杯内壁,使液体顺利流下,防止__液__体__ 飞溅 。 ③下层液体要从下口放出,恰好流尽时及时关闭活塞,防止 上层液体 流出。 ④上层液体要从上口倒出,保证上层液体尽量少地沾附下层液体 。
跟踪强化
1.目前从海水中提取的溴约占世界溴年产量的三分之一,从海水中提取溴的主
要步骤可表示为 A.氧化→吸收→吹出 C.吹出→氧化→吸收
√B.氧化→吹出→吸收
D.吹出→吸收→氧化
解析 从海水中提取溴,先用氧化剂将溴离子氧化为溴单质,再用热空气吹 出后用碱液吸收。
1234
2.目前从海水中提取溴常用的方法之一是用氧化剂把溴离子氧化成单质,再通
1234
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用__D___(填
字母)。
A.浓硫酸
B.新制氯水
C.酸性高锰酸钾溶液
D.过氧化氢溶液
理由是_双__氧__水___又__称__“__绿__色__氧__化__剂__”__,__其__参__加__氧___化__还__原__反__应__时__还__原__产__物__为__水__,
上层液体要从上口倒出保证上层液体尽量少地沾附分液漏斗液体飞溅上层液体下层液体海带紫菜中均含有丰富的碘元素从海带中提叏碘单质的流程如下思考解答下列问题
第1章 原子结构 元素周期律
核心素养发展目标
1.以海带提碘和海水提溴为例,体会元素周期律、元素周期表在分析、解决 实际问题中的价值。 2.以海带提碘和海水提溴为例,形成物质分离、富集、提取的基本思路,体 会绿色化学观念在生产实际中的应用。
高一化学海水提溴和海带提碘PPT 课件

3.从海水中提取溴的过程如图表示:
海水
酸化
氧化
吹出
吸收
酸
氧化剂
热空气
氧化
溴
氧化剂
(1)为什么要在酸性条件下,而不能在碱性条件下氧化溴离子? 答:氧化剂使用的是氯水,所以要在酸性条件下,因为Cl2+NaOH==NaCl+NaClO+H2O
(2)写出用氯气氧化溴离子的离子方程式__C__l2_+_2_B_r_-→__B_r_2+_2Cl-
华[素有片效中期含]二有年主要成分是(用分子式表示)____I_2___。 已知该药片不含糖衣,则华素片___不__是___(填“是”或“不是”)白色的。 为验证华素片中确有上述成分,进行如下实验: 取一粒药片放入研钵中研碎,再将粉末装入试管并加入约2mL蒸馏水, 再向该试管内加入约2mL___C__C_l4__(从酒精、四氯化碳)中选择,并用力振荡、静置。
; /branddtl/22 希岸精品酒店连锁加盟
知识点2:氯、溴、碘单质活泼性比较
1.下列各组物质之间能发生置换反应的是
(A )
A氯气通入碘化钠溶液中 C碘水加入溴化钠溶液中 中
B氟气通入氯化钠溶液 D溴水加入氯化钠溶液
2. 关于卤族元素的说法不正确的是 A.单质的熔、沸点随核电荷数的增加而逐渐升高 B.单质的颜色随核电荷数的增加而逐渐加深 C.单质跟H2的反应随核电荷数的增加而越来越难 D.氢化物的稳定性随核电荷数的增加而逐渐增强
液体分层,下层呈紫红色 实验后可能观察到的现象是________________________________,
选用该液体做实验的原因是___四__氯_化__碳__不__溶__于_水__,__且__碘__在__其_中__的__溶__解。度大于在水中的
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(
D)
3. 甲、乙、丙三种溶液中各含一种卤素离子,往甲中加淀粉和氯水,则溶液变 蓝色,再往丙中加淀粉和氯水,无明显现象。则甲、乙、丙依次含有 ( C )
A.Br-、I-、Cl-
B.Cl-、I-、Br-
C.I-、Br-、Cl-
D.Br-、Cl-、I-
4. 在KBr和KI 混合溶液中,通入过量的氯气,反应后蒸干溶液,灼热,残留物为( A ) A.KCl B.KCl和 KBr C.KCl和 KI D.KCl、Br2和 I2
知识点1:海水提溴和海带提碘
1. 下列哪组溶液混合后,振荡,静置,上层液体为无色,下层为橙色( C )
A.溴水、酒精
B.碘水、汽油
深红棕色
C.溴水、四氯化碳
刺激性气味 液
D.碘水、四氯化碳
2.单质溴在常温下是________,具有________气味,呈____态.苯是一种不溶于水 且比水轻的有机溶剂,溴_______ 易 溶于苯,现要把溴水从水中除去,加入苯充分 振荡后,再用_______ (仪器名称)分离得到溴和苯的混合液,这一实验方法称 分液漏斗 为_______ 萃取 。
(3)步骤④中可以观察的现象是 溶液分层,上层近无色,下层紫红色 。
5.关于药品华素片的使用说明书的部分内容如下: 华素片(西地碘片)使用说明书 [品名和组成] 品名:西地碘片 商品名:华素片 英文名:Cydiodine Tablets 华素片(西地碘片)的主要活性成分是分子碘,含量1.5mg/片,将碘利用分子分散技术制 [贮藏]遮光、密闭、在凉处保存 [有效期]二年 I2 华素片中含有主要成分是(用分子式表示)________ 。 不是 (填“是”或“不是”)白色的。 已知该药片不含糖衣,则华素片________ 为验证华素片中确有上述成分,进行如下实验: 取一粒药片放入研钵中研碎,再将粉末装入试管并加入约2mL蒸馏水, CCl4 (从酒精、四氯化碳)中选择,并用力振荡、静置。 再向该试管内加入约2mL________ 液体分层,下层呈紫红色 实验后可能观察到的现象是________________________________,
A氯气通入碘化钠溶液中 C碘水加入溴化钠溶液中 中
B氟气通入氯化钠溶液 D溴水加入氯化钠溶液
2. 关于卤族元素的说法不正确的是 A.单质的熔、沸点随核电荷数的增加而逐渐升高 B.单质的颜色随核电荷数的增加而逐渐加深 C.单质跟H2的反应随核电荷数的增加而越来越难 D.氢化物的稳定性随核电荷数的增加而逐渐增强
3.从海水中提取溴的过程如图表示:
海水 酸化
酸
氧化
吹出
吸收
氧化
溴
氧化剂
热空气
氧化剂
(1)为什么要在酸性条件下,而不能在碱性条件下氧化溴离子? 答:氧化剂使用的是氯水,所以要在酸性条件下,因为Cl2+NaOH==NaCl+NaClO+H2O Cl2+2Br-→Br2+2Cl(2)写出用氯气氧化溴离子的离子方程式______________ B 和_____. D (3)氧化后用热空气将生成的单质溴吹出,选用他的原因是_____
5.向氯化钙、溴化钠、碘化钾混合溶液中通入氯气后,若溶液中含有Br2, 则一定不含有 A.Cl2 B.I- C.Br- D.Cl-
( B)
四氯化碳不溶于水,且碘在其中的溶解度大于在水中的 选用该液体做实验的原因是________________________________。 碘易升华 说明书中的贮藏方法,是因为________________________________ 而提出的。
知识点2:氯、溴、碘单质活泼性比较
1.下列各组物质之间能发生置换反应的是 ( A )
4.海洋植物如海带、海藻中含有丰富的碘元素。 碘元素以离子的形式存在。实验室里海藻提取碘的流程如下:
①灼烧 海藻 海藻灰
浸泡Βιβλιοθήκη 海藻灰 悬浊液② 含碘离子溶液
③
蒸馏 单质碘 含碘的CCl4溶液
④ 含碘 水溶液
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是( B. D. )E. A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器 (2)指出提取碘的过程中有关的实验操作名称:② 过滤 ;④ 萃取 。
