大学有机化学第十章羧酸及其衍生物
有机化学——10羧酸衍生物和脂类

=
R C OH + N2 + H2O
3.霍夫曼降解反应
=
O R C NH2 + Br2
NaOH
R NH2 + NaBr + Na2CO3 + H2O
反应使碳链减少一个碳原子
=
O
O
五、碳酸衍生物
(一)脲(尿素)——碳酸的二元酰胺
1. 弱碱性 不能使石蕊试纸变色, 只能与强酸成盐
= = =
O R C NHOH +
=
R'COOH
O
R C O R'
=
+ H NH OH
O R C NHOH +
= =
R'OH
O
R C NH2 + H NH OH
O R C NHOH + NH3 异羟肟酸
3R C NHOH + FeCl3
=
异羟肟酸铁 (红~紫色)
可用做羧酸及其衍生物的定性检验
=
O
O (R C NHO)3Fe + 3HCl
(四)酯缩合反应
具有α-H的酯在碱的作用下与另一分子酯发生 反应称酯缩合反应或克莱森(Claisen)缩合反应
CH3 O O O O ① C2H5ONa C OC2H5 + H CH2 C O C2H5 CH3 C CH2 C OC2H5 + C2H5OH ②H
=
=
=
(五)还原反应
卤、酸酐和酯还原成伯醇
乙酰乙酸乙酯 β 丁酮酸乙酯
羧酸衍生物比羧酸容易还原。氢化铝锂可将酰
=
O R C O R C
有机化学--羧酸及其衍生物

POCl3
HCl↑
O R C OH
SOCl2
O R C Cl
SO2↑
低、高沸点 ↑ HCl 的酰氯制备 都适合
② 酸酐的生成
羧酸在脱水剂如五氧化二磷的存在下,加热。两分子羧 酸失去一分子水而形成酸酐。
R-C OH R-C OH O R-C O R-C + H2O
P2O5
△
(产率较低)
O
分子量较大的羧酸在乙酐(作脱水剂)存在下,失水生 成酸酐。反应平衡中发生了酸和酸酐的交换。 O O CH3-C 2R-C-OH + O CH3-C O
任何使酸根负离子稳定的因素都将增加其酸性,羧酸根负离 子愈稳定,愈容易生成,酸性就愈强。
(1)电子效应的影响
诱导效应:X—COOH
-I使酸性增强, +I使酸性减弱
X= F Cl Br I CHO 3.53 NO2 1.68
+N(CH ) 3 3
pKa 2.66 2.86 2.90 3.18
1.83
O CH3CH2 C
丙酰基
O C
苯甲酰基
CH3 CH3 CH3CH-CHCH2COOH CH3CH-CHCH21 COOH 4 3 2 CH2CH3 CH
5 6 3
CH3-C =CH-COOH CH3 3-甲基-2-丁烯酸
γ β α
4
3
2
1
3,4-二甲基戊酸 CH2-COOH CH2-COOH 丁二酸
羧酸铵盐 腈的水解为其逆反应:
酰胺
腈
O C OH + HNH-
O C NHN-苯基苯甲酰胺
+ H2 O
扑热息痛
3、羧基的还原 (LiAlH4)
第十章 羧酸及其衍生物

+ H OC2H5
18
H
+
O CH3C
18
OC2H5 + H2O
酰氧断裂
12
O CH3C OH
:OH
+H
+
OH CH3C OH 加成
-H2O
HOC2H5
OH CH3 C OH HOC2H5
OH CH3 C OC2H5
: : : : : : : :
质子迁 移
-H+
O CH3 C OC2H5
1
I 羧酸
一,结构 烃基与羧基相连的物质叫羧酸:一元羧酸通式为 RCOOH;羧基( COOH)就是羧酸的官能团 RCOOH;羧基(-COOH)就是羧酸的官能团. 就是羧酸的官能团.
O
ห้องสมุดไป่ตู้
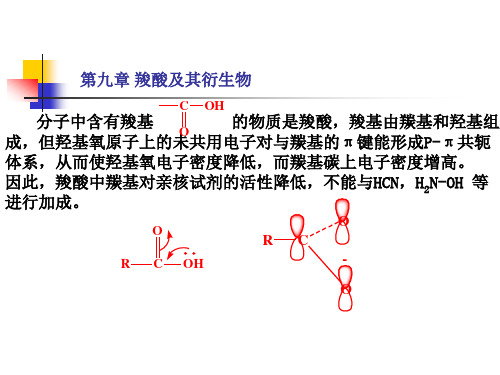
中碳为SP 杂化, OH 中碳为SP2 杂化,氧原子与羰基双键间存 在着P― 共扼.由于共扼, P―л 在着P―л共扼.由于共扼,使羧基中的羰基失去了典 型的羰基的性质(如不与NH OH作用 作用) 型的羰基的性质(如不与NH2OH作用);―OH 氧原 子上的电子云向羰基偏移,这有利于―OH氢的离解 氢的离解. 子上的电子云向羰基偏移,这有利于―OH氢的离解.
14
Br2 / P
(2)芳香环的取代反应 (2)芳香环的取代反应
COOH Br2 FeBr3
COOH
Br
5. 二元羧酸的受热反应
乙 二 酸 HOOCCOOH 丙 二 酸 HOOCCH 2COOH 丁二酸 CH 2 COOH CH 2 COOH 戊 二 酸 CH 2 CH 2COOH CH 2COOH
CH 3 COOH + C 2H 5 OH : 1 1 1 : 10
有机化学第10章羧酸及其衍生物
. 6H O 2
Ⅱ羧酸衍生物
羧酸分子中的羧基被不同基团取代的产物—羧酸的衍生物。 一、命名
酰氯和酰胺的命名相同,以它所含酰基命名
O O C CH 3 C Cl Cl CH3 C NH2 C NH2 O O
O H C N
CH3
O C H 3 C N H C H 2C H 3
CH3
N,N‘—二甲基甲酰胺(DMF)
O H2 R
'
+
-H R
+
O R C OR
'
H
(4)酰胺的形成
先得到铵盐,将铵盐加热,首先失去一分子水,生成酰胺,继续加热失水成腈。
O R C OH O O ONH
4
+
NH3
R
C
-H 2 O
R
C
NH2
-H 2 O
R
C
N
正好是腈水解的逆反应。 芳香、二元羧酸同样具有上述反应,可生成单酰氯、单酯也可生成二酰氯二酯。
2-丁烯酸
二元羧酸、 选取含有两个羧基的最长碳链,叫某二酸。
COOH H 3 CH 2 C H C HOOCCH COOH
2 CH 2 CH 2 CH 2 COOH
乙基丙二酸
HOOCCH=CHCOOH
已二酸
丁烯二酸 芳香酸:把芳环作为取代基
COOH COOH CH=CH-COOH HOOCH
2C
邻苯二甲酸
三、化学性质 1、酸性 RCOOH可看作 HOH中的H被酰基
R O C
取代的产物。
由于羰基的π 键与羟基氧原子上未共用电子对形成P-π 共轭体系,—OH氧上电子密度因向羰基转移而有所降低,使得—OH中氢氧间电 子密度降低,键强度减弱,以致—OH中的氢以质子形成离解,所以酸性比弱酸 和水强得多。但与强酸相比,羧酸只属于弱酸。
大学有机化学下学期复习题

N-亚硝基化物 油层 丙醇 水相
①HCl ②NaOH
乙醚提取蒸馏
41
(4)
酰化N-甲基苯胺
乙酰氯
水相(NaOH中和)
HCl
油相
乙醚提取
洗涤蒸馏
42
9.完成下列转换
Cl Cl
(1)
NH2 NO2
CH3
NH2 NO2
(2)
NO2
CH3
43
Cl
Cl
(1)
NH2 NO2
Cl
(CH3CO)2O
Cl
Cl HNO3
10%NaOH 水溶液
水层
辛酸盐
加盐酸 调PH至酸性
辛酸
己醛 有机层 和1-溴丁烷 饱和亚硫酸氢钠
有机层 1-溴丁烷
水层
白色固体
水层
白色固体
加盐酸 调PH至酸性
己醛
6
4、将下列化合物按指定性质的活泼程度从小到大排列成序
(1)将下列化合物按醇解反应速率快慢排序: A. 苯甲酰氯 B.丙烯酰氯 C. 乙酰氯
CH3
KMnO4 H+ COOH
CN
CONH2 1) SOCl2 2 ) NH3
CN P2O5
CN HNO3 H2SO4 NO2
Fe HCl
CN
NH2
CN NaNO2 HCl CN CuCN
48
(5)
Cl
CH2CH3
Cl
NH2
(6)
NHCH3 CH3
49
Cl
CH2CH3
Cl
NH2
(5)
KMnO4
36
6. 在一组分子量相近的伯、仲和叔胺中,为何通 常伯胺的沸点最高?
有机化学-- 羧酸及其衍生物

碱性水解
O
OH-
RC
OR'
O R C OR' OH
O R C + -OR'
OH
O
RC OH
H+
O
R C + HOR'
O-
同位素跟踪结果表明: 碱性水解时,发生酰氧键断裂。
O
O
C2H5C18OC2H5 + H2O NaOH CH3CONa + C2H518OH
碱性水解的讨论
1. 碱性水解速率与 [-OH]成正比。
OO C RO R
酸酐 carboxylic acid anhydride
RCN
腈 nitrile
➢羧酸及其衍生物的命名和物理性质 ➢羧酸及其衍生物的制备 ➢羧酸衍生物的水解、醇解和氨解 ➢羧酸及其衍生物的还原反应 ➢羧酸及其衍生物-碳的反应
羧酸及其衍生物的命名
HCO2H CH3CO2H CH3(CH2)16CO2H
(4) 在RCOOR'中, R对速率的影响是: 一级 > 二级 > 三级 R'对速率的影响是: 三级 > 一级 > 二级
CH3COOR'在盐酸中,于25OC时水解的相对速率v的 实验数据如下:
R': CH3 C2H5 CH(CH3)2 C(CH3)3
v: 1 0.97
0.53 1.15(历程不同)
2.98
CO2H OR
水杨酸: R = H O
阿司匹林: R = -CCH3
羧酸及其衍生物的制备
1. 羧酸的制备
(1)醇和醛的氧化
RCH2 OH
or O
RC H
KMnO4 or
大学有机化学羧酸及其衍生物习题答案

第十章羧酸和取代羧酸习题1.用系统命名法命名下列化合物(标明构型)。
(1){EMBED ChemDraw.Document.6.0 \* MERGEFORMAT |COOHCOOHClHHCl(2)(3)(4) (5) (6)(7) (8) (9)2.写出下列化合物的结构式。
(1)反-4-羟基环己烷羧酸(优势构象)(2)(2S,3R)-2-羟基-3-苯基丁酸(3)7,9,11-十四碳三烯酸(4)(R)-2-苯氧基丁酸(5)丙二酸二甲酯(6)(E)-4-氯-2-戊烯酸(7)2-甲基-4-硝基苯甲酸3.用化学方法分离下列各组混合物。
(1)辛酸、己醛、1-溴丁烷(2)苯甲酸、对甲酚、苯甲醚4.将下列各组化合物按酸性由大到小顺序排列。
(1)(A)丁酸(B)顺丁烯二酸(C)丁二酸(D)丁炔二酸(E)反丁烯二酸(2)(A)(B)(C)(D)(3)(A)α-氯代苯乙酸(B)对氯苯甲酸(C)苯乙酸(D)β-苯丙酸5.回答下列问题。
(1)为什么羧酸的沸点及在水中的溶解度较相对分子质量相近的其他有机物高?(2)苯甲酸和邻氯苯甲酸都是不溶于水的固体,能用甲酸钠的水溶液将其混合物分开,为什么?(3)如果不用红磷或三卤化磷作催化剂,可以采用什么方法使羧酸的α-卤代反应顺利进行?说明理由。
6.写出下列反应的主要产物。
(1) (2)(3)(4)(5) (6)(7) (8)(9) (10)7.下列化合物在加热条件下发生什么反应?写出主要产物。
(1)3-苯基-2-羟基丙酸(2)邻羟基苯乙酸(3)2-环戊酮羧酸(4)顺-β(邻羟基苯)丙烯酸(5)丁二酸(6)庚二酸8.用化学方法区别下列各组化合物。
(1)乙醇,乙醛,乙酸(2)水杨酸,2-羟基环己烷羧酸,乙酰水杨酸(3)甲酸,草酸,丙二酸(4)对甲基苯甲酸,对甲氧基苯乙酮,2-乙烯基-1,4-苯二酚9.指出下列反应式中存在的问题。
(1)(2)(3)(4)10.按由快到慢的次序排列下列醇或酸在酸催化下酯化时的速度。
有机化学10第10章 羧酸及其衍生物

• 取代基的供电子(+I效应)强弱次序:
•注意: 与苯环、1,3-丁二烯和烯烃的-,p-共轭效应比较: 共轭效应是指在共轭体系中原子间的一种相互影响,这种 影响造成分子更加稳定,内能更小,键长趋于平均化。 共 轭效应常与诱导效应同时存在,共同起作用。(苯的定位)
有机化合物酸性的强弱主要受其结构的电子效应、杂 化、氢键、空间效应和溶剂的影响。 1. 羧酸的酸性 (1) 脂肪族羧酸
CH3
KMnO 4 / NaOH
COOH
KMnO 4 / NaOH
C2 H5
CH3
K2Cr2O 7 / H2SO 4
COOH
NO2
NO2
CH(CH3)2
Na2Cr2O 7 / H2SO 4
COOH
COOH (CH2)6CH3
CH3
KMnO 4 / NaOH
COOH
侧链是叔烷 基,很难氧 化,强氧化 剂时环发生 破裂。
• 羧酸的沸点高于质量相近的醇——双分子缔合
O H O CH3 C O H O C CH3
R O H O R H O H O R R H
10.4 羧酸的化学性质
-H取 代反应
H C
O C O
C=O 基亲核加成 O H 键断裂而
呈酸性
R
H
脱羧反应
H
OH被取代反应
羧酸的化学反应包括: (1) O—H键的酸性; (2) —H取代反应 (3) —OH基取代反应; (4) C=O亲核加成 (5) 脱羧反应
第十章 羧酸及其衍生物、取代羧酸
(一)羧酸
10.1 羧酸的结构、分类和命名
——羧酸的分子中都含有羧基官能团
10.1.1 羧酸的结构
《羧酸及其衍生物 》课件

沸点和熔点
羧酸通常具有较高的沸点和熔 点,这取决于分子间的氢键形 成。
酸性
羧酸在水中可与碱发生中和反 应,产生相应的盐。
羧酸的化学性质
酯化反应 氧化反应 酰化反应
羧酸与醇反应生成酯,常用于合成香料和涂料。
羧酸可以被氧化剂氧化为相应的醛、酮或羧酸。
羧酸与胺类化合物反应生成酰胺,常用于药物合 成。
羧酸衍生物的合成方法
农业工业
在食品工业中,羧酸及其盐被用作防腐剂和增味剂。
羧酸衍生物被广泛用于制备农药和肥料,以提高农 作物的产量和质量。
结论和总结
通过本课件,我们了解了羧酸及其衍生物的基本概念、结构与分类、物理性质、化学性质、合成方法以及应用 领域。希望这些内容对大家的学习和工作有所帮助。
1
卤代羧酸
通过将羧酸与卤化物反应,生成相应的卤代羧酸。
2
酸酐
通过羧酸与酸性还原剂反应,生成相应的酸酐。
3
酯化反应
通过羧酸与醇反应,生成相应的酯。
羧酸及其衍生物的应用领域
化学工业
羧酸及其衍生物广泛用于制备染料、塑料和涂料等 化学产品。
制药工业
羧酸衍生物被广泛应用于药物合成和药物交付系统 的设计。
食品工业
《羧酸及其衍生物》PPT 课件
本课件将介绍羧酸及其衍生物的基本概念、结构与分类、物理性质、化学性 质、合成方法以及应用领域,旨在通过生动的内容让大家更好地理解羧酸及 其衍生物。
羧酸的基本概念
羧酸是一类分子中含有羧基(-COOH)的有机化合物,具有酸性。它们在许多生物和化学过程中起着重要的作 用。
羧酸的结构与分类
脂肪酸
由长链烃基与羧基组成,常见于天然油脂和脂 肪中。
羧酸盐
第十章羧酸及其衍生物芳香烃_2090.ppt

化学工业出版社
高职高专“十一五”规划教材
§10.1 羧 酸
二、羧酸的性质
(一) 物理性质 氢键缔合:
O HO
R CO H
CR O
医药化学 基础
化学工业出版社
高职高专“十一五”规划教材
§10.1 羧 酸
二、羧酸的性质
(二)化学性质 易发生化学反应的主要部位如下:
医药化学 基础
RO HC COH
H ④ ③② ①
§10.1 羧 酸பைடு நூலகம்
一、羧酸的分类和命名
(二)羧酸的命名 2. 系统命名法
二元脂肪酸:
HOOC(CH2)4COOH 己二酸
HOOCCH CHCOOH 丁烯二酸
OH HOOC CH2 C CH2 COOH
COOH 3-羟基-3-羧基戊二酸
医药化学 基础
化学工业出版社
高职高专“十一五”规划教材
§10.1 羧 酸
① 氧氢键断裂呈酸性 ② 羟基被取代,生成羧酸衍生物 ③ 羧基的还原和脱羧反应 ④ α- H的取代反应
化学工业出版社
高职高专“十一五”规划教材
§10.1 羧 酸
二、羧酸的性质
(二)化学性质
1. 酸性
O
R C OH
O
R C O- +H+
医药化学 基础
R C O O H+NaOR H C O O N a+H 2O + + + RCOOH NaHCO3 RCOONa CO2 H2O
医药化学 基础
H C O O H> C H 3 C O O H> C H 3 C H 2C O OH> (C H 3) 2C HC O O H> ( C H 3) 3C C OO H pK 3a .74 7.764.86 4.87 5.05
第十章 羧酸及其衍生物

第十章羧酸及其衍生物羧酸及其衍生物❖羧酸及其衍生物的结构特征;❖羧酸及其衍生物的物理和化学性质;❖乙酰乙酸乙酯和丙二酸酯的特性及其在有机合成上的应用;❖蜡和油脂,碳酸衍生物重点要求掌握羧酸及其衍生物的化学性质;乙酰乙酸乙酯在有机合成上的应用。
10.1 羧酸10.1.1 羧酸的构造、分类和命名1、羧酸的构造和分类分子中具有羧基的化合物,称为羧酸。
它的通式为 RCOOH。
2、命名由它的来源命名:甲酸最初是由蚂蚁蒸馏得到的,称为蚁酸。
乙酸最初是由食用的醋中得到,称为醋酸。
还有草酸、琥珀酸、苹果酸、柠檬酸。
系统命名:含羧基最长的碳链作为主链,根据主链上碳原子数目称为某酸.编号从羧基开始.3,4-二甲基戊酸3-甲基-2-丁烯酸芳香族羧酸可以作为脂肪酸的芳基取代物命名:羧酸常用希腊字母来标名位次,即与羧基直接相连的碳原子为α,其余位次为β、γ…,距羧基最远的为ω位。
二元酸命名:10.1.2 羧酸的物理性质在室温下10个碳原子以下的饱和一元羧酸是液体。
10个碳原子以上的羧酸为石蜡固体,挥发性很低,无气味。
4~9个碳原子的脂肪酸具有腐败恶臭、动物的汗液和奶油发酸变坏的气味。
饱和一元羧酸的沸点比相对分子质量相似的 醇还要高。
饱和一元羧酸的熔点随分子中碳原子数目的增加呈锯齿状的变化。
低级脂肪酸易溶于水,但随分子量的增高而降低。
甲酸与水通过氢键缔合在固态和液态,羧酸主要以二聚体形式存在。
低级的羧酸,在气相时仍以双分子缔合状态存在。
10.1.3 羧酸的化学性质OOH H HOH O HH HHOCRCOOHOORHO ORHCC2HOR H O HC Cα10.1.3.1 酸性羧酸具有弱酸性,在水溶液中存在着如下平衡:乙酸的离解常数K a 为1.75×10-5 甲酸的K a =2.1×10-4 , p Ka =3.75其他一元酸的K a 在1.1~1.8×10-5之间, p Ka 在4.7~5之间。
[精选]第十章羧酸及其衍生物资料PPT课件
![[精选]第十章羧酸及其衍生物资料PPT课件](https://img.taocdn.com/s3/m/9731d55a87c24028905fc310.png)
C H3 H H 2 2 S O4 OH3 C
O C OH C H3
MgBr
+O C O
CO 2MgBr H+ H2O
COOH
02.11.2020
Organic Chemistry
13
§13.2 羧酸的制法
四、醇、醛的氧化
[ O ]
O [ O ] O
R O H
RH
R O H
如:
OH
K M n O 4 + H 2 S O 4
羰基的亲核加成,然 后再消除(表现为羟 基的取代)。
02.11.2020
Organic Chemistry
19
§13.4 羧酸的化学性质
一、酸性
1、酸性与成盐
羧酸衍生物
• §13.6 分类命名 • §13.7 制法 • §13.8 物理性质 • §13.9 化学性质 • §13.10 重要的衍生物
02.11.2020
Organic Chemistry
2
§13.1 羧酸的分类和命名
02.11.2020
Organic Chemistry
3
§13.1 羧酸的分类和命名
p-π共轭使羧酸
分子中既不存在
典型羰基,也不
存在典型羟基。
Organic Chemistry
18
§13.4 羧酸的化学性质
O
O C
形 式 上 看 羧 基 是 由 一 个 C和 一 个 O组 H 成
OH 实 质 上 并 非 两 者 的 简 单 组 合
酸性
O
R CCOH
H
-活泼H的反应
羰基的亲核加 成,还原。
H 2C CH COOH
【全文】张文勤有机化学(第五版)第十章-羧酸及其衍生物

O Cl3C C OH △
CHCl3 + CO2
在脱羧反应中最典型的是羰基酸脱羧
二元羧酸的热分解反应
2. 脱水反应 丁二酸及戊二酸加热至熔点以上则脱水生成
环状酸酐
3. 脱羧及脱水反应
五元环或六元环化合物容易形成
六、羧酸的制备
1. 羧酸的工业合成 (了解) (1) 烃的氧化
烷烃氧化
芳烃氧化
(2) 由一氧化碳、甲醇或醛制备
应用: 由伯酰胺制备少一个碳原子的伯胺
5. 与HNO2的反应
酰胺只能是伯酰胺 可用来鉴别伯酰胺 四、酰胺的生成 1.羧酸衍生物的氨解
2.羧酸的铵盐加热失水而得
△
小结 羰基的亲核取代反应
① 水解
相应的羧酸
O
R-C-Cl
OO
反 应 速
R-C-O-C-R/
O
+ H-OH
度 R-C-OR/
递
O
增 R-C-NH2
遇水则又水解为酰胺和盐酸。
二、酰胺的物理性质 在常温下,除甲酰胺是液体外,其它酰胺多为
无色晶体。
熔点、沸点甚至比相对分子质量相近的羧酸还高。
低分子量酰胺易溶于水,随着相对分子质量的 增大,溶解度逐渐减小。 三、酰胺的化学性质
1.水解 酰胺与酯一样在酸碱催化下可水解,生成羧酸或盐。
实际上,酰胺的水解(O=C-N键断裂)较难
例:
9. 歧化反应
§11-4 羧酸衍生物的结构和命名
一、羧酸衍生物的结构
酰卤 酯 酸酐 酰胺
L=X,NH2,OR ………
羧酸衍生物 在结构上的 共同特点是 都含有酰基
羰基与杂原子相连
(1)L和碳相连的原子上有未共用 电子对,故具有给电子共轭效应 (2)与酰基相连的原子的电负性 都比碳大,故有吸电子诱导效应
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
d. CH3CH2CH2CH2OHபைடு நூலகம்e. C6H5OH f. H2CO3g. Br3CCO2H h. H2O
答案:
酸性排序g > a > b > c > f > e > h > d
10.3写出下列反应的主要产物
答案:
10.4用简单化学方法鉴别下列各组化合物:
10.5完成下列转化:
答案:
10.6怎样将己醇、己酸和对甲苯酚的混合物分离得到各种纯的组分?
答案:
10.7写出分子式为C5H6O4的不饱和二元羧酸的各种异构体。如有几何异构,以Z,E标明,并指出哪个容易形成酐。
答案:
(Z)易成酐(E)不易(Z)易成酐(E)不易成酐
10.8化合物A,分子式为C4H6O4,加热后得到分子式为C4H4O3的B,将A与过量甲醇及少量硫酸一起加热得分子式为C6H10O4的C。B与过量甲醇作用也得到C。A与LiAlH4作用后得分子式为C4H10O2的D。写出A,B,C,D的结构式以及它们相互转化的反应式。
答案:
第十章羧酸及其衍生物
10.1用系统命名法命名(如有俗名请注出)或写出结构式
n.尿素o.草酸p.甲酸q.琥珀酸r.富马酸s.苯甲酰基t.乙酰基
答案:a.2-甲基丙酸(异丁酸)b.邻羟基苯甲酸(水杨酸)c. 2-丁烯酸d 3-溴丁酸e.丁酰氯f.丁酸酐g.丙酸乙酯h.乙酸丙酯i.苯甲酰胺j.顺丁烯二酸
10.2将下列化合物按酸性增强的顺序排列:
