LiAlH4还原剂
浅谈氢负离子还原剂LiAlH4与NaBH4.

浅谈氢负离子还原剂LiAlH4与NaBH4张媚(西北大学化学系05级化学班西安 710069)摘要:本文总结它们所参与的反应类型,并介绍两者之间的异同点和相关反应机理,从而阐明它们在合成中的重要性。
关键字:四氢铝锂硼氢化钠还原一、引言众所周知,在有机合成中还原反应有着极为重要的地位。
其中,作为重要还原剂的氢负离子类化合物四氢铝锂和硼氢化钠更在合成反应中起着举足轻重的作用。
二、四氢铝锂和硼氢化钠四氢铝锂和硼氢化钠这两种还原即可还原许多类化合物,它们自身的理化常数为:1.还原卤代烷制备卤代烃例:CH3(CH2)8CH2Br机理:Li+ H3AlHCH3(CH2)8CH3CH2RXRCH3+AlH3+LiXCH3(CH2)6CH2X二甘醇二甲醚CH3(CH2)6CH3注意:四氢铝锂只能在无水条件下进行反应,而硼氢化钠没有此限制,这表明两种物质反应时所需要的介质是不一样的。
2.还原炔氢四氢铝锂还原为反式烯烃1 LiAlH4CH3CCH2CH3CHCH2注意:硼氢化钠不能还原炔烃 3.还原羰基化合物(1):醇的制备ORCORCORCORCR'NaBH4 或 LiAlH4或催化氢化ROR'LiAlH4Na, EtOHRCH2OHOHCHR'仲醇伯醇OHLiAlH4RCH2OH伯醇HNaBH4 或 LiAlH4或催化氢化RCH2OH伯醇以上表明,四氢铝锂可以还原醛、羧酸、酯、酮等羰基化合物,而硼氢化钠只能还原醛和酮以及酰卤等类化合物。
例:1. NaBH4CH3CHCHCHOCH3CHCHCH2OH2.H2O2. H2OCH3CHCHCH2OH例:CH3CHCHCHOO+LiAlH41.EtO2OH98%H2CCHCH2COOH,Et2H2CCHCH2CH2OHNaBH4CH3COOHO不反应特点:双键不受影响,四氢铝锂还原性强于硼氢化钠酰氯:O酐:RCOOCR'LiAlHCl2. H2ORCH2OHRC2. H2ORCH2OH+R'CH2OH:OH酮:机理:R1. NaBH42OBH3NaORORCHROBH2ORCHRCRHO2HCOOCHRB22OCHR2NaOCHROH4RCHR+B(OH)+NaOH(2):制备胺类CH3)22.H2ON,N-二甲基环己基甲酰胺2N(CH3)2(88%)N,N-二甲基环己基甲酰胺C6H5C6H52,2-二苯基环己酮6H5C6H5 22C6H5C6H5(80%) 2,2-二苯基环己胺RClRCNRCH2NH24.氢负离子还原羰基化合物的反应历程氢负离子的还原羰基化合物实质上就是亲核加成反应,四氢铝锂和硼氢化钠对羰基的还原反应原理是一样的,它们都不能还原碳碳双键;而且,这类羰基加成反应实际上为不可逆反应,通常无副反应,所以可用于完成某些特定的合成工作。
有机lialh4作用

有机lialh4作用
有机锂铝氢化物(LiAlH4)是一种常用的还原剂,它在有机合
成中具有广泛的应用。
它的作用主要体现在以下几个方面:
1. 还原酮和醛,LiAlH4可以将酮和醛还原为相应的醇。
它的
还原能力很强,可以将碳氧双键还原为碳碳单键,生成醇。
例如,
乙酰酮可以被LiAlH4还原为乙醇。
2. 还原酯和酰卤,LiAlH4可以将酯和酰卤还原为醇和相应的
氯化物。
这个反应通常用于制备醇化合物或氯化物。
3. 还原羧酸和酰胺,LiAlH4可以将羧酸和酰胺还原为醇和胺。
这个反应通常用于合成醇和胺化合物。
4. 还原烯烃和炔烃,LiAlH4可以将烯烃和炔烃还原为相应的烃。
这个反应通常用于合成烃化合物。
5. 还原其他官能团,除了上述常见的官能团,LiAlH4还可以
还原其他一些官能团,如酰亚胺、硝基、卤代烷基等。
需要注意的是,使用LiAlH4时需要在惰性气氛下进行,因为它与空气中的水分和氧气反应剧烈。
此外,LiAlH4是一种强还原剂,具有较高的反应活性,因此在使用时需要小心操作,并遵循安全操作规程。
总结起来,有机锂铝氢化物(LiAlH4)是一种常用的还原剂,可以将酮、醛、酯、酰卤、羧酸、酰胺、烯烃、炔烃等多种官能团还原为相应的化合物。
它在有机合成中发挥着重要的作用。
还原亚胺实验报告

一、实验目的1. 了解亚胺还原反应的基本原理和方法。
2. 掌握实验室常用的亚胺还原剂及其应用。
3. 学习实验操作技能,提高实验操作水平。
二、实验原理亚胺是一种含有氮杂环的有机化合物,具有不饱和性质。
在实验室中,亚胺可以通过还原反应转化为胺。
还原反应是利用还原剂将亚胺中的氮原子上的孤对电子提供给还原剂,使氮原子上的孤对电子被还原,从而实现亚胺向胺的转化。
常用的亚胺还原剂有:LiAlH4、NaBH4、LiBHA、DIBAL-H等。
其中,LiAlH4和NaBH4是实验室常用的亚胺还原剂,具有还原效率高、选择性好的特点。
三、实验材料与仪器1. 实验材料:(1)亚胺化合物:N-甲基苯甲酰亚胺(2)还原剂:LiAlH4(3)溶剂:乙醚(4)其他试剂:无水乙醚、干燥剂、吸滤瓶、布氏漏斗、烧杯、量筒、磁力搅拌器、滴定管等2. 实验仪器:(1)电子天平(2)滴定管(3)磁力搅拌器(4)烧杯(5)吸滤瓶(6)布氏漏斗(7)冷凝管(8)真空泵四、实验步骤1. 准备实验材料:将亚胺化合物N-甲基苯甲酰亚胺用乙醚溶解,配制成一定浓度的溶液。
2. 配制还原剂溶液:将LiAlH4加入无水乙醚中,配制成一定浓度的还原剂溶液。
3. 还原反应:将亚胺溶液滴入装有还原剂溶液的烧杯中,加入少量干燥剂,磁力搅拌,控制反应温度在0-10℃。
4. 反应完成后,用吸滤瓶过滤混合物,收集滤液。
5. 将滤液滴入装有干燥剂的烧杯中,静置过夜,使胺类化合物析出。
6. 滤出胺类化合物,用乙醚洗涤,干燥,得到目标产物。
五、实验结果与分析1. 反应条件对还原率的影响:(1)温度:实验发现,反应温度在0-10℃时,还原率较高,温度过高或过低均会影响还原率。
(2)还原剂用量:实验发现,在一定范围内,增加还原剂用量可以提高还原率,但过量使用还原剂会导致副反应增多,影响目标产物的纯度。
2. 还原剂对还原率的影响:实验对比了LiAlH4和NaBH4两种还原剂,发现LiAlH4的还原率较高,但NaBH4的副反应较少,适用于对反应条件要求不高的亚胺还原反应。
乙酸和lialh4反应方程式

乙酸和LiAlH4反应方程式1. 简介乙酸是一种常见的有机酸,化学式为CH3COOH,分子量为60.05。
它是一种无色液体,在常温下有刺激性气味。
乙酸广泛用于化工、医药、食品等行业。
LiAlH4是四乙基铝锂的盐类,是一种常见的还原剂,化学式为LiAlH4,分子量为37.95。
它是一种白色结晶固体,在室温下不稳定。
乙酸和LiAlH4在一定条件下会发生反应,生成特定的产物。
2. 反应方程式乙酸和LiAlH4反应的化学方程式如下:CH3COOH + LiAlH4 -> CH3CH2OH + LiAlO2H33. 反应机理乙酸和LiAlH4在反应中,LiAlH4发生了还原作用,将乙酸中的羧基还原为羟基。
具体来说,LiAlH4可被分解成Li+和AlH4-离子,AlH4-离子中的氢原子具有较强的还原性,可以与乙酸中的羧基发生反应。
在反应过程中,氢离子被转移至羧基上,生成乙醇。
LiAlO2H3也会生成并存在于体系中。
4. 反应条件乙酸和LiAlH4反应是在一定的温度、溶剂和反应物比例下进行的。
在通常情况下,该反应需要在惰性气氛下进行,以防止产生危险的氢气。
另外,通常选择无水乙醚作为溶剂,以提供合适的反应环境。
还需要控制好反应物的摩尔比,以保证反应达到预期的效果。
5. 应用领域乙酸和LiAlH4的反应在有机合成领域有着广泛的应用。
由于LiAlH4是一种强还原剂,可以将许多含氧官能团还原为对应的碳氢键,因此乙酸和LiAlH4反应可以用于合成醇类化合物。
反应条件相对温和,适用于多种官能团存在的底物,因此在有机合成中应用广泛。
6. 安全注意事项乙酸和LiAlH4反应需要在安全条件下进行,以防止可能的意外发生。
LiAlH4具有较强的还原性,易与空气中的水分和氧气发生反应,释放出氢气,并且可以引起火灾或爆炸。
在反应过程中需采取适当的安全措施,如佩戴防护眼镜、手套等个人防护装备,并注意控制反应条件,避免发生意外。
总结乙酸和LiAlH4反应是一种重要的有机合成反应。
酯基被四氢铝锂还原后的产物

酯基被四氢铝锂还原后的产物全文共四篇示例,供读者参考第一篇示例:酯基是一种含有氧原子的有机官能团,它是许多有机物分子中常见的结构元素。
酯基被还原后得到的产物通常具有一定的化学活性,因此对其进行研究具有重要的理论和应用意义。
本文将重点介绍酯基被四氢铝锂还原后的产物及其性质。
四氢铝锂是一种常用的有机金属试剂,在有机合成中被广泛应用。
其作用机理是通过产生一个亲硫反应物,再通过亲核取代反应,从而实现有机物的还原。
酯基被四氢铝锂还原后,通常可以得到醇或醚这两种产物。
首先我们来介绍酯基被四氢铝锂还原后得到醇的情况。
一般来说,当酯基中的羰基与四氢铝锂反应时,羰基被还原为羟基,即醇。
这是由于四氢铝锂是一种亲硫还原剂,能够与酯基中的羰基发生反应,生成一个中间体,经过进一步反应得到醇。
这种反应通常在无水无氧条件下进行,以避免醇的进一步氧化。
醇是一种重要的有机官能团,具有多种应用价值,可以用于合成醚、醚等化合物。
另一种可能的产物是酯基被四氢铝锂还原后得到醚。
在一些情况下,四氢铝锂还原酯基不仅可以生成醇,还可以生成醚。
这是由于四氢铝锂对酯基的亲核取代反应较强,往往可以使酯基中的两个碳原子连接起来形成环状结构,从而生成醚。
醇和醚是两种常见的氧含有官能团,在化学和生物学领域有着广泛的应用。
醇具有亲水性,可以作为溶剂、试剂或反应中间体,广泛应用于有机合成、催化剂和生物技术等领域。
醚则是一种惰性官能团,具有良好的溶解性和稳定性,可以作为溶剂、抗氧化剂等。
除了醇和醚,还有一些其他可能的产物,如醛、酮等。
这取决于具体的反应条件、底物结构等多种因素。
有机合成化学家们通过对酯基被四氢铝锂还原的研究,可以进一步了解有机物分子结构和性质之间的关系,为新药物合成、材料科学等领域的发展提供重要的理论基础。
酯基被四氢铝锂还原后的产物种类繁多,有着广泛的应用价值。
通过深入研究这些产物的结构和性质,可以帮助我们更好地理解有机化学反应的机理和规律,为有机合成化学的发展提供有力支持。
氢化铝锂

谢谢观看
用途
用途
主要用作羰基试剂、还原剂。
应急方法
防护措施
泄露应急处理
急救措施
泄露应急处理
隔离泄漏污染区,限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。不要直接 接触泄漏物。
小量泄漏:避免扬尘,使用无火花工具收集于干燥、洁净、有盖的容器中。转移至安全场所。 大量泄漏:用塑料布、帆布覆盖,减少飞散。与有关技术部门,确定清除方法。
防护措施
呼吸系统防护:可能接触毒物时,应该佩戴头罩型电动送风过滤式防尘呼吸器。必要时,建议佩戴自给式呼 吸器。
眼睛防护:呼吸系统防护中已作防护。 身体防护:穿化学防护服。 手防护:戴橡胶手套。 其他:工作现场严禁吸烟。工作毕,淋浴更衣。注意个人清洁卫生。
急救措施
皮肤接触:立即脱去被污染的衣着,用大量流动清水冲洗,至少15分钟。就医。 眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼 吸。就医。 食入:误服者用水漱口,给饮牛奶或蛋清。就医。
R1通常以氢化铝锂的熔化开始,温度范围为150~170℃,接着立即分解为Li3AlH6,但是R1是在低于LiAlH4 熔点的情况下进行的。在大约200℃时,Li3AlH6分解成LiH和Al(R2),接着在400℃以上分解成LiAl(R3)。 反应R1在实际中是不可逆的,而R3是可逆反应,在500℃时的平衡压强是25千帕。在有适当催化剂的情况下,R1 和R2反应可以在常温下发生。
化学性质
热分解反应 氢化铝锂在常温下是亚稳的。在长时间的贮存中,氢化铝锂会分解成Li3AlH6和LiH。这一过程可以通过钛、 铁、钒等助催化元素来加速。当加热氢化铝锂时,其反应机理分为3步:
氢负离子还原剂LiAlH4与NaBH4
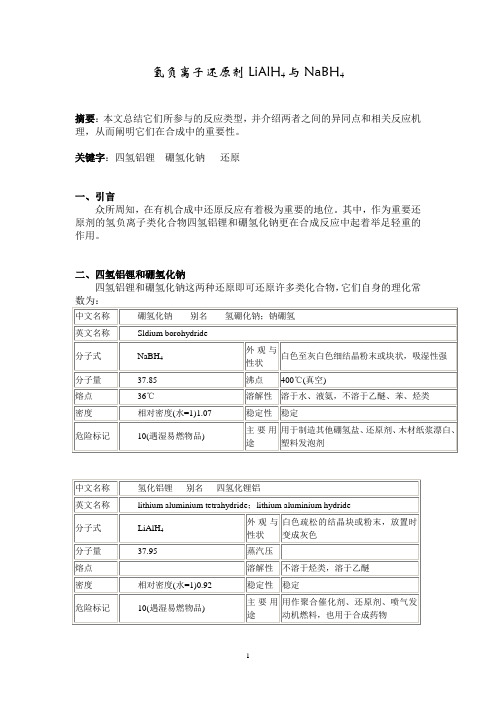
氢负离子还原剂LiAlH4与NaBH4摘要:本文总结它们所参与的反应类型,并介绍两者之间的异同点和相关反应机理,从而阐明它们在合成中的重要性。
关键字:四氢铝锂硼氢化钠还原一、引言众所周知,在有机合成中还原反应有着极为重要的地位。
其中,作为重要还原剂的氢负离子类化合物四氢铝锂和硼氢化钠更在合成反应中起着举足轻重的作用。
二、四氢铝锂和硼氢化钠四氢铝锂和硼氢化钠这两种还原即可还原许多类化合物,它们自身的理化常1.还原卤代烷制备卤代烃例:CH 3(CH 2)8CH 2Br LiAlH 4CH 3(CH 2)8CH 3机理:Li + H 3AlHCH 2RCH 3+AlH 3LiX++RCH 3(CH 2)6CH 2X4二甘醇二甲醚CH 3(CH 2)6CH 3注意:四氢铝锂只能在无水条件下进行反应,而硼氢化钠没有此限制,这表明两种物质反应时所需要的介质是不一样的。
2.还原炔氢四氢铝锂还原为反式烯烃CH 3C CH1 LiAlH 42CH 3CH CH 2注意:硼氢化钠不能还原炔烃3.还原羰基化合物(1):醇的制备RCH 2OH CH OHR'RR C OHO R C H O RCH 2OH ROR'O Na, EtOHRCH 2OHR C R'O LiAlH 4LiAlH 4NaBH 4 或 LiAlH 4或 催化氢化伯醇伯醇或伯醇NaBH 4 或 LiAlH 4或 催化氢化仲醇以上表明,四氢铝锂可以还原醛、羧酸、酯、酮等羰基化合物,而硼氢化钠只能还原醛和酮以及酰卤等类化合物。
例:1. NaBH 42.H 2OCH 3CH CHCH 2OHCH 3CH CHCHOCH 3CH CHCHO42CHCH 2OHCH 3CH 例:OHCH 3LiAlH 4OCH 322+98%H 2C CHCH 2COOH4,Et 22H 2CCHCH 2CH 2OHCH 3COOHNaBH 不反应特点:双键不受影响,四氢铝锂还原性强于硼氢化钠RCClOLiAlH RCH 2OH酰氯:2R C O OO4C R'R'CH 2OH酐:2. H 2ORCH 2OH +:酮:RCRO 21. NaBH 4RCHROHR R C ROBH 3HNa RC RO R C ROBH 2H RC RH O RC RO RC RO 2HCO B OCHR 2OCHR 2OCHR 2NaR C R OH H4B(OH)3NaOH++机理:(2):制备胺类21.LiAlH 4,N(CH 3)2CO Et 2OCH 2N(CH 3)2(88%)N,N-二甲基环己基甲酰胺N,N-二甲基环己基甲酰胺RCl NaCNRCNRCH 2NH 24.氢负离子还原羰基化合物的反应历程氢负离子的还原羰基化合物实质上就是亲核加成反应,四氢铝锂和硼氢化钠对羰基的还原反应原理是一样的,它们都不能还原碳碳双键;而且,这类羰基加成反应实际上为不可逆反应,通常无副反应,所以可用于完成某些特定的合成工作。
氢化铝锂和硼氢化钠的还原能力

氢化铝锂和硼氢化钠的还原能力以氢化铝锂和硼氢化钠的还原能力为标题,我们将探讨它们在化学反应中的应用和特点。
让我们了解一下氢化铝锂和硼氢化钠的基本性质。
氢化铝锂是一种无机化合物,化学式为LiAlH4。
它是一种白色结晶固体,可以溶解在无水乙醇和二甲基甲酰胺中。
氢化铝锂是一种强还原剂,具有很高的还原能力。
硼氢化钠(NaBH4)是一种无机化合物,化学式为NaBH4。
它是一种白色结晶固体,可以溶解在水和醇中。
硼氢化钠也是一种强还原剂,具有较高的还原能力。
氢化铝锂和硼氢化钠的还原能力主要体现在它们与其他化合物发生反应时。
其中,氢化铝锂在有机合成中广泛应用,可以还原酮、醛、酯等功能团。
它可以将酮还原成相应的醇,醛还原成相应的醇或醛醇混合物,酯还原成相应的醇和醚。
氢化铝锂还可以将羧酸酯还原成醇和醚。
这些还原反应在有机合成中非常重要,可以合成各种有机化合物,如醇、醚、胺等。
与氢化铝锂相比,硼氢化钠的还原能力稍弱一些,但它仍然是一种常用的还原剂。
硼氢化钠主要用于还原醛和酮。
它可以将醛还原成相应的醇,酮还原成相应的醇。
硼氢化钠还可以还原酸类和酯类化合物。
在有机合成中,硼氢化钠也是一种重要的还原剂。
氢化铝锂和硼氢化钠的还原能力在有机合成中有许多优点。
首先,它们具有较高的还原效率和选择性,可以在温和的条件下完成反应。
其次,它们对许多官能团都具有良好的兼容性,可以与其他官能团共存而不受干扰。
此外,氢化铝锂和硼氢化钠的操作相对简单,易于使用。
然而,氢化铝锂和硼氢化钠也有一些不足之处。
首先,它们对水和空气敏感,容易分解生成氢气。
因此,在使用时需要注意防止水和空气的接触。
其次,它们对一些特殊官能团,如羧酸和酮醇混合物,还原效果不佳。
此外,氢化铝锂和硼氢化钠的价格较高,对于大规模合成来说成本较高。
氢化铝锂和硼氢化钠是两种常用的还原剂,具有较高的还原能力。
它们在有机合成中起着重要的作用,可以还原各种功能团。
然而,使用时需要注意它们的操作条件和特点。
LiAlH4还原的后处理

LiAlH4 还原的后处理的一些新的体会.LAH 是很有用的还原剂,可以还原醛,酮,酸,酯,氰基,酰胺等等. 但如果对它的后处理不合适的话,很容易生成Al(OH)3胶状物,过滤非常困难,收率低. 常见的quech方法有1, 直接加水2, 加水,再加NaOH,再加水3, 加Na2SO4水溶液4,加15% NaOH 水溶液5,加Na2SO4.10H2O其中4,5方法最好. 那么加多少水合适呢? 你加多少克LAH,就加1.2倍量的水,然后加入NaOH, 配成15%的水溶液,将该溶液缓慢的滴加进去(特别是开始,要很缓慢的滴加). 这样加是有它的道理的. LiAlH4 + 2H2O--->LiAlO2 + 4H2 , LAH 的分子量是38, 水是18,但需要2摩尔的水. 这样加入少许过量的水,可以把所有的Li,Al元素转化为偏铝酸锂,偏铝酸锂是粗大颗粒,很容易过滤. 滤液直接浓缩干一般就是你要的产物,不需要做其他分离. 如果做的量少,加入Na2SO4.10H2O破坏LAH也是不错的方法,还是一样,加入相当于1.2eq LAH的Na2SO4.10H2O,直接过滤,蒸干就好了.最后,LAH虽然好用,但比较危险. 用的过程要非常小心,特别是量比较大的时候,开始加溶剂的时候,冷却,N2保护是必须的. GOOD LUCK!Quenching the LAH is really easy:if you used X milligrams of LAH, make sure your reaction is cooled to 0 degrees C, then add X microliters of water (Slowly! and make sure the reaction is in control.) then X microliters of 15% aq. NaOH, then 3X microliters of water.。
还原胺化试剂

还原胺化试剂
以下是一些常见的还原胺化试剂:
1. 硼氢化钠(NaBH4):是一种常用的还原胺化试剂,它可以在温和的条件下将醛或酮还原为胺。
但是,它对含有官能团的醛或酮反应效果不佳。
2. 氢化铝锂(LiAlH4):是一种强还原剂,可以在较温和的条件下将醛或酮还原为胺。
但是,它对含有官能团的醛或酮反应效果不佳,并且需要在无水条件下使用。
3. 三叔丁基硼(TBAB):是一种温和的还原胺化试剂,可以在室温下将醛或酮还原为胺。
但是,它对含有官能团的醛或酮反应效果不佳。
4. 二异丙基氨基锂(LDA):是一种强还原剂,可以在室温下将醛或酮还原为胺。
但是,它对含有官能团的醛或酮反应效果不佳,并且需要在无水条件下使用。
5. 三乙胺硼氢化锂(LiBH(sec-C4H9)3):是一种温和的还原胺化试剂,可以在室温下将醛或酮还原为胺。
它对含有官能团的醛或酮反应效果较好,并且不需要在无水条件下使用。
有机lialh4作用 -回复

有机lialh4作用-回复有机lialh4(LiAlH4)是一种强还原剂,被广泛用于有机合成的反应中。
它是由锂、铝和氢组成的无机化合物,在化学合成中扮演着重要的角色。
本文将一步一步回答有机lialh4的作用和其在有机合成中的应用。
第一部分:有机lialh4的性质和结构有机lialh4是一种无色固体,可以通过将氢气与铝和锂在高温下反应合成而成。
它的化学式为LiAlH4,分子量为37.95 g/mol。
其晶体结构由AlH4和Li离子组成,其中每个氢氧根离子(AlH4-)与一个锂离子形成离子晶格。
第二部分:有机lialh4的还原性质有机lialh4具有很强的还原能力,可以将众多有机化合物中的羰基(酮、醛、酰氯、酰丙酮等)还原成相应的醇。
它可以和酯、酰胺、酰卤等有机化合物反应,生成相应的醇、胺和取代产物。
第三部分:有机lialh4在有机合成中的应用1. 酮和醛的还原:有机lialh4可以将酮还原为相应的醇,例如将丙酮还原为异丙醇。
同时,它也可以将醛还原为醇,例如将丁醛还原为正丁醇。
2. 羧酸的还原:有机lialh4可以将羧酸(如酰丙酸)还原为醇,生成相应的醇和氢气。
3. 酯的还原:有机lialh4可以将酯还原为醇和相应的有机取代物。
例如,将乙酸乙酯还原为乙醇和乙腈。
4. 酰胺和酰卤的还原:有机lialh4可以将酰胺还原为胺,如将甲酰胺还原为甲胺;同时,它也可以将酰卤还原为相应的醇或胺。
5. 其他反应应用:有机lialh4还可以参与其它一些有机反应,如将酮和醛与酰氯、酰胺或酯反应,生成取代产物。
第四部分:一些实际应用案例1. 在制药领域,有机lialh4广泛用于合成各种药物活性成分,如对乙酰氨基酚和咖啡因等。
2. 在化学工业中,有机lialh4用于合成有机合成润滑剂等化学品。
3. 在有机合成研究中,有机lialh4被用来合成新型功能材料,如光学材料和电子材料等。
总结:有机lialh4作为强还原剂,在有机合成领域发挥着重要作用。
化学实验综合题(解析版)
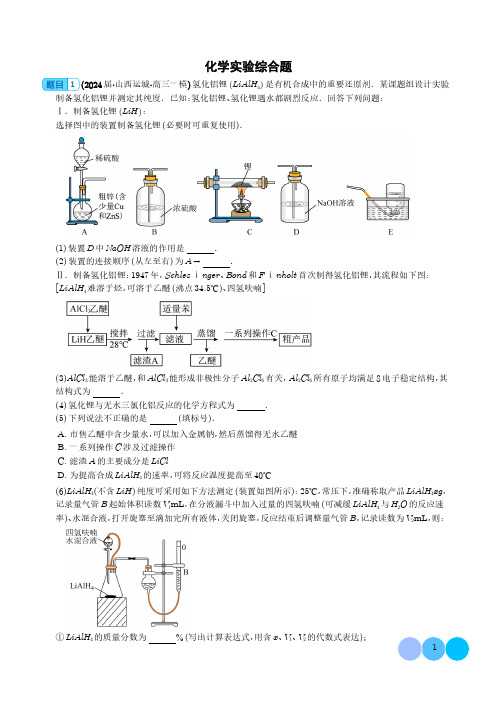
化学实验综合题1(2024届·山西运城·高三一模)氢化铝锂LiAlH4是有机合成中的重要还原剂.某课题组设计实验制备氢化铝锂并测定其纯度.已知:氢化铝锂、氢化锂遇水都剧烈反应.回答下列问题:Ⅰ.制备氢化锂LiH:选择图中的装置制备氢化锂(必要时可重复使用).(1)装置D中NaOH溶液的作用是.(2)装置的连接顺序(从左至右)为A→.Ⅱ.制备氢化铝锂:1947年,Schlesⅰnger、Bond和Fⅰnholt首次制得氢化铝锂,其流程如下图:[LiAlH4难溶于烃,可溶于乙醚(沸点34.5℃)、四氢呋喃](3)AlCl3能溶于乙醚,和AlCl3能形成非极性分子Al2Cl6有关,Al2Cl6所有原子均满足8电子稳定结构,其结构式为.(4)氢化锂与无水三氯化铝反应的化学方程式为.(5)下列说法不正确的是(填标号).A.市售乙醚中含少量水,可以加入金属钠,然后蒸馏得无水乙醚B.一系列操作C涉及过滤操作C.滤渣A的主要成分是LiClD.为提高合成LiAlH4的速率,可将反应温度提高至40℃(6)LiAlH4(不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品LiAlH4xg,记录量气管B起始体积读数V1mL,在分液漏斗中加入过量的四氢呋喃(可减缓LiAlH4与H2O的反应速率)、水混合液,打开旋塞至滴加完所有液体,关闭旋塞,反应结束后调整量气管B,记录读数为V2mL,则:①LiAlH的质量分数为%(写出计算表达式,用含x、V、V的代数式表达);②恒压分液漏斗的优点有、.注:量气管B 由碱式滴定管改装;25℃,常压下气体摩尔体积约为24.5L /mol 。
【答案】(1)除去H 2中混有的H 2S (2)D →B →C →B →E(3)(4)4LiH +AlCl 328℃LiAlH 4+3LiCl(5)D(6)38(V 1-V 2)4×245x平衡压强,使分液漏斗中的溶液顺利滴下消除滴入溶液的体积对所测气体体积的影响,减小实验误差【分析】Ⅰ.制备氢化锂首先制备氢气,即装置A 为制备氢气的装置,粗锌中含有少量Cu 和ZnS ,Cu 不与稀硫酸反应,ZnS 能与稀硫酸反应生成H 2S ,需要用NaOH 溶液除去H 2S ,即装置D 的作用是吸收硫化氢,因为氢化铝锂、氢化锂遇水都剧烈反应,因此需要干燥氢气,通过浓硫酸,然后再通过C 装置制备氢化锂,装置E 为收集氢气装置,据此分析。
氢化铝锂催化剂

氢化铝锂催化剂氢化铝锂(LiAlH4)是一种高效的还原剂,在有机合成中常用作羰基试剂和还原剂。
氢化铝锂具有很强的氢转移能力,是很强的还原剂,几乎没有选择性,可将醛、酮、酯、羧酸、酸酐、环氧化物还原为醇,将亚胺、酰胺、腈、脂肪族硝基化物还原为胺。
另外氢化铝锂也可将卤代烷烃还原为烷烃,能够对烯烃、炔烃发生氢铝化反应,得到C-Al中间体,进而与其他亲核剂发生加成反应。
氢化铝锂作为一种催化剂,主要应用于化学合成领域,尤其是在有机合成反应中,它可以有效地还原醛、酮、酸酐和酰胺等含有羰基的化合物。
此外,氢化铝锂还可以与NaH在四氢呋喃中进行复分解反应,高效地生产氢化铝钠(NaAlH4),这也是一种重要的还原剂。
在能源领域,氢化铝锂因其高储氢容量而被认为是一种潜在的便携式氢源。
然而,它的应用受到了脱氢反应温度较高的限制。
为了解决这个问题,研究人员在氢化铝体系中引入了氮化锂作为催化剂,这样可以显著降低初始脱氢温度,并提高氢容量的稳定性以下是一些具体的应用实例:有机合成中的还原剂:氢化铝锂在有机化学合成中常用于还原醛、酮和酸酐等含有羰基的化合物。
例如,它可以将醛或酮还原成相应的醇,这一过程称为羰基还原反应。
制备其他氢化物:氢化铝锂可以与NaH在四氢呋喃中进行复分解反应,高效地生产氢化铝钠(NaAlH4),这是一种同样重要的还原剂。
这种反应不仅提高了氢化铝钠的制备效率,还扩展了氢化铝锂的应用范围。
便携式氢源的开发:氢化铝锂因其高储氢容量而被研究作为便携式氢源。
为了克服其脱氢反应温度较高的问题,研究者们在氢化铝体系中引入了氮化锂作为催化剂。
这种催化剂的加入显著降低了初始脱氢温度,并提高了氢容量的稳定性。
例如,通过调整氮化锂的质量分数,可以将初始脱氢温度从140.0°C降至66.8°C,这对于氢能源的实际应用具有重要意义。
LiAlH4还原剂
参考文献:
◎《氢化铝锂的合成和应用》————吕 布 、王 松涛 、王守柱,(安徽中医学院有机化学教研室, 合肥 230038);
◎ 《合成氢化铝锉新工艺》;
◎《浅谈氢负离子还原剂LiAlH4与NaBH4 》 张媚(西北大学化学系05级化学班 西安 710069)
◎◎《化合物中的新秀—一—氢化铝铿锂氢》化—铝—》任—道—华任 ◎道《华有机合成》——黄培强,靳立人,陈安齐; 高等教育出版社,2004,6
CH3CH CHCH 2OH
1. LiAlH4,Et2O
H2C CHCH 2COOH
2. H2O
H2C CHCH 2CH2OH
但是当试剂过量或反应温度过高,则碳碳 双键和羰基均被还原。故通过降低反应温 度、缩短反应时间,可以以还原羰基为主。
3.3 腈 类
化 合 物 的 还 原
酰胺和酰亚胺可以被LiAlH4还原成碳 原子数相同的胺。
RCH3 + AlH3 + LiX
羰基化合物很容易被LiAlH4还原成羟基化合物, 这类反应室温下可在乙醚中平稳地、当量地进
行。
O RCH
O R C OH
NaBH4 或 LiAlH4或 催化氢化 LiAlH4
RCH2OH 伯醇 RCH2OH 伯醇
O R C OR'
LiAlH4 或 Na, EtOH
改进方法:
28~31℃
(加热回流)
3、LiAlH4的应用
●可将卤代烃还原成烃;
●一般来说一卤代物比二卤代物
3.1
活泼,在苛刻条件下三卤代物可被
卤
还原成烯烃;
代
●反应活性I>Br>Cl。
烃
的
CH3(CH2)8CH2Br LiAlH4
戊内酯和四氢铝锂反应

戊内酯和四氢铝锂反应
戊内酯与四氢铝锂(LiAlH4)反应,通常会被还原成相应的醇。
四氢铝锂是一种非常强的还原剂,它能够将醛、酮、酯、内酯等官能团还原为醇。
在有机化学合成中,这种反应非常常见,尤其是在合成醇类化合物时。
具体到戊内酯,它是一种内酯化合物,可以被四氢铝锂还原开环,生成相应的戊醇。
在实际操作中,这种还原反应通常在惰性溶剂如四氢呋喃(THF)中进行,以确保反应的顺利进行。
反应条件通常需要严格控制,比如在低温和氮气保护下进行,以避免副反应的发生。
此外,由于四氢铝锂对水和空气非常敏感,因此在操作过程中需要特别注意安全措施,确保反应体系的无水无氧状态。
戊内酯与四氢铝锂反应可以得到戊醇,这是一种重要的有机合成反应,广泛应用于有机化合物的制备中。
在进行这类反应时,实验者应严格遵守实验室的安全操作规程,确保反应的顺利进行和实验人员的安全。
lialh4相对分子

lialh4相对分子
LiAlH4是一种相对分子,它是一种常用的还原剂。
对于化学工作者来说,它是一种非常重要的化学试剂。
它的全称是四氢杂铝酸锂,是一种白色结晶性粉末。
LiAlH4的化学式为LiAlH4,摩尔质量为37.95 g/mol。
LiAlH4在有机合成反应中具有很高的还原能力。
它可以将酮、醛、酯等化合物还原为相应的醇或羧酸。
这种还原反应是通过LiAlH4的氢原子与有机化合物的氧原子发生反应来完成的。
这是一种非常重要的有机合成反应,因为它可以在不引入其他官能团的情况下将酮、醛等还原成醇。
LiAlH4的还原能力非常强大,但同时也非常危险。
在使用LiAlH4时,必须小心操作,遵循严格的安全操作规程。
由于其高度还原性,LiAlH4与水或醇等含有活泼氢原子的物质反应非常剧烈,甚至会引发爆炸。
因此,在使用LiAlH4时,需要在惰性气体氛围下进行,并且要使用干燥的溶剂。
除了在有机合成中的应用,LiAlH4还可以用于一些金属合金的制备。
它可以与铝、锂等金属反应,形成一些具有特殊性质的合金材料。
这些合金材料在航空航天、汽车制造等领域有着广泛的应用。
LiAlH4是一种非常重要的化学试剂,具有很高的还原能力。
它在有机合成反应中起着关键作用,可以将酮、醛等还原为醇或羧酸。
但
由于其危险性较大,使用时必须小心操作,遵循安全规程。
它还有一些其他的应用领域,如金属合金制备。
通过合理的使用和控制,LiAlH4可以为化学工作者提供很多便利,促进科学研究的发展。
三氯化铝与氢化铝锂反应

三氯化铝与氢化铝锂反应三氯化铝与氢化铝锂反应是一种常见的化学反应,它在有机合成和材料制备中具有重要的应用价值。
本文将从反应原理、反应条件、反应机理和应用等方面进行介绍。
我们来了解一下三氯化铝和氢化铝锂的基本性质。
三氯化铝(AlCl3)是一种无机化合物,具有白色结晶固体的形态。
它是一种强酸性物质,在水中能够迅速溶解,并能与水蒸气形成白色的烟雾。
氢化铝锂(LiAlH4)是一种无机化合物,是一种强还原剂,能够与许多有机物发生反应。
当三氯化铝与氢化铝锂反应时,会发生置换反应。
反应的化学方程式如下:2AlCl3 + LiAlH4 → 3LiCl + AlH3在这个反应中,三氯化铝的氯原子被氢化铝锂的氢原子替换,生成氯化锂和氢化铝。
氯化锂是无色晶体,是一种常见的无机化合物。
氢化铝是无色气体,是一种重要的还原剂,在有机合成中有广泛的应用。
接下来,我们来讨论一下反应的条件和机理。
三氯化铝与氢化铝锂的反应需要在惰性气氛下进行,通常在干燥的环境中进行。
反应温度一般在0-50摄氏度之间,过高的温度会导致反应剧烈进行,产生危险。
反应的机理主要涉及到氢化铝锂的脱氢反应和三氯化铝的置换反应。
氢化铝锂中的氢原子被三氯化铝的氯原子取代,生成氯化锂和氢化铝。
这个反应是一个放热反应,同时释放出氢气。
三氯化铝与氢化铝锂反应在有机合成中有广泛的应用。
氢化铝锂是一种强还原剂,能够将酮、醛、酯等羰基化合物还原为相应的醇或醚。
此外,它还能够还原烯烃、硝基化合物等。
这种反应在药物合成、天然产物的合成等领域有重要的应用。
三氯化铝与氢化铝锂反应是一种重要的化学反应,它在有机合成和材料制备中具有广泛的应用。
通过置换反应,三氯化铝中的氯原子被氢化铝锂中的氢原子取代,生成氯化锂和氢化铝。
这个反应在有机合成中可以用作还原剂,具有重要的应用价值。
希望通过这篇文章的介绍,能够增加对这个化学反应的了解和认识。
氢化铝锂相对原子质量

氢化铝锂相对原子质量
氢化铝锂是一种重要的无机化合物,其相对原子质量为题。
氢化铝锂是由铝和锂两种元素组成的化合物,化学式为LiAlH4。
它是一种强还原剂,可以在有机合成中起到很重要的作用。
氢化铝锂的相对原子质量是多少呢?我们先来看一下铝和锂的相对原子质量。
铝的相对原子质量是26.98,锂的相对原子质量是 6.94。
根据化学式LiAlH4,我们可以知道氢化铝锂中有一个铝原子和四个氢原子。
所以,氢化铝锂的相对原子质量可以通过以下计算得到:
相对原子质量 = 26.98 + 4 * 1.01 + 6.94 = 37.95
所以,氢化铝锂的相对原子质量为37.95。
氢化铝锂在有机合成中有很多重要的应用。
它可以被用作还原剂,将羰基化合物还原为相应的醇。
此外,氢化铝锂还可以将酯还原为醇、酮还原为醇和羧酸还原为醛等。
这些反应在有机合成中非常常见,因此氢化铝锂被广泛应用于制药、农药和染料等领域。
除了在有机合成中的应用,氢化铝锂还可以用于储氢材料的制备。
氢化铝锂可以与氢气反应,形成氢化铝锂的氢化物,这是一种具有较高储氢容量的材料。
因此,氢化铝锂在氢能源领域也具有很大的潜力。
氢化铝锂是一种重要的无机化合物,其相对原子质量为37.95。
它
在有机合成和氢能源领域有着广泛的应用前景。
我们相信,在未来的发展中,氢化铝锂将发挥越来越重要的作用,为人类带来更多的福祉。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH3(CH2)8CH2Br 机理: Li+ H3Al H
LiAlH4
CH3(CH2)8CH3
3.1 卤 代 烃 的 还 原
+ CH2 R
X
RCH3
+
AlH3 + LiX
羰基化合物很容易被LiAlH4还原成羟基化合物 还原成羟基化合物, 羰基化合物很容易被 这类反应室温下可在乙醚中平稳地、 这类反应室温下可在乙醚中平稳地、当量地进 行。
3.3 腈 类 化 合 物 的 还 原
酰胺和酰亚胺可以被LiAlH4还原成碳 酰胺和酰亚胺可以被 原子数相同的胺。 原子数相同的胺。
例:
3.4 酰 胺 和 酰 亚 胺 的 还 原
环氧化合物经氢化锂铝还原得到醇。 环氧化合物经氢化锂铝还原得到醇。 负氢离子进攻位阻较小的一边。 负氢离子进攻位阻较小的一边。顺序 是伯碳优先于仲碳,仲碳优先于叔碳。 是伯碳优先于仲碳,仲碳优先于叔碳。
◎
◎
氢化铝锂》 《化合物中的新秀——氢化铝锂》——任道华 任道华
黄培强, 《有机合成》——黄培强,靳立人,陈安齐; 有机合成》 黄培强 靳立人,陈安齐; 高等教育出版社, 高等教育出版社,2004,6 ,
◎
伯醇
反应机子的转移实现。 其还原过程是通过氢化锂铝的负氢离子的转移实现。
LiAlH4还原 ,β—不饱和羰基化合 还原α, 不饱和羰基化合 物,主要得到羰基还原产物 :
例:CH 3CH CHCHO 1. LiAlH 4 干乙醚 2. H 2 O CH 3CH CHCH 2OH
2、LiAlH4的合成 、
600~700℃
传统方法: 传统方法:
(加热回流) 加热回流)
28~31℃ ℃
改进方法: 改进方法:
3、LiAlH4的应用 、 的应用
可将卤代烃还原成烃; 可将卤代烃还原成烃; ●一般来说一卤代物比二卤代物 活泼,在苛刻条件下三卤代物可被 活泼 在苛刻条件下三卤代物可被 还原成烯烃; 还原成烯烃; 反应活性I>Br>Cl。 ●反应活性 。
H2C CHCH COOH 2
1. LiAlH4,Et2O 2. H2O
H2C CHCH CH2OH 2
但是当试剂过量或反应温度过高, 但是当试剂过量或反应温度过高,则碳碳 双键和羰基均被还原。 双键和羰基均被还原。故通过降低反应温 缩短反应时间,可以以还原羰基为主 可以以还原羰基为主。 度、缩短反应时间 可以以还原羰基为主。
讲解的主要内容: 讲解的主要内容:
• LiAlH4的简介 • LiAlH4的合成 • LiAlH4的应用(有机方面) 的应用(
1、LiAlH4的简介 、 的简介
★中文名称氢化锂铝或四氢锂铝; 中文名称氢化锂铝或四氢锂铝; ★多孔的微晶性粉末。久贮能变成 多孔的微晶性粉末。 灰色,在潮湿空气中易分解; 灰色,在潮湿空气中易分解; ★易跟水或醇反应而放出氢气,氢 易跟水或醇反应而放出氢气, 气随即燃烧; 气随即燃烧; ★加热至130℃时分解。溶于醚、 加热至 ℃时分解。溶于醚、 四氢呋喃; 四氢呋喃; ★有很强的还原性,可以对许多无 有很强的还原性 可以对许多无 机物和有机物起还原作用。 机物和有机物起还原作用。
3.5 环 氧 化 合 物 的 还 原
LiAlH4作为还原剂的优点: 作为还原剂的优点:
1.还原反应大都可在常温常压下进行,且具 还原反应大都可在常温常压下进行, 还原反应大都可在常温常压下进行 有工艺简单、操作方便、没有副产物。 有工艺简单、操作方便、没有副产物。 2.一般它不会使 一般它不会使C=C氢化,这便有可能由不 氢化, 一般它不会使 氢化 饱和的酮、 酸衍生物、 饱和的酮、醛、酸衍生物、硝基化物等等来 制取不饱和醇、胺、和相应的碳氢化物。 制取不饱和醇、 和相应的碳氢化物。 3。在LiAIH4分子中,氢的含量相当高,因 。 分子中,氢的含量相当高, 此只使用少量的试剂, 此只使用少量的试剂,便可取得较好还原效 果。 4.在使用 在使用LiAIH4的还原反应中,其收率都是 的还原反应中, 在使用 比较高的。
参考文献: 参考文献:
◎
《氢化铝锂的合成和应用》————吕 布 、王 氢化铝锂的合成和应用》 吕 王守柱, 安徽中医学院有机化学教研室 安徽中医学院有机化学教研室, 松涛 、王守柱,(安徽中医学院有机化学教研室 合肥 230038); ;
◎
《合成氢化铝锉新工艺》; 合成氢化铝锉新工艺》
《浅谈氢负离子还原剂LiAlH4与NaBH4 》 浅谈氢负离子还原剂 张媚(西北大学化学系05级化学班 张媚(西北大学化学系 级化学班 西安 710069) )
O R C H O R C OH O R C OR' O R C R' NaBH4 或 LiAlH4或 催化氢化 LiAlH4 或 Na, EtOH RCH2OH OH R CH R' 仲醇 伯醇 LiAlH4 RCH2OH 伯醇 NaBH4 或 LiAlH4或 催化氢化 RCH2OH 伯醇
3.2 羰 基 化 合 物 的 还 原
