碳原子数1-60烷烃同分异构体数
烷烃(同系物和同分异构体)
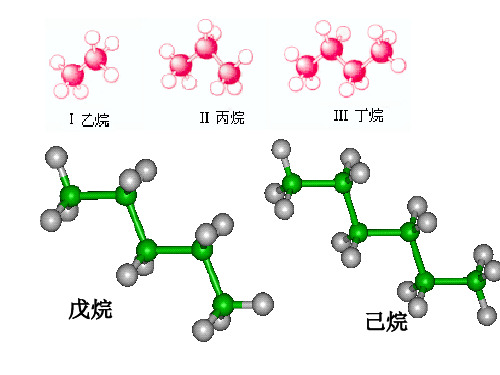
烷烃复 习一: 什么叫烷烃? 链状、单键、饱和
烷烃的通式是?其完全燃烧生成的水和二氧化碳 之比为多少? C2H2n+2 (n≥1) 已知10ml的某气态烷烃在50mlO2中充分燃烧,得到 液态水和体积为35ml的混合气体(所有气体都在同温同 压下测定),则该烃可能是什么?
烷烃的表示方法
有机物的几种表示方法
烷烃的化学性质
(1)烷烃的氧化反应 烷烃完全燃烧的通式: CnH2n+2+(3n+1)/2O2 → nCO2+(n+1)H2O
通常情况下,烷烃与高锰酸钾等强氧化剂不发 生反应,不能与强酸和强碱溶液反应。
(2)烷烃的取代反应
其它烷烃与甲烷一样,一定条件下能发生取
代反应。因为可以被取代的氢原子多,所以
H
C
H
C H
H
对称氢原子的概念
我们先看看最简单的甲烷分子… 我们知道甲烷的四个氢原 子是对称的。 如果将甲烷的四个氢原子 用甲基取代,结果会…?
由此可以得到两个规律…
对称氢原子确定的规律
同一碳原子上的氢原子完全对称 。 与同一碳原子相连的甲基上的氢原
子完全对称。
与同一碳原子相连的相同基团对应位置上的
烷烃组成和结构的表示方法
结构简式怎么写?------p23(有机化学)
1.将结构式中的C—H省略,其他的共价键一律不省略.C—C 可省也可不省.但其它如双键,叁键一律不能省. 实际上写结构简式的最简单处理方法就是省略C—H,
其它一概不变!
2.连在同一个C上的相同基团有时也可以合并,并带上括号. 3.同一条链上连续的相同的基团也可以合并,并带上括号
4、主链少三个碳原子
C C ∣ ∣ C -C - C - C ∣ ∣ C C
烷烃同分异构体:碳原子数为10以内的所有烷烃(共150种)

碳原子数为10以内的所有烷烃同分异体(共150种)1种)一、CH4同分异构体(共1、甲烷二、C同分异构体(共1种)2H61、乙烷同分异构体(共1种)三、C3H81、丙烷四、C同分异构体(共2种)4H101、丁烷2、2—甲基丙烷五、C同分异构体(共3种)5H121、戊烷2、2—甲基丁烷3、2 , 2—二甲基丙烷六、C同分异构体(共5种)6H141、己烷2、2—甲基戊烷3、3—甲基戊烷4、2 , 2—二甲基丁烷5、2 , 3—二甲基丁烷同分异构体(共9种)七、C7H161、庚烷2、2—甲基己烷3、3—甲基己烷4、3—乙基戊烷5、2 , 2—二甲基戊烷6、2 , 3—二甲基戊烷7、2 , 4—二甲基戊烷8、3 , 3—二甲基戊烷9、2 , 2 , 3—三甲基丁烷同分异构体(共18种)八、C8H181、辛烷2、2—甲基庚烷3、3—甲基庚烷4、4—甲基庚烷5、3—乙基己烷6、2 , 2—二甲基己烷7、2 , 3—二甲基己烷8、2 , 4—二甲基己烷9、2 , 5—二甲基己烷10、3 , 3—二甲基己烷11、3 , 4—二甲基己烷12、2—甲基—3—乙基戊烷13、3—甲基—3—乙基戊烷14、2 , 2 , 3—三甲基戊烷15、2 , 2 , 4—三甲基戊烷16、2 , 3 , 3—三甲基戊烷17、2 , 3 , 4—三甲基戊烷18、2 , 2 , 3 , 3—四甲基丁烷九、C同分异构体(共35种)9H201、壬烷2、2—甲基辛烷3、3—甲基辛烷4、4—甲基辛烷5、3—乙基庚烷6、4—乙基庚烷7、2 , 2—二甲基庚烷8、2 , 3—二甲基庚烷9、2 , 4—二甲基庚烷10、2 , 5—二甲基庚烷11、2 , 6—二甲基庚烷12、3 , 3—二甲基庚烷13、3 , 4—二甲基庚烷14、3 , 5—二甲基庚烷15、4 , 4—二甲基庚烷16、2—甲基—3—乙基己烷17、2—甲基—4—乙基己烷18、3—甲基—3—乙基己烷19、3—甲基—4—乙基己烷20、2 , 2 , 3—三甲基己烷21、2 , 2 , 4—三甲基己烷22、2 , 2 , 5—三甲基己烷23、2 , 3 , 3—三甲基己烷24、2 , 3 , 4—三甲基己烷25、2 , 3 , 5—三甲基己烷27、3 , 3 , 4—三甲基己烷28、3 , 3—二乙基戊烷29、2 , 2—二甲基—3—乙基戊烷30、2 , 3—二甲基—3—乙基戊烷31、2 , 4—二甲基—3—乙基戊烷32、2 , 2 , 3 , 3—四甲基戊烷33、2 , 2 , 3 , 4—四甲基戊烷34、2 , 2 , 4 , 4—四甲基戊烷35、2 , 3 , 3 , 4—四甲基戊烷同分异构体(共75种)十、C10H221、癸烷2、2—甲基壬烷3、3—甲基壬烷4、4—甲基壬烷5、5—甲基壬烷6、3—乙基辛烷7、4—乙基辛烷8、2 , 2—二甲基辛烷9、2 , 3—二甲基辛烷10、2 , 4—二甲基辛烷11、2 , 5—二甲基辛烷12、2 , 6—二甲基辛烷13、2 , 7—二甲基辛烷14、3 , 3—二甲基辛烷15、3 , 4—二甲基辛烷16、3 , 5—二甲基辛烷17、3 , 6—二甲基辛烷18、4 , 4—二甲基辛烷19、4 , 5—二甲基辛烷20、4—正丙基庚烷21、4—异丙基庚烷22、2—甲基—3—乙基庚烷23、3—甲基—3—乙基庚烷24、4—甲基—3—乙基庚烷25、2—甲基—4—乙基庚烷26、3—甲基—4—乙基庚烷27、4—甲基—4—乙基庚烷28、2—甲基—5—乙基庚烷29、3—甲基—5—乙基庚烷30、2 , 2 , 3—三甲基庚烷31、2 , 2 , 4—三甲基庚烷32、2 , 2 , 5—三甲基庚烷34、2 , 3 , 3—三甲基庚烷35、2 , 3 , 4—三甲基庚烷36、2 , 3 , 5—三甲基庚烷37、2 , 3 , 6—三甲基庚烷38、2 , 4 , 4—三甲基庚烷39、2 , 4 , 5—三甲基庚烷40、2 , 4 , 6—三甲基庚烷41、2 , 5 , 5—三甲基庚烷42、3 , 3 , 4—三甲基庚烷43、3 , 3 , 5—三甲基庚烷44、3 , 4 , 4—三甲基庚烷45、3 , 4 , 5—三甲基庚烷46、2—甲基—3—异丙基己烷47、3 , 3—二乙基己烷48、3 , 4—二乙基己烷49、2 , 2—二甲基—3—乙基己烷50、2 , 3—二甲基—3—乙基己烷51、2 , 4—二甲基—3—乙基己烷52、2 , 5—二甲基—3—乙基己烷53、3 , 4—二甲基—3—乙基己烷54、2 , 2—二甲基—4—乙基己烷55、2 , 3—二甲基—4—乙基己烷56、2 , 4—二甲基—4—乙基己烷57、3 , 3—二甲基—4—乙基己烷58、2 , 2 , 3 , 3—四甲基己烷59、2 , 2 , 3 , 4—四甲基己烷60、2 , 2 , 3 , 5—四甲基己烷61、2 , 2 , 4 , 4—四甲基己烷62、2 , 2 , 4 , 5—四甲基己烷63、2 , 2 , 5 , 5—四甲基己烷64、2 , 3 , 3 , 4—四甲基己烷65、2 , 3 , 3 , 5—四甲基己烷66、2 , 3 , 4 , 4—四甲基己烷67、2 , 3 , 4 , 5—四甲基己烷68、3 , 3 , 4 , 4—四甲基己烷69、2 , 4—二甲基—3—异丙基戊烷70、2—甲基—3 , 3—二乙基戊烷71、2 , 2 , 3—三甲基—3—乙基戊烷72、2 , 2 , 4—三甲基—3—乙基戊烷73、2 , 3 , 4—三甲基—3—乙基戊烷74、2 , 2 , 3 , 3 , 4—五甲基戊烷75、2 , 2 , 3 , 4 , 4—五甲基戊烷。
烷烃同分异构体数目口诀

烷烃同分异构体数目口诀烷烃是指沿着碳碳键链为C基组成的烃类分子,烷烃同分异构体指在具有相同碳链结构,相同碳链重量的情况下,由于键的分布方式不同,而表现出不同的化学性质,物理性质的同分异构体的总和就是烷烃同分异构体数目。
那么我们如何来计算烷烃同分异构体数目呢?“ 十 - 八” 口诀可以提供我们一个有用的参考,此口诀概括计算方法为:1. 如果烷烃的碳链上有 n 个碳原子,就有 n! 共n× ( n−1 ) × ( n−2 )×...×3×2×1 种构型2. 单路重复:程序从最后一个碳原子开始,将它沿着 clockwise方向折叠,折叠一次等于1个异构体,直到碳链回到原来的顺序,就产生一个环型构型3. 双螺旋重复:若有位靠近碳链起点 -ω和终点α上靠近的碳被折叠,继续从终点α开始,逆时针折叠碳链若干格,直到α与ω重合(落在同一位置),这种折叠产生的异构体等于碳链长度减一。
因此,计算烷烃同分异构体数目的口诀“ 十 - 八” 就用上述的方法便可以计算出。
例如,要计算 C6H12 的烷烃同分异构体数目,n=6,因此有6!= 6×5×4×3×2×1 =720 个烷烃同分异构体。
此外,同分异构体数量也可以使用“Hypothetical Geometric Isomers Formulae” 公式来计算,它将单路重复和双螺旋重复因子分开,当一个有多个构型时,分裂开组成的n组元素之和,即为同分异构体的总数 .当考虑环烷烃的时候,可以假设环状烷烃有两个 end--groups 和一个中心碳,以及其他碳中的基,因此可以转换为 n--alkane 的形式计算,例如 C6H12 -- Cyclohexane,则所得烷烃同分异构体数目为 n--alkane 中的 6!,即 720 个。
综上所述,烷烃同分异构体数目可以使用“ 十 - 八” 口诀或 HypotheticalGeometric Isomers Formulae 公式来计算,本文介绍了烷烃同分异构体数目的定义和计算方法,希望对你有所帮助。
烃基同分异构体数目表-概述说明以及解释

烃基同分异构体数目表-概述说明以及解释1.引言1.1 概述烃基同分异构体是有机化合物中的一种特殊存在形式,它们具有相同的分子式但结构不同,因此在物理、化学性质以及生物活性等方面表现出不同的特点。
烃基同分异构体的研究对于有机化学领域的发展有着重要的意义。
烃基同分异构体的数量庞大且种类繁多,每个分子式可以存在多个不同结构的同分异构体。
通过研究和统计不同烃基同分异构体的数目,可以更好地了解有机化合物的结构特点,分析它们在不同环境下的性质和反应行为,并为合成新的有机化合物提供参考和指导。
在石油、化工、医药等领域,烃基同分异构体的研究对于评价和预测化合物的性质和活性起着重要作用。
研究人员可以通过比较不同烃基同分异构体的特征和反应活性,选择最优的化合物用于特定的应用领域,提高化合物的性能和效率。
此外,烃基同分异构体的研究也为有机合成化学提供了新的思路和方法。
通过对不同烃基同分异构体的构建和转化反应的研究,可以开发出新的合成路线和催化剂,提高有机合成的效率和选择性。
综上所述,烃基同分异构体的研究具有重要的意义和应用前景。
通过统计烃基同分异构体的数目并分析其特点,可以深入了解有机化合物的性质和反应行为,为有机化学领域的发展和应用提供重要的参考和指导。
1.2文章结构文章结构部分的内容可以包括以下内容:在本文中,将按照以下结构来展开讨论烃基同分异构体的数目:1. 引言1.1 概述:简要介绍烃基同分异构体的概念和意义。
1.2 文章结构:阐述本文的结构和内容安排。
1.3 目的:说明本文的写作目的,以及通过研究烃基同分异构体的数目对相关领域的贡献。
2. 正文2.1 烃基同分异构体的概念和意义:详细介绍什么是烃基同分异构体,以及其在化学领域中的重要性和应用价值。
2.2 烃基同分异构体的分类和特点:对烃基同分异构体进行分类,并探讨其不同分类之间的特点和区别。
3. 结论3.1 烃基同分异构体的数目统计:对烃基同分异构体的数目进行统计和分析,如不同长度、碳链结构等因素对烃基同分异构体数目的影响。
烷烃同分异构体:碳原子数为10以内的所有烷烃(共150种)

碳原子数为10以内的所有烷烃同分异体(共150种)一、CH4同分异构体(共1种)1、甲烷二、C2H6同分异构体(共1种)1、乙烷三、C3H8同分异构体(共1种)1、丙烷四、C4H10同分异构体(共2种)1、丁烷2、 2—甲基丙烷五、C5H12同分异构体(共3种)1、戊烷2、 2—甲基丁烷3、 2 , 2—二甲基丙烷六、C6H14同分异构体(共5种)1、己烷2、 2—甲基戊烷3、 3—甲基戊烷4、 2 , 2—二甲基丁烷5、 2 , 3—二甲基丁烷七、C7H16同分异构体(共9种)1、庚烷2、 2—甲基己烷3、 3—甲基己烷4、 3—乙基戊烷5、 2 , 2—二甲基戊烷6、 2 , 3—二甲基戊烷7、 2 , 4—二甲基戊烷8、 3 , 3—二甲基戊烷9、2 , 2 , 3—三甲基丁烷八、C8H18同分异构体(共18种)1、辛烷2、 2—甲基庚烷3、 3—甲基庚烷4、 4—甲基庚烷5、 3—乙基己烷6、 2 , 2—二甲基己烷7、 2 , 3—二甲基己烷8、 2 , 4—二甲基己烷9、 2 , 5—二甲基己烷10、3 , 3—二甲基己烷11、3 , 4—二甲基己烷12、2—甲基—3—乙基戊烷13、3—甲基—3—乙基戊烷14、2 , 2 , 3—三甲基戊烷15、2 , 2 , 4—三甲基戊烷16、2 , 3 , 3—三甲基戊烷17、2 , 3 , 4—三甲基戊烷18、2 , 2 , 3 , 3—四甲基丁烷九、C9H20同分异构体(共35种)1、壬烷2、 2—甲基辛烷3、 3—甲基辛烷4、 4—甲基辛烷5、 3—乙基庚烷6、 4—乙基庚烷7、 2 , 2—二甲基庚烷8、 2 , 3—二甲基庚烷9、 2 , 4—二甲基庚烷10、2 , 5—二甲基庚烷11、2 , 6—二甲基庚烷12、3 , 3—二甲基庚烷13、3 , 4—二甲基庚烷14、3 , 5—二甲基庚烷15、4 , 4—二甲基庚烷16、2—甲基—3—乙基己烷17、2—甲基—4—乙基己烷18、3—甲基—3—乙基己烷19、3—甲基—4—乙基己烷20、2 , 2 , 3—三甲基己烷21、2 , 2 , 4—三甲基己烷22、2 , 2 , 5—三甲基己烷23、2 , 3 , 3—三甲基己烷24、2 , 3 , 4—三甲基己烷25、2 , 3 , 5—三甲基己烷26、2 , 4 , 4—三甲基己烷27、3 , 3 , 4—三甲基己烷28、3 , 3—二乙基戊烷29、2 , 2—二甲基—3—乙基戊烷30、2 , 3—二甲基—3—乙基戊烷31、2 , 4—二甲基—3—乙基戊烷32、2 , 2 , 3 , 3—四甲基戊烷33、2 , 2 , 3 , 4—四甲基戊烷34、2 , 2 , 4 , 4—四甲基戊烷35、2 , 3 , 3 , 4—四甲基戊烷十、C10H22同分异构体(共75种)1、癸烷2、 2—甲基壬烷3、 3—甲基壬烷4、 4—甲基壬烷5、 5—甲基壬烷6、 3—乙基辛烷7、 4—乙基辛烷8、 2 , 2—二甲基辛烷9、 2 , 3—二甲基辛烷10、2 , 4—二甲基辛烷11、2 , 5—二甲基辛烷12、2 , 6—二甲基辛烷13、2 , 7—二甲基辛烷14、3 , 3—二甲基辛烷15、3 , 4—二甲基辛烷16、3 , 5—二甲基辛烷17、3 , 6—二甲基辛烷18、4 , 4—二甲基辛烷19、4 , 5—二甲基辛烷20、4—正丙基庚烷21、4—异丙基庚烷22、2—甲基—3—乙基庚烷23、3—甲基—3—乙基庚烷24、4—甲基—3—乙基庚烷25、2—甲基—4—乙基庚烷26、3—甲基—4—乙基庚烷27、4—甲基—4—乙基庚烷28、2—甲基—5—乙基庚烷29、3—甲基—5—乙基庚烷30、2 , 2 , 3—三甲基庚烷31、2 , 2 , 4—三甲基庚烷32、2 , 2 , 5—三甲基庚烷33、2 , 2 , 6—三甲基庚烷34、2 , 3 , 3—三甲基庚烷35、2 , 3 , 4—三甲基庚烷36、2 , 3 , 5—三甲基庚烷37、2 , 3 , 6—三甲基庚烷38、2 , 4 , 4—三甲基庚烷39、2 , 4 , 5—三甲基庚烷40、2 , 4 , 6—三甲基庚烷41、2 , 5 , 5—三甲基庚烷42、3 , 3 , 4—三甲基庚烷43、3 , 3 , 5—三甲基庚烷44、3 , 4 , 4—三甲基庚烷45、3 , 4 , 5—三甲基庚烷46、2—甲基—3—异丙基己烷47、3 , 3—二乙基己烷48、3 , 4—二乙基己烷49、2 , 2—二甲基—3—乙基己烷50、2 , 3—二甲基—3—乙基己烷51、2 , 4—二甲基—3—乙基己烷52、2 , 5—二甲基—3—乙基己烷53、3 , 4—二甲基—3—乙基己烷54、2 , 2—二甲基—4—乙基己烷55、2 , 3—二甲基—4—乙基己烷56、2 , 4—二甲基—4—乙基己烷57、3 , 3—二甲基—4—乙基己烷58、2 , 2 , 3 , 3—四甲基己烷59、2 , 2 , 3 , 4—四甲基己烷60、2 , 2 , 3 , 5—四甲基己烷61、2 , 2 , 4 , 4—四甲基己烷62、2 , 2 , 4 , 5—四甲基己烷63、2 , 2 , 5 , 5—四甲基己烷64、2 , 3 , 3 , 4—四甲基己烷65、2 , 3 , 3 , 5—四甲基己烷66、2 , 3 , 4 , 4—四甲基己烷67、2 , 3 , 4 , 5—四甲基己烷68、3 , 3 , 4 , 4—四甲基己烷69、2 , 4—二甲基—3—异丙基戊烷70、2—甲基—3 , 3—二乙基戊烷71、2 , 2 , 3—三甲基—3—乙基戊烷72、2 , 2 , 4—三甲基—3—乙基戊烷73、2 , 3 , 4—三甲基—3—乙基戊烷74、2 , 2 , 3 , 3 , 4—五甲基戊烷75、2 , 2 , 3 , 4 , 4—五甲基戊烷。
烃基的同分异构体数目

烃基的同分异构体数目烃是一类由碳氢化合物构成的有机化合物,由于碳原子具有四个键合能力,烃分子可以存在不同的排列方式和结构,从而形成各种同分异构体。
同分异构体是指分子式相同,但结构或空间构型不同的化合物。
烃的同分异构体数目取决于碳原子数目、碳原子排列方式和键合方式等因素。
以下将根据烃的碳原子数目进行分类,讨论不同碳原子数的烃基同分异构体数目。
1. 单烷基(直链烷烃):单烷基是由一个或多个碳原子依次以单键相连构成的直链烷烃。
对于n个碳原子的单烷基,它的同分异构体数目可以通过CnH2n+2的分子式计算。
例如,当n=1时,甲烷(CH4)是唯一的结构;当n=2时,乙烷(C2H6)和丙烷(C3H8)是唯一的结构;当n=3时,有丙烷(C3H8)、异丙烷(C3H8)和丁烷(C4H10)等,总共有3个结构。
因此,n个碳原子的单烷基的同分异构体数目为2^(n-1),其中n为整数。
2. 环烷烃:环烷烃由一个或多个碳原子形成环状结构,并与其他碳原子以及氢原子相连构成的化合物。
环烷烃具有不同的环数和不同的碳原子排列方式,因此同分异构体数目较多。
对于n个碳原子的环烷烃,其同分异构体数目可以通过化学计数原理或荣格公式计算。
化学计数原理指出,对于含有环的化合物,其同分异构体数目等于具有相同分子式的开链同分异构体数目减去一个环的数目。
荣格公式则指出,对于n个碳原子的环烷烃,其同分异构体数目为CnH2n/(2n-2)。
以六个碳原子的环烷烃为例,己烷(C6H14)存在两个同分异构体,环己烷(C6H12)存在一个同分异构体,总共有三个结构。
3. 双烷基:双烷基由两个烷基基团连接而成,可以是直链的也可以是环状的。
对于n1和n2个碳原子的双烷基,其同分异构体数目为2^(n1-1) * 2^(n2-1),其中n1和n2分别表示两个烷基基团的碳原子数目。
例如,当n1=1,n2=2时,存在四个不同结构的双烷基。
4. 双键烃和环烯烃:双键烃由含有一个或多个双键的碳氢化合物组成,而环烯烃是含有一个或多个双键的碳环化合物。
电子式、结构式2、写出甲烷及氯气发生取代反应的化学方

构体。
正丁烷和异丁烷互为同分异构体。
正戊烷、异戊烷和新戊烷互为同分异构体。
C5H12
CH3CH2CH2CH2CH3
CH3CHCH2CH3 CH3
CH3 CH3CCH3
CH3
问:三种物质的沸点是否相同? 正>异>新
一般带有支链越多的同分异构体,熔沸点越低
HHH
||| H-C-C-C-H
|||
H HH
HHHHHH
∣∣∣∣∣∣
H-
C--
∣
C--
∣
C--
∣
C--
∣
C--
∣
∣C-H
HHHHHH
12
3
4
5
CH4 C2H6 C3H8 C4H10 C5H12
6
7
8
9 10
C6H14 C7H16 C8H18 C9H20 C10H22 烷烃分子式通式: CnH2n+2(n≥1)
碳原子数 6 7 分子式 C6H14 C7H16
3
C3H8 丙烷
8
C8H18
4
C4H10 丁烷
9
C9H20
5
C5H12 戊烷
10
C10H22
名称 己烷 庚烷 辛烷 壬烷 癸烷
烷烃简单命名:以碳原子个数为基础命名 ,称“某烷”。 ◆十个以下用“天干地支”命名:甲、乙、丙、丁、戊、己、 庚、辛、壬、癸。 ◆十以上用中文汉字表示:十一烷、二十烷、三十五烷等。
H
∣
H- C-H
∣
H
乙烷
HH
∣∣
H- C-C-H
∣∣
烷烃的同分异构体-烷烃的同分异构体数目怎么数

烷烃的同分异构体:烷烃的同分异构体数目怎么数《烷烃中的同分异构体》教学设计烷烃中的同分异构体教学设计烷烃的学习,是学生在有机化学的学习尚处于启蒙阶段,对有机物结构的知识了解较少的情况下展开的,因此。
如何使学生进一步了解有机物的结构知识,从结构的角度分析有机物种类繁多的原因,是教师教学的重点,也是学生学习的难点之一。
本节内容的教学可采用模型引导、驱动性问题情境的设置、学生主动搭建模型、体验小组合作探究等方法,使学生掌握同分异构现象、烷基等基本概念及同分异构体的书写方法,从而掌握知识与技能,体验探究知识的过程与方法,形成良好的情感态度与价值观。
一、教材分析1、教材的地位和作用本章知识起着连接高中化学必修和高中化学选修模块的作用,必修模块的有机化学具有双重功能,一方面提供有机化学最基本的核心知识,使学生从熟悉的有机化合物入手,了解有机化学研究的对象、目的、内容和方法,另一方面为尽一步学习有机化学的学生打好基础,帮助他们了解有机化学的概况和主要研究方法,激发他们深入学习的欲望。
而本节知识多从结构分析的观点,进而建立结构,性质,用途的认识关系,从本质上认识掌握研究有机物结构的方法,为今后有机化学的学习打下良好的基础,这就需要有同分异构体的概念,教材以烷烃的结构和性质为背景,介绍了有机物的这些基本概念,因此这节课的内容在这一章是举足轻重的。
2、教学目标(1)知识与技能理解烷烃同分异构体及烃基的概念,学会判断简单烷烃及烷基的同分异构体数目及灵活应用所学方法来解决实际问题。
(2)过程与方法通过学生用实物组装简单烷烃的结构模型,帮助学生建立对有机物空间结构图的想象模型,掌握科学研究有机化合物结构的方法,提高解决有关同分异构体书写判断等实际问题的能力,使学生形象思维和抽象思维相互结合从而来提高学生的学习能力。
(3)情感态度与价值观通过创设问题情境培养学生积极思维,增加对有机化学学习的兴趣,通过搭建模型,使学生主动探索和发现,培养积极的创新能力和勇于探索的学习品质。
烷烃所有同分异构体的计算机求解
烷烃所有同分异构体的计算机求解摘要:本文提出了烷烃同分异构体在计算机中的两种表示方法,并用来求解输出指定碳原子个数烷烃的所有同分异构体的分子构造问题。
正文:在种类繁多的有机化合物中,烃是最简单的一种。
它的特点是只含有碳和氢两种元素。
而烷烃又是烃中构造最简单的。
它的分子中碳原子都是饱和4价的,碳原子之间只以单键相互连接,其余的价则完全与氢原子相连。
在计算机表示中只需表示出其碳链即可。
在多碳原子的烷烃中由于分子中碳链构造的不同,同一种烷烃会存在多种同分异构体。
例如丁烷有两种分子构造:C|C-C-C-CC-C-C当碳原子数较少时,其同分异构体数量也较少,凭直观还易于写出其所有的同分异构体;但当碳原子数增加时,其同分异构体数将迅速增加(见表一)从表中可看出表明并没有求烷烃同分异构体数的通式,表一的结果是30年代有人用数学上的图论的方法推算出来的。
但这种方法并不能给出某种烷烃具体的同分异构体结构式。
如果手工求算要寻找大量的碳原子组合方式,最困难的一点是判断求出的同分异构体与已有的是否重复。
用计算机来求解关键也一样,下面分别从算法、数据结构和编程实现三方面来讨论。
一、算法用计算机解决这个问题实际上模拟了人在解决这个问题时的方法。
先写出一个最简单碳链——只有两个碳原子的碳链:1 43 C—C62 5然后可在这个基础上进一步扩展。
具体方法为向这个碳原子加入新的碳原子。
现在可供扩展碳原子的位置有六个,可逐一试放。
放在一个位置后,与已得到的构造进行比较,如果重复则只算一种;如果构造不同,则把这种新的构造储存下来。
在本例中显然六个位置放置后都只算同一种。
对于四个碳原子的情况,是根据三个碳原子的结果再推算的。
在三个碳原子的结构基础上对新形成的八个空位来试放第四个碳原子,判断重复性,可得两个同分异构体。
五个碳原子的情况又是由四个碳原子的两个同分异构体再扩展而来。
按这样的算法,实际上计算N个碳原子的烷烃时都要从三个碳原子的情况一步步推过来。
烷烃
4—甲基—3—乙基
⑦写名称
取代基在前,“某烷”在后,将两者名写在一起
6 7 8 CH3 CH2 —CH2 —CH3 | | 例: CH3—CH—CH2—CH2—CH—CH2—CH3 |2 1 3 4 5| CH3 CH3
2,2,5—三甲基—5—乙基辛烷
练习:用系统命名法命名下列有机物
CH3—CH2—CH2 | CH2 戊烷 | CH3 CH3 |2 1 5 4 3 CH3—CH2—CH—CH—CH3 | CH3
同分异构现象和同分异构体
[讨论]下面是正丁烷和异丁烷的组成和某些物质性质,试分析有 何异同并探讨其原因。 名 称 分子式 C4H10 相对分子质量 熔 58 点 沸 点 相对密度 0.5788 正丁烷 -138.4 -0.5
CH 3—CH—CH— CH2 —CH 3 2 CH 3 CH 3CHCH2CH 2CH 3
CH 3 或者: CH 3CH(CH3 )CH2CH 2CH 3
它们对应的结构简式:
乙烷: H H | | H-C-C-H | | H H 丙烷: H H H | | | H-C-C-C-H | | | H H H
CH3CHCH3 CH3
3烷烃的名称:
碳原子数 分子式 名称
1 CH4
2 C 2H 6
3 4 5 C3H8 C4H10 C5H12
甲烷 乙烷
丙 烷 丁烷
戊烷
6 7 8 9 10 碳原子数 分子式 C6H14 C7H16 C8H18 C9H20 C10H22 名称
己 烷 庚 烷 辛烷 壬烷 癸 烷
碳原子数大于十时,以汉字数字代表称某烷,
①找起点 主链中离支链最近端作为起点 先简单取代基 再繁取代基 ②编序号 用阿拉伯数字给主链碳原子编号 以确定支链的位置
同系物与同分异构体

同系物与同分异构体一、同系物1.概念:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
结构相似是指必须是同类物质,即有机物官能团的种类..要.相同;组成上相差一个或若干个CH2..和个数原子团是指其通式必须相同。
只有同时具备二条件的有机物才互为同系物。
2.同系物的判断方法判断有机物是否是同系物需要注意以下三点:a、同系物必须符合同一通式...........,但通式相同的不一定是同系物,如有机物的同分异构体均不是同系物。
b、同系物结构一定相似,..........但结构相似的不一定是同系物,如有机物的碳链异构和位置异构体。
c、同系物的分子组成上相差一个或若干个“...,.例如苯酚与苯甲醇在分子组成上相差一个..................CH..2.”.原子团“CH2”原子团,但它们不是同一类物质,所以也不是同系物.二、同分异构现象及同分异构体1.概念:具有相同的分子式而又具有不同结构的化合物互称为同分异构体.2.同分异构体的特点:(1)同分异构体具有相同的分子式、相同的最简式、相同的式量和相同的元素组成.分子式相同是前提条件。
(2)结构不同指的是:①碳链骨架不同;②官能团在碳链上的位置不同;③官能团的种类不同。
同分异构体也存在于无机物和有机物之间,无机物与无机物之间(了解即可).如:尿素CO(NH2)2和氰酸铵NH4CNO互为同分异构体。
3.同分异构体的书写同分异构体的书写通常是按碳链异构→位置异构→类别异构的顺序书写,若不按一定的顺序书写容易漏写和重写,如写分子式为C5H10的同分异构体。
⑴碳链异构:①CH2==CHCH2CH2CH31—戊烯②CH2==C(CH3)CH2CH32—甲基-1—丁烯③CH2==CHCH(CH3)CH33-甲基-1—丁烯⑵位置异构:①CH3CH==CHCH2CH32—戊烯②(CH3)2C==CHCH32-甲基—2-丁烯⑶类别异构:①环戊烷②甲基环丁烷③1,1—二甲基环丙烷④1,2—二甲基环丙烷⑤乙基环丙烷碳链异构3种,位置异构2种,类别异构5种,总共十种.4、同分异构体的种类:⑴碳链异构:指碳原子之间连接成不同的链状或环状结构而造成的异构。
日语入门五十音图

3n+1 + O2 2
无机氧化:电子的得失,氧化数的升降
有机氧化:加氧去氢为氧化,加氢去氧为还原
52
2.取代反应:有机化合物分子中原子或原子团
被其它原子或原子团取代的反应
(1)卤代反应:烷烃中的H被X代替的反应。 Br2, Cl2
hv hv hv hv
在紫外光漫射或高温下,甲烷易与氯,溴发生反应。
5.相对密度
分子量↑,密度↑,但<1。
49
练 习
将下列化合物按沸点由高到低顺序排列:
(1)3,3-二甲基戊烷 (2)正庚烷 (3)2-甲基庚烷 (4)正戊烷 (5)2-甲基己烷 答案:(3)(2)(5)(1)(4)
50
2.1.6 、烷烃的化学性质 烷烃分子, C—C , C—H σ键牢固,分子 极化度小,化学性质稳定,一般情况下不 与强酸、强碱、强氧化剂反应,特殊条件
CH3— CH—CH3 CH3
-11.7℃ 异丁烷
( 1 )同分异构现象:分子式相同结构不同的 现象。
6
6
(2)同分异构体:分子式相同而结构不同
的化合物。
结构:分子中原子间相互连接的方式和次序
以及原子或基团在空间的相对位置
7
7
同 分 异 构 体
构造异构
碳链异构
官能团异构
位置异构
互变异构
顺反异构 立体异构 构型异构 对映异构 构象异构
10
10
练习:写出戊烷的同分异构体的结构
C—C—C—C—C C | C—C—C—C C | C—C—C | C 正戊烷 b· p· 36.1℃
戊烷 C5H12
异戊烷
27.9℃
新戊烷 9.5℃
11
高考回归课本资料—— 人教版高中化学选修五《有机化学基础》课本“问题交流”“课后习题”参考答案

人教版高中化学选修五课本“问题交流”“课后习题”参考答案二、问题交流【学与问】按官能团的不同可以对有机物进行分类,并指出有机物的结构可以有多种形式表达──结构式、结构简式等,注意分析在学习有机物分类时往往做出的错误判断。
教师在教学中应注意展示一种官能团的多种书写形式,帮助学生灵活地找出有机物分子中原子之间的连接顺序与连接特点,确认有机物分子中官能团类别,也为学习有机物的结构特点和命名作好知识和能力的准备。
三、习题参考答案1A、D2D3(1)烯烃(2)炔烃(3)酚类(4)醛类(5)酯类(6)卤代烃二、问题交流【思考与交流】书写C5H12的三种同分异构体,复习有关同分异构现象和同分异构体的知识。
教师应引导学生巩固同分异构体的书写规律,强调碳链异构体的书写方法,即先写出直链烃,然后应用“减碳法”,从主碳链的末端减一个碳原子,减去的碳原子作为甲基支链,尝试着连接在除端碳原子外的主链的每一个碳原子上,用排除法将重复出现的结构式删除;再减少主链两个碳原子,分别以两个甲基、一个乙基作为支链连接在除端碳原子外的主链碳原子上……体现出思考问题的有序和严密性,避免学生书写同分异构体时,出现“漏写”或“重写”的错误。
【学与问】在练习书写己烷C6H14的5种同分异构体的结构简式时,由于己烷是饱和烃,因此书写时只考虑碳链异构。
可以视学生的实际情况,继续练习书写丁基(—C4H9)的同分异构体。
而在学生写出C3H6的同分异构体时,C3H6属于不饱和烃,首先引导学生判断是否存在碳链异构,其次思考是否存在官能团的位置异构,最后再考虑丙烯还存在着类别异构,即环丙烷的可能。
教师将解决问题的重点放在书写同分异构体时的思维有序性上。
必要时,可根据学生的实际情况,书写C4H8的同分异构体,进一步掌握书写规律,体会思维有序性对书写同分异构体的影响。
三、习题参考答案1.4 4 共价单键双键三键2.33.B4.C(CH3)45.CH3CH=CH2二、问题交流【学与问1】烷烃同分异构体的数目随着组成烷烃的碳原子数目的增多而迅速增大,并且烃基数目也会增多。
烷烃的同分异构体的书写

C C C C C |1234C C C C C 43|21烷烃的同分异构体的书写【学习目标】1掌握烃基的概念及简单烃基的书写,根和烃基的区别。
2理解同分异构体的概念,理解等效氢和等效碳原子.3能熟练应用烷烃同分异构体的书写规则书写烷烃的同分异构体。
一、烷烃的同分异构体1、烃基(1)定义:烃基:烃分子失去一个氢原子所剩余的部分叫做烃基;烷基:烷烃分子失去一个氢原子所剩余的部分叫做烷基。
烷基的通式: CnH2n+1 (n ≥1),通常用“R —”表示.【练习1】写出甲基、乙基的结构简式 、 。
写出丙烷(CH 3CH 2CH 3)分子失去一个氢原子后的烃基的结构简式、 。
(2)根和基的区别:“根" 电荷,“基" 电荷。
(填“带”或“不带”)例如:OH - 根能独立存在,而—OH 基不能单独存在,原因是存在不成对电子性质活泼。
2、烷烃同分异构体的书写方法(1)同分异构体:分子式相同,性质不同的有机化合物叫同分异构体。
这种现象叫同分异构现象。
(2)书写技巧:先写最长链;然后从最长链减少一个碳原子作为取代基,在剩余的碳链上连接,即主链由长到短,支链由整到散,位置由中心排向两边(2) 以戊烷(C 5H 12)为例:①先写出最长的碳链:C-C —C —C —C 正戊烷 (氢原子及其个数省略了)②然后直连减少一个碳原子:③然后写减少二个碳原子的 :CH 3C (CH 3)2CH 3 ④最后,根据碳原子四个价键,添氢原子即可。
戊烷的同分异构体如下:CH 3CH 2CH 2CH 2CH 2CH 3CH 3CHCH 2CH 3CCH 3CH3CH3CH3(b.p, 36.1)?(b.p, 28 )?(b.p, 9.5 )?正戊烷异戊烷新戊烷通过书写C 5H 10的同分异构体归纳总结书写规律:1. 写出所有碳原子连成一线的碳链作为第一种情况:2. 去掉一个碳原子形成一个甲基接在剩余五个碳的碳链中间..: 3. 去掉两个碳原子形成两个甲基连在剩余四个碳的碳链中间:其中又分成两种情况①两个甲基接在中间同一个碳原子上;②两个甲基接在中间不同碳原子上。
烷烃

附表:烷烃的碳原子数与其对应的同分异构体数
碳原 子数 同分 异体 数
1
1
2
1
3
1
4
2
5
3
6
5
7
8
9 10
9 18 35 75
练习1:
1 互为同位素,___ 2 是同素异形体, 下列五组物质中___
___ 5 是同分异构体,___ 4 是同系物,___ 3 是同一物质。
1、 3、
12 6
C
14 6
CH3CH2CH2CH3 CH3(CH2)3CH3
癸烷
十七烷
CH3(CH2)8CH3
CH3(CH2)15CH3
【练习】下列物质是否为同系物?
A、CH3CH2OH 和 CH3COOH B、CH2=CH2和
CH2 CH2
CH2
C、 CH3CH2CH3和 CH3CH3 D、CH3CH2CH3 和 C(CH3)4
(2)含有18个氢原子的烷烃
(3)相对分子质量为128的烷烃
【讨论与交流】 分析表中数据,讨论烷烃物理性质存在哪些规律?
名称 甲烷 结构简式 CH4 常温时 熔点/℃ 沸点/℃ 相对密度 的状态 气 -182.5 -161.5 水溶性 不溶
乙烷
丙烷 丁烷 戊烷 癸烷 十六烷 十七烷
CH3CH3
CH3CH2CH3 CH3(CH2)2CH3 CH3(CH2)3CH3 CH3(CH2)8CH3 CH3(CH2)14CH3 CH3(CH2)15CH3
CH2 CH3
试比较同系物、同分异构体、同素异形体、同位素 四个名词的含义。 同系物 分子组成相差 一个或几个 CH2原子团 结构相似 有机化合物 同分异构 体 分子式 相同 同素异 形体 同种 元素 同位素 质子数相 同,中子 数不同 ——
什么叫有机物它有哪些组成元素

CH2Cl2 、CHCl3、CCl4是不溶于水的无色油状液体
仔细观察这些方程式有什么共同点? 有机物分子里的某些原子或原子团被其它原 子或原子团所代替的反应叫取代反应
特征: 有上有下,取而代之 CH3Cl、CH2Cl2 、CHCl3、CCl4是甲烷与氯气 反应的四种取代产物,它们的空间构型怎样?
2、组成元素:
碳、 氢、氧、氮、硫、磷、卤素等
主要元素
其他元素
只含碳、氢元素的有机物叫烃。
烃字的由来:
火 + 气 =烃
tàn qīng
例1.下列物质属于烃的是( BEJ )
A.H2S B.C10H22 C.CH3Cl
D.C2H5OH E.C2H4
F.H2
G.金刚石 H.CH3COOH
I.CO2
①通式__同___(填“同”或“不同”)
②是__同____一同类别的物质;
③组成元素不_同____;
14n
④⑤分结子构式相似递;变,相对分子相质似量相差
;
练一练:
B
1、下列各组是同系物的是( )
A、CH3CH2CH2CH3 B、CH3CH3
C、CH2=CH2
CH3CH(CH3)CH3
CH3CH(CH3)CH3
C原子数目5~16,是液体;
C原子数目16以上,是固体
② 烷烃的熔沸点随C原子数目的增加 而升高。
③ 烷烃的相对密度随C原子数目的
增加而高,且均小于1,不溶于水。
思考:怎样分离液态烷烃与水的混合物?
5、化学性质(与甲烷相似)
(1)氧化反应(燃烧)
请用通式写出烷烃完全燃烧的
化学方程式? 均不能使KMnO4溶液、溴水褪色, 不与强酸,强碱反应。 烃燃烧的通式呢?烃用CxHy表示
化学必修二—烷烃
正己烷
异己烷
新己烷
正: 直链烷烃
异
CH3CHCH3
新
CH3 CH3CCH2CH3
2)系统命名法(IUPAC命名法) )系统命名法( 命名法) 命名法 a. 选最长碳链作主链,支链作取代基。遇多个等长碳链,则 选最长碳链作主链,支链作取代基。遇多个等长碳链, 取代基多的为主链。 取代基多的为主链。
2-甲基 -5-(1,1-二甲基丙基)癸烷 甲基 ( , 二甲基丙基 二甲基丙基) e. 名称的排列顺序 中文名称按基团顺序规则,较小的基团列在前; 中文名称按基团顺序规则,较小的基团列在前;英文名称 按基团首字母的字顺先后列出。 按基团首字母的字顺先后列出。
CH2CH2HC3 CH3CH2CH2CHCHCH2CH2CH2CH3 CHCH3 CH3
顺序大的基团称较优基团。 顺序大的基团称较优基团。
支链上连有取代基, d. 支链上连有取代基,则从和主链相连的碳原子开始将支链 碳原子依次编号,并将取代基位号、 碳原子依次编号,并将取代基位号、名称连同支链名写在 括号内。 括号内。
1 2 3 4 5
1'
6
2'
7
3'
8
9
10
CH3CHCH2CH2CHCH2CH2CH2CH2CH3 CH3 H3C C CH2 CH3 CH3
5-丙基 异丙基壬烷 丙基-4-异丙基壬烷 丙基 4-isopropyl-5-propylnonane [注意 注意] 注意 1)相同取代基数目用汉文数字二、三 ...表示; )相同取代基数目用汉文数字二、 表示; 表示 2)取代基位号用阿拉伯数字表示; )取代基位号用阿拉伯数字表示; 3)阿拉伯数字与汉字之间必须用短横线分开; )阿拉伯数字与汉字之间必须用短横线分开; 4)阿拉伯数字之间必须用逗号分开。 )阿拉伯数字之间必须用逗号分开。
有机化合物同分异构体数目查找方法与技巧

有机化合物同分异构体数目查找方法与技巧作者:包军宋正华来源:《理科考试研究·高中》2015年第02期存在同分异构现象是有机化合物结构的重要特征之一,同时也是有机化合物种类繁多的原因之一,同分异构体的查找非常好地体现了思维的有序性、分类思想以及基础有机化学知识的综合运用,故其成了高考必考点之一,因此,无论高考备考,还是培养运用分类思想和有序思维分析问题的习惯,学习并掌握有机化合物同分异构体数目查找方法与技巧都显的非常必要.一、等效碳法(取代法)1.烷烃同分异构体数目的查找(1)简单烷基同分异构体种类的查找烷烃从分子式(C4H10)开始,随着碳原子数增加出现同分异构现象,甲烷、乙烷和丙烷均没有同分异构体,甲烷、乙烷和丙烷分子分别去掉1个氢原子得到的烷基是查找其它烷烃同分异构体的基础,甲基(-CH3)和乙基(-CH2CH3或-C2H5)均只有一种,丙基(-C3H7)有正丙基(-CH2CH2CH3)和异丙基[-CH(CH3)2]两种.(1)简单烷烃(含碳原子数少于等于8)同分异构体数目查找是其它有机化合物同分异构体查找的基础,烷烃同分异构体数目查找关键是碳链骨架排列,为了查找的全面又不重复,可按照以下步骤:(1)将所有碳原子直线连接作为主链,(2)主链碳原子依次减少,(3)去掉1个碳作为甲基从中心到末端的倒数第2个碳依次连接,左右对称位置只连1次,(4)当需要从主链去掉2个碳时,首先按照乙基连接于主链,与甲基连接时顺序相同,只是只能从中心到倒数第3个碳,然后再变换成2个甲基在主链上按照同、邻和间的位置排列,(5)当需要从主链去掉3个碳时,首先作为正丙基,其次作为异丙基,然后分为1个甲基和1个乙基,最后分为3个甲基,按照上述类似的方法连接于主链书写查找.(2)其它烷基同分异构体数目查找烷烃去掉一个氢原子所得烷基种类的查找,首先写出该烷烃分子式对应所有同分异构体碳的骨架,书写碳链骨架时,每一个碳原子周围的碳碳单键在同一平面内夹角相等,完全处于面对称的碳原子为同种碳原子(等效碳),那么某烷基(由相应烷烃去掉1个氢原子)同分异构体的种类查找方法为:由该烷基碳原子写出的所有碳链中碳原子的种类减去季碳原子的种类所得的差.如丁基(-C4H9)的种类查找方法为:首先写出四个碳原子构成的所有碳链(见图1):CCCCCCCC图1丁基的查找碳链书写碳链a共有2种碳原子,碳链b共有2种碳原子,上述两种碳链中没有季碳原子,所以(-C4H9)的种类数目=2+2-0=4,同样的方法可以得出戊基(-C4H9)的种类数目=3+4+2-1=8.复杂烷烃(含碳原子数多于8)同分异构体种类的查找可按照上述进行综合应用.2.含苯环有机化合物同分异构体数目查找含苯环有机化合物同分异构体数目查找分为苯环上单取代和多取代两类,单取代同分异构体数目多少取决于该取代基的同分异构体数目,多取代同分异构体数目是在确定取代基构造的基础上,以两个取代基在苯环上的邻、间、对位置关系进行查找,若有3个取代基且其中2个相同,则以两个相同的取代基进行邻、间、对分布,再查找第3个取代基的可连位置情况为宜,若3个各不相同,任意选取两个按照邻、间、对分布后再查找第3个取代基的位置情况,取代基3个以上采取类似的方法.3.取代基型烃的有机化合物同分异构体数目查找当一种有机化合物(题目)结构中确定由1个末端取代基和另一部分组成时,通常使用等效碳法(取代法),如确定该结构中含有-X、-CHO、-OH、-COOH、-OOCH、-NH2和-Ph 等,首先书写碳骨架(含除要研究的取代基外的其它官能团),然后按照烷基数目查找方法(等效碳法)查找其同分异构体数目.如分子式为C5H11Cl的同分异构体数目、分子式为C5H12O且可与金属钠反应放出氢气的化合物数目和分子式为C10H14的单取代芳香烃数目等.2.等效键法(嵌入法)当一种有机化合物(题目)结构中确定有二价结构和另一部分组成时,通常使用等效键法(嵌入法),如结构中确定含有“CCOCOCOO”等,查找此类有机化合物同分异构体数目时,首先写出指定要求除二价结构外的结构式,然后根据处于对称面的单键为同类单键,找出所有单键的种类,接下来将二价结构分为两类,即对称的如“CCOCO”和不对称的如“COO”,对于含有对称性二价结构的同分异构体数目就等于除二价结构外的结构式中单键的种类,对于含有不对称的二价结构的同分异构体数目就等于除二价结构外的结构式中两端不对称单键二倍加上两端对称单键的种类,如查找分子式为C7H8O的同分异构体中含有苯环的同分异构体的种类:首先确定二价结构“-O-”,然后找出题目中去掉“-O-”剩余结构中单键种类,即HHHCHHHHH中的单键碳氢键4种、碳碳单键1种,单键共5种,因此分子式为C7H8O的同分异构体中含有苯环的同分异构体共有5种;再如分子式为C5H10O2能与NaOH溶液反应的同分异构体的数目查找:首先确定不对称二价结构“O”,然后找出去掉“O”剩余结构中单键种类,即HCHHCHHCHHCHHH和CCHHHHCHHHCHHH,其中碳氢单键共4种、对称碳碳单键1种和不对称碳碳单键2种,因此分子式为C5H10O2能与NaOH溶液反应的同分异构体的种类为1+(4+2)×2=13(种).三、综合运用高考愈来愈注重对方法和能力的考查,对查找有机化合物同分异构体数目能力要求同样越来越高,表现为许多题目解决需要等效碳法(取代法)、芳香烃同分异构体查找方法和等效键法(嵌入法)的综合运用,如:分子式为C5H11O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯种类,首先应用等效键法(嵌入法)找到其水解分别产生甲酸、乙酸、正丙酸、正丁酸和异丁酸等5种以及1-甲醇、2-甲醇、2-甲基-1-丙醇、2-甲基-2-丙醇、1-丙醇、2-丙醇、乙醇和甲醇等8种,然后再将两类分别组合成酯,即5×8=40(种);再如:扁桃酸CHCOOHOH有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体种类查找,首先确定1个末端取代基“-OOCH”,然后按照芳香烃同分异构体查找方法,即邻、间、对3种甲基苯酚基础上应用效碳法(取代法)找到符合题意的同分异构体共13种.总之,同分异构体数目查找题目素材来源广泛,变化灵活,既便于高考较好地对方法与能力考查,又培养学生有机化学基础的学科素养,从而避免学生应用死记硬背的方式应对,最终利于学生养成学习时善于探究方法、思考时积极运用有序性逻辑的良好习惯.。
烷烃

判断:
CH3 CH3-CH2-CH2-CH3 与 CH3-CH-CH3是同种物质吗? C4H10 异丁烷
分子式:C4H10 名称: 正丁烷
名
称
熔
点
沸
点
正丁烷 异丁烷
-138.4℃ -159.6℃
-0.5℃ -11.7℃
相对密度 0.5788
0.557
带有支链越多的同分异构体,沸点越低
二、同分异构现象和同分异构体
丙烷:
H H H | | | H-C-C-C-H | | | H H H
丁烷
H H H H | | | | H-C-C-C-C-H | | | | H H H H
思考:它们的分子结构有哪些共同的特点?
一、烷烃的结构和性质 1、结构:
⑴ 碳原子之间都以单键(C—C)结合成链状
⑵ 碳原子其余的价键都跟氢原子结合达到饱和 饱和链烃 或烷烃
②3-甲基-2-乙基戊烷 ③3,3-二甲基丁烷 ④2,2-二甲基丁烷 ⑤2,3,3-三甲基丁烷
⑥2-乙基-3-甲基丁烷
⑦2,3-二乙基丁烷
练习:写出下面烃的名称。
3
2 1
4
5 6
2—甲基丁烷
3,4—二甲基己烷
练习:写出下面烃的名称。
2 1 3 4
2,3—二甲基丁烷
1 7 6 5 4 3 3 3
8 9
2 2
3,4,5,5—四甲基壬烷
练习:写出下面烃的名称。
CH3—CH—CH2—CH—CH2
5、6
1
2
3
4
5
CH3
1 2 3
C2H5 CH3
(2)系统命名法(IUPAC)
选碳链: 选择最长的碳链做主链(长) 当不同碳链的碳原子数相同时,选择支链最多的一个作主链(多) 编位号: 离主链最近的支链一端开始编号(近) 不会出现1—甲基,2—乙基,3—丙基…… 若两个相同支链离两端一样近,而中间还有支链,则按支链编号 相加最小一端开始(小) 当两个不同支链离两端一样近,从简单的支链一端开始编号(简) 写名称: 取代基,写在前,编号位,短线连 相同基,合并算,不同基,简到繁 阿拉伯数字与文字之间用“—”隔开;阿拉伯数字之间用“,”隔 开。
