15实验十五 烟酸片的含量测定
HPLC法测定烟酸片的溶出度

色 谱 条 件 色 谱 柱: 赛 默 飞 Hypersil Gold C18 柱 11.0356、11.0438、11.0445、11.0550, 平 均 峰 面 积 为
(4.6 mm×250 mm,5 μm); 流 动 相:0.1% 三 乙 胺 11.0420,RSD=0.07%(n=6),结果表明该方法精密度良好。
2.20 ~ 39.93 mg•L-1 浓度范围内显良好的线性关系(r=1), 置 100 mL 容量瓶中,加水溶解并稀释至刻度,作为对照
平均回收率为 99.51%(n=9),RSD 为 0.79%。结论 : 该 品溶液。
方法准确、可靠,可用于烟酸片的溶出度测定。
溶出度供试品溶液的制备 取本品按照溶出度测定法
差异均不大,峰型均保持良好,本文流动相系统耐用性较好。
拓展测定比较 按处方比例自制三批样品,采用高效
液相法和紫外分光光度法对更多批次烟酸片溶出度进行拓
展测定比较,并采用统计学分析方法对测定结果差异进行
了分析评价,结果,高效液相法与紫外分光光度法测定结
果基本一致。
参考文献 [1] 孙丹杰 . 托伐他汀与烟酸缓释片联合治疗高脂血症 的疗效分析 [J]. 母婴世界 ,2019,(18):104-104. [2] 韩奕奕 , 王霞 , 马颖清 , 等 . 乳粉中烟酸和烟酰胺 含量测定能力验证结果与分析 [J]. 食品安全质量检测学 报 ,2020,(17):93-99. [3] 国家药典委员会 . 中华人民共和国药典:二部 [S]. 北京:中国医药科技出版社,2020:1410-1411. [4] 韩 素 超, 张 红 中, 祖 振 涛, 等 .JJF( 浙)10962014《药物溶出度仪校准规范》问题探讨 [J]. 计量与测试 技术,2020,(10):104-105. [5] 刘晓雨,胡洋,王卓,等 . 烟酸在水中的溶解度及 介稳性质的研究 [J]. 化学工程,2019, 47(7):35-40. [6] 纪 世 彬 . 高 效 液 相 色 谱 - 二 极 管 阵 列 检 测 器 法 测 定 复 合 维 生 素 B 片 中 5 种 组 分 的 溶 出 度 [J]. 安 徽 医 药 ,2020,24(8):1512-1514. [7] 蔡迪鸣 .HPLC 法同时测定党参中烟酸及党参炔苷 含量的方法探究 [J]. 医药前沿,2018, 8(18):398-398. [8] 黄 丹, 丁 家 昱, 刘 秀 秀, 等 . HPLC 测 定 盐 酸 烟 酰美金刚胺中的烟酸及其他有关物质 [J]. 华西药学杂志, 2017, 32(4):421-423. [9]Cellar Nicholas A.,McClure Sean C.,Reddy Todime M.,et al.A new sample preparation and separation combination for precise, accurate, rapid, and simultaneous determination of vitamins B-1, B-2, B-3, B-5, B-6, B-7, and B-9 in infant formula and related nutritionals by LC-MS/MS[J].Analytica Chimica Acta,2016,934:180-185. 作者简介:梁晓云,女,主管药师,主要从事食品药
烟酸和烟酰胺的含量测定培训PPT

新标准代替 GB 5009.89-2016
主要变化内容
1. 高效液相色谱法调整为第一法,微生物法调整为第二法; 2. 增加了第二法 微生物法 中的微孔板法、试样处理后调节
pH的要求; 3. 修改了第二法 微生物法 的标准曲线浓度范围、精密度和
定量限。
第一法 高效液相色谱法
第一法 高效液相色谱法
3. 烟酸和烟酰胺标准混合工 作液
分别准确吸取标准混合中间液 1.0 mL、2.0 mL、5.0 mL、10.0 mL、20.0 mL 于 100 mL 容量 瓶中,加水定容至刻度,混匀,得到质量浓度分别为 1.0 μg/mL、2.0 μg/mL、5.0 μg/mL、 10.0 μg/mL、20.0 μg/mL 的标准混合工作液。临用现配。
1. 盐酸溶液(5.0 mol/L):量取 415 mL 盐酸,加水定容至1000 mL。 2. 盐酸溶液(0.1 mol/L):量取 8.3 mL 盐酸,加水定容至1000 mL。 3. 氢氧化钠溶液(5.0 mol/L):称取氢氧化钠 200 g,加水定容至1
000 mL。 4. 氢氧化钠溶液(0.1 mol/L):吸取20mL氢氧化钠溶液(5.0 mol/L),
哪些食物可以补充烟酸?
烟酸在食物中分布广泛,含量丰富,例如动物为基础的食物有:动物肝脏、肾脏、鱼肉、禽类肉;植物为 基础的食物有:蘑菇、花生、全谷、坚果等等,还有些特殊的营养强化食物等
烟酸需要额外补充吗?
一般人不需要除膳食以外额外补充烟酸,也尚未见膳食摄 入烟酸过量引起中毒的报道。烟酸摄入过量,易出现皮肤潮红、 恶心、呕吐、糖耐量异常等不良反应,因此一般不建议过量服用。
4. 氢氧化钠溶液A(10mol/L):称取 400g氢氧化钠,加水溶解并稀释至1 000 mL。
药物分析实验指导书(11版大纲)
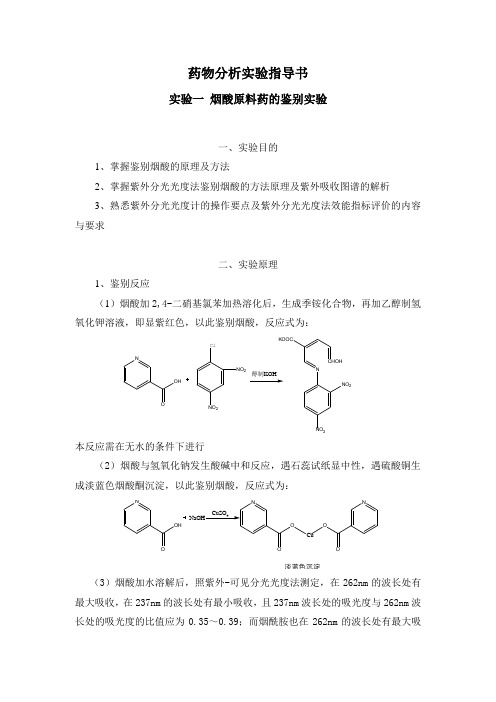
药物分析实验指导书实验一烟酸原料药的鉴别实验一、实验目的1、掌握鉴别烟酸的原理及方法2、掌握紫外分光光度法鉴别烟酸的方法原理及紫外吸收图谱的解析3、熟悉紫外分光光度计的操作要点及紫外分光光度法效能指标评价的内容与要求二、实验原理1、鉴别反应(1)烟酸加2,4-二硝基氯苯加热溶化后,生成季铵化合物,再加乙醇制氢氧化钾溶液,即显紫红色,以此鉴别烟酸,反应式为:NOHOCl醇制KOHNCHOHKOOCNO22NO2NO2本反应需在无水的条件下进行(2)烟酸与氢氧化钠发生酸碱中和反应,遇石蕊试纸显中性,遇硫酸铜生成淡蓝色烟酸酮沉淀,以此鉴别烟酸,反应式为:NOH OONOOCu淡蓝色沉淀(3)烟酸加水溶解后,照紫外-可见分光光度法测定,在262nm的波长处有最大吸收,在237nm的波长处有最小吸收,且237nm波长处的吸光度与262nm波长处的吸光度的比值应为0.35~0.39;而烟酰胺也在262nm的波长处有最大吸收,在245nm波长处有最小吸收,在A254nm/A262nm为0.63~0.67。
因此可用该方法来区别烟酸和烟酰胺。
三、实验内容与操作(一)仪器和试剂1、仪器紫外分光光度计、配对比色杯一对、试管(25ml,2支)、电炉、药物天平、烧杯(50ml,2只)、容量瓶(100ml、10ml各2只)、移液管(1ml,2只)、乳钵(小号1个,配乳槌)。
2、试剂烟酸、0.4%氢氧化钠试液(取氢氧化钠0.4g,加水使溶解成100ml,即得)、2,4-二硝基氯苯、乙醇制氢氧化钾试液(取氢氧化钾3.5g,加100ml95%乙醇使溶解,静止后取上清液)、硫酸铜溶液(取硫酸铜12.5g,加水溶解成100ml,即得),蒸馏水、95%乙醇(二)实验步骤1、鉴别(1)取烟酸约4mg,加2,4-二硝基氯苯8mg,研匀,置试管中,缓缓加热溶化后,再加热数秒钟,放冷,加乙醇制氢氧化钾试液3ml,即显紫红色。
(2)取烟酸约50mg,加水20ml溶解后,滴加0.4%氢氧化钠溶液至遇石蕊试纸显中性反应,加硫酸铜试液3ml,即缓缓析出淡蓝色沉淀。
药品检验考试题(A)

药品检验考试题(A)一、名词或符号解释:(20分)1、系统误差:2、Beer-lambert定律:3.、药物的杂质:4药品认证:5、处方药:二、填空题:(20分)1、调配处方时必须经过_______,对有配伍禁忌或超剂量的处方应_______,必要时经处方医师更正或者_______,方可调配。
2、偶然误差服从_______规律,因此可采取_______的措施减免偶然误差。
3、以下二个数据,根据要求需保留三位有效数字;1.05499修约为_______;4.715修约为_______。
4、721分光光度计的光源为_______,测定时选用_______比色皿。
5、国家根据非处方药品的_______,将非处方药分为甲类和乙类6、按化学反应类型分类,滴定分析法分为_______、_______、_______和_______等四大类。
7、酸碱滴定中,指示剂的选择原则是:指示剂的_______处于或部分处于_______之内。
8、生产新药或已有国家标准的药品,须经_______批准,并发给_______。
9、衡量正常色谱峰与不正常色谱峰时,应采用_______ 。
水解乙酰胆碱的酶是。
三、单选题:(20分)1、测定精密度好,表示().A: 系统误差小B: 偶然误差小C: 相对误差小D: 标准偏差小2、下列叙述正确的是().A: 溶液pH为11.32,读数有四位有效数字B: 0.0150g试样的质量有4位有效数字C: 测量数据的最后一位数字不是准确值D: 从50mL滴定管中,可以准确放出5.000mL 标准溶液3、分析天平的称样误差约为0.0002克,如使测量时相对误差达到0.1%,试样至少应该称( ) 克。
A: 0.1000克以上B: 0.1000克以下C: 0.2克以上D: 0.2克以下4、下列哪些要求不是重量分析对称量形式的要求().A: 必须稳定B: 颗粒要粗大C: 摩尔质量要大D: 必须有确定的化学组成5、制定《中华人民共和国药品药品管理法》的目的不包括()A、保证药品质量B、保障人体用药安全C、保障人民身体健康和用药的合法权益D、加强药品监督管理E、发展现代药和传统药6、《药品经营许可证》的有效期为()A、5年B、4年C、2年D、1年7、在分光光度分析中,某有色溶液的最大吸收波长().A: 随溶液浓度的增大而增大B: 随溶液浓度的增大而减小C: 与有色溶液浓度无关D: 随溶液浓度的变化而变化8、欲使色谱图趋于正态分布曲线,其色谱柱的塔板数应为()A 10以上B 100以上C 100以下D 103以上9、国家食品药品监督管理局主管()A、制定药品行业发展规划B、制定药品行业的产业政策C、全国药品监督管理工作D、药品审批E、药品质量监督检查10、药物作用的两重性指()A.既有对因治疗作用,又有对症治疗作用B.既有副作用,又有毒性作用C.既有治疗作用,又有不良反应D.既有局部作用,又有全身作用E.既有原发作用,又有继发作用四、多选题:(10分)1、配制NaOH标准溶液,以下操作正确的是()。
食品中烟酸(维生素PP)的测定(NO2)

食品中烟酸(维生素PP)的测定一、概述•烟酸又名维生素PP、尼克酸、抗癞皮病因子等,属水溶性维生素,是具有生物化学活性的吡啶-3-羟酸及其衍生物的总称•烟酸和维生素B1、维生素B2一起参与碳水化合物和能量的代谢、促进血液循环及皮肤健康、维持正常神经系统,也是合成性激素不可或缺的物质•自然界中的烟酸广泛存在于食物中,植物性食物中存在的主要形式为烟酸,动物性食物中主要以烟酰胺形式存在烟酸的化学式为C6H5NO2,相对分子质量为123.11,化学名称为吡啶-3-羟酸(3-pyridinecarboxylicacid),结构式如下一、概述•烟酸为无色针状晶体,味苦。
性质比较稳定,在酸、碱、氧、光或加热条件下不易破坏,烟酸溶于水,溶于乙醇,但不溶于乙醚。
紫外扫描于198 nm、263 nm处有两个特征波长,其中最大紫外吸收波长为263 nm。
•目前尚未见到因食源烟酸摄入过多而引起中毒的报告,所见烟酸的毒副作用大多为临床大剂量使用烟酸所致。
当口服剂量为30 mg/d~1000 mg/d,有人出现血管扩张的症状;当口服剂量达到3 g/d~9 g/d时,可引起黄疸和血清转氨酶升高,但作用机制尚不十分清楚。
•目前大多数国家制定烟酸膳食参考摄入量为13 mg/d~20 mg/d。
我国推荐的膳食摄入量为男性14 mg/d,女性13 mg/d,和美国一致二、食品中烟酸的测定【说明1】(GB/T 5009.89-2003)微生物法【说明1】•标准方法的来源:• 1.本标准根据全国卫生标准技术委员会“第七个五年计划期间卫生标准研制计划第四项食品卫生标准中理化检验方法制标任务”,由原中国预防医学科学院营养与食品卫生研究负责建立并起草,内蒙古自治区卫生防疫站、青岛医学院等多家科研单位组成协作组反复验证后提出的。
• 2.本法主要是在参照AOAC 944.13以及美国《维生素分析方法》等文献的基础上建立的,适用于所有食品的分析1范围【说明2]•本标准规定了用微生物方法测定食品中的烟酸含量。
HPLC法测定人血浆中烟酸和烟尿酸含量方法探究

HPLC法测定人血浆中烟酸和烟尿酸含量方法探究[目的]建立一个同时测定人血浆中烟酸及其活性代谢物烟尿酸的RP-HPLC方法,并用于临床药代动力学研究。
[方法]取1ml人血浆于一干净试管中,加入20μl内标甲硝唑,涡旋10s,再加入3ml乙腈,涡旋1min,3000rpm下离心5min,将上清全部取出置于另一干净试管,加入3ml氯仿,涡旋5min,3000rpm下离心5min,取水溶层(上层)200μl和100μl流动相混匀,取20μl进样,检测波长为262nm。
[结果]烟酸,烟尿酸和内标甲硝唑的保留时间为 4.5min,7.5min和105min。
烟酸和烟尿酸日内与日间精密度的RSD均小于11%,烟酸和烟尿酸在50ng/ml到5000ng/ml范围内线性均良好,烟酸的其他代谢物如烟酰胺、N-甲基烟酰胺等无干扰。
标签:烟酸和烟尿酸;色谱法;高效液相;血样处TB烟酸为B族维生素之一,对人类和动物的营养有着重要的作用。
很多文献都报道了烟酸在脂代谢中的药理作用和烟酸在治疗高脂血症中的广泛应用,但关于烟酸及其代谢产物的药动学研究却鲜有报道,在国内同时测定烟酸和烟尿酸的方法还未见报道。
为更好地研究烟酸降血脂作用和副作用的机制,建立一个简便快捷准确测量生物样品中烟酸及其代谢产物浓度的方法是很有意义和非常必要的。
在烟酸测定初级阶段,一系列技术得到了广泛应用,如微生物法、色度法、传统柱色谱法、气液色谱法等,在过去的20年里,高效液相色谱法得到了普遍应用。
本法即在前人基础上用高效液相色谱法测定人血浆中烟酸及其活性代谢产物烟尿酸的含量。
1 仪器与试剂1.1 仪器Waters高效液相色谱系统(Waters 600泵,Waters 2487型紫外检测器,N2000型色谱工作站);AUW120 D电子分析天平;台式离心机(上海安亭科学仪器厂);KQ3200型超声波清洗器(昆山市超声仪器有限公司);IKA VORTEX Genious 3涡旋器。
HPLC法测定烟酸注射液中烟酸的含量及有关物质

HPLC法测定烟酸注射液中烟酸的含量及有关物质谭建平;陈禧翎;郑思嘉【期刊名称】《国际医药卫生导报》【年(卷),期】2012(18)12【摘要】目的建立高效液相色谱法用于烟酸注射液中烟酸的含量测定及有关物质检查.方法用碳十八烷基硅烷键合硅胶为填充剂;以乙腈-0.05 mol/L磷酸二氢钠溶液(用磷酸调节pH值至2.5)(1∶99)为流动相;检测波长为262nm.结果重复性及回收率结果良好,重复性的RSD为0.07%(n=6),烟酸与相关杂质分离度好,烟酸的最低检出限为0.04μg/ml,线性范围为0.004983~ 0.19932 mg/ml(R=0.9999),平均回收率为100.2%(RSD=0.40%).结论高效液相色谱法准确可靠,可用于烟酸注射液中烟酸的含量测定及烟酸注射液有关物质的检查,操作简便、准确度高.%Objective To establish a high performance liquid chromatography (HPLC) method for determination of the concentration and related substances in niacin injection.Methods niacin can be separated on Waters symmetry C18 column (5 um; 4.6 × 150 mm) with a mixture of 0.05 mol/L sodium phosphate (adjust pH value to 2.5 with phosphoricacid):acetonitrile (99∶1) as mobile phase and detected at 262 nm.Results The result of reproducibility was 0.07% (n=6).Niacin was well separated from other impurity with this method.The lowest detection limit was 0.04 μ g/ml,the standard curve was linear in the concentration range of 0.004 983~0.199 32 mg/ml and the correlation coefficient was 0.999 9.The average recovery rate was 100.2% (RSD=0.40%).Conclusion The method issimple and accurate.It is adopted to determine the concentration and related substances of niacin injection.【总页数】4页(P1785-1788)【作者】谭建平;陈禧翎;郑思嘉【作者单位】510250 广州白云山明兴制药有限公司;510250 广州白云山明兴制药有限公司;510250 广州白云山明兴制药有限公司【正文语种】中文【相关文献】1.HPLC法测定左卡尼汀注射液中的含量及有关物质A [J], 李红英;于得才2.HPLC法测定党参中烟酸和党参炔苷的含量 [J], 高欢;李阳;闫辉;李灿;吕青涛;容蓉3.反相HPLC法测定烟酸占替诺及有关物质的含量 [J], 孙晓波;周亮;徐永丽4.HPLC梯度洗脱法测定丙泊酚中/长链脂肪乳注射液的含量及有关物质 [J], 焦旭雯;梁蔚阳;陈华5.HPLC法测定人血浆中烟酸和烟尿酸含量方法探究 [J], 陈冬因版权原因,仅展示原文概要,查看原文内容请购买。
烟酰胺片含量及有关物质测定方法改进

ChinaPharmaceuticals
·研究· Drug Research
·检验检测·
doi:10.3969/j.issn.1006-4931.2019.09.010
烟酰胺片含量及有关物质测定方法改进
李志远,刘 屹,左文松
(云南省食品药品监督检验研究院,云南 昆明 650106)
摘要:目的 建立测定烟酰胺片含量及有关物质的高效液相色谱(HPLC)法。方法 色谱柱采用 UITimateXB-C18柱(250mm×4.6mm, 5μm),流 动相为甲醇 -pH6.0的 0.05mol/L醋 酸铵溶液(10∶90),柱温 为 30℃,流 速为 1.0mL/min,进 样量为 20μL,检 测器为 PDA。结果 按新建 HPLC法测定 73批样品的含量,与 2015年版《中国药典(二部)》紫外分光光度(UV)法测定结果无显著差异(t=0.79,P> 0.05)。按 2015年版《中国药典 牗二部 牘》薄层色谱 牗TLC牘法检测,均未检出烟酸及其他杂质;按新建 HPLC法测定,均检出烟酸杂质,大部
nicotinicacidimpuritiesweredetected,andtheotherimpuritiesweredetectedinmostofthesamples.Conclusion TheestablishedHPLC
methodissimple,accurateandreliable.ItcanbeusedforthecontentdeterminationofnicotinamideandrelatedsubstancesinNicotinamide
烟酰胺片(NicotinamideTablets)系吡啶衍生物 3-吡 啶甲酰胺,属于水溶性 B族维生素类药物,在体内与核 糖、磷酸、腺嘌呤形成烟酰胺腺嘌呤二核苷酸(辅酶Ⅰ) 和烟酰胺腺嘌呤二核苷酸磷酸(辅酶Ⅱ),为脂质代谢、 组织呼吸的氧化作用和糖原分解所必需,缺乏时会影响 细胞的正常呼吸和代谢,进而引起糙皮病;胃肠道易吸收, 吸收后分布到全身组织,半衰期(t1/2)约为 45min,经肝 脏代谢,治疗量仅少量以原形自尿排出,但过量服用时排 泄量增加。烟酰胺与异烟肼有拮抗作用,长期服用异烟肼 时应适当补充烟酰胺;烟酰胺无扩张血管作用,可用于高 血压患者。2015年版《中国药典(二部)》收载有薄层色谱 (TLC)法测定其有关物质,紫外分光光度(UV)法测定含 量犤1-2犦。高效液相色谱 牗HPLC牘法测定其含量和有关物质 也有文献犤3-6犦报道。本研究中选择 2种不同的方法测定烟 酰胺片的含量及有关物质,为该药的质量控制提供更加 简便、准确、高效的评价方法犤7-9犦。现报道如下。 1 仪器与试药
大学《药物分析》章节试题及答案(五)

大学《药物分析》章节试题及答案第十二章药物制剂分析一、选择题1.下列说法不正确的是( B )(A)凡规定检查溶解度的制剂,不再进行崩解时限检查(B)凡规定检查释放度的制剂,不再进行崩解时限检查(C)凡规定检查融变时限的制剂,不再进行崩解时限检查(D)凡规定检查重量差异的制剂,不再进行崩解时限检查(E)凡规定检查含量均匀度的制剂,不再进行重量差异时限检查2.对于平均片重在0.30g以下片剂,我国药典规定其重量差异限度为( C )(A)±3% (B)±5%(C)±7.5% (D)±10% (E)以上均不对3.片剂重量差异限度检查法中应取药片( D )片。
(A)6片 (B)10片 (C)15片(D)20片 (E)2片4.含量均匀度检查主要针对( A )(A)小剂量的片剂 (B)大剂量的片剂 (C)所有片剂(D)难溶性药物片剂 (E)以上均不对5.下列关于溶解度的叙述错误的是( E )(A)溶解度检查主要适用于难溶性药物 (B)溶解度检查法分为转蓝法和浆法(C)溶解度检查法规定的温度为37℃ (D)凡检查溶解度的片剂,不再进行崩解时限检查(E)溶解度与体内的生物利用度直接相关6.注射剂中加入抗氧剂有许多,下列答案不属于抗氧剂的为( D )(A)亚硫酸钠 (B)焦亚硫酸钠 (C)硫代硫酸钠 (D)连四硫酸钠 (E)亚硫酸氢钠7.药典规定,采用碘量法测定维生素C注射液的含量时,加入( B )为掩蔽剂,消除抗氧剂的干扰(A)氯仿 (B)丙酮 (C)乙醇 (D)甲酸 (E)以上均不对8.中国药典规定,硫酸亚铁片的含量测定采用( B )法以消除糖类赋形剂的干扰。
(A)高锰酸钾法 (B)铈量法 (C)碘量法 (D)溴量法 (E)络合滴定法9.复方阿司匹林片中咖啡因的含量测定方法为( B )(A)滴定法 (B)剩余碘量法 (C)配合滴定法 (D)银量法 (E)以上都不是10.为了防止阿司匹林的水解,在制备复方阿司匹林片时,常加入( B )为稳定剂。
婴幼儿食品和乳品中烟酸和烟酰胺的测定

婴幼儿食品和乳品中烟酸和烟酰胺的测定一、方法提要烟酸在人体内转化为烟酰胺,烟酰胺是辅酶Ⅰ和辅酶Ⅱ的组成部分,参与体内脂质代谢,组织呼吸的氧化过程和糖类无氧分解的过程。
它能促进消化系统的健康,减轻胃肠障碍;减轻腹泻现象;使皮肤更健康;使人体能充分地利用食物来增加能量;它是婴幼儿不可缺少的维生素之一。
本实验根据《食品安全国家标准—婴幼儿食品和乳品中烟酸和烟酰胺的测定》中提供的方法进行分析测定。
试样经热水提取、酸性沉淀蛋白质后,以C18色谱柱分离,用紫外检测器定量。
二、试剂及标准溶液配制2.1试剂淀粉酶:酶活力≥1.5U/mg。
盐酸(分析纯)。
氢氧化钠(分析纯)。
盐酸(2.4mol/L):准确移取10mL盐酸于50mL容量瓶中,用水定容。
氢氧化钠溶液(2.5mol/L):称取 5.0g氢氧化钠于50mL容量瓶中,用水定容。
高氯酸(HClO4):体积分数为60%。
甲醇(CH4O):色谱纯。
异丙醇(C3H8O):色谱纯。
庚烷磺酸钠(C7H15NaO3S):优级纯。
2.2标准溶液配制2.2.1烟酸及烟酰胺标准储备液(1.0mg/mL):称取烟酸及烟酰胺标准品各0.1 g(精确到0.0001g),分别置于100mL容量瓶中,用水溶解定容。
2.2.2烟酸及烟酰胺混合标准中间液(40µg/mL):分别准确吸取烟酸及烟酰胺标准储备液2mL至50mL定量瓶中,用水定容。
临用前配制。
2.2.3烟酸及烟酰胺混合标准系列测定液:分别准确吸取烟酸及烟酰胺混合标准中间液1.0mL、2.0mL、5.0mL、10.0mL,至50mL容量瓶中用水定容。
该标准系列浓度分别为0.80µg/mL、1.60µg/mL、4.00µg/mL、8.00µg/mL。
临用前配制。
三、仪器及工作条件3.1仪器高效液相色谱仪,带紫外检测器(北东西分析仪器有限公司)。
pH计:精度为0.01。
超声波振荡器。
天平:感量为0.1mg。
食品安全国家标准食品烟酸和烟酰胺的测定(编制说明)

食品安全国家标准食品烟酸和烟酰胺的测定(编制说明)《食品安全国家标准食品中烟酸和烟酰胺的测定》(征求意见稿)编制说明一、标准起草的基本情况根据卫计委《2010年食品安全国家标准清理完善工作安排》(卫办监督函[2010]607号)的要求,本标准受国家卫计委食品安全标准与监测评估司和食品安全国家标准审评委员会的委托,编制组承担了《食品中烟酸的测定》(GB/T5009.89-2003)国家标准的修订工作。
该标准从2014年6月开始制订,2015年3月完成编制和实验室内验证工作,2015年5月完成实验室间验证工作。
接到标准整合任务后,国家乳制品质量监督检验中心针对整合食品安全国家标准《食品中烟酸的测定》的具体工作要求组织了标准起草小组,专门组织技术人员成立研究工作组,通过各种途径查阅收集了大量相关技术资料,收集整理现行食品中烟酸的测定方法,以《食品安全国家标准食品营养强化剂使用标准》(GB 14880-2012)为基础,根据原有的研究成果,制定了开展研究的技术路线。
拟定了标准初稿和编制说明框架,工作组根据相关方面意见和实验室内验证结果,对标准初稿进行了修改和完善,在此基础上,形成标准征求意见稿。
本标准的编制遵循GB/T 1.1-2000《标准化工作导则第1部分:标准的结构和编写规则》和GB/T 20001.4-2001《标准编写规则第4部分:化学分析方法》的要求进行编制。
本标准是根据国卫办食品函〔2014〕386号《国家卫生计生委办公厅关于印发食品安全国家标准整合工作方案的通知》要求,以《食品中烟酸的测定》(GB/T 5009.89—2003)为基础,对现有国内外方法进行总结和整理,比较了各方法的原理、适用范围和技术参数;将《食品安全国家标准婴幼儿食品和乳品种烟酸和烟酰胺的测定》(GB 5413.15-2010)、《肉与肉制品维生素PP含量测定》(GB/T 9695.25-2008)等2项标准统一整合并修订为新的标准。
烟酸的制备实验报告(3篇)

第1篇一、实验目的1. 学习烟酸的制备原理和方法;2. 掌握实验操作技能,包括反应物的称量、混合、加热、冷却、过滤等;3. 分析实验结果,了解烟酸的物理性质和化学性质。
二、实验原理烟酸(Niacin),又称维生素B3,是一种水溶性维生素,对人体健康具有重要作用。
烟酸可以通过还原烟酰胺(Nicotinamide)或其衍生物得到。
本实验采用还原烟酰胺的方法制备烟酸,具体反应如下:烟酰胺 + 还原剂→ 烟酸 + 还原产物三、实验药品及试剂1. 烟酰胺(C6H5NO2):0.5g;2. 氢氧化钠(NaOH):2g;3. 硫酸亚铁(FeSO4·7H2O):0.5g;4. 水浴锅;5. 烧杯;6. 玻璃棒;7. 研钵;8. 滤纸;9. 酒精灯;10. 天平。
四、实验仪器1. 烧杯(100mL);2. 玻璃棒;3. 研钵;4. 滤纸;5. 酒精灯;6. 天平。
五、实验步骤1. 称取0.5g烟酰胺和2g氢氧化钠,置于研钵中,研磨均匀;2. 将研磨好的混合物转移至烧杯中,加入0.5g硫酸亚铁,搅拌均匀;3. 将烧杯置于水浴锅中,加热至50℃左右,保持20分钟;4. 取出烧杯,冷却至室温;5. 用滤纸过滤反应液,收集滤液;6. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;7. 将烧杯置于水浴锅中,加热至沸,保持10分钟;8. 取出烧杯,冷却至室温;9. 用滤纸过滤反应液,收集滤液;10. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;11. 将烧杯置于水浴锅中,加热至沸,保持10分钟;12. 取出烧杯,冷却至室温;13. 用滤纸过滤反应液,收集滤液;14. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;15. 将烧杯置于水浴锅中,加热至沸,保持10分钟;16. 取出烧杯,冷却至室温;17. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;18. 将烧杯置于水浴锅中,加热至沸,保持10分钟;19. 取出烧杯,冷却至室温;20. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;21. 将烧杯置于水浴锅中,加热至沸,保持10分钟;22. 取出烧杯,冷却至室温;23. 用滤纸过滤反应液,收集滤液;24. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;25. 将烧杯置于水浴锅中,加热至沸,保持10分钟;26. 取出烧杯,冷却至室温;27. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;28. 将烧杯置于水浴锅中,加热至沸,保持10分钟;29. 取出烧杯,冷却至室温;30. 用滤纸过滤反应液,收集滤液;31. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;32. 将烧杯置于水浴锅中,加热至沸,保持10分钟;33. 取出烧杯,冷却至室温;34. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;35. 将烧杯置于水浴锅中,加热至沸,保持10分钟;36. 取出烧杯,冷却至室温;37. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;38. 将烧杯置于水浴锅中,加热至沸,保持10分钟;39. 取出烧杯,冷却至室温;40. 用滤纸过滤反应液,收集滤液;41. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;42. 将烧杯置于水浴锅中,加热至沸,保持10分钟;43. 取出烧杯,冷却至室温;44. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;45. 将烧杯置于水浴锅中,加热至沸,保持10分钟;46. 取出烧杯,冷却至室温;47. 用滤纸过滤反应液,收集滤液;48. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;49. 将烧杯置于水浴锅中,加热至沸,保持10分钟;50. 取出烧杯,冷却至室温;51. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;52. 将烧杯置于水浴锅中,加热至沸,保持10分钟;53. 取出烧杯,冷却至室温;54. 用滤纸过滤反应液,收集滤液;55. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;56. 将烧杯置于水浴锅中,加热至沸,保持10分钟;57. 取出烧杯,冷却至室温;58. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;59. 将烧杯置于水浴锅中,加热至沸,保持10分钟;60. 取出烧杯,冷却至室温;61. 用滤纸过滤反应液,收集滤液;62. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;63. 将烧杯置于水浴锅中,加热至沸,保持10分钟;64. 取出烧杯,冷却至室温;65. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;66. 将烧杯置于水浴锅中,加热至沸,保持10分钟;67. 取出烧杯,冷却至室温;68. 用滤纸过滤反应液,收集滤液;69. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;70. 将烧杯置于水浴锅中,加热至沸,保持10分钟;71. 取出烧杯,冷却至室温;72. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;73. 将烧杯置于水浴锅中,加热至沸,保持10分钟;74. 取出烧杯,冷却至室温;75. 用滤纸过滤反应液,收集滤液;76. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;77. 将烧杯置于水浴锅中,加热至沸,保持10分钟;78. 取出烧杯,冷却至室温;79. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;80. 将烧杯置于水浴锅中,加热至沸,保持10分钟;81. 取出烧杯,冷却至室温;82. 用滤纸过滤反应液,收集滤液;83. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;84. 将烧杯置于水浴锅中,加热至沸,保持10分钟;85. 取出烧杯,冷却至室温;86. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;87. 将烧杯置于水浴锅中,加热至沸,保持10分钟;88. 取出烧杯,冷却至室温;89. 用滤纸过滤反应液,收集滤液;90. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;91. 将烧杯置于水浴锅中,加热至沸,保持10分钟;92. 取出烧杯,冷却至室温;93. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;94. 将烧杯置于水浴锅中,加热至沸,保持10分钟;95. 取出烧杯,冷却至室温;96. 用滤纸过滤反应液,收集滤液;97. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;98. 将烧杯置于水浴锅中,加热至沸,保持10分钟;99. 取出烧杯,冷却至室温;100. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;101. 将烧杯置于水浴锅中,加热至沸,保持10分钟;102. 取出烧杯,冷却至室温;103. 用滤纸过滤反应液,收集滤液;104. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;105. 将烧杯置于水浴锅中,加热至沸,保持10分钟;106. 取出烧杯,冷却至室温;107. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;108. 将烧杯置于水浴锅中,加热至沸,保持10分钟;109. 取出烧杯,冷却至室温;110. 用滤纸过滤反应液,收集滤液;111. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;112. 将烧杯置于水浴锅中,加热至沸,保持10分钟;113. 取出烧杯,冷却至室温;114. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;115. 将烧杯置于水浴锅中,加热至沸,保持10分钟;116. 取出烧杯,冷却至室温;117. 用滤纸过滤反应液,收集滤液;118. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;119. 将烧杯置于水浴锅中,加热至沸,保持10分钟;120. 取出烧杯,冷却至室温;121. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;122. 将烧杯置于水浴锅中,加热至沸,保持10分钟;123. 取出烧杯,冷却至室温;124. 用滤纸过滤反应液,收集滤液;125. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;126. 将烧杯置于水浴锅中,加热至沸,保持10分钟;127. 取出烧杯,冷却至室温;128. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;129. 将烧杯置于水浴锅中,加热至沸,保持10分钟;130. 取出烧杯,冷却至室温;131. 用滤纸过滤反应液,收集滤液;132. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;133. 将烧杯置于水浴锅中,加热至沸,保持10分钟;134. 取出烧杯,冷却至室温;135. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;136. 将烧杯置于水浴锅中,加热至沸,保持10分钟;137. 取出烧杯,冷却至室温;138. 用滤纸过滤反应液,收集滤液;139. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;140. 将烧杯置于水浴锅中,加热至沸,保持10分钟;141. 取出烧杯,冷却至室温;142. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;143. 将烧杯置于水浴锅中,加热至沸,保持10分钟;144. 取出烧杯,冷却至室温;145. 用滤纸过滤反应液,收集滤液;146. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;147. 将烧杯置于水浴锅中,加热至沸,保持10分钟;148. 取出烧杯,冷却至室温;149. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;150. 将烧杯置于水浴锅中,加热至沸,保持10分钟;151. 取出烧杯,冷却至室温;152. 用滤纸过滤反应液,收集滤液;153. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;154. 将烧杯置于水浴锅中,加热至沸,保持10分钟;155. 取出烧杯,冷却至室温;156. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;157. 将烧杯置于水浴锅中,加热至沸,保持10分钟;158. 取出烧杯,冷却至室温;159. 用滤纸过滤反应液,收集滤液;160. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;161. 将烧杯置于水浴锅中,加热至沸,保持10分钟;162. 取出烧杯,冷却至室温;163. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;164. 将烧杯置于水浴锅中,加热至沸,保持10分钟;165. 取出烧杯,冷却至室温;166. 用滤纸过滤反应液,收集滤液;167. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;168. 将烧杯置于水浴锅中,加热至沸,保持10分钟;169. 取出烧杯,冷却至室温;170. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;171. 将烧杯置于水浴锅中,加热至沸,保持10分钟;172. 取出烧杯,冷却至室温;173. 用滤纸过滤反应液,收集滤液;174. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;175. 将烧杯置于水浴锅中,加热至沸,保持10分钟;176. 取出烧杯,冷却至室温;177. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;178. 将烧杯置于水浴锅中,加热至沸,保持10分钟;179. 取出烧杯,冷却至室温;180. 用滤纸过滤反应液,收集滤液;181. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;182. 将烧杯置于水浴锅中,加热至沸,保持10分钟;183. 取出烧杯,冷却至室温;184. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;185. 将烧杯置于水浴锅中,加热至沸,保持10分钟;186. 取出烧杯,冷却至室温;187. 用滤纸过滤反应液,收集滤液;188. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;189. 将烧杯置于水浴锅中,加热至沸,保持10分钟;190. 取出烧杯,冷却至室温;191. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;192. 将烧杯置于水浴锅中,加热至沸,保持10分钟;193. 取出烧杯,冷却至室温;194. 用滤纸过滤反应液,收集滤液;195. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;196. 将烧杯置于水浴锅中,加热至沸,保持10分钟;197. 取出烧杯,冷却至室温;198. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;199. 将烧杯置于水浴锅中,加热至沸,保持10分钟;200. 取出烧杯,冷却至室温;201. 用滤纸过滤反应液,收集滤液;202. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;203. 将烧杯置于水浴锅中,加热至沸,保持10分钟;204. 取出烧杯,冷却至室温;205. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;206. 将烧杯置于水浴锅中,加热至沸,保持10分钟;207. 取出烧杯,冷却至室温;208. 用滤纸过滤反应液,收集滤液;209. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;210. 将烧杯置于水浴锅中,加热至沸,保持10分钟;211. 取出烧杯,冷却至室温;212. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;213. 将烧杯置于水浴锅中,加热至沸,保持10分钟;214. 取出烧杯,冷却至室温;215. 用滤纸过滤反应液,收集滤液;216. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;217. 将烧杯置于水浴锅中,加热至沸,保持10分钟;218. 取出烧杯,冷却至室温;219. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;220. 将烧杯置于水浴锅中,加热至沸,保持10分钟;221. 取出烧杯,冷却至室温;222. 用滤纸过滤反应液,收集滤液;223. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;224. 将烧杯置于水浴锅中,加热至沸,保持10分钟;225. 取出烧杯,冷却至室温;226. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;227. 将烧杯置于水浴锅中,加热至沸,保持10分钟;228. 取出烧杯,冷却至室温;229. 用滤纸过滤反应液,收集滤液;230. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;231. 将烧杯置于水浴锅中,加热至沸,保持10分钟;232. 取出烧杯,冷却至室温;233. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;234. 将烧杯置于水浴锅中,加热至沸,保持10分钟;235. 取出烧杯,冷却至室温;236. 用滤纸过滤反应液,收集滤液;237. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;238. 将烧杯置于水浴锅中,加热至沸,保持10分钟;239. 取出烧杯,冷却至室温;240. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;241. 将烧杯置于水浴锅中,加热至沸,保持10分钟;242. 取出烧杯,冷却至室温;243. 用滤纸过滤反应液,收集滤液;244. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;245. 将烧杯置于水浴锅中,加热至沸,保持10分钟;246. 取出烧杯,冷却至室温;247. 将滤液转移至烧杯中,加入适量的水,搅拌均匀;248. 将烧杯置于水浴锅中,加热至沸,保持10分钟;249. 取出烧杯,冷却至室温;250. 用滤纸过滤反应液第2篇一、实验目的1. 学习烟酸(维生素B3)的制备原理和方法;2. 掌握实验室合成烟酸的操作技能;3. 了解烟酸的理化性质和应用领域。
烟酰胺的含量测定方法

烟酰胺的含量测定方法烟酰胺的含量测定方法烟酰胺的含量测定方法摘要:本文通过外标法用来检测烟酰胺含量值,并且在此条件下能够检测烟酰胺的最后的含量值是比较可靠的,基于此烟酰胺和烟酸得可以更好的分离,使之具有准确可靠,专属性强,稳定简便等系列特点。
关键词:外标法烟酰胺含量值一、仪器与材料1.仪器Kromasil C18色谱柱,Agilent LC1100高效液相色谱仪,; Hypersil C18色谱柱(250mm×4.6mm,5μm); ,CP225D电子天平,SHIMADZU UV2450紫外-可见分光光度计。
2.材料烟酰胺对照品;烟酰胺;磷酸二氢钾,分甲醇,乙腈,色谱纯。
二、方法与结果1.色谱条件采用Agilent 110型高效液相色谱仪,Kro-masil C18色谱柱(4.6mm×250mm,5μm),流动相:磷酸二氢钾溶液(0.01mol.L-1)-水-甲醇-乙腈(1/79/15/5);流速0.8 mL.min-1;柱温:20.0℃检测波长:262nm;进样量:10μL。
柱温:室温。
2.测定方法量测定:精密称取本品约10mg,置100mL量瓶中,加水适量,振摇使溶解,用水稀释至刻度,摇匀,做为供试品溶液(100μg.L-1),精密量取10μL,照2.1项下的色谱条件,注入液相色谱仪,另取烟酰胺对照品适量,加水溶解并稀释制成含烟酰胺100μg.L-1的对照品溶液,同法测定。
按外标法以峰面积计算含量。
3.线性试验3.1精密称取烟酰胺对照品0.04055g置100mL量瓶中,加水溶解并稀释成含烟酰胺405.5μg.mL-1的浓对照品溶液,并稀释成2.028~405.5μg.mL-1的6个浓度的溶液(精密吸取浓对照品溶液1mL,分别置200mL、100mL、50mL、25mL量瓶中;精密吸取3mL、5mL,分别置25mL量瓶中,分别加水稀释至刻度),另取浓对照品溶液,形成7个浓度的溶液,照2.1项下的色谱条件进样10μL ,以峰面积Y对浓度X(μg.L-1)作线性回归,结果:在2.028~405.5μg.mL-1浓度范围内,测得的峰面积与与烟酰胺溶液的浓度呈良好的线性关系:Y=19.76X+3.565,r=0.9999。
食品安全国家标准 食品中烟酸和烟酰胺的测定

食品安全国家标准食品中烟酸和烟酰胺的测定1范围本标准规定了食品中烟酸和烟酰胺的测定方法。
本标准第一法为微生物法,适用于各类食品包括以天然食品为基质的强化食品中烟酸和烟酰胺总量的测定;第二法为高效液相色谱法,适用于含量较高或强化食品中烟酸和烟酰胺的测定。
第一法微生物法2原理烟酸是植物乳杆菌Lactobacillμs plantarμm(A TCC 8014)生长所必需的营养素,在一定控制条件下,将植物乳杆菌液接种至添加试样液的培养液中,培养一段时间后测定透光率,根据烟酸含量与透光率的标准曲线计算出试样中烟酸的含量。
3试剂和材料除非另有说明,本方法所用试剂均为分析纯,水为GB/T 6682规定的二级水。
培养基可购买符合测试要求的商品化培养基。
3.1试剂3.1.1盐酸(HCl)。
3.1.2氢氧化钠(NaOH)。
3.1.3氯化钠(NaCl)。
3.1.4浓硫酸(H2SO4)。
3.1.5溴麝香草酚蓝(C27H28Br2O5S):pH指示剂。
3.1.6乙醇(C2H5OH)。
3.2试剂配制3.2.1盐酸溶液(1 mol/L):用量筒量取吸取83 mL盐酸,于1000 mL烧杯中,加917mL 水,混匀。
3.2.2盐酸溶液(0.1 mol/L):吸取3.2.1盐酸溶液10mL,加水溶解至100mL。
3.2.3氢氧化钠溶液(1 mol/L):称取40 g氢氧化钠于1000 mL烧杯中,加水溶解并稀释至1000 mL,混匀。
3.2.4氢氧化钠溶液(0.1 mol/L):吸取3.2.3氢氧化钠溶液10mL,加水溶解至100mL。
3.2.5生理盐水(0.9%):称取9g氯化钠(NaCl),溶解于1000ml水中,分装10mL于试管中,121℃灭菌15min,备用。
3.2.6乙醇溶液(25%):量取200 mL无水乙醇与800 mL水混匀。
3.2.7硫酸溶液(1 mol/L):于2000mL烧杯中先注入700mL水,用量筒量取56mL硫酸沿烧杯壁缓慢倒入水中,用水稀释到1000mL。
异烟肼片的含量测定

3H2O ⒍ 析出过量的I2可用标准Na2S2O3溶液滴定:I2+2Na2S2O3 =
Na2S4O6+2NaI
葡萄糖注射液的分析 三.实验方法
1. 鉴别取本品,缓缓滴入温热的碱性酒石酸铜试液
仪器
分析天平、容量 瓶、酸式滴定管 、滴定台、硅胶 G薄层板、点样 毛细管、层析缸 等
4.实验步骤
1.异烟肼中游离肼杂质检查
取本品,加水制成50 mg/ml的异烟肼水溶液,作 为供试品溶液。 另取硫酸肼加水制成每1 ml中约含有0.20 mg(相 当于游离肼50 µg)的溶液,作为对照品溶液。
照薄层色谱法,吸取供试品溶液10 µl和对照品溶 液2 µl,分别点于同一硅胶G薄层板上,以异丙醇 -丙酮(3 : 2)为展开剂,展开,晾干,喷以乙醇 制的对-二甲氨基苯甲醛试液,放置15分钟后检视。 在供试品溶液主斑点前方与对照品溶液主斑点相 应位置,不得显黄色斑点。
葡萄糖注射液的分析
⒈ I2与NaOH作用:I2+2NaOH = NaIO+NaI+H2O ⒉ C6H12O6和NaIO定量作用:C6H12O6+NaIO = C6H12O7+NaI ⒊ 总反应式:I2+C6H12O6+2NaOH = C6H12O7+2NaI+H2O ⒋ C6H12O6作用完后,剩下未作用的NaIO在碱性条件下发生
三、主要器材(写所用药品信息与最主要的仪器) 1 阿司匹林肠溶片的信息:生产厂家、规格、生产批号 、生产日期、有效期 2 试剂: 名称 规格 2主要仪器:如分析天平、纳氏比色管、容量瓶、酸式滴 定管、碱式滴定管、滴定台、水浴锅等。
11
含量计算思考题解答

× D ×平均片重
标示量% =
W ×标示量
×100%
0.312 1 × 1000×0.0120 × 323 100 ×100% 标示量% = 0.0110 ×0.01 = 105.37
3
2 分光光度法—(2)百分吸光系数法
例4 盐酸布桂秦片含量测定(中国药典2000年版) 取20片称重3.00g (标示量10mg/片),研细,精密称 取0.0459g,置100mL量瓶, 加0.1mol/L盐酸溶解并稀释到 刻度,精密量取滤液2.0mL,置100mL量瓶, 0.1mol/L盐酸 稀释到刻度, 照分光光度法,在252nm测吸光度为0.412 1% =671. 计算标示量 %. E1cm 平均片重=0.3002/20=0.0150 A 1 1% × E1cm L 100
× D ×平均片重
标示量% =
W ×标示量
×100%
0.412 1 × 5000×0.0150 × 671 100 ×100% 标示量% = 0.0459 ×0.010 = 100.3
4
例5:某注射液含量测定方法
1% 已知:被测物的 E1cm =481 注射液标示量:0.5g/20ml
D=200×250/5=10000
V × T × F ×平均片重 ×100 标示量%= W ×标示量
25.02 ×12.31/1000 ×0.1005/0.1×0.3584 = ×100% 0.3729 ×0.3 1 = 99.17
例2 异烟肼片含量测定(中国药典2000年版)
(1)取样 20片 总重2.4220,研细 称取0.2560g (2)溶液制备 100 mL水定容, 滤过取续滤液25mL ,加 水50mL,盐酸20mL与甲基橙1滴 (3)测定 溴酸钾滴定液(0.01635mol/L)滴定至粉红色 消失,消耗溴酸钾滴定液16.10mL。 每1mL溴酸钾滴定液(0.01667mol/L)相当于3.429mg异烟 肼. (0.1g/片)
紫外分光光度法测定烟酸片含量

紫外分光光度法测定烟酸片含量文丽丽;张立升;吕文军【摘要】目的采用紫外分光光度法测定烟酸片的含量.方法以水为溶剂,在262 nm波长处测定吸光度,绘制标准曲线.结果该法测定平均回收率为99.5%,RSD=0.56% (n =9),线性范围为14.51~33.85 μmg,r =0.997.结论本法测定烟酸含量方法简便,快速,结果与药典法基本一致.【期刊名称】《哈尔滨医药》【年(卷),期】2012(032)001【总页数】2页(P14-15)【关键词】紫外分光光度法;烟酸;含量测定【作者】文丽丽;张立升;吕文军【作者单位】黑龙江省黑河市药品检验所,黑龙江黑河164300;黑龙江省黑河市第一人民医院,黑龙江黑河164300;黑龙江省黑河市药品检验所,黑龙江黑河164300【正文语种】中文【中图分类】R977.2烟酸是临床上应用广泛的维生素类药物,用于防治糙皮病等烟酸缺乏病。
也用作血管扩张药,治疗高脂血症。
烟酸片质量标准收载于《中国药典》2010年版二部,标准中含量采用的是氢氧化钠(0.1mol/L)滴定的方法[1],滴定的测定方法人为因素比较多,不同人操作结果差异比较大,而原标准中鉴别项下为紫外分光光度法,故尝试以此方法来检测含量,为更好的保证该药有效性提供有力依据。
1 仪器与试药UV-2100紫外分光光度计(日本岛津);AE240电子天平(瑞士METTLER),烟酸对照品(批号100434-200301,中国药品生物制品检定所),所有试验用水均为纯化水。
2 实验方法与结果2.1 溶液的制备2.1.1 对照品溶液的制备:精密称取烟酸对照品12.09mg置100mL量瓶中,加水70mL,振摇15min,使烟酸溶解后,加水稀释至刻度,摇匀,作为对照品溶液。
2.1.2 供试品溶液的制备:取烟酸片20片(标示量为100 mg),精密称定,研细,精密称取0.106 7 g(约相当于烟酸100 mg),置100mL量瓶中,加水70mL,振摇15min,使烟酸溶解后,加水稀释到刻度,摇匀,用干燥滤纸滤过,作为供试品溶液。
烟酸含量及提取方法研究
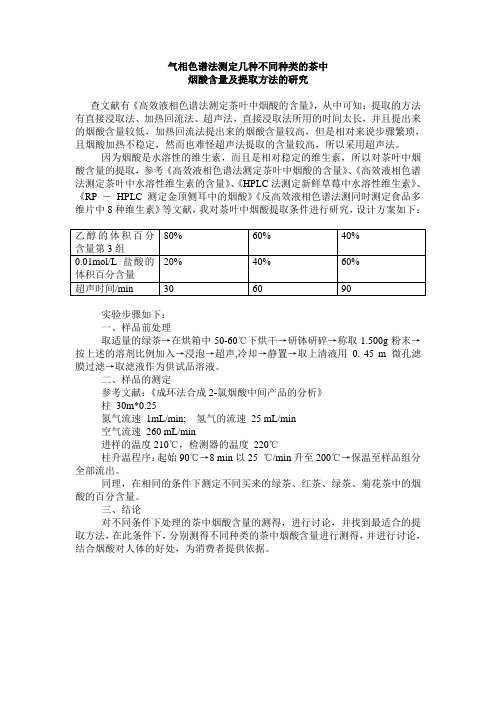
气相色谱法测定几种不同种类的茶中
烟酸含量及提取方法的研究
查文献有《高效液相色谱法测定茶叶中烟酸的含量》,从中可知:提取的方法有直接浸取法、加热回流法、超声法,直接浸取法所用的时间太长,并且提出来的烟酸含量较低,加热回流法提出来的烟酸含量较高,但是相对来说步骤繁琐,且烟酸加热不稳定,然而也难怪超声法提取的含量较高,所以采用超声法。
因为烟酸是水溶性的维生素,而且是相对稳定的维生素,所以对茶叶中烟酸含量的提取,参考《高效液相色谱法测定茶叶中烟酸的含量》、《高效液相色谱法测定茶叶中水溶性维生素的含量》、《HPLC法测定新鲜草莓中水溶性维生素》、《RP -HPLC 测定金顶侧耳中的烟酸》《反高效液相色谱法测同时测定食品多维片中8种维生素》等文献,我对茶叶中烟酸提取条件进行研究,设计方案如下:
实验步骤如下:
一、样品前处理
取适量的绿茶→在烘箱中50-60℃下烘干→研钵研碎→称取1.500g粉末→按上述的溶剂比例加入→浸泡→超声,冷却→静置→取上清液用0. 45 m 微孔滤膜过滤→取滤液作为供试品溶液。
二、样品的测定
参考文献:《成环法合成2-氯烟酸中间产品的分析》
柱30m*0.25
氮气流速1mL/min; 氢气的流速25 mL/min
空气流速260 mL/min
进样的温度210℃,检测器的温度220℃
柱升温程序:起始90℃→8 min以25 ℃/min升至200℃→保温至样品组分全部流出。
同理,在相同的条件下测定不同买来的绿茶、红茶、绿茶、菊花茶中的烟酸的百分含量。
三、结论
对不同条件下处理的茶中烟酸含量的测得,进行讨论,并找到最适合的提取方法,在此条件下,分别测得不同种类的茶中烟酸含量进行测得,并进行讨论,结合烟酸对人体的好处,为消费者提供依据。
复方烟酸片烟酸释放度检测方法的建立

复方烟酸片烟酸释放度检测方法的建立发布时间:2021-07-15T14:44:43.307Z 来源:《医师在线》2021年15期作者:陈海刚傅超婷[导读] 复方烟酸缓释片是以缓释烟酸与辛伐他汀为主药制成的复方口服固体制剂,陈海刚傅超婷海南通用三洋药业有限公司 570312复方烟酸缓释片是以缓释烟酸与辛伐他汀为主药制成的复方口服固体制剂,已在国外上市但未在国内上市,原研药缓释烟酸辛伐他汀片由美国Abbott公司研制,2008年2月获FDA批准上市,商品名为SIMCOR,用于治疗单用辛伐他汀或单用缓释烟酸治疗效果欠佳的高甘油三酯血症(Fredrickson分型Ⅳ)患者,降低其TG。
本文参照缓释烟酸/洛伐他汀片(商品名:ADVICOR?)FDA申报资料[1]中烟酸释放度测定法及中国药典2005年版二部烟酸片[2]溶出度测定法,对复方烟酸片烟酸释放度进行了系统研究,确定了烟酸释放度检测方法,为今后有效地控制本品烟酸体外释放溶出行为的研究提供了科学依据。
一、样品及仪器样品:复方烟酸缓释片,海南通用三洋药业有限公司自制。
样品规格、批号详见下表:规格(1) 0.5g/20mg:每片含烟酸0.5g与辛伐他汀20mg;批号:070924、070926、070928、规格(2) 1.0g/20mg:每片含烟酸1.0g与辛伐他汀20mg。
批号:071210、071212、071214对照品:烟酸(批号:100434-200301)、辛伐他汀(批号:100601-200502)均由中国药品生物制品检定所提供。
仪器:ZRS-8G智能溶出试验仪(天津大学无线电厂);紫外-可见分光光度。
二、烟酸释放度方法的建立2.1 仪器装置、释放介质及转速的选择参照缓释烟酸/洛伐他汀片(商品名ADVICOR?)FDA申报资料[5]中烟酸释放度测定法及中国药典2005年版二部烟酸片[4]溶出度测定法,选取溶出度测定法(中国药典2005年版二部附录Ⅹ C第一法)装置(转篮法)测定烟酸释放度,以水900ml为释放介质,转速为每分钟100转。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验十三 烟酸片的含量测定
一、 实验目的
1. 掌握烟酸片的测定原理及方法。
2. 掌握片剂分析的基本操作技术。
二、实验原理
烟酸具有酸性,可用碱滴定液滴定测定含量。
供试品加水使溶解后,加酚酞指示液,用氢氧化钠滴定液(0.1mol/L )滴定,记录氢氧化钠滴定液的使用量,计算,即得。
标示量(%)%100_
⨯⨯⨯⨯⨯=
S
W W
F T V
本品含烟酸应为标示量的95.0%~105.0%。
三.实验仪器和试剂: 1.仪器:
分析天平、碱式滴定管、研钵、烧杯、水浴锅、锥形瓶 2.试剂
水(新沸放置至室温)、 氢氧化钠滴定液(0.1mol/L )、酚酞指示液 试药:烟酸片 四、实验内容
取本品10片,精密称定,研细,精密称取适量(约相当于烟酸0.2g ),加新沸过的冷水50mL ,溶解后,置水浴上加热并时时振摇使烟酸溶解,放冷至室温,加酚酞指示液3 滴,用氢氧化钠滴定液(0.1mol/L )滴定,记录消耗氢氧化钠滴定液的体积数(mL ),每 1mL 氢氧化钠滴定液(0.1mol/L )相当于12.31mg 的烟酸(C 6H 5NO 2 ),即得。
按中国药典规定,判断是否合格。
六、注意事项
1. “精密称取”系指称取重量应准确至所称取重量的千分之一, “精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。
2. 水浴上加热时,要时时振摇。
七、思考题
1.烟酸片为什么可以采用氢氧化钠直接滴定?。
