盐酸莫西沙星滴眼液中文版
盐酸莫西沙星滴眼液说明书(英文)

VIGAMOX®(moxifloxacin hydrochloride ophthalmic solution)0.5% as baseDESCRIPTION: VIGAMOX® (moxifloxacin HCl ophthalmic solution) 0.5% is a sterile ophthalmic solution. It is an 8-methoxy fluoroquinolone anti-infective for topical ophthalmic use.Chemical Name:1-Cyclopropyl-6-fluoro-1,4-dihydro-8-methoxy-7-[(4aS,7aS)-octahydro-6H-pyrrolol[3,4-b]pyridin-6-yl]-4-oxo-3-quinolinecarboxylic acid, monohydrochloride.Moxifloxacin hydrochloride is a slightly yellow to yellow crystalline powder. Each mL of VIGAMOX® solution contains 5.45 mg moxifloxacin hydrochloride equivalent to 5 mg moxifloxacin base.Contains: Active: Moxifloxacin 0.5% (5 mg/mL); Inactives: Boric acid, sodium chloride, and purified water. May also contain hydrochloric acid/sodium hydroxide to adjust pH to approximately 6.8.VIGAMOX® solution is an isotonic solution with an osmolality of approximately 290 mOsm/kg.CLINICAL PHARMACOLOGY:Pharmacokinetics: Plasma concentrations of moxifloxacin were measured in healthy adult male and female subjects who received bilateral topical ocular doses of VIGAMOX® solution 3 times a day. The mean steady-state C max (2.7 ng/mL) and estimated daily exposure AUC (45 ng·hr/mL) values were 1,600 and 1,000 times lower than the mean C max and AUC reported after therapeutic 400 mg oral doses of moxifloxacin. The plasma half-life of moxifloxacin was estimated to be 13 hours.Microbiology:Moxifloxacin is an 8-methoxy fluoroquinolone with a diazabicyclononyl ring at the C7 position. The antibacterial action of moxifloxacin results from inhibition of the topoisomerase II (DNA gyrase) and topoisomerase IV. DNA gyrase is an essential enzyme that is involved in the replication, transcription and repair of bacterial DNA. Topoisomerase IV is an enzyme known to play a key role in the partitioning of the chromosomal DNA during bacterial cell division.The mechanism of action for quinolones, including moxifloxacin, is different from that of macrolides, aminoglycosides, or tetracyclines. Therefore, moxifloxacin may be active against pathogens that are resistant to these antibiotics and these antibiotics may be active against pathogens that are resistant to moxifloxacin. There is no cross-resistance between moxifloxacin and the aforementioned classes of antibiotics. Cross resistance has been observed between systemic moxifloxacin and some other quinolones.In vitro resistance to moxifloxacin develops via multiple-step mutations. Resistance to moxifloxacin occurs in vitro at a general frequency of between 1.8 x 10-9 to < 1 x 10-11 for Gram-positive bacteria.Moxifloxacin has been shown to be active against most strains of the following microorganisms, both in vitro and in clinical infections as described in the INDICATIONS AND USAGE section:Aerobic Gram-positive microorganisms:Corynebacterium species*Micrococcus luteus* Staphylococcus aureus Staphylococcus epidermidis Staphylococcus haemolyticus Staphylococcus hominis Staphylococcus warneri* Streptococcus pneumoniae Streptococcus viridans group*Efficacy for this organism was studied in fewer than 10 infections.The following in vitro data are also available, but their clinical significance in ophthalmic infections is unknown. The safety and effectiveness of VIGAMOX® solution in treating ophthalmological infections due to these microorganisms have not been established in adequate and well-controlled trials.The following organisms are considered susceptible when evaluated using systemic breakpoints. However, a correlation between the in vitro systemic breakpoint and ophthalmological efficacy has not been established. The list of organisms is provided as guidance only in assessing the potential treatment of conjunctival infections. Moxifloxacin exhibits in vitro minimal inhibitory concentrations (MICs) of 2 µg/ml or less (systemic susceptible breakpoint) against most (≥ 90%) of strains of the following ocular pathogens.Aerobic Gram-positive microorganisms:Listeria monocytogenesStaphylococcus saprophyticus Streptococcus agalactiae Streptococcus mitis Streptococcus pyogenesStreptococcus Group C, G and FAerobic Gram-negative microorganisms:Acinetobacter baumannii Acinetobacter calcoaceticus Citrobacter freundii Citrobacter koseriEnterobacter aerogenes Enterobacter cloacae Escherichia coli Klebsiella oxytoca Klebsiella pneumoniae Moraxella catarrhalis Morganella morganii Neisseria gonorrhoeae Proteus mirabilis Proteus vulgarisPseudomonas stutzeriClinical Studies:In two randomized, double-masked, multicenter, controlled clinical trials in which patients were dosed 3 times a day for 4 days, VIGAMOX® solution produced clinical cures on day 5-6 in 66% to 69% of patients treated for bacterial conjunctivitis. Microbiological success rates for the eradication of the baseline pathogens ranged from 84% to 94%. Please note that microbiologic eradication does not always correlate with clinical outcome in anti-infective trials.INDICATIONS AND USAGE: VIGAMOX® solution is indicated for the treatment of bacterial conjunctivitis caused by susceptible strains of the following organisms:Aerobic Gram-negative microorganisms:Acinetobacter lwoffii*Haemophilus influenzae Haemophilus parainfluenzae*Other microorganisms:Chlamydia trachomatisAnaerobic microorganisms:Clostridium perfringens Fusobacterium species Prevotella speciesPropionibacterium acnes Other microorganisms:Chlamydia pneumoniae Legionella pneumophila Mycobacterium avium Mycobacterium marinum Mycoplasma pneumoniaeC 21H 24FN 3O 4•HCl Mol Wt 437.9O O FHCH 3N O HHO NN HH+C l -Aerobic Gram-positive microorganisms:Corynebacterium species*Micrococcus luteus* Staphylococcus aureus Staphylococcus epidermidis Staphylococcus haemolyticus Staphylococcus hominis Staphylococcus warneri* Streptococcus pneumoniae Streptococcus viridans group*Efficacy for this organism was studied in fewer than 10 infections.CONTRAINDICATIONS: VIGAMOX® solution is contraindicated in patients with a history of hypersensitivity to moxifloxacin, to other quinolones, or to any of the components in this medication.WARNINGS:NOT FOR INJECTION.VIGAMOX® solution should not be injected subconjunctivally, nor should it be introduced directly into the anterior chamber of the eye.In patients receiving systemically administered quinolones, including moxifloxacin, serious and occasionally fatalhypersensitivity (anaphylactic) reactions have been reported, some following the first dose. Some reactions were accompanied by cardiovascular collapse, loss of consciousness, angioedema (including laryngeal, pharyngeal or facial edema), airwayobstruction, dyspnea, urticaria, and itching. If an allergic reaction to moxifloxacin occurs, discontinue use of the drug. Serious acute hypersensitivity reactions may require immediate emergency treatment. Oxygen and airway management should be administered as clinically indicated.PRECAUTIONS:General: As with other anti-infectives, prolonged use may result in overgrowth of non-susceptible organisms, including fungi. If superinfection occurs, discontinue use and institute alternative therapy. Whenever clinical judgment dictates, the patient should be examined with the aid of magnification, such as slit-lamp biomicroscopy, and, where appropriate, fluorescein staining.Patients should be advised not to wear contact lenses if they have signs and symptoms of bacterial rmation for Patients: Avoid contaminating the applicator tip with material from the eye, fingers or other source.Systemically administered quinolones including moxifloxacin have been associated with hypersensitivity reactions, evenfollowing a single dose. Discontinue use immediately and contact your physician at the first sign of a rash or allergic reaction.Drug Interactions: Drug-drug interaction studies have not been conducted with VIGAMOX® solution. In vitro studies indicate that moxifloxacin does not inhibit CYP3A4, CYP2D6, CYP2C9, CYP2C19, or CYP1A2 indicating that moxifloxacin is unlikely to alter the pharmacokinetics of drugs metabolized by these cytochrome P450 isozymes.Carcinogenesis, Mutagenesis, Impairment of Fertility: Long term studies in animals to determine the carcinogenic potential of moxifloxacin have not been performed. However, in an accelerated study with initiators and promoters, moxifloxacin was not carcinogenic in rats following up to 38 weeks of oral dosing at 500 mg/kg/day (approximately 21,700 times the highest recommended total daily human ophthalmic dose for a 50 kg person, on a mg/kg basis).Moxifloxacin was not mutagenic in four bacterial strains used in the Ames Salmonella reversion assay. As with other quinolones, the positive response observed with moxifloxacin in strain TA 102 using the same assay may be due to the inhibition of DNA gyrase. Moxifloxacin was not mutagenic in the CHO/HGPRT mammalian cell gene mutation assay. An equivocal result was obtained in the same assay when v79 cells were used. Moxifloxacin was clastogenic in the v79chromosome aberration assay, but it did not induce unscheduled DNA synthesis in cultured rat hepatocytes. There was no evidence of genotoxicity in vivo in a micronucleus test or a dominant lethal test in mice.Moxifloxacin had no effect on fertility in male and female rats at oral doses as high as 500 mg/kg/day, approximately 21,700 times the highest recommended total daily human ophthalmic dose. At 500 mg/kg orally there were slight effects on sperm morphology (head-tail separation) in male rats and on the estrous cycle in female rats.Pregnancy: Teratogenic Effects.Pregnancy Category C: Moxifloxacin was not teratogenic when administered to pregnant rats during organogenesis at oral doses as high as 500 mg/kg/day (approximately 21,700 times the highest recommended total daily human ophthalmic dose); however, decreased fetal body weights and slightly delayed fetal skeletal development were observed. There was no evidence of teratogenicity when pregnant Cynomolgus monkeys were given oral doses as high as 100 mg/kg/day (approximately 4,300 times the highest recommended total daily human ophthalmic dose). An increased incidence of smaller fetuses was observed at 100 mg/kg/day.Since there are no adequate and well-controlled studies in pregnant women, VIGAMOX® solution should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus.Nursing Mothers: Moxifloxacin has not been measured in human milk, although it can be presumed to be excreted in human milk. Caution should be exercised when VIGAMOX® solution is administered to a nursing mother.Pediatric Use: The safety and effectiveness of VIGAMOX® solution in infants below 1 year of age have not been established.There is no evidence that the ophthalmic administration of VIGAMOX® solution has any effect on weight bearing joints, even though oral administration of some quinolones has been shown to cause arthropathy in immature animals.Geriatric Use: No overall differences in safety and effectiveness have been observed between elderly and younger patients.ADVERSE REACTIONS:The most frequently reported ocular adverse events were conjunctivitis, decreased visual acuity, dry eye, keratitis, oculardiscomfort, ocular hyperemia, ocular pain, ocular pruritus, subconjunctival hemorrhage, and tearing. These events occurred in approximately 1-6% of patients.Nonocular adverse events reported at a rate of 1-4% were fever, increased cough, infection, otitis media, pharyngitis, rash, and rhinitis.DOSAGE AND ADMINISTRATION:Instill one drop in the affected eye 3 times a day for 7 days.HOW SUPPLIED: VIGAMOX® solution is supplied as a sterile ophthalmic solution in Alcon’s DROP-TAINER® dispensing system consisting of a natural low density polyethylene bottle and dispensing plug and tan polypropylene closure. Tamper evidence is provided with a shrink band around the closure and neck area of the package.3 mL in 4 mL bottle - NDC 0065-4013-03Storage: Store at 2°C - 25°C (36°F - 77°F).Rx OnlyManufactured byAlcon Laboratories, Inc.Fort Worth, Texas 76134 USALicensed to Alcon, Inc. by Bayer HealthCare AG. U.S. PAT. NO. 4,990,517; 5,607,942; 6,716,830©2003-2006, 2008 Alcon, Inc.Aerobic Gram-negative microorganisms:Acinetobacter lwoffii*Haemophilus influenzae Haemophilus parainfluenzae *Other microorganisms:Chlamydia trachomatis340745-0408。
盐酸莫西沙星滴眼液技术转让及项目分析-20200804

广州市桐晖药业有限公司
广州市桐晖药业有限公司盐酸莫西沙星滴眼液
桐晖药业提供技术转让
项目基本信息
中文名称:盐酸莫西沙星滴眼液
英文名称:Moxifloxacin Hydrochloride Eye Drops
规格:5ml:25mg、3ml:15mg
适应症:用于治疗敏感微生物引起的细菌性结膜炎
注册分类:化药4类
项目简介
感染性眼病是眼科常见疾病,常导致眼部组织不同程度损伤,从而对视力产生不同程度的影响,甚至致盲。
感染性眼病的治疗主要是经验性使用广谱抗生素,而全身性广谱抗生素的广泛使用会导致眼部G+菌和G-菌对旧抗生素产生耐药,极大增加了治疗难度。
临床需要新的广谱低耐药抗菌药物应对当前感染性眼病难治局势。
喹诺酮类药物抗菌谱广,抗菌作用强,在感染性眼病的治疗中发挥着举足轻重的作用。
作为最新一代喹诺酮类的代表药物-莫西沙星,在保留原有抗G-菌活性的基础上,显著增强了对G+菌、厌氧菌、非典型病原体的抗菌活性,并减少了耐药。
研究显示盐酸莫西沙星滴眼液在细菌性结膜炎中的细菌清除率可高达95%,48h临床治愈率可达到81%。
盐酸莫西沙星滴眼液是眼部抗感染治疗的优选用药。
盐酸莫西沙星滴眼液自2003年美国上市至今,获得美国眼科学会临床指南、美国验光学会循证临床实践指南、英国视光师学院临床管理指南等多个权威指南的一致推荐。
0.5%盐酸莫西沙星滴眼液于2018年12月17日获中国国家药品监督管理局批准,成为中国感染性眼病治疗新选择。
研发进度:待申报
合作方式:委托开发、联合开发。
拜复乐(莫西沙星)

【药品名称】通用名称:拜复乐商品名称:拜复乐【英文名称】汉语拼音:baifule【成份】盐酸莫西沙星氯化钠【性状】本品为黄色的澄明液体【作用类别】【适应症】成人(大于18岁)上呼吸道和下呼吸道感染,如,急性窦炎,慢性支气管炎急性发作,社区获得性肺炎,及皮肤及软组织感染。
【规格】250ml:0.4g × 1【用法用量】推荐剂量一次400mg,一日一次,慢性支气管炎急性发作:5天。
社区获得性肺炎:序贯给药推荐总疗程为7—14天。
急性窦炎:7天。
治疗皮肤及软组织感染的推荐为7天。
【不良反应】绝大多数不良反应为轻中度胃肠道反应,中枢神精系统不良反应,皮肤过敏等【禁忌】已知对该注射液的任何成份或其他喹诺酮类过敏者。
禁用于儿童,青少年,孕妇及哺乳期妇女。
【药物毒理】莫西沙星是具有广谱活性和杀菌作用的8—甲氧基氟喹诺酮类药物。
莫西沙星在体外显示对革兰阳性菌,革兰阴性菌,厌氧菌,抗酸菌和非典型微生物和支原体,衣原体和军团菌具有广谱抗菌活性。
杀菌作用机制为干扰拓扑异构酶Ⅱ和Ⅳ。
拓朴异构酶是控制DNA拓朴和在DNA复制,修复和转录中关键的酶。
【贮藏】干燥条件下贮藏。
【包装】瓶批准文号:国药准字J20040068生产企业:德国拜耳(拜耳医药保健分装)处方类型:本品为处方药!基本药理本品是广谱和具有抗菌活性的8-甲氧基氟喹诺酮类抗菌药。
抗菌机制为干扰II、IV拓扑异构酶。
本品是具有浓度依赖性的杀菌活性。
临床用途本品适应症为治疗患有上呼吸道和下呼吸道感染的成人,如急性窦炎,慢性支气管炎急性发作,社区获得性肺炎,以及皮肤和软组织感染给药途径及用量任何适应症推荐一次400mg,一日一次,服用时间不受饮食影响治疗时间:慢性支气管炎急性发作:5天;社区获得性肺炎:10天;急性窦炎:7天;治疗皮肤和软组织感染推荐治疗时间为7天药物相互作用抗酸药、矿物质和多种维生素同服,本品会形成多价螯合而减少药物吸收,因此抗酸药、含镁、铝和其它矿物质如铁等制剂需服用本品4小时前或2小时后慎与下列药物合用:1a类(如奎宁丁普鲁卡因)或III类(如胺碘酮索托落尔)抗心律失常药西沙必利红霉素抗精神病药物和三环类抗抑郁药食物和乳制品:食物的摄入不影响莫西沙星的吸收因此莫西沙星的服用时间不受进食的影响抗酸药矿物质和多种维生素:莫西沙星与抗酸药矿物质和多种维生素同时服用会因为与这些物质形成多价螯合物而减少药物的吸收这将导致血浆中的药物浓度比预定值低因此抗酸药抗逆转录病毒和其他含有镁铝和其他矿物质如铁等的制剂需要在口服莫西沙星4小时前或2小时后服用雷尼替丁:与雷尼替丁同时服用不会影响莫西沙星的吸收特性其吸收参数(CmaxTmaxAUC)均提示莫西沙星不受胃酸缺乏的影响钙补充剂:当给予高剂量补充剂时仅观察到吸收率稍有减少而吸收范围保持不变高剂量钙补充剂对莫西沙星的吸收不具有临床意义茶碱:莫西沙星对稳态时茶碱的药代动力学无影响提示莫西沙星对P450酶的1A2亚型无影响当服用莫西沙星治疗时达到稳态的茶碱浓度未升高因此服用莫西沙星时不必调整茶碱的用量华法令:据观察莫西沙星与华法令同时服用未发现对凝血酶原时间和凝血的其他参数有影响口服避孕药:莫西沙星与口服避孕药同时服用未发现有相互作用抗糖尿病药:优降糖和莫西沙星同时服用未发现有相互作用伊曲康唑:莫西沙星与伊曲康唑同时服用时伊曲康唑的药时曲线下面积(AUC)仅少量改变伊曲康唑对莫西沙星的药代动力学无显著性影响当服用伊曲康唑时给予莫西沙星不需要调整剂量反之亦然地高辛:莫西沙星对地高辛的药代动力学没有严重影响反之亦然吗啡:肠外给予吗啡同时服用莫西沙星并不减少口服莫西沙星的生物利用度且Cmax(17%)仅稍有下降普鲁苯辛:在一项观察普鲁苯辛对肾脏排泄功能影响的研究中未发现对莫西沙星的全身清除和肾脏清除有明显影响因此当这两种药同时服用时不必调整剂量炭:同时口服炭及400 mg莫西沙星能减少药物的全身利用在体内能阻止80%药物吸收药物过量时利用活性炭能在吸收早期阻止药物的进一步进入全身系统注意事项1.喹诺酮药物使用可诱发癫痫的发作,因此此类病人服用本品要注意2.本品应避免用QT间期延长的患者。
硫酸莫西沙星滴眼液的服用方法与剂量

硫酸莫西沙星滴眼液的服用方法与剂量硫酸莫西沙星滴眼液是一种常用的眼科药物,用于治疗眼部感染和眼表炎等眼部疾病。
正确的服用方法和剂量对于药物的疗效和安全性至关重要。
本文将详细介绍硫酸莫西沙星滴眼液的服用方法与剂量。
1. 确定滴眼液的使用剂量硫酸莫西沙星滴眼液的剂量通常由医生根据患者的病情和需要进行调整,因此在使用之前最好先咨询医生或眼科专家。
通常,成人的常见剂量为每次1-2滴,每天3-4次;儿童的剂量则根据年龄和体重来确定。
2. 准备滴眼液在使用滴眼液之前,首先要确保双手清洁。
可以用肥皂和清水洗手,然后擦干。
3. 打开滴眼液瓶盖将药瓶保持倒立方向,用一只手握住瓶身,用另一只手打开瓶盖。
注意,不要让瓶口接触到任何表面,以免污染滴眼液。
4. 倾斜头部将头向后倾斜或者向一侧倾斜以便于滴眼液。
5. 滴眼液用您的一只手拉下下眼睑,用另外一只手将滴眼液瓶的末端放在眼睛内侧的结膜囊上。
然后,轻轻地挤压滴眼液瓶以滴入正确的剂量。
当完成滴眼后,请轻轻地闭上眼睛,避免将眼液流出。
6. 处理滴眼液残液用纸巾或干净的棉签擦拭滴眼液残留在眼睛周围的区域,防止其渗入眼睛或污染周围的皮肤。
7. 盖好药瓶盖在使用滴眼液之后,记得将药瓶盖盖好,以免滴眼液受到污染。
8. 注意事项在使用硫酸莫西沙星滴眼液时,还需要注意以下事项:- 不要与其他眼药水混合使用,以免降低药物的疗效。
- 尽量避免接触到眼球或其他物体,以防止交叉感染。
- 使用滴眼液时,若感觉视力模糊或产生刺激感,请立即停止使用并咨询医生。
- 根据医生的建议进行药物的使用时间和疗程。
总结:硫酸莫西沙星滴眼液是一种用于治疗眼部感染和眼表炎等眼部疾病的药物。
在使用时,需要根据医生的建议确定正确的剂量。
通过正确的滴眼方法,可以确保药物的有效吸收和使用的安全性。
然而,在使用过程中,也要注意遵循医生的指导,避免交叉感染和不适反应的发生。
若有不适或疑问,请咨询医生或眼科专家。
盐酸吗啉胍滴眼液使用说明书

盐酸吗啉胍滴眼液使用说明书
请仔细阅读说明书并在医师指导下使用
盐酸吗啉胍滴眼液使用说明书
【药品名称】
通用名称:盐酸吗啉胍滴眼液
汉语拼音:Yansuan Malingua Diyanye
【成份】本品主要成分为盐酸吗啉胍,其化学名为N-(2-胍基-
乙亚氨基)-吗啉的盐酸盐。
分子式:C6H13N5OHCl 分子量:207.66 【性状】本品为无色澄明液体。
【适应症】
用于病毒性结膜炎。
【用法用量】滴眼。
一次1~2滴,每2小时1次。
【不良反应】可引起出汗、食欲不振及低血糖等反应。
【禁忌】对本品过敏者禁用。
【注意事项】本品性状发生改变禁止使用。
【孕妇及哺乳期妇女用药】尚不明确。
【药物相互作用】尚不明确。
【药理毒理】本品能抑制病毒的DNA和RNA聚合酶,从而抑制病毒繁殖。
在人胚肾细胞上,1%浓度对DNA病毒(腺病毒,疱疹病毒)和RNA病毒(埃可病毒)都有明显抑制作用,对病毒增殖周期各个阶段均有抑制作用。
对游离病毒颗粒无直接作用。
【贮藏】遮光,密闭,在凉暗处保存。
【有效期】暂定24个月。
说明书字数:517。
盐酸莫西沙星氯化钠注射液说明书产品手册

核准日期:修改日期:盐酸莫西沙星氯化钠注射液说明书请仔细阅读说明书并在医师指导下使用。
【药品名称】通用名称:盐酸莫西沙星氯化钠注射液商品名称:拜复乐Avelox 英文名称:Moxifloxacin Hydrochloride and Sodium Chloride Injection 汉语拼音:Yansuan Moxishaxing Lühuana Zhusheye【成份】化学名称:1-环丙基-7-(S,S)-2,8-重氮-二环4.3.0壬-8-基-6-氟-8-甲氧-1,4-二氢-4-氧-3-喹啉羧酸盐酸盐。
化学结构式:O F COOH H H N N N O H3C H x HCl 分子式:C21H24FN3O4HCl 分子量:437.9 辅料:氯化钠、盐酸、氢氧化钠、注射用水。
【性状】本品为黄色的澄清液体。
【适应症】成人≥18岁上呼吸道和下呼吸道感染,如:急性窦炎,慢性支气管炎急性发作,社区获得性肺炎;以及皮肤和软组织感染。
【规格】250ml : 莫西沙星0.4g与氯化钠2.0g。
【用法用量】给药方法:根据中国健康受试者心脏所能耐受的输液速率以及国内I、II、III期临床研究的结果,推荐本品的输液时间应为90分钟。
国外推荐0.4g莫西沙星静脉给药的输液时间应大于60分钟。
剂量范围成人:推荐剂量为一次0.4g,一日一次一次1瓶,一日一次。
疗程:根据症状的严重程度或临床反应决定疗程。
治疗上呼吸道和下呼吸道感染时通常可按照下列疗程:慢性支气管炎急性发作:5天社区获得性肺炎:序贯给药静脉给药后继续口服用药推荐的总疗程为7~14天。
急性窦炎:7天治疗皮肤和软组织感染的推荐疗程为7天。
莫西沙星可以在开始治疗时静脉给药,之后再根据患者情况口服片剂给药。
0.4g莫西沙星注射液在临床试验中最多用过14天。
给药方法:静脉给药0.4g的时间应为90分钟。
莫西沙星既可以单独给药也可以与一些相容的溶液一同滴注。
盐酸莫西沙星氯化钠注射液说明书

盐酸莫西沙星氯化钠注射液说明书【药品名称】通用名:盐酸莫西沙星氯化钠注射液商品名:拜复乐?Avelox?英文名:MoxifloxacinHydrochlorideandSodiumChlorideInjection汉语拼音:-8-基}-6-氟-8-甲氧分子式:C21分子量:【性状】【适应症】成人(≥18【规格】250ml∶0.4g莫西沙星,2.0g氯化钠。
【用法用量】给药方法:根据中国健康受试者心脏所能耐受的输液速率以及国内I、II、III期临床研究的结果,推荐本品的输液时间应为90分钟。
(国外推荐0.4g莫西沙星静脉给药的输液时间应大于60分钟。
) 剂量范围(成人):推荐剂量为一次0.4g,一日一次(一次1瓶,一日一次)。
疗程:根据症状的严重程度或临床反应决定疗程。
治疗上呼吸道和下呼吸道感染时通常可按照下列疗程:慢性支气管炎急性发作:5天社区获得性肺炎:序贯给药(静脉给药后继续口服用药)推荐的总疗程为7~14天。
急性窦炎:7天0.4g给药方法:静脉给药给药:注射用水0.9%15%葡萄糖注射液10%葡萄糖注射液40%葡萄糖注射液20%木糖醇注射液林格氏液乳酸林格氏液Aminofusin10%(生产厂家:Pharmacia&Upjohn)JonosterilD5(生产厂家:FreseniusKabi)若莫西沙星注射液需与其它药物合用,每种药物需单独给药(见不相容性)。
只有澄明的溶液才能使用。
老年人儿童肝损害者肾损害腹膜种族差异对高加索人、日本人、黑人及其他种族人群进行了可能的种族间差别试验,未发现临床相关的药代动力学差别。
因此,不同种族间不必调整药物剂量。
【不良反应】在莫西沙星的临床试验中,绝大多数的不良反应为轻中度(约90%),由于不良反应导致停用莫西沙星治疗的病人为3.6%,序贯治疗(静脉给药后继续口服用药)为5.7%。
根据莫西沙星的临床试验总结出的常见不良反应(其相关程度分为很可能、可能和无法评估)列表如下:发生率≥1%<10%全身症状:腹痛、头痛、注射部位反应(如水肿/过敏/炎症/疼痛)心血管系统:合并低血钾症患者QT间期延长消化系统:恶心、腹泻、呕吐、消化不良、肝功能化验异常发生率≥舌炎、γ症神经系统:失眠、眩晕、神经质、嗜睡、焦虑、震颤、感觉异常呼吸系统:呼吸困难皮肤和附件:皮疹、瘙痒、多汗泌尿生殖系统:阴道念珠菌病、阴道炎发生率≥0.01%<0.1%全身症状:骨盆疼、面部浮肿、背疼、实验室检验异常、过敏反应、腿疼心血管系统:低血压、血管扩张、外周性水肿消化系统:胃炎、舌变色、吞咽困难、黄疸(主要为胆汁淤积性)、腹泻(难辨梭菌)血液和淋巴系统:凝血活酶减少、凝血酶原增加/国际标准化比值降低、血小板减少、贫血代谢和营养:高血糖、高血脂、高尿酸血症、LDH(乳酸脱氢酶)增高(与肝功能检查异常有关)骨骼肌肉:关节炎、肌腱异常)、弱视发生率≥发生率消化系统:伪膜性结肠炎(在极少数病例伴有危及生命的并发症),肝炎(主要为胆汁淤积性)肌肉骨胳系统:肌腱断裂皮肤和附件:斯蒂文斯-约翰逊综合征(Stevens-JohnsonSyndrome)神经系统:精神病反应心血管系统:报道在极少数病例尤其是在有严重的潜在性致心律失常条件的病人出现,包括尖端扭转型室速的室性快速性心律失常和心脏停搏。
盐酸莫西沙星滴眼液中文版

盐酸莫西沙星滴眼液中文版0.5%的盐酸莫西沙星滴眼液说明书概述:0.5%盐酸莫西沙星是一种无菌滴眼液。
它是一种用于8-甲氧基氟喹诺酮局部眼科的抗菌药物。
主要成分的化学结构式:分子式:c21h24fn3o4hcl分子量:437.9化学名称:1-环丙基-7-{s,s-2,8-重氮-双环[4.3.0]非-8-基}-6-氟-8-甲氧基-1,4-二氢-4-氧基-3-喹啉羧酸氯化氢。
盐酸莫西沙星是一种微黄色或黄色结晶性粉末。
每毫升溶液中含有5.45毫克莫西沙星,相当于5毫克莫西沙星盐酸盐。
其中:主药:莫西沙星0.5%(5mg/ml);辅助材料:硼酸、氯化钠、纯化水。
还可能含有盐酸/氢氧化钠,以将pH值调节至约6.8。
盐酸莫西沙星滴眼液是具有约290mosm/kg渗透压浓度的等渗溶液。
临床药理学:药代动力学:健康成年男性和女性受试者在双眼局部使用盐酸莫西沙星滴眼液,测量其血浆浓度,并获得每日三次的用药方案。
平均稳态血浆浓度Cmax(2.7ng/ml)和药物暴露的药时曲线AUC(45nghr/ml)下面积预计为每天1000次和1600次,低于口服莫西沙星400 mg后获得的Cmax和AUC值。
莫西沙星的血浆半衰期估计为13小时。
微生物学:莫西沙星是具有抗菌活性的8-甲氧基氟喹诺酮类抗菌药,7位的二氮杂环取代能阻止活性流出。
莫西沙星抑制拓扑异构酶ii(dna促旋酶)和拓扑异构酶iv。
DNA回旋酶是一种参与细菌DNA复制、转录和修复的必需酶。
拓扑异构酶IV是一种已知的酶,在细菌细胞分裂的染色体DNA分裂中起关键作用。
莫西沙星具有体外抗菌活性。
对糖肽类、大环内酯类和四环素类的耐药机制不影响莫西沙星的抗菌活性。
莫西沙星与这些抗生素之间没有交叉耐药性。
到目前为止,还没有发现质粒介导的耐药性。
莫西沙星具有对革兰阳性菌高活性和耐药突变的低选择性。
其耐药率很低1.8x10-9-1x10-11。
已证明,氟沙星对以下微生物的体外感染具有临床适应症:需氧革兰氏阳性菌:单核细胞增生李斯特菌、腐生葡萄球菌、无乳链球菌、缓激肽链球菌、化脓性链球菌C、G和f 组需氧革兰氏阴性菌:鲍曼不动杆菌、醋酸钙、福氏不动杆菌、柠檬酸、,产气肠杆菌、阴沟肠杆菌、大肠杆菌、产酸克雷伯菌、肺炎克雷伯菌、卡他莫拉、淋病摩根氏菌、奇异变形杆菌普通变形杆菌施氏假单胞菌厌氧微生物:产气荚膜梭菌梭杆菌种普雷沃种痤疮丙酸杆菌其他微生物:肺炎衣原体嗜肺军团菌鸟分枝杆菌分枝杆菌肺炎支原体临床研究:在两项随机、双盲、多中心临床对照试验中,患者接受盐酸莫西沙星滴眼液治疗,每天3次,持续4天,66%至69%的患者接受细菌性结膜炎治疗,持续5-6天,微生物根除基线病原体的成功率在84%至94%之间。
莫西沙星说明书

莫西沙星说明书莫西沙星,主要剂型有片剂、注射剂。
本品对革兰阴性菌、革兰阳性菌、支原体、衣原体及脊髓炎病毒等均具有良好的抗菌活性。
莫西沙星说明书是怎样的呢?本文是店铺整理的莫西沙星说明书资料,仅供参考。
莫西沙星信息介绍中文别名编辑1-环丙基-7-﹛(S,S)-2,8-重氮-二环[4.3.0]壬-8-基﹜-6-氟-8-甲氧-1,4-二氢-4-氧-3-喹啉羧酸[1]英文别名编辑4-dihydroquinoline-3-carboxylic acid(1'S,6'S)-1-Cyclopropyl-7-(2,8-diazabicyclo[4.3.0]non-8-yl)-6-fluoro-8-methoxy-4-oxo-1,分子式编辑C21H24FN3O4分子量编辑401.4314CAS号编辑151096-09-2性状编辑浅黄色至黄色粉末或晶体功能编辑莫西沙星为人工合成的喹诺酮类抗菌药,是一类较新的合成抗菌药。
具有抗菌性强、抗菌谱广、不易产生耐药并对常见耐药菌有效、半衰期长、不良反应少等优点。
药品编辑英文名 Moxifloxacin成品剂型:片剂、水针剂其他名称:莫昔沙星、拜复乐原料产地:印度总代理商:拜耳医药保健有限公司【适应症】治疗患有上呼吸道和下呼吸道感染的成人。
如急性窦炎、慢性支气管炎急性发作、社区获得性肺炎、以及皮肤和软组织感染。
【药理毒性】本品为第四代喹诺酮类广谱抗菌药,是广谱和具有抗菌活性的8-甲氧基氟喹诺酮类抗菌药。
莫西沙星在体外显示出对革兰阳性菌、革兰阴性菌、厌氧菌、抗酸菌和非典型微生物如支原体、衣原体和军团菌有广谱抗菌活性。
抗菌机制为干扰Ⅱ、Ⅳ拓扑异构酶。
拓扑异构酶是控制DNA拓扑和DNA复制、修复和转录中的关键酶。
莫西沙星在体内活性高。
【药代动力学】莫西沙星口服后吸收良好,生物利用度约90%。
[2] 达峰时0.5~4小时。
莫西沙星给药不受进食影响。
半衰期达12小时。
同服二、三价阳离子抗酸药可明显减少吸收。
莫西沙星说明书

莫西沙星说明书一、药品名称通用名称:莫西沙星商品名称:_____英文名称:Moxifloxacin二、成分本品主要成份为莫西沙星。
化学名称:1-环丙基-7-{(S,S)-2,8-二氮杂双环430壬-8-基}-6-氟-8-甲氧基-4-氧代-1,4-二氢-3-喹啉羧酸盐酸盐。
化学结构式:_____分子式:C₂₁H₂₄FN₃O₄·HCl分子量:4379三、性状本品为黄色至棕黄色薄膜衣片,除去包衣后显淡黄色至黄色。
四、适应症用于治疗成人(≥18 岁)敏感细菌所引起的下列感染:1、急性细菌性鼻窦炎。
2、慢性支气管炎急性发作。
3、社区获得性肺炎。
4、非复杂性皮肤和皮肤组织感染。
5、复杂性腹腔内感染。
五、规格_____六、用法用量剂量范围:一次 04g(1 片),一日 1 次。
1、慢性支气管炎急性发作:5 天。
2、社区获得性肺炎:10 天。
3、急性细菌性鼻窦炎:7 天。
4、治疗皮肤和软组织感染的推荐治疗时间为 7 天。
服用方法:口服,用水送服,服用时间不受饮食影响。
七、不良反应1、全身症状:乏力、念珠菌病、疼痛、不适。
2、心血管系统:心动过速、高血压、低血压、心悸。
3、消化系统:恶心、腹泻、呕吐、消化不良、肝功能检测异常。
4、血液和淋巴系统:贫血、白细胞减少、血小板减少。
5、神经系统:头晕、头痛、眩晕、失眠、嗜睡、震颤。
6、呼吸系统:呼吸困难、咳嗽。
7、皮肤和附件:皮疹、瘙痒、多汗。
八、禁忌1、已知对莫西沙星、其他喹诺酮类药物或任何辅料过敏者禁用。
2、禁用于患有可导致 QTc 间期延长的心律失常或正在服用可导致QTc 间期延长药物的患者。
3、患有低钾血症患者禁用。
九、注意事项1、致残和潜在的不可逆转的严重不良反应,包括肌腱炎和肌腱断裂,周围神经病变,中枢神经系统的影响。
2、肌腱炎和肌腱断裂:使用莫西沙星可能会增加肌腱炎和肌腱断裂的风险,在使用过程中一旦出现疼痛、肿胀、炎症等症状,应立即停止使用并休息,及时就医。
盐酸左氧氟沙星滴眼液说明书-推荐下载
外
【不良反应】 最常报道的不良反应是暂时性视力下降、发烧、头痛、暂时性眼热、眼痛或不适、咽炎
及畏光,发生率约1%-3%。其他发生率低于1%的不良反应有:过敏、眼睑水肿、眼睛干 燥及瘙痒。 【禁 忌】
对盐酸左氧氟沙星或其他喹诺酮类药物及本品任何组分过敏者禁用。 【注意事项】
1. 本品只限于滴眼用,不能用于结膜下注射,也不能直接滴入眼睛前房内。 2. 和其他抗感染药一样,延长使用本品将可能导致非敏感微生物的过度生长,包括真 菌。因此本品不应长期使用。 3. 喹诺酮类药物全身用药时,即使只有一次,也有可能发生过敏反应,某些反应伴有 心血管虚脱、丧失知觉、血管性水肿(包括咽、喉或脸部水肿)、气道阻塞、呼吸困 难、荨麻疹、瘙痒等。如果发生皮疹或其他过敏反应的症状,应立即停止用药并咨询医 生。 4. 使用时注意避免污染容器前端。 5. 建议细菌性结膜炎、角膜炎患者不戴接触透镜。 【孕妇及哺乳期妇女用药】 由于目前尚缺乏怀孕妇女使用左氧氟沙星滴眼液的资料,因此对于怀孕妇女,只有在判 断药物的潜在利益大于对胎儿的潜在风险时,才能使用本品。根据氧氟沙星的研究报道,推 测左氧氟沙星可通过人乳汁排泄,因此哺乳期妇女慎用。 【儿童用药】 1岁以下婴儿使用本品的疗效及安全性尚未确立。未成熟动物口服喹诺酮类药物可引起 关节病,但没有证据证明左氧氟沙星滴眼液对承重关节有任何影响。 【老年用药】 老年人使用本品的疗效及安全性与其他成人患者无总体差别。 【药物相互作用】 尚缺乏有关本品的药物相互作用资料。但是,已经证明某些喹诺酮类药物全身用药时可 增加茶碱的血药浓度,干扰咖啡因的代谢,增加口服抗凝药华法林及其衍生物的作用,如果 同服环孢菌素,患者可能会有一过性血清肌酐升高。 【药物过量】
பைடு நூலகம்
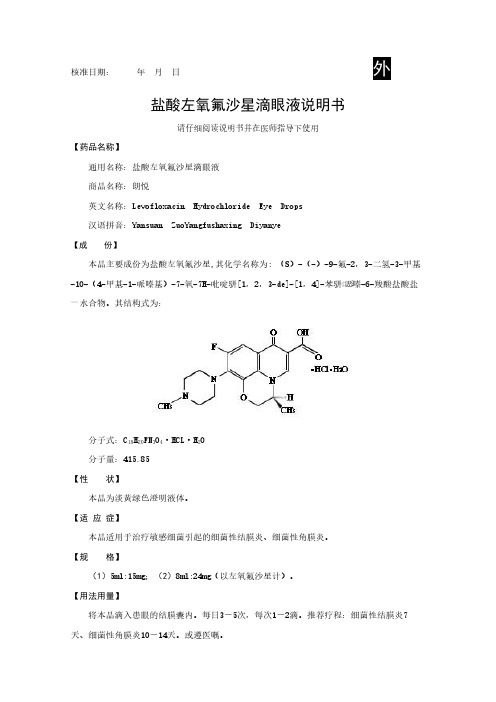
分子式:C18H20FN3O4·HCL·H2O 分子量:415.85 【性 状】 本品为淡黄绿色澄明液体。 【适 应 症】 本品适用于治疗敏感细菌引起的细菌性结膜炎、细菌性角膜炎。 【规 格】 (1)5ml:15mg;(2)8ml:24mg(以左氧氟沙星计)。 【用法用量】 将本品滴入患眼的结膜囊内。每日3-5次,每次1-2滴。推荐疗程:细菌性结膜炎7 天、细菌性角膜炎10-14天。或遵医嘱。
盐酸莫西沙星滴眼液说明书

核准日期修改日期 盐酸莫西沙星滴眼液说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:盐酸莫西沙星滴眼液英文名称:Moxifloxacin Hydrochloride Eye Drops汉语拼音:Yansuan Moxishaxing Diyanye【成份】本品主要成份为盐酸莫西沙星化学名称:1-环丙基-6-氟-1,4-二氢-8-甲氧-7-[(4aS,7aS )-八氢-6H-吡咯并[3,4-b]吡啶-6-基]-4-痒代-3-喹啉羧酸盐酸盐化学结构式:分子式:C 21H 24FN 3O 4·HCl分子量:437.9辅料:氯化钠,硼酸,氢氧化钠和/或盐酸,纯化水【性状】本品为淡黄绿色的澄明液体。
【适应症】用于治疗由下列敏感微生物引起的细菌性结膜炎:革兰氏阳性菌:棒状杆菌属*藤黄微球菌*金黄色葡萄球菌表皮葡萄球菌溶血性葡萄球菌人葡萄球菌瓦氏葡萄球菌*肺炎链球菌草绿色链球菌群*革兰氏阴性菌:鲁氏不动杆菌*流感嗜血杆菌副流感嗜血杆菌*鲍氏不动杆菌琼氏不动杆菌*嗜麦芽窄食单胞菌*金黄杆菌属*其它微生物:沙眼衣原体*针对此类微生物感染的有效性研究例数少于10例。
【规格】按C21H24FN3O4计,5ml:25mg(0.5%,w/v)【用法用量】患眼每次滴入1滴,每日3次,连续使用7天。
【不良反应】在莫西沙星滴眼液的临床试验中,报告出现了下列不良反应,根据惯用方法将以下不良反应归类:非常常见(≥1/10),常见(≥1/100至<1/10),不常见(≥1/1000至<1/100),罕见(≥10000至<1/1000),非常罕见(<1/10000)。
在每一个频率上市后监测过程中发现的其他不良反应包括如下一些。
根据现有的数据尚不能推测发生频率。
在每一个系统器官分类内,副作用按严重程度下降的顺序排列。
【禁忌】禁用于对莫西沙星、其它喹诺酮类药物或此药物中任何成份有过敏史的患者。
【注意事项】1.不得注射。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
0.5%的盐酸莫西沙星滴眼液说明书
概述:0.5%的盐酸莫西沙星是无菌滴眼液,它是8 - 甲氧基氟喹诺酮类局部眼科使用的抗菌药。
主要组成成分化学结构式:
分子式:C21H24FN3O4·HCl
分子量:437.9
化学名:1-环丙基-7-{S,S-2,8-重氮-二环[4.3.0] non-8-yl}-6-氟-8-甲氧-1,4-二氢-4-氧-3-喹啉羧酸氢氯化物。
盐酸莫西沙星是一种微黄色或黄色结晶性粉末。
每毫升溶液中含有5.45毫克莫西沙星,相当于5毫克莫西沙星盐酸盐。
包括:主药:莫西沙星0.5%(5毫克/毫升);辅料:硼酸,氯化钠,和纯净水。
也可能包含盐酸/氢氧化钠调节pH值约6.8。
盐酸莫西沙星滴眼液是具有约290 mOsm/kg渗透压浓度的等渗溶液。
临床药理学:
药代动力学:健康成年男性和女性受试者通过双眼局部使用盐酸莫西沙星滴眼液,测定其血浆浓度,求得每天3次的用药方案。
平均稳态血药浓度C max (2.7 ng/mL), 药物暴露的药时曲线下面积AUC (45 ng·hr/mL),每天预计1000和
1600次,要低于400毫克剂量口服莫西沙星治疗后所得的C max和AUC值。
莫西沙星的血浆半衰期估计为13小时。
微生物学:
莫西沙星是具有抗菌活性的8-甲氧基氟喹诺酮类抗菌药,7位的二氮杂环取代能阻止活性流出。
莫西沙星抑制拓扑异构酶II(DNA促旋酶)和拓扑异构酶IV。
DNA促旋酶是人体必需的涉及复制,转录和修复细菌DNA的酶。
拓扑异构酶IV是在细菌细胞分裂中染色体DNA的分区过程中发挥关键作用的已知酶。
莫西沙星在体外显示出对病原体具有抗菌活性。
导致对糖肽类、大环酯类和四环素类耐药的耐药机制不影响莫西沙星的抗菌活性。
莫西沙星和这些抗菌药无交叉耐药性。
至今未发现质粒介导的耐药性的出现。
莫西沙星具有对革兰阳性菌高活性和耐药突变的低选择性。
其耐药率很低1.8 x 10-9- 1 x 10-11 。
西沙星已经显示具有针对以下微生物体外感染带来的临床适应症:
需氧革兰氏阳性菌:
单核细胞增生斯特氏菌
腐生葡萄球菌
无乳链球菌
缓症链球菌
化脓性链球菌
链球菌C组,G和F
需氧革兰氏阴性菌:
鲍曼不动杆菌
醋酸钙不动杆菌弗氏柠檬酸杆菌枸橼酸杆菌
产气肠杆菌
阴沟肠杆菌
大肠杆菌
产酸克雷伯菌肺炎克雷伯菌卡他莫拉菌
摩氏摩根
淋病奈瑟菌
奇异变形杆菌普通变形杆菌施氏假单胞菌厌氧微生物:产气荚膜梭菌梭杆菌种
普雷沃种
痤疮丙酸杆菌其他微生物:肺炎衣原体
嗜肺军团菌
鸟分枝杆菌
分枝杆菌
肺炎支原体
临床研究:
在两个随机、双盲、多中心的临床对照试验中,患者每天服用3次药物持续4天, 盐酸莫西沙星滴眼液的临床治疗方案,在66%至69%的患者中治疗细菌性结膜炎持续5 - 6天,根除基线病原体微生物成功率从84%到94%不等。
请注意:微生物学的根除并不总是临床抗感染试验的结果。
适应症:盐酸莫西沙星滴眼液的解决方案被批准用于治疗敏感菌及以下生物体菌株所致的细菌性结膜炎:
需氧革兰氏阳性菌:
棒状杆菌属*
藤黄微球菌*
金黄色葡萄球菌
表皮葡萄球菌
溶血葡萄球菌
葡萄球菌
肺炎链球菌
草绿色链球菌组
需氧革兰氏阴性菌:
洛菲不动杆菌
流感嗜血杆菌
副流感嗜血杆菌*
其他微生物:
沙眼衣原体
*对该敏感菌导致的临床适应症的有效性研究少于10种。
警告:
不能用于注射。
盐酸莫西沙星滴眼液不应该注射到结膜下,也不应被直接注射到眼睛前房。
单剂量全身给予喹诺酮类药物,包括莫西沙星的患者,有过严重甚至偶尔致命的超敏(过敏)反应的报告。
这些过敏反应伴随着心血管功能衰竭,意识障碍,血管性水肿(包括喉,咽或面部水肿),气道阻塞,呼吸困难,荨麻疹,瘙痒等。
一旦莫西沙星发生过敏性反应,立即停止使用这种药物的。
严重的急性过敏反应可能需要立即抢救。
氧气及呼气量可作为抢救的临床指标。
注意事项:
一般当莫西沙星滴眼液与其他抗菌药联用,长时间使用可能导致非敏感微生物,包括真菌的过度生长。
如果发生二次感染,请停止使用并实行替代疗法。
临床诊断发现,患者需要借助放大检查的帮助,如裂隙灯生物显微镜检查,并在适当情况下,进行荧光素染色检查。
如果患者有细菌性结膜炎的症状,应尽量不要戴隐形眼镜。
患者须知:避免滴眼液前端与眼睛,手指或其他地方接触污染,单剂量(包括小于单剂量)全身给予喹诺酮类药物,包括莫西沙星的患者,出现超敏(过敏)反应,立即停止使用,在出现皮疹或过敏反应的第一个迹象时,咨询医生。
药物相互作用:尚未对莫西沙星溶液进行药物- 药物相互作用的研究。
体外研
究表明莫西沙星不能抑制CYP3A4,CYP2D6,CYP2C9,CYP2C19,CYP1A2,表明莫西沙星不可能改变这些细胞色素P450同工酶代的药代动力学。
致癌性,致突变性,生育力损害:对动物的长期研究未发现莫西沙星致癌的证据。
然而,在大鼠身上进行对于人类的致癌作用加速试验(诱发和促进测定),发现致癌性在大鼠口服给药500毫克/公斤/天38周后(约21,700倍,达到最高。
对于50公斤的人,建议每日剂量按照1毫克/公斤计算)。
使用菌株进行Ames试验,检测莫西沙星是否具有致突变性。
5株Ames试验中4次为阴性,相同测定条件下其它喹诺酮类TA102的Ames试验为阳性。
可能是由于抑制了DNA旋转酶。
体外试验显示大剂量的莫西沙星可致V79细胞出现染色体异常,但莫西沙星并不诱导大鼠肝细胞的外DNA合成。
小鼠体试验核仁测定为阴性结果,并且其对小鼠的显性致死测定为阴性。
当雄性和雌性大鼠口服剂量高达500毫克/公斤/天时,给予莫西沙星后没有对生殖力产生影响。
500毫克/公斤对雄性大鼠的精子形态和雌性大鼠的发情周期影响轻微。
约21,700倍的每日人眼用药的最大剂量。
妊娠致畸作用。
妊娠C类:在子代口腔器官形成期给予孕鼠高达500毫克/公斤/天(约21,700倍的每日人眼用药的最大剂量)的剂量,莫西沙星不致畸。
然而,对怀孕的猴子给予口服剂量高达100毫克/公斤/天(约4,300倍每日人眼用药的最大剂量)。
降低胎儿体重,稍微延迟胎儿骨骼发育进行观察,没有证据表明莫西沙星致畸。
在100毫克/千克/天时,观察到更小的胎儿致畸的发生率增加。
由于在妊娠妇女中无适当和良好的对照研究,莫西沙星溶液在怀孕时使用对胎儿仅存在潜在风险。
哺乳母亲:莫西沙星没有在人类乳汁中测得,可以推测莫西沙星不可能通过人类乳汁排出。
但对哺乳母亲用药应谨慎行使。
老年用药:莫西沙星的药代动力学不受年龄影响。
不良反应:最常见的眼部不良反应为结膜炎,视力下降,干眼症,角膜炎,眼不适感,眼部充血,眼痛,眼瘙痒,结膜下出血和撕裂。
发生这些事件的患者约1-6%。
1-4%患者的不良反应为发热,咳嗽加重,感染,中耳炎,咽炎,皮疹和
鼻炎。
剂量与用法:
受感染的眼睛滴一滴,每日3次,连用7天。
包装规格:
莫西沙星的无菌滴眼液是以Alcon’s DROP-TAINER(R) 作为点胶系统,由天然低密度的聚乙烯瓶和棕褐色的聚丙烯滴嘴封闭构成。
围绕包装和颈部区域设有收缩带。
3mL装入4mL 瓶中- NDC 0065-4013-03
贮藏: 2°C - 25°C (36°F - 77°F)。
厂商:由美国得克萨斯州沃斯堡爱尔康实验室研发。
由拜耳医药保健授权给爱尔康公司。
美国专利:NO. 4,990,517; 5,607,942; 6,716,830(C)2003-2006, 2008 爱尔康公司。
