FDA透皮贴剂总结
透皮贴 质量标准 fda

透皮贴质量标准fda全文共四篇示例,供您参考第一篇示例:透皮贴是一种通过皮肤吸收药物的给药方式,它被广泛应用于医学治疗中。
在透皮贴产品的质量标准方面,美国食品药品监督管理局(FDA)是全球公认的权威机构之一。
本文将重点探讨透皮贴产品的质量标准及其在FDA管理下的相关要求。
透皮贴产品的质量标准对于药品的疗效和安全性至关重要。
在FDA的监管下,透皮贴产品必须符合一系列严格的要求,包括药物的成分、剂量、制备工艺、包装和标签等方面。
这些要求旨在确保透皮贴产品在使用过程中能够达到预期的治疗效果,并且对患者没有不良的安全风险。
FDA对于透皮贴产品的质量标准主要体现在几个方面。
首先是药物成分的纯度和质量。
透皮贴作为一种给药方式,要求药物的成分应当符合特定的纯度标准,确保药物在透皮贴中的稳定性和有效性。
其次是透皮贴的制备工艺。
这包括药物与透皮贴胶合剂的混合、成型、包装等工艺流程,要求严格遵循GMP(Good Manufacturing Practice)的要求,以确保产品的质量稳定性和一致性。
FDA还对透皮贴产品的包装和标签提出了严格的要求。
包装应具备良好的密封性和稳定性,以保护药物不受外界环境的影响。
产品的标签应当清晰明了地标注药物成分、剂量、使用方法、注意事项等信息,以便患者正确、安全地使用透皮贴产品。
在进行透皮贴产品的注册和上市申请时,制造商必须向FDA提交完整的产品质量控制文件和相关的临床试验数据,以证明产品符合FDA的质量标准和安全性要求。
FDA将通过审评这些文件和数据来决定是否批准该产品上市销售。
一旦产品上市销售后,FDA还将定期对透皮贴产品进行抽样检验和质量监管,以确保产品在市场上的持续符合质量标准。
透皮贴产品的质量标准是保障患者安全和治疗效果的重要保障之一。
在FDA的监管下,透皮贴产品必须严格遵循一系列的质量标准和要求,以确保产品的质量稳定和安全有效。
制造商应当充分重视透皮贴产品质量标准的要求,并积极配合FDA的监管,以生产和销售高质量的透皮贴产品,造福广大患者。
硕士论文--多奈哌齐透皮贴剂的药学研究

多奈哌齐透皮给药研究
Study of Donepezil Transdermal Patch
Abstract
Donepezil(DPB)is a piperidine—based reversible acety7lcholinesterase inhibitor. Currently DPB is the most prescribed pharmacological agent for the treatment of mild to moderate Alzheimer’S disease.It also plays the important role in improving the patient’S mental state and keeping the brain active.Now the drug dosage form of DPB has tablets and capsules.Researches have showed that aizheimer’S disease is the most common cause of
研究结果表明当使用混合丙烯酸酯压敏胶作为基质时(B/C=3/I,w/w),多奈哌齐 经皮贴剂中药物浓度超过15%wt_i产生结晶,透皮贴剂能够保证长时间的给药需求, 贴剂中有关物质的生成量较少,药物的稳定性较好,但药物的体外经皮渗透速率较低, 需要加入促渗剂提高药物的经皮渗透速率。使用脂肪酸酯1和有机酸作为混合促渗剂时, 能够起到协同促渗作用,与对照组相比,可将多奈哌齐累积透过量提高2.7倍。使用最 优处方进行大鼠体内药代动力学实验,结果表明,与口服给药相比,多奈哌齐经皮给药 后,血药浓度垒少可以维持48小时以上,药物生物利用度显著提高,-、I‘均滞留时间和 半衰期也相应显著延长。
尼派(尼古丁透皮贴剂)使用说明

尼派(尼古丁透皮贴剂)【用法用量】从使用本品开始,应要求患者完全停止吸烟。
本品适用于年龄超过18岁的成年人。
一日一次,一次一片本品,并应贴用24小时。
【注意事项】1.严格按用法用量使用,不得超量,疗程应不超过3个月。
2.现有关资料表明,与安慰剂比较,短期使用尼古丁透皮贴剂有效。
戒烟后的远期疗效并不取决于本品,而主要取决于患者的毅力和是否接受了进一步的心理支持治疗。
3.使用本品时,应要求患者完全停止吸烟。
应告诫患者,如果在使用本品时继续吸烟,将增加吸烟所带来的危害,包括心血管方面的不良反应。
4.下列疾病的患者,应慎重考虑尼古丁可能引起的不良反应,请在医师指导下使用:稳定性心绞痛、急性心肌梗塞后、闭塞性周围动脉性疾病、脑血管疾病、心力衰竭、肾脏或肝脏功能异常、糖尿病、未得到控制的高血压、甲状腺功能亢进、消化道溃疡、嗜铬细胞瘤。
5.尼古丁是毒性物质,如被迅速吸收,毫克剂量水平即有潜在的致命危险。
6.过敏反应:临床研究发现,少数患者使用本品后,可出现接触性过敏。
对于这种患者,当使用其它含有尼古丁的产品(包括烟草)时,可能会再度出现接触性过敏。
7.如果使用本品后出现长期失眠症状,可在贴用16小时后揭除(即夜间不使用)。
8.有报道在已知有肌无力(如重症肌无力、肌无力综合征)病史患者使用本品后症状加重。
9.对出现严重或持续性皮肤不良反应的患者,应建议中断治疗。
10.戒烟可能导致行为改变。
尚无资料显示适当剂量的尼古丁透皮贴剂会影响使用者的驾驶和机械操控能力。
11.几片尼古丁透皮贴剂同时使用可导致尼古丁严重过量。
用药过量的症状和体征与急性尼古丁中毒相同。
非吸烟者的症状包括:苍白、出汗、恶心、流涎、呕吐、腹泻、头痛、头晕、听力和视力下降,震颤、意识不清、肌无力、惊厥、虚脱、缺乏神经反应和呼吸衰竭。
致死剂量可引起患者外周或中枢性呼吸麻痹,较少情况下出现心脏衰竭,随即导致惊厥和死亡。
若患者表现出用药过量的症状,应立即揭去本品。
2024年透皮贴剂市场需求分析

透皮贴剂市场需求分析引言透皮贴剂是一种通过皮肤进行药物递送的贴剂,以其方便使用、无需注射和剂型灵活性等优势,受到越来越多消费者的青睐。
本文将对透皮贴剂市场的需求进行分析,包括市场规模、市场趋势、消费者需求等方面。
市场规模透皮贴剂市场在过去几年取得了快速增长。
预计到2025年,全球透皮贴剂市场规模将超过100亿美元。
这一增长主要受益于人们对便捷、无创的药物递送方式的需求以及透皮贴剂技术的不断改进。
市场趋势1. 长期药物治疗的需求增加随着人口老龄化趋势的加剧,慢性疾病的发病率不断上升。
透皮贴剂作为一种能够提供长期药物治疗的方式,在满足患者需求方面具有巨大潜力。
特别是对于老年人和长期病患,透皮贴剂的使用更为方便,减少了口服药物带来的麻烦。
2. 个性化药物递送需求增加不同人群对药物的吸收和反应有所差异,个体化治疗已成为医疗领域的一个重要趋势。
透皮贴剂由于其能够根据个体特征调整药物递送速率的优势,正逐渐成为个性化治疗的首选方法。
3. 医学美容市场的快速增长透皮贴剂作为一种无创方式,已经被广泛应用于医学美容领域。
透皮贴剂能够提供局部治疗、美容养护等服务,因此在医学美容市场快速发展。
随着人们对美容需求的增加,透皮贴剂市场将继续受益于这一趋势。
消费者需求1. 便捷性透皮贴剂的便捷性是消费者选择的重要因素之一。
相比口服药物,透皮贴剂无需注射,操作简单,方便携带,在日常生活中更为方便使用。
2. 无创性透皮贴剂无需刺破皮肤,减少了注射带来的疼痛和恢复时间。
对于那些害怕注射的人群,透皮贴剂是一种可行的替代方式。
3. 减少药物副作用透皮贴剂能够减少药物在体内的浓度峰值,提供稳定的治疗效果,从而减少了药物副作用的发生。
这对于长期使用药物的患者来说尤为重要。
4. 个性化治疗透皮贴剂的个性化递送特性满足了不同人群对药物的个体差异需求。
消费者对于能够根据自身需要调整药物递送速率的透皮贴剂表现出了强烈的兴趣。
结论透皮贴剂市场在近年取得了快速增长,并且有望继续保持良好的发展势头。
FDA批准的透皮贴挤仿制药的载药量、贴片面积与原研药的对比表-精品
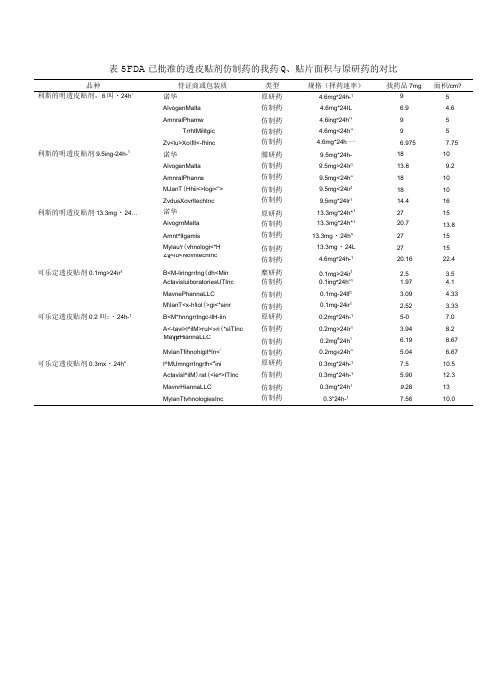
表5FDA已批准的透皮贴剂仿制药的我药Q、贴片面积与原研药的对比品种恃证商或包装质类型规格(择药速率)找药品7mg 面枳/cm? 利斯的明透皮贴剂,6叫・24h' 诺华原研药 4.6mg e24h-19 5AlvogenMalta 仿制药 4.6mg*24IL 6.9 4.6AmnralPhamw 仿制药 4.6ing e24h'19 5TrrhtMilitgic 仿制药 4.6mg<24h'' 9 5Zv<lu>Xo\fll<-fhInc 仿制药 4.6mg*24h一 6.975 7.75 利斯的明透皮贴剂9.5ing-24h-1诺华朦研药9.5mg*24h- 18 10AlvogenMalta 仿制药9.5mg>24Ir113.8 9.2AmnralPhanns 仿制药9.5mg<24h" 18 10MJanT(Hhii<>logi<"> 仿制药9.5mg<24ir118 10ZvdusXovrltechInc 仿制药9.5mg*24Ir114.4 16利斯的明透皮贴剂13.3mg・24…诺华原研药13.3mg*24h*127 15AivogrnMalta 仿制药13.3mg*24h*120.7 13.8Amnt^lIgamis 仿制药13.3mg・24h" 27 15Mylau r r(vhnologi<*H 仿制药13.3mg・24L 27 15Zv<lu<NovrltechInc< 仿制药 4.6mg e24h-120.16 22.4 可乐定透皮贴剂0.1mg>24ir1B<M-liringrrIng(dh<Min 糜研药0.1mg>24ir1 2.5 3.5ActavisluiboratoriesUTInc 仿制药0.1ing e24h"1 1.97 4.1MavnePhannaLLC 仿制药0.1mg-24If1 3.09 4.33M\lanT<x-h!iol(>gi<*sinr 仿制药0.1mg-24ir1 2.52 3.33 可乐定透皮贴剂0.2叫:・24h-1B<M*hnngrrIngc-llH-iin 原研药0.2mg e24h-15-0 7.0A<-tavi>l^ilM>rul<»ri(*sITInc 仿制药0.2mg>24Ir1 3.94 8.2Ma\nrHiannaLLC1F 仿制药0.2mg#24h1 6.19 8.67MvlanTfihnohigit^ln<(仿制药0.2mg«24h" 5.04 6.67 可乐定透皮贴剂0.3mx・24h" I^MUmngrrIngrlh<a ini 原研药0.3mg*24h-17.5 10.5Actavisl^ilM)rat(<ie a>ITInc 仿制药0.3mg*24h-1 5.90 12.3MavnrHiannaLLC 仿制药0.3mg*24h19.28 13MylanTtvhnologiesInc 仿制药0.3"24h-17.56 10.0。
化学仿制药透皮贴剂药学研究技术指导原则(试行)

202012一、概述 (1)二、透皮贴剂仿制药药学研究的整体思路与要求 (1)三、处方与制备工艺研究 (2)(一)处方 (2)1.原料药 (2)2.辅料与材料 (3)3.标识 (4)(二)工艺 (4)1.典型工艺步骤 (4)2.工艺研究 (4)3.批量 (5)四、质量与特性研究 (5)(一)一般要求 (5)(二)特性质量研究 (6)1.体外释放 (6)2.体外透皮 (8)3.体外黏附性能 (8)4.药物残留 (9)5.制剂中原料药热力学稳定性 (9)6.黏合剂杂质 (9)7.热效应 (10)8.基质结构的微观评估 (10)五、稳定性研究 (10)六、名词解释 (11)七、参考文献 (12)一、概述透皮贴剂(Transdermal Patch)系指用于完整皮肤表面能将药物输送透过皮肤进入血液循环系统起全身作用的贴剂。
透皮贴剂通过扩散而起作用,其释放速度受到药物浓度影响。
本指导原则主要针对透皮贴剂化学仿制药。
透皮贴剂按照含有活性物质的支撑层的结构特点通常可分为骨架型(Matrix Type)和储库型(Reservoir Type)。
骨架型贴剂通常由背衬层(Backing Membrane)、含有活性物质的支撑层(Drug-in-Adhesive Matrix)、黏合层(Contact Adhesive)、保护层(Release Liner)等组成。
储库型贴剂通常由含药液态或半固态凝胶用热封区域截留在背衬层和控释材料之间制成【1,2,3】。
本指导原则仅为化学仿制药透皮贴剂的药学方面相关研发研究工作提供参考,重点讨论透皮贴剂在药学方面的特殊性问题,对其他药学一般性问题可参照已发布的相关指导原则执行。
本指导原则仅代表药品监管部门目前对于该剂型的观点和认识。
在符合现行法规的要求下,可采用替代的研究方法,但应提供详细的研究资料或与监管机构沟通。
二、透皮贴剂仿制药药学研究的整体思路与要求研究者应当按照国家局发布的《化学仿制药参比制剂遴选与确定程序》【4】选择参比制剂。
透皮贴剂质量研究报告范文

透皮贴剂质量研究报告范文透皮贴剂质量研究报告范文一、引言透皮贴剂作为一种外用药物给药系统,在临床上得到了广泛应用。
其特殊的贴搁形式和透皮给药的特点,使得透皮贴剂能够提供持续、控制释放的药物治疗效果,极大地方便了患者使用。
然而,透皮贴剂的疗效和安全性主要取决于其质量,因此研究透皮贴剂的质量显得尤为重要。
二、材料与方法本次研究选取了5种常见透皮贴剂作为研究对象,包括A、B、C、D和E五个品牌。
通过一系列的质量检测方法对透皮贴剂进行评价,主要包括以下几个方面:1. 外观检查与包装:检查透皮贴剂外观是否完好,包装是否符合要求。
2. 厚度测定:使用数显厚度计对透皮贴剂进行测定。
3. 吸附量测定:将透皮贴剂放入已知体积的溶剂中溶解,测定溶剂中药物含量。
4. 药物释放性能:通过模拟人体皮肤条件,使用流经式离体释放试验器来测定透皮贴剂的药物释放性能。
5. 粘性评估:使用牵拉试验仪对透皮贴剂的粘性进行评估。
6. 纯度检测:采用高效液相色谱法(HPLC)对透皮贴剂中的药物纯度进行检测。
三、结果与讨论1. 外观检查与包装:所有透皮贴剂均符合外观检查要求,并且包装完好。
2. 厚度测定:透皮贴剂的测定结果表明,A品牌平均厚度为0.2mm,B品牌为0.25mm,C品牌为0.18mm,D品牌为0.22mm,E品牌为0.15mm。
3. 吸附量测定:透皮贴剂在溶剂中的吸附量测试结果表明,A 品牌的吸附量为98% ± 2%,B品牌为97% ± 1%,C品牌为95% ± 3%,D品牌为98% ± 1%,E品牌为95% ± 3%。
4. 药物释放性能:透皮贴剂在流经式离体释放试验器中的药物释放性能测试结果如下:A品牌的6小时释放量为96% ± 2%,B品牌为95% ± 3%,C品牌为92% ± 2%,D品牌为94% ± 1%,E品牌为90% ± 3%。
透皮贴剂市场分析报告

透皮贴剂市场分析报告1.引言1.1 概述概述部分:透皮贴剂作为一种新型的给药方式,其在药物给药领域有着广阔的市场前景和应用前景。
透皮贴剂采用贴附在皮肤表面的方式,通过透皮吸收的方式将药物释放到人体内部,避免了药物经过肠道消化和肝脏代谢的过程,提高了药物的生物利用度,减少了药物的副作用,具有使用方便、依从性好、效果持久等优势。
本报告将对透皮贴剂市场进行深入分析,探讨透皮贴剂的市场现状、优势和应用领域以及发展趋势,为相关行业提供全面、客观的市场数据和发展趋势,帮助企业树立正确的市场意识和发展方向。
1.2 文章结构文章结构包括引言、正文和结论三个部分。
在引言部分,我们将简要介绍透皮贴剂市场的背景和重要性,并说明文章的结构。
正文部分将详细分析透皮贴剂市场的现状、优势和应用领域以及市场发展趋势。
结论部分将对透皮贴剂市场的前景进行展望,提出行业发展建议,并总结全文的结论。
通过这样的结构安排,我们将全面深入地分析透皮贴剂市场的各个方面,为读者提供全面的市场分析报告。
1.3 目的目的部分的内容:本报告的目的在于对透皮贴剂市场进行全面深入的分析,包括市场现状、市场发展趋势以及透皮贴剂的优势和应用领域。
通过对市场情况的研究分析,为相关企业提供市场前景展望和行业发展建议,帮助行业内企业更好地把握市场机会,制定有效的市场营销策略,推动透皮贴剂市场的良性发展。
1.4 总结综上所述,透皮贴剂市场作为一种新型的药物给药方式,在医药行业中具有广阔的发展前景。
通过本报告对透皮贴剂市场现状、优势和应用领域以及市场发展趋势的分析,可以看出透皮贴剂具有明显的优势和应用潜力。
未来随着技术的不断创新和市场需求的增加,透皮贴剂市场必将进一步壮大,为药品的治疗效果和患者的治疗体验带来重要的改善。
我们对透皮贴剂市场的前景和行业发展提出乐观的展望,并为进一步拓展该市场提出了相应的建议。
希望本报告能够为相关从业人员提供有益的参考和启发,推动透皮贴剂市场的持续健康发展。
2024年透皮贴剂市场调查报告

2024年透皮贴剂市场调查报告背景介绍透皮贴剂是一种通过皮肤透过靶向给药的剂型,逐渐受到消费者和医生的青睐。
随着人们对健康意识的提高,透皮贴剂市场的规模也在不断增长。
市场调查方法本次市场调查采用了问卷调查和市场研究的方法。
问卷调查针对消费者和医生两个群体,通过随机抽样的方式进行,共有1000名消费者和200名医生参与。
市场研究则通过搜集相关数据和报告进行。
市场规模根据市场研究数据分析,透皮贴剂市场的规模在过去五年间平均每年增长10%。
预计在未来几年中,市场规模将继续增长。
消费者需求调查数据显示,消费者对透皮贴剂的需求主要集中在以下几个方面: - 便捷性:消费者希望使用透皮贴剂更为方便,能够随时随地使用。
- 高效性:消费者对透皮贴剂的疗效要求较高,希望能够快速缓解症状。
- 安全性:消费者对透皮贴剂的安全性有一定的担忧,希望能够选择到经过严格检验认证的产品。
医生推荐调查数据显示,医生对透皮贴剂的认可度较高,并且愿意推荐给适合的患者。
其中,医生推荐透皮贴剂的主要原因包括: - 避免肠胃刺激:透皮贴剂给药可以避免经肠胃的副作用,减轻患者的不适感。
- 短效药物给药:透皮贴剂适用于一些需要频繁给药但又不需要长时间维持药物浓度的情况。
- 药物稳定性:透皮贴剂可以保持药物稳定,减少药物的损失和变质。
市场竞争透皮贴剂市场竞争激烈,主要竞争对手包括国内外大型制药企业和一些创新型科技公司。
这些企业通过不断创新和提高产品质量来争夺市场份额。
目前,市场上主要的透皮贴剂产品包括止痛类、激素类、抗血小板类等。
市场发展趋势根据市场研究数据和专家意见,透皮贴剂市场未来的发展趋势主要包括: - 产品多样化:透皮贴剂产品将变得更加多样化,适应不同患者和治疗需求。
- 技术创新:透皮贴剂的制备技术将进一步创新,提高质量和使用体验。
- 市场区域扩大:透皮贴剂市场将拓展到更多的地区,满足不同地区的需求。
总结透皮贴剂市场在消费者需求和医生推荐的共同推动下,持续增长。
芬太尼透皮贴使用注意事

换贴时间及更换部位
➢ 72小时换贴
➢ 换贴时间不建议少于48小时。
➢ 新贴用药:更换粘贴部位,几天后方可在相同的部位 重复贴用。避免以前毛囊炎或造成药物蓄积。
➢ 注意固定程度使其充分与皮肤接触,确保药物能充分 吸收,及时检查贴膜的固定
➢ 旧贴处理:72小时后,更换新贴,揭下旧贴,将粘性部 分对折,放回原包装袋内,按麻醉药品回收处理。因 使用后的废贴残余药量可达50%以上。
发较少,为最适宜位置。避开手肘、腋下等褶皱处,一般 选择前胸、上臂位置。
• 贴敷部位如有毛发,应在使用前剪除但禁忌用备皮刀,以
防皮肤损伤。
对于卧床患者,不宜贴在后背,容易
导致卷边脱落。
对于大小便失禁或床上大小便患者不宜贴敷 在大腿内侧
对于较瘦的患者或恶液质患者,贴剂尽量在有一定 皮下组织处,避开骨隆突处;出汗较多患者不宜贴 附在躯干部位皮肤,而在上臂内侧或大腿内侧汗液 较少,适宜贴敷,以减少卷边或脱落机会。
贴敷前用温水清洗皮肤,待干后方可贴敷
贴敷时操作者的手一定不要接触 FTP的粘贴面,并需将FTP 平整贴在皮肤上,再用手掌用力按压至少30s,以确保贴剂 与皮肤完全平整的接触
贴敷时患者皮肤要处于自然放松无张力状态,以防止贴敷 时由于贴膜或皮肤张力过大,而皮肤恢复自然状态时导致 的贴膜皱褶。
芬太尼透皮贴的健康宣教
➢ 芬太尼透皮贴不能马上起效果,通常需要 12-24 小时才能达到 稳态,因此刚使用芬太尼透皮贴的前 24小时也有可能出现疼痛 控制不佳,需要使用短效镇痛药处理,24 小时后则可以持续有 效 72 小时。
• 3)轻中度肝/肾功能不全患者。芬太尼的代谢产物无药理活 性,不会加重肾损伤。
• 4)其他:如口服依从性较差患者等。
中重度癌痛患者应用芬太尼透皮贴剂的效果分析

龙源期刊网 中重度癌痛患者应用芬太尼透皮贴剂的效果分析作者:李平来源:《健康必读(上旬刊)》2018年第11期【摘要】目的:以我院46例中重度癌痛患者为研究对象,分析芬太尼透皮贴剂的应用效果和不良反应,评估芬太尼透皮贴剂的临床应用价值。
方法:对46例晚期癌痛患者在家中应用芬太尼透皮贴剂治疗前后的疼痛强度、生活质量、用药不良反应等情况变化进行追踪观察,总结各方面情况,评估芬太尼透皮贴剂的临床应用价值。
结果:91.5%患者均表示自己的疼痛程度得到了一定的缓解,芬太尼透皮贴剂的应用有效地提高了自己的生活质量水平。
只有8.5%的患者由于恶心腹泻等消化系统方面的不良反应或芬太尼透皮贴剂的价格较高而中断芬太尼透皮贴剂的使用。
结论:从患者的直观感觉反馈来看,芬太尼透皮贴剂的持续止痛效果优于传统阿片类药物,而且芬太尼透皮贴剂作为一种非创伤性的持续给药途径,在患者依从性、安全性方面要优于传统的阿片类药物。
芬太尼透皮剂明显缓解中重癌痛患者疼痛,提高患者生活质量,药品不良反应较少,值得推广使用。
【中图分类号】R181.3+2;;;;;;【文獻标识码】B;;;;;【文章编号】1672-3783(2018)11-0049-01疼痛是癌症患者最难忍受困扰、也是临床最常见的癌症并发症之一。
临床上约有半数以上非卧床癌症患者以中重度癌性疼痛为主诉,而这些癌性疼痛的患者中约有1/3的疼痛程度为重度疼痛。
目前对于癌性疼痛的患者最常用的治疗方法就是通过口服或注射等方式给予阿片类药物,可以迅速有效缓解疼痛。
然而当癌症进入进展期时,患者对止痛的需求从快速止痛转向了持续有效,改变止痛药物的给药途径以满足患者的持续止痛提供了一条新的解决办法[1]。
我院采用芬太尼透皮贴剂晚期癌痛患者获得一定疗效。
芬太尼为合成于1960年的苯基哌啶类衍生物,化学名称为N-[1-(2-苯乙基HYPERLINK"https:///lemma/ShowInnerLink.htmlemmaId=143922353&ss_c=ssc.citiao.link"\t"_blank")-4-哌啶基]-N-苯基-丙酰胺,本品属于阿片类镇痛药物。
透皮贴剂的研究进展与临床应用

透皮贴剂的研究进展与临床应用透皮贴剂是指通过贴于皮肤上,通过皮肤屏障直接输送药物到体内的一种药物给药途径。
与口服、注射等传统给药途径相比,透皮贴剂具有操作简便、剂量准确、缓释效果好、避免胃肠道刺激等优点,因此在临床上得到广泛应用。
1.药物输送技术的改进:透皮贴剂的核心是药物的输送技术,其目标是通过通过皮肤屏障将药物有效地输送到体内。
近年来,随着纳米技术的兴起,研究人员利用纳米级别的载体物质,如纳米粒子、纳米胶囊等,来增加药物在皮肤上的扩散能力,从而提高透皮吸收效果。
2.透皮输送的药物种类的扩展:传统透皮贴剂主要用于传输小分子药物,如镇痛剂、抗焦虑药等。
但随着研究的深入,越来越多的大分子药物,如胰岛素、生长激素等,也开始进入透皮贴剂的研究范围。
这些大分子药物的透皮输送挑战较大,需要更加精细的药物控制释放技术。
3.透皮贴剂的生物可用性研究:生物可用性是衡量药物在体内有效吸收的指标。
近年来,研究人员开始关注透皮贴剂的生物可用性,通过体外和体内实验研究药物在透皮贴剂中的释放和吸收过程,以及对体内组织的分布情况,从而进一步优化透皮贴剂的设计和制备。
透皮贴剂在临床上已经有了广泛的应用,下面以几个典型的透皮贴剂为例进行介绍:1.镇痛贴剂:透皮镇痛贴剂是常用的一种透皮贴剂,它通过皮肤屏障将镇痛药物输送到病人体内,用于缓解疼痛。
这种贴剂的优点是可以保持吸收药物的恒定浓度,从而提供长效的镇痛效果。
2.避孕贴:避孕贴是一种新型的透皮贴剂,它通过在皮肤上贴附含有雌激素和孕激素的贴片,以达到避孕的效果。
避孕贴相比口服避孕药具有使用方便、口服药物带来的副作用较少等优点。
3.尼古丁贴:尼古丁贴是一种用于戒烟的透皮贴剂,它通过皮肤屏障将尼古丁输送到体内,起到减轻烟草戒断症状的作用。
尼古丁贴的优点是通过缓慢释放尼古丁,可以帮助烟民逐步戒掉对尼古丁的依赖。
综上所述,透皮贴剂作为一种新型的药物给药途径,具有许多优点,同时在研究层面也取得了不少进展。
经皮给药系统-透皮贴剂研究进展

经皮给药系统-透皮贴剂研究进展药学2班万国运 2010071202【摘要】经皮给药系统(Transdermal Drug Delivery Systems,TDDS)或称经皮吸收制剂(Transdermal Thrapeutic Systems,TTS)是指经皮肤贴敷方式用药,药物由皮肤吸收进入全身血液循环并达到有效血药浓度、实现疾病治疗或预防的一类制剂。
常用的剂型为贴剂或贴片,还包括软膏剂、硬膏剂、涂剂和气雾剂等。
贴剂指可粘贴于皮肤的薄片层状制剂,包括皮肤局部传递和透皮传递的贴剂,药物透过皮肤吸收分别进入局部靶组织或全身循环系统产生治疗作用。
贴剂一般载药量较小 ,只适合于活性高 ,用量少的药物,具有延长作用时间,减少用药次数,用药方便,避免首过效应,减少胃肠道刺激的优点。
笔者通过查阅文献从透皮贴剂的研究历史、皮肤的构造、透皮贴剂的常用基质、贴剂种类,以及影响透皮吸收的因素及促进透皮吸收的方法等方面的研究进展做一综述。
【关键词】经皮给药;透皮贴剂;压敏胶;渗透促进剂;【前言】随着生物医药技术发展和生活水平的提高,人们对健康的关注逐渐加强,对医疗产品有了更高的要求,不但要求有良好的治疗效果,还要求最大限度的降低副作用和减轻治疗过程中病人的不适感。
另一方面,现代生物医药技术的发展促进了药物新剂型的出现,用口服或注射等常见方式给药,已不能充分发挥其治疗疾病的功效。
为了满足新的需求,经皮给药这一古老的给药方法以其独特的优势得到了医药工作者的关注,经皮给药可以使药物避免肝脏的首过效应和肠胃灭活,能够维持血液中药物浓度的稳定,提高药物利用率。
此外,经皮给药系统体积小巧,操作简单,具有良好的应用前景,因此,国内外对经皮给药的研究越来越广泛和深入。
透皮贴剂作为经皮给药制剂的一种,已广泛用于日常生活疾病的治疗,下文就透皮贴剂的相关研究做一简要概述。
1.研究历史经皮给药制剂的历史渊源[1]很早,在公元前1300年前的甲骨文就有中药经皮给药的记载。
透皮贴片市场分析报告

透皮贴片市场分析报告1.引言1.1 概述概述:透皮贴片是一种能够通过皮肤将药物逐渐释放到体内的贴片形式的药物制剂。
与传统的口服药物相比,透皮贴片具有更加便捷、减少肝脏代谢、降低胃肠道刺激等优点。
随着人们对健康意识的提高和医疗条件的改善,透皮贴片作为一种新型的药物给药方式,受到了越来越多人的关注和青睐。
本报告将对透皮贴片市场进行深入分析,探讨透皮贴片的定义、作用,以及市场现状和发展趋势,并展望其未来的发展前景,同时也分析透皮贴片在发展过程中面临的机遇与挑战。
希望通过本报告的分析,能够为相关行业提供有益的参考和指导。
文章结构部分内容如下:1.2 文章结构本报告共分为三个部分,分别是引言、正文和结论。
引言部分将对透皮贴片市场进行概述,并介绍本报告的目的和结构。
正文部分将分析透皮贴片的定义和作用,以及市场现状和发展趋势,为读者提供全面的市场分析。
结论部分将展望透皮贴片市场的前景,并探讨透皮贴片的发展机遇和挑战,最后对全文进行总结。
1.3 目的目的:本报告旨在对透皮贴片市场进行深入分析,以揭示其市场现状和发展趋势,为相关投资者和企业提供可靠的市场情报和决策参考。
通过对透皮贴片的定义和作用进行解释,结合市场现状分析和发展趋势预测,进一步展望未来透皮贴片市场的发展前景,探讨透皮贴片的发展机遇与挑战。
希望通过本报告的撰写,能够为相关行业提供有益的思考和指导,促进透皮贴片市场的健康发展。
1.4 总结本文对透皮贴片市场进行了深入分析,通过对透皮贴片的定义和作用进行说明,揭示了透皮贴片在医疗领域的重要地位。
同时,通过对透皮贴片市场现状的分析,我们了解到透皮贴片市场的规模和发展状况。
此外,我们还对透皮贴片市场的发展趋势进行了探讨,分析了未来透皮贴片市场的发展方向和机遇。
总的来说,透皮贴片市场具有巨大的潜力和发展空间,在未来将会迎来更加广阔的发展前景。
然而,我们也要清醒地认识到,透皮贴片市场面临着一些挑战和风险,需谨慎应对。
FDA透皮贴剂总结
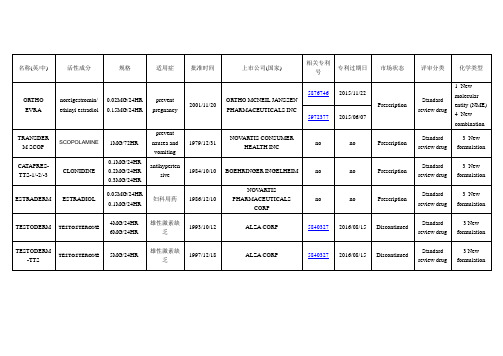
ESTRADIOL
0.0375MG/24HR
0.05MG/24HR
0.06MG/24HR
0.075MG/24HR0.025MG/24HR
0.1MG/24HR
Prevent cardiovascular disease
1994/12/22
BAYER HEALTHCARE PHARMACEUTICALS INC
NICOTINE
NICOTINE
14MG/24HR
21MG/24HR
7MG/24HR
1997/10/20
AVEVA
Over the counter
Standard review drug
3 New formulation
TRANSDERM-NITRO
NITROGLYCERIN
0.1MG/HR
0.2MG/HR
8OTC
(over-the-counter)switch
6098623
2010/06/08
ESTRADIOL
020538
ESTRADIOL
0.0375MG/24HR
0.75MG/24HR
0.05MG/24HR
0.1MG/24HR
NOVARTIS
Discontinued
Standard review drug
2003/11/21
BAYER HEALTHCARE PHARMACEUTICALS INC
5252334
2010/10/12
Prescription
Standard review drug
4 New combination
5393529
2012/02/28
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Discontinued
Standard review drug
3 New formulation
TESTODERM -TTS
TESTOSTERONE
5MG/24HR
雄性激素缺乏
1997/12/18
ALZA CORP
5840327
2016/08/15
Discontinued
Standard review drug
Standard review drug
3 New formulation
NICODERM CQ
NICOTINE
21MG/24HR
1991/11/07
SANOFI AVENTIS US
5508038
2013/04/16
Over the counter
Standard review drug
3 New formulation
0.1MG/24HR
1999/09/20
ORTHO MCNEIL PHARM
Discontinued
Standard review drug
3 New formulation
ESTRADIOL
075182
ESTRADIOL
0.0375MG/24HR
0.05MG/24HR
0.075MG/24HR0.025MG/24HR
名称(英/中)
活性成分
规格
适用症
批准时间
上市公司(国家)
相关专利号
专利过期日
市场状态
评审分类
化学类型
ORTHO EVRA
norelgestromin/
ethinyl estradiol
0.02MG/24HR
0.15MG/24HR
prevent pregnancy
2001/11/20
ORTHO MCNEIL JANSSEN PHARMACEUTICALS INC
Standard review drug
3 New formulation
5332576
2011/02/26
Prescription
46.1MG/PATC H
5446070
2011/02/27
ALORA
ESTRADIOL
0.075MG/24HR
0.025MG/24HR
0.05MG/24HR
0.1MG/24HR
FEMPATCH
ESTRADIOL
0.025MG/24HR
激素类用药
1996/12/03
PARKE DAVIS PHARMACEUTICAL RESEARCH DIV WARNER LAMBERT CO
no
no
Discontinued
Standard review drug
3 New formulation
5474783
2012/12/22
Prescription
Standard review drug
5 New manufacturer
5656286
2014/08/12
5958446
2012/12/22
6024976
2014/01/07
ESTRADIOL
ESTRADIOL
0.075MG/24HR0.05MG/24HR
ANDRODERM
TESTOSTERONE
2.5MG/24HR
5MG/24HR
testosterone deficiency
1995/09/29
WATSON LABORATORIES INC
4855294
2008/09/06
Prescription
Standard review drug
3 New formulation
NOVARTIS PHARMACEUTICALS CORP
no
no
Prescription
Standard review drug
3 New formulation
TESTODERM
TEST24HR
雄性激素缺乏
1993/10/12
ALZA CORP
5840327
赛诺菲-安万特
5508038
2013/04/16
Over-the
-counter
Standard review drug
3 New formulation
VIVELLE
ESTRADIOL
0.0375MG/24HR
0.075MG/24HR0.025MG/24HR
Prevent cardiovascular disease
妇科用药
1996/12/20
WATSON LABORATORIES INC
5122383
KEY PHARMACEUTICALS INC SUB SCHERING PLOUGH CORP
5186938
2010/02/16
Prescription
NICODERM CQ
NICOTINE
7MG/24HR
14MG/24HR
21MG/24HR
Stop
Smoking aid
1991/11/07
SANOFI AVENTIS US LLC
5152997
2010/12/11
5164190
2010/12/11
NICOTROL
NICOTINE
15MG/16HR
Prevent smoking aid
1996/03/22
MCNEIL CONSUMER HEALTHCARE强生旗下
5501236
2010/06/08
Discontinued
Standard review drug
Standard review drug
3 New formulation
HABITROL
NICOTINE
7MG/24HR
14MG/24HR
21MG/24HR
Stop smoking aid
1999/11/12
NOVARTIS CONSUMER HEALTH INC
no
no
Over the counter
antihypertensive
1984/10/10
BOEHRINGER INGELHEIM
no
no
Prescription
Standard review drug
3 New formulation
ESTRADERM
ESTRADIOL
0.05MG/24HR 0.1MG/24HR
妇科用药
1986/12/10
0.4MG/HR
0.6MG/HR
0.8MG/HR
抗心绞痛
1996/02/27
NOVARTIS PHARMACEUTICALS CORP
no
no
Discontinued
NITRO-DUR
NITROGLYCERIN
0.1MG/HR
0.2MG/HR
0.4MG/HR
0.6MG/HR
0.8MG/HR
抗心绞痛
1995/04/04
2010/10/12
CLIMARA PRO
ESTRADIOL;LEVONORGESTREL
0.045MG
Prevent cardiovascular disease or dementia
2005/12/27
BERLEX LABS
Prescription
Standard review drug
6 New indication
0.0375MG/24HR
0.05MG/24HR
0.075MG/24HR0.025MG/24HR
0.1MG/24HR
Prevent cardiovascular disease
1996/07/31
NOVARTIS
Prescription
Standard review drug
5 New manufacturer
1994/10/28
NOVARTIS PHARMACEUTICALS CORP
5300291
2011/04/05
Discontinued
Standard review drug
3 New formulation
0.05MG/24HR
0.1MG/24HR
Prescription
VIVELLE
-DOT
ESTRADIOL
阿维发药物释放系统公司
no
no
Over the counter
Standard review drug
3 New formulation
HABITROL
NICOTINE
7MG/24HR
14MG/24HR
21MG/24HR
Stop smoking aid
1991/11/27
NOVARTIS
no
no
Discontinued
1992/1/28
AVEVA
no
no
Discontinued
Standard review drug
3 New formulation
PROSTEP
NICOTINE
11MG/24HR
22MG/24HR
Stop smoking aid
1998/12/23
AVEVA DRUG DELIVERY SYSTEMS INC
NICOTINE
NICOTINE
14MG/24HR
21MG/24HR
7MG/24HR
1997/10/20
