食品中有机锡含量的测定
氢化物原子荧光光谱法测定食品中的锡

氢化物原子荧光光谱法测定食品中的锡发表时间:2018-03-14T13:13:47.550Z 来源:《防护工程》2017年第31期作者:王志红[导读] 自1810年罐头食品问世以来,罐头生产已经成为现代食品工艺中的一大支柱工业。
如皋市综合检验检测中心江苏南通 226500 摘要:自1810年罐头食品问世以来,罐头生产已经成为现代食品工艺中的一大支柱工业,罐头食品也已成为各国人民日常生活中的必需品?但由于罐头食品的包装容器一般为镀锡金属罐,罐装食物接触镀锡层会导致锡的溶出,而锡对人体有毒副作用,尤其是有机锡毒性较大?国家标准方法测定锡常用原子荧光光谱法,样品前处理方法为湿法消解,该方法酸用量大?环境污染严重,且待测元素易污染或损失?微波消解在密封状态下进行,待测元素不易污染或损失,试剂用量小,废酸?废气排放量少,已有微波消解原子荧光光谱法测定锡的报道,但均单独采用微波消解,未见与其它方法进行结合处理?为避免样品消解不充分,同时也为消除试样酸度差异对锡测定的影响,本工作以硫酸辅助微波消解处理样品,采用氢化物发生-原子荧光光谱法测定罐头食品中锡含量? 关键词:微波消解;原子荧光;罐头食品;锡对于测定食品中锡的前处理,国家标准方法中采用湿式消解法,该法由于敞开?耗时长?酸的用量大,易导致锡的损失和实验室环境污染,危害操作者的健康,而且高氯酸为易爆物,易产生安全事故?微波消解技术是近年发展起来极有前景的样品预处理技术,与前法相比,具有操作简便快速?试剂用量少?样品消解彻底?待测元素损失少?安全环保等突出优点?笔者将微波消解技术与氢化物原子荧光光谱技术相结合测定罐头食品中锡,同时对不同酸体系进行微波消解前处理样品的效果?赶酸程序对分析结果的影响以及氢化物原子荧光光谱法测定锡的仪器条件和各参数进行研究并优化,取得满意效果,现介绍如下?一、材料与方法(一)仪器与试剂 AFS-230E型双道原子荧光分光光度计;MARS微波消解系统;锡空心阴极灯;屏蔽气和载气均为高纯氩气?本法所用试剂由18.2MΩ超纯水配制,所用玻璃器皿皆用10%的硝酸溶液浸泡12h以上,硝酸?盐酸?硫酸均为优级纯,其余试剂为分析纯?氢氧化钾溶液2g/L;硼氢化钾(KBH4)溶液10g/L;硫脲(100g/L)+抗坏血酸(100g/L)混合液;载流为2%的硫酸溶液?锡标准应用溶液(100μg/L):将锡标准贮备液(质量浓度为100μg/mL,购买于国家标准物质中心,编号为GBW(E)080546,以2%的硫酸溶液逐级稀释而成?(二)样品消解准确称取匀浆试样约0.5g于消解罐内,对于易消解的果蔬罐头食品加入8.0mL硝酸,对于油脂丰富的鱼肉罐头食品则加入6.0mL硝酸?2.0mL盐酸溶液混匀,拧紧盖子放置过夜?然后按如下表1消解程序行进样品消解处理?待微波消解仪停止工作后,小心解压,打开消解罐,缓慢加入1.0mL浓硫酸,置于130℃的精确控温电热消解器上加热赶酸至体积剩余2~3mL即取出冷却,将消解液转移至25mL比色管中,纯水定容至25mL?分别取溶液5.0mL于10mL比色管中,加入硫脲+抗坏血酸混合液,纯水至刻度,摇匀放置15min后上机测定?同时做双份空白试验?(三)仪器工作条件光电倍增管负高压:280V;灯主电流60mA,辅电流30mA;原子化器高度:8mm;载气流量:300mL/min;屏蔽气流量:600mL/min;积分方式:峰面积;延迟时间:0.5s;读数时间:7s?(四)标准曲线的绘制手动配制锡标准系列,浓度为10?20?40?80?100μg/L,上机测定相应的荧光值,制作标准曲线?二、结果与讨论(一)微波消解条件的选择 1.微波消解酸体系的选择硫酸的沸点高,在密闭的消解罐中易产生高热,因而对消解罐的耐热性要求高,应尽可能少用?硝酸是一种强氧化性酸,是最常用于消解过程的酸?盐酸是非氧化性酸,有弱还原性,它可以溶解许多金属,并且通过加入其他的酸可以加快溶解的速度?过氧化氢通常与酸混合使用,可以在有机物预消解后再加入避免激烈反应?综合考虑后本文选用了硝酸?硝酸-盐酸2种体系来消化样品?实验结果表明,对于易消解的果蔬罐头,2种消解体系的消解效果都良好,消解液都呈澄清状态?而对于油脂丰富的鱼肉罐头食品用硝酸消化后样品仍呈较浑浊状态,只有采用硝酸-盐酸混合体系才可得到澄清的样品消化液?为避免样品在加酸后反应过于剧烈,可采取放置过夜预消化,再进行微波加热?2.微波消解预处理样品后,后续的赶酸程序也相当关键?除根据待测元素的性质选择不同的加热温度外,还要注意赶酸的程度?赶酸不彻底酸度太高对后续的分析有影响,过分彻底(即所剩溶液体积太少),待测元素会挥发损失,致使分析结果偏低,甚至不能检出?笔者发现在测定锡时此现象特别明显,这是由于锡发生氢化反应要求的酸度范围窄,而且它具有易溶于浓酸,微溶于稀酸,难溶于水的性质所导致的结果?为了解决此问题,本研究采用在微波消解处理样品后,先加入难挥发的浓硫酸1.0mL,再置于130℃的精确控温电热消解器上进行加热,经多次试验表明,以最终消解液体积剩余2~3mL时,赶酸程度达到最佳?现以易消解的椰汁罐头为样品,称样0.50g加1.0μg锡标准液,按表1中的微波消解程序操作,以不同的混合体系消解?赶酸程序预处理样品,每一序号样品均作6次平行测定,进行准确度和精密度比对试验,结果见表2?从表2中可见,以6.0mLHNO3+2mLHCl混合体系消解,加1.0mL浓硫酸后再作赶酸处理,其准确度最好,精密度最高?(二)氢化物发生反应条件的选择试验在最佳仪器条件下,测定相同质量浓度的锡标准液(50μg/L)的荧光值?1.酸的种类和酸度的选择氢化物发生需要适当的酸度,硫酸?盐酸均可采用?本试验分别选择硫酸?盐酸作载流,酸度范围在0.5%~6%之间测定荧光值,结果见图1?图1氢化物原子荧光光谱法中酸度对荧光强度的影响由图1可见,两种酸作介质产生荧光的效果相当,试验中虽然两种酸的酸度为1%时产生荧光值都高于其它酸含量,但在此酸度下,锡质量浓度在0~100μg/L的标准曲线线性差,相关系数难以达到0.9990,而酸度为2%时,线性关系良好,相关系数大于0.9995,灵敏度也能符合分析要求(方法最低检出限0.059mg/kg),综合考虑最终试验选择2%的硫酸溶液作为载流和溶液介质?2.硼氢化钾含量的选择硼氢化钾是产生原子态锡的强还原剂,其含量大小直接影响到荧光强度,如果硼氢化钾用量不足还原不完全,导致结果偏低;用量过大,产生过量的氢气使氢化物稀释,导致灵敏度下降?由于硼氢化钾的不稳定性,需要配制在一定质量浓度的氢氧化钾溶液中,经试验选择2g/L的氢氧化钾溶液为稳定剂较合适?其他条件不变,使硼氢化钾质量浓度在5~25g/L范围内测定荧光值,硼氢化钾质量浓度在一定范围内,随质量浓度增大荧光值升高,质量浓度达10g/L时荧光值基本恒定,故还原剂质量浓度选择为10g/L?(三)仪器参数的选择1.灯电流的选择增大灯电流强度,荧光信号会增强,可提高方法的灵敏度,但灯电流过大会发生自吸现象,致使噪声过大,而且会大大缩短灯的使用寿命?通过实验,综合考虑灵敏度?灯的使用寿命并结合实际工作的需要,选择锡灯在主电流60mA?辅电流30mA时,可得到满意的检测结果?2.原子化器高度的选择原子化器高度与待测元素的原子化效率有关?原子化器高度过低时,光源射到炉口所引起的反射光过强,会降低荧光强度,灵敏度低;原子化器过高时,背景噪音过大,灵敏度和测定精密度均会下降?试验表明测定锡的理想高度为8mm?3.载气与屏蔽气流量的选择载气流量大小对氩氢火焰的稳定性与产的荧光强度都有密切关系?载气流量过小氩氢火焰不稳定,测量的重复性差;流量过大时,锡的氢化物被稀释致使灵敏度降低?经试验载气流量选择300mL/min,屏蔽气流量选择600mL/min,测定效果最佳?4.标准曲线线性范围及检出限在本实验条件下,对标准曲线的线性进行测定,锡质量浓度在0~100μg/L的范围内,标准曲线线性方程为1=16.2081×C+5.8154,其相关系数为0.9996?根据本仪器给定的检出限测定程序,连续11次测定空白溶液的荧光信号,自动计算出仪器的检出限为0.5946μg/L,根据取样量0.5g,定容体积为25mL,再2倍稀释测定,得方法最低检测质量分数为0.059mg/kg。
食品中锡的测定作业指导书

食品中锡的测定GB/T5009.16-20031、范围本标准规定了食品中锡的测定方法。
本标准适用于各类食品中锡的测定。
本方法检出限:氢化物原子荧光光谱检出限:0.23 ng/mL,标准曲线线性范围:0ng/mL~200ng/mL。
2、原理试样经酸加热消化,锡被氧化成四价锡,在硼氢化钠的作用下生成锡的氧化物,并由载气带入原子化气中进行原子化,在特制锡空心阴极灯的照射下,基态锡原子被激发至高能态,在去活化回到基态时,发射出特征波长的荧光,其荧光强度与锡的含量成正比。
与标准系列比较定量。
3、试剂3.1 硝酸+高氯酸混合酸(4+1)。
3.2 硫酸溶液(1+9):量取100mL硫酸倒入900mL水中混匀。
3.3 硫脲(150g/L)+ 抗坏血酸(105g/L):分别称取15g硫脲和15g抗坏血酸溶于水中,并稀释至100mL(此溶液需置于棕色瓶中避光保存)。
3.4 硼氢化钠溶液(7g/L):称取7.0g硼氢化钠,溶于氢氧化钠溶液(5g/L)中,并定容至1000mL.3.5 锡标准应用液:准确吸取100μg/mL锡国家标准溶液(标准号:BW 3035)1.0 m/L于100mL容量瓶中,用硫酸溶液(1+9)定容至刻度。
此溶液浓度为1μg/mL。
4、仪器双道原子荧光光度计、电热板。
5、分析步骤5.1 试样制备将肉罐头磨成匀浆备用5.2 试样消化5.2.1 称取式样1.0g~5.0g于锥形瓶中,加1.0mL浓硫酸,10.0mL硝酸+高氯酸混合酸(4+1),3粒玻璃珠,放置过夜。
次日置电热板上加热消化,如酸液过少,可适当不加硝酸,继续消化至冒白烟,待液体体积近1mL时取下冷却。
用水将消化试样转入50mL容量瓶中,加水定容至刻度,摇匀备用。
同时做空白试验。
5.2.2 分别取定容后试样10mL于15mL比色管中,加入2mL硫脲(150g/L)+抗坏血酸(150g/L)混合溶液,摇匀。
5.3 标准曲线的配制标准曲线:分别吸取锡标准应用液0.0、0.1、0.5、1.0、1.5、2.0mL ,于15mL 比色管中,分别加入硫酸溶液(1+9)2.0、1.9、1.5、1.0、0.5、0.0mL ,用水定容至10mL ,再加入2mL 硫脲(150g/L )+抗坏血酸(150g/L )混合溶液。
MM FS CNG 食品中锡的测定方法

MMFSCNG0157 食品 锡 分光光度法MM_FS_CNG_0157食品中锡的测定方法1.适用范围本方法适用于食品中锡的测定。
最低检出浓度:为2mg/kg。
2.原理概要样品经消化后,在弱酸性溶液中四价锡离子与苯芴酮形成微溶性橙红色络合 物,在保护性胶体存在下与标准系列比较定量。
3.主要仪器和试剂3.1.主要试剂酒石酸溶液(100g/L)、氨水(1+1)。
抗坏血酸溶液(10g/L)、动物胶溶液(5g/L),临用时配制。
酚酞指示液(10g/L):称取1g酚酞,用乙醇溶解至100mL。
硫酸(1+9):量取10mL硫酸,倒入90mL水内,混匀。
苯芴酮溶液(0.1g/L):称取0.010g苯芴酮,加少量甲醇及硫酸(1+9)数滴溶解,以甲醇稀释至100mL。
锡标准溶液:准确称取0.1000g金属锡(99.99%),置于小烧杯中,加10mL硫酸,盖以表面皿,加热至锡完全溶解,移去表面皿,继续加热至发生浓白烟,冷却,慢慢加50mL水,移入100mL容量瓶中,用硫酸(1+9)多次洗涤烧杯,洗液并入容量瓶中定容,混匀。
此溶液每毫升相当于1.0mg锡。
锡标准使用液:吸取10.0mL锡标准溶液,置于100mL容量瓶中,以硫酸(1+9)稀释至刻度,混匀。
如此再次稀释至每毫升相当于10.0μg锡。
3.2.仪器分光光度计。
4.过程简述4.1.样品消化4.1.1.粮食、粉丝、粉条、豆干制品、糕点、茶叶等及其他含水分少的固体食品:称取5.00g或10.00g的粉碎样品,置于250~500mL定氮瓶中,先加水少许使湿润,加数粒玻璃珠、10~15mL硝酸液,放置片刻,小火缓缓加热,待作用缓和,放冷。
沿瓶壁加入5mL或10mL硫酸,再加热,至瓶中液体开始变成棕色时,不断沿瓶壁滴加硝酸溶液至有机质分解完全。
加大火力,至产生白烟,待瓶口白烟冒净后,瓶内液体再产生白烟为消化完全,该溶液应澄明无色或微带黄色,放冷。
在操作过程中应注意防止爆沸或爆炸。
食品中锡的测定..

第一法 氢化物原子荧光光谱法
2 原理
试样经消化后,在硼氢化钠的作用下生成锡的氢化物(SnH4), 并由载气带入原子化器中进行原子化,在锡空心阴极灯的照射下,基 态锡原子被激发至高能态,在去活化回到基态时,发射出特征波长的 荧光,其荧光强度与锡含量成正比,与标准系列溶液比较定量。
3 试剂和材料
注:除特别注明外,本方法所使用试剂均为分析纯,水为GB/T6 682规定的二级水。
食品安全国家标准 食品中锡的测定 (GB5009.16-2014
前 言
本标准代替GB/T5009.16—2003《食品中锡的 测定》。 本标准与GB/T5009.16—2003相比,主要变化如下: ———标准名称修改为“食品安全国家标准 食品中锡的测定”; ———修改了标准溶液配制; ———增加了罐头食品的试样制备方法; ———修改了仪器测定部分的描述; ———增加了方法定量限; ———修改了方法检出限; ———修改了计算公式。
5.5
仪器测定
按照5.3设定好仪器测量最佳条件,根据所用仪器的型 号和工作站设置相应的参数,点火及对仪器 进行预热,预热30min后进行标准曲线及试样溶液的 测定。
食品中有机锡农药残留及重金属含量测定

第一作者E-mail:***************收稿日期:2020-04-171前言比重大于5的金属被称为重金属。
人们了解的重金属大部分具有毒性,如铅(Pb)、铬(Cr)、汞(Hg)等重金属,生物毒性明显;镍(Ni)、钴(Co)、锌(Zn)、铜(Cu)等,具有一定毒性;砷(As)不属于重金属,但其危害性与重金属高度相似,因此也归属于重金属范畴[1,2]。
2重金属的危害As:以“砒霜”为人们熟知,毒性极强,也是当前公认的致癌物,可引起肾癌、膀胱癌、肺癌以及皮肤癌。
锡(Sn):吸入过多会引起口干舌燥、呼吸困难、胸闷、腹泻、恶心、头晕等症状,还会降低血钙含量,症状严重时会引起肠胃炎。
Sn 中毒会对患者的肝脏功能与神经系统造成严重损害。
钒(V):对人的呼吸道、咽、鼻、眼均具有刺激,容易引起咳嗽,还会与钙(Ca)竞争,降低血钙含量。
V 经吸收后可进入全身,累及心脏、肠胃以及神经系统等。
Ni:硬度高,耐碱、酸,流行病学发现,Ni 化合物是引起Ni 冶炼工人肺癌、鼻癌的重要原因。
Co:Co 的同位素中,除了59Co 是稳定同位素无放射性以外,其余的4种同位素均具有放射性。
60Co 的辐射性极强,对血液细胞组织损害极大,会造成白细胞计数降低,引发血液系统疾病,严重时罹患白血病。
Cr:毒性与价态关系密切,Cr 6+极易被人体吸收,其毒性是Cr 3+的100倍。
Cr 6+可通过黏膜、呼吸道、皮肤、消化等进入人体。
由消化道侵入时,常引起腹痛、呕吐;经呼吸道侵入可引起支气管炎、咽炎、鼻炎等;经皮肤侵入常引起湿疹、皮炎等。
Cr 6+还有致突变、致癌、致畸的危害。
Hg:俗名水银,容易转化为甲基汞(CH 3Hg),CH 3Hg 毒性极强,进入人体会侵犯神经系统,导致动作迟缓、肌肉震颤、手脚麻木、头晕头痛等。
Hg 中毒可引起尿毒症、血尿、肝炎以及肾炎。
Pb:对骨骼造血功能、男性生殖系统、消化系统以及神经系统均有危害。
3食品有机锡农药残留的测定3.1背景三唑锡(C 20H 35N 3Sn)与毒菌锡(C 18H 16OSn)都是广泛使用的有机锡农药。
原子荧光双标准比较法快速测定食品中的锡

原子荧光双标准比较法快速测定食品中的锡徐雅莉(河南蓝呈检测技术有限公司,河南郑州 450000)摘 要:为建立一种快速测定食品中锡的方法,以豆豉鱼罐头、黄桃罐头和真空包装鸡为样品,湿法消解后,用原子荧光双标准比较法与标准曲线法对照测定。
结果表明,锡的检出限为0.17 µg/L,相对标准偏差0.55%~1.5%,回收率为104.00%~104.14%。
该法与国家标准方法相比,无需绘制标准曲线、不用测定空白溶液,快速简便、成本较低,工作效率得到较大提高,为食品中锡的测定提供了一种新型的分析技术,有一定的创新性和推广应用价值。
关键词:锡;原子荧光;双标准比较法Rapid Determination of Tin in Food by Atomic Fluorescence Double Standard Comparison MethodXU Yali(Henan Lancheng Detection Technology Co., Ltd., Zhengzhou 450000, China) Abstract: To establish a method for quickly measuring tin in food, by using canned tempeh fish, canned yellow peach and vacuum packaged chicken as samples, the double standard comparison method of atomic fluorescence and the standard curve method were used.The results showed that the detection limit of tin was 0.17 g/L, with a relative standard deviation of 0.55% to 1.5%, and a recovery rate of 104.00% to 104.14%.Compared with the national standard method, this method does not need to draw a standard curve or determine a blank solution, which is fast and simple, with low cost, and the work efficiency is greatly improved, which provides a new analysis technology for the determination of tin in food, and has certain innovation and popularization and application value.Keywords: tin; atomic fluorescence; double standard comparison method锡是人体必需微量元素,能促进合成蛋白质和核酸,参与黄素酶的生物反应,增强体内环境的稳定性并抑制癌细胞的生成[1]。
实验八 罐头食品中锡含量的测定
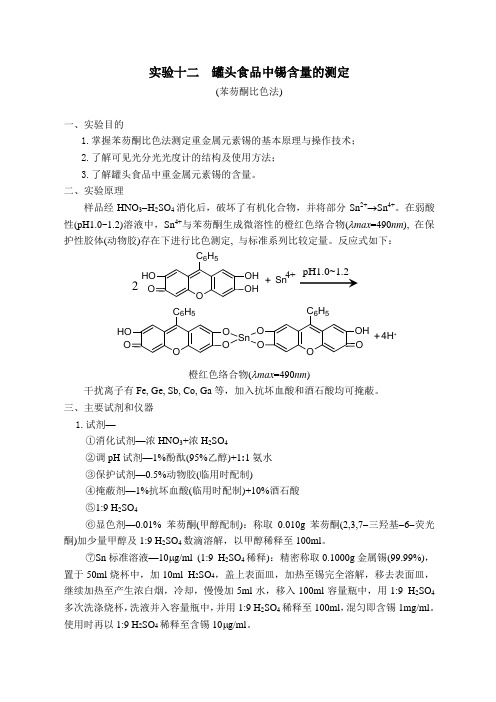
实验十二 罐头食品中锡含量的测定(苯芴酮比色法)一、实验目的1.掌握苯芴酮比色法测定重金属元素锡的基本原理与操作技术;2.了解可见光分光光度计的结构及使用方法;3.了解罐头食品中重金属元素锡的含量。
二、实验原理样品经HNO 3-H 2SO 4消化后,破坏了有机化合物,并将部分Sn 2+→Sn 4+。
在弱酸性(pH1.0~1.2)溶液中,Sn 4+与苯芴酮生成微溶性的橙红色络合物(λmax =490nm ), 在保护性胶体(动物胶)存在下进行比色测定, 与标准系列比较定量。
反应式如下:橙红色络合物(λmax =490nm )干扰离子有Fe, Ge, Sb, Co, Ga 等,加入抗坏血酸和酒石酸均可掩蔽。
三、主要试剂和仪器1.试剂—①消化试剂—浓HNO 3+浓H 2SO 4②调pH 试剂—1%酚酞(95%乙醇)+1:1氨水③保护试剂—0.5%动物胶(临用时配制)④掩蔽剂—1%抗坏血酸(临用时配制)+10%酒石酸⑤1:9 H 2SO 4⑥显色剂—0.01% 苯芴酮(甲醇配制):称取0.010g 苯芴酮(2,3,7-三羟基-6-荧光酮)加少量甲醇及1:9 H 2SO 4数滴溶解,以甲醇稀释至100ml 。
⑦Sn 标准溶液—10μg/ml (1:9 H 2SO 4稀释):精密称取0.1000g 金属锡(99.99%),置于50ml 烧杯中,加10ml H 2SO 4,盖上表面皿,加热至锡完全溶解,移去表面皿,继续加热至产生浓白烟,冷却,慢慢加5ml 水,移入100ml 容量瓶中,用1:9 H 2SO 4多次洗涤烧杯,洗液并入容量瓶中,并用1:9 H 2SO 4稀释至100ml ,混匀即含锡1mg/ml 。
使用时再以1:9 H 2SO 4稀释至含锡10μg/ml 。
O C 6H 5OH OH O H O +Sn 2 4+ pH1.0~1.2 Sn O C 6H 5O O O H O OC 6H 5O O OH O +4H +2.仪器—①可见光分光度计②具塞比色管,50ml③容量瓶及K 氏烧瓶等常规玻璃器皿四、测定方法—1.样品处理①将样品捣碎并搅拌均匀,称取适量样品 (5.00 g )入250~500mlK 氏烧瓶。
实验 苯芴酮比色法测定食品中的锡含量

实验六罐头食品中锡含量的测定——苯芴酮比色法(本法参照GB/T 5009·16-2003)――蘑菇罐头一、原理在强酸条件下,使食品中的C、H、O、S等非欲测组分完全氧化,并以气(汽)态逸出,重金属元素形成高价态的离子以游离状态存在于消化液中。
样品经消化后,在弱酸介质中四价锡离子与苯芴酮生成微溶性橙红色络合物,在保护性胶体存在下,溶解的橙红色络合物的浓度与锡的含量成正比(即反应液颜色的深浅与锡的含量成正比),因而可用比色法测定。
加入抗坏血酸(Vc),酒石酸作为掩蔽剂,可消除铁的干扰。
显色反应式:二、样品、试剂和仪器(一)样品品名:厂家:(二)试剂1.消化试剂:浓硫酸浓硝酸2.10%酒石酸溶液。
每组配40ml50ml/2组3.1%抗坏血酸溶液,临用时配制。
每二组配50ml4.0.5%动物胶溶液,临用时配制。
每二组配40ml。
配制动物胶溶液,应加热搅拌,防止糊底。
5.酚酞指示液:1%乙醇溶液。
6.1:1氨水。
7.1:9硫酸:量取10ml硫酸,倒入90ml水内,混匀。
每二组配200ml8.0.01%苯芴酮溶液:称取0.010g苯芴酮(1,3,7-三羟基-9-苯基蒽醌)加少量甲醇及1:9硫酸数滴溶解,以甲醇稀释至100ml。
9.锡标准溶液: 精密称取0.1000g金属锡(99.99%),置于小烧杯中,加10ml硫酸,盖以表面皿,加热至锡完全溶解,移去表面皿,继续加热至发生浓白烟,冷却,慢慢加50ml 水,移入100ml容量瓶中,用1:9硫酸多次洗涤烧杯,洗液并入容量瓶中,并稀释至刻度,混匀。
此溶液每毫升相当于1mg锡。
10.锡标准使用液: 吸取10.0ml锡标准溶液,置于100ml容量瓶中,以1:9硫酸稀释至刻度,混匀。
如此再次稀释至每毫升相当于10μg锡。
(已配完,公用)(三)仪器分光光度计。
三、测定步骤1.试样消化称取5.00~10.00g捣碎试样于小烧杯中,用10ml硝酸将样品移入250~500mL凯氏烧瓶中,加数粒玻璃珠,放置片刻后,小火缓缓加热,待作用缓和,放冷。
食品分析中汞和锡的测定

双硫腙的结构式:
蓝黑色结晶性粉末,易被空气氧化,可加 入二氧化硫水溶液保护;易溶于四氯化碳 和氯仿,其溶液不稳定,微溶于乙醇,不 溶于水
原理:
样品经消化后,汞离子在酸性溶液 中可与双硫腙生成橙色络合物,溶于三 氯甲烷,与标准系列比较定量。
试剂
硝酸 硫酸
氨水
三氯甲烷(不应含有氧化物) 硫酸(1:35):量取5mL硫酸,缓缓倒入150mL水中,冷后加水至180mL
锡标准使用液的配制
准确称取0.1g金属锡(99.99%)置于小烧杯中, 加10mL硫酸,盖以表面皿,加热至锡完全溶解,移去 表面皿,继续加热至发生浓白烟,冷却,慢慢加入 50mL水,,移入100mL容量瓶中,,用硫酸(1:9)多 次洗涤烧杯,洗液并入容量瓶中,并稀释至刻度,混 匀。此溶液相当于每毫升1.0mg锡。
汞含量的测定——双硫腙比色法 锡含量的测定——氢化物原子荧 光光谱法
汞含量的测定—双硫腙比色法
汞俗称水银,为银白色液态金属,汞易蒸发,在空 气中以蒸气状态存在。汞的化合物能溶于水或稀酸, 毒性很大。常见的汞化物有氯化高汞、氧化汞、硝酸 汞、碘化汞等,均属于烈性毒物。汞的化合物在工农 业和医药等方面应用极广,极容易造成环境污染。环 境中的微生物能使无机汞转化为有机汞,如甲基汞、 二甲基汞等烷基汞化合物其毒性更大,所以不慎混入 食品或误食或食用污染了汞的食品而引起中毒的事件 较为多见。
准确称取0.1355)使其溶解后,移入100mL容 量瓶中,并稀释至刻度,此溶液每毫升相当于 1.0mg汞。
汞标准使用液的配制
吸取1.0mL汞标准溶液,置于100mL容量瓶 中,加硫酸(1:35)稀释至刻度,此溶液每毫 升相当于10.0ug汞。再吸取此液5.0mL置于 50mL容量瓶中,加硫酸(1:35)稀释至刻度, 此溶液每毫升相当于1.0ug汞。
有机锡的检测方法

有机锡的检测方法我折腾了好久有机锡的检测方法,总算找到点门道。
我一开始真是瞎摸索,就知道有机锡这东西挺难搞的。
最开始我按照一般金属检测那套来试,那就是大错特错了。
我想着都是金属嘛,就用那些检测常见金属元素的试剂,结果啥都没检测出来,感觉自己特别蠢。
后来呢,我就上网查资料,看到有说到气相色谱法。
这个气相色谱听起来就特别高大上。
我就想去实验室试一下。
这就好比要在一个大迷宫里找东西一样,气相色谱仪就是我的地图。
不过这个方法可难了,首先,样品的制备就特别讲究。
要把样品处理得特别干净,得像洗特别珍贵的宝石一样仔细,不能有一点杂质,不然就会干扰结果。
在准备样品的时候,我可出了不少错。
有一回忘记把样品里别的有机物除掉了,结果那个色谱峰啊,乱得像一团麻,根本没法看。
后来我就知道了,在做有机锡检测的样品准备工作时,一定要把有机锡从各种其他物质中分离出来。
我是这样做的,先用有机溶剂萃取,就像从混合果汁里把一种特定的水果挑出来一样,然后再经过一些消化处理。
还有一回,我尝试用液相色谱法检测有机锡,感觉这个方法也许会更简单一点,毕竟我之前对液相色谱的操作比较熟。
但是我又错了,液相色谱法对于有机锡检测来说,灵敏度不够。
就好比你用小铲子去挖宝藏,但是宝藏埋得太深了,小铲子根本挖不到,液相色谱就这么不给力。
我还没有试过原子吸收光谱法,我也不确定这个方法可不可以用来检测有机锡。
不过我倒是知道有一些其他的研究人员会用一些特殊的探测器,结合一些特定的化学反应来检测,就像钓鱼一样,用特定的鱼饵去钓特定的鱼,比如用一些对有机锡有特定吸附性能的材料,让有机锡分子都聚集到上面然后再检测,这个听起来很不错,我正打算去试试。
我现在觉得啊,检测有机锡一定要多尝试几种方法,每个方法就像不同的工具一样,总有一把适合打开这个检测谜题的锁。
另外检测之前样本的处理是重中之重,这就像要搭一个稳固的地基才能盖高楼一样,要是地基不稳,那检测结果肯定好不了。
石墨炉法测定罐头食品中锡

石墨炉法测定罐头食品中锡作者:李谦来源:《现代食品》 2019年第19期李?谦1,2(1.宁夏回族自治区食品检测研究院,宁夏?银川?750000;2.国家农副加工产品质量监督检验中心(宁夏),宁夏?银川?750000)Li?Qian1,2(1.Ningxia Hui Autonomous Region Food Inspection and Research Institute, China National Quality Supervision, Yinchuan?750000, China;2.Inspection Center for Processed Agricultural Products, Yinchuan?750000, China)摘?要:本文建立了一种石墨炉原子吸收法测定罐头食品中锡含量的方法,分别从标准溶液的酸度、石墨炉原子吸收的灰化温度以及原子化温度三方面进行优化,最终确立锡元素的石墨炉原子吸收测定条件。
结果表明,在0~100 ng·mL-1的浓度范围内,锡元素相关系数R为0.999 3。
采买市场上6种品牌马口铁罐装食品进行测定,其锡含量的范围为0.56~27.5 mg·kg-1,远远低于GB 2762-2017《食品安全国家标准食品中污染物限量》中规定镀锡薄板容器包装的食品中锡≤250 mg·kg-1,可以放心食用。
测定检出限为0.57 mg·kg-1,定量限为1.71 mg·k g-1。
同时做添加标准品实验,测定回收率分别在94%~108%,符合国家标准要求。
该方法准确可靠,值得推广。
关键词:石墨炉法;罐头食品;锡Abstract:A method for determination of tin in canned food by graphite furnace atomic absorption spectrometry was developed. The experiments were optimized from the acidity of standard solution, the ashing temperature of graphite furnace atomic absorption and the atomization temperature, and finally the determinationconditions of tin in graphite furnace atomic absorption were established. The concentration range of standard curve of tin element is 0~100 ng·mL-1 , and the linear correlation coefficient is R=0.999 3. Six shopping market brand tin canned food, determination of the content of tin content in the range 0.56~27.5 mg·kg-1, far below the GB 2762-2017 ‘national food safe ty standards specified in thelimitedcontamination in food’ tin plate container to pack the food in the 250 mg·kg-1 or less,it is safe to eat. The detection limit was 0.57 mg·kg-1, thequantitative limit is 1.71 mg·kg-1. At the same time, experiments were conductedto add standard substances, and the recovery rates were 94%~108%, which fully met the requirements of national standard. The method is accurate, reliable and worthy.Key words:Graphite furnace method; Tin food; Sn中图分类号:O657.31罐头包装材料中涂有锡层,可能会溶解到罐头食品中。
进出口食品中有机锡类农药残留量的测定编制说明

中华人民共和国出入境检验检疫局行业标准《进出口食品中有机锡类农药残留量的测定》编制说明一、任务来源本标准是按照国家认证认可监督管理委员会2012年下达的行业标准制修订计划―《进出口食品中有机锡类农药残留量的测定》(计划编号2012B324r)而制定的,本标准整合替代行业标准SN 0150-1992和SN/T 1990-2007。
本标准由国家认证认可监督管理委员会提出并归口,由秦皇岛出入境检验检疫局承担研究和起草工作。
二、编制依据本标准是按照GB/T 《标准化工作导则第1部分:标准的结构和编写的规则》、GB/T 《标准编写规则第4部分:化学分析方法》和最新修订的行业标准SN/T 0001-XXXX《出口食品化妆品理化测定方法标准的基本规定》(以下简称《基本规定》)的要求编写的。
三、立项背景有机锡类农药主要包括三环锡、三唑锡、苯丁锡等,这类化合物常用做杀螨剂类农药,可用于苹果、柑橘、梨、茶树、棉花、蔬菜、花卉等作物。
三种化合物均具有一定的毒性,而且在环境中有较好的稳定性,残留期较长,因而存在对人体的潜在健康风险。
目前我国已经于1987年禁用三环锡类农药,而三唑锡是三环锡的替代产品,二者的主要官能团相同,均为三环己基锡。
我国最新实施的食品安全国家标准《食品中农药最大残留限量GB 2763-2012》规定了苹果、梨、柑橘、番茄等水果和蔬菜中三唑锡和苯丁锡的残留限量,限量浓度为mg/kg。
欧盟、日本和美国等国家和团体也对食品中有机锡类农药提出限量要求,例如日本肯定列表规定了134种食品中三环锡的限量水平,国内外共有约632项各类食品中苯丁锡的限量要求[1]。
研究建立食品中有机锡类农药残留的检测方法,对于规范进出口商品检验行为,应对国外贸易技术壁垒,维护国家经济利益和保护国民健康和安全具有重要的意义。
目前我国针对各类食品中有机锡类农药的检测方法已有若干标准,其中,SN 0150-1992规定了出口水果(包括苹果、香蕉和柑桔等)中三唑锡残留量检验方法,该方法采用甲基碘化镁衍生,结合气相色谱和火焰光度检测法进行;SN 0592-1996规定了出口粮谷及油籽中苯丁锡残留量检验方法,该方法采用浓盐酸将目标物氯化,通过气相色谱电子俘获检测器进行检测;SN/T 1990-2007规定了气相色谱质谱法用于检测进出口食品中三唑锡和三环锡残留量,检测的食品类型包括茶叶、水果、蔬菜、粮谷、肉类和蜂蜜等多种样品基质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
食品安全国家标准食品中有机锡的测定1范围本标准规定了食品中有机锡的气相色谱-脉冲火焰光度检测器检测方法㊂本标准适用于鱼类㊁贝类㊁葡萄酒和酱油等样品中二甲基锡㊁三甲基锡㊁一丁基锡㊁二丁基锡㊁三丁基锡㊁一苯基锡㊁二苯基锡㊁三苯基锡的测定㊂2原理分别以一甲基锡为单取代有机锡的内标,三丙基锡为二㊁三取代有机锡的内标,采用内标法定量㊂在试样中定量加入一甲基锡和三丙基锡内标,超声辅助将有机锡提取出来,有机溶剂萃取,提取后的样品溶液经凝胶渗透色谱净化㊁戊基格林试剂衍生㊁衍生化产物再经弗罗里硅土(F l o r i s i l)净化,采用气相色谱-脉冲火焰光度检测器(G C-P F P D)测定㊂3试剂和材料除非另有说明,本方法所用试剂均为分析纯,水为G B/T6682规定的一级水㊂3.1试剂3.1.1正己烷(n-C6H14):重蒸㊂3.1.2四氢呋喃(C H2C H2O C H2C H2):重蒸㊂3.1.3乙酸乙酯(C H3C O O C2H5):重蒸㊂3.1.4环己烷(C6H12):重蒸㊂3.1.5甲醇(C H3O H)㊂3.1.6无水乙醚(C2H5O C2H5)㊂3.1.7溴代正戊烷(n-C5H12B r)㊂3.1.8无水硫酸钠(N a2S O4):将无水硫酸钠置干燥箱中,于120ħ干燥4h,冷却后,密闭保存㊂3.1.9氯化钠(N a C l)㊂3.1.10硫酸(H2S O4):优级纯㊂3.1.11盐酸(H C l):优级纯㊂3.1.12氢溴酸(H B r)㊂3.1.13乙二胺四乙酸二钠(E D T A N a2)㊂3.1.14金属钠(N a)㊂3.1.15镁条(M g)㊂3.1.16环庚三烯酚酮(t r o p o l o n e):98%㊂3.1.17弗罗里硅土(F l o r i s i l):0.147mm~0.25mm(60目~100目),120ħ烘烤12h㊂3.1.18聚苯乙烯凝胶:0.075mm~0.147mm(100目~200目),或同类产品㊂3.2试剂配制3.2.1环庚三烯酚酮-正己烷溶液(0.03%):量取正己烷100m L,加入0.03g环庚三烯酚酮混匀㊂3.2.2氯化钠溶液(20g/L):称取氯化钠100g,溶于水并稀释至500m L㊂3.2.3饱和氯化钠溶液:在100m L水中加入过量氯化钠,水浴使溶解,恢复室温后要求结晶析出㊂3.2.4甲醇-水溶液(4+1):取甲醇适量,制备甲醇-水(4+1)溶液,并根据每1m L甲醇加1μL盐酸的要求,加入盐酸,制得含盐酸的甲醇-水(4+1)溶液㊂3.2.5氢溴酸-四氢呋喃溶液(1+20):取氢溴酸和四氢呋喃各适量,按照1+20的比例制备成溶液㊂3.3标准品3.3.1有机锡标准品及其标准溶液:见附录A㊂除二甲基锡㊁三丁基锡纯度为95%外,其他标准品纯度均大于97%㊂3.3.2内标:一甲基锡(MMT)和三丙基锡(T P r T)标准品:纯度>98%㊂3.4标准溶液配制3.4.1有机锡标准贮备液:准确称取有机锡的标准品适量,置于10m L烧杯中,加入甲醇-水溶液(3.2.4)溶解,转移到10m L容量瓶中,并稀释至刻度㊂于-20ħ冰箱保存㊂3.4.2内标标准贮备溶液:准确称取内标适量,置于10m L烧杯中,加入甲醇-水溶液(3.2.4)溶解,转移到10m L容量瓶中,并稀释至刻度㊂于-20ħ冰箱保存㊂3.4.3有机锡标准及内标中间溶液:量取有机锡标准或内标贮备液适量,用甲醇-水溶液(3.2.4)稀释100倍,质量浓度见附录A㊂于-20ħ冰箱保存㊂3.4.4有机锡标准及内标工作溶液:量取有机锡标准或内标中间液适量,置于10m L容量瓶中,加入甲醇-水溶液(3.2.4)并稀释至刻度,浓度见附录A㊂于-20ħ冰箱保存㊂4仪器和设备4.1气相色谱仪(G C):配脉冲火焰光度检测器(P F P D),硫滤光片㊂4.2色谱柱:D B-1毛细管柱或等效柱,柱长30m,膜厚0.25μm,内径0.25mm㊂4.3组织匀浆器㊂4.4振荡器㊂4.5超声波清洗器㊂4.6旋转蒸发仪㊂4.7氮气浓缩器㊂4.8三口瓶㊁分液漏斗和加热回流装置㊂4.9加热磁力搅拌装置㊂4.10玻璃层析柱㊂4.11分析天平:感量为1m g㊂4.12电加热套㊂5分析步骤5.1戊基格林试剂的合成5.1.1乙醚重蒸与除水:在35ħ下,采用全玻璃蒸馏装置重蒸两次㊂在蒸馏的乙醚中,加入光洁金属钠片,至不再产生明显气泡后,放置1h~2h,继续加入金属钠片,保存备用㊂5.1.2溴代正戊烷的重蒸:量取溴代正戊烷100m L,置于蒸馏瓶中,在140ħ下,采用全玻璃蒸馏装置重蒸两次,馏分避光收集㊂5.1.3镁屑的制备:取镁条,刮去表面氧化膜层,用剪刀剪成约0.3mm的碎屑,用正己烷洗涤2次~ 3次,挥干,保存备用㊂5.1.4戊基溴化镁的合成:称取镁屑10g,置500m L三口瓶中,加入重蒸乙醚100m L,加入搅拌子㊂在搅拌下,滴加重蒸溴代正戊烷60m L和重蒸乙醚50m L的混合溶液㊂反应发生后,停止搅拌㊂当反应速度减缓后,继续滴加上述溴代正戊烷和乙醚的混合溶液,并搅拌㊂调节滴加速度,使反应瓶中的乙醚保持微沸状态㊂当反应缓慢时,开始加热,保持反应发生,继续加热回流至反应完全,得到戊基溴化镁溶液约200m L,溶液呈灰黑色混浊状态㊂将合成的戊基溴化镁分装至棕色小瓶中,封口,干燥器内保存㊂5.2试样制备鱼去皮及刺,制成肉糜;贝类试样取可食组织制成匀浆;葡萄酒和酱油试样混合均匀㊂鱼贝类试样制成匀浆后,可采用冷冻干燥,制成冻干粉末,置-20ħ以下低温保存㊂5.2.1试样提取5.2.1.1鱼类样品准确称取试样适量,加入乙二胺四乙酸二钠0.15g和20g/L氯化钠溶液5m L,摇匀,加入内标工作溶液50μL,加入氢溴酸-四氢呋喃溶液(1+20)(3.2.5)15m L,超声5m i n㊂如果为湿样,加入饱和氯化钠溶液1m L,摇匀,加入内标工作溶液50μL,加入氢溴酸-四氢呋喃溶液(1+20)(3.2.5)15m L,超声5m i n㊂5.2.1.2贝类样品准确称取试样适量,加入20%氯化钠溶液5m L,摇匀,加入内标工作溶液50μL,加入氢溴酸-四氢呋喃溶液(1+20)(3.2.5)15m L,超声5m i n㊂5.2.1.3葡萄酒等液体样品量取试样10m L,加入氯化钠2g,摇匀,加入内标工作溶液50μL,加入氢溴酸-四氢呋喃溶液(1+20)(3.2.5)15m L,超声5m i n㊂5.2.2试样溶液的净化在试样溶液中加入含0.03%环庚三烯酚酮的正己烷25m L,振荡萃取40m i n,离心10m i n (3000r/m i n),静置分层,吸取有机相转移至茄形瓶中,在残渣中加入正己烷10m L,振荡萃取10m i n,离心10m i n(3000r/m i n),静置分层,吸取有机相㊂合并至茄形瓶中,旋转蒸发浓缩至近干㊂5.2.3凝胶渗透色谱净化5.2.3.1凝胶柱的装填:取聚苯乙烯凝胶,用四氢呋喃-乙酸乙酯(1+1)溶液浸泡过夜㊂用玻璃棉封堵内径为1.7c m~1.8c m的玻璃层析柱底端,湿法加入浸泡好的凝胶,凝胶自然沉降,稳定后柱长约为15c m㊂5.2.3.2净化:在试样提取液的浓缩残渣中加入四氢呋喃-乙酸乙酯(1+1)溶液1m L,将此溶液全部转移至层析柱上,用1m L 四氢呋喃-乙酸乙酯(1+1)溶液洗涤茄形瓶㊂待层析柱中试液溶液的液面降至接近凝胶时,将洗液转移至柱上㊂用四氢呋喃-乙酸乙酯(1+1)溶液洗脱,弃去0m L~18m L 流分,收集18m L ~33m L 流分,收集流出体积15m L ㊂5.2.4 戊基溴化镁格林试剂衍生将5.2.3.2收集的净化溶液旋转蒸发浓缩近干,加入环己烷10m L ,继续旋转蒸发浓缩至约1m L ,转移至10m L 离心管中,用环己烷洗涤茄形瓶,合并在离心管中,并定容至2m L ㊂用1m L 注射器加取上述合成的戊基溴化镁格林试剂0.8m L ,涡旋振荡混匀,超声反应15m i n 后,逐滴加入0.5m o l /L 硫酸约3m L ,振摇,终止衍生反应,涡旋振摇,静置使上层溶液澄清㊂5.2.5 弗罗里硅土(F l o r i s i l)柱净化5.2.5.1 层析柱装填:用玻璃棉封堵玻璃柱底端后,从底部到顶部依次装入活化弗罗里硅土(F l o r i s i l)1.5g ㊁无水硫酸钠2g ,用正己烷10m L 预淋洗㊂5.2.5.2 净化:将5.2.4衍生溶液的上层有机相全部转移至弗罗里硅土柱上,当柱中溶液的液面降至无水硫酸钠层时,用正己烷洗脱,收集洗脱液5m L ,在氮气流下浓缩至约1m L 后,转移至另一根填以1.5g 弗罗里硅土(F l o r i s i l )和2g 无水硫酸钠的层析柱上,用正己烷-甲苯(5+1)溶液10m L 预淋洗,用正己烷-甲苯(5+1)溶液洗脱,收集10m L 流分㊂5.2.6 浓缩在氮气流下,将5.2.5.2净化的试样溶液浓缩定容至1.0m L ,转移进进样小瓶中,待G C 测定㊂5.3 仪器参考条件气相色谱参考条件:a ) 色谱柱1):D B -1柱(或等效柱),柱长30m ,膜厚0.25μm ,内径0.25mm ㊂1) 给出这一信息是为了方便本标准的使用者,并不表示对该产品的认可,如果其他等效产品具有相同的效果,则可使用这些等效的产品㊂b ) 采用不分流方式,进样口温度280ħ㊂c ) 柱温程序:开始温度为50ħ,保持1m i n ;以10ħ/m i n 升温至120ħ;5ħ/m i n 升温至200ħ;10ħ/m i n 升温至280ħ,保持5m i n㊂d ) 载气为高纯氮气(纯度>99.999%)㊂e ) 脉冲火焰光度检测器参考条件:模式:硫滤光片;温度:350ħ;燃气和助燃气流速:空气121m L /m i n ,氢气22m L /m i n ,空气211m L /m i n ;光电倍增管电压:550V ;门槛时间:4m s;门延迟时间:5m s ;激发电压:100m V ㊂5.4 标准曲线制作准确称取不含有机锡的对应食物样品作为空白基质适量,加入5m L20%氯化钠溶液,分别加入有机锡混合标准溶液0μL ㊁10μL ㊁30μL ㊁50μL ㊁100μL ㊁200μL ㊁400μL 及内标工作溶液50μL ,按试样提取与净化过程要求同步操作㊂吸取标准系列溶液1μL 注入气相色谱仪进行分析,得到色谱图(参见附录B .1及附录B .2),以保留时间定性㊂5.5 试样溶液的测定吸取试样溶液1μL 注入气相色谱仪中,得到色谱图(参见附录B .3),以保留时间定性㊂计算目标化合物与内标的峰面积或峰高比,以标准系列溶液中目标有机锡的进样量(n g)与对应的目标有机锡与内标的峰面积或峰高比绘制线性曲线,根据线性曲线计算试样中有机锡含量㊂6分析结果的表述试样中目标有机锡含量(以S n计)的质量分数按式(1)计算:(1)X=Aˑfm式中:X 试样中目标有机锡含量(以S n计),单位为微克每千克(μg/k g)或微克每升(μg/L);A 试样色谱峰与内标色谱峰的峰高比值对应的目标有机锡质量(以S n计),单位为纳克(n g);f 试样稀释因子;m 试样称样量,单位为克(g)或毫升(m L)㊂计算结果以重复性条件下获得的两次独立测定结果的算术平均值表示,结果保留三位有效数字㊂7精密度在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的20%㊂8其他本方法定量限(以S n计)为:二甲基锡0.5μg/k g㊁三甲基锡1.2μg/k g㊁一丁基锡1.5μg/k g㊁二丁基锡0.5μg/k g㊁三丁基锡0.6μg/k g㊁一苯基锡1.7μg/k g㊁二苯基锡0.8μg/k g㊁三苯基锡0.8μg/k g㊂。
