天然气物理化学性质
天然气及其组分的物理化学性质

编号:SY-AQ-09384( 安全管理)单位:_____________________审批:_____________________日期:_____________________WORD文档/ A4打印/ 可编辑天然气及其组分的物理化学性质Physical and chemical properties of natural gas and its components天然气及其组分的物理化学性质导语:进行安全管理的目的是预防、消灭事故,防止或消除事故伤害,保护劳动者的安全与健康。
在安全管理的四项主要内容中,虽然都是为了达到安全管理的目的,但是对生产因素状态的控制,与安全管理目的关系更直接,显得更为突出。
天然气的主要成分为甲烷,此外还含有乙烷、丙烷、丁烷等烃类气体,氮、CO2、H2S及微量氢、氦、氩等非烃类气体,一般气藏天然气的甲烷含量在90%以上。
油田伴生气中甲烷含量占65%~80%,此外还含有相当数量的乙烷、丙烷、丁烷等烃类气体。
一、天然气主要组分的物理化学性质天然气主要组分的物理化学性质见表1-3-1。
表1-3-1天然气主要组分在标准状态下的物理化学性质名称分子式相对分子质量摩尔体积Vm/(m3/kmol)气体常数R(J/kg·K) 密度ρ/(kg/m3)临界温度Tc/K临界压力Pc/MPa高热值Hh/(MJ/m3)高热值Hh/(MJ/kg)低热值H1/(MJ/m3)甲烷CH4 16.043 22.362 518.75 0.7174 190.58 4.544 39.842 35.906 乙烷C2H6 30.07 22.187276.64 1.3553 305.42 4.816 70.351 55.367 64.397 丙烷C3H8 44.097 21.936 188.65 2.0102 369.82 4.194101.266 51.908 93.240 正丁烷n-C4H10 58.124 21.504 143.130 2.703 425.18 3.747 133.886 50.376 123.649 异丁烷i-C4H10 58.124 21.598 143.13 2.6912 408.14 3.600 133.048 49.532 122.853 正戊烷C15H12 72.151 20.891115.27 3.4537 46.965 3.325 169.377 49.438 156.733 氢H22.016 22.427 412.67 O.0898 33.25 1.280 12.74549.042 10.786 氧O2 31.999 22.392 259.97 1.4289 154.33 4.971 —141.926 —氮N2 23.01322.403 296.95 1.2507 125.97 3.349 ——氦He 3.016 22.42 281.17 0.1345 3.35 0.118 ——二氧化磺CO2 44.010 22.26 189.04 1.9768 304.25 7.290 ———硫化氢H2S34.07622.18 244.17 1.5392 373.55 8.890 25.364 23.383 空气28.066 22.40 287.24 1.2931 132.4 3.725 —16.488—水蒸气H2O18.01521.629461.760.8330647.0021.830—名称低热值H1/(MJ/kg)爆炸极限(体积分数)/% 动力黏度μ×106/(Pa·s)运动黏度υ×106/(m2/s)沸点/℃定压比热容Cp/(kJ/m3·K)绝热指数K导热系数λ/[W/(m·K)] 偏心因子上限下限甲烷5.015.010.60 14.50 -161.49 1.545 1.309 0.03024 0.0104 乙烷50.05 2.9 13.0 8.77 6.41-88.00 2.244 1.1980.01861 0.0986 丙烷47.515 2.19.57.65 3.81-42.05 2.960 1.161 0.01512 0.1524 正丁烷46.383 1.58.56.97 2.53-0.05 3.710 1.144 0.01349 0.2010 异丁烷45.745 1.88.5-11.72 —1.144 —0.1848 正戊烷45.65 1.4 8.3 6.48 1.85 36.06 —1.121 —0.2539 氢45.381 4.0 75.98.52 93.00 -252.75 1.298 1.407 0.2163 氧120.111 ——19.86 13.60 -182.98 1.315 1.400 0.02500.0213 氮——17.00 13.30 -195.78 1.302 1.402 0.02489 0.04氦————-269.95 —1.640 ——二氧化碳———14.30 7.09-78.200.6201.304 0.01372 0.225硫化氢4.3 45.5 11.90 7.63-60.20 1.557 1.320 0.01314 0.100 空气15.192 ——17.50 13.40-192.501.3061.4010.02489—水蒸气——8.6010.12—1.4911.3350.016170.3480二、天然气中有机硫化合物的主要性质天然气中除含有H2S外,还含有数量不等的硫醇、硫醚以及微量的二硫化碳、硫化羰。
表- 液态天然气的物理化学特性及危险属性

表- 液态天然气的物理化学特性及危险属
性
液态天然气(LNG)是一种常见的液化石油气。
它是由天然气
经过冷却和压缩而成,以便在储存和运输过程中占据较小的体积。
液态天然气在低温条件下存在,因此具有较高的物理化学特性和危
险属性。
液态天然气的化学式为C3H8,相对分子质量为44.097 g/mol。
它的液态密度为0.571 g/cm³,沸点为-42.1 °C,熔点为-187.7 °C,
闪点为-188.0 °C。
液态天然气具有自燃温度为460 °C,爆炸限度在2.1%到9.5%之间。
它不溶于水,也是非导电的。
主要成分为甲烷,含量大于等于90%。
液态天然气是高度易燃气体,因此具有危险性。
其物质容易燃烧,能形成爆炸性混合物,并且在高温下具有自燃性。
爆炸时会生成有毒气体。
在处理液态天然气的火灾时,适合使用干粉、二氧化碳、泡沫和水雾等灭火剂。
液态天然气的危险品运输编号为
UN1978,危险品分类编号为2.1,包装标志为3。
在液态天然气的应急处置中,需要避免火源。
如发生泄漏,需要立即采取适当的减压和通风处理,并迅速撤离人员到安全区域,以防止扩散。
以上是液态天然气的物理化学特性及危险属性的基本信息。
如需更多详细信息,请参考相关文献或咨询专业人士。
车用CNG气瓶安全使用需知

车用CNG气瓶安全使用需知一、天然气的物理化学性质和CNG气瓶使用工况天然气的主要成分是甲烷,它是无色、无味气体,密度为0.717g/L(标准状况),比空气轻,极难溶于水的可燃性气体,爆炸极限为5%-15%,与空气混合能形成爆炸性混合物,遇热源和明火有燃烧爆炸的危险。
而甲烷属微毒类气体,低浓度时,对人基本无毒,但浓度过高时,使空气中氧含量明显降低,使人窒息。
当空气中甲烷达25%-30%时,可引起头痛、头晕、乏力、注意力不集中、呼吸和心跳加速。
若不及时脱离,可致窒息死亡。
CNG气瓶的公称工作压力一般为20—25MPa,设计温度:-5-50℃范围。
二、CNG汽车一定要规范改装,要遵守国家安全法规,由取得压力容器安装1级资质,有可靠的技术和设备的改装点进行改装。
合肥现有四家持证单位,名称及电话为:合肥星月(5580101)、合肥润安(4242177)、合肥大联合(3456013)和安徽东方(5539948)。
不可盲目自选改装车辆。
三、改装后的CNG汽车气瓶应到市特种设备安全监察部门办理气瓶使用登记手续,持证使用。
四、CNG汽车第一次充气时,要注意先用天然气进行“冲洗”(或用氮气置换),即将天然气充入气瓶使瓶内压力达到以0.5—0.6Mpa,然后放出天然气减压至0.2—0.3Mpa,如此反复三次再充气至气瓶的额定工作压力。
五、气瓶中的天然气量不允许用尽,应保持压力在0.3Mpa以上,防止空气进入气瓶。
六、出车前先缓慢开启气瓶阀门,后缓慢开启高压总阀,观察高压气表,检查燃料供给系统的泄漏情况,若没有泄漏再检查汽车电气系统是否漏电,在确认没有漏电、漏气时方可起动。
开启气瓶阀门时不允许站在气瓶阀正面。
七、压缩天然气汽车进入加气位置后,发动机必须熄火,驻车制动,关闭所有电器电源。
充气完毕后在加气站工作人员的指挥下,缓慢驶离,不得猛踩油门。
行驶中一旦发现漏气,应立即关闭所有电源,查出漏气部位和原因,及时处理,如泄漏严重,应关闭气瓶阀门,待天然气散发后再作处理,必要时放掉全部天然气。
天然气知识基础

液压子站与传统子站优劣比较
项目 占地面积 液压子站 3- 4亩 普通子站 5亩以上 原由 液压子站设备简单,用拖车替代 传统子站的储气装置 1 .液压子站耗电量小,电机不大 于32KW;传统子站压缩机75KW左 右。 2.液压拖车泄气率高,拖车余气 小于1 20Nm 3;传统子站拖车泄气 率低,余气大于800Nm 3 液压装置噪音小于75dB(距设备1 米处); 压缩机噪音大于1 20dB
(1)从气田开采的气田气或称纯天然气; (2)伴随石油一起开采出来的石油气,也称石油伴生气; (3)凝析气田气,天然气从地层流出井口后,随着压力和 温度的下降,分离为气液两相,气相是凝析气田天然气,液相 是凝析液,叫凝析油。 (4)从井下煤层抽出的矿井气(俗称:瓦斯)。
四、天然气及其成分的物理化学性质
五、天然气压缩与节流
1、压缩:利用加压装置或设备使管道(储气装置)内 天然气压力升高,以提高管线的输送能力或对气体进行 储存,以满足其它工艺要求的过程,称为压缩。 2、节流:具有一定压力、充满管道的天然气在流经管 道内的节流件时,流束将在节流件处形成局部收缩,从 而使流速增加,静压降低,此种现象称为节流。
二、天然气的组分
天然气是一种多组分的混合气体,主要成分是烷烃,其中 甲烷(CH4)占绝大多数,另有少量的乙烷(C2H6)、丙烷和丁 烷,此外一般还含有硫化氢、二氧化碳、氮和水气,以及微量 的惰性气体,如氦和氩等。在标准状况下,甲烷至丁烷以气体 状态存在,戊烷以上为液体。
三、天然气的分类(按矿藏分类)
4.高压表:气瓶的高压管路经过过流保护阀后安装了高压
表,能指示气瓶内的压力
5.其它:油气转换开关等部件,选型的重点是减压阀和混 合器。因为在其它条件不变的条件下,这两个部件直接影 响CNGV的主要性能,其它的部件大多数属于标准件,基本 上是成熟的、定型的产品,选配比较容易。
燃气基础知识

2、压力单位换算 1个标准大气压=101325Pa(约0.1MPa)=1.033kgf/cm3=10.33mH2O(水柱〕
=760mmHg〔毫米汞柱〕 1MPa=1000KPa=1000000Pa 1bar=1000mbar 1bar=0.1MPa=1公斤压力=100KPa 1KPa=10mbar
30
应用:天然气水露点要求〔℃〕: 在天然气交接点的压力和温度条件下,天然气的水露点应比最低环境温度低5℃。 天然气水蒸汽来源:生产过程中携带或长输管线吹扫、枯燥不彻底余水。 天然气水蒸汽枯燥不彻底危害:在输送过程中易因水分含量过大损害设备:如对管
道腐蚀加重,调压时易结冰引起调压失灵等故障。压缩过程中水分吸热,变成气态, 气压升高,损害设备;大气温度低到达天然气的水露点,易造成加气机冰堵。故天然 气应首先进行脱水处理,合格前方可使用。CNG需进行枯燥。
高 压 A 2.5MPa<P≤4.0MPa
36
三、城市燃气管网系统介绍
城市燃气输配系统主要是燃气管网,管网系统按压力分如下四类: 一级系统:仅用低压系统分配供给,适用于小城镇。 两级系统:中压〔A〕和低压或中压〔B〕和低压两级管道构成,适用于一般城镇和小型城市。 三级系统:高、中、低压三种压力级别管道构成的管网系统, 大中型和中型城市。 多级系统:高压〔A、B〕、中压〔A、B〕和低压系统构成,适用于大型城市、多类型用户地区。
天然气高热值与低热值之间存在着燃烧时生成的水的汽化潜热。 低热值=高热值-水蒸气的气化潜热
甲烷在标准状态下 : 高热值为39.82MJ/m3;低热值为35.88MJ/m3
15
五、天然气的物理特性四-热值〔续〕
几种不同地天然气及液化石油气的热值〔 kcal/Nm3 〕
天然气的组成及危害

天然气的组成及危害天然气的组成天然气主要组分为甲烷,通常占90%以上,还含有一些乙烷、丙烷、丁烷及戊烷以上的烃类,并且有少量的二氧化碳、氮气、硫化氢、氢气等非烃类组分。
我国油气田中普遍含硫化氢较少,但四川所产天然气中含硫化氢较多。
含量约在0.1%左右。
天然气的物理化学性质相对密度:0.55-0.75闪点:-218℃自燃点:500-700℃(典型干气)爆炸下限:3.6%-6.5%爆炸上限:13%-17%最小点火能:0.3-0.4MJ(典型干气)天然气的低位发热量(扣除水的气化潜热后的发热量):35-39MJ/Nm3天然气的危害甲烷等轻烃本身无毒,为单纯窒息性气体。
但硫化氢是一种剧毒气体,天然气中如果含有较多的硫化氢,大量吸入会损害健康。
油气井井喷失控钻井分"钻探井"和"生产井"两种,钻探井的目的是要搞清地下是否有石油或天然气;钻生产井是为了把地层中的油、气开采出来。
当钻井遇到地下油、气、水层时,地下的油、气或水串进井内的泥浆里,加快了泥浆流动和循环的速度,地下油、气压力失去控制,造成油、气、水等混合物沿着环空迅速喷到地面。
为什么油井会发生井喷失控?地下压力是怎样形成的?原来,在井眼未形成之前,地层四周应力处于平衡状态,压力相对稳定。
井眼形成以后,地层压力平衡受到破坏,地层下的流体由于流动而产生压力。
钻井时为了平衡地层压力,保证钻井正常进行,要不断地往井内注入泥浆,并随时根据地层压力的变化调整泥浆比重,使井底压力始终与地层压力保持平衡,而油井井喷失控则是由于种种原因,使井底压力低于地层压力,井下压力失去平衡造成的。
在钻井的过程中发生井喷失控的事故,根据我国玉门、四川、大庆、中原等油气田发生的一些井喷失控事故的发生分析,大多数是在钻入高压油、气层时,由于施工设计不准确,泥浆性能不好,操作技术不当,或井下发生严重漏失等原因造成的。
井喷失控如不能及时控制,很容易发生火灾,井喷失控一旦发生火灾将会造成巨大损失。
燃气基础知识

燃气基础知识一、天然气、液化石油气、焦炉煤气、水煤气主要成分及物理、化学性质1. 天然气主要成分:甲烷分子式:CH4理化性质:无色无味的气体,能被液化和固化。
能溶于乙醇、乙醚,微溶于水。
易燃,燃烧时呈青白色火焰,火焰温度约为1950℃。
1立方米天然气爆炸当量相当于7-14公斤TNT炸药。
相对密度:0.415(-164℃)凝固点:-183.2℃沸点:-161.5℃自然点:540℃爆炸极限:5.3%~15%最易引燃浓度:7.5%产生最大爆炸压力的浓度:9.8%最大爆炸压力:7kg/平方厘米最小引燃能量:0.28毫焦燃烧热值:8500千卡/立方米灭火剂:干粉、雾状水、泡沫、二氧化碳2. 液化石油气主要成分:丙烷、丁烷、丙烯、丁烯分子式:C3H8、C4H10、C3H6、C4H8理化性质:液化石油气比空气重,低毒性,有一定臭味,燃烧温度400-530度,爆温1500度以上。
1立方米液态液化石油气可变成约250立方米气体,1公斤液化石油气爆炸当量相当于10~20公斤TNT炸药。
自然点:426.7℃-540℃爆炸极限:2%~10%最小引燃能量:0.25毫焦爆速:2000~3000m/s燃烧热值:22000千卡/立方米灭火剂:干粉、雾状水、泡沫3. 液化石油气、天然气不完全燃烧液化石油气、天然气等燃气燃烧时,如果通风不好,易造成不完全燃烧,产生大量的一氧化碳。
一氧化碳无色无味,有毒性,空气中最大容许浓度为30毫克/立方米。
一氧化碳与血红蛋白的亲和力要比与氧气的亲和力大200-300倍,而解离却慢3600倍。
空气中一氧化碳的含量达千分之二,20~30分钟人可能中毒死亡;达百分之一,1~2分钟内可能中毒死亡。
人员中毒后,应及时到通风良好的地方,最好送医院高压氧仓治疗。
4. 焦炉煤气、水煤气焦炉煤气、水煤气及发生炉煤气这些人造气体燃料是由煤炭气化制成,又统称为煤制气。
焦炉煤气的平均组成为:H246%-61% 、CO 4.0%-8.5% 、CH421%-30% 、CmHn 1.5%-3.0%、CO2 1.0%-4.0%、 N2 3.6%-26%、 O2 0.3%-1.7% 焦炉煤气的自燃点为500-600度,热值为4000—4500千卡/立方米,其发热温度高约为2100~2130℃。
天然气物理化学性质

海底天然气物理化学性质第一节海底天然气组成表示法一、海底天然气组成海底天然气是由多种可燃和不可燃的气体组成的混合气体。
以低分子饱和烃类气体为主,并含有少量非烃类气体。
在烃类气体中,甲烷(CH4)占绝大部分,乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)和戊烷(C5H12)含量不多,庚烷以上(C5+)烷烃含量极少。
另外,所含的少量非烃类气体一般有氮气(N2)、二氧化碳(CO2)、氢气(H2)、硫化氢(H2S)和水汽(H2O)以及微量的惰性气体。
由于海底天然气是多种气态组分不同比例的混合物,所以也像石油那样,其物理性质变化很大,它的主要物理性质见下表。
海底天然气中主要成分的物理化学性质二、海底天然气容积分数和摩尔分数定义混合物中各组分的容积为V i ,总容积V ;摩尔分数y i :i 组分的摩尔数n i 与混合物总摩尔数n 的比值。
∑=='i i i i V VV V y ; 1='∑i y ;∑==ii i i n n n n y ; 1=∑i y 由分压定律,存在P i V= n i R M T ;P i V=n R M T 由分容定律,存在PV i = n i R M T ;PV=n R M Tppn n y i i i ==; i i i i y n n V V y ==='结论:对于理想气体混合物,任意组分的摩尔分数可以用该组分的分压与混合物总压的比值表示,且摩尔分数与容积分数相等。
三、海底天然气分子量标准状态下,1kmol 天然气的质量定义为天然气的平均分子量,简称分子量。
∑=i i M y M 四、海底天然气密度(1)平均密度混合气体密度指单位体积混合气体的质量。
按下面公式计算: 0℃标准状态 ∑=i i M y 414.221ρ; 20℃标准状态 ∑=i i M y 055.241ρ 任意温度与压力下 i i i i V y M y ∑∑=/ρ (2)相对密度在标准状态下,气体的密度与干空气的密度之比称为相对密度。
天然气的物理化学性质

C3、C7、C20 10%、20%、70%
二、天然气的组成
1、天然气:(烃类、非烃类) uNatural gas:指从地下采出的,常温常压下相态
为气态的烃类和少量非烃类气体组成的混合物。 lHydrocarbon:CnH2n+n
C1(70~98%)、C2(<10%) C3~C5(百分之几)、C6+(甚微) lNon-hydrocarbon:H2S、CO2、N2、CO、Ar、He
m1 14.4387 Kg m2 1.5035 Kg m3 2.20485 Kg
u求:体系的质量组成、摩尔组成和体积组成
二、天然气的组成
l体系的质量组成
气相
体系的总质量m
C1, C2, C3
3
m mi m1 m2 m3 i 1 18.14705
3
G1 m1 / mi 14.4387 /18.14705
n2 0.05 n3 0.05
二、天然气的组成
体系的总摩尔数n:
气相
C1, C2, C3
3
n ni n1 n2 n3 i 1 0.9 0.05 0.05
1
yi
ni
/ n3
i1
i
ni
体系中各组分的摩尔组成:
y1 n1 0.9 y2 n2 0.05 y3 n3 0.05
第二章
天然气的物理化学性质
第二章 天然气的物理化学性质
u确定天然气在各状态下物性参数的方法: l直接取气样进行实验测定; l根据天然气各组分的物理性质、物理规律利用
混合规则进行计算。
第二章 天然气的物理化学性质
第一节 第二节 第三节 第四节 第五节 第六节 第七节
天然气的组成和分类 天然气的分子量、相对密度、密度和比容 天然气偏差系数的确定 天然气的等温压缩系数 天然气的体积系数和膨胀系数 天然气的粘度 天然气含水量和溶解度
天然气理化特性表和液化天然气理化特性表

组分
LNG是以甲烷为主要成分的烧类混合物,其中含有通常存在于天然气中少量的乙烷、丙烷、氮等其它组分。
物理性质
LNG作为一种沸腾液体大量的储存于绝热储罐中,任何传导至储罐中的热量都会导致一些液体蒸发,一般情况下,蒸发气包括20%的氮,80%的甲烷和微量乙烷。
密度
LNG的密度取决于其组分,通常在430kg∕m3-470kg∕m3之间。
天然气主要组分为甲烷,其毒性因其他化学组成的不同而异。
液化天然气理化特性表
理化特性
相对分子量(kg/kmol):16.41沸点温度/C:-162.6
密度/(kg∕m3)131.6
O0Ct101.325Pa条件下单位体积和液体生成的气体体积/(m3∕m3):590
O0CtIOL325Pa条件下单位质量和液体生成的气体体积/(m3∕103kg):1.367毒性:LNG和天然气是无毒的。
主要用途:主要用作燃料和用于炭黑、氢、乙块、甲醛等的制造。
危害信息
【燃烧和爆炸危险性】
极易燃,与空气混合能形成爆炸性混合物,遇热源和明火有燃烧爆炸危险。
【活性反应】
与五氧化漠、氯气、次氯酸、三氟化氮、液氧、来自氟化氧及其他强氧化剂剧烈反应。
【健康危害】
纯甲烷对人基本无毒,只有在极高浓度时成为单纯性窒息剂。皮肤接触液化气体可致冻伤。
天然气理化特性表
特别
警示
极易燃气体。
理化特性
无色、无臭、无味气体。微溶于水,溶于醇、乙醒等有机溶剂。分子量16.04,熔点-182.5C,沸点T6L5C,气体密度0.7163g∕L,相对蒸气密度(空气=1)0.6,相对密度(水=1)0.42(-164βC),临界压力4.59MPa,临界温度-82.6℃,饱和蒸气压53.32kPa(T68.8C),爆炸极限5.0%〜16%(体积比),自燃温度537℃,最小点火能0.28mJ,最大爆炸压力0.717MPa<>
天然气物理化学性质

天然气物理化学性质一、物理性质1. 密度天然气密度较小,一般为 0.7-0.9 kg/m³,约为空气的1/5-1/8,因此天然气比空气轻。
2. 比热容天然气的比热容较低,一般在 2-3 kJ/(kg•℃)左右,这意味着加热天然气所需的能量较少,燃烧时也能释放更多的热量。
3. 蒸汽压由于天然气的分子量较小,因此蒸汽压也较低。
在常温下,天然气的蒸汽压非常低,几乎可以忽略不计。
4. 粘度天然气的粘度极低,比液化石油气还要低,一般为0.015-0.02 Pa•s,因此流动性非常好。
二、化学性质1. 氧化性天然气是一种可燃气体,含有大量的甲烷、乙烷等烷烃和少量的烯烃、芳香烃等物质,因此在空气中容易燃烧并释放大量的热能。
2. 惰性天然气在大多数情况下不会发生化学反应,是一种具有较高化学惰性的气体。
但在高温高压的条件下,天然气也会发生一些特殊的化学反应。
3. 可溶性天然气在水中的可溶性非常低,每升水中只能溶解数毫升的天然气,因此在生产和运输过程中需要采用一系列的处理工艺来进行天然气的脱水和脱酸等处理。
4. 酸碱性天然气本身是一种中性物质,不具有酸碱性。
三、在工业生产中的应用1. 燃气天然气具有燃烧热值高、燃烧清洁、供应安全稳定等优点,被广泛应用于城市燃气和工业燃料等领域。
目前已有大量的城市建立了天然气供应系统,供应给民用和工业用户。
2. 化工原料天然气中含有大量的甲烷、乙烷等有机物质,这些物质可以通过加工制造成为化工原料,制造丙烷、丙烯、烯烃等物质,广泛应用于化工生产中。
3. 发电天然气发电是现代发电技术的主要形式之一,利用天然气发电可以实现高效节能、绿色环保等好处,受到越来越广泛的关注。
在中国,天然气发电正在逐渐成为重要的电源之一。
四、结论天然气作为一种重要的能源资源,具有燃烧热值高、燃烧清洁、供应安全稳定等优点,被广泛应用于各个领域。
但是,天然气也存在一些问题,比如难以存储和运输、价格波动较大等。
天然气密度和相对密度

• 压力:压力升高,天然气相对密度增大
• 杂质含量:杂质含量越高,天然气相对密度越大
变化规律
• 在一定温度和压力下,天然气相对密度与组成成分呈正相关
• 在一定组成成分和压力下,天然气相对密度与温度呈负相关
• 在一定组成成分和温度下,天然气相对密度与压力呈正相关
04
天然气密度与相对密度的应用领域
天然气勘探与开发中的密度与相对密度应用
• 粘度:较低,一般为1~0.03mPa·s
• 热值:较高,一般为35~40MJ/m³
化学性质
• 燃烧性:易燃,与空气混合能形成爆炸性气体
• 稳定性:在常温常压下稳定,不易发生化学反应
• 腐蚀性:对金属有一定的腐蚀性,特别是铜和铁
天然气的主要用途及市场需求
主要用途
市场需求
• 燃料:发电、供暖、烹饪等
影响
• 误差可能导致天然气密度和相对密度的测量结果不准确,影响天然气勘探、开发、
输送等方面的决策
• 误差可能导致天然气计量和计价的不合理,影响天然气市场的公平性和稳定性
天然气密度与相对密度测量误差的控制方法
设备选择
方法优化
操作规范
数据处理
• 选择精度高、稳定性好
• 根据天然气成分和测量
• 制定详细的测量操作规
• 在一定组成成分和温度下,天然气密度与压力呈正相关
03
天然气相对密度的概念与计算方法
天然气相对密度的定义及其意义
定义
• 天然气相对密度指天然气密度与空气密度的比值,单位为无
意义
• 反映天然气在空气中的浓度,与天然气泄漏、扩散等现象密切相关
• 影响天然气管道泄漏检测、储气库安全运行等方面的技术参数选择
天然气及其组分的物理化学性质

天然气及其组分的物理化学性质一、天然气的定义、分类及成分天然气是指从地球内部产生,通过地层破裂、孔隙和裂隙等天然通道,自然释放到地面上或岩石层中含有气体的地层中产生的混合气体。
天然气主要由甲烷及其伴生气体组成,包括乙烷、丙烷、丁烷等烷烃和少量的非烷类气体如CO2、H2S、氮等。
1. 烷烃类气体烷烃类气体是天然气中的主要组分,其中以甲烷含量最高,占天然气的50%~98%。
甲烷化学式为CH4,分子式中只包含碳和氢两种元素,成分简单。
甲烷是最轻、相对稳定和不易形成其他化合物的烷基化合物。
乙烷的分子式为C2H6,其含量在天然气中通常为2%~20%。
丙烷含量较少,通常占天然气的2%以内。
2. 非烷类气体天然气中还含有一些非烷类气体,包括CO2、H2S、氮等。
此类气体的含量较低,但是对天然气的运输、处理和使用都有一定的影响。
二、物理化学性质1. 密度天然气是一种相对较轻的气体,在标准条件下(温度为15℃,气压为101.325kPa)其密度约为0.65~0.85kg/m³,低于空气密度,故在空气中会上升。
由于天然气密度较低,自重力非常小,因此天然气在地层中的运移和分布受到很多因素的制约,需要相对较高的地层压力和孔隙度才能保持稳定的储集和运输状态。
2. 燃烧性能天然气是一种较为理想的化石燃料,具有高燃烧效率和低污染排放等优点。
天然气的燃烧热值高、燃烧过程稳定,生成的二氧化碳、水蒸气等废气排放量较小,相比煤、石油等传统化石燃料来说更环保。
天然气燃烧时生成的NOx等有害气体排放量也相对更少,但是气体中的硫化氢等成分在燃烧过程中也会生成二氧化硫等有害气体。
3. 溶解性天然气主要成分甲烷在水中的溶解度非常小,表现为不易被水溶解。
常温常压下,1L水只能溶解22.5ml甲烷,极端情况下最高可至50ml/L。
由于天然气中含有一部分CO2等成分,其溶解度要高于甲烷,导致水与天然气的接触面积越大,溶解率就越高。
天然气储存过程中,通常还需要与储气库内的地层水接触,因此溶解度的问题也是储存过程中需要考虑的重要因素。
天然气的性质和特点

天然气的性质和特点1、天然气是一种易燃易爆气体,和空气混合后,温度只要达到550℃就燃烧。
在空气中,天然气的浓度只要达到5-15%就会爆炸。
2、天然气无色,比空气轻,不溶于水。
一立方米气田天然气的重量只有同体积空气的55%左右,一立方米油田伴生气的重量,只有同体积空气的75%左右。
3、天然气的主要成分是甲烷,本身无毒,但如果含较多硫化氢,则对人有毒害作用。
如果天然气燃烧不完全,也会产生一氧化碳等有毒气体。
4、天然气的热值较高,一立方米天然气燃烧后发出的热量是同体积的人工煤气(如焦炉煤气)的两倍多,即35.6-41.9兆焦/立方米(约合8500-10000千卡/立方米)。
5、天然气可液化,液化后其体积将缩小为气态的六百分之一。
每立方米天然气完全燃烧需要大约十立方米空气助燃。
6、一般油田伴生气略带汽油味,含有硫化氢的天然气略带臭鸡蛋味。
天然气的主要成分是甲烷,甲烷本身是无毒的,但空气中的甲烷含量达到10%以上时,人就会因氧气不足而呼吸困难,眩晕虚弱而失去知觉、昏迷甚至死亡。
天然气中如含有一定量的硫化氢时,也具有毒性。
硫化氢是一种具有强烈臭鸡蛋味的无色气味,当空气中的硫化氢浓度达到0.31毫克/升时,人的眼、口、鼻就会受到强烈的刺激而造成流泪、怕光、头痛、呕吐;当空气中的硫化氢含量达到1.54毫克/升时,人就会死亡。
因此,国家规定:对供应城市民用的天然气,每立方米中硫化氢含量要控制在20毫克以下天然气的化学组成天然气是指烃类气体。
地壳中,天然气就其产状分析,有游离态、溶解态(溶于原油和水中)、吸附态和固态气水合物四种类型。
从分布特点又可分为聚集型和分散型两类。
气藏气、气顶气、凝析气、油溶气属聚集型,也称为常规型天然气;水溶气、煤层气、固态气水合物则属分散型,也称为非常规型天然气。
从与油藏的关系划分,气顶气、油溶气以及油藏之间或油藏上方的、在成因上与成油过程相伴的气藏气,均归于伴生气;与油没有明显联系的或仅含有极少量原油的气藏气,成因上与煤系有机质或未成熟的有机质有关而生成的天然气称之为非伴生气。
第1章天然气的物理化学性质

Cp Cv
K
2016/12/21
西南石油学院储运研究所
43
低压下气体在各种温度下的比热也可按下式计算
C A BT CT DT
p 2
3
• A、B、C、D——计算常数,不同气体的值见 表1-5 • 气体混合物(天然气)在低压下的比热可根据 各组分的比热用摩尔分数加合法或质量分数加 合法求得,即 Cp yi C pi
34
2016/12/21
西南石油学院储运研究所
1.2.3 天然气的密度和相对密度(比重)
密度定义
体在此标准状态下的密度为 气体在某压力、温度下的密度为:
2016/12/21
西南石油学院储运研究所
35
天然气的重度 二.相对密度(即比重)
空=1.293kg/m3(在0C、101325Pa下) 空=1.205kg/m3(在20C、101325Pa下)
第一章 天然气的物理化学性质
第一节 天然气的化学组成与分类
• 一.天然气输送方法
•
液化天然气(LNG)是天然气经净 化处理后,通过低温冷却而成的液态 产物,其体积为原气态体积的1/600。 为在常压下保持液态,必须将其冷却 至-162℃以下。液态时,可以用液化 天然气运输船运输。液化天然气运达 接收的港口后,卸入接收站的低温储 罐中储存,然后通过加热再气化后, 以气态形式用管道输送至用户。目前 我国正在积极发展液化天然气系统。 广东、上海、大庆、长庆等地均已建 大宗天然气的输送方法目前只有两种,一是用管 与输油不同,天然气的管道输送 或在建液化天然气生产装置。 必然是上下游一体化的,开采、 道输送,二是将天然气液化后用专用的油轮运输。 收集、处理、运输和分配是在统 一的连续密闭的系统中进行的。
表- 天然气液化过程中的物理化学性质及危险特征
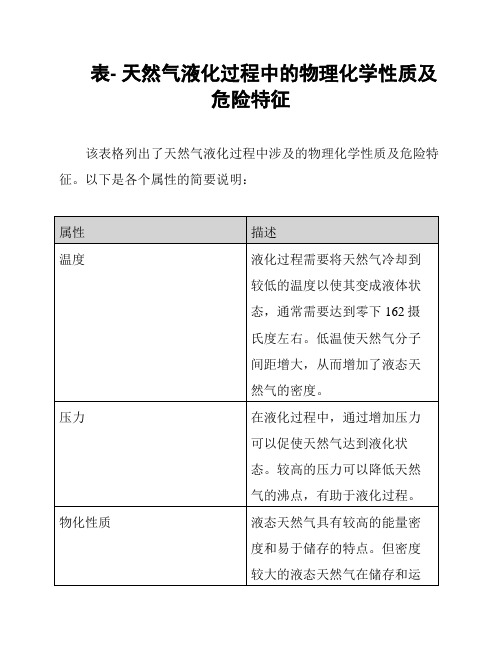
该表格列出了天然气液化过程中涉及的物理化学性质及危险特征。以下是各个属性的简要说明:
属性
描述
温度
液化过程需要将天然气冷却到较低的温度以使其变成液体状态,通常需要达到零下162摄氏度左右。低温使天然气分子间距增大,从而增加了液态天然气的密度。
压力
在液化过程中,通过增加压力可以促使天然气达到液化状态。较高的压力可以降低天然气的沸点,有助于液化过程。
物化性质
液态天然气具有较高的能量密度和易于储存的特点。但密度较大的液态天然气在储存和运பைடு நூலகம்过程中需要特殊的设施和措施以确保安全。
危险特征
液态天然气具有易燃、易爆的特性,一旦泄漏或受到外部火源点燃,可能引发火灾或爆炸。在使用和储存过程中需要特殊的安全措施,如防爆装置和泄漏监测系统。
以上是表格中包含的物理化学性质和危险特征的简要描述。这些信息对于研究和处理天然气液化过程中的安全问题非常重要。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
海底天然气物理化学性质第一节海底天然气组成表示法一、海底天然气组成海底天然气是由多种可燃和不可燃的气体组成的混合气体。
以低分子饱和烃类气体为主,并含有少量非烃类气体。
在烃类气体中,甲烷(CH4 )占绝大部分,乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)和戊烷(C5H12)含量不多,庚烷以上(C5+)烷烃含量极少。
另外,所含的少量非烃类气体一般有氮气(N2)、二氧化碳(CO2)、氢气(H2)、硫化氢(H2S)和水汽(H2O)以及微量的惰性气体。
由于海底天然气是多种气态组分不同比例的混合物,所以也像石油那样,其物理性质变化很大,它的主要物理性质见下表。
海底天然气中主要成分的物理化学性质二、海底天然气容积分数和摩尔分数定义混合物中各组分的容积为V i ,总容积V ;摩尔分数y i :i 组分的摩尔数n i 与混合物总摩尔数n 的比值。
∑=='ii i i V VV V y ; 1='∑i y ;∑==ii i i n nn n y ; 1=∑iy由分压定律,存在P i V= n i R M T ;P i V=n R M T 由分容定律,存在PV i = n i R M T ;PV=n R M Tpp n n y i i i ==; i i i iy n n V V y ==='结论:对于理想气体混合物,任意组分的摩尔分数可以用该组分的分压与混合物总压的比值表示,且摩尔分数与容积分数相等。
三、海底天然气分子量标准状态下,1kmol 天然气的质量定义为天然气的平均分子量,简称分子量。
∑=i i M y M 四、海底天然气密度(1)平均密度混合气体密度指单位体积混合气体的质量。
按下面公式计算: 0℃标准状态 ∑=i i M y 414.221ρ; 20℃标准状态 ∑=i i M y 055.241ρ 任意温度与压力下 i i i i V y M y ∑∑=/ρ (2)相对密度在标准状态下,气体的密度与干空气的密度之比称为相对密度。
对单组分气体:a ρρ/=∆ a ρ:空气密度,kg/m 3; 在0P =101.325kPa ,0T =273.15K 时;a ρ=1.293 kg/m 3 在0P =101.325kPa ,0T =293.15 K 时;a ρ=1.206 kg/m 3。
对混合气体: ∑∆=∆i i y 五、海底天然气虚拟临界参数和对比参数(1)临界参数使气体压缩成液态的极限温度称为该气体的临界温度。
当温度等于临界温度时,使气体压缩成液体所需压力称为临界压力,此时状态称为临界状态。
混合气体的虚拟临界参数可按凯(Kay )法则计算:∑=ci i c T y T ; ∑=ci i c P y P ; ∑=ci i c y ρρ适用:各组分的临界压力和临界比容接近(<20%),且任意二组分的临界温度满足0.5< T ci /T cj <2的条件,否则,可能有很大计算误差。
(2)对比参数海底天然气的压力、温度、密度与其临界压力、临界温度和临界密度之比称为天然气对比压力、对比温度和对比密度。
c r P P P /=; c r T T T /=; c r ρρρ/=;或 c r ννν/=第二节 天然气气体状态方程一、理想气体状态方程PV=RT ;PV M =R M T ;PV=mRT=nR M T 假设:分子是质点没有体积;分子间无作用力。
当压力足够低、温度足够高,可近似使用理想气体状态方程。
二、实际气体状态方程(1)范德瓦耳方程荷兰物理学家范德瓦耳考虑了分子体积和分子间吸力的影响: (P+a/V 2)(V-b )=RT (2)R-K 方程瑞得里奇-邝(Redlich-Kwong )方程是在范得瓦尔方程的基础上进行修正,于1949年提出的。
解决了实际气体性质定量计算的问题。
)(5.0b V V T ab V RT P +--=(3)SRK 方程Soave 于1972年在R-K 方程的基础上提出了另外的形式,解决在计算饱和气相密度时精度较差的问题。
)(b V V ab V RT P +--=(4)PR 状态方程为进一步提高对热力学性质和气液平衡数据预测的准确性,Peng 和Robinson 在Soave 模型基础上于1976年改进,提出PR 状态方程。
)()(b V b b V V ab V RT P -++--=(5)L-E-E 方程是一个多参数状态方程,其形式为:()))((b V b V V bcb V V a b V RT p +-++--=(6)BWRS 方程本尼迪科特-韦勃-鲁宾1940年提出了能适应气液两相的8参数BWR 状态方程,随后由Starling-Han 在关联大量实验数据的基础上,对BWR 方程进行修正,1970年提出了到目前认为用于天然气计算最精确的方程式之一的BWRS 方程。
3240302000)()(ρρρT d a bRT TE T D T C A RT B RT P --+-+--+=)ex p()1()(22235γργρρρα-++++Tc T b a三、带压缩因子的状态方程Z 压缩因子或压缩系数:表示实际气体与理想气体的差别。
Z 是一个状态参数,通过实验来确定。
但对理想气体,在任何状态下都有Z=1。
),(1r r r T P f =ρ c c c c RT P Z ρ=r r c cc c r ZT PZ ZRTP P RT Z ==ρ ),,,(r c r r Z T P f Z ρ'= ; ),,(2c r r Z T P f Z =c Z 在0.23~0.31范围内,化为:),(3r r T P f Z =表达式叫修正的对比态原理。
第三节 海底天然气的物理性质、热力性质和燃烧性质一、海底天然气物理性质 (一)粘度1.粘度分为动力粘度和运动粘度。
动力粘度μ,单位Pa ·S ,常用泊(P )、厘泊(cp )。
1 Pa ·S =10P=1000cP在常压下混合动力粘度:()()∑∑=iiii iiM yM yμμ在不同温度下的粘度:5.10273273⎪⎭⎫⎝⎛++=T C T C T μμ2.运动粘度ν,单位m 2/S ,常用托(St)、厘托(cst )。
1m 2/S=104 St =106 cst3.动力粘度与运动粘度的关系为: ν=μ/ρ(二)湿度 1.海底天然气含水量及水露点天然气中含水汽多少用湿度或含水量来描述,与压力、温度和组成条件有关。
饱和含水量:一定条件下,天然气与液态水达到相平衡时气相中的含水汽量。
绝对湿度:单位体积天然气中含有的水汽质量,单位为kg/m 3或mg/m 3。
饱和湿度:在一定温度和压力下,天然气含水汽量若达到饱和,则这个饱和时的含水汽量。
相对湿度:指同温度下,天然气实际的绝对湿度和饱和湿度之比。
水露点温度:在一定压力下,逐渐降低温度,天然气中水蒸气开始冷凝结露的温度,是表征天然气含水量的参数之一。
2.海底天然气的烃露点海底天然气烃露点:指一定组成的天然气,在一定压力下冷凝,当析出第一滴烃类液珠时的温度。
二、海底天然气的热力性质 1.比热和比热容比热:在不发生相变和化学变化的条件下,加热单位质量的物质时,温度升高1℃所吸收的热量。
单位为KJ/(kg ·K )或KJ/(kg ·℃)。
比热容:同样条件下,加热单位体积的物质时,温度升高1℃所吸收的热量,称为此物质的比热容,单位为KJ/(m 3·K )或KJ/(m 3·℃)。
气体的比热还分为质量定容热容C V 和质量定压热容C P 。
V V T u C )(∂∂=;P P ThC )(∂∂=; (1) 对于理想气体而言,这两种比热之差等于气体常数 R C C V P =-0纯组分理想气体:43205432T F T E T D T C B C i i i i i Pi++++= 混合物质量定压热容: 00Piii P C y C ∑= (2)实际气体比热容1)计算法 2)查图法ρρρ)()(222TP T C T V ∂∂-=∂∂或ρρρρd T P T C C V V )(22020∂∂-+=⎰2.焓气体内能和体积与压力乘积之和称为气体的焓,H=U+pV 或h=u+pv 。
(1)理想气体焓单组分:h i 0=A i +B i T+C i T 2+D i T 3+E i T 4+F i T 5 混合气体: 00i ii h y h ∑=(2)实际气体焓 1)计算法 2)查图法 3.熵熵是状态参数,随状态变化而变化,只决定于初始状态与终了状态。
与路径无关。
熵的变化表征了可逆过程中热交换的方向与大小。
(1)理想气体熵单组分:s i 0=B i lnT+2C i T+3/2D i T 2+4/3E i T 3+5/4F i T 4+G i 混合气体:s 0=∑y i s i 0 (2)实际气体熵1)计算法 2)查图法 4.导热系数物质导热能力的特性参数,指沿着导热方向上温度梯度为1K/m 时,单位时间内通过单位面积的热量,物质的基本性质之一,单位J/(m ·s ·k)或W/(m ·k)。
(1)查图、查表法对于混合气体的导热系数,在查得各组分的导热系数后,按下列方法计算 1)压力较低,根据各组分摩尔组成按Ribblett 公式计算λ=∑y i λi M i 1/3/∑y i M i 1/32)高压气体,按低压气体计算所得的导热系数,根据计算状态的对比压力和对比温度对其进行修正,查修正系数。
(2)计算法1)低压单组分气体的导热系数用Misic 和Thodos 基于量纲分析提出的经验公式: 对于甲烷、环烷烃和芳香烃,在T r <1时:r p T M c Γ⨯=-71045.4λ对于其它碳氢化合物及其它对比温度范围()Γ-=-M c T p r 32714.552.1410λ 3221610088.1cc p M T =Γ2)低压混合气体的导热系数低压下混合气体的导热系数可按Ribblet 计算,平均误差在3%左右。
3)温度对气体导热系数的影响 单组分:⎪⎭⎫⎝⎛++=15.27315.2730T C T C λλ混合气体:()()()()∑=ii i iT T Y T T 1212λλλλ 4)压力对气体导热系数的影响压力对气体的影响可根据对比密度进行计算:ρx <0.5时 (λ-λ0)ГZ c 5=(2.69654×10-4)(e 0.535ρr -1) 0.5<ρx <2.0时 (λ-λ0)ГZ c 5=(2.51972×10-4)(e 0.67ρr –1.069) 2.0<ρx <2.8时 (λ-λ0)ГZ c 5=(5.74673×10-5)(e 1.155ρr +2.016) 压力对混合气体导热系数的影响,仍可用上述公式计算,对比密度与气体种类无关,临界参数要按混合气体的视临界参数计算。
