奥司他韦说明书
奥司他韦的作用与功效

奥司他韦的作用与功效奥司他韦(Orlistat)是一种处方药,被用于治疗肥胖症。
它是一种脂肪酶抑制剂,可以阻止脂肪在小肠内被分解和吸收,从而降低体重和脂肪含量。
首先,让我们了解一下肥胖症的定义。
肥胖症是一种与食物摄入过多而导致体内能量过剩的疾病。
它是世界范围内的健康问题,同时也是许多其他疾病的风险因素,如糖尿病、高血压、心脏病和某些癌症。
奥司他韦的作用机制是通过抑制胰脂肪酶(也称为脂肪酶)的活性,减少脂肪的消化和吸收。
胰脂肪酶是一种在小肠内分解脂肪的酶,而奥司他韦可以与它结合并抑制其活性。
这样,未被分解的脂肪会通过大肠排出体外,而不会被人体吸收。
因此,奥司他韦的使用可以使人体摄入的脂肪量减少,并降低体脂肪的积累。
奥司他韦使用的主要指标是BMI(体质指数)大于30 kg/m^2的肥胖者,或者BMI大于等于27 kg/m^2但伴有高血压、糖尿病、高血脂等相关疾病的超重者。
BMI是根据一个人的身高和体重计算出来的一个值,可以用来评估一个人的体重状况。
一般来说,BMI在18.5到24.9之间被认为是正常体重,25到29.9之间被认为是超重,30以上则被认为是肥胖。
然而,奥司他韦并不适合所有的肥胖患者。
有些人可能有禁忌症或不适应症,如严重的肝脏疾病、胆固醇代谢异常、胰岛素依赖糖尿病等。
此外,奥司他韦也不能替代健康的饮食和运动习惯,它只能作为辅助治疗手段之一。
使用奥司他韦的患者仍需在服药期间配合健康的饮食和适量的运动。
奥司他韦可以减少体重和脂肪含量,但其效果在每个人身上可能不同。
临床试验证明,使用奥司他韦的患者在三个月的治疗期间平均可减少5%的体重。
然而,这并不意味着它可以一劳永逸地解决肥胖问题。
一旦停止使用奥司他韦,体重和脂肪含量往往会重新增加。
这是因为奥司他韦作用的是脂肪吸收的环节,而不是摄入的环节。
因此,长期维持良好的饮食和运动习惯仍然是保持健康体重的关键。
奥司他韦的副作用主要与其作用机制有关,包括脂溢性大便、腹泻、肛门排油、胃部不适和肠胀气等。
磷酸奥司他韦胶囊使用指南

三、注意事项
• (四)各站点参照本次下发药物数量,当 达菲储备低于30%时,报告中心予以采购补 充。
• (五)请各站点按每周一上午11:30前将 上周磷酸奥司他韦胶囊使用情况填写《区 疾控中心下发的磷酸奥司他韦胶囊各站点 使用情况一览表》(零使用的也要填写), 发生使用的应同时填写《磷酸奥司他韦使 用登记表》,要求做到账物相符。请各站 点按时将相关电子版报表发至中心郭先锋 处。
磷酸奥司他韦胶囊 使用指南
近日顺德区出现首例H7N9禽流感病 例,目前防控形势非常严峻。各级医 务人员要高度重视,做到“早发现、 早报告、早诊断、早治疗”,及早预 防重症和死亡病例的发生。为有效防 控人感染H7N9禽流感疫情,减少重症 和死亡病例发生,要求各站点按本指 引要求,认真做好药物使用等相关工 作。
ቤተ መጻሕፍቲ ባይዱ
一、使用对象
(一)有明确禽类接触史的流感样病例因经 济原因拒绝使用达菲者,重点注意老人和 基础病患者。 (二)接触过感染H7N9禽流感病例且未采取 有效防护措施的医务人员及病例的密切接 触者。
二、磷酸奥司他韦胶囊用法
病例治疗:建议先给药3天,成人2次/日,1 粒/次。儿童请参照药物说明书使用。 预防用药:每日一次,每次一粒,连续7天。
三、注意事项
• (一)该磷酸奥司他韦胶囊作为应急药物 储备,使用时不能再收取病人药费。
• (二)各站点要建立免费使用的管理制度, 按附件登记表内容做好服药者相关信息记 录,并由服用者或监护人签名确认。
• (三)接诊单位要指派专人做好服药者健 康状况追踪;结合实际注意做好病例转诊, 定点收治等工作。
奥司他韦说明书

核准日期:磷酸奥司他韦胶囊说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:磷酸奥司他韦胶囊商品名称:英文名称:oseltamivir phosphate capsules 汉语拼音:linsuan aositawei jiaonang 【成份】本品主要成份为磷酸奥司他韦。
化学名称:(3r,4r,5s)-4-乙酰氨基-5-氨基-3(1-乙丙氧基)-1-环己烯-1-羧酸乙酯磷酸盐。
分子量:410.4 【性状】【适应症】1.用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
2.用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
【规格】75毫克(以奥司他韦计)【用法用量】磷酸奥司他韦可以与食物同服或分开服用。
但对一些病人,进食同时服药可提高药物的耐受性。
流感的治疗在流感症状开始的第一天或第二天(理想状态为36小时内)就应开始治疗。
剂量指导成人和青少年磷酸奥司他韦在成人和13岁以上青少年的推荐口服剂量是每次75毫克,每日2次,共5天。
儿童对1岁以上的儿童推荐按照下列体重-剂量表服用磷酸奥司他韦用于与流感患者密切接触后的流感预防时的推荐口服剂量为75毫克,每日1次,至少7天。
同样应在密切接触后2天内开始用药。
磷酸奥司他韦用于流感季节时预防流感的推荐剂量为75毫克,每日1次。
有数据表明连用药物6周安全有效。
服药期间一直具有预防作用。
特殊人群用药指导肾功能不全患者流感治疗:对肌酐清除率大于30毫升/分钟的患者不必调整剂量。
对肌酐清除率在10-30毫升/分钟的患者,推荐使用剂量减少为每次75毫克,每日1次,共5天。
不推荐将磷酸奥司他韦用于肌酐清除率小于10毫升/分钟的患者和严重肾功能衰竭、需定期进行血液透析或持续腹膜透析的患者。
无肾功能衰竭儿童的用药剂量资料(见【药代动力学】和【注意事项】)。
流感预防:对肌酐清除率大于30毫升/分钟的患者不必调整剂量。
磷酸奥司他韦颗粒小儿使用剂量是多少

磷酸奥司他韦颗粒小儿使用剂量是多少根据美国疾病控制和预防中心(CDC)和世界卫生组织(WHO)的建议,磷酸奥司他韦颗粒小儿使用剂量如下:
1.治疗流感病毒感染:
- 新生儿(0-2周龄):2 mg/kg,每天2次,共给药5天。
- 婴幼儿(2周-1岁):3 mg/kg,每天2次,共给药5天。
- 儿童(1-12岁):3 mg/kg,每天两次,共给药5天。
- 青少年(12-18岁):75 mg,每天两次,共给药5天。
2.流感病毒暴露预防:
-新生儿(0-2周龄):不适用。
-婴幼儿(2周-1岁):不适用。
- 儿童(1-12岁):3 mg/kg,每天一次,给药10天。
- 青少年(12-18岁):75 mg,每天一次,给药10天。
需要注意的是,儿童使用磷酸奥司他韦颗粒的剂量应根据儿童的具体
体重计算。
此外,磷酸奥司他韦颗粒在服用前应该与食物一起服用,以减
少对胃肠的刺激。
在使用磷酸奥司他韦颗粒治疗或预防流感病毒感染时,建议儿童患者
在医生的指导下使用药物,严格按照药物说明或医生的建议使用,不得自
行调整剂量。
此外,儿童在使用磷酸奥司他韦颗粒期间可能出现一些副作用,如恶心、呕吐、腹泻、头痛等。
如果出现严重不良反应,应及时就医并告知医生正在使用磷酸奥司他韦颗粒。
总之,儿童使用磷酸奥司他韦颗粒的剂量需根据体重进行计算,具体剂量应在医生的指导下进行。
另外,药物使用期间需要密切关注儿童的反应,并确保遵循医生的建议使用药物。
奥司他韦颗粒说明书Word 文档
【药品名称】磷酸奥司他韦颗粒【商品名称】可威【英文名称】Oseltamivir Phosphate Granules【汉语拼音】Linsuan Aositawei Keli【成份】本品主要成份为磷酸奥司他韦。
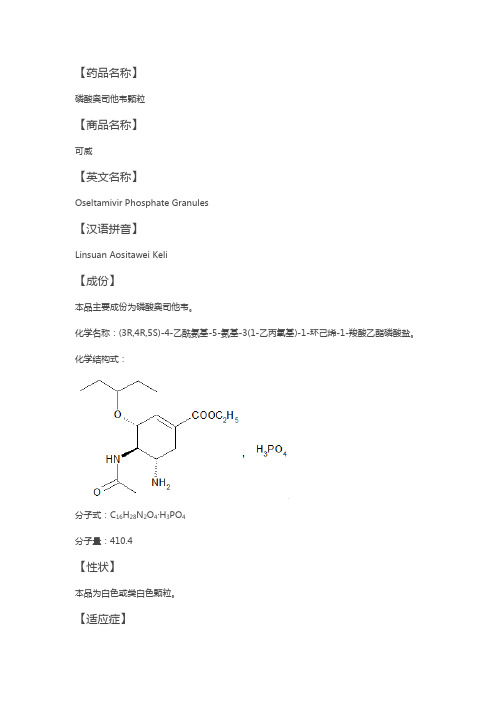
化学名称:(3R,4R,5S)-4-乙酰氨基-5-氨基-3(1-乙丙氧基)-1-环己烯-1-羧酸乙酯磷酸盐。
化学结构式:分子式:C16H28N2O4·H3PO4分子量:410.4【性状】本品为白色或类白色颗粒。
【适应症】1.用于1岁及1岁以上儿童和成人的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
2.用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
【规格】15mg(以奥司他韦计);25mg(以奥司他韦计)【用法用量】本品用温开水完全溶解后口服。
磷酸奥司他韦可以与食物同服或分开服用。
但对一些病人,进食同时服药可提高药物的耐受性。
流感的治疗在流感症状开始的第一天或第二天(理想状态为36小时内)就应开始治疗。
剂量指导成人和青少年磷酸奥司他韦在成人和13岁以上青少年的推荐口服剂量是每次75毫克,每日2次,共5天。
儿童对1岁以上的儿童推荐按照下列体重-剂量表服用流感的预防磷酸奥司他韦用于与流感患者密切接触后的流感预防时的推荐口服剂量为75毫克,每日1次,至少7天。
同样应在密切接触后2天内开始用药。
磷酸奥司他韦用于流感季节时预防流感的推荐剂量为75毫克,每日1次。
有数据表明连用药物6周安全有效。
服药期间一直具有预防作用。
特殊人群用药指导肾功能不全患者流感治疗:对肌酐清除率大于30毫升/分钟的患者不必调整剂量。
对肌酐清除率在10-30毫升/分钟的患者,推荐使用剂量减少为每次75毫克,每日1次,共5天。
不推荐将磷酸奥司他韦用于肌酐清除率小于10毫升/分钟的患者和严重肾功能衰竭、需定期进行血液透析或持续腹膜透析的患者。
无肾功能衰竭儿童的用药剂量资料(见【药代动力学】和【注意事项】)。
奥司他韦颗粒

磷酸奥司他韦颗粒本词条由“科普中国”百科科学词条编写与应用工作项目审核。
磷酸奥司他韦颗粒,适应症为:1.成人和1岁及1岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
2.成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
用法用量本品用温开水完全溶解后口服。
磷酸奥司他韦可以与食物同服或分开服用。
但对一些病人,进食同时服药可提高药物的耐受性。
流感的治疗在流感症状开始的第一天或第二天(理想状态为36小时内)就应开始治疗。
剂量指导儿童对1岁以上的儿童推荐按照下列体重-剂量表服用体重推荐剂量(服用5天)≤15 kg 30mg (2包), 每日2次>15-23kg 45mg,(3包)每日2次>23-40kg 60mg,(4包)每日2次>40kg 75mg,(5包)每日2次成人和青少年磷酸奥司他韦在成人和13岁以上青少年的推荐口服剂量是每次75毫克,每日2次,共5天。
流感的预防磷酸奥司他韦用于与流感患者密切接触后的流感预防时的推荐口服剂量为75毫克,每日1次,至少7天。
同样应在密切接触后2天内开始用药。
磷酸奥司他韦用于流感季节时预防流感的推荐剂量为75毫克,每日1次。
有数据表明连用药物6周安全有效。
服药期间一直具有预防作用。
适应症1.用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
2.用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
规格15 mg(以奥司他韦计);25 mg(以奥司他韦计)特殊人群用药指导肾功能不全患者流感治疗:对肌酐清除率大于30毫升/分钟的患者不必调整剂量。
对肌酐清除率在10-30毫升/分钟的患者,推荐使用剂量减少为每次75毫克,每日1次。
共5天。
不推荐将磷酸奥司他韦用于肌酐清除率小于10毫升/分钟的患者和严重肾功能衰竭、需定期进行血液透析或持续腹膜透析的患者。
奥司他韦的正确服用方法和注意事项

奥司他韦的正确服用方法和注意事项一、奥司他韦治疗什么?奥司他韦是一种神经氨酸酶抑制剂。
它能防止病毒体从宿主细胞中释放,具有抗甲型和乙型流感病毒的作用。
普通感冒和流感虽然都是急性呼吸道疾病,但普通感冒以鼻病毒或冠状病毒最常见;流感则由甲型或乙型流感病毒导致,偶尔由丙型流感病毒引起。
奥司他韦只对流感有用,对普通感冒无效!二、奥司他韦对儿童的安全性药品说明书用于1岁及1岁以上儿童的甲型和乙型流感治疗,对1岁以下儿童治疗流感的安全性和有效性尚未确定。
但在我国2020年版《儿童流感诊断与治疗专家共识》中提到用于三个月以上儿童流感的预防和治疗,奥司他韦是安全的。
三、奥司他韦的正确服用方法和注意事项1、在流感症状开始的第一天或第二天(理想状态为36小时内)服用奥司他韦获益最大。
2、食物不影响奥司他韦在体内的吸收,饭前饭后服用都没有问题,但跟食物同服可以减轻药物对胃肠道的刺激。
3、用于治疗时,一天两次,连服5天,若治疗5天后,患者病情严重,则可考虑给予更长的疗程。
4、用于与流感患者亲密接触后的预防时,一天一次,服用至少10天。
5、需要提醒的是,足够的疗程治疗非常重要,即便服药期间症状减轻很多,也不建议自行停药。
四、漏服奥司他韦,该怎么办?任何时候,漏服了都应该尽快补服,但是如果距离下一次的服药时间短于2小时的话,则应跳过漏服的那次剂量,下一次的剂量正常服用就可以了,切莫把两次的剂量一起服用。
五、服用奥司他韦,可能的不良反应有哪些?服用奥司他韦,常见会引起恶心、呕吐、腹泻、腹痛、失眠的不良反应,甚至也会发生一些严重过敏反应和行为异常、谵妄、幻觉、精神错乱等的精神障碍现象。
所以家长们不要盲目囤货或自行给小孩服用。
六、奥司他韦和退烧药有无相互作用?奥司他韦和退烧药对乙酰氨基酚无临床显著的药物相互作用,当两者联合使用时,奥司他韦或对乙酰氨基酚都不需要调整剂量。
七、服用奥司他韦,小孩可以马上接种流感疫苗吗?由于奥司他韦可能会抑制活疫苗病毒的复制和降低疫苗的疗效,应避免服用奥司他韦前2周内或给药后48h内接种减毒活流感疫苗。
奥司他韦

奥司他韦(Oseltamivir)于1999年在瑞士上市,2001年10月在我国上市,其化学名称为(3R,4R,5S)-4-乙酰胺-5-氨基-3(1-乙基丙氧基)-1-环己烯-1-羧酸乙酯,化学物质登记号CASRN为196618-13-0。
奥司他韦口服后经肝脏和肠道酯酶迅速催化转化为其活性代谢物奥司他韦羧酸,奥司他韦羧酸的构型与神经氨酸的过渡态相似,能够竞争性地与流感病毒神经氨酸酶(NA,neu-raminidase,也有称作神经氨酸苷酶)的活动位点结合,因而是一种强效的高选择性的流感病毒N A抑制剂(NAIs),它主要通过干扰病毒从被感染的宿主细胞中释放,从而减少甲型或乙型流感病毒的传播。
目前市场上销售的达菲为罗氏制药独家生产的抗流感药物,其通用名称为磷酸奥司他韦(Oseltamivirphosphate),也就是前面所说的奥司他韦的磷酸盐,化学物质登记号CASRN为204255-11-8。
达菲于1999年被美国FDA批准上市,在中国已于2004年7月上市。
从药物经济学的角度来看,尽管使用达菲的药品费用并不算低,每天服用两次,每次75mg,药品零售价相当于每天60元,5天一个疗程相当于300元左右。
但是由于达菲是一种非常有效的流感治疗用药,并且可以大大减少并发症(主要是气管与支气管炎、肺炎、咽炎等)的发生和抗生素的使用,因而是目前治疗流感的最常用药物之一,也是公认的抗禽流感、甲型H1N1病毒最有效的药物之一。
日本卫生部门对抗流感药物“达菲”可能产生的副作用展开调查。
2007年,2月2 6日午夜,一名14岁男孩在服用“达菲”后从仙台市一座公寓楼的11层跳下身亡,这是日本在过去17个月里发生的第18起与这种畅销药物有关的青少年死亡事件。
在这起最新死亡案件中,这名男孩的医生让其连续服用“达菲”5天。
26日,这名男孩服用了2片“达菲”。
当晚,在其醒来后,他告诉其母亲他要去洗手间,然后,他却拉开正门走了出去。
奥司他韦用法用量

奥司他韦用法用量作用功效奥司他韦是其活性代谢产物奥司他韦羚酸盐的前体药物,奥司他韦羚酸盐是选择性的流感病毒神经氨酸酶抑制剂。
奥司他韦的活性代谢产物(奥司他韦羚酸盐)能够抑制甲型和乙型流感病毒的神经氨酸酶活性,通过抑制病毒从被感染的细胞中释放,从而减少甲型或乙型流感病毒的播散主治疾病●用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗●用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防适用症状可缓解甲流及乙流的相关症状,如发热、头痛、全身肌肉、关节酸痛、乏力、食欲减退、咽喉痛、干咳、鼻塞、流涕等。
联合用药功效●高热患者可能联合应用退热药,咳嗽咳痰患者严重者可以给予止咳祛痰药●可能联合应用中草药或中成药如牛黄清感胶襄等其他抗病毒药物用前须知奥司他韦不能取代流感疫苗。
在使用减毒活流感疫苗两周内不应服用本品,在服用本品后48h内不应使用减毒活流感疫苗。
禁用人群已知对本品的任何成份过敏者禁用。
慎用人群●尚未进行重度肝功能不全患者使用本品的安全性和药代动力学的研究,因此此类患者慎用本品。
●尚未研究本品在诱析的终未期肾病惠者中的药代动力学,因此此类患者慎用本品。
●应对现有安全性和获益信息、流行病毒株的致病性和奸娠或哺乳期妇女的基本条件进行评估,以确定好娠及哺乳期妇女是否可以服用本品。
特殊人群用药须知●妊娠:应对现有安全性和获益信息、流行病毒株的致病性和妊娠妇女的基本条件进行评估,以确定妊娠女是否可以服用本品●哺乳:有限证据证明,奥司他韦及其代谢产物可于人乳汁中检出,但浓度非常低,对于婴儿来说低于治疗剂量。
鉴于此,以及流行病毒株的致病性和哺乳母亲的基本条件,可以考虑给予本品。
●儿童: 1岁以上儿童按体重给予相应的用药剂量;1岁以下儿童的安全性和有效性尚未确定。
●老年人:无需调整用药剂量。
●肝功能不全者:对轻、中度肝功能不全患者用于治疗和预防流感时无需调整剂量。
但用于严重肝功能不全患者的安全性和药代动力学尚未研究。
达菲Tamiflu(磷酸奥司他韦胶囊)说明书

2.1% 3.7% 2.5% 1.2% 1.2% 1.9% 1.5% 0.4%
1.6% 3.5% 3.1% 1.7% 1.0% 1.0% 1.0% 1.0%
皮肤和皮下组织改变:有极少病例报告出现发红(皮疹),皮炎和大疱疹。
肝脏和胆道:有极少病例报告有流感样疾病的患者出现了肝炎和肝酶升高。
48(3.2%) 11(0.7%) 30(2.0%) 24(1.6%)
第 3 页 共 15 页
头痛 咳嗽**
失眠 眩晕 乏力
14(2.0%) 12(1.7%) 7(0.8%) 3(0.4%) 7(1.0%)
13(1.8%) 9(1.2%) 8(1.1%) 7(1.0%) 7(1.0%)
251(17.5%) 86(6.0%) 14(1.0%) 3(0.2%) 107(7.5%)
7.在免疫抑制的患者中奥司他韦治疗和预防流感的安全性和有效性尚不确定。
8.在合并有慢性心脏或/和呼吸道疾病的患者中奥司他韦治疗流感的有效性尚不确定。
这些人群中治疗组和安慰剂组观察到的并发症发生率无差别。
第 6 页 共 15 页
9.磷酸奥司他韦不能取代流感疫苗。磷酸奥司他韦的使用不应影响每年接种流感疫苗。 磷酸奥司他韦对流感的预防作用仅在用药时才具有。只有在可靠的流行病学资料显示社区出 现了流感病毒感染后才考虑使用磷酸奥司他韦治疗和预防流感。
不良事件
安慰剂 N=517
奥司他韦,2 毫克/千克 N=515
呕吐
9.3%
15.0%
腹泻
10.6%
9.5%
腹痛
3.9%
4.7%
恶心
4.3%
3.3%
中耳炎
11.2%
8.7%
奥司他韦说明书

奥司他韦说明书一、药品名称通用名称:奥司他韦商品名称:_____二、成分本品主要活性成分为奥司他韦。
三、性状本品为灰白色和浅黄色双色胶囊,内容物为白色至黄白色粉末。
四、适应症1、用于成人和 1 岁及 1 岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
患者应在首次出现症状 48 小时以内使用。
2、用于成人和 13 岁及 13 岁以上青少年的甲型和乙型流感的预防。
五、规格胶囊剂:_____mg/粒六、用法用量1、治疗(1)成人和 13 岁以上青少年的推荐口服剂量是每次 75mg,每日 2 次,共 5 天。
(2)1 岁以上的儿童应根据体重给药:体重≤15kg,每次 30mg,每日 2 次;体重 151 23kg,每次 45mg,每日 2 次;体重 231 40kg,每次 60mg,每日 2 次;体重>40kg,每次 75mg,每日 2 次。
2、预防(1)成人和 13 岁以上青少年的推荐口服剂量是每次 75mg,每日 1 次,至少 7 天。
(2)1 岁以上的儿童应根据体重给药:体重≤15kg,每次 30mg,每日 1 次;体重 151 23kg,每次 45mg,每日 1 次;体重 231 40kg,每次 60mg,每日 1 次;体重>40kg,每次 75mg,每日 1 次。
七、不良反应1、最常见的不良反应是恶心、呕吐、头痛等,这些症状通常是轻微和短暂的,多数在服药后的 1 2 天内自行缓解。
2、少数患者可能会出现过敏反应,如皮疹、瘙痒、呼吸困难等。
如果出现严重过敏反应,应立即停药并就医。
3、还有部分患者可能会出现精神神经系统症状,如幻觉、异常行为等。
八、禁忌对本品的任何成分过敏者禁用。
九、注意事项1、奥司他韦应在医生的指导下使用,患者不应自行增减剂量或停药。
2、用药期间,如果症状没有改善或加重,或者出现新的症状,应及时就医。
3、奥司他韦可能会影响驾驶和操作机器的能力,因此在用药期间应避免从事这些活动。
奥司他韦胶囊用法用量

奥司他韦胶囊用法用量奥司他韦胶囊用法用量磷酸奥司他韦胶囊用法用量:每粒胶囊含98.5mg磷酸奥司他韦。
一般剂量磷酸奥司他韦的推荐口服剂量是每次一粒,每日两次,共5天。
在流感症状开始的第一天或第二天就应该开始治疗。
磷酸奥司他韦可以与食物同服或分开服(见药代动力学)。
对有一些病人,与进食同时服药可增强对药物的耐受性。
特殊剂量指导肾功能不全患者:对肌酐清除率大于30ml/min的患者不必调整剂量。
对肌酐清除率小于30ml/min者,推荐使用剂量降为每次一粒,每日一次,共5天。
奥司他韦胶囊功效作用奥司他韦有两种剂型,一种是成人片剂或胶囊,另一种是儿童或幼儿颗粒剂。
2、服用奥司他韦后,部分患者会出现恶心、呕吐等不适,需要密切观察副作用;3、奥司他韦是处方药,需要在医院或药房开具。
奥司他韦的主要药效是抗病毒,可以抑制流感病毒的活性,达到消除病毒的治疗效果,并治疗由甲型和乙型流感病毒感染引起的各种不良症状。
同时,可以退烧,促进体温尽快恢复。
此外,还可以用作青少年和成年人预防流感的药物。
奥司他韦主要用于治疗流感。
可消除甲型和乙型流感病毒感染引起的头晕、头痛、流鼻涕等不良反应,并能有效抑制流感病毒在体内的活动,防止其过度繁殖。
临床上,该药物通常用于成人流感患者,尤其是在首次出现症状后48小时内。
奥司他韦具有解热作用,特别是对流感病毒感染引起的发热。
患者服用后可以在短时间内将体温恢复到正常水平,以防止持续发热症状。
奥司他韦能有效预防流感。
对于13岁及以上的青少年和成年人,在医生的指导下合理服用奥司他韦胶囊可以有效降低甲型和乙型流感的发病率。
奥司他韦属于神经氨酸酶抑制剂,临床上称为乙酯前体药物。
其药理作用是促进体内酯酶的转化,促进其转化为具有活性的羧基奥司他韦,并与流感病毒表面的神经氨酸酶结合,从而有效切断和抑制感染细胞,达到治疗流感的效果。
磷酸奥司他韦胶囊的副作用1、全身不良反应。
脸部或舌肿胀、变态反应、过敏反应或者是过敏样反应,以及体温过低。
磷酸奥司他韦胶囊说明书

磷酸奥司他韦胶囊说明书药品名称:磷酸奥司他韦胶囊药品类型:处方药、医保工伤用药用途分类:其他抗病毒药一、成份1.1.主要成份:磷酸奥司他韦;1.2.化学名称:(3R,4R,5S)-4-乙酰胺-5-胺基-3(1-丙氧乙酯)-1-环己烷-1羧酸乙酯磷酸盐(1:1);1.3.化学结构式:1.4.分子式:C16H28N2O4.H3PO41.5.分子量:410.4二、性状本品为灰白色和浅黄色双色胶囊,内容物为白色至黄白色粉末。
三、适应症3.1.用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
患者应在首次出现症状48小时以内使用。
3.2.用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
四、规格75mg(以奥司他韦计)。
五、用法用量磷酸奥司他韦可以与食物同服或分开服用。
但对一些病人,进食同时服药可提高药物的耐受性。
5.1.流感的治疗:在流感症状开始的第一天或第二天(理想状态为36小时内)就应开始治疗。
5.2.剂量指导:成人和青少年:磷酸奥司他韦胶囊在成人和13岁以上青少年的推荐口服剂量是每次75毫克,每日2次,共5天。
儿童:对1岁以上的儿童推荐按照下列体重-剂量表服用。
体重推荐剂量(服用5天)≤15kg;每日2次;30mg/次,>15-23kg;每日2次;45mg/次>23-40kg;每日2次;60mg/次>40kg;每日2次;75mg/次5.3.流感的预防:磷酸奥司他韦用于与流感患者密切接触后的流感预防时的推荐口服剂量为75毫克,每日1次,至少7天。
同样应在密切接触后2天内开始用药。
磷酸奥司他韦用于流感季节时预防流感的推荐剂量为75毫克,每日1次。
有数据表明连用药物6周安全有效。
服药期间一直具有预防作用。
六、不良反应6.1.全身:脸部或舌部肿胀、变态反应、过敏反应/过敏样反应、体温过低6.2.皮肤:皮疹、皮炎、荨麻疹、湿疹、中毒性表皮坏死松解症、Stevens-Johnson综合症、多形性红斑6.3.消化系统:肝炎、肝功能检查异常6.4.心脏:心律失常6.5.胃肠道:胃肠道出血、出血性结肠炎6.6.神经:癫痫发作6.7.代谢:糖尿病恶化6.8.精神:行为异常、谵妄,包括以下症状,如幻觉、易激动、意识水平改变、意识模糊、梦魇、妄想。
达菲(磷酸奥司他韦胶囊)说明书

达菲说明书【药品名称】达菲(磷酸奥司他韦胶囊)【汉语拼音】Dafei【主要成分】本品主要成份为磷酸奥司他韦。
【性状】本品为灰白色和浅黄色双色胶囊,内容物为白色至黄白色粉末。
【药理作用】磷酸奥司他韦是其活性代谢产物的药物前体,其活性代谢产物(奥司他韦羧酸盐)是选择性的流感病毒神经氨酸酶抑制剂。
神经氨酸酶是病毒表面的一种糖蛋白酶,其活性对新形成的病毒颗粒从被感染细胞中释放和感染性病毒在人体内进一步播散至关重要。
磷酸奥司他韦的活性代谢产物能够抑制甲型和乙型流感病毒的神经氨酸酶活性。
在体外对病毒神经氨酸酶活性的半数抑制浓度低至纳克水平。
在体外观察到活性代谢产物抑制流感病毒生长,在体内也观察到其抑制流感病毒的复制和致病性。
本品通过抑制病毒从被感染的细胞中释放,从而减少了甲型或乙型流感病毒的播散。
对自然获得的和实验室性流行性感冒进行的研究显示:应用磷酸奥司他韦并没有影响人体对感染产生正常的体液免疫反应。
对灭活疫苗的抗体反应并没有受磷酸奥司他韦治疗的影响。
【药代动力学】吸收口服给药后,磷酸奥司他韦在胃肠道被迅速吸收,经肝脏或/和肠壁酯酶迅速转化为活性代谢产物(奥司他韦羧酸盐)。
至少75%的口服剂量以活性代谢产物的形式进入体内循环。
相对于活性代谢物,少于5%的药物以药物前体的形式存在。
活性代谢产物的血浆浓度与服用剂量成比例,并且不受进食影响(见【用法用量】)。
分布人体内活性代谢产物(奥司他韦羧酸盐)的平均分布容积(Vss)约为23升。
对白鼬,大鼠和兔的研究显示,药物的活性代谢产物可以到达所有流感病毒感染的部位。
研究显示,口服磷酸奥司他韦后其活性代谢产物在肺、支气管、肺泡灌洗液、鼻粘膜、中耳和气管中均可达到抗病毒的有效浓度水平。
活性代谢产物与人血浆蛋白的结合可以忽略不计(约为3%)。
代谢磷酸奥司他韦由主要位于肝脏和肠壁的酯酶几乎完全转化为活性代谢产物(奥司他韦羧酸盐)。
磷酸奥司他韦或其活性代谢产物都不是主要细胞色素P450同工酶的底物或抑制剂,所以不会因为对这些酶竞争而引发药物间相互作用。
磷酸奥司他韦使用说明

磷酸奥司他韦使用说明【功能主治】 . 奥尔菲适用于成人和 岁及 岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有 效治疗甲型和乙型流感 但是乙型流感的临床应用数据尚不多) . 奥尔菲适用于成人和 岁及 岁以上青少年的甲型和乙型流感的预防 【主要成分】 奥尔菲主要成分为磷酸奥司他韦 【包装规格】 mg 【用法用量】 . 磷酸奥司他韦可以与食物同服或分开服用 但对一些病人 进食同时服药可提高药物 的耐受性 . 流感的治疗 在流感症状开始的第一天或第二天(理想状态为 小时内) 就应开始治疗 . 剂量指导 ( ) 成人和青少年,磷酸奥司他韦在成人和 岁以上青少 年的推荐口服剂量是每次 毫克 每日 次 共 天 ( ) 儿童 对 岁以上的儿童 体重≤ 千克 推荐剂量(服用 天) 毫克 每日 次 体重> - 千克 推荐剂量(服用 天) 毫克 每日 次 体重> - 千克 推荐剂量(服用 天) 毫克 每日 次 体重> 千克 推荐剂量(服用 天) 毫克 每日 次 . 流感的预防 磷酸奥司他韦用于与流感患者 密切接触后的流感预防时的推荐口服剂量为 毫克 每日 次 至少 天 同样应在密切接 触后 天内开始用药 . 磷酸奥司他韦用于流感季节时预防流感的推荐剂量为 毫克 每日 次 . 有数据表明连用药物 周安全有效 服药期间一直具有预防作用 . 特殊 人群用药指导(肾功能不全患者) ( ) 流感治疗 对肌酐清除率大于 毫升/分钟的患 者不必调整剂量 对肌酐清除率在 - 毫升/分钟的患者 推荐使用剂量减少为每次 毫 克 每日 次 共 天 ( ) 不推荐将磷酸奥司他韦用于肌酐清除率小于 毫升/分钟的患 者和严重肾功能衰竭 需定期进行血液透析或持续腹膜透析的患者 无肾功能衰竭儿童的 用药剂量资料(见【药代动力学】和【注意事项】) ( ) 流感预防 对肌酐清除率大于 毫升/分钟的患者不必调整剂量 ( ) 对肌酐清除率在 - 毫升/分钟的患者推荐剂量 降低为磷酸奥司他韦 毫克隔日 次或每日 毫克 ( ) 不推荐用于终末期肾功能衰竭的 患者 包括慢性定期血液透析 持续腹膜透析或肌酐清除率小于 毫升/分钟的患者(见 【药代动力学】) ( ) 肝功能不全患者 用于肝功能不全患者治疗和预防流感时剂量不 需要调整(见【药代动力学】) 【不良反应】 . 临床研究经验 . 成人治疗试验 . 在成人流感治疗的 III 期临床试验中 共有 名患者参加试验 分别接受安慰剂 毫克磷酸奥司他韦和 毫克磷酸奥司他韦治疗 报告的不良事件中发生率最高的是恶心和呕吐 . 症状是一过性的 常在第一次服药时 发生 绝大多数的情况下没有导致患者停用研究药物 . 在推荐剂量下 即 毫克 每 日 次 有 例患者由于恶心中途退出试验 另有 名患者因为呕吐中途退出试验 . 在成1人 III 期临床试验中 一些不良事件的发生率在磷酸奥司他韦组比安慰剂组高 发生率≥ %的不良事件如表 所示 . 这些数据总结了健康的年轻人和高危患者 (指流感并发症的 发生风险高的人群 例如年老患者 患有慢性心脏病或者呼吸道疾病的患者) 无论是否 与药物有关 磷酸奥司他韦组比安慰剂组发生率高的不良反应包括恶心 呕吐 支气管炎 失眠和头晕 . 总的来看 高危患者中不良反应的发生率与健康成年人的发生率相似 . 流感预防的试验 总共 人参加了 III 期流感预防的试验 包括青年 成人和老年 人 其中 人服用了推荐剂量的奥司他韦 毫克 每日 次 共 周 虽然服药的时间很长 但与流感治疗的试验相比不良事件的发生率相似 . 在流感预防的试验中下列不良 事件的发生率在服用磷酸奥司他韦组高于安慰剂组 也高于流感治疗试验中相应的不良 事件发生率 疼痛 流涕 消化不良和上呼吸道感染 但是这些不良事件在磷酸奥司他韦 组和安慰剂组的相差不到 % 老年人在服用磷酸奥司他韦和安慰剂的安全性方面与年龄 较小的人群相比差别无临床意义 . 儿童中的治疗试验 在奥司他韦治疗流感的 III 期 临床试验中 共有 名 - 岁患儿参加试验 包括 名无基础疾病的 - 岁患儿和 名 有哮喘病史的 - 岁患儿 . 共有 名儿童接受了奥司他韦口服混悬液治疗 报告发 生率最高的不良事件是呕吐 其他比较常见的不良事件是腹痛 鼻衄 耳痛和结膜炎 这 些不良事件一般只出现一次 继续服药也可缓解 大多数情况下不会导致停止治疗 . 上市后经验 皮肤和皮下组织改变 有极少病例报告出现发红(皮疹) 皮炎和大疱疹 . 肝脏和胆道 有极少病例报告有流感样疾病的患者出现了肝炎和肝酶升高 . 有个 案报道出现了胰腺炎 血管性水肿 喉部水肿 支气管痉挛 面部水肿 嗜酸粒细胞升高 白细胞下降和血尿 【注意事项】 . 自磷酸奥司他韦上市后 陆续收到流感患者使用磷酸奥司他韦治疗发生自我伤害和谵 妄事件的报告 大部分报告来自日本 主要是儿科患者 但磷酸奥司他韦与这些事件的相 关性还不清楚 在使用该药物治疗期间 应该对患者的自我伤害和谵妄事件等异常行为进 行密切监测 . 尚无证据显示磷酸奥司他韦对甲型流感和乙型流感以外的其他疾病有 效 . 奥司他韦对 岁以下儿童治疗流感的安全性和有效性尚未确定 . 奥司他韦对 岁以下儿童预防流感的安全性和有效性尚未确定 . 在健康状况差或不稳定必须入院 的患者中奥司他韦的安全性和有效性尚无资料 . 在免疫抑制的患者中奥司他韦治疗 和预防流感的安全性和有效性尚不确定 . 在合并有慢性心脏或/和呼吸道疾病的患者 中奥司他韦治疗流感的有效性尚不确定 这些人群中治疗组和安慰剂组观察到的并发症 发生率无差别 . 磷酸奥司他韦不能取代流感疫苗 磷酸奥司他韦的使用不应影响每年 接种流感疫苗 磷酸奥司他韦对流感的预防作用仅在用药时才具有 只有在可靠的流行病 学资料显示社区出现了流感病毒感染后才考虑使用磷酸奥司他韦治疗和预防流感 . 对肌酐清除率在 - 毫升/分钟的患者 用于治疗和预防的推荐剂量应做调整 磷酸奥司 他韦不推荐用于肌酐清除率小于 毫升/分钟的患者 和严重肾功能衰竭需定期进行血液 透析和持续腹膜透析的患者(见【药代动力学】和【用法用量】) . 无肾功能衰竭儿 童的药物剂量的资料 . 没有观察到药物对患者驾驶车辆或者操纵机械的能力产生影 响 但是必须考虑流感本身可能造成的影响2【禁忌】对奥尔菲的任何成分过敏者禁用【孕妇用药】 . 妊娠 ( ) 对大鼠和家兔进行的动物生殖研究中 没有观察到药物具有致畸性 ( ) 在 项大鼠分娩前后的研究中给予母鼠中毒剂量的磷酸奥司他韦 有 项研究出现未断 奶幼鼠的生长迟滞 产程也延长 ( ) 在对大鼠进行的生育和生殖毒性研究中 所采用奥司他韦的剂量没有对大鼠生育能 力产生影响 ( ) 大鼠和家兔的胚胎所接受的药物暴露量约为母鼠 母兔的 %- % ( ) 对于妊娠妇女服用磷酸奥司他韦治疗目前尚无足够的数据 因此不可能评价磷酸奥 司他韦导致胎儿畸形或胎儿毒副反应的潜在可能性 因此只有在预期利益大于潜在危险 时妊娠妇女才可服用磷酸奥司他韦 . 哺乳 ( ) 对哺乳期大鼠 奥司他韦和其活性代谢产物(奥司他韦羧酸盐)可从乳汁中分泌 ( ) 目前尚不知奥司他韦和其活性代谢产物会不会从人乳中分泌 ( ) 由动物试验数据初步推断 估算人乳中每日约有 . 毫克奥司他韦 . 毫克活性代谢 产物 因此只有在对哺乳母亲的预期利益大于对婴儿的潜在危险时才可服用磷酸奥司他 韦 【儿童用药】 . 用药剂量参见【用法用量】 . 磷酸奥司他韦对 岁以下儿童的安全性和有效性尚未确定 【老年用药】 用于老年患者治疗和预防时剂量不需要调整(见【药代动力学】)3。
奥司他韦干混悬剂与颗粒剂、胶囊剂适应症、用法用量、使用方法和储存等不同特点

奥司他韦干混悬剂与颗粒剂、胶囊剂适应症、用法用量、使用方法和储存等不同特点适应症不同奥司他韦是流感病毒神经氨酰酶抑制剂,用于甲型和乙型流感的治疗和预防,但不同剂型之间对于适应症人群有着明显区分。
奥司他韦颗粒和胶囊剂适用于成人和 1 岁及以上儿童流感的治疗及成人和 13 岁及以上青少年流感的预防。
对重症病例的高危人群有预防使用指征,其中儿童高危人群划分为年龄 < 5 岁,而在 5—13 岁人群中的预防使用适应症并不明确。
奥司他韦干混悬剂的治疗适应症为 2 周龄以上人群,预防适应症为 1 岁及以上人群,可补充这一阶段人群治疗和预防用药适应症。
不同剂型奥司他韦治疗及预防适应症用法用量不同奥司他韦颗粒和胶囊剂的说明书中,成人和 1 岁及以上儿童的治疗剂量,以及成人和 13 岁及以上青少年的预防剂量。
奥司他韦干混悬剂2 周龄以上人群的治疗,及 1 岁以上人群的预防,填补了儿童流感预防的用法用量。
不同剂型奥司他韦治疗及预防用法用量使用方法不同药物确定好剂量之后,不同剂型也存在着不同的使用方法,并各具优势。
奥司他韦干混悬剂配备给药器,可精准控制儿童用药剂量,对低龄儿童,给药灵活方便;奥司他韦颗粒可直接温开水冲服,易于操作、方便给药;奥司他韦胶囊剂可掩盖药物苦味,对有正常吞咽功能的成人友好,可在购买不到儿童剂型时拆开使用其内含物。
1、奥司他韦干混悬剂:使用前需分散于水中,服用前需摇匀。
1)配置奥司他韦混悬液轻轻拍打奥司他韦干混悬剂的瓶身,使药物粉末松散,取出包装内附赠的塑料量杯,并根据量杯刻度取 55 mL 凉开水倒入瓶中,拧紧瓶盖,充分振摇瓶子 15 秒,塞回塑料内塞。
2)量取和服用正确剂量①包装内含有 3mL和10 mL的给药器,如需剂量为1.0—3.0 mL,使用 3 mL 给药器;如需剂量大于3.0 mL—10 mL,则使用 10 mL 给药器。
检查确认瓶盖已拧紧,然后振摇已配好的奥司他韦混悬液,根据需要服用的剂量,使用不同规格的给药器取药。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【商品名】达菲【产品名称】磷酸奥司他韦胶囊【英文名】OseltamivirPhosphateCapsules【汉语拼音】LinSuanAoSiTaWeiJiaoNang【主要成份】本品主要成分为磷酸奥司他韦。
化学名称:(3R,4R,5S)-4-乙酰氨基-5-氨基-3(1-乙丙氧基)-1-环己烯-1-羧酸乙酯磷酸盐化学结构式:分子式:C16H28N2O4·H3PO4分子量:410.4【性状】本品为灰色和淡黄色双色胶囊,内容物为白色至黄白色粉末,可含有块状物。
【适应症】1.用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。
患者应在首次出现症状48小时以内使用。
2.用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
【用法用量】磷酸奥司他韦可以与食物同服或分开服用。
但对一些病人,进食同时服药可提高药物的耐受性。
流感的治疗在流感症状开始的第一天或第二天(理想状态为36小时内)就应开始治疗。
剂量指导成人和青少年磷酸奥司他韦胶囊在成人和13岁以上青少年的推荐口服剂量是每次75mg,每日2次,共5天。
儿童对1岁以上的儿童推荐按照下列体重-剂量表服用。
流感的预防磷酸奥司他韦用于与流感患者密切接触后的流感预防时的推荐口服剂量为75mg,每日1次,至少10天。
同样应在密切接触后2天内开始用药。
磷酸奥司他韦用于流感季节时预防流感的推荐剂量为75mg,每日1次。
有数据表明连用药物6周安全有效。
服药期间一直具有预防作用。
特殊人群用药指导老年患者用药在治疗和预防流感时,对于老年患者的用药剂量无需调整(见【药代动力学】特殊人群药代动力学)。
肾功能不全患者流感治疗:对肌酐清除率大于60ml/分钟的患者不必调整剂量。
对肌酐清除率大于30ml/分钟但不大于60ml/分钟者,推荐使用剂量减少为每次30mg,每日两次,共5天。
对肌酐清除率大于10ml/分钟但不大于30ml/分钟者,推荐使用剂量减少为每次30mg,每日一次,共5天。
对于定期血液透析患者,如果在透析间期流感症状在48小时内加重,可在透析开始前给予30mg的起始剂量。
为了维持治疗水平的血药浓度,应在每次透析结束后给予30mg剂量。
对于腹膜透析患者,建议在透析开始前给予本品30mg,之后每5天给药30mg进行治疗(见【药代动力学】特殊人群药代动力学和【注意事项】)。
尚未研究奥司他韦在不进行透析的终末期肾病(即肌酐清除率<10ml/分钟)患者中的药代动力学。
因此,不能对这类患者的用药剂量提供建议。
流感预防:对肌酐清除率大于60ml/分钟的患者不必调整剂量。
对肌酐清除率大于30ml/分钟但不大于60ml/分钟者,推荐使用剂量减少为每次30mg,每日一次。
对肌酐清除率大于10ml/分钟但不大于30ml/分钟者,推荐使用剂量减少为每次30mg,隔日一次。
对于定期血液透析病人,如果在透析间期流感症状在48小时内加重,可在透析开始前给予30mg的起始剂量。
为了维持治疗水平的血药浓度,应在每两次透析结束后给予30mg剂量。
对于腹膜透析患者,建议在透析开始前给予本品30mg,之后每7天给药30mg进行预防(见【药代动力学】特殊人群药代动力学和【注意事项】)。
尚未研究奥司他韦在不进行透析的终末期肾病(即肌酐清除率<10ml/分钟)患者中的药代动力学。
因此,不能对这类患者的用药剂量提供建议。
肝功能不全患者用于轻中度肝功能不全患者治疗和预防流感时不需要调整剂量(见【药代动力学】)。
本品用于严重肝功能不全患者的安全性和药代动力学尚未研究。
免疫功能低下患者流感治疗:对于18岁及以上的成人免疫功能低下患者进行10天的治疗评估(见【不良反应】和【临床试验】),结果显示用于治疗流感时无需调整剂量。
流感预防:1岁及1岁以上免疫功能低下病人用于预防季节性流感时,推荐使用12周。
无需调整剂量。
【药理毒理】药理作用磷酸奥司他韦是其活性代谢产物(奥司他韦羧酸盐)的前体药物,奥司他韦羧酸盐是选择性的流感病毒神经氨酸酶抑制剂。
神经氨酸酶是病毒表面的一种糖蛋白酶,其活性对新形成的病毒颗粒从被感染细胞中释放和感染性病毒在人体内进一步播散至关重要。
同时也有报道指出神经氨酸酶对病毒进入未感染细胞也具有一定作用。
磷酸奥司他韦的活性代谢产物能够抑制甲型和乙型流感病毒的神经氨酸酶活性。
在体外对病毒神经氨酸酶活性的半数抑制浓度低至纳克水平。
活性代谢产物在体外可抑制流感病毒感染和复制,在体内也观察到其抑制流感病毒的复制和致病性。
奥司他韦通过抑制病毒从被感染的细胞中释放,从而减少了甲型或乙型流感病毒的播散。
磷酸奥司他韦未影响人体对感染产生正常的体液免疫反应。
对灭活疫苗的抗体反应未受磷酸奥司他韦治疗的影响。
毒理研究遗传毒性:奥司他韦及其活性代谢物的标准组合遗传毒性试验结果均为阴性。
生殖毒性:奥司他韦1500mg/kg对雌性和雄性大鼠的生育力均未见不良影响。
奥司他韦1500mg/kg未见对大鼠和小鼠胚胎-胎仔发育产生影响。
大鼠围产期给予奥司他韦1500mg/kg/天,可引起分娩时间延长,安全剂量(500mg/kg/天)下奥司他韦及其代谢物的暴露量为人体暴露量的480倍和44倍。
致癌性:奥司他韦大鼠和小鼠为期2年的致癌性试验,以及活性代谢产物转基因Tg:AC小鼠6个月致癌性试验,均未见明显致癌性。
其他:在哺乳大鼠中,奥司他韦及其代谢物可通过乳汁分泌。
奥司他韦对豚鼠具有潜在的皮肤致敏性。
奥司他韦对兔眼具有可逆的刺激性。
单次经口给予磷酸奥司他韦657mg/kg及以上剂量,对成年大鼠没有影响,但对七日龄幼鼠可产生毒性,包括死亡;剂量为500mg/kg 时,包括连续给药(在出生后7-21天,每天给药500mg/kg),未观察到不良反应。
【药代动力学】吸收口服给药后,磷酸奥司他韦迅速被胃肠道吸收,经肝脏或/和肠壁酯酶迅速转化为活性代谢产物(奥司他韦羧酸盐)。
至少75%的口服剂量以活性代谢产物的形式进入体内循环。
相对于活性代谢物,少于5%的药物以药物前体的形式存在。
活性代谢产物的血浆浓度与服用剂量成比例,并且不受进食影响(见【用法用量】)。
分布人体内活性代谢产物(奥司他韦羧酸盐)的平均分布容积(Vss)约为23升。
对白鼬,大鼠和兔的研究显示,药物的活性代谢产物可以到达所有流感病毒感染的部位。
研究显示,口服磷酸奥司他韦后其活性代谢产物在肺、支气管、肺泡灌洗液、鼻粘膜、中耳和气管中均达到抗病毒的有效浓度水平。
活性代谢产物与人血浆蛋白的结合可以忽略不计(约为3%)。
代谢磷酸奥司他韦由主要位于肝脏和肠壁的酯酶几乎完全转化为活性代谢产物(奥司他韦羧酸盐)。
磷酸奥司他韦或其活性代谢产物都不是主要细胞色素P450同工酶的底物或抑制剂,所以不会因为对这些酶竞争而引发药物间相互作用。
清除吸收的奥司他韦主要通过转化为活性代谢产物而清除(>90%)。
活性代谢产物不再被进一步代谢,而是由尿排泄。
活性代谢产物达到峰浓度后,血浆浓度下降半衰期为6~10小时。
超过99%的活性代谢产物由肾脏排泄。
肾脏的清除率(18.8升/小时)超过肾小球滤过率(7.5升/小时),表明除了肾小球滤过外,还有肾小管分泌这一途径。
口服放射性物质标记的药物研究表明少于20%的剂量由粪便排出。
特殊人群药代动力学:≥1岁的儿童在1-16岁儿童中进行了单剂量奥司他韦的药代动力学研究。
在一项临床试验中对3-12岁儿童进行了小样本多剂量药代动力学研究。
结果表明按体重计算,年轻患者对奥司他韦和其活性代谢产物的清除均较成人快,所以在给定mg/kg的剂量下,儿童的暴露量低。
儿童2mg/千克的剂量以及30mg或45mg的单位剂量,与成人75mg胶囊(约1mg/千克)剂量的奥司他韦羧酸盐暴露量相当。
12岁以上儿童的奥司他韦的药代动力学与成人相似。
无肾功能衰竭儿童的药物代谢资料。
老年人给予相同剂量的磷酸奥司他韦,老年人(年龄在65-78岁之间)的稳态活性代谢产物的机体利用度同青年人相比高25~35%,而老年人和青年人的药物半衰期相似。
考虑到机体的利用度和耐受性,老年人不必调整剂量(见【用法用量】)。
肾功能不全患者对不同程度的肾功能不全患者给予100mg磷酸奥司他韦,每日2次,服用5天,结果显示活性代谢产物的暴露剂量与肾功能的降低程度呈反比(参考剂量见【用法用量】)。
肝功能不全患者体外研究表明,肝功能不全患者并没有像预期那样表现出体内奥司他韦水平显著增高或其活性代谢产物水平显著降低(见【用法用量】)。
免疫力低下患者群体药代动力学分析表明,与成人非免疫低下患者相比,成人免疫低下患者接受奥司他韦治疗(见【用法用量】免疫功能低下患者),活性代谢物的暴露量增加(至50%)。
但是,由于活性代谢产物的安全性范围较宽,成人免疫低下患者无需调整剂量。
【不良反应】1.临床试验安全性特征总结达菲的整体安全性特征基于2646例成人/青少年和859例儿童流感患者的数据,和临床试验中接受达菲预防流感的1943例成人/青少年和148例儿童患者的数据。
在成人/青少年的治疗研究中,最常见的药物不良反应为恶心、呕吐和头痛,大多数药物不良反应是在治疗第一天或第二天时的单独个例,并且在1-2天内自行缓解。
在成人/青少年的预防研究中,最常见的药物不良反应为恶心、呕吐、头痛和疼痛。
儿童患者最常见的药物不良反应为呕吐。
大部分患者没有因为上述药物不良反应事件而停药。
临床试验中药物不良反应总结列表临床试验中药物不良反应根据MedDRA系统器官分类列出。
每种药物不良反应(表1)相应频率根据以下惯例分类:十分常见(≥1/10);常见(≥1/100~<1/10);偶见(≥1/1,000~<1/100);罕见(≥1/10,000~<1/1,000)和十分罕见(<1/10,000)。
成人和青少年的流感治疗与预防在成人/青少年的治疗与预防研究中,推荐剂量下(治疗:75mg每日2次,连续服用5天;预防:75mg每日1次,最多6周)最常见的(≥1%)的药物不良反应,且与安慰剂相比,达菲的发生率至少高1%的药物不良反应,请参见表1。
流感治疗研究中的人群包括其它健康成人/青少年和“有风险的”患者(患者出现流感相关并发症的风险较高,例如老年患者和患有慢性心脏病/或呼吸系统疾病的患者)。
一般情况下,“有风险的”患者中的安全性特征与其他健康成人/青少年中的特征相似。
即使预防研究中的给药周期更长,但接受推荐剂量本品(75mg每天1次,最长持续6周)进行预防的患者的安全性特征与治疗研究中观察到的特征相似(表1)。
1在临床研究中,接受奥司他韦用于治疗或预防流感的成人和青少年患者≥1%不良反应总结(与安慰剂组差异≥1%)a仅报告奥司他韦组的发生频率分类一岁以上儿童流感的治疗和预防共有1481名儿童(包括1-12岁无其他病症的儿童和6-12岁哮喘儿童)参加奥司他韦治疗流感的临床试验。
