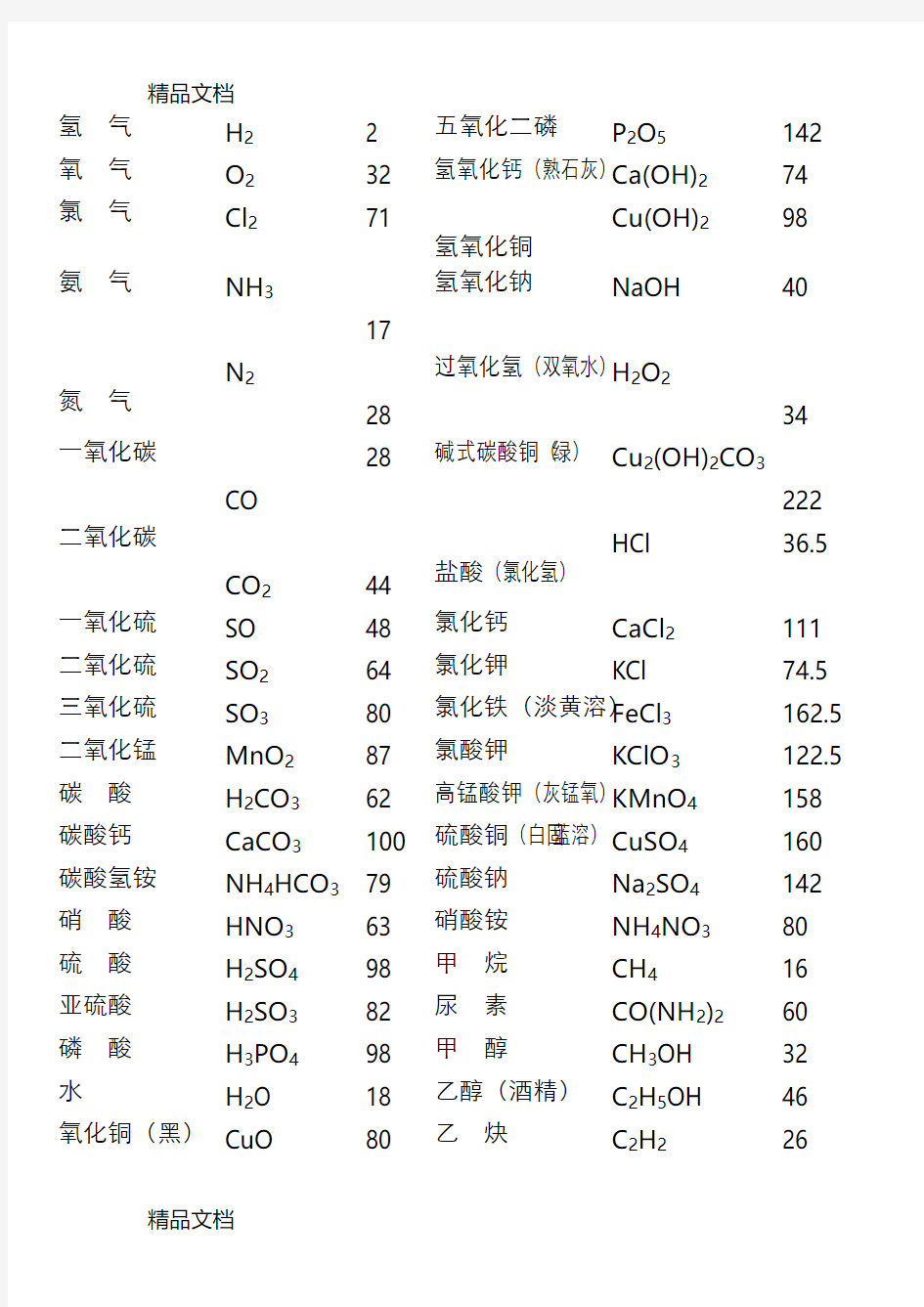
初中常用相对分子质量及计算公式(汇编)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氢气H
2
2 五氧化二磷P2O5142
氧气O
2
32 氢氧化钙(熟石灰)Ca(OH)274
氯气Cl
271
氢氧化铜
Cu(OH)298
氨气NH
3
17
氢氧化钠NaOH 40
氮气N2
28
过氧化氢(双氧水)H
2
O2
34
一氧化碳
CO 28 碱式碳酸铜(绿)Cu2(OH)2CO3
222
二氧化碳
CO244 盐酸(氯化氢)
HCl 36.5
一氧化硫SO 48 氯化钙CaCl
2
111
二氧化硫SO
2
64 氯化钾KCl 74.5
三氧化硫SO
3
80 氯化铁(淡黄溶)FeCl3162.5
二氧化锰MnO
2
87 氯酸钾KClO3122.5
碳酸H
2
CO362 高锰酸钾(灰锰氧)KMnO4158
碳酸钙CaCO
3
100 硫酸铜(白固蓝溶)CuSO4160
碳酸氢铵NH
4
HCO379 硫酸钠Na2SO4142
硝酸HNO
3
63 硝酸铵NH4NO380
硫酸H
2
SO498 甲烷CH416
亚硫酸H
2
SO382 尿素CO(NH2)260
磷酸H
3
PO498 甲醇CH3OH 32
水H
2
O 18 乙醇(酒精)C2H5OH 46
氧化铜(黑)CuO 80 乙炔C
2
H226
氧化镁(白)MgO 40 乙酸(醋酸)CH
COOH 60
3
氧化钙(白)CaO 56
四氧化三铁(黑)Fe
O4232
3
氧化铁(红)Fe
O3160
2
氧化亚铁(黑)FeO 72
硫酸亚铁(淡绿)FeSO
152
4
硫酸锌(白/无)ZnSO
161
4
初中化学常用计算公式
一. 常用计算公式:
(1)相对原子质量= 某元素一个原子的质量/ 一个碳原子
质量的1/12
(2)设某化合物化学式为AmBn
①它的相对分子质量=A的相对原子质量×m+B的相对原
子质量×n
②A元素与B元素的质量比=A的相对原子质量×m:B的相
对原子质量×n
③A元素的质量分数ω=A的相对原子质量×m /AmBn的相对分子质量
(3)混合物中含某物质的质量分数(纯度)=纯物质的质量/混合物的总质量× 100%
(4)标准状况下气体密度(g/L)=气体质量(g)/气体体积(L)
(5)纯度=纯物质的质量/混合物的总质量× 100% =
纯物质的质量/(纯物质的质量+杂质的质量) × 100%=
1- 杂质的质量分数
(6)溶质的质量分数=溶质质量/溶液质量× 100% =溶质质量/(溶质质量+溶剂质量) × 100%
(7)溶液的稀释与浓缩
M浓× a%浓=M稀× b%稀=(M浓+增加的溶剂质量) × b%稀
(8)相对溶质不同质量分数的两种溶液混合
M浓× a%浓+M稀× b%稀=(M浓+M稀) × c%
(9)溶液中溶质的质量
=溶液的质量×溶液中溶质的质量分数
=溶液的体积×溶液的密度
